药品包装用铝箔检验操作规程
药包材微生物限度检查操作规程

药包材微生物限度检查操作规程药包材微生物限度检查操作规程一、目的与范围为保障药包材的卫生质量,规范药包材微生物限度检查操作,本操作规程适用于药包材微生物限度检查。
二、术语与定义1. 药包材:指用于药品包装的材料,如玻璃瓶、铝箔、袋子等。
2. 微生物限度:指药包材中的微生物污染的数量不能超过一定的限度。
3. 检查样品:指从药包材中取样检查的样品。
三、操作流程1. 准备工作1.1 检查人员应在工作前进行手部消毒,并佩戴洁净工作服、帽子和口罩。
1.2 检查仪器设备应进行清洁和消毒,确保无污染。
1.3 首次使用检查样品前,应进行无菌处理。
2. 取样2.1 根据药包材的特点,选择合适的取样方法,如剪刀剪取、刮取等。
2.2 取样时应注意避免污染,避免手部和工具的直接接触。
2.3 取样应充分代表药包材的不同部位和不同批次。
3. 样品处理3.1 将取样的药包材放入无菌容器中,避免接触外界环境。
3.2 添加合适的培养基,保证微生物生长。
3.3 药包材中的微生物落菌数较多时,可对样品进行稀释处理。
4. 培养和观察4.1 将培养基接种完毕后,密封容器,确保无菌。
4.2 将培养基置于适宜的温度和湿度条件下培养。
4.3 观察培养基是否出现细菌、真菌等微生物的生长。
5. 计数和判断5.1 培养基培养一定时间后,根据培养基上的菌落形态、颜色等特征进行初步判断。
5.2 将培养基进行放大培养,使用显微镜观察细菌、真菌的形态和结构,进行进一步鉴定。
5.3 使用计数板对菌落进行计数,记录每种微生物的数量。
5.4 根据国家规定的微生物限度标准,判断样品是否合格。
6. 结果记录和分析6.1 将检查结果记录在相应的记录表中,包括药包材名称、样品编号、微生物种类和数量等信息。
6.2 对合格的样品进行合格认证,对不合格的样品进行处理和记录。
6.3 对不合格的样品进行原因分析,查明污染源,并采取相应的措施进行处理和纠正。
四、操作注意事项1. 所有操作应在洁净室中进行,避免外界空气和微生物的污染。
YBB00152002-2015药用铝箔

1.目的:建立铝箔质量铝箔的质量标准。
2.范围:适用于铝箔质量铝箔验收检查。
3.责任:质量保证部、生产部、物料部。
4.内容:4.1引用标准:YBB00152002-2015药用铝箔、《中国药典》2015年版二部4.2物料代码:4.3.供应商:4.4取样程序:本品按《取样操作规程》(编号:)进行取样。
4.5.检查内容4.5.1 外观取本品适量,在自然光线明亮处,正视自测。
表面应洁净、平整、涂层均匀。
文字、图案印刷应正确、清晰、牢固、色度应与标准样本一致。
4.5.2 针孔度取长400mm,宽250mm(当宽小于250mm时,取卷幅宽)试样十片,逐张置于针孔检查台(800mm×600mm×300mm或适当体积的木箱,木箱内安装30W日光灯,木箱上面放一块玻璃板,玻璃板衬黑纸并留有400mm×250mm空间以检查试样的针孔)上,在暗处检查其针孔。
不应有密集的、连续的、周期性的针孔;每一平方米中,直径大于0.3mm的针孔不允许有;直径为0.1~0.3mm的针孔数不得过1个。
4.5.3阻隔性能水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GB1037-88)的规定进行。
试验时热封面向湿度低的一侧,试验温度(38±2)℃,相对湿度(90±9)%,不得过0.5g/(m²·24h)。
4.5.4 粘合层热合强度除另有规定外,取100mm×100mm的本品二片,另取100mm×100mm的标准聚氯乙烯固体药用硬片(或聚氯乙烯/聚偏二氯乙烯固体药用复合硬片)二片。
将试样的粘合层面,向PVC面(或PVC/PVDC复合硬片的PVDC面)进行叠合。
置于热封仪进行热合,热合条件为:温度155℃±5℃,压力0.2MPa,时间1S,热合后取出放冷,用标准载切器切成15mm宽的试样,取中间三条供试验,试样应在温度23℃±2℃,相对湿度50±5%的环境中,放置4小时以上,并在上述条件下进行试验。
药品包装用铝箔检验标准

药品包装用铝箔检验标准1、目的:确保公司因生产需要而购进的包装材料符合规定的要求。
2、适用范围:本检验规程适用于固体药品(片剂、胶囊剂等)铝塑泡罩包装(PTP)用的铝箔(以下简称铝箔)。
3、质量标准和检验方法:3.1各种铝箔应符合我司的样品(包括双方确认的材质)或设计稿,并达到相应规格要求及配合尺寸。
3.2 外观要求与检验方法:3.2.1 表面:铝箔表面应平整、涂层均匀,无明显裂纹和变形,无余料堆积等。
3.2.2 文字图案:要求与公司样稿相符,文字、图案必须清晰、牢固;在高温热合后,文字、图案仍清晰,不变色。
印刷位置允许有±1.5mm的偏差,无印刷模糊等缺陷。
3.2.3 洁净度:铝箔外观应洁净,不得有灰尘、杂质等污染。
3.2.4 接头数:每1000m内不多于2个,并在接头处加一标记3.2.5卷面及端面:应缠紧、缠齐,端面应平整,不允许有塔形、错层、松层或管芯自由脱落现象,不允许有严重碰伤、压陷。
3.2.6 绕卷裁切面平整度:保护层、外侧印刷、铝箔基材值均小于1mm。
3.2.7 针孔度:不应有密集的、连续性的、周期性的针孔,1m2中d>0.3mm不允许有,d=0.1-0.3mm不超过1个。
3.2.8外包装:包装箱上应标明产品名称、容量、生产厂名、生产日期、数量、检验者代号等信息,同时包装纸箱不得脏及破损并内衬塑料保护袋,用胶带“工”字形封箱,对于易擦伤的阀或罩子等须用塑料袋、卫生的纸等相隔,出厂前产品必须附出厂检验报告单。
外观检验以目测为主,于正常光源下,30cm距离处目测。
3.3功能(物理机械性能)要求与检测方法:3.3.1粘合层热封强度:其指标应≥5.88N/15mm。
检验方法:按GB 12255-90中6.4.1规定的方法进行。
3.3.2保护层粘合性其胶带试验应无明显剥落现象。
:检验方法:按GB12255-90中6.4.2规定的方法进行。
3.3.3保护层耐热性:在200℃时,应无明显粘落。
001 内包装材料检验操作规程
SOP/QC(03)001-01 内包装材料检验操作规程文件类别:操作规程江西中兴汉方药业有限公司目的:制定药品内包装材料检验标准操作规程,并按规程进行检验,保证检验操作规范化。
依据:《内包装材料质量标准》;药品生产质量管理规范(2010年修订)。
范围:适用于公司所有药品内包装材料的检验。
责任:质量控制科主任及检验员对本规程执行负责。
质量保证科主任及监控员对本规程的实施负责。
质量管理部经理负领导责任。
正文:公司药品用内包装材料种类主要包括:药品包装用铝箔、聚氯乙烯固体药用硬片、药用低密度聚乙烯袋(内)。
所有内包装材料应先检测微生物限度,再做其它项目的检验。
1内包装材料微生物限度检验:1.1内包材微生物限度检验供试液的制备:药品包装用铝箔、聚氯乙烯固体药用硬片、药用低密度聚乙烯袋(内)供试液的制备:取试样内层面面积约为20 cm2,将无菌棉签用pH7.0无菌氯化钠-蛋白胨缓冲液稍沾湿,在板孔范围内擦抹5次,擦拭方法按示1所示:示1 示2换1支棉签再擦抹5次,擦拭方法按示2所示。
每个位置用2支棉签共擦抹10次,共擦抹5个位置合计100 cm2。
每支棉签抹完后立即剪断,投入盛有30ml的pH7.0无菌氯化钠-蛋白胨缓冲液已灭菌的锥形瓶中。
全部棉签投入瓶中后,将瓶迅速摇晃1min,即得供试液。
1.2内包装材料的需氧菌、霉菌、酵母菌检查:1.2.1供试品的检査1)按计数方法适用性试验确认的计数方法进行供试品中需氧菌总数、霉菌和酵母菌总数的测定。
2)胰酪大豆胨琼脂培养基或胰酪大豆胨液体培养基用于测定需氧菌总数;沙氏葡萄糖琼脂培养基用于测定霉菌和酵母菌总数。
3)阴性对照试验以稀释液代替供试液进行阴性对照试验,阴性对照试验应无菌生长,如阴性对照有菌生长,应进行偏差调査。
1.2.2试验前的准备:1)无菌室无菌程度应符合规定;见《沉降菌监测规程》、《悬浮粒子监测规程》、浮游菌监测规程》。
2)供试品及所有已灭菌的平皿、试管、吸管、量筒、培养基等移至传递窗内并打开紫外灯。
药用包装用铝箔检验操作规程
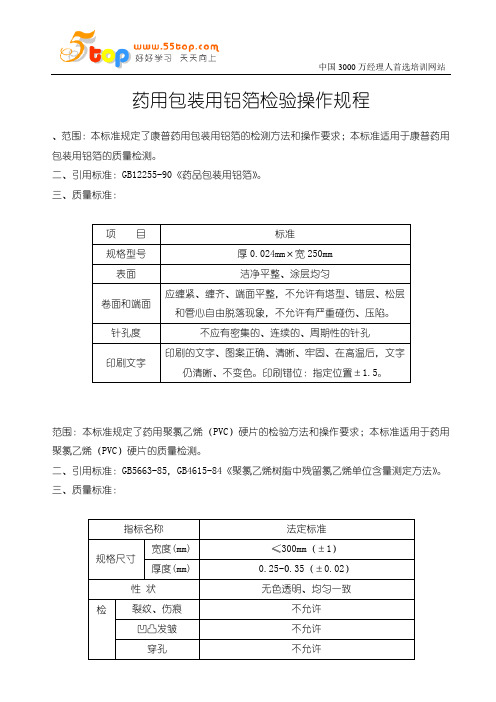
药用包装用铝箔检验操作规程、范围:本标准规定了康普药用包装用铝箔的检测方法和操作要求;本标准适用于康普药用包装用铝箔的质量检测。
二、引用标准:GB12255-90《药品包装用铝箔》。
三、质量标准:范围:本标准规定了药用聚氯乙烯(PVC)硬片的检验方法和操作要求;本标准适用于药用聚氯乙烯(PVC)硬片的质量检测。
二、引用标准:GB5663-85,GB4615-84《聚氯乙烯树脂中残留氯乙烯单位含量测定方法》。
三、质量标准:四、仪器:烘箱、游标卡尺。
五、试验方法1、外观检验在60cm距离正视观察2、加热伸缩率试验2.1设备:加热试验选用老化试验箱或烘臬,共控温精度为±1℃。
长度测定选用精度0.02mm的游标卡尺。
2.2 试样;从硬片上切取正方形试片二片(如图 1所示),每片宽度120mm。
找准中心划出纵向AB、横向CD间距为100mm互相垂直90℃二条线。
2.3 操作:将试片平放在玻璃板上,置于1001℃的试验箱中,持续10min,取出冷却至室温,然后准确测定每片AB、CD线段长度。
2.4 计算;先求得两片AB、CD的平均值,并按式(1)算出纵向和横向的伸缩率:L2-L1S% = ——————×100% (1)L1式中:S:伸缩率;L1:加热前的标点间的距离,mm;L2:加热后的标点间的距离,mm。
六、检测规则1、聚氯乙烯硬片以同一配方,同一工艺,同一规格为一批。
每批数量不得超过20t。
2、尺寸、公差及外观应逐卷检验。
3、物理性能及化学性能急性毒性试验的验收以厂家检验报告书为依据。
4、检验结果应按下列规定处理。
4.1 公差及外观,其中一项不合格,则该卷为不合格品。
4.2 物理性能不论任何一项不合格,应重新以原批中加倍取样复试仍不合格,则整批不得作为药用包装材料。
铝箔包装袋检验操作规程

铝箔包装袋检验操作规程1. 引言铝箔包装袋广泛应用于食品、药品、化妆品等行业,保障产品的安全和质量。
为了确保铝箔包装袋符合相关标准和要求,制定本操作规程,指导检验人员进行有效的检验工作。
2. 目的本操作规程的目的是规范铝箔包装袋的检验流程,确保产品质量的稳定性和一致性,减少缺陷的发生,保障用户的安全。
3. 适用范围本操作规程适用于铝箔包装袋的检验工作。
4. 术语定义•铝箔包装袋:由铝箔和塑料膜复合而成的包装材料。
•检验项目:对铝箔包装袋进行的各项检验内容。
•缺陷:铝箔包装袋在生产或运输过程中出现的问题,影响产品质量或使用性能的不符合项。
5. 检验工具和设备•放大镜•灯光设备•外观检验台•称重器•测厚仪6. 检验流程6.1 准备工作1.确保检验人员已经接受相关培训,熟悉检验操作规程。
2.准备好所需的检验工具和设备,并确保其正常使用状态。
6.2 外观检验1.将铝箔包装袋放置在外观检验台上。
2.使用放大镜对铝箔包装袋进行仔细观察,检查是否存在以下缺陷:–脱层:铝箔与塑料膜之间出现脱层现象。
–破损:铝箔包装袋表面出现破损、裂纹等情况。
–污染:铝箔包装袋表面出现污渍或异物。
–粘结不良:铝箔与塑料膜之间粘结不牢固。
6.3 尺寸测量1.使用测厚仪对铝箔包装袋的厚度进行测量,并记录测量结果。
2.使用称重器对铝箔包装袋的重量进行测量,并记录测量结果。
6.4 物理性能测试在需要进行物理性能测试的情况下,按照相应的测试方法进行测试,并记录测试结果。
6.5 结果判定根据检验项目的要求和标准,对检验结果进行判定: - 如果所有检验项目均符合要求,则判定为合格。
- 如果存在一个或多个检验项目不符合要求,则判定为不合格。
6.6 记录与报告1.将检验结果记录在检验记录表中。
2.根据需要,编制检验报告,并将其归档保存。
7. 备注事项1.检验人员应随时保持检验工具和设备的整洁和完好,并在使用前进行校验。
2.对于发现的缺陷,应及时进行记录和报告,并采取相应的措施进行处理。
药品包装用铝箔(YBB00152002)

精心整理国家药品监督管理局国家药品包装容器(材料)标准(试行)YBB00152002药品包装用铝箔囊剂等)检查台0.1—的规定0.5g/(m 2的向PVC 度155±进行180°角方向剥离,不得低于7.0N/15mm(PVC);不得低于6.0N/15mm(PVDC)。
【保护层粘合性】取一张纵向长90mm ,宽为全幅的试样(注意试样不应有皱折)。
将试样平放在玻璃板上,保护层向上,取聚酯胶粘带(与铝箔的剥离力不小于2.94N/20mm)一片,横向均匀地贴压试样表面,以160°~180°方向迅速剥离(见图1),保护层表面应无明显脱落。
图1【保护层耐热性】取100mm×100mm 试样三片,分别将试样的保护层与铝箔原材叠合,置于热封仪中,进行热封(热封条件:温度200℃,压力0.2Mpa ,时间1s),取出放冷,将试样与铝箔原材分开,观察保护层表面应无明显粘落。
【粘合剂涂布量差异】取100mm×100mm试样五片,分别精密称定(质量m1),用乙酸乙酯或其他溶剂擦去粘合剂,再精密称定(质量m2)。
m1与m2之差即为粘合剂的涂布量,同时计算五片涂布量的平均值,各片涂布量与平均值之间的差异均应在±10.0%以内。
【开卷性能】取100mm×100mm试样四片,将试样粘合层与保护层叠合,置于一块大小适宜的平板上,依次在试样上放置20mm×20mm的小平板与1.0kg砝码(见图2),于40℃烘箱中,保温2h后,取出,观察,粘合层面与保护层面不得粘合。
图2【破裂强度】取40mm×40mm试样三片,分置破裂强度仪上,测定,均不得低于98Kpa。
【荧光物质】取100mm×100mm试样五片,分别置于紫外灯下,在254nm和365nm波长4mg。
500ml)℃维持30min1ml,煮沸3)滴国药典0.9%21分钟,J)测定。
药品包装用铝箔质量标准

xxxx药业股份有限公司
一、目的:建立药用铝箔质量标准,确保所用药用铝箔的质量。
二、范围:本规定适用于药用铝箔的质量控制。
三、责任:xx生产区、xx生产区、xx生产区。
四、内容:
1.标准来源:国家药品包装容器(材料)标准 YBB00152002-2015药用铝箔
2.技术要求
3.贮存条件:通风干燥,防暴晒,防污染,防虫蛀,防腐蚀气液,距地面高度大于150mm。
4.相关标准操作规程:药用铝箔检验操作规程(SOP-ZL-JG(BC)-008)、物料取样标准操作规程(SOP-ZL-QA-001)。
5.企业统一指定的物料名称:药用铝箔。
6.内部使用的物料代码:详见产品所对应的药用铝箔物料代码。
7.经批准的供应商:见合格供应商目录。
8.印刷包装材料的实样或样稿:见包装材料样稿。
9.注意事项:标准中未明确的项目,以包材标准样张为准,每批产品需与标准样张进行核对。
10.复验期:执行“物料有效期及复验期管理规程(SMP-WL-008)”相关规定。
11.文件附件:共0份。
12.修订及变更历史:。
纯铝箔袋药品真空铝箔袋安全操作及保养规程

纯铝箔袋药品真空铝箔袋安全操作及保养规程简介
纯铝箔袋药品真空铝箔袋是一种常见的药品包装材料,能够保证药品在运输、存储、销售过程中的质量和安全。
本文将介绍纯铝箔袋药品真空铝箔袋的安全操作及保养规程,以帮助用户正确使用和保护这种包装材料。
安全操作规程
1. 放置与加工
•箭头方向下垂直摆放
•避免摔打或碰撞
•避免温度过高或受潮
2. 开口封闭
•在使用前先检查包装袋的密封性,确认是否有裂口或破损
•使用专业的真空封口机对铝箔袋口进行严密封闭
•严禁使用手工封口、胶带封口、夹子封口等方式进行封闭
3. 存储与运输
•存放于通风干燥处,避免震动或磕碰
•存放在干燥、阴凉处,避免阳光直射或受潮
•运输前应对包装袋进行检查,避免运输途中因挤压、摔打等造成破损
4. 使用
•使用前确认铝箔袋上的标签信息是否正确
•使用前先清洁双手,防止污染内部药品
•先将空气抽出,再封闭铝箔袋
•严禁将铝箔袋暴露在阳光下或高温环境中
保养规程
1. 清洁
•定期对铝箔袋进行清洁
•可以用普通的纯净水和软布擦拭较为轻微的污渍
•对于较为难清除的污渍,可以使用专业的清洁剂进行清理
2. 消毒
•对于需要经常消毒的铝箔袋,应定期进行消毒处理
•可以选用消毒液进行消毒处理,注意消毒液的选择与使用方法
3. 维护
•长时间不使用的铝箔袋建议存放于干燥、通风的处所
•为了延长使用寿命,可以使用专业的防腐剂进行处理结论
正确的纯铝箔袋药品真空铝箔袋的安全操作及保养规程可以保证药品在运输、存储、销售过程中的质量和安全,提高药品的保质期及使用效果,从而确保患者用药的安全和可靠性。
药品包装铝箔检验操作规程

药品包装铝箔检验操作规程一、目的和范围为确保药品包装铝箔的质量,保护药品的安全和有效性,制定本操作规程。
本操作规程适用于药品包装铝箔的质量检验。
二、检验项目和方法1.外观检验外观检验是对药品包装铝箔外观质量进行检查。
方法:(1)通过目检,检查铝箔表面是否有凹痕、划痕、氧化、污染等缺陷;(2)通过触摸,检查铝箔表面是否光滑;(3)通过称量,检查铝箔的重量是否符合标准。
2.厚度检验厚度是衡量药品包装铝箔质量的重要指标,需进行检验。
方法:(1)使用测厚仪,将测厚仪轻轻放置在铝箔表面上,记录测得的厚度值;(2)进行多次测量,并取平均值作为样品的厚度。
3.耐热性检验耐热性是指药品包装铝箔在高温情况下是否能保持其物理性能和化学稳定性的能力,需进行检验。
方法:(1)将铝箔样品放置在高温箱中,升温至一定温度并保持一定时间;(2)取出样品,进行外观检查,看是否出现脱色、变形等现象;(3)通过触摸,检查铝箔是否仍然光滑。
4.折叠强度检验折叠强度是指药品包装铝箔在折叠后的抗拉强度,需进行检验。
方法:(1)将铝箔样品按一定尺寸进行折叠;(2)使用试验机进行拉力测试,记录拉力值;(3)根据标准确定样品的抗拉强度是否合格。
三、检验设备和仪器1.目检仪2.测量尺和天平3.测厚仪4.高温箱5.试验机四、检验记录和报告1.检验员应当编制检验记录,包括样品编号、检验项目、检验结果等内容。
2.检验记录应进行归档,以备追溯。
3.检验结果应及时汇总,编制检验报告。
五、检验频率和流程1.根据药品包装铝箔的使用情况、供应商资质等因素,确定检验频率。
2.药品包装铝箔进货后,按照操作规程进行外观、厚度、耐热性和折叠强度的检验。
3.根据检验结果,判断样品是否合格。
4.对不合格的样品,应进行重新检验,并严格控制不合格品的使用和销售。
六、质量不合格的处理1.对于质量不合格的药品包装铝箔,应立即停止使用。
2.销毁不合格品,以防止误用。
七、操作注意事项1.检验人员应经过专业培训,并具备相应的检验技能。
药用包装铝箔工艺

药用包装铝箔工艺药用包装铝箔是一种具有高阻隔性能、防潮、防菌、防氧化的材料,常用于药品、食品等包装领域。
以下是药用包装铝箔的工艺流程:1.铝箔选材药用包装铝箔应选用符合国家相关标准的优质铝箔材料,如12μm或15μm的铝箔。
铝箔应表面平整、无划痕、无折痕,并具有足够的强度和韧性。
2.铝箔清洗在铝箔裁剪和成形前,需要进行清洗处理。
清洗的目的是去除铝箔表面的油污、尘埃和手指印等杂质,以确保药品的卫生安全。
清洗后的铝箔应立即进行干燥处理。
3.铝箔热处理热处理是提高铝箔强度和韧性的重要步骤。
热处理过程中,铝箔经过加热和冷却的循环处理,可以改变其内部结构,提高机械性能。
热处理后的铝箔应平整无皱褶,无变形。
4.铝箔成形根据药品包装的要求,将清洗并热处理后的铝箔裁剪成所需形状和尺寸。
在成形过程中,应注意保持铝箔的平整度和清洁度。
5.铝箔封合将成形的铝箔与其它包装材料进行封合,以形成一个封闭的包装体系。
封合过程应确保封口处平整、无凸起或凹陷,同时也要确保封合强度符合要求。
6.包装质量检测在封合完成后,应对药用包装铝箔进行质量检测。
检测项目包括外观检测(如封口处是否有气泡、皱褶等)、密封性能检测(如是否漏气)、阻隔性能检测(如透氧率、透湿率等)等。
只有符合质量标准的包装才能进入下一道工序。
7.包装标识打印根据药品包装的标识要求,利用数字印刷机或激光打印机等设备将标识打印在药用包装铝箔上。
标识内容应清晰、易读,包括药品名称、生产日期、有效期等重要信息。
同时也要确保标识颜色鲜艳、持久不褪色。
8.包装入库最后一道工序是将打印好标识的药用包装铝箔进行整理、入库。
在入库前,应确保药用包装铝箔的数量、规格等信息准确无误。
药品包装用铝箔(YBB00152002)

国家药品监督管理局国家药品包装容器(材料)标准(试行)YBB00152002药品包装用铝箔Aluminium foils packaging for medicine本标准适用于与聚氯乙烯(PVC)、聚偏二氯乙烯(PVDC)等硬片粘合,用于固体药品(片剂、胶囊剂等)包装用的铝箔。
本品涂有保护层和粘合层。
【外观】取本品适量,在自然光线明亮处,正视目测。
表面应洁净、平整、涂层均匀。
文字、图案印刷应正确、清晰、牢固。
【针孔度】取长400mm,宽250mm(当宽小于250mm时,取卷幅宽)试样十片,逐张置于针孔检查台(800mm×600mm×300mm或适当体积的木箱,木箱内安装30W日光灯,木箱上面放一块玻璃板,玻璃板衬黑纸并留有400mm×250mm空间以检查试样的针孔)上,在暗处检查其针孔。
不应有密集的、连续性的、周期性的针孔;每一平方米中,直径大于0.3mm的针孔不允许有;直径为0.1—0.3mm的针数不得过1个。
【阻隔性能】水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GB1037-88)的规定进行。
试验时热封面向湿度低的一侧,试验温度(38±2)℃,相对湿度(90±5)℃,不得过0.5g/(m2·24h) 。
【粘合层热合强度】除另有规定外,取100 mm×100mm的本品二片,另取100 mm×100mm 的标准聚乙烯固体药用硬片(或聚氯乙烯/聚偏二氯乙烯固体药用复合硬片)二片。
将试样的粘合层面,向PVC面(或PVC/PVDC复合硬片的PVDC面)进行叠合。
置于热封仪进行热合,热合条件为:温度155℃±5℃,压力0.2Mpa,时间1s,热合后取出放冷,用标准裁切器切成15mm宽的试样,取中间三条供试验,试样应在温度23℃±2℃以,相对湿度50%±5%的环境中,放置4小时以上,并在上述条件下进行试验。
药品包装用铝箔

药品包装用铝箔分类:包材质量标准来源国家药品监督管理局YBB00152002本标准适用于与聚氯乙烯(PVC)、聚偏二氯乙烯(PVDC)等硬片粘合,用于固体药品(片剂、胶囊剂等)包装用的铝箔。
本品涂有保护层和粘合层。
[外观]取本品适量,在自然光线明亮处,正视目测。
表面应洁净、平整、涂层均匀。
文字、图案印刷应正确、清晰、牢固。
[针孔度]取长400mm,宽250mm(当宽小于250mm时,取卷幅宽)试样十片,逐张置于针孔检查台(800mm×600mm×300mm或适当体积的木箱,木箱内安装30W日光灯,木箱上面放一块玻璃板,玻璃板衬黑纸并留有400mm×250mm空间以检查试样的针孔)上,在暗处检查其针孔。
不应有密集的、连续性的、周期性的针孔;每一平方米中,直径大于0.3mm的针孔不允许有;直径为O.1~0.3 mm的针孔数不得过1个。
[阻隔性能]水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GBl037-88)的规定进行。
试验时热封面向湿度低的一侧,试验温度(38±2)℃,相对湿度(90±5)%,不得过0.5g/(m2.24h)。
[粘合层热合强度]除另有规定外,取100mm ×100mm的本品二片,另取100mm×l00mm的标准聚氯乙烯固体药用硬片(或聚氯乙烯/聚偏二氯乙烯固体药用复合硬片)二片。
将试样的粘合层面,向PVC面(或PVC/PVDC复合硬片的PVDC面)进行叠合。
置于热封仪进行热合,热合条件为:温度155℃±5℃,压力0.2MPa,时间1s,热合后取出放冷,用标准载切器切成15mm宽的试样,取中间三条供试验,试样应在温度23℃±2℃,相对湿度50%土5%的环境中,放置4小时以上,并在上述条件下进行试验。
调整好拉力试验机并使记录器指针为零点。
设定拉伸速度200mm/min±20mm/min。
药品包装用铝箔YBB

药品包装用铝箔Y B B 公司标准化编码 [QQX96QT-XQQB89Q8-NQQJ6Q8-MQM9N]国家药品监督管理局国家药品包装容器(材料)标准(试行)YBB00152002药品包装用铝箔Aluminium foils packaging for medicine 本标准适用于与聚氯乙烯(PVC)、聚偏二氯乙烯(PVDC)等硬片粘合,用于固体药品(片剂、胶囊剂等)包装用的铝箔。
本品涂有保护层和粘合层。
【外观】取本品适量,在自然光线明亮处,正视目测。
表面应洁净、平整、涂层均匀。
文字、图案印刷应正确、清晰、牢固。
【针孔度】取长400mm,宽250mm(当宽小于250mm时,取卷幅宽)试样十片,逐张置于针孔检查台(800mm×600mm×300mm或适当体积的木箱,木箱内安装30W日光灯,木箱上面放一块玻璃板,玻璃板衬黑纸并留有400mm×250mm空间以检查试样的针孔)上,在暗处检查其针孔。
不应有密集的、连续性的、周期性的针孔;每一平方米中,直径大于的针孔不允许有;直径为—的针数不得过1个。
【阻隔性能】水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GB1037-88)的规定进行。
试验时热封面向湿度低的一侧,试验温度(38±2)℃,相对湿度(90±5)℃,不得过(m2·24h) 。
【粘合层热合强度】除另有规定外,取100 mm×100mm的本品二片,另取100 mm×100mm的标准聚乙烯固体药用硬片(或聚氯乙烯/聚偏二氯乙烯固体药用复合硬片)二片。
将试样的粘合层面,向PVC面(或PVC/PVDC复合硬片的PVDC面)进行叠合。
置于热封仪进行热合,热合条件为:温度155℃±5℃,压力,时间1s,热合后取出放冷,用标准裁切器切成15mm宽的试样,取中间三条供试验,试样应在温度23℃±2℃以,相对湿度50%±5%的环境中,放置4小时以上,并在上述条件下进行试验。
药品包装用铝箔质量标准

1.目的建立药品包装用铝箔检验的质量标准2.适用范围适用于本公司药品包装用铝箔的质量检验3.职责质检员、质检室主任对本标准的实施负责4.依据国家药品监督管理局药包材标准(YBB00152002)5.检查内容5.1 外观取本品适量,在自然光线明亮处,正视自测。
表面应洁净、平整、涂层均匀。
文字、图案印刷应正确、清晰、牢固、色度应与标准样本一致。
5.2 针孔度取长400mm,宽250mm(当宽小于250mm时,取卷幅宽)试样十片,逐张置于针孔检查台(800mm×600mm×300mm或适当体积的木箱,木箱内安装30W日光灯,木箱上面放一块玻璃板,玻璃板衬黑纸并留有400mm×250mm空间以检查试样的针孔)上,在暗处检查其针孔。
不应有密集的、连续的、周期性的针孔;每一平方米中,直径大于0.3mm的针孔不允许有;直径为0.1~0.3mm的针孔数不得过1个。
5.3阻隔性能水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GB1037-88)的规定进行。
试验时热封面向湿度低的一侧,试验温度(38±2)℃,相对湿度(90±9)%,不得过0.5g/(m²·24h)。
5.4 粘合层热合强度除另有规定外,取100mm×100mm的本品二片,另取100mm×100mm的标准聚氯乙烯固体药用硬片(或聚氯乙烯/聚偏二氯乙烯固体药用复合硬片)二片。
将试样的粘合层面,向PVC面(或PVC/PVDC复合硬片的PVDC面)进行叠合。
置于热封仪进行热合,热合条件为:温度155℃±5℃,压力0.2MPa,时间1S,热合后取出放冷,用标准载切器切成15mm宽的试样,取中间三条供试验,试样应在温度23℃±2℃,相对湿度50±5%的环境中,放置4小时以上,并在上述条件下进行试验。
调整好拉力试验机并使记录器指针为零点。
药品包装用铝箔检验操作规程

目的:为检验药品包装用铝箔规定一个标准的程序,以便获得准确的实验数据。
范围:适用于药品包装用铝箔的检验。
职责:检验室主任、检验员。
规程:1.外观:取本品适量,在自然光线明亮处,正视目测。
表面应洁净、平整、涂层均匀。
文字、图案印刷应正确、清晰、牢固。
2.检查2.1 针孔度取长400mm,宽250mm(当宽小于250mm时,取卷幅宽)试样十片,逐张置于针孔检查台(800mm×600mm×300mm或适当体积的木箱,木箱内安装30W日光灯,木箱上面放一张玻璃板,玻璃板衬黑纸并留有400㎜×250㎜空间以检查试样的针孔)上,在暗处检查其针孔。
不应有密集的、连续性的、周期性的针孔;每一平方米中,直径大于0.3mm的针孔不允许有;直径为0.1~0.3mm的针孔数不得过1个为符合规定。
2.2 荧光物质取100mm×100mm试样五片,分别置于紫外灯下,在254nm和365nm波长处观察,其保护层及粘合层的荧光,不得呈片状为符合规定。
2.3 挥发物取100mm×100mm试样二片,精密称定(质量m a),130℃干燥20分钟后,置于干燥器中,放置30分钟,再精密称定(质量m b),干燥前后试样质量之差(m a-m b)不得过4mg为符合规定。
2.4 溶出物试验取本品内表面积300㎝2,切成3㎝×0.3cm的小片,水洗,室温干燥后,置于500ml的锥形瓶中,加水200ml,以适当的方法封口后,置高压蒸汽灭菌器内,(110±2)℃维持30分钟,放冷至室温,作为供试液;另取水同法操作,作为空白液,进行以下试验:2.4.1 易氧化物精密量取水浸液20ml,精密加入高锰酸钾液(0.002mol/L)20ml与稀硫酸1ml,煮沸3分钟,迅速冷却,加入碘化钾0.1g,在暗处放置5分钟,用硫化硫酸钠液(0.01mol/L)滴定,滴定至近终点时,加入淀粉指示液0.25ml,继续滴定至无色,另取水空白液同法操作,二者消耗滴定液之差不得过1.5ml。
药用铝箔国家标准

中华人民共和国国家标准GB 12255-90药品包装用铝箔Aluminium foils packaging for medicine1 主题内容与适用范围本标准规定了药品铝塑泡罩(PTP)用涂有保护层和粘合层的硬质纯铝箔的品种、规格、技术要求、试验方法、检验规则、标志、包装、运输、储存要求。
本标准适用于固体药品(片剂、交囊剂等)铝塑泡罩包装(PTP)用的铝箔。
2 引用标准GB 191 包装储运图标标志GB 3198 工业用纯铝箔GB 5663 药用聚氯乙烯(PVC)硬片中华人民共和国3 代号PTP (press through package)------铝塑泡罩包装。
4 品种规格4.1 品种分Ⅰ、Ⅱ、Ⅲ、Ⅳ四种形式,见图1及表1。
表1注:1)铝箔基材应符合GB 3198规定。
2)内侧印刷应使用无毒药用油墨。
4.2 规格尺寸及允许偏差应符合表2要求。
表25 技术要求5.1 外观应符合表3的要求。
表35.2 印刷质量5.2.1 印刷文字、图案正确、清晰、牢固;在高温热合后,文字、图案仍清晰,不变色。
5.2.2 印刷错位:指定位置±1.5mm。
5.3 物理性能应符合表4要求。
表45.4 化学性能应符合表5要求。
5.5 异常毒性试验应符合中华人民共和国药典1985年版第二部附录中的规定。
6 试验方法6.1 规格尺寸检验6.1.1 厚度检验用精度为0.5~1.0μ的千分卡或LG-1光学厚度仪测定。
6.1.2 宽度检验用分度值为0.5mm的钢直尺测量。
6.1.3 长度检验用随机的长度计数器测量。
6.2 外观检验6.2.1 表面:目测检验。
6.2.2 接头数检验:随机记录,实用时复核。
6.2.3 卷面和端面:目测检验。
6.2.4 载切面绕卷平整度检验:用分度值为0.5mm的深度游标卡尺测定。
6.2.5 针孔度的检验6.2.5.1 仪器与设备、针孔检查台:800mm×600mm×300mm或适当体积的木箱,木箱内安装30W日光灯,木箱上面放一块玻璃板,玻璃板衬黑纸并留有400mm×250mm空间以检查试样的针孔。
药用铝箔包装材料的质量及其检验

药用铝箔包装材料的质量及其检验药品的泡罩包装亦称为PTP,它采用的材料主要是药用铝箔、药用聚氯乙烯(PVC)以及印刷材料、保护剂、粘合剂等。
它的生产过程是将药品放在经吸塑成形的塑料硬片凹坑内,再用一张经过凹版印刷并涂有保护剂和粘合剂的铝箔与该塑料硬片压合封口。
铝箔是采用纯度为99%以上的电解铝,经过压延制作而成。
铝具有资源丰富、价格低、容易加工等优点,作为药品包装材料使用时,铝箔是包装材料中唯一的金属材料。
铝箔无毒、无味,具有优良的导电性和遮光性,有极高的防潮性、阻气性和保味性,能最有效地保护被包装物;是一种至今尚未能被代替的包装材料,无论是何种蒸镀金属薄膜,还是涂布的特种薄膜都不能完全取代铝箔。
在现代包装装潢领域中,几乎所有需要不透光或高阻隔的复合软包装材料均采用铝箔做阻隔层。
由于铝箔具有上述优点,且重量轻,具有一定的强度,而且印刷性良好,可以在上面印制各种文字或图案。
当制做成泡罩包装时,用时稍加压力便可将其压破,患者取药便利,携带方便。
因此这种包装形式在医药包装领域得到广泛应用,是当今主要包装潮流之一。
制做药用铝箔包装的方式是将铝箔在专用的机械上进行印刷涂布,在生产过程中,出现了一些质量问题,现进行总结讨论,并且需制定严格的材料检验方法和制度,以利于提高原材料以及产品的质量。
一、铝箔材料质量及其检测方法1·1药用铝箔针孔度及其检测:金属铝具有高度致密的金属晶体结构,理论上完美的铝箔能完全阻隔任何气体、水蒸汽和光线。
但事实上由于铝箔生产采用轧制工艺,轧制油的质量、轧制辊表面的状况、工艺操作技术及生产现场环境等诸多因素的影响,铝箔尤其是薄铝箔不可避免地出现各种缺陷,针孔就是其中最主要的一种。
针孔的大小和数量是衡量铝箔产品质量水平的重要尺度之一。
也正是由于针孔的存在,使得氧气、水蒸汽等对铝箔的透过量并不为零。
铝箔针孔的大小和数量对铝箔及其复合材料的防潮性、阻气性和遮光性有着决定性的影响。
药品包装用铝箔检验标准

药品包装用铝箔检验标准1、目的:确保公司因生产需要而购进的包装材料符合规定的要求。
2、适用范围:本检验规程适用于固体药品(片剂、胶囊剂等)铝塑泡罩包装(PTP)用的铝箔(以下简称铝箔)。
3、质量标准和检验方法:3.1各种铝箔应符合我司的样品(包括双方确认的材质)或设计稿,并达到相应规格要求及配合尺寸。
3.2 外观要求与检验方法:3.2.1 表面:铝箔表面应平整、涂层均匀,无明显裂纹和变形,无余料堆积等。
3.2.2 文字图案:要求与公司样稿相符,文字、图案必须清晰、牢固;在高温热合后,文字、图案仍清晰,不变色。
印刷位置允许有±1.5mm的偏差,无印刷模糊等缺陷。
3.2.3 洁净度:铝箔外观应洁净,不得有灰尘、杂质等污染。
3.2.4 接头数:每1000m内不多于2个,并在接头处加一标记3.2.5卷面及端面:应缠紧、缠齐,端面应平整,不允许有塔形、错层、松层或管芯自由脱落现象,不允许有严重碰伤、压陷。
3.2.6 绕卷裁切面平整度:保护层、外侧印刷、铝箔基材值均小于1mm。
3.2.7 针孔度:不应有密集的、连续性的、周期性的针孔,1m2中d>0.3mm不允许有,d=0.1-0.3mm不超过1个。
3.2.8外包装:包装箱上应标明产品名称、容量、生产厂名、生产日期、数量、检验者代号等信息,同时包装纸箱不得脏及破损并内衬塑料保护袋,用胶带“工”字形封箱,对于易擦伤的阀或罩子等须用塑料袋、卫生的纸等相隔,出厂前产品必须附出厂检验报告单。
外观检验以目测为主,于正常光源下,30cm距离处目测。
3.3功能(物理机械性能)要求与检测方法:3.3.1粘合层热封强度:其指标应≥5.88N/15mm。
检验方法:按GB 12255-90中6.4.1规定的方法进行。
3.3.2保护层粘合性其胶带试验应无明显剥落现象。
:检验方法:按GB 12255-90中6.4.2规定的方法进行。
3.3.3保护层耐热性:在200℃时,应无明显粘落。
GMP质量体系铝箔检验操作规程

GMP质量体系铝箔检验操作规程GMP质量体系是指药品生产企业建立完善的质量管理体系,确保产品符合GMP规范。
铝箔是药品包装的常用材料之一,对其进行检验以确保其质量符合要求是非常重要的。
本文将会详细介绍GMP质量体系下铝箔检验的操作规程。
一、检验设备和仪器1.精密天平:用于测量铝箔的重量。
2.厚度测量仪:用于测量铝箔的厚度。
3.强度试验仪:用于检测铝箔的强度和抗拉性能。
4.疲劳试验机:用于测试铝箔的疲劳寿命和延展性。
5.高温烘箱:用于测试铝箔在高温下的稳定性和耐热性。
6.外观检查灯箱:用于进行铝箔外观的检查。
二、操作规程1.样品的选择和准备1.1根据标准规定,选择代表性的样品进行检验。
1.2将样品从仓库中取出,注意避免样品受潮、变形和受到其他污染。
1.3将样品编号,并记录样品的相关信息,如生产批号、生产日期等。
2.外观检查2.1将样品放置在外观检查灯箱下,观察铝箔的外观,检查是否有瑕疵、氧化、污染、损坏等。
2.2记录观察结果,并根据标准规定进行评价和分类。
3.重量测量3.1使用精密天平将铝箔样品放置,并记录初始重量。
3.2将氧化膜或其他不符合要求的部分去除,再次称重,并记录。
3.3根据标准规定,计算铝箔的净重,并与标准要求进行对比。
4.厚度测量4.1使用厚度测量仪测量铝箔的厚度,并记录结果。
4.2根据标准要求,对测量结果进行评价和分类。
5.强度和抗拉性能测试5.1将样品切割成标准尺寸的试样。
5.2使用强度试验仪进行试样的强度和抗拉性能测试,并记录测试结果。
5.3根据标准要求,对测试结果进行评价和分类。
6.疲劳测试6.1将试样放置在疲劳试验机上,并进行疲劳寿命和延展性测试。
6.2记录测试结果,并根据标准要求进行评价和分类。
7.高温稳定性测试7.1将铝箔样品放置在高温烘箱中,根据标准要求设定温度、时间。
7.2取出样品,观察其外观和性能变化,并记录结果。
7.3根据标准要求,对测试结果进行评价和分类。
8.结果分析和报告8.1根据各项检验结果,对样品的质量进行评价和分类,并生成检验报告。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
药品包装用铝箔检验操
作规程
Document number:PBGCG-0857-BTDO-0089-PTT1998
药品包装用铝箔检验操作规程
1适用范围
本标准适用于进厂药品包装用铝箔的检验。
2职责
检验员:严格按本操作规程检验进厂药品包装用铝箔。
QC主管:监督检查执行情况。
3品种
保护层/铝箔基材/粘合层。
4规格尺寸及偏差
取1m药品包装用铝箔用精度为的千分尺测定两边、中间等各部位的厚度,用精度为的直尺测定其宽度,共测6处,其结果应符合下表要求。
若有一项不合格,则该卷为不合格。
5外观质量
5.1.取1m药品包装用铝箔检验,应符合下列要求。
5.2.针孔度检查
5.2.1.仪器设备
针孔检查台:在适当体积的木箱内安装30W日光灯,木箱上面放一块
玻璃板,玻璃板衬黑纸并留有400mm×250mm空间以检查试样的针孔。
5.2.2.检查方法
在成品中取长400mm(当宽小于250mm时取卷幅宽)试样10张,逐
张放在针孔检查台上,在暗处检查其针孔。
5.2.3.结果判断
5.2.3.1.不应有密集的、连续性的、周期性的针孔。
1m2中d>不允许;d=不超
过1个。
5.2.3.2.针孔度检查如有一张不合格,可重复取样检验,如仍为不合格,则该卷
为不合格品。
6印刷质量
6.1.印刷文字、图案
印刷文字、图案应正确、清晰、牢固。
在高温热合后,文字、图案仍清晰,不变色。
6.2.印刷错位
用分度值为的直尺测量,应在指定位置±内。
6.3.文字内容及图案
与标准样张核对,文字、图案、符号应无错漏。
6.4.印刷色泽
色泽均匀,与标准样张核对,同批及不同批之间不允许有明显色差。
备注:凡无文字、图案的铝箔不检查.、.、.项。
7微生物限度
7.1.供试品的制备
用开口面积为20 cm2的消毒过的金属模板压在试样的内层面上,将无菌棉签用无菌生理盐水稍沾湿,在板孔范围内擦抹5次,换1支棉签再擦抹5次,每个位置用2支棉签共擦抹10次。
共擦抹5个位置100 cm2。
每支棉签擦抹完后立即剪断,投入30ml无菌生理盐水中。
待全部棉签均投入瓶中后,将瓶迅速摇晃1min,静置10min,即得1:1供试液。
7.2.操作方法:按《微生物限度检查SOP》(1302·005)检查。
7.3.判定
7.3.1.细菌总数不得过1000个/100cm2,霉菌总数不得过100个/100cm2,大肠
杆菌及活螨不得检出,则判符合规定。
7.3.2.若任何一项超出规定,则判不符合规定。
8取样:按《物料取样SOP》(1302·001)、GB2828取样检验。
9编号:B-002
10用途:用于固体制剂铝塑包装。
11复检周期:第一次复检周期6个月,第二次复检周期6个月。
12编制依据:
《药品包装用铝箔质量标准》1103·002
《中国药典》2000年版附录。
