电解与极化作用-学生
10电解和极化作用

Pt │ H2(g) │ H+(aq) │O2(g) │ Pt
RT 1 E反 E ln pH2 pO2 2F p p
V实 际 V理 论
要使电解池顺利地进行连续反应,除了克服作 为原电池时的可逆电动势外,还要克服由于极化在 阴、阳极上产生的超电势 (阴) 和 (阳) ,以及克服电
H 高的金属:Pb, Cd , Hg , Zn, Bi , Sn 2 H 2 居中的金属:Fe , Co, Ni , Cu,W , Au H 2 低的金属:Pt , Pd
阳极上的反应 电解时阳极上发生氧化反应。发生 氧化的物质通常有:(1)阴离子,如 Cl , OH 等, (2)阳极本身发生氧化。 (1) 金属的溶解反应顺序直接以φe判断(不考虑超电势) (2) 析氧反应:要考虑超电势 当i=10A∙m-2时,析氧的超电势在不同金属上的超电势
+
(1) 金属的析出反应顺序直接以φe判断(不考虑超电势) (2) 析氢反应:要考虑超电势
氢超电势的Tafel方程:η= a + b lg J 式中,a、b为经验常数,称为Tafel常量。其中, a与电极材料、表面状态、溶液组成、温度等有关。 b对大多数金属来说,值相近,约为0.116V。 所以,氢超电势的大小主要由a决定。a越大,氢 超电势越大。
大小顺序如下:Co<Fe<Cu<Ni<Cd<Pt
从超电势的大小来看,用Pt作为阴阳极的电极材料,可 以有效阻止析氧反应和析氢反应的发生,尽可能保证 金属的溶解和析出反应顺序不受干扰。
三 电解过程的应用 注意事项:
①考虑阴阳极的所有反应
②随电解的进行,溶液浓度改变, 电极电势会随之 发生变化, 实际分解电压也会有相应变化
第十章电解与极化作用

第十章 电解与极化作用【复习题】【1】什么叫分解电压?它在数值上与理论分解电压(即原电池的可逆电动势)有何不同?实际操作时用的分解电压要克服哪几种阻力?【答】 分解电压就是能使某电解质溶液连续不断地发生发生明显电解时所必须的最小外加电压。
实际上,分解电压要大于原电池的可逆电动势E 可逆。
E (实际分解)=E (理论分解)+η(阳)+η(阴)+IR 。
所以在实际操作时不仅要克服理论分解电压,还要克服极化和电阻引起的电势降等阻力,其中主要是由于电极的极化作用所致。
【2】产生极化作用的原因主要有哪几种?原电池和电解池的极化现象有何不同? 【答】极化作用的类型有很多,主要有浓差极化和化学极化等。
对于原电池,随着电流密度的增大,由于极化作用,负极的电极电势比可逆电势越来越大,正极的电极电势比可逆电势越来越小,两条曲线有相互靠近的趋势,原电池的电动势逐渐减小。
对于电解池,随着电流密度的增大,由于极化作用,阴极的电极电势比可逆电势越来越负,阳极的电极电势比可逆电势越来越正,两条曲线有相互远离的趋势,电解池的外加电压逐渐增大。
【3】什么叫超电势?它是怎么产生的?如何降低超电势的数值?【答】 在有电流通过电极时,电极电势偏离于平衡值的现象称为电极的极化,为了明确地表示出电极极化的状况,常把某一电流密度下的电势ψ不可逆与ψ平之间的差值称为超电势,它的产生有浓差极化、化学极化和电阻极化(电解过程中在电极表面上生成一层氧化物的薄膜或其他物质)。
在外加电压不太大的情况下,将溶液剧烈搅动可以将低浓差极化,设法降低溶液内阻可以将低电阻极化,还可以加入去极化剂可以将低化学极化。
【4】析出电势与电极的平衡电势有何不同?由于超电势的存在,使电解池阴、阳极的析出电势如何变化?使原电池正、负极的电极电势如何变化?超电势的存在有何不利和有利之处?【答】由于超电势的存在,在实际电解时要使正离子在阴极析出,外加于阴极的电势要比平衡电势更负一些;要使负离子在阳极析出,外加于阳极的电势必须比可逆电极的电势更正一些,即:ϕϕηϕϕη=+=-阳阳,析出阳,可逆阴阴,析出阴,可逆对于电解池,由于超电势的存在,阴极的析出电势会更负,阳极的析出电势会更正,外加电压要更大,所消耗的能量就越多。
电解与极化作用习题及答案

电解与极化作用习题及答案电解与极化作用习题及答案电解和极化是化学中重要的概念,它们在电化学、电解池和电池等领域中起着关键作用。
本文将介绍一些与电解和极化相关的习题,并提供相应的答案,帮助读者巩固和加深对这些概念的理解。
习题一:什么是电解?请简要解释电解的过程。
答案:电解是指在电解质溶液或熔融状态下,通过外加电压使溶液中的离子发生氧化还原反应的过程。
电解过程中,正极(阳极)发生氧化反应,负极(阴极)发生还原反应。
电解是一种将电能转化为化学能的过程。
习题二:什么是极化?请简要解释极化现象的产生原因。
答案:极化是指在电解质溶液或电解池中,极板表面产生的电荷分布不均匀的现象。
极化现象的产生原因主要有两个:电解质溶液中的离子在电场作用下会向电极移动,导致电极表面聚集正负离子;同时,电极表面的化学反应会导致电极上生成一层物质,阻碍离子在电极表面的移动,从而引起极化。
习题三:电解铜(II)硫酸溶液时,正极和负极上分别发生什么反应?写出反应方程式。
答案:正极上发生的反应是Cu2+离子还原为Cu金属,反应方程式为:Cu2+ + 2e- -> Cu负极上发生的反应是水分子还原为氢气和氢氧根离子,反应方程式为:2H2O + 2e- -> H2 + 2OH-习题四:在电解银氨溶液时,正极和负极上分别发生什么反应?写出反应方程式。
答案:正极上发生的反应是Ag+离子还原为Ag金属,反应方程式为:Ag+ + e- -> Ag负极上发生的反应是水分子还原为氢气和氢氧根离子,反应方程式为:2H2O + 2e- -> H2 + 2OH-习题五:电解池中,正极和负极上的电子流动方向分别是什么?为什么?答案:在电解池中,正极上的电子流动方向是从电解质溶液向电极流动,负极上的电子流动方向是从电极向电解质溶液流动。
这是因为正极是氧化反应发生的地方,需要电子供给;负极是还原反应发生的地方,需要电子接受。
习题六:电解质溶液中的离子浓度对电解过程有何影响?请简要解释。
11章电解池与极化作用全解

可逆电池:电极反应是在电流趋于零的平衡条件 下进行的,此时的电极电势为可逆电 极电势或平衡电极电势。
实际上电池对外供电或进行电解时,都有一定的电流 通过电极,使电极反应在偏离平衡态下进行而成为不 可逆过程,导致电极电势也偏离平衡电极电势。现以 电解池为例讨论这种偏离现象产生的原因及在实际中 的意义。
由于化学反应本身的迟缓性而引起的的电极极化。
电极反应总是分若干步进行,若其中一步反应速
率较慢,需要较高的活化能。为了使电极反应顺利进
行所额外施加的电压称为称为活化超电势。
例:2H+ + e– H2
e
v反应 慢,阴极积累电子e- 2H+ + 2e– H2
电化学极化使阴极电势降低,使阳极电势升高
两种极化结果均使 阴极电势降低
7
§11.2 极化作用
1. 电极的极化
定义:电流通过电极时,电极电势偏离其平衡电极 电势的现象称为电极的极化。
阳极极化: E阳 E阳, 平 使 E阳 变大(正) 阴极极化: E阴 E阴, 平 使 E阴 变小(负)
离子扩散速率慢 浓差极化 极化产生的原因:
反应速率慢 电化学极化
8
(1) 浓差极化 由于电极表面附近薄液层的浓度和本体溶液的 浓度的差异所导致的电极极化。
所以标准氢电极中的 铂电极要镀上铂黑。
影响超电势的因素很多,如电极材料、电极表面状态、电
流密度、温度、电解质的性质、浓度及溶液中的杂质等。
14
Tafel 公式(Tafel’s equation)
早在1905年,Tafel 发现,对于一些常见的电 极反应,超电势与电流密度之间在一定范围内存 在如下的定量关系:
电解与极化作用

第九章 电解与极化作用前边讨论的电池与电极都是可逆的,那么应用能斯特公式来处理电化学体系时,它的前提就是该体系必须是处于热力学平衡态,但是对于一些现实的电化学过程来说一般都是不可逆过程,因此应用Nernst 公式研究电化学问题就具有很大的局限性。
事实上当原电池或电解池,只要有电流通过,就有极化作用发生,该过程就是不可逆过程。
研究不可逆电极反应及其规律性对电化学工业是十分重要的,所以我们要讨论不可逆电极过程。
在这一部分除了讨论电解池中的极化作用外,还要简单介绍一些电解在工业上的应用上及金属的防腐和化学电源等。
§9-1 电极的极化1、不可逆条件下的电极电势一个不可逆电池所具备的条件有两个:①电池反应在充电与放电时互为逆反应;②通过电池的电流I →0,即没有电流通过电池。
显然组成可逆电池的两个电极都是可逆电极,那么可逆电极的电极反应都是在可逆的条件下发生的。
这时电极所具有的电势就称为可逆电极电势。
可逆电极电势对许多电化学和热力学问题的解决是相当重要的。
但是在实践当中许多电化学过程,如进行电解和使用化学电源做电功时,并不是在可逆情况下进行的,也就是说要有电流通过电池或电解池,此时的电极反应就是不可逆的了,不可逆电极的电极电势用“I ϕ”表示,当然这个电极电势与可逆电极的电极电势r ϕ是不相同的,那么我们就把电极在有限电流通过时所表现的电极电位I ϕ与可逆电极电势产生偏差的现象叫做电极的极化。
偏差的大小(绝对值),称为“过电势”。
用“η”表示,||r I ηϕϕ=-,对于原电池,在可逆放电时,两电极的端电压是最大的,这个端电压就是电动势E ,它等于两个可逆电极的电位差。
()()()()r r r r E ϕϕϕϕ=-=-正阳阴负在不可逆条件下进行放电,两电极的端电压用E I 表示,它一定要小于原电池的电动势E ,E I <E ,E I =E-△E其电动势的降低主要是由于两个因素引起的,当有电流通过时, ①电池具有一定的内阻R 的消耗电位降IR ;②不可逆条件电极要产生极化,也会造成电动势下降,所以不可逆电池两电极的电位差通常就叫端电压。
物理化学课件6.3章电解与极化作用

实验材料
电解槽、电极、电源、电解质溶液等。
电解实验的设计与操作
实验步骤 1. 准备实验材料,配置电解质溶液。
2. 将电极插入电解槽中,连接电源。
电解实验的设计与操作
3. 观察并记录电极反应现象,测量电流和电压。 4. 分析实验数据,得出结论。
极化作用的实验研究方法
实验目的
通过实验研究,探究极化作用对电极反应的影响,理解极化作用的原理。
电解分离与提纯
总结词
电解分离和提纯是利用电解的原理将混 合物中的不同组分进行分离或提纯的方 法。
VS
详细描述
电解分离是通过电解过程中不同物质在电 极上的吸附、氧化还原反应等特性差异实 现分离。电解提纯则是利用电解过程将杂 质去除,实现物质的纯化。
05 极化作用的应用
电化学反应器
电解槽
利用电解原理进行物质转 化的设备,如氯碱工业中 的隔膜电解槽和电解水制 氢装置。
详细描述
电镀是将金属离子在电场作用下还原成金属并沉积在阴极表面,用于表面防护和装饰。电冶金则是利 用电解过程提取金属,从矿石或盐类等原料中分离和提纯金属。
电解制取气体
总结词
电解水是制取氢气和氧气的常用 方法,具有清洁、高效的特点。
详细描述
通过电解水可以将水分子分解成 氢气和氧气,分别在阴极和阳极 析出。电解水制取的气体可用于 燃料电池、医疗、潜水等领域。
电极反应的极化曲线
极化曲线是描述电极电势与电流密度之间关系的曲线,可以用来研究电极反应的动 力学过程和机理。
在极化曲线上,可以根据电流密度的大小来判断电极反应的速率快慢,以及电极电 势偏离可逆电势的程度。
通过测量不同温度下的极化曲线,可以研究电极反应的热力学性质和动力学过程。
电解与极化作用

物理化学论文电解与极化作用化工093班姓名:李寒萌学号:12 号电解与极化作用一、分解电压使电能转变成化学能的装置称为电解池。
当直流电通过电解质溶液,正离子向阴极迁移,负离子向阳极迁移,并分别在电极上起还原和氧化反应,从而获得还原产物和氧化产物。
若外加一电压在一个电池上,逐渐增加电压直至使电池中的化学反应发生逆转,这就是电解。
实验表明,对任一电解槽进行电解时,随着外加电压的改变,通过该电解槽的电流亦随之变化。
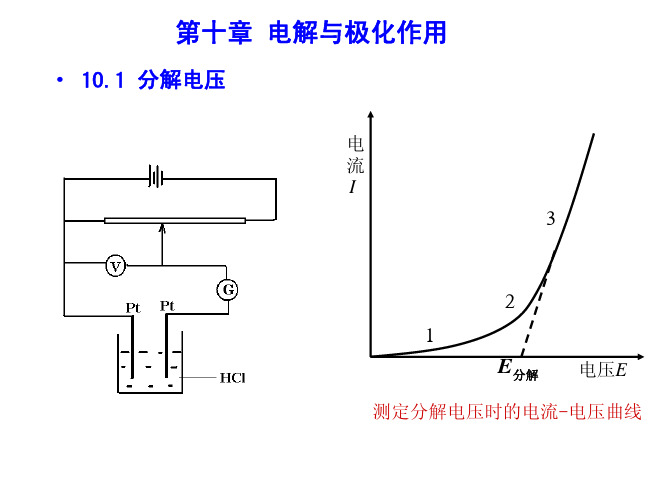
例如,使用两个铂电极电解HCl 溶液时,使用图9.1 的线路装置,改变可变电阻,记录电压表和电流表的读数,则可测量电解槽两端电位差与电流强度的关系曲线。
开始时,当外加电压很小时,几乎没有电流通过电解槽;电压增加,电流略有增加;当电流增加到某一点后,电流随电压增大而急剧上升,同时电极上有连续的气泡逸出。
在两电极上的反应可表示如下:阴极2H+(a H+)+2e.→H2(g, p)阳极2Cl-.(a Cl-)→Cl2(g, p)+2e. 图9.1 分解电压的测定装置当电极上有气泡逸出时,H2和Cl2的压力等于大气压力。
电解过程分析:当开始加外电压时,还没有H2和Cl2生成,它们的压力几乎为零,稍稍增大外压,电极表面上产生了少量的H2和Cl2,压力虽小,但却构成了一个原电池(自发地进行如下反应)(-) H2(p)→2H+ (a H+)+2e-(+) Cl2(g)+2e-→2Cl-(a Cl-)此时,电极上进行反应的方向正好与电解所进行的反应的方向相反。
它产生了一个与外加电压方向相反的反电动势E b。
由于电极上的产物扩散到溶液中了,需要通过极微小的电流使电极产物得到补充。
继续增大外加电压,电极上就有H2和Cl2继续产生并向溶液中扩散,因而电流也有少许增加,相当于图9.2 中I-E 曲线上的1-2段。
此时由于p H2和p Cl2不断增加,对应于外加电压的反电动势也不断增加,直至气体压力增至等于外界大气压力时,电极上就开始有气泡逸出,此时反电动势E b达到最大值E b, max将不再继续增加。
207-223 第十章电解与极化作用

为了不使 H2 析出,问溶液的 pH 值应控制在多少为好?
解:若 E(Zn2+|Zn)>E(H+|H2),则 Zn(S)析出而 H2 不能析出.
即: -0.763V+ 0.5916V lg10−5 >-0.05916V pH-0.75V 2
pH>2.72.
例 3 25°时,用 Zn 电极作为阴极,电解 a±=1 的 ZnSO4 水溶液。
( ) 阳极
H2O ⎯⎯→ 2H+
aH+
+
1 2
O2
(g
)
+
2e−
E阳,析出
=
E O2 H2O H+
+
RT 2F
ln
a2 H+
+O2
= 1.23
V+ RT 2F
ln (0.01)2
+ 0.5
V = 1.612
V
( ) E分解 = E阳,析出 − E阴,析出 = 1.612 + 0.17 V=1.782 V
(1)已知,水溶液为中性,则 Zn2+在 Zn 的平衡电极电势 Ee(Zn2+|Zn)及 H2 在 Zn 电 极上析出的平衡电极电势 Ee(H+|H2)各位多少?
(2)又知在某一电流密度下,H2 在 Zn 极上的超电势为 0.7 V,则 H2 在 Zn 上实际析出 的电势 EH2=?
(3) 若 Zn 在 Zn 电极上的超电势可忽略不计,则上述电解过程中在 Zn 极上优先析出的 是什么?
E 分解=E 可逆+△E 不可逆+IR 2.产生极化作用的原因主要有哪几种?原电池和电解池的极化现象有何不同? 答:产生极化作用的主要原因是电化学极化和浓差极化。电解时,电流密度愈大,超电 势愈大。外加电压也要增大,所消耗能量越多。原电池放电时,有电流在电极上通过,随着 电流密度增大。由于极化作用,正极比可逆电视愈来愈小,负极比可逆电势愈来愈大,原电 池的电动势逐渐减小,它所能作的电功逐渐减小。 3.什么叫超电势?它是怎样产生的?如何降低超电势的数值? 答:把某一电流密度下的电势 φ 与 不可逆 φ 可逆之间的差值称为超电势,超电势产生的原因 有,电化学极化和浓差极化,及电解过程中,在电极表面形成一层氧化膜或其他物质,从而 对电流的通过产生阻力(电阻超电势),在外加电压不大的情况下,把溶液剧烈搅动可以降 低浓差极化,但由于电极表面扩散层的存在,不可能把浓差极化完全除去。除此之外,还可 以加入去极化剂和减小体系的阴值 R 来减低超电势的值。 4.析出电势与电极的平衡电势有何不同?由于超电势的存在,使电解池阴、阳极的析出
第十章 电解与极化作用

电解过程中在两电极上实际发生的反应为: 阴极 2H+(aq)+ 2e- → H2(g) 阳极 2OH- →H2O(l) +O2(g) +2e由于阴极和阳极上分别生成氢气和氧气,因此也就构 成了一个对抗电解过程的原电池: Pt (s) | H2(g)|H2SO4 (0.5 mol dm-3)|O2 (g) | Pt (s) 该电池的标准电动势为1.229 V,从理论上讲分解电压 应该等于该可逆电池的电动势。 从这个意义上讲此可逆电池的电动势被称为理论分 解电压。实际上只有当外加电压比理论分解电压大一定 数值时,电解才能以明显速率进行。
(b)扩散是指某种粒子从高浓度向低浓度方向转移的现 象。 由于电化学反应,某种离子在电极表面放电,会使 电极表面附近该离子的浓度和本体溶液产生差别。通 常情况下,当阳离子在阴极还原时,电极附近溶液中 该离子浓度小于本体溶液中的浓度;阳极氧化生成某 种离子时,电极附近溶液中该离子浓度要大于本体溶 液中的浓度。应该注意扩散和对流二者的区别,扩散 是指某种粒子相对于溶剂的运动,而对流是指整个液 体(包括溶剂和粒子)的运动。
(c)电迁移是指液相中带电粒子在电场力作用 下引起的迁移。
上述三种传质过程在发生电化学反应的系统都会同时发 生,但在不同位置或不同情况下会有所不同。例如在远 离电极的本体溶液其扩散和电迁移可以忽略不计,主要 发生的是对流;而在电极附近的薄层溶液中扩散或电迁 移起重要作用。当参与反应的粒子在电极表面附近的薄 层溶液中扩散速率为传质控制步骤时引起的极化现象 称之为浓差极化(第2种定义) 。 用搅拌和升温的方法可以减少浓差极化,但也可以 利用滴汞电极上的浓差极化进行极谱分析。
如用银电极电解AgNO3溶液,阴极附近Ag+沉积到银电极 上,使 电极附近的Ag+浓度(ce)比本体溶液的浓度(c)减少。 φ平=φøAg+/Ag-(RT/F)㏑(1/c) φ不可逆=φøAg+/Ag-(RT/F)㏑(1/ce) 因为c>ce,所以φ平,阴>φ不可逆,阴 ,这两个由浓度不 同而产生的电极电势的差值就是浓差超电势(>0)。 阴极 η阴=φ平,阴-φ不可逆,阴 =(RT/F)㏑(c/ce) >0
第十章电解与极化作用本章要求:1.了解分解电压的意义,要使电解池

第十章 电解与极化作用本章要求:1.了解分解电压的意义,要使电解池不断工作必须克服哪几种阻力?2.了解什么是极化现象,什么是超电势?极化作业有哪几种?如何降低极化作用?3.了解电解的一般过程及应用,特别是有关电解分离提纯方面的应用。
4.了解金属腐蚀的类型以防止金属腐蚀的常用方法。
电解池:使电能转变成化学能的装置当一个电池与外接电源反向对接时,只要外加电压大于该电池的电动势E ,电池中的反应逆向发生,原电池就要变成电解池,要使电解池继续正常工作,外加电压要比电池电动势E 大很多,这些额外的电能一部分用来克服电阻,一部分用来克服电极的极化作用极化作用:当电流通过电极时,电极电势偏离其平衡的现象,且该过程是步可逆过程。
§10.1 分解电压在电池上外加一个直流电源,并逐渐增加电压,使电池中的物质在电极上发生化学反应,称为电解。
如电解HCl 水溶液阴极: ).(()p g aH e H H 222→+-++阳极:).(p g Cl e Cl 222→--- 总反应: )()()(p P aq Cl H HCl 222+−−→−电解 分解装置P118图10.1,并绘制电流─电压曲线。
由P118图10. 电流─电压曲线可看出:① 当开始加外电压时,还没有)()(g g Cl H 22和生成,P=0 电路中几乎没有电流通过。
② 当稍增大外电压,电极表面有少量)()(g g Cl H 22和产生,其压力虽小,却构成了一个原电池,产生了与外加电压方向相反的反电动b E 由于压力很小,低于大气压力,产生气体不能离开电极自由逸出,而是扩散到溶液中消失,此时此时就需要通入极微小的电流使电极产物得到补充,相当于图1─2段。
③ 继续增大外电压,电极时上)()(g g Cl H 22和继续产生,当22cL H P P 和等于外界大气压力时,电极上开始有气泡逸出,此时反电动势b E 达到了最大值MAX b E 而不在继续增加,若此时继续增大外电压,则电流急曾,如图曲线2─3段直线部分。
10章 电解与极化作用

二、电极极化的原因 有电流通过电极时, 电极上会发生一系列过程(离子 的扩散、电极反应…), 每一步或多或少存在阻力, 要克服这些阻力需要一定的推动力, 反映在电极上表 现为电极电势的偏离. 根据极化产生的不同原因,通常把极化大致分为两类 :浓差极化和电化学极化。 (1)浓差极化 当有限电流通过电极时,由于 离子扩散的迟缓性导致电极表面与本体溶液离子浓
2H (aq) 2e H2 (g) i /A 1 阳极 2OH (aq) H 2 O(l) O 2 (g) 2e 2 对抗电解过程的具有反电动势的原电池: 阴极
(Pt) H2(g)|H2SO4(0.5mol· dm-3)|O2(g)(Pt)
1 O 2 E0 E /V 3
在缄性溶液中:
H2O Me e Me H OH
(b) H3O+和已被吸附电极表面的H原子反应生 成H2; 也为电化学脱附.
H3O Me - H e Me H2 H2O
④ 吸附在电极上的H原子化合为H2
Me H Me H 2Me H2
⑤ H2从电极上扩散到溶液内或形成气泡逸出.
2
2
2
0.894V
2
可见,由于氢超电势的存在,H2析出困难的多; 即使在 pH = 4 的溶液, H2析出也在Cd之后,此时:
H ,析 0.2366 H 0.7166 V
2 2
可见, 由于氢超电势存在, 使得活动次序在H 之 前的活泼金属能优先析出; 甚至Na+在汞阴极上也会 生成钠汞齐, 不会放出H2.
例2 电解 CdSO4(a± = 1) 水溶液, 氢在金属Cd 析出超电势为0.48V. 解: 在阴极上析出反应:
10章_电解与极化作用

(1)电解池中两电极的极化曲线 随着电流密度的增大,两电极上的超电势也增大 阳极析出电势变大 阴极析出电势变小 由于极化使外加的电压增加,额外消耗了电能。
最小电压,称为分解电压。
我们把外加电压等于分解电压时两极的电极电势 分别称为它们的析出电势。
若外加电压大于分解电压,则电流 I = ( V – Emax) /R ,R 指电解池电阻。
以下,我们由表列实验结果,来分析分解电压与原电池的 电动势(即理论分解电压,由能斯特方程算得值)的关系。
表:10.1 几种电解质溶液的分解电压(室温,铂电极)
4.氢超电势
电解质溶液通常用水作溶剂,在电解过程中,H+ 在阴极会与金属离子竞争还原。
利用氢在电极上的超电势,可以使比氢活泼的金 属先在阴极析出,这在电镀工业上是很重要的。
例如,只有控制溶液的pH,利用氢气的析出有超 电势,才使得镀Zn,Sn,Ni,Cr等工艺成为现实。
氢在几种电极上的超电势
从氢气在几种电极上的超电势,在石墨和汞等材 料上,超电势很大,而在金属Pt,特别是镀了铂黑 的铂电极上,超电势很小,所以标准氢电极中的铂电 极要镀上铂黑。
电解质 浓度 c / mol ·dm-3 电解产物
E分解 /V
E理论/ V
HCl
1
HNO3
1
H2SO4
0.5
NaOH
1
CdSO4
0.5
NiCl2
0.5
H2 + Cl2
1.31
1.37
H2 + O2
浙江大学物理化学(甲)第十章(电解与极化作用)

平
0.814 0.799 0.015 V
10
注意: 式中氧电极的标准电极电势为碱性条件 qOH-,O2=0.401V 实际分解电压:E分解=(OH-,O2-Ag+Ag)不可逆 由于浓差极化,使得: 阴极:不可逆> 阳极:不可逆 > 浓差极化使得实际分解电压: E分解=(阳-阴)不可逆 > E理论分解=(阳-阴)平衡 由于浓差极化主要是由离子在溶液中的扩散速率缓慢 引起的,所以可以通过搅拌或升高电解温度,可以降低浓差 极化。
Ag+
AgNO3( m )
8
阴极反应: Ag+ + e Ag (s) 由于Ag+的扩散速率小于Ag+在阴极上的沉积速度,使得在 阴极附近(10-3~10-2cm)Ag+的浓度 me 小于本体溶液的浓 度m。 当 I = 0时,电极的可逆电势为:
θ 可逆 Ag
Ag
RT 1 ln F m(Ag )
14
G
电 极 2 电 极 1
电位计
甘汞电极 电解质溶液
① 由电极1、电极2和可变电阻、电源,组成一个电解池。
② 由电极1与甘汞电极组成一个电池。 实验: ① 通过调节可变电阻,逐渐改变加到电解池上的电压, 通过电流计测出流经电解池的电流密度J。 ② 由电位计测出在电流密度为J时,电池的电动势E
15
2
通过本章电极极化的讨论,结合前一章可逆电池的平衡 性质,才能比较全面地分析、解决电化学的问题。
本章主要介绍三方面的内容: (1)电极的极化作用
(2)金属腐蚀与防腐和电化学的应用 (3)化学电源 §10.1 分解电压 1. 分解电压测定 在电解一给定的电解液时,对电解池至少需要施加多 少大的电压才能使电解顺利进行分解电压。 以铂电极电解0.1mol· -3的NaOH水溶液为例,说明 dm 分解电压的测定。
10-物化-下-第十章-电解与极化作用

根据Tafel 公式,η~lnj 为直线,j (<1) →0,η→―∞, 与事实不符。当j→0,η→0,φ不可逆→ φ可逆。 即电流密度很小时,氢超电势不符合Tafel 公式,而遵守 η=ωj 即η与j成正比。 电解时H 在阴极放电机理: 电解时 +在阴极放电机理:(p.125) 对氢超电势研究较多的原因: 对氢超电势研究较多的原因: (p.126)
a
M
,2
a a
M
Z+
,1 ,2
= 10
7
M
Z+
若以溶液中的残余量小于 10-7mol/l 作为判断是否分离彻底 的标准,只须计算出当溶液中某种金属离子的浓度从1~10-7 mol/l 变化时电极电势的差值,即可将浓度差值转化到电势的 差值来进行判断。 当 浓度为c1时,φ1=φө+(0.059/z)lgc1 ; 当 浓度为c2时,φ2=φө+(0.059/z)lgc2 ; 若 c1=10-7mol/l ,c2=1mol/l , ∆φ=φ2-φ1=(0.059/z)lg(c2/c1)= (0.059×7)/z 则:当 z=1 时, ∆φ=0.41 伏 当 = = 当 z=2 时, ∆φ=0.21 伏 = = 当 z=3 时, ∆φ=0.14 伏 = = 利用上述原理,也可使两种离子同时在阴极上析出而形成 合金,即调整两种离子的浓度,使其具有相等的析出电势。
练习题: 练习题 1. 298K和pө下,用Zn电极电解含Zn2+的水溶液。若要使 Zn2+的浓度降到10-7mol/kg时才允许H2(g)析出,问应如何控制 溶液的pH值?设H2 (g)在Zn (s)上的超电势为0.7V并假定此值与 溶液浓度无关;已知:φө(Zn2+/Zn)=-0.763V,假定各离子活 度系数均为1。 解: Zn2+的浓度为10-7mol/kg时 φ(Zn2+/Zn)=φө(Zn2+/Zn) +(RT/2F)lna(Zn2+) =-0.736+(RT/2F)ln10-7=-0.97V φ(Zn2+/Zn) =φ(H+/H2)析 =φ(H+/H2)平=φө (H+/H2)+(RT/2F)lna(H+ )2-η -0.97 =-0.05916pH-0.7 pH = 4.56
物理化学09章电解与极化作用

离的目的。
为了使分离效果较好,后一种离子反应时,前一种
离子的活度应减少到107 以下,这样要求两种离子的析出
电势相差一定的数值。
当 z 1 E 0.41V
E RT ln107 zF
z 2 E 0.21V z 3 E 0.14V
上一内容 下一内容 回主目录
返回
3/26/2020
9.3 电解时电极上的反应
极化曲线(polarization curve)
上一内容 下一内容 回主目录
返回
3/26/2020
氢超电势
电解质溶液通常用水作溶剂,在电解过程中,H+ 在阴极会与金属离子竞争还原。
利用氢在电极上的超电势,可以使比氢活泼的金 属先在阴极析出,这在电镀工业上是很重要的。
例如,只有控制溶液的pH,利用氢气的析出有超 电势,才使得镀Zn,Sn,Ni,Cr等工艺成为现实。
上一内容 下一内容 回主目录
返回
3/26/2020
氢气在几种电极上的超电势
金属在电极上析出时超电势很小,通常可忽略不 计。而气体,特别是氢气和氧气,超电势值较大。
氢气在几种电极上的超电 势如图所示。可见在石墨和汞 等材料上,超电势很大,而在 金属Pt,特别是镀了铂黑的铂电 极上,超电势很小,所以标准 氢电极中的铂电极要镀上铂黑。
(1)电解池中两电极的极化曲线
随着电流密度的增大,两 电极上的超电势也增大,阳极 析出电势变大,阴极析出电势 变小,使外加的电压增加,额 外消耗了电能。
上一内容 下一内容 回主目录
返回
3/26/2020
极化曲线(polarization curve)
上一内容 下一内容 回主目录
返回
3/26/2020
物理化学第十章 电解与极化作用
3、析出电势 :
ϕ阳,不可逆 = ϕ阳,析出 = ϕ阳,可逆 + η阳 ϕ阴,不可逆 = ϕ阴,析出 = ϕ阴,可逆 − η阴
三、极化曲线-超电势的测定 1、测定超电势的装置
2、电解池中两电极的极化曲线
j(电流密度)
阴极曲线
阳极曲线
E可逆+ΔE不可逆
E可逆
η阴
η阳
电
−ϕ
+ϕ
电解池中两电极的极化曲线
正极: 负极:
LiCoO 2 , LiNiO 2 , LiMn 2 O 2
石墨,焦炭
2
正极反应: L i C o O
+
充 + Z Z Z X L i C o O + x L i + YZ Z Z 1 -x 2 放 −
充 ZZZ X Li C 负极反应: C+xLi + xe YZZ Z x 放
总反应:
Ag + (a ) Ag ( s ) Ag + (a ) + e − → Ag ( s ) RT 没有电流通过时 : ϕ Ag + / Ag (可逆) = ϕ + + ln a Ag + Ag / Ag F RT θ 有电流通过时:ϕ Ag + / Ag (不可逆) =ϕ + + ln a’ + Ag / Ag Ag F 扩散速度小于电极反应速度,a’ + < a Ag +
3、原电池中两电极的极化曲线
η阳
j(电流密度)
E可逆 -ΔE不可
η阴
负 极 曲 线 E可逆
正 3;ϕ
电解池中两电极的极化曲
4、氢超电势
第十章 电解与极化作用

2017/11/22
Shenming
6
第十章 电解与极化作用
当 外 压 增 至 23 段 , 氢气和氧气的压力等于 大气压力,呈气泡逸出, 反电动势达极大值 Eb,max。 再增加电压,使I 迅速增加。将直线外延 至 I =0 处,得 E( 分解 ) 值,这是使电解池不断 工作所必需外加的最小 电压,称为分解电压。
物理化学
Physical Chemistry
第十章 电解与极化作用
在实际的电化学过程中,无论是把电能转 变成化学能,还是把化学能转变成电能,即不
论是电解池还是原电池,都不可能在没有电流
通过的情况下运行,因为 I→0意味着没有任何 生产价值。因此,实际过程中的电极是有电流 通过的,即实际的电极过程是不可逆电极过程, 这种情况下的电极电势叫不可逆电极电势。 2017/11/22
见教材p126-129。
Shenming
27
第十章 电解与极化作用
§10.3 电解时电极上的竞争反应 一、 析出电势
在一个指定的电解池中,每一种离子从溶液中析出 时的电极电势称为相应物质的析出电势。它所对应的是 实际电极电势,在一定温度下析出电势既与溶液的浓度 有关,也与超电势有关。因而析出电势是前面所讲的不 可逆电极电势或实际电解时的电极电势。 实际分解电压 确定了阳极、阴极析出的物质后,将两 者的析出电势相减,就得到了实际分解电压。因为电解 池中阳极是正极,电极电势较高,所以用阳极析出电势 减去阴极析出电势。
26
第十章 电解与极化作用
历史上对氢的超电势研究较多的原因:
(1)在许多实际的电化学系统中均会遇到氢的 氧化还原反应; (2)在水溶液电镀工业中,氢在阴极上析出是 不可避免的副反应; (3)金属腐蚀过程与氢的氧化还原过程密切相关;
电解和极化作用

金属型电解质
在熔融状态下能导电的金 属氧化物,如氧化铝、氧 化铁等。
电解质的导电性
电离程度
电解质在水溶液中的导电能力与其电离程度成正 比,电离程度越大,导电能力越强。
带电粒子
电解质在水溶液中导电依赖于带电粒子的运动, 带电粒子越多,导电能力越强。
离子迁移率
带电粒子在电场作用下的迁移率决定了电解质的 导电能力,迁移率越大,导电能力越强。
对物质导电性的影响
01
极化作用可以改变物质内部的电子分布,从而影响物质的导电
性能。
对物质介电常数的影响
02
介电常数是表征物质电介质性能的重要参数,极化作用可以显
著改变物质的介电常数。
对物质光学性质的影响
03
由于极化作用可以改变物质内部电子云的分布,因此对物质的
光学性质如折射率、反射率等也有重要影响。
对未来研究的展望
随着对电解和极化作用认识的深入,未来研究将更加 关注复杂电化学体系的反应机制和动力学过程,以揭
示更广泛的规律和现象。
输标02入题
新型电化学电极材料和电解质的研发将为电解和极化 作用提供更多可能性,有助于提高电化学过程的效率 和稳定性。
01
03
随着可持续发展理念的深入人心,电解和极化作用在 可再生能源转换和储存、环境治理等方面的应用将得
当物质处于外电场中时,物质中 的电荷会受到电场力的作用,产 生相对位移,导致极化现象的产
生。
热运动的影响
在热运动的作用下,物质中的原子 或分子的电子云分布会发生不规则 的涨落,从而导致极化现象的产生。
晶体结构的作用
物质的晶体结构对其极化性质也有 重要影响,不同晶体结构的物质具 有不同的极化率。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4801
电池 Pb(s)│H2SO4(m)│PbO2(s),作为原电池时,负极是,正极是;作为电解池时,阳极是,阴极是。
4802
当电池的电压小于它的开路电动势时,则表示电池在: ( )
(A) 放电
(B) 充电
(C) 没有工作
(D) 交替地充放电
4815
电解HNO3, H2SO4, NaOH, NH3·H2O, 其理论分解电压均为1.23 V。
其原因是
_________________________________________________________。
4816
从理论上分析电解时的分解电压, E分解=__________________________, 而且随电流强度I的增加而_____________。
4851
电化学中电极反应的速度以 ______ 表示,极化是 _________________________
的现象,极化主要有 _________, _________。
超电势是。
4855
当发生极化现象时,两电极的电极电势将发生如下变化: ( )
(A) φ平,阳>φ阳;φ平,阴>φ阴
(B) φ平,阳<φ阳;φ平,阴>φ阴
(C) φ平,阳<φ阳;平,阴<φ阴
(D) φ平,阳>φ阳;φ平,阴<φ阴
4857 298 K、0.1 mol·dm-3的 HCl 溶液中,氢电极的热力学电势为 -0.06 V,电解此溶液
为: ( )
时,氢在铜电极上的析出电势φ
H2
(A) 大于 -0.06 V
(B) 等于 -0.06 V
(C) 小于 -0.06 V
(D) 不能判定
4858 电池放电时,随电流密度增加阳极电位变 ________,阴极电位变 ________,正
极变 ________ ,负极变_____。
4859 电解过程中,极化作用使消耗的电能 ________;在金属的电化学腐蚀过程中,极
化作用使腐蚀速度 ________ 。
4860 (1) 设阳极和阴极的超电势均为 0.7 V,还原电位均为 1.20 V,则阳极电位等
于__________ ,阴极电位等于__________ 。
(2) 电池充电时,充电电压比平衡电动势高、低还是相等 _________ 。
4866 氢气在金属电极上析出时, 根据条件不同, 超电势随电流密度变化关系分别可用=R e j或
=a + b lg j表示, 前者适用于情况, 而后者适用于____________情况。
4870 Tafel公式=a+blg j 的适用范围是: ( )
(A) 仅限于氢超电势
(B) 仅限于j 0, 电极电势稍有偏差的情况
(C) 仅限于阴极超电势, 可以是析出氢, 也可以是其他
(D) 可以是阴极超电势, 也可以是阳极超电势
4889 下列示意图描述了原电池和电解池中电极的极化规律, 其中表示原电池阳极的是:
( )
(A) 曲线1 (B) 曲线2
(C) 曲线3 (D) 曲线4
4908 某含有 Ag+,Ni2+ ,Cd2+ (活度均为1)离子的pH = 2 的溶液,电解时, H2与各金属在阴极析出的先后顺序为 ________、________、_________、__________。
(已知φө (Ag+/Ag)= 0.799 V,φө (Ni2+/Ni)= -0.23 V,φө (Cd2+/Cd)= -0.402 V 。
H2在 Ag 上超电势=0.20 V,在 Ni 上, =0.24 V,在 Cd 上, =0.30 V)
4909 以 Cu 为电极,电解 1 mol·dm-3 CuSO4溶液 (pH = 3), 则在阴极上的电极反应
_________________________,阳极上的电极反应 _________________________ 。
已知: H2在 Cu 电极上, = 0.5 V, φө (Cu2+/Cu)= 0.337 V ,
O2在 Cu 电极上, = 0 V, φө (O2/H+,H2O)= 1.229 V 。
4910 以石墨为阳极,电解 0.01 mol·kg-1 NaCl 溶液,在阳极上首先析出: ( )
(A) Cl2 (B) O2
(C) Cl2与 O2混合气体 (D) 无气体析出
已知:φө (Cl2/Cl-)= 1.36 V , (Cl2)= 0 V ,
φө (O2/OH-)= 0.401V , (O2) = 0.8 V 。
4921 电解金属盐的水溶液时, 在阴极上: ( )
(A) 还原电势愈正的粒子愈容易析出
(B) 还原电势与其超电势之代数和愈正的粒子愈容易析出
(C) 还原电势愈负的粒子愈容易析出
(D) 还原电势与其超电势之和愈负的粒子愈容易析出
4925 电解氢氧化钾溶液,制备氢气和氧气的阳极反应是 _________________________ ;
阴极反应是 _________________________ 。
4932 用铜电极电解 0.1mol·kg-1的 CuCl2水溶液,阳极上的反应为 ( )
(A) 2Cl- ─→ Cl2+ 2e-
(B) Cu ─→ Cu2++ 2e-
(C) Cu ─→ Cu++ e-
(D) 2OH-─→ H2O + 1
2
O2+ 2e-
4940 25℃时, H2在锌上的超电势为 0.7 V,φө (Zn2+/Zn) = -0.763 V,电解一含有
Zn2+(a=0.01) 的溶液,为了不使 H2析出,溶液的 pH值至少应控制在 ( )
(A) pH > 2.06
(B) pH > 2.72
(C) pH > 7.10
(D) pH > 8.02
4946 电解时, 在阳极上首先发生氧化作用而放电的是: ( ) (A) 标准还原电势最大者
(B) 标准还原电势最小者
(C) 考虑极化后,实际上的不可逆还原电势最大者
(D) 考虑极化后,实际上的不可逆还原电势最小者
4947 通电于含有相同浓度的Fe2+, Ca2+, Zn2+, Cu2+的电解质溶液, 已知
φө (Fe2+/ Fe) = -0.440 V ,φө (Ca2+/ Ca) = -2.866 V
φө (Zn2+/ Zn) = -0.7628 V ,φө (Cu2+/ Cu) = 0.337 V
当不考虑超电势时, 在电极上金属析出的次序是: ( )
(A) Cu → Fe → Zn → Ca
(B) Ca → Zn → Fe → Cu
(C) Ca → Fe → Zn → Cu
(D) Ca → Cu → Zn → Fe
4948 金属活性排在H2之前的金属离子, 如Na+ 能优先于H+在汞阴极上析出, 这是由于: ( )
(A) φө (Na+/ Na) <φө (H+/ H2)
(B) (Na) < (H2)
(C) φ(Na+/ Na) <φ(H+/ H2)
(D) H2在汞上析出有很大的超电势, 以至于φ(Na+/ Na) >φ(H+/ H2)
5102 一贮水铁箱上被腐蚀了一个洞,今用一金属片焊接在洞外面以堵漏,为了延长铁
箱的寿命,选用哪种金属片为好? ( )
(A) 铜片 (B) 铁片
(C) 镀锡铁片 (D) 锌片
5106 下列对铁表面防腐方法中属于"电化保护"的是: ( )
(A) 表面喷漆 (B) 电镀
(C) Fe表面上镶嵌Zn块 (D) 加缓蚀剂
5154 将铅蓄电池在 10.0 A 电流下充电 1.5 h,则 PbSO4分解的量为:
(M r(PbSO4)= 303 ) ( )
(A) 0.1696 kg (B) 0.0848 kg
(C) 0.3392 kg (D) 0.3564 kg
5165 电池在恒温、恒压及可逆情况下放电, 则其与环境的热交换为 ( )
(A) r H (B) T r S
(C) 一定为零 (D) 与r H与T r S均无关
5113
铜板上有一些铁的铆钉, 长期暴露在潮湿的空气中, 在_____________________
部位特别容易生锈。
(注:本资料素材和资料部分来自网络,仅供参考。
请预览后才下载,期待您的好评与关注!)。
