化工原理第七章习题答案
化工原理1-7章习题答案

目录第一章流体流动与输送机械 (2)第二章非均相物系分离 (32)第三章传热 (42)第四章蒸发 (69)第五章气体吸收 (73)第六章蒸馏 (95)第七章固体干燥 (119)第一章 流体流动与输送机械1. 某烟道气的组成为CO 2 13%,N 2 76%,H 2O 11%(体积%),试求此混合气体在温度500℃、压力101.3kPa 时的密度。
解:混合气体平均摩尔质量kg/mol 1098.2810)1811.02876.04413.0(33--⨯=⨯⨯+⨯+⨯=∑=i i m M y M ∴ 混合密度333kg/m 457.0)500273(31.81098.28103.101=+⨯⨯⨯⨯==-RT pM ρm m2.已知20℃时苯和甲苯的密度分别为879 kg/m 3和867 kg/m 3,试计算含苯40%及甲苯60%(质量%)的混合液密度。
解:8676.08794.012211+=+=ρρρa a m混合液密度 3kg/m 8.871=m ρ3.某地区大气压力为101.3kPa ,一操作中的吸收塔塔内表压为130kPa 。
若在大气压力为75 kPa 的高原地区操作该吸收塔,且保持塔内绝压相同,则此时表压应为多少?解:''表表绝+p p p p p a a =+=∴kPa 3.15675)1303.101)(''=-==+(-+真表a a p p p p4.如附图所示,密闭容器中存有密度为900 kg/m 3的液体。
容器上方的压力表读数为42kPa ,又在液面下装一压力表,表中心线在测压口以上0.55m ,其读数为58 kPa 。
试计算液面到下方测压口的距离。
解:液面下测压口处压力 gh p z g p p ρρ+=∆+=10题4 附图m 36.255.081.990010)4258(30101=+⨯⨯-=+ρ-=ρ-ρ+=∆∴h g p p g p gh p z5. 如附图所示,敞口容器内盛有不互溶的油和水,油层和水层的厚度分别为700mm 和600mm 。
化工原理课后习题答案第七章吸收习题解答

第七章 吸 收7-1 总压101.3 kPa ,温度25℃时,1000克水中含二氧化硫50克,在此浓度范围内亨利定律适用,通过实验测定其亨利系数E 为4.13 MPa , 试求该溶液上方二氧化硫的平衡分压和相平衡常数m 。
(溶液密度近似取为1000kg/m 3)解:溶质在液相中的摩尔分数:50640.01391000501864x ==+ 二氧化硫的平衡分压:*34.13100.0139kPa=57.41kPa p Ex ==⨯⨯相平衡常数:634.1310Pa40.77101.310PaE m P ⨯===⨯7-2 在逆流喷淋填料塔中用水进行硫化氢气体的吸收,含硫化氢的混合气进口浓度为5%(质量分数),求填料塔出口水溶液中硫化氢的最大浓度。
已知塔内温度为20℃,压强为1.52×105 Pa ,亨利系数E 为48.9MPa 。
解:相平衡常数为:6548.910321.711.5210E m P ⨯===⨯ 硫化氢的混合气进口摩尔浓度:15340.04305953429y ==+若填料塔出口水溶液中硫化氢达最大浓度,在出口处气液相达平衡,即:41max 0.0430 1.3410321.71y x m -===⨯7-3 分析下列过程是吸收过程还是解吸过程,计算其推动力的大小,并在x - y 图上表示。
(1)含NO 2 0.003(摩尔分率)的水溶液和含NO 2 0.06 (摩尔分率) 的混合气接触,总压为101.3kPa ,T=15℃,已知15℃时,NO 2水溶液的亨利系数E =1.68×102 kPa ;(2)气液组成及温度同(1),总压达200kPa (绝对压强)。
解:(1)相平衡常数为:51311.6810Pa 1.658101.310Pa E m P ⨯===⨯ *1 1.6580.0030.00498y m x ==⨯=由于 *y y >,所以该过程是吸收过程。
化工原理第七章干燥课后习题及答案

第七章 干 燥湿空气的性质【7-1】湿空气的总压为.1013kPa ,(1)试计算空气为40℃、相对湿度为%60ϕ=时的湿度与焓;(2)已知湿空气中水蒸气分压为9.3kPa ,求该空气在50℃时的相对湿度ϕ与湿度H 。
解 湿空气总压.1013p kPa =(1).06ϕ=,40℃时水蒸气的饱和蒸气压.7375s p kPa = 湿度 ..../ (067375)06220622002841013067375s s p H kg kg p p ϕϕ⨯==⨯=--⨯.水干气焓 ()..1011882492I H t H =++(...)../= 10118800284402492002841133kJ kg +⨯⨯+⨯= (2) 湿空气中水汽分压.93V p kPa = 50℃时水的饱和蒸气压.1234s p kPa = 相对湿度 ..9307541234V s p p ϕ===. 湿度 . (93)0622=062200629101393V V p H kg kg p p =⨯=--.水/干气 【7-2】空气的总压为101.33kPa ,干球温度为303K ,相对湿度%70ϕ=,试用计算式求空气的下列各参数:(1)湿度H ;(2)饱和湿度s H ;(3)露点d t ;(4)焓I ;(5)空气中的水汽分压V p 。
解 总压.,.101333033007p kPa t K ϕ====℃, (1) 30℃时,水的饱和蒸气压.4241s p kPa = 湿度 ...? (074241)062206220018810133074241s s p H kg kg p p ϕϕ⨯==⨯=--⨯..水/干气(2) 饱和湿度 (4241)0622062200272101334241s s s p H kg kg p p ==⨯=--.水/干气 (3)露点d t 时的饱和湿度.00188s H kg kg =水/干气 .0622ss sp H p p =- (1013300188)2970622062200188s s s pH p kPa H ⨯===++从水的饱和蒸气压为 2.97kPa 查得水的饱和温度为23.3℃,故空气的露点.233℃d t =(4) .3000188t H kg kg ==℃,水/干气时,空气的焓为()..1011882492H H t H =++(...)../= 1011880018830249200188782kJ kg +⨯⨯+⨯=干气 (5) t=30℃时的.4241s p kPa =水汽分压 ...074241297V s p p kPa ϕ==⨯=【7-3】在总压为101.3kPa 下测得湿空气的干球温度为50℃,湿球温度为30℃,试计算湿空气的湿度与水汽分压。
管国峰版化工原理课后习题答案第七章汇总

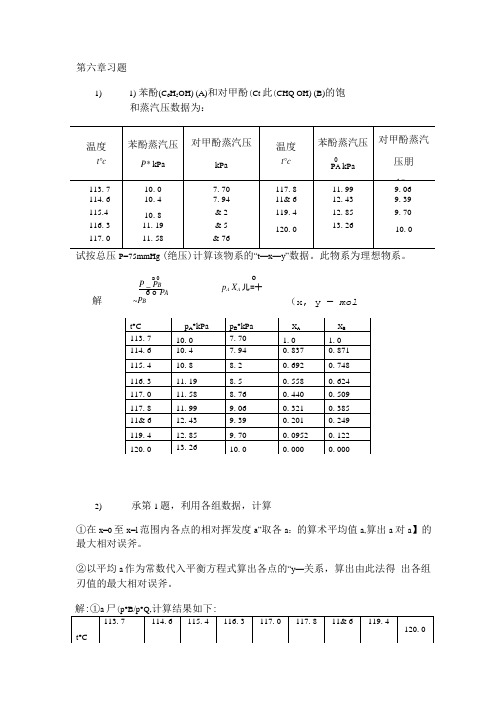
第六章习题1)1)苯酚(CaOH ( A )和对甲酚(C 6H 4 (CH ) O H( B )的饱 和蒸汽压数据为:试按总压P=75mmHg 绝压)计算该物系的“t — x —y ”数据。
此物系为理想物系。
①在X=0至X=1范围内各点的相对挥发度a i ,取各a i 的算术平均值a ,算出a 对a i 的最大相对误差。
②以平均a 作为常数代入平衡方程式算出各点的“ y —X i ”关系,算出由此法得 出各组y i 值的最大相对误差。
解:①a . = ( p 0B / p 0A )j ,计算结果如下:2)承第1题,利用各组数据算P A X AyA= PP A — P B解: X A60-A =1.318最大误差=沁空十6%n1.299c 、a x i2) yi = -------- i----1 中 / a -1) Xia1.318O.—。
. 一2.60咒10」最大误差=0.3853)已知乙苯(A )与苯乙烯(B )的饱和蒸汽压与温度的关系可按下式算得:= 16.0195- 3279.47/59.95) In 必=16.0193- 3328.57/[r- 63.72)式中p 0的单位是mmH ,T 的单位是K 。
问:总压为60mmHg 绝压)时,A 与B 的沸点各为多少C?在上述总压和 65C 时,该物系可视为理想物系。
此物系的平衡汽、液相浓度各为多少摩尔分率?解:令p 0A= P ,算得的t 为A 的沸点Ln60 =16.0195-3279.47/(T -59.95)•••T A =334.95K =61.80C令p 0B = p ,算得的t 为B 的沸点Ln60 =16.0193-3328.57/(T -63.72)「•TB = 342.85K =69.7C2) p= 60mmHg, t = 650C = 338.15K= 16.0195 -3279.47/(338.15 —59.95)Lnp 0B = 16.0193 - 3328.57/(338.15 - 63.72)二 p 0B =48.92mmHgLnp 0A 二 p 0A =68.81mm Hg60-48.92 CL" 68.81X0.557 “cX A = ------------- =0.557 、A = ------------- = 0.63968.81-48.924)苯(A)和甲苯(B)混合液可作为理想溶液,其各纯组分的蒸汽压计算式为1昭去:=6一9011211/0+ 2208)10^ 7?^ = 6.955-1345X^ + 219.5)式中p0的单位是mmH, t的单位是°C。
化工原理 第七章 干燥课后习题及答案

第七章 干 燥湿空气的性质【7-1】湿空气的总压为.1013kPa ,(1)试计算空气为40℃、相对湿度为%60ϕ=时的湿度与焓;(2)已知湿空气中水蒸气分压为9.3kPa ,求该空气在50℃时的相对湿度ϕ与湿度H 。
解 湿空气总压.1013p kPa =(1).06ϕ=,40℃时水蒸气的饱和蒸气压.7375s p kPa = 湿度 ..../ (067375)06220622002841013067375s s p H kg kg p p ϕϕ⨯==⨯=--⨯.水干气焓 ()..1011882492I H t H =++(...)../= 10118800284402492002841133kJ kg +⨯⨯+⨯= (2) 湿空气中水汽分压.93V p kPa = 50℃时水的饱和蒸气压.1234s p kPa = 相对湿度 ..9307541234V s p p ϕ===. 湿度 . (93)0622=062200629101393V V p H kg kg p p =⨯=--.水/干气 【7-2】空气的总压为101.33kPa ,干球温度为303K ,相对湿度%70ϕ=,试用计算式求空气的下列各参数:(1)湿度H ;(2)饱和湿度s H ;(3)露点d t ;(4)焓I ;(5)空气中的水汽分压V p 。
解 总压.,.101333033007p kPa t K ϕ====℃, (1) 30℃时,水的饱和蒸气压.4241s p kPa = 湿度 ...? (074241)062206220018810133074241s s p H kg kg p p ϕϕ⨯==⨯=--⨯..水/干气(2) 饱和湿度 (4241)0622062200272101334241s s s p H kg kg p p ==⨯=--.水/干气 (3)露点d t 时的饱和湿度.00188s H kg kg =水/干气.0622ss sp H p p =- (1013300188)2970622062200188s s s pH p kPa H ⨯===++从水的饱和蒸气压为 2.97kPa 查得水的饱和温度为23.3℃,故空气的露点.233℃d t =(4) .3000188t H kg kg ==℃,水/干气时,空气的焓为()..1011882492H H t H =++(...)../= 1011880018830249200188782kJ kg +⨯⨯+⨯=干气 (5) t=30℃时的.4241s p kPa =水汽分压 ...074241297V s p p kPa ϕ==⨯=【7-3】在总压为101.3kPa 下测得湿空气的干球温度为50℃,湿球温度为30℃,试计算湿空气的湿度与水汽分压。
化工原理 第七章 干燥课后习题及答案

第七章 干 燥湿空气的性质【7-1】湿空气的总压为.1013kP a ,(1)试计算空气为40℃、相对湿度为%60ϕ=时的湿度与焓;(2)已知湿空气中水蒸气分压为9.3kPa ,求该空气在50℃时的相对湿度ϕ与湿度H 。
解 湿空气总压.1013p k P a =(1).06ϕ=,40℃时水蒸气的饱和蒸气压.7375s p k P a = 湿度..../ (0673750622)0622002841013067375ssp H kg kgp p ϕϕ⨯==⨯=--⨯.水干气焓 ()..1011882492I H t H =++ (...)../= 10118800284402492002841133k J k g +⨯⨯+⨯= (2) 湿空气中水汽分压.93V p kPa = 50℃时水的饱和蒸气压.1234s p k P a = 相对湿度 ..9307541234V s p p ϕ===.湿度. (93)0622=062200629101393V Vp H kg kgp p =⨯=--.水/干气【7-2】空气的总压为101.33kPa ,干球温度为303K ,相对湿度%70ϕ=,试用计算式求空气的下列各参数:(1)湿度H ;(2)饱和湿度s H ;(3)露点d t ;(4)焓I ;(5)空气中的水汽分压V p 。
解 总压.,.101333033007p k P a t K ϕ====℃, (1) 30℃时,水的饱和蒸气压.4241s p k P a = 湿度... (0742410622)06220018810133074241ssp H kg kgp p ϕϕ⨯==⨯=--⨯..水/干气 (2) 饱和湿度 (4241)0622062200272101334241s s sp H kg kgp p ==⨯=--.水/干气(3)露点d t 时的饱和湿度.00188s H kg kg =水/干气.0622s s sp H p p =- (10133001882970622062200188)s s spH p kPaH ⨯===++从水的饱和蒸气压为 2.97kPa 查得水的饱和温度为23.3℃,故空气的露点.233℃d t =(4) .3000188t H kg kg ==℃,水/干气时,空气的焓为()..1011882492H H t H=++(...)../= 1011880018830249200188782kJ kg +⨯⨯+⨯=干气 (5) t=30℃时的.4241s p k P a =水汽分压 ...074241297V s p p kPa ϕ==⨯=【7-3】在总压为101.3kPa 下测得湿空气的干球温度为50℃,湿球温度为30℃,试计算湿空气的湿度与水汽分压。
化工原理习题答案第七章

的平衡分压,kPa ; x 为溶液中氧的摩尔分数。
空气中氧的体积分数为 21%,试求 总压为101kPa 时,每m 3水中可溶解多少g 氧?(答:11.4gm",或 耐 m^3 )解:Pe = 0.21 101.3 =21.3kPa ,Pe7-3 .用清水吸收混合气中的 NH 3,进入常压吸收塔的气体含 NH 3体积分数为6%,吸收后气体含NH 3体积分数为0.4%,出口溶液的摩尔比为0.012kmolNH 3 kmol - 水。
此物系的平衡关系为 Y” =2.52X o 气液逆流流动,试求塔顶、塔底处气相推动 力各为多少?(答:顶 厶总= 0.00402,底=0.034 )塔顶气相推动力 Y 2二0.00402,塔底气相推动力 心第=第一丫叩=0.064 —0.03024 = 0.034。
7-4 .用水吸收空气中的甲醇蒸汽,在操作温度300K 下的溶解度系H =2 k m om ; k P a ,传质系数 kG 二 0.056kmol m ° h 二 kPa 」,k L = 0.075knol m h A kmol -1 m 3 o 求总传质系数K G 以及气相阻力在总阻力中所占常数m ,解: 总压力为 100kPa o (答:H = 0.59kmol m " kPa J , m = 0.943)1 17 Ac 0.582kmol m , 101 1000c 0.582 1 J3 H 0.59mol Pa m , Pe 0.98667.4 7 60 ccccc y 0.0099 1 0 01 0131 17 x 0.0 1 0 51 100 + 17 18 7-1 . 100g 水中溶解1gNH 3,从手册查得 20°C 时NH 3的平衡分压为 986.6Pa ,在此浓度以内服从亨利定律。
试求溶解度系数 H (单位为kmol mkPa _1 )和相平衡m 」-0.943o6.42 10“32 18 1000=11.4g0.0099 0.01057-2 100C 时氧在水中的溶解度的表达式P * =3.313 106x ,式中P”为氧在气相中21.3 3.313 10 =6.42 10^,解:0.004 1 - 0.004二 0.0402塔丫,=2.52X =2.52 0.012 =0.03024,塔丫,=2.52X =2.52 0 =0,= 0.064,丫2 =—-1- Y 20.06 1-0.061的分数。
【精品】化工原理第7章课后习题答案.doc
解:(x, y — mol第六章习题1)1) 苯酚(C 6H 5OH) (A)和对甲酚(Ct 此(CHQ OH) (B)的饱和蒸汽压数据为:P=75mmHg “t—x —y”2)承第1题,利用各组数据,计算①在x=0至x=l 范围内各点的相对挥发度a”取各a :的算术平均值a,算出a 对a 】的最大相对误斧。
②以平均a 作为常数代入平衡方程式算出各点的“y—关系,算出由此法得 出各组刃值的最大相对误斧。
D 0P _ P B 6 o - P A ~P B op A X A 儿=十"丝= 1.318最大误差= 1.318-1.299L299 =1.46%60-48.92 68.81-48.92 =0.5576&81x0.55760=0.639a x.y.= ---------------------'1 + ( or -1) x.Q按1.318计,结果如下:3)已知乙苯(A)与苯乙烯(B)的饱和蒸汽压与温度的关系可按下式算得: In 卩:=16.0195-3279.47/(7-59.95)In 加=16.0193-3328.57/(7-63.72)式中P°的单位是mmHg, T的单位是K。
问:总压为60mmHg (绝压)吋,A与B的沸点各为多少。
C ?在上述总压和65°C 吋,该物系可视为理想物系。
此物系的平衡汽、液相浓度各为多少摩尔分率?解:1)令= p,算得的/为A的沸点厶"60 = 16.0195 — 3279.47/( T — 59.95):.T A =334.95^ =61.8° CS B = p,算得的/为B的沸点Ln60 = 16.0193-3328.57/(7- 63.72).•.T B=342.85^=69.7°C2) p = 6QmmHg, t = 65°C = 33&15KLnp°A = 16.0195 — 3279.47 / (338.15 — 59.95)p°A = 68.81mmHgLnp°B = 16.0193 - 3328.57/(338.15-63.72) p°B = 4&92mmHg760-595.3 1436.7 —595.3 -0.19571436.7x0.1957760=0.374)苯(A)和甲苯(B)混合液可作为理想溶液,其各纯组分的蒸汽压计算式为log ^ = 6.906-1211/(/+220.8)log 巩=6.955-1345/0+219.5)式中P。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
7-1.g 100水中溶解31gNH ,从手册查得C 200时3NH 的平衡分压为86.6Pa 9,在此浓度以内服从亨利定律。
试求溶解度系数H (单位为13kPa m kmol --⋅⋅)和相平衡常数m ,总压力为kPa 100。
(答:13kPa m0.59kmol --⋅⋅=H , 0.943m =)解:3m kmol 582.010*******1-⋅==c ,31m Pa mol 59.09866.0582.0--⋅⋅===Pe c H ,0099.03.1011007604.7==e y , 0105.018100171171=+=x , 943.00105.00099.0===x y m e 。
7-2.C 100时氧在水中的溶解度的表达式x p 6*10313.3⨯=,式中*p 为氧在气相中的平衡分压,kPa ;x 为溶液中氧的摩尔分数。
空气中氧的体积分数为%21,试求总压为kPa 101时,每3m 水中可溶解多少g 氧(答:3m g 4.11-⋅ ,或3m 0.35mol -⋅ )解:kPa 3.213.10121.0=⨯=Pe ,6661042.610313.33.2110313.3-⨯=⨯=⨯=Pe x , 36m g 4.11100018321042.6--⋅=⨯⨯⨯=c 。
7-3.用清水吸收混合气中的 3NH ,进入常压吸收塔的气体含3NH 体积分数为%6,吸收后气体含3NH 体积分数为%4.0,出口溶液的摩尔比为13kmol kmol 012.0-⋅⋅NH 水。
此物系的平衡关系为X Y 52.2=*。
气液逆流流动,试求塔顶、塔底处气相推动力各为多少(答:顶00402.02=ΔY ,底034.01=ΔY )解:064.006.0106.01111=-=-=y y Y ,0402.0004.01004.01222=-=-=y y Y , 塔底:03024.0012.052.252.2=⨯==X Y e ,塔顶:0052.252.2=⨯==X Y e , 塔顶气相推动力00402.02=∆Y ,塔底气相推动力034.003024.0064.01,11=-=-=∆e Y Y Y 。
7-4.用水吸收空气中的甲醇蒸汽,在操作温度300K 下的溶解度系13kPa m 2kmol --⋅⋅=H ,传质系数112kPa h m 0.056kmol ---⋅⋅⋅=G k ,3-112m km ol h m 0.075km ol ⋅⋅⋅⋅=--L k 。
求总传质系数G K 以及气相阻力在总阻力中所占的分数。
(答:11-2kPa h m 0.0408kmol --⋅⋅⋅=G K , 73.0)解:112kPa h m kmol 0408.0075.021056.011111---⋅⋅⋅=⨯+=+=LG G HK K K ,气相阻力所占分率:73.0075.021056.01056.01=⨯+=η。
7-5.从矿石焙烧送出的气体,含体积分数2%9SO ,其余视为空气。
冷却后送入吸收塔,用水吸收其中所含2SO 的%95。
吸收塔的操作温度为C 300,压力为kPa 100。
每小时处理的炉气量为3m 1000(C 300、kPa 100时的体积流量),所用液气比为最小值的2.1倍。
( 解:099.009.011111=-=-=y Y , 00495.0099.0)95.01()1(12=⨯-=-=Y Y η,1h kmol 6.36)09.01(3032734.221000-⋅=-⨯=V ,进吸收塔2SO 的分压kPa 12.909.03.1013.1011=⨯==y P ,由平衡关系内插得溶液平衡浓度为()O H 100kg kgSO2877.02-1⋅,换算为摩尔比3,11047.218/10064/877.0-⨯==e x ,1.3800247.000495.0099.0,121min =-=-=⎪⎭⎫⎝⎛e x Y Y V L ,69.451.382.12.1min=⨯=⎪⎭⎫⎝⎛=V L V L , 11minmin h kg 25100h mol 5.13941.386.36--⋅=⋅=⨯=⎪⎭⎫⎝⎛=V L V L , 1min h kg 30120251002.12.1-⋅=⨯==L L ,121x Y Y V L -=⇒32111006.269.4500495.0099.0-⨯=-=-=VL Y Y x 。
7-6.用煤油从苯蒸气与空气的混合物中回收苯,要求回收%99。
入塔的混合气中,含苯%2(摩尔分数)。
入塔的煤油中,含苯%02.0。
溶剂用量为最小用量的5.1倍,操作温度为C 500 ,压力为kPa 100。
平衡关系为X Y 36.0=*,总传质系数13s m km ol 015.0--⋅⋅=⋅a K Y 。
入塔气体的摩尔流量为12s m kmol 015.0--⋅⋅。
求填料层高度。
( 答:m 12=Z )解:02.01=y ,0002.0)99.01(02.02=-=y ,0002.02=x ,357.00002.036.002.00002.002.021,2121,21min =--=--=--=⎪⎭⎫⎝⎛x x y y X X Y Y V L e e ,536.0357.05.15.1min=⨯=⎪⎭⎫⎝⎛=V L V L , 0371.00002.0)0002.002.0(536.01)(2211=+-=+-=x y y L V x ,672.0536.036.01===L mV A ,]1))(11ln[(1112221A mx y mx y A A N OG +----=12]672.0)0002.036.00002.00002.036.002.0)(672.01ln[(672.011=+⨯-⨯---=m 1015.0015.0==Ω=ya OG K V H , m 12112=⨯=⋅=OG OG N H H 。
7-7.在填料塔内用稀硫酸吸收空气中所含的3NH 。
溶液上方3NH 的分压为零(相平衡常数0m =)。
下列情况所用的气、液流速及其他操作条件都大致相同,总传质单元高度OG H 都可取为.5m 0。
试比较所需填料层高度有何不同。
混合气中含摩尔分数3%1NH ,要求回收%90。
混合气中含3%1NH ,要求回收%99。
混合气中含3%5NH ,要求回收%99。
作了上述比较之后,你对塔高与回收率的关系能获得什么概念(答:(1)m 1=Z ;(2)m 25.2=Z ;(3)m 25.2=Z )解:⑴01.01=y ,00101.01.001.099.01.001.02=⨯+⨯=y ,1000101.001.02221==--mx y mx y , 01==LmVA ,查图得:2=OG N ,m 125.0=⨯=⋅=OG OG N H Z ; ⑵01.01=y ,0001.001.001.02=⨯=y ,1000001.001.021==y y , 查图得:5.4=OG N ,m 25.25.45.0=⨯=⋅=OG OG N H Z ; ⑶05.01=y ,000505.001.005.099.001.005.02=⨯+⨯=y ,99000505.005.021==y y ,查图得:5.4=OG N ,m 25.25.45.0=⨯=⋅=OG OG N H Z 。
7-8.今有连续逆流操作的填料吸收塔,用清水吸收原料气中的甲醇。
已知处理气量为13h m 1000-⋅(操作状态),原料中含甲醇3m g 100-⋅,吸收后水中含甲醇量等于与进料气体中相平衡时浓度的%67。
设在常压、C 025下操作,吸收的平衡关系取为X Y 15.1=,甲醇回收率要求为%98,12h m km ol 5.0--⋅⋅=Y k ,塔内填料的比表面积为32m m 200-⋅=a 塔内气体的空塔气速为1s m 5.0-⋅。
试求:(1)水的用量为多少1h kg -⋅(2)塔径;(3)传质单元高度OG H ;(4)传质单元数OG N ;(5)填料层高度。
(答: ; m 686.0 ; m 84.0 ; h kg 11501==⋅=-OG H D L m 1.6 ; 89.8==Z N OG )解:⑴07.04.22/132/1010031=⨯=-y , ∴0753.007.0107.01=-=Y ,312105.1)98.01(0753.0)1(-⨯=-⨯=-=ϕY Y ,0439.015.10753.067.067.0%671*11=⨯=⨯==m Y X X , 02=X ,11h kmol 38298273)07.01(4.22100025273273)1(4.221000-⋅=⨯-⨯==+⨯-⨯=y V , 68.100439.0105.10753.032121=-⨯-=--=-X X Y Y V L ,131h kg 1015.1h km ol 8.633868.168.1--⋅⨯=⋅=⨯==V L ;⑵13s m 36001000-⋅=s V ,1s m 5.0-⋅=u , ∴m 84.05.014.33600100044=⨯⨯⨯==u V D s π; ⑶m 686.084.042005.0382=⨯⨯⨯=Ω=πa K V H Y OG ;⑷用解析法:]))(1ln[(112221L Vm mX Y mX Y L V m L V mN OG +----=89.8]68.115.1)01015.100753.0)(68.115.11ln[(68.115.1113=+-⨯---=-; ⑸m 1.689.8686.0=⨯=⋅=OG OG N H Z 。
7-9.直径为m 88.0的填料吸收塔内,装有拉西环填料,填料层高为m 6。
每小时处理3m 2000含%5丙酮与空气的原料气操作条件为1个大气,C 025。
用清水作吸收剂,塔顶出口废气含丙酮%263.0(以上均为摩尔分数),出塔溶液中每千克含丙酮g 2.61,操作条件下的平衡关系为X Y 2=。
试计算:(1)气相总体积传质系数a K Y ;(2)每小时可回收丙酮多少千克(3)若将填料层加高m 3,又可以多回收多少千克丙酮(答:1113h kg 56.6 , h kg 225 , h mkm ol 8.176----⋅⋅⋅⋅=a K Y )解:塔截面积()222m 61.088.044===ππd S ,惰性气体量1h kmol 7.77)05.01(2982734.222000-⋅=-⨯=V , 526.005.0105.01=-=Y ,00263.000263.0100263.02=-=Y ,02=x ,0198.018/8.93858/2.6158/2.611=+=x ,0396.00198.021,=⨯=e y ,0412.00396.010396.01,=-=e Y ,0114.00412.00526.01=-=∆Y , 00263.0000263.02=-=∆Y ,006.000263.00114.0ln 00263.00114.0ln2121=-=∆∆∆-∆=∆Y Y Y Y Y m ,1321h m kmol 8.176006.0661.0)00263.00526.0(7.77)(--⋅⋅=⨯⨯-=∆Ω-=∆=m m A Ya Y Z Y Y V Y Z N K ; 丙酮回收量:1h kg 22508.58)00263.005.0(2982734.222000-⋅=⨯-⨯=m ,OG OG N H Z ⋅=,72.061.08.1767.77=⨯=Ω=Ya OG K V H , 33.872.06===OG OG H Z N ,418.000263.005.00198.02121=-=--=y y x x L V , 836.0418.02=⨯=LmV ,增加填料层高度后,传质单元数变为5.1272.09===OG OG H Z N , 当5.12=OG N ,836.0=LmV时,从图上读得:4021=y y ,回收率:975.0025.01112121=-=-=-y yy y y , 原回收率:9474.005.000263.005.0121=-=-y y y , 可多回收丙酮量:()1h kg 56.608.589474.0975.005.02982734.222000-⋅=⨯-⨯⨯⨯=∆m 。
