显热与潜热的区分
显热潜热

中文名称:显热英文名称:sensible heat定义:人与环境间通过对流、辐射和传导途径交换的热量,即非蒸发性散热。
定义显热系指当此热量加入或移去后,会导致物质温度的变化,而不发生相变。
物质的摩尔量、摩尔热容和温差三者的乘积为显热。
即物体不发生化学变化或相变化时,温度升高或降低所需要的热称为显热。
原理物体在加热或冷却过程中,温度升高或降低而不改变其原有相态所需吸收或放出的热量,称为“显热”。
它能使人们有明显的冷热变化感觉,通常可用温度计测量出来。
注:(如将水从20℃的升高到80℃所吸收到的热量,就叫显热。
)公式显热计算公式Q=m·c(t₂-t₁) Q=质量·比热(温度差)显热主要表现在由于空气干球温度的变化而发生的热量转移,比如空气干球温度的升高或降低而引起的热量。
潜热的发生总会伴随着物质相态的变化,简单的理解就是水在沸腾的时候要吸收很多的热量而温度没多大的变化。
所以,在空调负荷的计算时,因为空气里含有水蒸汽,所以就要计算其显热负荷和潜热负荷。
显热对固态、液态或气态的物质加热,只要它的形态不变,则热量加进去后,物质的温度就升高,加进热量的多少在温度上能显示出来,即不改变物质的形态而引起其温度变化的热量称为显热。
如对液态的水加热,只要它还保持液态,它的温度就升高;因此,显热只影响温度的变化面不引起物质的形态的变化。
例如机房中、其计算机或程控交换机的发热量很大,它属于显热。
对液态的水加热,水的温度升高,当达到沸点时,虽然热量不断的加入,但水的温度不升高,一直停留在沸点,加进的热量仅使水变成水蒸气,即由液态变为气态。
这种不改变物质的温度而引起物态变化(又称相变)的热量称为潜热。
如计算机房中、工作人员人体发热以及换气带进来的空气含湿量,这些热量称为潜热。
(全热等于显热与潜热之和。
)如果要求的气温高于露点温度, 则没有水蒸汽的产生或者水珠的产生,即湿度没有变化,也就是所说的显热交换!如果要求的气温低于露点温度,就会有潜热交换。
显热与潜热的区分

显热与潜热的区分集团文件版本号:(M928-T898-M248-WU2669-I2896-DQ586-M1988)显热、潜热、热湿比及焓显热主要表现在由于空气干球温度的变化而发生的热量转移,比如空气干球温度的升高或降低而引起的热量。
潜热的发生总会伴随着物质相态的变化,简单的理解就是水在沸腾的时候要吸收很多的热量而温度没多大的变化。
所以,在空调负荷的计算时,因为空气里含有水蒸汽,所以就要计算其显热负荷和潜热负荷。
显热对固态、液态或气态的物质加热,只要它的形态不变,则热量加进去后,物质的温度就升高,加进热量的多少在温度上能显示出来,即不改变物质的形态而引起其温度变化的热量称为显热。
如对液态的水加热,只要它还保持液态,它的温度就升高;因此,显热只影响温度的变化面不引起物质的形态的变化。
例如机房中、其计算机或程控交换机的发热量很大,它属于显热。
对液态的水加热,水的温度升高,当达到沸点时,虽然热量不断的加入,但水的温度不升高,一直停留在沸点,加进的热量仅使水变成水蒸气,即由液态变为气态。
这种不改变物质的温度而引起物态变化(又称相变)的热量称为潜热。
如计算机房中、工作人员人体发热以及换气带进来的空气含湿量,这些热量称为潜热。
(全热等于显热与潜热之和。
)如果要求的气温高于露点温度, 则没有水蒸汽的产生或者水珠的产生,即湿度没有变化,也就是所说的显热交换!如果要求的气温低于露点温度,就会有潜热交换。
潜热,相变潜热的简称,指单位质量的物质在等温等压情况下,从一个相变化到另一个相吸收或放出的热量。
这是物体在固、液、气三相之间以及不同的固相之间相互转变时具有的特点之一。
固、液之间的潜热称为熔解热(或凝固热),液、气之间的称为汽化热(或凝结热),而固、气之间的称为升华热(或凝华热)。
显热:随着潮湿空气的温度变化而吸收或放出的热量(比热*温度变化);潜热:随着潮湿空气中的水蒸气浓度的变化有关的热量(汽化热*凝结热);全热(焓):显热和潜热之和,一般状态下焓值与全热值相同。
显热与潜热的区别

显热与潜热的区别
热是指物理性质上的声音、光学等形式能量的总称,它与所有物质有着千丝万缕的关系。
按热的量的不同,可分为显热和潜热。
显热是指物体表面温度上升,当在物体上施加热时,物体自身的内能量转换热量,从
而导致表面温度升高,产生显热。
这种热能可以用低层次的实验测量出来,在一定时间内,显热量也可通过计算计算出来。
因为它可直接感知,因此可以被测量和计算出来,也就是
显热。
潜热是指物体中由于化学反应、过程改变,压缩或膨胀变形等现象,产生的热变化而
无法感知的隐藏热。
比如,在化学反应过程中,物质的温度不一定会发生改变,但是却有
可能产生易于检测的热变化,这种热变化就是潜热。
潜热也可以用于衡量,但一般只能通
过模拟方法来计算和观察,而不能够直接测量。
由以上可以看出,显热和潜热都是物体表面上释放出来的热量,两者之间的不同之处
是显热可以直接测量和衡量,潜热则只能模拟来研究和观察。
由于热是由物质之间相互作用,转移或产生而成的,在不同形式下热能都有其一定的转移规律,从而影响热变化,提
高热传递效率。
因此,掌握两者之间的规律和特性,以便更好地使用热能,这对石油、煤炭、热电、热力等热源的开发运用都非常重要。
潜热和显热有什么区别

潜热和显热有什么区别
二者的区别主要体现在性质、特点及放出的热量上。
显热指物体在加热或冷却过程中,温度升高或降低而不改变其原有相态所需吸收或放出的热量。
它能使人们有明显的冷热变化感觉;潜热指在物体吸收或放出热量过程中,其相态发生了变化(如气体变成液体),但温度不发生变化,这种吸收或放出的热量叫“潜热”。
潜热和显热的区别
1、性质不同:显热是当此热量加入或移去后,会导致物质温度的变化,而不发生相变。
潜热是相变潜热的简称,是物质在等温等压情况下,从一个相变化到另一个相吸收或放出的热量。
2、特点不同:潜热是物体在固、液、气三相之间以及不同的固相之间相互转变时具有的特点之一。
显热是物体不发生化学变化或相变化时,温度升高或降低所需要的热。
3、热量放出不同:显热是随着潮湿空气的温度变化而吸收或放出的热量。
潜热是随着潮湿空气中的水蒸气浓度的变化有关的热量。
冷凝除湿 潜热和显热

冷凝除湿潜热和显热
冷凝除湿是指利用冷凝原理将空气中的水蒸气凝结成水滴,从而降低空气中的湿度。
这个过程中,热量会释放出来,这种热量称为潜热。
潜热是水从气态变为液态时所释放的热量,因为水分子在液态中比在气态中更紧密地排列,所以需要释放一定的热量。
除湿的另一个重要参数是显热。
显热是指空气中温度的变化,当空气中的水分被除去时,空气中的温度会发生变化。
如果除湿过程中没有冷却空气,则显热是零,因为湿度的减少与温度的升高是平衡的。
但如果采用空气冷却的方式除湿,则显热是有的,因为空气被冷却了,温度下降了。
综合来看,冷凝除湿可以有效地降低空气中的湿度,但除湿时也需要注意潜热和显热的变化,避免对环境造成不必要的影响。
- 1 -。
显热与潜热的区别

显热与潜热显热:对固态、液态或气态的物质加热,只要它的形态不变,则热量加进去后,物质的温度就升高,加进热量的多少在温度上能显示出来,即不改变物质的形态而引起其温度变化的热量称为显热。
潜热:潜热是物质发生相变过程吸收或放出的热量。
比如对液态的水加热,水的温度升高,当达到沸点时,虽然热量不断的加入,但水的温度不升高,一直停留在沸点,加进的热量仅使水变成水蒸气,即由液态变为气态。
这种不改变物质的温度而引起物态变化(又称相变)的热量称为潜热。
1Kg液体完全变为同温度下的饱和蒸气所吸收的热量,称为该温度下的汽化潜热,用符号r表示,单位kJ/kg。
两个概念:显热是物质不发生相变(固、液、气转变)吸收或放出热量潜热是物质发生相变过程吸收或放出的热量。
如1mol水(100℃)蒸发成1mol水蒸汽(100℃)需要吸收40.62kj 的热量,这部分热量就是潜热;而1mol 60℃水升温至100℃(无水蒸汽生成)需要吸收的热量(约3.014kj)就是显热。
简单的说显热是物质不发生相变时吸收或放出的热量 ,它有一个明显的现象是:热量转移过程中伴有温度的变化.而潜热是物质发生(相变)过程中吸收或放出的热量,在这个过程中虽然有热量的变化,但温度一般保持恒定不变,即相变前后的温度是相同的.物质发生相变(物态变化),在温度不发生变化时吸收或放出的热量叫作“潜热”。
物质由低能状态转变为高能状态时吸收潜热,反之则放出潜热。
例如,液体沸腾时吸收的潜热一部分用来克服分子间的引力,另一部分用来在膨胀过程中反抗大气压强做功。
熔解热、汽化热、升华热都是潜热。
潜热的量值常常用每单位质量的物质或用每摩尔物质在相变时所吸收或放出的热量来表示。
在一级相变中,吸收或释放热量,伴随体积的变化,但系统的温度不变。
所吸收或放出的热量称为“相变潜热”。
相变潜热与发生相变的温度有关,单位质量的某种物质,在一定温度下的相变潜热是一定值。
汽化潜热就是说,把1KG饱和水变成1KG干饱和蒸汽所需要的热量。
物体的熔化与显热与潜热

熔化过程中,物 质吸收热量,温 度保持不变。
物质从固态熔化 成液态时,需要 吸收热量,这个 热量称为潜热。
在பைடு நூலகம்化过程中, 物质吸收的潜热 会转化为物质的 内能,使物质的 状态发生改变。
熔化过程中的潜 热变化是物质熔 化的重要特征之 一,对于理解物 质的热性质和热 力学过程具有重 要意义。
熔化过程中显热与潜热的关系
熔化过程中显热与潜热的概念
熔化过程中显热与潜热对物质性质 的影响
添加标题
添加标题
添加标题
添加标题
熔化过程中显热与潜热的变化规律
熔化过程中显热与潜热的实际应用
熔化过程中的热 量传递
熔化过程中的热量来源
熔化热:熔化过 程中吸收的热量, 与物质的种类和 温度有关。
显热:熔化过程 中吸收的热量, 与物质的种类和 温度有关。
潜热:熔化过程 中吸收的热量, 与物质的种类和 温度有关。
热传导:熔化过 程中热量传递的 方式之一,通过 物质内部的微观 粒子运动实现热 量传递。
熔化过程中的热量传递方式
热传导:熔化过程中,热量通过物体内部原子或分子的振动,从高温区域传递到低温区域。
热对流:熔化过程中,由于温度差异引起的流体流动,将热量从一处传递到另一处。
热辐射:熔化过程中,物体表面会以电磁波的形式向外辐射热量,同时也会吸收外界热辐射的热 量。
热传递的综合方式:在实际熔化过程中,热量传递通常会同时存在多种方式,如热传导与热对流 同时发生。
熔化过程中的热量传递效率
熔化过程:物质从固态变为液态的过程,需要吸收热量 热量传递方式:热传导、热对流和热辐射 热量传递效率影响因素:材料性质、熔化温度、熔化速度等 提高热量传递效率的方法:选用导热性能良好的材料、优化熔化工艺等
显热与潜热的解释

显热与潜热的解释
嘿,朋友!你知道啥是显热不?就好比说,你大夏天跑了一身汗,
这时候你感觉热得要命,那种能让你明显感觉到的热,就是显热啦!
就像你喝了一杯烫水,嘴里立马能感觉到的那种烫烫的感觉,这就是
显热在“作祟”呀!
那潜热又是啥呢?哎呀呀,这可有点神奇咯!就好像冬天的时候,
水会变成冰,这过程中其实有热量在偷偷变化呢,但你可能感觉不太到,这就是潜热啦!比如说,你把一块冰放在手里,过了一会儿它化
成了水,这中间就有潜热在起作用呢。
显热和潜热,它们就像是一对好兄弟,但又各有各的特点。
显热呢,总是大大咧咧地出现,让你一下子就察觉到它。
可潜热呢,就像个害
羞的小孩,偷偷地在那儿捣鼓,不仔细去感受还真发现不了它。
你想想看,夏天的阳光直直地晒在你身上,那股热浪滚滚的感觉,
就是显热在发威呀!但当水蒸发变成水蒸气的时候,这里面也有潜热
在“搞鬼”呢,你能明白不?
“哎呀,那这么说我有点懂了呀!”你可能会这么说。
对呀对呀,就
是这么回事!显热和潜热在我们生活中无处不在呢。
它们影响着天气
的变化,影响着我们的生活。
就像我们每天呼吸的空气,里面都有着
它们的身影呢。
所以呀,别小看了这显热和潜热,它们可重要着呢!它们就像是大
自然的小魔术,悄悄地改变着周围的一切。
你说神奇不神奇?
我的观点就是:显热和潜热虽然看不见摸不着,但它们真的非常重要,对我们的生活有着深远的影响,我们应该好好去了解和认识它们。
各种热效应

• 例如,在黑色冶金中,溶解热往往是指1摩尔溶 质溶于铁液中形成浓度为1%(质量)溶液时的热 效应:Al(l)== 〔Al〕 -43095 J/ mol
热的单位:常用卡、千卡(大卡)表示,卡的定义 是:1克水从14.5℃升温1℃所吸收的热为1卡。
二、相变热(相变潜热):当物质吸热或放 热而其温度不变时,物质的聚集状态(物态) 就将发生变化,叫做相变。所吸或所放的热 叫做相变潜热或简称相变热。
蒸发热、凝结热、熔化热、凝固热、升华热
三、化学反应的各种热效应 混合理想气体是指任一气体组分的分压力为p的状态;
冶金过程的热效应
热效应:在没有非膨胀功的条件下,体系所 吸(放)的热与体系的状态函数u、H的改变 之间呈现最简单的关系,可以直接用所吸 (放)的热来量度其内能或热焓的改变。这 种条件下所吸放的热叫做相应的过程的热效 应。
各种热效应
一、显热和潜热:系统与环境间发生热传递, 系统若发生温度改变涉及的热称为显热,没 有温度改变涉及的热称为潜热。
纯液体(或纯固体)物质的标准态是标准压 力p下的纯液体(或纯固体)。 溶液中溶质的标准态,是在指定温度T和标准 压力p,浓度c=1 mol/L
任一化学反应的热效应等于产物生成热的总 和与反应物生成热总和之差。
2为该物质的燃烧热。
习惯上也以处于稳定状态,1大气压和25℃(298K)
为准。对于有机化合物,完全燃烧指碳变为CO2,氢
变成H2O,硫变为SO3,等等。例如,甲烷的燃烧热:
潜热显热焓等解释

空调行业常见名词解释潜热物质发生相变(物态变化),在温度不发生变化时吸收或放出的热量叫作“潜热”。
物质由低能状态转变为高能状态时吸收潜热,反之则放出潜热。
例如,液体沸腾时吸收的潜热一部分用来克服分子间的引力,另一部分用来在膨胀过程中反抗大气压强做功。
熔解热、汽化热、升华热都是潜热。
潜热的量值常常用每单位质量的物质或用每摩尔物质在相变时所吸收或放出的热量来表示。
在一级相变中,吸收或释放热量,伴随体积的变化,但系统的温度不变。
所吸收或放出的热量称为“相变潜热”。
相变潜热与发生相变的温度有关,单位质量的某种物质,在一定温度下的相变潜热是一定值。
若用U1和U2分别表示1相和2相单位质量的内能,用V1和V2分别表示1相和2相单位质量的体积,于是单位质量的物质由1相转变为2相时所吸收的相变潜热可用下式表示l=(U2-U1)+P(V2-V1)=h2-h1式中P是作用于系统的外部压强,hl和h2分别为1相和2相单位质量的焓。
上式相变潜热公式表明,相变潜热l包括内潜热(U2-U1)和外潜热〔P(V2-V1)两部分。
显热物体在加热或冷却过程中,温度升高或降低而不改变其原有相态所需吸收或放出的热量,称为“显热”。
它能使人们有明显的冷热变化感觉,通常可用温度计测量出来。
(如将水从20°C的升高到80°C所吸收到的热量,就叫显热。
)相对湿度某温度时空气的绝对湿度跟同一温度下水的饱和汽压的百分比,叫做当时空气的相对湿度.如果用p表示某温度时空气的绝对湿度,用P表示同一温度下水的饱和汽压,用B表示相对湿度,那么某一温度时水的饱和汽压可以从下面的表里查出来.因此,知道了绝对湿度就可以算出相对湿度来;反过来,知道了相对湿度也可以算出绝对湿度来.假如空气的绝对湿度p=800Pa,当气温是20°C时,空气的相对湿度是当气温是10C C时,空气的相对湿度在住人的房间里,适宜的相对湿度是60%左右.水稻在抽穗扬花期,最适宜的相对湿度是70%〜80%.相对湿度relativehumidity湿度的一种表示方式。
全热、显热、潜热、湿负荷详解

全热、显热、潜热、湿负荷详解一、前言很多暖通初学人员对全热、显热、潜热、湿负荷之间的慨念和关系始终没有弄明白,这类问题在各类暖通论坛上很多,每个人各有说法,但很少有人能够完整的阐述清楚,如果这些慨念混淆会影响深入的学习暖通知识,因此本人通过整理书本上的各种慨念及本人理解,把这它们之间的关系予以重新解释,以便于大家理解。
二、定义和慨念1.显热(w):显热系指当此热量加入或移去后,会导致物质温度的变化,而不发生相变。
物质的摩尔量、摩尔热容和温差三者的乘积为显热。
即物体不发生化学变化或相变化时,温度升高或降低所需要的热称为显热。
2.潜热(w):潜热,相变潜热的简称,指单位质量的物质在等温等压情况下,从一个相变化到另一个相吸收或放出的热量。
这是物体在固、液、气三相之间以及不同的固相之间相互转变时具有的特点之一。
固、液之间的潜热称为熔解热(或凝固热),液、气之间的称为汽化热(或凝结热),而固、气之间的称为升华热(或凝华热)。
3.湿负荷(kg/h):湿负荷是指空调房间的湿源(人体散湿、敞开水池(槽)表面散湿、地面积水等)向室内的散湿量,也就是为维持室内含湿量恒定需从房间除去的湿量。
4.余湿量:余湿量就是为维持室内含湿量恒定需要去除的湿量。
它由:1、人体散湿 2、设备散湿 3、维护结构和地面散湿 4、新风和渗透风带来的湿量等组成,不过一般只考虑1、2两项,然后加一定的安全系数。
三、它们之间的关系1.显热与显冷负荷的关系:要使空气的温度上升,而又不发生物质相变(如冷凝水)所需的能量就是显热。
2.潜热与湿负荷的关系:要除去空气中多余的湿量,需要消耗能量,而消耗的这部分能量就是潜热。
3.全热=显热+潜热显热来处理显冷负荷;潜热来处理是湿负荷。
所以,空调总冷负荷=显冷负荷+湿负荷。
四、分析:1.单纯的使空气温度提升消耗的这部分能量叫显热,在温度提升的过程中没有发生物质相变;而使物质发生相变,但温度却不升高或降低所消耗的这部分能量叫潜热。
相变热力学能变化

相变热力学能变化相变是物质在温度和压力变化下,由一种物态转变为另一种物态的过程。
在相变过程中,会伴随着能量的转移和变化,这种能量变化称为相变热力学能变化。
相变热力学能变化通常可以分为两个部分:潜热和显热。
潜热是指在相变过程中,单位质量的物质吸收或释放的热量,而不引起温度的变化。
显热则是指在相变过程中,单位质量的物质吸收或释放的热量,同时引起温度的变化。
潜热是相变过程中最显著的能量变化。
相变过程中,物质在保持温度不变的情况下,吸收或释放潜热。
例如,当水从液态变为气态时,需要吸收潜热,而当水从气态变为液态时,会释放潜热。
潜热的大小取决于物质的性质和相变的类型。
在相变过程中,潜热的转移使得物质的温度保持不变,因此相变过程常常被用来作为温度计的基础。
显热是指在相变过程中,由于温度的变化而引起的能量变化。
相变过程中,物质的温度会随着能量的吸收或释放而发生变化。
例如,当水从固态变为液态时,它吸收热量并升温;而当水从液态变为气态时,它释放热量并降温。
显热的大小取决于物质的性质和相变的类型。
相变热力学能变化的大小和方向取决于物质的性质和外界条件。
一般来说,相变热力学能变化是一个吸热过程,即在相变过程中,物质吸收热量。
然而,也有一些特殊情况下的相变是放热过程,即在相变过程中,物质释放热量。
这取决于物质的性质以及外界条件的变化。
相变热力学能变化对于物质的性质和应用具有重要的影响。
相变热力学能变化的大小和方向可以用来研究物质的相变行为,例如研究物质的熔点、沸点等。
相变热力学能变化还可以用来研究物质的热传导性质,例如研究物质的导热系数。
此外,相变热力学能变化在工程应用中也具有重要的意义,例如在冷却系统中利用水的相变热来实现冷却效果。
相变热力学能变化是物质在相变过程中伴随的能量转移和变化。
它包括潜热和显热两个部分,潜热是在相变过程中保持温度不变时吸收或释放的热量,显热是由于温度的变化而引起的能量变化。
相变热力学能变化的大小和方向取决于物质的性质和外界条件。
显热和浅热

显热和潜热
虽然热量是物体吸收或放出热的多少,但是有的物体吸收或放出热量只有温度的变化,而无状态的变化;有的物体吸收或放出热量只有状态的变化,而无温度的变化。
它们的区别是:
前者吸收或放出的是显热,后者吸收或放出的是潜热。
1)显热
物体吸收或放出热量时,物体只有温度的升高或降低,而状态却不发生变化,这时物体吸收或放出的热量叫做显热。
显热可以触摸或感觉出来,也可以用温度计测量出来。
例如,30℃的水吸热后温度升高至60℃,其吸收的热量为显热;反之,60℃的水降温到30℃时,所放的热量也为显热。
2)物体吸收或放出热量时,物体只有状态的变化,而温度却不发生变化,这时物体吸收或放出的热量叫做潜热。
潜热因温度不变,所以无法用温度计测量。
物体相变时所吸收或放出的热量均为潜热,分别称为汽化潜热、液化潜热、溶解潜热、凝固潜热、升华潜热和凝华潜热。
例如,在常压下,水加热到沸点100℃后,如果继续加热,水将汽化为水蒸气,汽化过程中温度仍为100℃显热不变,这时吸收的热量为汽化潜热:反之,高温的水蒸气冷却到100℃后再继续降温,水蒸气将冷为水.冷凝过程中温度保持100℃不变,这时放出的热量为液化潜热。
制冷系统中的制冷剂一般选用蒸发潜热数值大的物质,这是因为制冷剂在蒸发器中主要是利用由液态吸热变为气态的相变过程来达到制冷目的的,这个热就是蒸发潜热。
热分析知识点

显热:在恒压和恒容不作非体积功的条件下,仅因系统温度改变而与环境交换的
热称为显热。
潜热:在一定温度、压力下系统发生相变时与环境交换的热。
影响热重曲线的主要因素?试推导热重仪器中试样表观增重与气体密度的
关系。
根据所推导的表观增重公式说明影响表观增重的因素。
答:影响热重曲线的主要因素包括:1 仪器因素(1)浮力和对流(2)挥发物的再凝集(3)坩埚与试样的反应及坩埚的几何特性2实验条件(1)升温速率(2)气氛的种类和流量3.试样影响(1)试样自身的结构缺陷情况、表面性质(2)试样用量(3)试样粒度
影响表观增重的因素: V、0 、T。
热光学法:是在程序控温条件下测量物质的光学性质与温度的关系的一种技术。
热电学法:在程序控温下,测量试样的电学特性与温度关系的方法。
热重分析仪主要由天平、炉子、程序控温系统、记录系统等几个部分构成。
最常用的测量的原理有两种,即变位法和零位法。
所谓变位法,是根据天平梁倾斜度与质量变化成比例的关系,用差动变压器等检知倾斜度,并自动记录。
零位法是采用差动变压器法、光学法测定天平梁的倾斜度,然后去调整安装在天平系统和磁场中线圈的电流,使线圈转动恢复天平梁的倾斜,即所谓零位法。
由于线圈转动所施加的力与质量变化成比例,这个力又与线圈中的电流成比例,因此只需测量并记录电流的变化,便可得到质量变化的曲线。
逸出气分析:在程序控温下,对从物质中逸出的挥发性物质的性质和(或)数量与温度关系的分析。
初中九年级(初三)物理热量、比热容、显热和潜热.doc
3、热量、比热容、显热和潜热
(1)、热量Q:物体吸热和放热多少的物理量。
发生在两个温度不同的物体之间,温度高的
物体失去能量,温度低的物体得到能量,直到温度相等。
标准单位:焦J、千焦KJ
工程单位:千卡Kcal 转换:1Kcal=4.2KJ
(2)比热容
单位质量的某种物质,温度升高或降低1K所变化的热量,称为这种物质的比热容,
简称比热,用符号c表示。
热量公式:Q=cm(T-T0) 其中m为物质的质量。
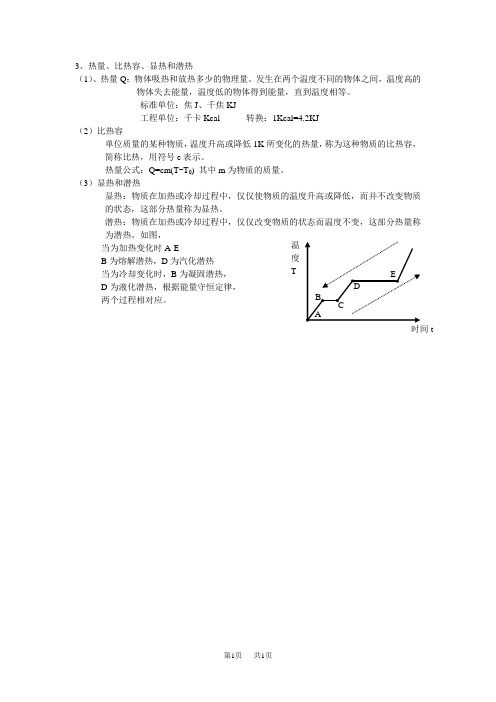
(3)显热和潜热
显热:物质在加热或冷却过程中,仅仅使物质的温度升高或降低,而并不改变物质
的状态,这部分热量称为显热。
潜热:物质在加热或冷却过程中,仅仅改变物质的状态而温度不变,这部分热量称
为潜热。
如图,Array当为加热变化时A-E
B为熔解潜热,D为汽化潜热
当为冷却变化时,B为凝固潜热,
D为液化潜热,根据能量守恒定律,
两个过程相对应。
第1页共1页。
概念

1.蒸发温度:在一定压力下,液体制冷剂在蒸发器中汽化的温度。
2.蒸发压力:制冷剂液体在蒸发器中汽化是的压力,即蒸发温度下的饱和压力。
3.过热度:相同压力下的过热蒸汽温度与饱和蒸汽温度的差值。
4.显热:工质的相态不改变而使其温度升降所需加入或移出得热量。
5.潜热:在一定温度下,每1千克的饱和液体汽化为干饱和蒸汽所需加入的热量称汽化潜热;每1千克的干饱和蒸气冷凝为饱和液体需移出得热量成为凝结潜热。
6.吸气压力:压缩机进口处气体制冷剂的压力,可近似看作蒸发压力。
7.排气压力:压缩机排出口的制冷剂的压力,可近似看作凝结压力。
8.冷凝温度:气体制冷剂在冷凝器中放热冷凝的温度,即对应与冷凝压力下的饱和温度。
9.过冷度:相同压力下,冷凝温度与膨胀阀前液体制冷剂的温度之差。
即饱和温度与
过冷温度之差。
液氢气化潜热显热

液氢气化潜热显热
液氢的气化潜热和显热是描述氢从液态到气态相变时吸收或释放的热量。
在氢从液态转变为气态的过程中,需要吸收热量使氢分子脱离液态状态,这个过程中的热量称为气化潜热。
相反,当氢从气态转变为液态时,会释放热量,这个过程中的热量称为显热。
1.气化潜热(Latent Heat of Vaporization):液态氢转变为气态氢时,需要吸收的热量称为气化潜热。
这个过程中,分子脱离液态排列形成气态,因此需要克服分子之间的吸引力,需要能量。
气化潜热是指单位质量的液态氢在常压下转变为气态时吸收的热量。
对于氢气,其气化潜热在常压下约为46100 J/mol。
2.显热(Sensible Heat):氢气从气态转变为液态时,释放的热量称为显热。
这个过程中,气态分子减速并排列成液态,释放出原先储存在动能中的热量。
显热是指单位质量的气态氢在常压下转变为液态时释放的热量。
这些热量值在设计和操作液态氢系统时非常重要,因为它们决定了液态氢的处理和储存过程中需要考虑的能量变化。
全热、显热、潜热、湿负荷详解

全热、显热、潜热、湿负荷详解一、前言很多暖通初学人员对全热、显热、潜热、湿负荷之间的慨念和关系始终没有弄明白,这类问题在各类暖通论坛上很多,每个人各有说法,但很少有人能够完整的阐述清楚,如果这些慨念混淆会影响深入的学习暖通知识,因此本人通过整理书本上的各种慨念及本人理解,把这它们之间的关系予以重新解释,以便于大家理解。
二、定义和慨念1.显热(w):显热系指当此热量加入或移去后,会导致物质温度的变化,而不发生相变。
物质的摩尔量、摩尔热容和温差三者的乘积为显热。
即物体不发生化学变化或相变化时,温度升高或降低所需要的热称为显热。
2.潜热(w):潜热,相变潜热的简称,指单位质量的物质在等温等压情况下,从一个相变化到另一个相吸收或放出的热量。
这是物体在固、液、气三相之间以及不同的固相之间相互转变时具有的特点之一。
固、液之间的潜热称为熔解热(或凝固热),液、气之间的称为汽化热(或凝结热),而固、气之间的称为升华热(或凝华热)。
3.湿负荷(kg/h):湿负荷是指空调房间的湿源(人体散湿、敞开水池(槽)表面散湿、地面积水等)向室内的散湿量,也就是为维持室内含湿量恒定需从房间除去的湿量。
4.余湿量:余湿量就是为维持室内含湿量恒定需要去除的湿量。
它由:1、人体散湿 2、设备散湿 3、维护结构和地面散湿 4、新风和渗透风带来的湿量等组成,不过一般只考虑1、2两项,然后加一定的安全系数。
三、它们之间的关系1.显热与显冷负荷的关系:要使空气的温度上升,而又不发生物质相变(如冷凝水)所需的能量就是显热。
2.潜热与湿负荷的关系:要除去空气中多余的湿量,需要消耗能量,而消耗的这部分能量就是潜热。
3.全热=显热+潜热显热来处理显冷负荷;潜热来处理是湿负荷。
蒸汽的潜热和显热

蒸汽的潜热和显热蒸汽是我们生活中常见的物质,也是许多工业和能源转换过程中不可或缺的重要组成部分。
蒸汽的潜热和显热是蒸汽在热力学过程中的两个重要物理量,具有重要的理论和实践意义。
一、潜热和显热的定义1. 潜热:指单位质量的物质在恒定压力下由液态转变为蒸汽时所吸收或放出的热量。
也就是说,在液态和气态之间转化时不发生温度变化的热量。
2. 显热:指单位质量的物质从一定的温度下升高到另一温度时所吸收或放出的热量。
也就是说,在温度变化过程中发生的热量。
二、潜热和显热的应用1. 工业应用在工业生产中,蒸汽是一种广泛应用的动力源和热源。
例如,在能源转换中,发电厂中的锅炉产生的蒸汽被输送到蒸汽涡轮上,在涡轮转动的过程中释放显热,将机械能转换成电能。
在化学工艺中,蒸汽常用于化学反应、干燥和蒸馏等过程中。
2. 节能减排在节能减排的理念下,人们广泛使用蒸汽作为替代能源。
在汽车工业中,火车和船舶的蒸汽机已被燃油发动机所取代。
在空调系统中,蒸汽压缩循环系统已经成为了效率较高的、能源利用率比传统空调高50%以上的最佳选择。
三、潜热和显热的研究1. 热力学热力学是研究热和其他形式的能量之间相互转化的学科,热力学基本原理是能量守恒和热力学第二定律。
潜热和显热的研究是热力学领域的重要内容,为了更好地研究蒸汽的能量转化过程和蒸汽的性质,热力学理论方面也在不断更新和完善中。
2. 工程应用工程应用方面,随着科学技术的不断发展,人们对蒸汽的研究也不断深入。
例如,在蒸汽发生器中的燃气中加入水蒸汽等技术,可以减少污染物的排放,并获得更高的热效率。
而智能控制技术的应用可以使蒸汽的潜热和显热的利用更加高效。
总之,蒸汽的潜热和显热是蒸汽的重要物理量,其在工业、能源转换和环保等领域的应用得到了广泛认可。
通过深入的研究和国际合作,相信未来会有更多的新技术和新应用形式不断涌现,为我们的生活带来更多的福祉。
什么是显热

什么是显热?什么是潜热?物体在加热或冷却过程中,温度升高或降低而不改变其原有相态所需吸收或放出的热量,称为“显热”。
它能使人倍受明显的冷热变化感觉,通常可用温度计来测量出来这。
(如将水从20℃升高到80℃所吸收的热量,就叫显热)在物体吸收或放出热量过程中,其相态发生了变化(如气体变成液体……),但温度不发生变化,这种吸收或放出的热量叫“潜热”。
“潜热”不能用温度计测量出来,人体也无法感觉到,但可通过实验计算出来。
饱和空气在吸收一定冷量(即放出热量)后,一部分水蒸气相变成液态水,而此时饱和空气温度并不下降,这部分放出的热量就是“潜热”。
为了维持室内恒温恒温湿,在某一时刻供给房间的热量,为热负荷;为了维持室内相对湿度恒定所需除去的湿量是湿负荷。
显热对固态、液态或气态的物质加热,只要它的形态不变,则热量加进去后,物质的温度就升高,加进热量的多少在温度上能显示出来,即不改变物质的形态而引起其温度变化的热量称为显热。
如对液态的水加热,只要它还保持液态,它的温度就升高;因此,显热只影响温度的变化不影响形态的变化。
例如在机房中,其计算机或程控交换机的发热很大,它属于显热。
对液态的水加热,水的温度升高,当达沸点时,虽然热量不断加入,但水的温度不升高,一直停留在沸点,加进的热量仅使水变水蒸气,即由液态变为气态。
这种不改变物质的温度而引起物态变化(又称相变)的热量称为潜热。
如计算机房中、工作人员人体发热以及换气带进来的空气含湿量,这些热量称为潜热。
(全热等于显热与潜热之和)。
显热:状态不变的情况,产生的热量传递;潜热:状态变化,同时产生热量传递(如:冰蓄冷)物质的分子或原子的相聚叫相,物质的一种状态转化为另一种状态叫相变。
何忠伟2012/11/30。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
显热、潜热、热湿比及焓
显热主要表现在由于空气干球温度的变化而发生的热量转移,比如空气干球温度的升高或降低而引起的热量。
潜热的发生总会伴随着物质相态的变化,简单的理解就是水在沸腾的时候要吸收很多的热量而温度没多大的变化。
所以,在空调负荷的计算时,因为空气里含有水蒸汽,所以就要计算其显热负荷和潜热负荷。
显热对固态、液态或气态的物质加热,只要它的形态不变,则热量加进去后,物质的温度就升高,加进热量的多少在温度上能显示出来,即不改变物质的形态而引起其温度变化的热量称为显热。
如对液态的水加热,只要它还保持液态,它的温度就升高;因此,显热只影响温度的变化面不引起物质的形态的变化。
例如机房中、其计算机或程控交换机的发热量很大,它属于显热。
对液态的水加热,水的温度升高,当达到沸点时,虽然热量不断的加入,但水的温度不升高,一直停留在沸点,加进的热量仅使水变成水蒸气,即由液态变为气态。
这种不改变物质的温度而引起物态变化(又称相变)的热量称为潜热。
如计算机房中、工作人员人体发热以及换气带进来的空气含湿量,这些热量称为潜热。
(全热等于显热与潜热之和。
)
如果要求的气温高于露点温度, 则没有水蒸汽的产生或者水珠的产生,即湿度没有变化,也就是所说的显热交换!如果要求的气温低于露点温度,就会有潜热交换。
潜热,相变潜热的简称,指单位质量的物质在等温等压情况下,从一个相变化到另一个相吸收或放出的热量。
这是物体在固、液、气三相之间以及不同的固相之间相互转变时具有的特点之一。
固、液之间的潜热称为熔解热(或凝固热),液、气之间的称为汽化热(或凝结热),而固、气之间的称为升华热(或凝华热)。
显热:随着潮湿空气的温度变化而吸收或放出的热量(比热*温度变化);
潜热:随着潮湿空气中的水蒸气浓度的变化有关的热量(汽化热*凝结热);
全热(焓):显热和潜热之和,一般状态下焓值与全热值相同。
湿负荷是指空调房间的湿源(人体散湿、敞开水池(槽)表面散湿、地面积水等)向室内的散湿量,也就是为维持室内含湿量恒定需从房间除去的湿量。
值通常用房间的余热(Q)余湿(W)的比值来计算,在焓湿图中热湿比线通过房间的设计状态点,此时ε线描述了送入房间的空气吸热吸湿后使房间状态稳定在设计状态点的变化方向和过程。
焓表征物体吸收的热量(在等压过程中)〖enthalpy〗为一个体系的内能与体系的体积和外界施加于体系的压强的乘积之和。
焓是一个状态函数,也就是说,系统的状态一定,焓的值就定了。
焓的定义式(物理意义)是这样的:H=U+pV [焓=流动内能+推动功]
其中U表示热力学能,也称为内能(Internal Energy),即系统内部的所有能量;
p是系统的(Pressure),V是系统的体积(V olume) 。
