第2章反应作业答案
高中化学二课时作业:第二章化学反应与能量第二节第课时化学能转化为电能含答案

第二节化学能与电能第1课时化学能转化为电能[目标导航]1。
熟悉能源的分类和化学能与电能的转化关系。
2.知道原电池是利用氧化还原反应将化学能转化为电能的装置,通过实验会说明原电池的原理,以及判断原电池的正、负极。
3.会正确书写电极反应式,熟知原电池的应用。
一、一次能源和二次能源1.能源按其来源可分为一次能源和二次能源。
能源类别定义实例一次能源直接从自然界中取得的能源太阳能、风能、地热能、潮汐能、煤、石油、天然气等二次能源由一次能源经过加工、转换得到的能源电能(水电、火电、核电)、蒸汽能、机械能等2.二次能源-—火力发电(1)火力发电原理:首先通过化石燃料燃烧,使化学能转变为热能,加热水使之汽化为蒸汽以推动蒸汽轮机,然后带动发电机发电. (2)能量转换过程:化学能错误!热能错误!机械能错误!电能.其中能量转换的关键环节是燃烧。
(3)火力发电弊端:①煤属于不可再生资源,用一点少一点,用煤发电会造成资源的浪费。
②能量经过多次转化,利用率低,能量损失大.③煤燃烧会产生有害物质(如SO2、CO、NO2、粉尘等),污染环境。
【议一议】1.判断正误(1)根据一次能源和二次能源的划分,氢气为二次能源。
()(2)电能是现代社会中应用最广泛、使用最方便、污染最小的一种二次能源.()(3)火力发电是化学能间接转化为电能的过程.()(4)水力发电是将化学能转化为电能的过程。
()答案(1)√(2)√(3)√(4)×二、化学能直接转化为电能1.按要求完成下列实验,并填表2.原电池(1)概念:是将化学能转化为电能的装置;原电池的反应本质是氧化还原反应。
(2)构成条件①原电池反应必须是自发的氧化还原反应,②具有活动性不同的两个电极(金属与金属或金属与能导电的非金属),③两电极均插入电解质溶液中,④电解质溶液、电极、导线形成闭合回路。
(3)原电池的工作原理原电池总反应式:Zn+2H+===Zn2++H2↑。
(4)能量转化过程:原电池在工作时,负极失电子,电子通过导线流向正极,被氧化性物质得到,闭合回路中形成电流,化学能转变为电能.【议一议】2.判断正误:(1)HCl+NaOH===NaCl+H2O是放热反应,可以设计成原电池.()(2)将铜片和锌片用导线连接插入酒精中,电流表指针发生偏转.()(3)在铜-锌-稀硫酸原电池中,电子由锌通过导线流向铜,再由铜通过电解质溶液到达锌。
2020-2021学年人教版必修1 第2章第2节 离子反应 作业

第2节离子反应1.制备(NH4)2Fe(SO4)2·6H2O的实验中,需对过滤出产品的母液(pH<1)进行处理。
室温下,分别取母液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是()A.通入过量Cl2:Fe2+、H+、NH+4、Cl-、SO2-4B.加入少量NaClO溶液:NH+4、Fe2+、H+、SO2-4、ClO-C.加入过量NaOH溶液:Na+、Fe2+、NH+4、SO2-4、OH-D.加入过量NaClO和NaOH的混合溶液:Na+、SO2-4、Cl-、ClO-、OH-解析Cl2过量,Fe2+不能大量存在:2Fe2++Cl2 ===2Fe3++2Cl-,A错误;NaClO具有强氧化性,Fe2+不能大量存在,同时H+与ClO-生成弱电解质HClO,B错误;Fe2+、NH+4与OH-不能大量共存,C错误。
答案 D2.下列关于离子共存或离子反应的说法正确的是()A.某无色溶液中可能大量存在H+、Cl-、MnO-4B.pH=2的溶液中可能大量存在Na+、NH+4、SiO2-3C.Fe2+与H2O2在酸性溶液中的反应:2Fe2++H2O2+2H+===2Fe3++2H2OD.稀硫酸和Ba(OH)2溶液反应:H++SO2-4+Ba2++OH-===BaSO4↓+H2O 解析A项,酸性条件下MnO-4将Cl-氧化为Cl2,不能大量共存且MnO-4显紫色;B项,酸性条件下,H+与SiO2-3生成H2SiO3沉淀,不能大量共存;C项,酸性条件下H2O2将Fe2+氧化为Fe3+,正确;D项,不符合定组成规律,正确的为:2H++SO2-4+Ba2++2OH-===BaSO4↓+2H2O,错误。
答案 C3.常温下,下列各组离子一定能在指定溶液中大量共存的是() A.使酚酞变红色的溶液中:Na+、Al3+、SO2-4、Cl-B.K wc(H+)=1×10-13 mol·L-1的溶液中:NH+4、Ca2+、Cl-、NO-3C.与Al反应能放出H2的溶液中:Fe2+、K+、NO-3、SO2-4D.水电离的c(H+)=1×10-13 mol·L-1的溶液中:K+、Na+、AlO-2、CO2-3解析A项,使酚酞变红色的溶液呈碱性,OH-与Al3+不能大量共存。
高分子课程第二章作业(含答案解释)

高分子化学第二章课后作业(共100分)1、简述逐步聚合的实施方法。
(10分)答案:2、影响线形缩聚物聚合度的因素有哪些?两单体非等化学计量,如何控制聚合度?(10分)备注:影响线形缩聚物聚合度中的第四个因素(反应条件)未回答的也可以给予满分。
另外批改时注意两单体非等化学计量的公式(应该有部分写成两单体等化学计量公式)3、己二酸与下列化合物反应,哪些能形成聚合物并说明原因。
(10分)A.乙醇B.乙二醇C.甘油D.苯胺E.己二胺答案:己二酸(f=2)为2官能度单体,因此能与己二酸形成聚合物的化合物有:乙二醇(f=2)、甘油(f=3)、己二胺(f=2)。
其中与乙二醇(f=2)、己二胺(f=2)形成线形缩聚物,与甘油(f=3)形成体形缩聚物。
答案解释:4、聚酯化和聚酰胺化的平衡常数有何差别?对缩聚条件有何影响?(10分)答案:(1)聚酯化反应平衡常数小,K=4,低分子副产物水的存在限制了聚合物分子量的提高,对聚合反应的条件要求较高,反应须在高温和高真空条件下进行,体系中水的残留量应尽量低,这样才能得到高聚合度的聚合物。
(2)聚酰胺化反应平衡常数中等,K=300-400,水对分子量有所影响,对聚合反应的条件要求相对温和。
聚合早期,可在水介质中进行;聚合后期,须在一定的减压条件下脱水,提高反应程度。
5、分别按Carothers法和Flory统计法计算下列混合物的凝胶点:(10分)(1)邻苯二甲酸酐和甘油按照摩尔比为1.5:0.98进行缩聚(2)邻苯二甲酸酐、甘油、乙二醇按照摩尔比为1.5:0.99:0.002进行缩聚答案:(1)Carothers法:邻苯二甲酸酐(f=2)官能度为2,甘油(f=3)官能度为3,邻苯二甲酸酐和甘油按照摩尔比为1.5:0.98进行缩聚的情况下,属于两基团不相等平均官能度=(2*3*0.98)/(1.5+0.98)=2.371,凝胶点=2/2.371=0.844Flory统计法:由题可知甘油(f=3)官能度为3,则支化单元分率ρ=1,基团比r=(0.98*3)/ (1.5*2)=0.98,f=3则凝胶点=1/[0.98+0.98*1*(3-2)]1/2=0.714(2)Carothers法:邻苯二甲酸酐(f=2)官能度为2,甘油(f=3)官能度为3,乙二醇(f=2)官能度为2,邻苯二甲酸酐、甘油、乙二醇按照摩尔比为1.5:0.99:0.002进行缩聚的情况下,属于两基团不相等平均官能度=2*(0.99*3+0.002*2)/(1.5+0.99+0.002)=2.387,凝胶点=2/2.387=0.838Flory统计法:由题可知甘油(f=3)官能度为3,则支化单元分率ρ=0.99*3/(0.99*3+0.002*2) =0.999,基团比r=(0.99*3+0.002*2)/(1.5*2)=0.991,f=3则凝胶点=1/[0.991+0.991*0.999*(3-2)]1/2=0.71解题思路:(1)首先判断该体系是属于两基团数相等还是两基团数不等;(2)Carothers法:根据体系的类型选择合适的公式计算出平均官能度,进而计算出凝胶点;(3)Flory统计法:根据体系的类型,得到官能度f为多少(此处注意与平均官能度不是一个概念,官能度f为多官能度单体的官能度),选择合适的公式计算出支化单元分率、基团比,进而计算出凝胶点。
高中化学 第二章 化学物质及其变化 第3节 氧化还原反应作业2 新人教版必修1

第3节氧化还原反应1.过氧化氢溶液可作为采矿业废液消毒剂,如消除采矿废液中剧毒的氰化钾,反应方程式为KCN+H2O2+H2O A+NH3↑(已配平),请回答:(提示:3KC N-、122H O-)(1)生成物A的化学式是__________________________________________。
(2)该反应是否是氧化还原反应?________(填写“是”或“否”),其理由是_____________________。
若是,则被还原的元素是________。
【答案】(1)KHCO3(2)是有元素化合价的升降氧2.已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu + 8HNO3 (稀)3Cu(NO3)2+ 2NO↑+ 4H2O(1)被氧化的元素是,被还原的元素是,发生氧化反应的物质是,发生还原反应的物质是。
(2)用双线桥法表示反应电子得失的方向和数目:。
(3)用单线桥法表示反应电子得失的方向和数目:。
【答案】(1)Cu N Cu HNO3(2) (3)3.已知As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO42AsH3↑+6ZnSO4+3H2O。
(1)请用双线桥法标出电子转移的方向和数目____________________________________。
(2)As2O3在上述反应中显示出来的性质是____________(填序号)。
A.氧化性B.还原性C.酸性 D.碱性(3)该反应的氧化产物是__________,还原产物是________。
(4)若生成0.2 mol AsH3,则转移的电子数为___________。
【答案】(1)(2)A(3)ZnSO4 AsH3(4)1.2N A4.饮用水中的3NO -对人类健康会产生危害,为了降低饮用水中3NO -的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将3NO -还原为N 2,其化学方程式为 10Al+6NaNO 3+4NaOH10NaAlO 2+3N 2↑+2H 2O 。
第二章 化学反应的方向部分作业的提示

第二章 化学反应的方向一、选择题(每题2分,共40分)1.如果系统经过一系列变化,最后又变到初始状态,则系统的 (A ) Q =0,W =0,ΔU =0,ΔH =0 (B ) Q ≠ 0,W ≠0,ΔU =0,ΔH =Q (C )Q =-W ,ΔU =Q+W ,ΔH =0 (D ) Q ≠ W ,ΔU =Q+W ,ΔH =02.体系的性质有广延性质和强度性质,下列哪一组均属广延性质 (A )T ,V ,H ,U ; (B )U ,S ,G ,H ; (C )S ,H ,G ,T (D )S ,T ,V ,G 。
3.在下列反应中,r m ΔH 等于AgBr(s)的f m ΔH 的反应是 (A ). Ag+ (aq) + Br- (aq) → AgBr (s) (B ). 2Ag (s) + Br 2 (g)→2AgBr (s)(C ). Ag (s) +12 Br 2 (l) → AgBr (s) (D ) Ag (aq) +12Br 2 (g) → AgBr (s)4.若某体系所吸收的热量,全部用于体系的内能增加,则所需的条件是:①封闭系统 ②不做体积功和其它功 ③恒压 ④恒温(A )①和②; (B )①和③;(C )①和④;(D )②和④。
5.一般来说,以下哪种情况会导致熵值较小? (A) 分子数较多; (B )气体的量增加; (C) 分子对称性增加; (D )固体物质液化。
6.在标准条件下石墨燃烧反应的焓变为-393.6 kJ·mol-1,金刚石燃烧反应的焓变为-395.5kJ·mol-1,则石墨转变成金刚石反应的焓变为 (A ). -789.1 kJ·mol-1 (B ). 0 (C ). +1.9 kJ·mol-1 (D )-1.9 kJ·mol-17.25℃时NaCl 晶体在水中的溶解度约为6 mol·L -1,若在1L 水中加入1 mol NaCl ,则 NaCl (s) + H 2O (l) → NaCl (aq)的(A ). ΔS > 0,ΔG > 0 (B ) ΔS > 0,ΔG < 0 (C ). ΔG > 0,ΔS < 0 (D ). ΔG < 0,ΔS < 0 8.下列物质中可以认为具有最大摩尔熵的是(A ). Li (g) (B ). Li (s) (C ). LiCl·H 2O (s) (D ). Li 2CO 3 (s) 9.下列反应中,r m ΔS 值最大的(A ). C (s) + O 2 (g) → CO 2 (g) (B ). 2SO 2 (g) + O 2 (g) →2SO 3 (g)(C ). CaSO 4 (s) + 2H 2O (l) → CaSO 4·2H 2O (s) (D ). 2NH 3 (g) →3H 2 (g) + N 2 (g) 10.下列热力学函数中数值不为零的是:(A )f m ΔH (Cl 2,g);(B )f m ΔG (Br 2,l);(C )f m ΔG (Hg,l);(D )m S (H 2,g)。
高中化 第2章 化反应的方向、限度与速率 第1节 化反应的方向作业 鲁科4

第2章化学反应的方向、限度与速率第1节化学反应的方向基础巩固1.下列说法正确的是()A.放热反应不一定是自发进行的反应B.吸热反应一定是非自发进行的C.自发进行的反应一定容易发生D.反应速率快的一定是自发进行的2.ΔH-TΔS作为化学反应方向的判据,它适用的条件是()A.温度、压强一定 B.压强一定C.温度、体积一定 D.体系中物质的状态一定3.下列反应中,在高温下不能自发进行的是( )A.CO(g)===C(s,石墨)+12O2(g)B.2N2O5(g)===4NO2(g)+O2(g)C.(NH4)2CO3(s)===NH4HCO3(s)+NH3(g)D.MgCO3(s)===MgO(s)+CO2(g)4.以下自发反应可用能量判据来解释的是()A.硝酸铵自发地溶于水B.2N2O5(g)===4NO2(g)+O2(g)ΔH=56.7 kJ·mol-1C.(NH4)2CO3(s)===NH4HCO3(s)+NH3(g)ΔH=74。
9 kJ·mol-1D.2H2(g)+O2(g)===2H2O(l)ΔH=-571.6 kJ·mol-15.碳酸铵在室温下就能自发地分解产生氨气,下面对其说法正确的是()A.碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大B.碳酸铵分解是因为外界给予了能量C.碳酸铵分解是吸热反应,根据焓判据不能自发分解D.碳酸盐都不稳定,都能自发分解6.有A、B、C、D四个反应:________;另两个反应中,在温度高于________K时可自发进行的反应是________;在温度低于________K时自发进行的反应是________。
能力提升7.下列有关反应的方向说法正确的是()A.放热的自发过程都是熵值减小的过程B.吸热的自发过程常常是熵值减小的过程C.水自发地从高处流向低处,是趋向能量最低状态的倾向D.只根据焓变来判断化学反应的方向是可以的8.能用能量判据判断下列过程的方向的是( )A.水总是自发地由高处往低处流B.放热反应容易自发进行,吸热反应不能自发进行C.有序排列的火柴散落时成为无序排列D.多次洗牌以后,扑克牌的毫无规律的混乱排列的几率大9.对于化学反应能否自发进行,下列说法中错误的是()A.若ΔH<0,ΔS>0,任何温度下都能自发进行B.若ΔH>0,ΔS<0,任何温度下都不能自发进行C.若ΔH>0,ΔS>0,低温时可自发进行D.若ΔH<0,ΔS<0,低温时可自发进行10.已知“凡气体分子总数增大的反应一定是熵增加的反应”.下列反应不可能自发进行的是( )A.2O3(g)===3O2(g)ΔH<0B.2CO(g)===2C(s)+O2(g)ΔH>0C.N2(g)+3H2(g)===2NH3(g) ΔH<0D.CaCO3(s)===CaO(s)+CO2(g)ΔH>011.已知100 kPa、298。
普通化学习题与解答第二章

题目:在等温、等压条件下自发反应总是向着 ΔH - TΔS < 0 的方向进行,因此,在等温、等压条件下,自发反 应总是向着 ΔH - TΔS < 0 的方向进行。
● 解答:K = [C][D] / ([A][B]^2) ● 题目:在一定温度下,向一个容积不变的容器中通入1mol N2和3mol H2及固体催化剂,使之反应:N2(g) + 3H2(g) ⇌ 2NH3(g);ΔH = -92.4kJ/mol,平衡时容器内气体压强为起始时的80%。此时,若向容器
中充入1mol N2、3mol H2和1mol NH3,则平衡移动的方向为____。 解答:向容器中充入$1molN_{2}$、$3molH_{2}$和$1molNH_{3}$,等效为开始充入$2molN_{2}$、$6molH_{2}$,与原起始量之比 相同,为等效平衡,平衡时各物质的浓度相等,则平衡不移动,故答案为:不移动。
● A.NH3的体积分数一定小于反应前混合气体的2v逆(NH3) ● C.平衡时体系中N2、H2、NH3的物质的量之比一定为1:3:2 ● D.平衡时体系中N2、H2、NH3的物质的量之和一定等于起始时体系的总物质的量
● 题目:请写出下列反应的平衡常数表达式:A + 2B → C + D 解答:K = [C][D] / ([A][B]^2)
添加标题
注意事项:在书写平衡常数表达式时,需要注意各组分的化学计量数,它反映了反应中各物质的计 量关系。在本题中,化学计量数分别是1、2、3、4。
题目:请写出下列反应的平衡常数表达式:A + 2B → 3C + 4D 解答:平衡常数表达式为 K = [C]^3[D]^4/[A][B]^2 解释:根据平衡常数的定义,平衡常数等于生成物浓度幂之积与反应物浓度幂之积的比值 注意事项:在书写平衡常数表达式时,需要注意反应物和生成物的浓度幂之积的次序和指数
作业题解(第2章 化学反应的方向和程度)

12.反应PCl5(g) ⇌ PCl3(g) +Cl2(g)在523K和 1.01325×105Pa下达平衡时,其分解百分率为80%,求 该条件下反应的平衡常数Kp。
12.解:设开始时PCl5为1mol PCl5(g) ⇌ PCl3(g) + Cl2(g) 起始时物质的量/mol 1 0 0
KC
x / 152
2
11. 在某温度时,反应 CO (g) + H2O(g) ⇌CO2(g)+ H2(g) 的Kc=1.0, 问2mol CO与多少 mol H2O(g) 在密闭容器中反 应,才能使50%(摩尔分数)的CO转变为CO2 。
解:设有x mol H2O(g),设密闭容器体积为V dm3。 CO (g) + H2O(g) ⇌ CO2(g) + H2(g) 起始浓度/ mol· dm-3 2/V x/V 0 0 平衡浓度/ mol· dm-3 1/V (x-1)/V 1/V 1/V 1 1 c(CO2 ) c ( H 2 ) KC V V 1 x 1 c(CO ) c( H 2O ) V V 1 1.0 x 1 解得: x 2.0mol
第二章 化学反应的方向 和程度习题解答
• 1.不用查表,指出下列各组物质中熵值由大到小的顺序。 • (1) O2(l), O3( g), O2(g) • (2) K(s) , KCl(s) , Na(s) • 解:(1)S(O3,g)> S(O2,g)> S(O2,l) • (2) S(KCl,s)> S(K,s)> S(Na,s)
=(-635.09 ) +(-393.50 ) - (-1206.92 ) =178.33 kJ· mol-1
鲁科版高中化学选择性必修一第2章第2节化学反应的限度(第2课时)作业含答案

2.2.2反应条件对化学平衡的影响【练概念】1.一定条件下,在恒容密闭容器中发生反应22CO NO CO NO ++,达到化学平衡后,降低温度,混合物的颜色变浅,下列有关该反应的说法正确的是( )A.正反应为吸热反应B.正反应为放热反应C.降温后CO 的浓度增大D.降温后各物质的浓度不变2.在一密闭容器中,反应A(g)B(g)a b 达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B 的浓度是原平衡时的60%,则( )A.平衡向逆反应方向移动了B.物质A 的转化率减小了C.物质B 的质量分数增大了D.a b >3.下列事实不能用勒·夏特列原理加以解释的是( )A.夏天,打开啤酒瓶时会在瓶口逸出气体B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体C.氢气与碘蒸气反应达到平衡后压缩混合气体,气体颜色变深D.将盛有二氧化氮和四氧化二氮混合气体的密闭容器置于冷水中,混合气体颜色变浅4.利用工业产生的尾气2CO 可合成绿色燃料甲醇,其反应原理为12232CO (g)3H (g)CH OH(g)H O(g)49.0kJ mol H -++∆=-⋅,当该反应达到平衡时,下列措施能提高甲醇产率的是( )A.使用合适的催化剂B.及时分离产物3CH OH(g)C.降低反应体系的温度D.增大容器容积,减小压强5.下列对化学平衡移动的分析错误的是( )①已达平衡的反应22C(s)H O(g)CO(g)H (g)++,当增加反应物的物质的量时,平衡一定向正反应方向移动②已达平衡的反应223N (g)3H (g)2NH (g)+,当增大2N 的浓度时,平衡向正反应方向移动,2N 的平衡转化率一定增大③有气体参加的反应达到平衡状态时,若减小反应容器容积,平衡一定移动④有气体参加的反应达平衡状态时,在恒压反应容器中充入稀有气体,平衡一定不移动A.仅①④B.①②③④C.仅②③④D.仅①②③ 【练能力】6.在容积不变的密闭容器中,一定条件下进行如下反应:1222NO(g)2CO(g)N (g)2CO (g)373.2kJ mol H -++∆=-⋅。
9 第二章 氧化还原反应(学生版)

第二章 氧化还原反应一、知识梳理 (一)化学反应的类型化学反应从不同的角度可以有多种分类方法。
如:木炭在氧气中燃烧生成二氧化碳的反应,C+O :皇鉴co :,它既是化合反应,又是氧化反应。
化学反应的类型一般有两种分类方法。
1.根据反应物和生成物的类别以及反应前后物质种类的多少,把化学反应分为化合反应、分解反应、置换反应和复分解反应,即通常所说的四种基本类型的反应。
各类物质间的相互关系四种基本类型的反应: 反应类型 表达式 举例化合反应 A+B →AB H 2+O 2−−−→点燃2H 2O 分解反应 AB →A+B KClO 32M nO ∆−−−→2KCl+3O 2↑ 置换反应 A+BC →AC+B Zn+2HCl →ZnCl 2+H 2↑ 复分解反应AB+CD →AD+CBNaOH+HCl →NaCl+H 2O【思考】下列两个化学反应属于上述四种基本反应类型中的哪一种? ①Fe+ 4O 2 −−−→点燃Fe 3O 4 ②CH 4+2O 2−−−→点燃CO 2+2H 2O2.根据反应中物质是否得到氧或失去氧,把化学反应分为氧化反应和还原反应。
氯化反应和还原反应:反应类型 得失氧的情况 举例氧化反应 物质得到氧的反应 S+O 2−−−→点燃SO 2 还原反应物质失去氧的反应CuO+H 2∆−−→Cu+H 2O(二)氧化还原反应氧化铜失去氧发生还原反应,氢气得到氧发生氧化反应。
这两个截然相反的过程是在一个反应中发生的。
在化学反应中,一种物质与氧化合,必然同时有另一种物质中的氧被夺去。
也就是说,有一种物质被氧化,必然有一种物质被还原。
氧化反应和还原反应一定是同时发生的。
从下图可以看出,氧化铜失去氧,铜的化合价从+2价下降到0价,铜元素被还原;氢气得到氧,氢的化合价从0价上升到+1价,氢元素被氧化。
物质所含元素化合价升高的反应是氧化反应,物质所含元素化合价降低的反应是还原反应,有元素化合价升降的化学反应是氧化还原反应。
燃烧学导论第二版第二章作业答案

根据定义:STOICHACTUALA /F |A /F |化学当量反应: 3822222C H a(O 3.76N )3CO 4H O 3.76aNairStoichfuelMW A /F | 4.76a()MW a x y /4 (x=3, y=8,所以a=5)6.15096.4485.28)5(76.4)(76.4|/===fuel air Stoich MW MW a F A当量比:87.00.186.15|/|/===ΦACTUAL STOICH F A F A化学当量反应:81822C H a(O 3.76N )productsa=x+y/4=8+18/4=12.5products N O H C →++22188475.12)1(1 kmol C8H18 与12.5kmolO2和47kmolN2混合 (a ) 81822818000f ,C H f ,O f ,N C H H(1)h 12.5h 47h (J /kmol )2of ,O h 0 2of ,Nh 00f ,C8H18h ?(511页,表B.2)02341f ,C8H18123456h 4184(a a /2a /3a /4a a )T K ()/1000可以算出(298K时):0f ,C8H18h 224,109kJ /kmol)/(109,224)0(47)0(5.12)109,224)(1(188H C kmol J H -=++-=(b )1kmol混合物中有多少mol异辛烷?多少mol氧气?多少mol氮气?0165.0)475.121/(1188=++=H C x 2066.0)475.121/(5.122=++=O x 7769.0)475.121/(472=++=N x每1kmol混合物的焓:0mixi f ,i ih x h ; ii tot x N /Nmix kmol kJ h mix --=++-=/3700)0(7769.0)0(2066.0)109,224(0165.0c) 1kmol混合物有多少千克?(=混合物的分子量乘以1kmol/1000,数值上等于分子量)mix mix mix h h /MW260.30)014.28(7769.0)999.31(2066.0)23.114(0165.0=++==∑i i mix MW x MWmix3700h 122.27kJ /kg 30.260低位热值的概念从哪里来?是一种燃烧焓。
人教版必修1 第2章第3节 氧化还原反应 作业

第3节 氧化还原反应(满分:100分,考试时间:45分钟)一、选择题:本题包括10小题,每小题4分,共40分。
1.下列说法正确的是( )A .金属单质在反应中只能作还原剂,非金属单质在反应中只能作氧化剂B .氧化剂在反应中失去电子,还原剂在反应中得到电子C .氧化剂具有氧化性,还原剂具有还原性D .阳离子只有氧化性,阴离子只有还原性解析:选C A 项,非金属单质在反应中可以做氧化剂也可做还原剂,例如氢气和氧气反应时,氢气做还原剂,氧气做氧化剂,错误;B 项,氧化剂得到电子,还原剂失去电子,错误;D 项,阳离子可能有还原性,例如亚铁离子,错误。
2.下列叙述正确的是( )A .元素的单质一定由氧化或还原该元素的化合物制得B .在化学反应中,得电子越多的氧化剂,其氧化性就越强C .阳离子只能得到电子被还原,阴离子只能失去电子被氧化D .含有最高价元素的化合物不一定具有很强的氧化性解析:选D3.下列关于氧化还原反应的叙述正确的是( )A .H 2还原CuO 的反应只属于还原反应B .置换反应都是氧化还原反应,所以3CO +Fe 2O 3=====高温2Fe +3CO 2既是置换反应又是氧化还原反应C .3O 2=====电火花2O 3是氧化还原反应D .复分解反应一定不是氧化还原反应解析:选 D 氧化还原反应是一个整体,氧化反应和还原反应必然同时发生在同一个反应中,在H 2+CuO Cu +H 2O 过程中,对CuO 而言是化合价降低被还原,发生了还原反应,对H 2而言,则是化合价升高被氧化,发生了氧化反应。
置换反应都是氧化还原反应,但CO 与Fe 2O 3的反应不是置换反应,所以B 错。
复分解反应只是反应物互相交换成分重新组合成新的物质,没有电子转移,所以,复分解反应一定不是氧化还原反应。
C 中反应前后氧元素的化合价都没变化,属于非氧化还原反应。
4.下列不属于四种基本反应类型,但属于氧化还原反应的是( )A .2KClO 3=====MnO 2△2KCl +3O 2↑B .2Na +Cl 2=====点燃2NaClC .Zn +2HCl===ZnCl 2+H 2↑D .Fe 2O 3+3CO=====高温2Fe +3CO 2解析:选D A 是分解反应,B 为化合反应,C 为置换反应,D 不属于四种基本反应类型;它们均是氧化还原反应。
生物反应工程第二章作业
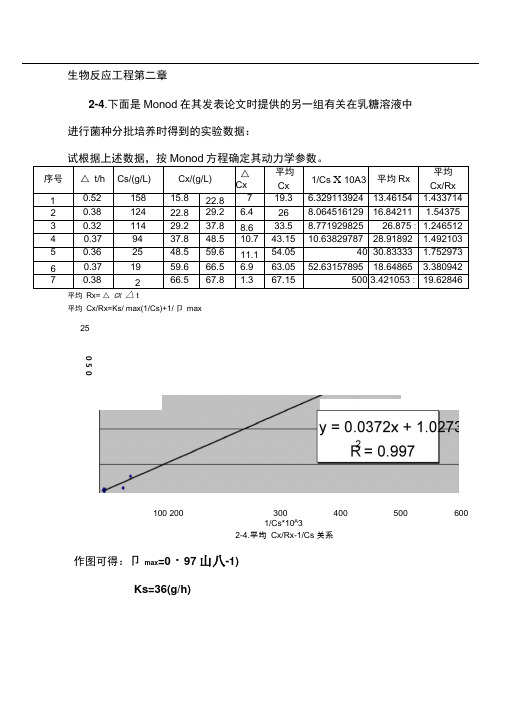
生物反应工程第二章2-4.下面是Monod在其发表论文时提供的另一组有关在乳糖溶液中进行菌种分批培养时得到的实验数据:试根据上述数据,按Monod方程确定其动力学参数。
序号△ t/h Cs/(g/L) Cx/(g/L)△Cx平均Cx1/Cs X 10A3 平均Rx平均Cx/Rx1 0.52 158 15.8 22.8 7 19.3 6.329113924 13.46154 1.4337142 0.38 124 22.8 29.2 6.4 26 8.064516129 16.84211 1.543753 0.32 114 29.2 37.8 8.6 33.5 8.771929825 26.875 : 1.2465124 0.37 94 37.8 48.5 10.7 43.15 10.63829787 28.91892 1.4921035 0.36 25 48.5 59.6 11.1 54.05 40 30.83333 1.7529736 0.37 19 59.6 66.5 6.9 63.05 52.63157895 18.64865 3.3809427 0.38 2 66.5 67.8 1.3 67.15 500 3.421053 :19.62846平均Rx= △ CX t平均Cx/Rx=Ks/ max(1/Cs)+1/ 卩max251/Cs*10A32-4.平均Cx/Rx-1/Cs 关系作图可得:卩max=0・97山八-1)Ks=36(g/h)0 5 02 11600100 200 300 400 5002-5•得:⑴口 max =0・299山八-1)K s =0 ・269(g/h)(2) Y x/s =(C xt -C xo )/(C so -C st )=0.65(3) t d =ln2/ 卩 max =0・693/0・299=2.318(h)2-6 •在一连续操作的机械搅拌实验反应器中用乳糖培养大肠杆菌,该 反应器体积为1L ,加入乳糖的初试浓度为 Cs0=160mg/L 。
《普通化学》第2章作业题解(化学反应的方向和程度)

0 -393.50
S298⊖/J·K-1·mol-1 52.3 5.740 51.55 213.64
ΔH298⊖ = 0 - 393.50 - (-580.7 ) - 0 = 187.2 kJ·mol-1 ΔS298⊖ = 51.55 + 213.64 - 52.3 - 5.740
= 207.15 J·K-1·mol-1
= 204.28 J·K-1·mol-1
ΔG ⊖
2021/1/14T
=
ΔH298⊖-
TΔS298⊖
<
0
⇒
T
H
298
S
298
580 .7 1000 204 .28
2843 K
(2)
SnO2 (s) + C(s) ≜ Sn(s) + CO2 (g)
ΔfH298⊖ /kJ·mol-1 -580.7 0
ΔGT⊖ = ΔH298⊖ - TΔS298⊖ < 0 ⇒
T
H
298
S
298
187.2 1000 207.15
903.7K
2021/1/14
(3)
SnO2 (s) + 2H2(g) ≜ Sn(s) + 2H2O(g)
ΔfH298⊖ /kJ·mol-1 -580.7
0
0 -241.82
S298⊖/J·K-1·mol-1 52.3 130.574 51.55 188.72
= 39.75 + 213.64 - 92.9 = 160.49 J·K-1·mol-1 T=298 K时, ΔG⊖ = ΔH298⊖ - TΔS298⊖
= 178.33 - 298×160.49×10-3 = 130.50 kJ·mol-1
燃烧学导论第二版第二章作业答案

根据定义:STOICHACTUALA /F |A /F |F =化学当量反应: 3822222C H a(O 3.76N )3CO 4H O 3.76aN ++?+airStoich fuelMW A /F | 4.76a()MW = a x y /4=+ (x=3, y=8,所以a=5)6.15096.4485.28)5(76.4)(76.4|/===fuel air Stoich MW MW a F A当量比:87.00.186.15|/|/===ΦACTUAL STOICH F A F A化学当量反应:81822C H a(O 3.76N )products ++?a=x+y/4=8+18/4=12.5products N O H C →++22188475.12)1(1 kmol C8H18 与12.5kmolO2和47kmolN2混合(a ) 81822818000f ,C H f ,O f ,N C H H (1)h 12.5h 47h (J /kmol )=++2o f ,O h 0= 2o f ,N h 0=0f ,C8H18h ?=(511页,表B.2)02341f ,C8H18123456h 4184(a a /2a /3a /4a a )T K q q q q q q -=+++-+=()/1000可以算出(298K时):0f ,C8H18h 224,109kJ /kmol =-)/(109,224)0(47)0(5.12)109,224)(1(188H C kmol J H -=++-=(b )1kmol混合物中有多少mol异辛烷?多少mol氧气?多少mol氮气?0165.0)475.121/(1188=++=H C x 2066.0)475.121/(5.122=++=O x 7769.0)475.121/(472=++=N x每1kmol混合物的焓:0mix i f ,i ih x h =å; i i tot x N /N =mix kmol kJ h mix --=++-=/3700)0(7769.0)0(2066.0)109,224(0165.0c) 1kmol混合物有多少千克?(=混合物的分子量乘以1kmol/1000,数值上等于分子量)mix mix mix h h /MW =260.30)014.28(7769.0)999.31(2066.0)23.114(0165.0=++==∑i i mix MW x MWmix 3700h 122.27kJ /kg 30.260-==-低位热值的概念从哪里来?是一种燃烧焓。
高中化学第2章化学反应速率与化学平衡第2节第2课时化学平衡常数作业含解析第一册

第2课时化学平衡常数A级·基础达标练一、选择题1.已知下列反应的平衡常数:H2(g)+S(s)H2S(g),K1;S(s)+O2(g)SO2(g),K2。
则反应:H2(g)+SO2(g)O2(g)+H2S(g)的平衡常数为(D)A.K1+K2B.K-K2C.K1×K2D.错误!2.T℃时,在3 L的密闭容器中充入4 mol光气(COCl2),发生反应COCl2(g)CO(g)+Cl2(g),同时还发生反应2CO(g)2C(s)+O2(g),当反应达到平衡时,测得CO(g)和C(s)的物质的量分别为 2 mol和 1 mol,则该温度下,CO(g)+Cl2(g)COCl2(g)的平衡常数K为(D)A.错误!B.2C.13D.错误!解析:T℃时,在3 L的密闭容器中充入4 mol光气,同时发生的反应还有2CO(g)2C(s)+O2(g),当反应达到平衡时,测得CO(g)和C(s)的物质的量分别为2 mol和1 mol,设消耗COCl2(g)物质的量为xCOCl2(g)Cl2(g)+CO(g)起始量(mol)400变化量(mol)x x x平衡量(mol)4-x x x2CO(g)2C(s)+O2(g)起始量(mol)x00变化量(mol)110.5平衡量(mol)210.5x=3 mol则平衡浓度为COCl2(g)为错误!mol·L-1,Cl2(g)为1 mol·L-1,CO(g)为错误!mol·L-1。
COCl2(g)Cl2(g)+CO(g)的平衡常数K′=错误!=2,则该温度下,Cl2(g)+CO(g)COCl2(g)的平衡常数K=错误!。
3.在密闭容器中充入SO2与18O2发生反应2SO2+O2错误!2SO3,反应一段时间后,含18O的物质是(D)A.只有O2B.只有SO2C.SO2和O2D.SO2、O2和SO3解析:反应过程中化学键断裂,存在原子有S、16O、18O,原子重新组合生成物质,反应是可逆的,最终SO3、SO2、O2中都含18O.4.一定条件下,可逆反应2A(g)B(g)+3C(g),在下列四种状态中,处于平衡状态的是(D)正反应速率逆反应速率A.v(A)=2 mol·L-1·min-1v(B)=2 mol·L-1·min-1B.v(A)=2 mol·L-1·min-1v(C)=2 mol·L-1·min-1C.v(A)=1 mol·L-1·min-1v(B)=2 mol·L-1·min-1D.v(A)=1 mol·L-1·min-1v(C)=1。
920124-李狄-电化学原理-第二章-作业

电极反应
() ()
Zn Zn2 2e Hg2Cl2 2e 2Hg 2Cl
电池反应
Zn Hg 2Cl 2 Zn2 2Hg 2Cl
E
E0
RT 2F
ln
Zn 2
Cl
2
E
E0
RT 2F
ln
Zn 2
Cl
2
E
E0
RT 2F
ln(cZn 2
)(c Cl
)2
E
E0
RT 2F
ln
4c3
3
E0
m' '
nF ' ' F ' '
m' ' ' '
lg ' 0.0822 lg 0.082 0.3046 ' 0.496
' ' 2 0.0591 0.0082
' '
电池2是有迁移浓差电池,且电极对阴离子可逆
(2)Eb t RT ln( ' ) 2t RT ln( ' )
nF ''
电极反应
() H 2 2H 2e () I 2 2e 2I
电池反应
H 2 I 2 2HI
E
E0
RT 2F
ln
1
HI 2
E0
0
0
0(350C)
0(250C) 1.310 4(t 250C)
0.5346 1.310 4(350C 250C) 0.5333V
(3)该反应的△G0值 (4)该反应的平衡常数K值 (5)如果把上述反应改写成1/2H2(101325 Pa)+1/2I2=2HI (α=1),以上各问的答案是否会改变
2020-2021学年人教版必修1第2章第2节离子反应第1课时作业(word版)

酸、碱、盐在水溶液中的电离(40分钟70分)一、选择题(本题包括11小题,每小题4分,共44分)1.下列说法正确的是( )A.酸、碱、盐都是电解质B.电解质都是易溶于水的物质C.氧化物都是电解质D.氢化物都不是电解质【解析】选A。
电解质是根据化合物能否电离出离子划分的,不是根据化合物的水溶性划分的,B 项错。
氧化物有的是电解质,如Na2O、CaO等;有的不是电解质,如CO2、SO2等,C项错。
氢化物有的是电解质,如HCl、HF等;有的不是电解质,如CH4、NH3等,D项错。
【补偿训练】2.电解质是指在水溶液中或熔融状态下能够导电的化合物。
几位同学对此定义中关键词发表了以下理解或看法,你认为不正确的是( )A.“或”字意味着水溶液中、熔融状态下这两个条件只需具备其中之一就行了B.“能够导电”是指该物质本身能够导电,而不是它发生反应后的生成物能导电C.“化合物”指明了该物质不能是单质,更不能是混合物D.像硫酸钡、碳酸钙这样难溶的化合物就不可能是电解质了【解析】选D。
溶解性与是否为电解质无关。
如易溶的物质乙醇不是电解质,而难溶的BaSO4却是电解质。
3.下列物质中,属于电解质的是()A.二氧化氮B.蔗糖C.铜D.硝酸钾【解析】选D。
从物质类别上说,酸、碱、盐和水属于电解质。
【方法规律】电解质判断的三个角度1.从物质类别判断2.从物质性质看:电解质在一定条件下可以导电,条件是溶于水或熔融状态下,二者具备其一即可。
3.从是否自身电离看:电解质溶于水或熔融状态时,电解质自身发生电离,有些非电解质如NH3、CO2等,溶于水也能导电,但都不是自身电离产生的离子。
【补偿训练】4.下列物质属于非电解质的是 ( )A.NH3B.(NH4)2SO4C.Cl2D.CH3COOH【解析】选A。
A项,NH3溶于水可以导电,但不是NH3发生了电离,而是NH3·H2O电离出的离子,所以NH3不是电解质,而是非电解质;B项的(NH4)2SO4是盐,是电解质;C项Cl2为单质,不是化合物,既不是电解质,也不是非电解质;D项CH3COOH是酸,是电解质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第2章均相反应动力学作业题答案
2-1 一分批进行的均相酶反应,底物的初始浓度为3×10-5mol/L ,Km=1×10-3mol/L ,经过2min 后,底物转化了5%。
假定该反应符合M-M 方程,试问当该反应经过10min 、30min 和60min 时,该底物转化了多少?
2-1 答案:。
,;,;,,时,,,),(,而,,,可视为一级反应,
785.0X min 60t 537.0X min 30t 236.0X min 10t ,e 1X ,026.02
95
.0ln k %5X min 2t e 1X t k X 11
ln
X 1C C t k C C ln dt k C dC C k dt
dC C k C K r r ,C K ,C K C r r S S S t 026.0S 1S t k S 1S
S 0S S 1S
0S t
01C C S S S 1S
S 1S m max S 0S m S
m S
max S 1S 0
S
======-==-=
==-==--===-
=-==
〉〉+=--⎰⎰
2-2 某酶反应,其Km=0.01mol/L 。
为了求其最大反应速率r max 值,现通过实验测得该反应进行5min 时,底物已转化了10%,
已知C S0=3.4×10-4mol/L ,并假定该反应可用M-M 方程表示。
试求: (1)最大反应速率r max 为多少?
(2)反应15min 后,底物浓度为多少?
2-2答案:。
)(,时,,,),(,而,,,可视为一级反应,
L /mol 1048.2)271.01(104.3X 1C C ,271.0e 1e 1X min
L /mol 101.201.0021.0K k r ,021.05
9
.0ln k %10X min 5t e 1X t k X 11ln
X 1C C t k C C ln dt k C dC C k dt
dC C k C K r r ,C K ,C K C r r 44S 0S S 15021.0t 021.0S 4m 1max 1S t k S 1S
S 0S S 1S
0S t
01C
C S S S 1S
S 1S m max S 0S m S
m S
max S 1S 0
S --⨯----⨯=-⨯=-==-=-=⋅⨯=⨯===-=
==-==--===-=-==
〉〉+=⎰⎰
2-3试根据下列实验数据确定r
max 、K
m
和K
I
值,并说明该酶反应是属于竞争
由图可得:(1/r max )×102=1,r max =100μmol/Lmin 。
1/Km=0.43,
Km=2.33×10-4mol/L ,1/KmI=0.22,KmI=4.54×10-4mol/L ,KmI= Km (1+C I /K I ) K I =2.32×10-4μmol /L 。
2-4 某一酶反应Km 值为4.7×10-5mol/L ,r max =22μmol/(L · min),C S =2 ×10-4mol/L ,C I = 5×10-4mol /L ,K I = 5 × 10-4mol /L 。
试分析计算在竞争性抑制、非竞争性抑制、反竞争性抑制三种情况下的反应速率和抑制程度。
2-4答案:竞争性:min L /mol 53.13C )K C 1(K C r r S
I
I
m S
max SI ⋅μ=++=
非竞争性:min L /mol 68.6)
C K )(K C 1(C r r S m I
I S
max SI ⋅μ=++=
反竞争性:min L /mol 58.7)
K C
1(C K C r r I
I S m S
max SI ⋅μ=++=
无抑制时:min L /mol 81.17C K C r r S
m S
max SI ⋅μ=+=
则竞争性:24.0r r r i S SI
S =-=
非竞争性:625.0r r r i S
SI
S =-=
-1
1 2 3 4 5 6 7 -0.5 -0.4 -0.3 -0.2 -0.1 0
0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9
1
1.1
反竞争性:574.0r r r i S
SI
S =-=
2-5 在某种水解酶的作用下葡萄糖-6-硫酸可以分解为葡萄糖和硫酸。
在一定的酶浓度下,测得M -M 方程中的参数K m =6.7 ×10-4mol/L ,r max =3 ×10-7mol/(L ·min) 。
对该反应,半乳糖-6-硫酸是一竞争性抑制剂。
当C S0= 2 ×10-5mol/L , C I0= 1×10-5mol/L 时,测得反应速率r SI =1.5 ×10-9mol/(L ·min) 。
试求K mI 和K I 值。
2-5答案:
L /mol 1098.3)K C 1(K K L
/mol 1002.2K ,C )K C
1(K C r r 3I
I
m mI 6I S
I I m S
max SI --⨯=+
=⨯=++=。
