胆固醇人类合成途径、酶及药物整理
胆固醇的合成和代谢

胆固醇的合成和代谢胆固醇是一种脂质类有机物,是人体内常见的一种脂类。
它在人体内起着重要的生物学功能。
胆固醇具有调节细胞膜的流动性、合成维生素D、产生胆酸等多种作用。
然而,胆固醇在体内产生过程中,也存在着一定的问题。
本文将对胆固醇的合成和代谢进行详细的论述。
一、胆固醇的合成胆固醇主要在肝脏和肠道中合成。
肝脏是胆固醇合成的主要场所,其合成主要通过内源性合成和摄入的方式完成。
1. 内源性合成内源性合成是通过一系列的酶催化反应在肝脏细胞中完成的。
首先,乙酰辅酶A与乙酰基辅酶A羧化酶发生反应,生成乙酰辅酶A羧化酶。
接着,乙酰辅酶A羧化酶与缩醛酯酶和甲基戊二酰辅酶A还原酶作用,最终生成胆固醇。
2. 摄入食物中摄入的胆固醇也是人体胆固醇含量的重要来源。
当摄入的食物中胆固醇较多时,肠道吸收的胆固醇会超过肝脏的合成能力,导致胆固醇水平的增加。
二、胆固醇的代谢胆固醇除了通过合成获得外,还通过一系列代谢反应在体内进行转化或排泄。
1. 胆固醇酯化在肠道中,胆固醇会与长链脂肪酸酯化生成胆固醇酯,然后结合胆固醇转运蛋白(CETP)转运到其它脂蛋白中,形成低密度脂蛋白(LDL)和高密度脂蛋白(HDL)。
2. 转运和吸收胆固醇通过转运蛋白从肠道吸收,并结合胆汁酸形成混合胆汁,然后进一步转运到肝脏中。
在肝脏中,部分胆固醇被胆盐转运蛋白(ABCG5/G8)运到胆汁中,排出体外。
3. 胆固醇代谢途径胆固醇在体内主要代谢为胆酸和胆色素。
胆酸合成途径是胆固醇代谢的另一重要环节。
胆酸合成需要经历多个酶催化反应,最终生成胆酸,并通过胆道排泄到肠道中。
三、胆固醇的调节机制由于胆固醇是一种重要的生理物质,体内对其合成和代谢有一套严密的调节机制。
1. 受体介导的内吞作用胆固醇与脂蛋白结合后通过受体介导的内吞作用,进入细胞内部。
这个过程是细胞摄取外源性胆固醇的重要途径。
2. 胆固醇合成抑制一旦细胞内胆固醇水平过高,会通过转录因子SREBPs(胆固醇调节元件结合蛋白)抑制胆固醇合成相关酶基因的表达。
胆固醇的合成与代谢途径

胆固醇的合成与代谢途径胆固醇是体内一种重要的脂质物质。
它的主要作用是构建细胞膜,制造激素和胆汁,同时还可能对心血管系统产生影响。
人体内胆固醇的合成和代谢途径复杂,下面让我们来了解一下。
一、胆固醇的合成胆固醇的合成主要发生在肝脏和小肠中,包括以下几个步骤:1、乙酰辅酶A的转化:在肝细胞中乙酰辅酶A首先转化为乙酰丙酮酸。
2、缬氨酸和丙酮酸的合成:乙酰丙酮酸接下来与缬氨酸结合,经过一系列催化反应后生成羟甲基戊二酸。
3、胆固醇的前体物质:羟甲基戊二酸接下来通过一系列催化反应分解成异戊二烯丙酰辅酶A,然后再转化为色氨酸,接着是一系列的反应后最终合成甲基戊二酸。
4、甲基戊二酸的转化:甲基戊二酸经过一系列的化学反应,最终合成出胆固醇。
这一过程主要需要受到3-羟基-3-甲基戊二酸的介导。
二、胆固醇的代谢胆固醇的代谢过程十分复杂。
从摄入膳食中的胆固醇开始,到最终经过多次转化变成胆酸和排泄,期间经历了以下几个步骤:1、膳食胆固醇的吸收:大部分的膳食胆固醇被小肠粘膜吸收,进入小肠细胞内部。
小部分的膳食胆固醇经过酯化反应后和其他脂质物质一起被吸收,形成胆固醇酯。
2、肝脏中胆固醇的代谢:膳食中的胆固醇在被吸收后,需要经过肝脏代谢后才能达到其他细胞。
肝脏将血液中的胆固醇提取出来,一部分被转化为胆汁酸,一部分是胆固醇酯储存在肝细胞里面。
3、胆汁中胆固醇的排泄:肝脏将胆汁酸和胆固醇酯合成胆汁排放进入肠道,一部分胆固醇被肠道吸收,剩下的胆固醇排泄出体外。
4、胆固醇的运输:胆固醇主要通过低密度脂蛋白和高密度脂蛋白进行运输,在血液中达到目的组织后,才能被细胞吸收利用。
总的来说,胆固醇的合成和代谢途径非常复杂,需要多种物质的参与。
人体内胆固醇合成与代谢的平衡关系对我们的健康有重要的影响,合理的饮食和生活习惯能够有效地影响胆固醇平衡关系。
口腔执业医师考试辅导:胆固醇代谢

口腔执业医师考试辅导:胆固醇代谢
胆固醇代谢
胆固醇是人体主要的固醇类化合物,它既是生物膜及血浆脂蛋白的重要成分,又是类固醇激素、胆汁酸及维生素D的前体,体内可自行合成。
(1)胆固醇合成部位和合成原料和关键酶
全身各组织均可合成胆固醇,肝是合成胆固醇的主要场所。
合成胆固醇的原料为乙酰辅酶A和NADPH,此外还需ATP提供能量。
胆固醇合成的关键酶是HMG CoA还原酶。
(2)胆固醇合成的调节
β-羟-β甲戊二酸单酰CoA(HMG-CoA)还原酶是胆固醇合成的限速酶,也是各种因素对胆固醇合成的调节点。
胆固醇的合成受到下列因素的调节:
①饥饿与饱食:饥饿与禁食可抑制肝合成胆固醇。
②胆固醇:胆固醇可反馈抑制肝脏合成胆固醇,它主要抑制HMG-CoA还原酶的合成。
③激素:胰岛素和甲状腺素能增加胆固醇的合成。
胰高血糖素和皮质醇能减少胆固醇的合成。
甲状腺素还可促进胆固醇在肝脏内转变成胆汁酸,因此甲状腺功能亢进时,患者血清胆固醇含量反见下降。
(3)胆固醇的转化
①转变为胆汁酸:主要去路是在肝内转化成胆汁酸。
②转化为类固醇激素:胆固醇是肾上腺、睾丸和卵巢等内分泌合
成及分泌类固醇激素的原料。
③转化为7-脱氢胆固醇:在皮肤,胆固醇可被氧化为7-脱氢胆固醇,经紫外线照射转变成维生素D。
例题(单选):胆固醇不能转化成
A.胆汁酸
B.维生素D3
C.睾酮
D.雌二醇
E.胆红素
答案:E。
胆固醇合成和代谢的生物化学机制

胆固醇合成和代谢的生物化学机制胆固醇是人体内最为重要的脂类物质之一,是细胞膜的一种重要成分,也是许多激素合成的原料。
但是,胆固醇水平过高会导致心血管疾病等健康问题。
因此,身体必须控制其胆固醇水平,这需要多种机制共同发挥作用,包括胆固醇生合成、胆固醇运输、胆固醇代谢和胆固醇的降解等。
胆固醇的生合成胆固醇是从乙酰辅酶A途径合成的,这个途径也被称为胆固醇生合成途径。
胆固醇生合成始于醋酸的羧化,然后通过一系列中间代谢产物,最终形成胆固醇。
其中参与合成途径的酶包括乙酰辅酶A羧化酶、乙酰辅酶A酯化酶、酮酸还原酶等,这些酶还需要多种辅助因子来协同作用。
与胆固醇生合成途径有关的基因共有20多种,它们分布在不同的染色体和不同的细胞类型中。
这些基因编码着酶和辅助因子,与胆固醇生成相关的基因的表达水平和活性受到多个因素的影响,包括营养状态、激素水平、代谢产物的浓度等。
近年来,关于胆固醇生合成途径的研究在调控机制和基因表达方面取得了许多进展,这些研究不仅深入解释了人体中胆固醇的生成和代谢机制,还在疾病的预防和治疗方面有着重要的应用价值。
胆固醇的代谢在胆固醇合成途径之外,人体还有一些重要的代谢途径可以调节胆固醇水平,这些途径主要包括胆汁酸代谢、胆固醇酯化和胆固醇与甘油三酯代谢等。
胆汁酸是由胆固醇代谢过程中形成的一种产物,大部分胆汁酸从肝脏排泄到肠道,被转化为胆酸和胆酸的盐酸,分别参与脂肪吸收和代谢。
然而,在肠道中,胆汁酸也有可能重新被吸收进入身体内部,再次循环代谢,这个过程被称为肠道内胆汁酸回收。
胆固醇酯化是一种调节胆固醇水平的重要途径,酯化后的胆固醇在代谢中较难参与细胞内脂类代谢,并且可以贮存在脂肪组织中。
胆固醇酯化是由一种称为胆固醇酯转移酶的酶催化的,该酶将胆固醇与一种称为脂类酰辅酶A的代谢产物结合,形成胆固醇酯。
胆固醇和甘油三酯有密切的关系,甘油三酯是一种与胆固醇代谢相近的物质,它们同属于脂类代谢产物,都需要多种酶和代谢途径的共同实现和调节,并且它们之间也有着相应的相互干扰和调节作用。
胆固醇合成与代谢调控

胆固醇合成与代谢调控胆固醇是一种脂质,在体内广泛存在,而且对于我们的身体很有必要。
在人体中,胆固醇是一种重要的组成部分,它在细胞中起着维持细胞膜完整性、合成荷尔蒙、维持神经系统健康等重要作用。
但是,如果胆固醇含量过多,就会增加动脉粥样硬化、心脏病等心血管疾病的风险。
因此,研究胆固醇的合成和代谢调控对于预防和治疗这些疾病十分重要。
一、胆固醇的合成途径胆固醇的合成主要发生在肝脏和肠道中,而且合成的起点都是从醋酸开始。
醋酸可以通过三个途径转化成胆固醇,分别是类固醇原路(mevalonate)途径、非类固醇原路(non-mevalonate)途径以及嗜氧呼吸(aerobic respiration)途径。
其中,类固醇原路途径是胆固醇合成的主要途径,它包括两个阶段:第一阶段是醋酸—丙酮酸—胆酸酰辅酶A(acetyl-CoA)途径,第二阶段是胆固醇合成途径。
在这个过程中,mRNA等因子的作用是必不可少的。
二、胆固醇的代谢调控胆固醇的合成与代谢调控主要由两种基础机制实现,分别是靶点反应和反馈抑制。
靶点反应是指正常代谢活动期间合成胆固醇的靶点反应机制。
在这个过程中,膳食胆固醇的摄入和肝脏胆固醇的合成从变量方面受到调节,从而控制胆固醇的代谢。
反馈抑制则是旨在降低细胞内胆固醇水平的机制。
在这个过程中,有三种非常重要的酶参与了胆固醇代谢调控,分别是胆固醇酰辅酶A还原酶(HMG-CoA reductase)、胆固醇酯酶(ACAT)和胆固醇7α-羟化酶(CYP7A1)。
HMG-CoA reductase是限制胆固醇合成的主要酶,因此可以作为一个“瓶颈”来调节胆固醇合成。
ACAT参与了胆固醇在细胞中的储存和利用,而CYP7A1则被认为是胆固醇代谢的限制因子。
三、胆固醇与健康胆固醇的含量过多会增加心血管疾病、脑血管疾病等的风险。
因此,通过改变饮食习惯、增加体育锻炼等方式来控制胆固醇含量是非常重要的。
此外,药物治疗也是控制胆固醇含量的有效手段之一。
脂肪酸与胆固醇的合成与代谢

脂肪酸与胆固醇的合成与代谢脂肪酸与胆固醇是人体内重要的脂类物质,在维持人体健康和正常生理功能方面具有重要作用。
本文将探讨脂肪酸与胆固醇的合成与代谢过程,以及它们在人体内的功能和调节机制。
一、脂肪酸的合成与代谢1.1 脂肪酸的合成在人体内,脂肪酸的合成主要发生在肝脏和脂肪组织中。
脂肪酸的合成过程被称为脂肪酸合成途径,主要依赖于一系列酶的参与。
首先,由葡萄糖酶磷酸化酶(glucokinase)催化的葡萄糖经糖酵解途径产生的乙酰辅酶A(Acetyl-CoA)是脂肪酸合成的前体物质。
然后,乙酰辅酶A与二氢异戊酸(Malonyl-CoA)在脂肪酸合成酶复合物的催化下,通过一系列反应逐渐合成长链脂肪酸。
最后,脂肪酸通过脂肪酸合成酶的催化与甘油酯结合形成三酰甘油(Triglyceride),被储存在脂肪细胞中。
1.2 脂肪酸的代谢脂肪酸代谢包括脂肪酸的氧化和合成反应。
脂肪酸氧化是指将脂肪酸分解为乙酰辅酶A,进而通过TCA循环(三羧酸循环)产生能量。
脂肪酸氧化发生在线粒体内,经过一系列酶的催化作用,脂肪酸被解体为乙酰辅酶A分子,并进入TCA循环产生能量。
此外,脂肪酸还可通过β氧化作用进一步分解为辅酶A和乙酰辅酶A,提供更多的能量供给。
二、胆固醇的合成与代谢2.1 胆固醇的合成胆固醇合成主要发生在肝脏和肠道上皮细胞中。
胆固醇合成是复杂的生物合成过程,主要依赖于多个酶的催化。
胆固醇的合成途径包括两个主要过程:前体物质戊二酸(Acetyl-CoA)通过一系列反应转化为甲酰辅酶A(Methylmalonyl-CoA),然后合成胆固醇。
胆固醇的合成过程是一个调控严格的代谢途径,受到多个酶和转运蛋白的调控。
2.2 胆固醇的代谢胆固醇的代谢主要通过两条途径进行:胆固醇酯化和胆汁酸合成。
胆固醇酯化是指将胆固醇与脂肪酸结合形成胆固醇酯,以便在脂蛋白颗粒中进行转运。
胆固醇酯可以被转运到组织细胞中,也可以通过胆固醇酯酶的催化重新释放为游离胆固醇。
胆固醇的合成与调控

胆固醇的合成与调控胆固醇是一种重要的脂类化合物,广泛存在于人体细胞中。
它在机体内起着不可或缺的生理功能,并参与多种代谢途径。
然而,高胆固醇水平与心血管疾病之间存在紧密的联系,因此了解胆固醇的合成与调控机制显得尤为重要。
一、胆固醇的合成过程胆固醇的合成主要发生在肝脏和小肠上皮细胞中。
这个过程通常被称为内源性胆固醇合成,约占全身胆固醇的80%。
具体的合成过程可以分为几个关键步骤。
首先是醋酸与乙酰辅酶A的缩合,形成一种6碳酮体——羟甲戊二酮。
随后,羟甲戊二酮进一步转化为甲戊二酮,并通过一系列酶的作用逐步合成甾体内异构酶。
此过程中,乙酰辅酶A与洛尔氏反应的关键酶物质是HMG-CoA还原酶和HMG-CoA合酶。
在胆固醇的合成过程中,HMG-CoA还原酶与HMG-CoA合酶等酶发挥着重要的调控作用。
同时,还受到许多内外因素的影响,例如胰岛素、糖皮质激素和雌激素等。
二、胆固醇的调控机制胆固醇的合成和代谢是一个复杂的过程,其中存在许多调控机制,以维持胆固醇的正常水平。
主要的调控机制包括内源性和外源性的胆固醇调控。
内源性胆固醇调控主要通过转录因子SREBP(内质网膜蛋白SREBP)调控。
在细胞内,SREBP通过结合内质网上的SCAP (SREBP切割激活蛋白)而转移到高尔基体,并被S1P(SREBP切割蛋白)和S2P(SREBP切割激活蛋白)酶切割,释放出活性的SREBP。
活性的SREBP进入细胞核,并与基因组中调控胆固醇合成的基因启动子结合,从而促进胆固醇合成。
外源性胆固醇调控主要通过LDL受体介导。
人体通过食物摄入胆固醇,肠道细胞合成胆盐以帮助胆固醇吸收。
胆盐通过胆汁流向小肠,并与胆固醇形成混合胆汁。
混合胆汁经过肝脏重新吸收胆固醇,将其转运至体内需要的部位。
当体内胆固醇水平过高时,LDL受体的合成和表达会受到调控。
LDL受体可以识别血液中载脂蛋白LDL(低密度脂蛋白)上的胆固醇,并介导其从血液中清除。
因此,LDL受体的增加可以帮助降低体内胆固醇水平。
高中生物校本课程-胆固醇代谢

细胞定位:细胞质、光面内质网
(二)合成原料
1分子胆固醇 18乙酰CoA + 36ATP + 16(NADPH+H+)
葡萄糖有氧氧化
磷酸戊糖途径
乙酰CoA通过柠檬酸-丙酮酸循环出线粒体
(三)合成基本过程
线粒体中 乙酰CoA
原料
柠檬酸-丙 酮酸循环
入胞质
HMG-CoA
2.引起AS的脂蛋白
脂蛋白残粒
CM和VLDL经LPL水解生成CM残粒与IDL, 并转变成富含胆固醇酯和ApoE的颗粒沉积于血 管壁,经清道夫受体介导摄取进入巨噬细胞引起 AS的增强作用。
变性LDL
乙酰LDL 、 氧化LDL 、 糖化LDL 经修饰的LDL,如OX-LDL会激活巨噬细胞,使 巨噬细胞摄取乙酰LDL而转变成泡沫细胞,促进 AS形成。
HDL2在CETP介导下,与VLDL、LDL进行CE交换,同时也转 运TG,以VLDL、LDL形式经肝脏摄取,最终使末梢组织的FC输
送到肝脏。HDL主要功能是参与胆固醇逆转运(RCT) (胆固醇
逆转运)
三、动脉粥样硬化(AS)
1.概述
AS是指动脉内膜的脂质、血液成分的沉积,平滑肌 细胞及胶原纤维增生,伴有坏死及钙化等不同程度病变 的一类慢性进行性病理过程。AS主要损伤动脉内壁膜。
限速酶
HMG-CoA 还原酶
胆固醇酯
胆固醇
鲨烯
甲基羟戊酸 (MVA)
胆固醇合成的调节
限速酶
饱食 胰岛素 甲状腺素
HMG-CoA还原酶
胆固醇 饥饿禁食
胰高血糖素
➢酶的活性具有昼夜节律性 (午夜最高,中午最低)
胆固醇代谢的分子机制和疾病关联性

胆固醇代谢的分子机制和疾病关联性胆固醇是一种重要的脂质物质,它在人体中具有多种重要的生理功能。
但是胆固醇的过高或者过低都会对人体健康产生负面影响。
因此人们对于胆固醇代谢的分子机制和疾病关联性的研究颇为关注。
一、胆固醇的代谢途径胆固醇在人体的代谢过程中,可以通过三种途径进行代谢。
1、内源性途径:合成胆固醇的主要器官是肝脏,肝细胞内的HMG-CoA加酰酶A可以催化醋酶酰转移,合成甲基戊烯基二磷酸(Mevalonate),经过一系列酶的介导,最后形成胆固醇。
2、外源性途径:胆汁是肝脏合成的一种液体,胆汁中含有很多胆固醇。
当食物进入小肠时,胆汁中的胆固醇就可以被摄入人体。
3、代谢途径:胆固醇在人体内存在两种形式,一种是自由态的游离胆固醇,另一种是与载脂蛋白结合的胆固醇。
人体通过代谢途径,将游离胆固醇和载脂蛋白结合的胆固醇代谢成为胆酸和类固醇。
二、胆固醇的疾病关联性在人体内,胆固醇的代谢失衡会引起多种疾病。
主要有以下几种。
1、高胆固醇血症:如果人体内的胆固醇过高,就会导致高胆固醇血症。
高胆固醇血症是一种多发病,它的发生与饮食、运动、年龄、性别等因素都有关系。
2、冠心病:胆固醇过多会沉积在血管壁上形成动脉粥样硬化斑块,严重时甚至会引发冠心病。
3、糖尿病:胆固醇过多可以引起胰岛素抵抗,从而导致糖尿病的发生。
4、癌症:胆固醇过多会增加乳腺、结肠、前列腺等癌症的发生率。
5、肝病:肝脏是胆固醇的合成器官,长期摄入高胆固醇的食物,会增加患肝病的风险。
三、胆固醇代谢的分子机制人们对于胆固醇代谢的分子机制进行了大量研究,发现许多基因和蛋白质与胆固醇代谢有关。
1、HMG-CoA还原酶:HMG-CoA还原酶是胆固醇生物合成途径的限速酶,它可以控制胆固醇的合成速率。
2、LDL受体:LDL受体是从细胞外界血浆中扫描LDL的膜蛋白,可以从血液中清除LDL,控制胆固醇的水平。
3、胆固醇酯转移酶:胆固醇酯转移酶可以将胆固醇与脂肪酸结合成为胆固醇脂肪酸酯,使其转移到其他组织中。
参与胆固醇合成的酶

参与胆固醇合成的酶
胆固醇合成的关键酶,是β-羟基-β-甲基戊二酸单酰辅酶A。
从胆固醇的合成途径可以知道,胆固醇除了可以用来储藏血脂,也是激素合成所必需的原料。
胆固醇合成后,一部分作为能量储存在肝脏以及皮下组织,以备不时之需。
另外一部分就会进一步代谢,参与性激素、皮质类固醇激素等合成。
对于偏瘦的病人,一方面体内的脂肪动员会增加,使胆固醇分解增加,满足机体必需的能量要求。
另一方面病人的激素水平相对也会偏低,更容易出现激素水平异常。
所以胆固醇也并不是越低越好,太低会导致储存的能量不够,合成激素所需要的原料也不够,容易出现激素减退的症状。
通常建议将胆固醇控制在较合适的范围内,并且也要控制好胆固醇合成的限速酶。
如果相关的酶缺乏或者酶出现异常,也会导致胆固醇合成异常,出现高脂血症。
这种情况的高脂血症,就不是饮食过多所引起。
参与胆固醇合成的酶

参与胆固醇合成的酶
胆固醇合成是一个复杂的生物化学过程,涉及多个酶的参与。
以下是一些参与胆固醇合成的主要酶:
1.乙酰辅酶A羧化酶(Acetyl-CoA carboxylase):这个酶催化
乙酰辅酶A羧化为丙酰辅酶A,这是胆固醇合成的起始物质。
2.醇酸还原酶(HMG-CoA还原酶):HMG-CoA还原酶将
HMG-CoA(β-羟基-β-甲基戊二酸辅酶A)还原为辅酮A。
3.HMG-CoA合成酶(HMG-CoA synthase):该酶催化戊二酸
羟甲基戊二酸辅酶A转化为HMG-CoA。
4.麦角固醇环化酶(Lanosterol synthase):这个酶参与将
HMG-CoA转化为麦角固醇,麦角固醇是最早合成的四环甾体,是胆固醇的前体。
5.胆固醇7-脱氢酶(Cholesterol 7-alpha-hydroxylase):该酶
催化胆固醇的7位产生羟基,是胆固醇合成途径中的关键控制点。
6.肌酸激酶(Squalene monooxygenase):这个酶介导麦芽酰
辅酶A转化为肌酸,这是胆固醇合成过程的最后一个中间产物。
这些酶是胆固醇合成途径中的关键酶,参与胆固醇的生物合成和调控。
它们的活性和调控受多种因素的影响,包括激素、营养状态和基因表达等。
了解这些酶的功能和调控有助于深入理
解胆固醇代谢,并为相关疾病的研究和药物开发提供基础。
脂质代谢途径概述

脂质代谢途径概述脂质代谢是指人体内脂质(主要指脂肪和胆固醇)的合成、降解和调节过程。
脂质代谢对于维持人体的能量平衡以及细胞膜结构的稳定非常重要。
本文将就脂质代谢的主要途径进行概述,包括脂肪合成、脂肪酸β氧化、胆固醇合成和胆固醇转运等。
一、脂肪合成途径脂肪合成主要发生在肝脏和脂肪组织中的细胞质内。
它的起始物质是乙酰辅酶A,这种物质由卟啉辅酶含有乙酰基团的物质和CoA酯化产生。
脂肪酸合成的过程中,乙酰辅酶A通过羧化和还原,最终合成出饱和长链脂肪酸。
然后,脂肪酸通过酰基化合成甘油三酯。
甘油三酯可以在需要消耗能量的时候释放出脂肪酸。
二、脂肪酸β氧化途径脂肪酸β氧化是脂肪酸的主要代谢途径。
当机体需要能量时,脂肪酸在线粒体中经过一系列的化学反应进行分解,产生较多的三酰甘油和乙酰辅酶A。
其中,乙酰辅酶A能进一步参与三羧甘油磷酸循环产生能量。
三、胆固醇合成途径人体内的胆固醇主要是通过内源合成来补充的。
胆固醇合成主要发生在肝脏和小肠上皮细胞中的内质网。
首先,乙酰辅酶A和乙二酰辅酶A通过酶的作用转化为HMG-CoA。
然后,HMG-CoA经过一系列酶的调节,最终合成胆固醇。
胆固醇可以用于合成细胞膜和各种激素。
四、胆固醇转运途径胆固醇在体内的转运主要通过两种方式进行:一是通过高密度脂蛋白(HDL)转运;二是通过低密度脂蛋白(LDL)转运。
HDL主要负责从细胞和组织中将多余的胆固醇收集起来,并将其转运至肝脏进行代谢和排泄。
而LDL则负责将胆固醇从肝脏转运至细胞和组织,供它们所需。
总结:脂质代谢是人体维持生命所必需的重要过程之一,它涉及脂肪酸的合成和降解、胆固醇的合成和转运等多个方面。
脂肪合成、脂肪酸β氧化、胆固醇合成和胆固醇转运是脂质代谢的主要途径。
通过这些途径,人体能够保持能量平衡,调节脂质水平,维持正常的生理功能。
深入了解脂质代谢途径的工作机制和调控方式有助于我们更好地认识脂质代谢的生理和病理过程,为相关疾病的治疗和预防提供理论指导。
有关胆固醇合成的叙述

有关胆固醇合成的叙述
胆固醇是一种脂类物质,它在人体中发挥着重要作用,包括维持细胞膜的稳定性、促进消化系统对脂肪的吸收和参与一些激素的产生等。
胆固醇的合成是一个复杂的生物过程,主要发生在肝脏和一些其他组织中。
胆固醇的合成主要依赖于一系列酶的协同作用。
首先,在细胞质中,乙酰辅酶A通过一系列反应转化为羟甲戊二酰辅酶A。
接下来,羟甲戊二酰辅酶A通过多个酶的催化作用,逐步合
成色氨酸、异戊酸和戊二酰辅酶A。
然后,戊二酰辅酶A被
转化为戊二酸,再经过一系列酶的作用,最终形成胆固醇。
胆固醇合成的调控主要通过一种称为HMG-CoA还原酶的酶
来实现。
HMG-CoA还原酶是合成胆固醇的关键酶,在胆固醇
合成过程中,通过调控该酶的活性来控制胆固醇的合成速率。
当细胞内胆固醇浓度较高时,胆固醇会抑制HMG-CoA还原
酶的活性,从而降低胆固醇的合成。
此外,胆固醇的合成还受到内源性和外源性调节因子的影响。
内源性因子包括细胞内胆固醇浓度、脂质代谢产物和一些激素等。
外源性因子则包括膳食中的胆固醇和脂肪含量等。
当胆固醇摄入过多时,胆固醇合成会被调节为低水平。
反之,当胆固醇摄入不足时,胆固醇合成会被调节为高水平。
总的来说,胆固醇的合成是一个复杂的生物过程,受到多个内外源性因子的调节。
了解胆固醇合成的调控机制,有助于我们更好地理解胆固醇在人体中的生理功能和疾病发生的机制。
胆固醇

定义及原理胆固醇生物合成的原料是乙酰辅酶A,合成途径可分为5个阶段:(1)乙酰乙酰辅酶A与乙酰辅酶A生成二羟甲基戊酸(6C中间代谢产物);(2)从二羟甲基戊酸脱羧形成异戊二烯单位(5C中间代谢产物);(3)6个异戊二烯单位缩合生成鲨烯(30C-中间代谢物);(4)鲨烯通过成环反应转变成羊毛脂固醇(30C中间代谢物);(5)羊毛脂固醇转变成胆固醇(27C化合物)。
胆固醇除作为细胞膜及血浆脂蛋白的重要组分外,还是许多重要类固醇如胆汁酸、肾上腺皮质激素、雌性激素、雄性激素、维生素D3等的前体。
生物体内许多生理活性物质如维生素A、E及K,胡萝卜素,橡胶,叶绿素的植醇侧链,多种芳香油的主要成分及萜类中的碳氢化合物;昆虫的保幼激素,蜕皮素等与胆固醇的生成相似;也是以乙酰辅酶A为原料,衍化生成异戊烯醇磷酸酯。
作为合成上述生物分子的结构单位前体。
胆固醇的分解代谢也在肝脏内进行。
胆固醇大部分可转变为胆汁酸。
小部分经肠道内细菌作用转变为粪固醇随粪便排出体外。
胆固醇代谢失调能给机体带来不良影响。
血浆胆固醇含量增高是引起动脉粥样硬化的主要因素,动脉粥样硬化斑块中含有大量胆固醇,是胆固醇在血管壁中堆积的结果,由此可引起一系列心血管疾病。
肝胆固醇的来源及释放途径胆固醇是体内最丰富的固醇类化合物,它既作为细胞生物膜的构成成分,又是类固醇类激素、胆汁酸及维生素D的前体物质。
因此对于大多数组织来说,保证胆固醇的供给,维持其代谢平衡是十分重要的。
胆固醇广泛存在于全身各组织中,其中约1/4分布在脑及神经组织中,占脑组织总重量的2%左右。
肝、肾及肠等内脏以及皮肤、脂肪组织亦含较多的胆固醇,每100g组织中约含200至500mg,以肝为最多,而肌肉较少,肾上腺、卵巢等组织胆固醇含量可高达1%-5%,但总量很少。
人体固醇的来源靠体内合成及从食物摄取,正常人每天膳食中约含胆固醇300-500mg,主要来自动物内脏、蛋黄、奶油及肉类。
植物性食品不含胆固醇,而含植物固醇如β谷固醇、麦角固醇等,它们不易为人体吸收,摄入过多还可抑制胆固醇的吸收。
胆固醇类化合物的合成与应用

胆固醇类化合物的合成与应用胆固醇,作为一种重要的生物分子,存在于人体和许多动植物中,具有多种生理功能。
然而,高胆固醇摄入与某些心血管疾病的发生息息相关。
因此,了解和研究胆固醇类化合物的合成与应用显得尤为重要。
一、胆固醇的合成途径胆固醇是人体内胆固醇代谢的关键物质,其合成途径复杂而精细。
胆固醇的合成主要发生在肝脏和肠道。
它主要通过脂肪酸合成途径,从较简单的物质合成出来。
胆固醇的合成途径涉及到多个酶的催化作用,其中包括甲羟乙酰辅酶A羧化酶、甲羟戊酰辅酶A羧化酶和前胆固醇酮还原酶等。
深入研究这些合成途径有助于进一步理解胆固醇的生理功能。
二、胆固醇的应用领域1. 药物领域。
胆固醇作为重要的原料,可用于合成多种降脂药物。
例如,他汀类药物常常以胆固醇为起点,通过一系列合成反应合成而成。
这类药物通过抑制体内胆固醇的合成,从而降低血浆中的胆固醇水平,起到降低血脂和保护心血管健康的作用。
2. 化妆品领域。
胆固醇是一种理想的皮肤保护剂。
它具有良好的保湿性能和渗透力,并能够提高表皮层的水分含量。
因此,在化妆品领域,胆固醇被广泛应用于各种面霜、乳液等保湿护肤产品中,有助于改善肌肤的湿润度和光滑度。
3. 生物燃料领域。
随着全球能源危机的日益严峻,生物燃料的研究备受关注。
胆固醇在这方面的应用不容忽视。
研究发现,某些微生物能够通过发酵过程将胆固醇转化为生物燃料,如乙醇。
这为寻找一种可持续发展的能源方向提供了新的思路。
4. 生物医学领域。
胆固醇在生物医学领域有广泛的应用前景。
由于胆固醇在细胞膜中的重要作用,研究人员通过改变胆固醇结构,探索其在细胞内的作用机制,并开发针对细胞膜的靶向药物。
此外,胆固醇还可用于制备荧光探针,用于细胞成像和疾病诊断。
三、胆固醇类化合物的合成方法胆固醇类化合物的合成方法有多种途径,如化学合成、发酵合成和生物合成等。
其中,化学合成是最常用的方法之一。
化学合成方法需要合成多个中间体,以最终得到目标产物。
这种方法虽然效率较高,但成本较高且操作繁琐。
简述胆固醇合成的基本过程

简述胆固醇合成的基本过程
胆固醇是一种重要的脂类物质,它在人体中起着许多生理功能。
胆固醇的合成主要发生在肝脏和小肠黏膜上。
下面是胆固醇合成的基本过程:
1. 起始物质:胆固醇合成的起始物质是乙酰辅酶A,它是一种来自脂肪酸代谢的中间产物。
2. 乙酰辅酶A转化:乙酰辅酶A首先被转化为羟甲基戊二酸(HMG-CoA)。
3. HMG-CoA还原酶:HMG-CoA进一步被HMG-CoA还原酶酶催化,转化为辅酶A和甲基戊二酸。
4. 甲基戊二酸激酶:甲基戊二酸被甲基戊二酸激酶催化,转化为甲羰基戊二酸。
5. 甲羰基戊二酸减亚甲基酶:甲羰基戊二酸被甲羰基戊二酸减亚甲基酶催化,转化为异戊二烯醇酸。
6. 异戊二烯醇酸脱氢酶:异戊二烯醇酸被异戊二烯醇酸脱氢酶催化,转化为戊二酮酸。
7. 戊二酮酸重排酶:戊二酮酸被戊二酮酸重排酶催化,转化为脱氢胆酮酸。
8. 脱氢胆酮酸还原酶:脱氢胆酮酸被脱氢胆酮酸还原酶催化,转化为胆酮酸。
9. 胆酮酸环化酶:胆酮酸被胆酮酸环化酶催化,转化为胆甾二烯酸。
10. 胆甾二烯酸还原酶:胆甾二烯酸被胆甾二烯酸还原酶催化,转化为胆固醇。
这是胆固醇合成的基本过程。
在此过程中,一系列的酶反应逐步将乙酰辅酶A转化为胆固醇。
胆固醇在人体中具有重要的生理功能,例如作为细胞膜的组成成分、合成激素和维生素D等。
简述胆固醇合成的基本过程 -回复

简述胆固醇合成的基本过程-回复胆固醇是一种脂质类化合物,它在人体中起着至关重要的角色。
它在维持细胞膜的稳定性、合成激素、维生素D和胆汁酸等方面发挥着重要的作用。
然而,当胆固醇水平过高时,它可能会导致动脉粥样硬化等一系列心血管疾病。
因此,了解胆固醇合成的基本过程对我们保持合适的胆固醇水平至关重要。
胆固醇的合成起源于简单的化合物,最终由多个酶催化的反应逐步进行,形成胆固醇分子。
简单来说,胆固醇的合成可以分为四个主要步骤:1. 乙酰辅酶A(Acetyl-CoA)的转化;2. 合成甲酸(Acetic acid);3. 甲酸转化为胆固醇前体,4. 胆固醇的最后合成。
第一步:乙酰辅酶A(Acetyl-CoA)的转化乙酰辅酶A是胆固醇合成的起点,在胆固醇合成之前,它必须转化为一些中间产物。
这个过程需要多个酶的参与。
首先,乙酰辅酶A与氧化物还原酶反应,生成醋醛缩酮(Acetoacetyl-CoA)。
接下来,醋醛缩酮与乙酰辅酶A反应,生成3-羟基-3-甲酰辅酶A(3-hydroxy-3-methylglutaryl-CoA, HMG-CoA)。
第二步:合成甲酸(Acetic acid)在第一步生成的3-羟基-3-甲酰辅酶A经过脱羧反应后,生成甲酸。
这个反应由HMG-CoA脱羧酶催化,并通过NAD和NADH的变化来推动反应。
第三步:甲酸转化为胆固醇前体在第二步生成的甲酸会被转化为异戊二酸(mevalonic acid),这个过程由甲酸合成酶(ACS)催化,并形成碳骨架。
接下来,异戊二酸进一步被磷酸化,生成肌酸酸(mevalonate pyrophosphate)。
这个步骤需要ATP 的能量。
第四步:胆固醇的最后合成在第三步生成的肌酸酸通过一系列反应转化为胆固醇。
这些反应中涉及到多个酶的催化。
其中,一系列脱氢酶和异构酶的存在,将异戊二酸的碳骨架逐步转化为胆固醇的结构。
最后,通过甾族不饱和键的生成以及其他结构上的变化,胆固醇合成完成。
生物合成胆固醇的限速步骤

生物合成胆固醇的限速步骤
1 胆固醇的基本概念
胆固醇是一种有机分子,可以由酰基化合物(例如甘油三酯和脂
肪酸)组成,主要存在于动物细胞的细胞膜中。
它的重要功能包括建
筑物细胞膜,保护细胞免受自由基的攻击,包装和运输脂质,以及作
为激素,调节血液中脂肪水平。
2 生物合成胆固醇的限速步骤
生物合成胆固醇的过程可分为三个基本步骤:(1) 甲基传递,(2) 内源性胆固醇合成,以及(3) 胆固醇吸收,分解和重新运输。
第一步,甲基传递,是皮质醇活性相关因子(CAR)催化的一种转
移甲基的步骤,其中将甲基从嵌键甲基转移到另一项化合物上,形成
一种称为甲基组装的产物。
第二步,内源性胆固醇合成,由CAR启动三环体系统酶来启动,
此系统酶将三份单体甲烷基脂肪酸组装到一个环中,以形成3碳底物。
随后,三连聚体系统酶将三环底物变为七环胆固醇(也称为胆固醇)。
第三步,胆固醇的吸收,利用LDL受体作为胆固醇的来源,将胆
固醇从体外脂质胶囊中吸收进入体内,再经过胆固醇酶的催化作用,
将胆固醇分解成脂肪酸和尿酸,回到体外,回到LDL脂质胶囊,或分
别与小分子脂肪酸发生反应,制成脂质酰基化反应,继续传递内源性
胆固醇。
3 结论
胆固醇的生物合成,涉及三个基本步骤:甲基传递,内源性胆固
醇合成和胆固醇的吸收,分解和重新运输。
只有通过正确的限速步骤,才能确保胆固醇的正常释放,以及维持血浆中的胆固醇水平。
胆固醇生物合成总览乙酰
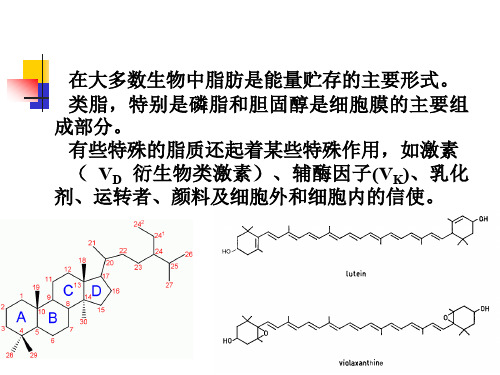
类脂,特别是磷脂和胆固醇是细胞膜的主要组 成部分。
有些特殊的脂质还起着某些特殊作用,如激素 ( VD 衍生物类激素)、辅酶因子(VK)、乳化 剂、运转者、颜料及细胞外和细胞内的信使。
29.1 贮存脂肪
29.1.1 贮存脂肪
脂类是所有营养物质中单位质量具有最多能量的化合物 (38 kJ / g 或9.0 kcal / g )。 来自膳食的脂肪必先转化为贮存脂肪。脂肪仓库中贮存的
内源胆固醇酯/B100
内 源 胆 固 醇 酯 / A1、 A2
转运内源性胆固醇经 细胞膜受体介导传递 至肝细胞内水解,并 转化成低密度脂蛋白。
转运内源性胆固醇酯, 由细胞膜受体介导至 肝和其他组织细胞内 水解。
转运磷脂和胆固醇酯 至肝组织内水解,有 清除血中胆固醇的作 用。
胆固醇及其转化产物
(3)胆固醇沉积引起的疾病:动脉粥样硬化,许多心血 管疾病。 4 种不同的生化突变导致家族高胆固醇血症:内
氧化中---NAD
f.脱去或延伸的单位:
g.羟酯基中间体 合成中 D型
氧化中 L型
9.2.1.6 脂肪酸链的加长和去饱和(自读)
在动物体中脂肪酸合成停止在16碳脂肪酸及软脂 酸而终止,更长的脂酸链或不饱和脂肪酸等都是把 软脂酸作为前体来合成的。 A碳链的延长
a.线粒体中 b.内质网中 B碳链的去饱和
脂蛋白是磷脂和蛋白质环绕着胆固醇 和三脂酰甘油的核构成。
29.2 脂类的合成
29.2.1脂肪酸的生物合成
29.2.1.1 乙酰—CoA的作用
脂肪酸合成与降解过程不同,掺入二碳单位是不是以乙
酰CoA的形式而是丙二酸单酰CoA的形式。
O C
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
P35610 3 drugs no structure
enzymes for the pathway
1. Acetyl-CoA acetyltransferase, cytosolic
Reactions: Drugs:
DB01915 S-Hydroxycysteine unknown
1WL4-protein crystal drug-protein interaction with S-Hydroxycysteine
DB00641
DB00439
Simvastatin
Cerivastatin And other 14 drugs
inhibitor
Inhibitor
1HW9-enzyme crystal drug-protein interaction with Simvastatin
—3—
enzymes for the pathway
Aminoglutethimide
DB00357
inhibitor
and other 10 drugs
3N9Y-enzyme crystal without drug
—2—
enzymes for the pathway
2. 3 beta-hydroxysteroid dehydrogenase/Delta 5-->4-isomerase type 1
Omega-3-acid DB09539 inhibitor ethyl esters
5TXF-structural analogues of Sterol O-acyltransferase 1
— 13 —
steroid hormone synthesis
steroid hormone synthesis
Reactions:
Drugs:
DB00282 Pamidronate inhibitor
2F89-enzyme crystal drug-protein interaction with Pamidronate
—5—
enzymes for the pathway
6. Diphosphomevalonate decarboxylase
98 drugs
6 protein crystal structures solved
steroid hormone synthesis
7 enzymes incredibly control the complex metabolism. 98 drugs
P05108 13 drugs
P15538
3LD6-enzyme crystal drug-protein interaction with Ketoconazole
— 12 —
enzymes for the pathway
14. Sterol O-acyltransferase 1
Reactions:
Drugs:
DB01094 DB00973 Hesperetin Ezetimibe inhibitor inhibitor
Systematically organize data found
metabolism network known in homo sapiens
Cholesterol synthesis
bile acid syn steroid hormone syn
brief metabolism pathways of cholesterol and some feature molecules
Steroid Hormone Synthesis
85 drugs with 6 protein structures with drugs solved
contents
Bile Acid Synthesis
5 drugs with 3 protein structures with drugs solved
— 11 —
enzymes for the pathway
12. Lanosterol 14-alpha demethylase
Reactions: Drugs:
DB01007 DB01167 Tioconazole inhibitor
Itraconazole Inhibitor
DB05667 Levoketoconazole and other 8 drugs
10. Squalene monooxygenase
Reactions: Drugs:
DB00735 Naftifine inhibitor
DB00857 Terbinafine
DB01091 Butenafine DB04927 NM100060
inhibitor
inhibitor
6FHO-structural analogues of Squalene monooxygenase
4. Cytochrome P450 11B1, mitochondrial
Reactions: Drugs:
DB00196 Fluconazole inhibitor DB00252 Phenytoin inhibitor
DB00257 Clotrimazole inhibitor and other 10 drugs
4. Mevalonate kinase
Reactions: Drugs:
FARNESYL DB04695 unknown THIOPYROPHOSPHATE
2R3V-enzyme crystal without drug
—4—
enzymes for the pathway
5. Phosphomevalonate kinase
Drugs Inventory
122 drugs with 24 protein structures with drugs solved
cholesterol synthesis
cholesterol synthesis
32 drugs 15 protein crystal structures solved
— 10 —
DB08846 Ellagic Acid
inhibitor
enzymes for the pathway
11. Lanosterol synthase
Reactions:
Drugs:
DB02016
DB03696
R048-8071
Lanosterol
unknown
unknown
1W6J-enzyme crystal drug-protein interaction With R048-8071
P10460 4 drugs no structure P05093 P05093 5 drugs
P08686 1 drug
P15538 13 drugs
P08686
P15538
P05093
P05093
P28845
18 drugs
P10460
P11511 45 drugs 3 structures
—1—
cholesterol synthesis
Q9BWD1 1 drug 1 structure Q01581 P04035 18 drugs 7 structures Q03426 1 drug Q15126 1 drug 1 structure P53602 1 drug 1 structure
P37268 1 drug Q14534 5 drugs no structure P48449 2 drugs 2 structures
Drugs:
DB00710 DB00884
Ibandronate Risedronate
inhibitor inhibitor
Dimethylallyl DB01785 Diphosphate unknown Isopentyl DB02508 Pyrophosphate unknown
2F94-enzyme crystal drug-protein interaction with Ibandronate
Reactions: Drugs:
DB00399 Zoledronic acid inhibitor
3N45-enzyme crystal drug-protein interaction Without Zoledronic acid
—6—
enzymes for the pathway
7. Isopentenyl-diphosphate Delta-isomerase 1
Reactions:
Drugs:
DB00630 Alendronic acid inhibitor
2DHO-enzyme crystal Without drug
—7—
enzymes for the pathway
8. Farnesyl pyrophosphate synthase
Reactions:
P14324
P14324 9 drugs 5 structuresຫໍສະໝຸດ Q13907 1 drug
Q16850 8 drugs 1 structure
P76062
The only two out of fourteen enzymes marked with blue are not drug targets.
—8—
and other 9 drugs
enzymes for the pathway
9. Squalene synthase
Reactions:
Drugs:
