化工原理实验报告精馏实验
化工原理实验—精馏

化工原理实验—精馏1. 概述精馏是一种常用的分离技术,广泛应用于化工工艺中。
它通过将混合液加热至蒸发,然后在冷凝器中冷却并凝结回液体,从而实现混合物中组分的分离。
本实验旨在通过精馏实验,掌握精馏原理、操作步骤和相关设备的使用方法。
2. 实验原理2.1 精馏原理精馏是基于液体混合物中各组分的不同沸点而进行的分离过程。
在加热的作用下,沸点较低的组分会先蒸发,经过冷凝器冷却后变为液体回流,而沸点较高的组分则会滞留在容器中。
通过收集冷凝后的液体,我们可以分离出混合物中的不同组分。
2.2 实验设备在精馏实验中,主要使用以下设备:•加热设备:电热板、油浴等;•冷凝器:通常采用水冷型冷凝器,通过循环冷却水实现液体冷凝;•分馏柱:用于增加接触面积,提高分离效果;•采样装置:用于采集样品,检测组分浓度等。
2.3 操作步骤精馏实验的基本步骤如下:1.准备实验设备:包括加热设备、冷凝器、分馏柱等;2.准备混合液:按照实验要求,将需要分离的混合液制备好;3.装配设备:将冷凝器安装在分馏柱上方,连接好相应的管道和热源;4.开始加热:逐渐加热混合液,将其中的沸点较低组分蒸发出来;5.冷却和回流:通过冷凝器使蒸发的组分冷却并凝结成液体,回流到容器中;6.收集液体:将回流液体收集,并记录途中温度和时间等相关数据;7.结束实验:实验完成后,及时关闭加热设备和冷凝器,整理实验装置。
3. 实验操作及数据记录3.1 实验设备准备首先,确保实验室环境安全,检查仪器设备是否齐全,并找到精馏实验所需的各种设备:•电热板:用来提供加热源;•分馏柱:用来增加接触面积,提高分离效果;•冷凝器:通常为水冷型冷凝器,确保冷却效果良好。
3.2 实验样品准备按照实验要求,取出需要分离的混合液样品。
注意记录样品的成分和浓度等信息。
3.3 装配设备将冷凝器安装在分馏柱上方,并连接好相应的管道和热源。
确保连接紧密,无泄漏。
3.4 开始实验1.打开电热板,设置适当的加热温度;2.将混合液置于分馏烧瓶中,放入加热设备中;3.监测温度变化:通过温度计等工具,记录样品温度的变化。
精馏实验实验报告3篇

精馏实验实验报告3篇精馏实验实验报告1学院:化学工程学院姓名:学号:专业:化学工程与工艺班级:同组人员:课程名称:化工原理实验实验名称:精馏实验实验日期北京化工大学实验五精馏实验摘要:本实验通过测定稳定工作状态下塔顶、塔釜及任意两块塔板的液相折光度,得到该处液相浓度,根据数据绘出x-y图并用图解法求出理论塔板数,从而得到全回流时的全塔效率及单板效率。
通过实验,了解精馏塔工作原理。
关键词:精馏,图解法,理论板数,全塔效率,单板效率。
一、目的及任务①熟悉精馏的工艺流程,掌握精馏实验的操作方法。
②了解板式塔的结构,观察塔板上汽-液接触状况。
③测定全回流时的全塔效率及单塔效率。
④测定部分回流时的全塔效率。
⑤测定全塔的浓度(或温度)分布。
⑥测定塔釜再沸器的沸腾给热系数。
二、基本原理在板式精馏塔中,由塔釜产生的蒸汽沿塔逐板上升与来自塔顶逐板下降的回流液,在塔板上实现多次接触,进行传热与传质,使混合液达到一定程度的分离。
回流是精馏操作得以实现的基础。
塔顶的回流量与采出量之比,称为回流比。
回流比是精馏操作的重要参数之一,其大小影响着精馏操作的分离效果和能耗。
回流比存在两种极限情况:最小回流比和全回流。
若塔在最小回流比下操作,要完成分离任务,则需要无穷多塔板的精馏塔。
当然,这不符合工业实际,所以最小回流比只是一个操作限度。
若操作处于全回流时,既无任何产品采出,也无原料加入,塔顶的冷凝液全部返回塔中,这在生产中午实际意义。
但是由于此时所需理论板数最少,又易于达到稳定,故常在工业装置的开停车、排除故障及科学研究时采用。
实际回流比常取最小回流比的1.2~2.0倍。
在精馏操作中,若回流系统出现故障,操作情况会急剧恶化,分离效果也将变坏。
板效率是体现塔板性能及操作状况的主要参数,有以下两种定义方法。
(1)总板效率EE=N/Ne式中E——总板效率;N——理论板数(不包括塔釜);Ne——实际板数。
(2)单板效率EmlEml=(xn-1-xn)/(xn-1-xn__)式中 Eml——以液相浓度表示的单板效率;xn ,xn-1——第n块板和第n-1块板的液相浓度;xn__——与第n块板气相浓度相平衡的液相浓度。
化工原理含实验报告(3篇)

第1篇一、实验目的1. 理解并掌握化工原理中的基本概念和原理。
2. 通过实验验证理论知识,提高实验技能。
3. 熟悉化工原理实验装置的操作方法,培养动手能力。
4. 学会运用实验数据进行分析,提高数据处理能力。
二、实验内容本次实验共分为三个部分:流体流动阻力实验、精馏实验和流化床干燥实验。
1. 流体流动阻力实验实验目的:测定流体在圆直等径管内流动时的摩擦系数与雷诺数Re的关系,将测得的~Re曲线与由经验公式描出的曲线比较;测定流体在不同流量流经全开闸阀时的局部阻力系数。
实验原理:流体在管道内流动时,由于摩擦作用,会产生阻力损失。
阻力损失的大小与流体的雷诺数Re、管道的粗糙度、管道直径等因素有关。
实验中通过测量不同流量下的压差,计算出摩擦系数和局部阻力系数。
实验步骤:1. 将水从高位水槽引入光滑管,调节流量,记录压差。
2. 将水从高位水槽引入粗糙管,调节流量,记录压差。
3. 改变流量,重复步骤1和2,得到一系列数据。
4. 根据数据计算摩擦系数和局部阻力系数。
实验结果与分析:通过实验数据绘制~Re曲线和局部阻力系数曲线,与理论公式进行比较,验证了流体流动阻力实验原理的正确性。
2. 精馏实验实验目的:1. 熟悉精馏的工艺流程,掌握精馏实验的操作方法。
2. 了解板式塔的结构,观察塔板上汽-液接触状况。
3. 测定全回流时的全塔效率及单板效率。
4. 测定部分回流时的全塔效率。
5. 测定全塔的浓度分布。
6. 测定塔釜再沸器的沸腾给热系数。
实验原理:精馏是利用混合物中各组分沸点不同,通过加热使混合物汽化,然后冷凝分离各组分的方法。
精馏塔是精馏操作的核心设备,其结构对精馏效率有很大影响。
实验步骤:1. 将混合物加入精馏塔,开启加热器,调节回流比。
2. 记录塔顶、塔釜及各层塔板的液相和气相温度、压力、流量等数据。
3. 根据数据计算理论塔板数、全塔效率、单板效率等指标。
4. 绘制浓度分布曲线。
实验结果与分析:通过实验数据,计算出了理论塔板数、全塔效率、单板效率等指标,并与理论值进行了比较。
化工原理实验--精馏实验
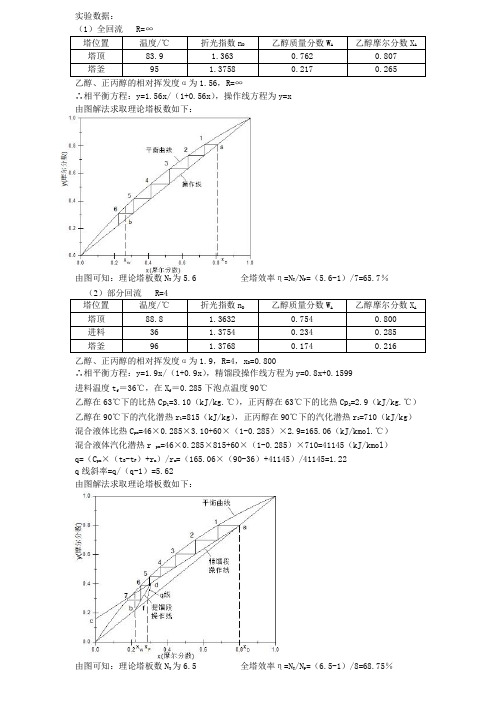
实验数据:
(1)全回流 R=∞
乙醇、正丙醇的相对挥发度α为1.56,R=∞
∴相平衡方程:y=1.56x/(1+0.56x),操作线方程为y=x
由图解法求取理论塔板数如下:
由图可知:理论塔板数N T为5.6 全塔效率η=N T/N P=(5.6-1)/7=65.7%
乙醇、正丙醇的相对挥发度α为1.9,R=4,x D=0.800
∴相平衡方程:y=1.9x/(1+0.9x),精馏段操作线方程为y=0.8x+0.1599
进料温度t f=36℃,在X f=0.285下泡点温度90℃
乙醇在63℃下的比热Cp1=3.10(kJ/kg.℃),正丙醇在63℃下的比热Cp2=2.9(kJ/kg.℃)乙醇在90℃下的汽化潜热r1=815(kJ/kg),正丙醇在90℃下的汽化潜热r2=710(kJ/kg)混合液体比热C pm=46×0.285×3.10+60×(1-0.285)×2.9=165.06(kJ/kmol.℃)
混合液体汽化潜热r pm=46×0.285×815+60×(1-0.285)×710=41145(kJ/kmol)
q=(C pm×(t B-t F)+r m)/r m=(165.06×(90-36)+41145)/41145=1.22
q线斜率=q/(q-1)=5.62
由图解法求取理论塔板数如下:
由图可知:理论塔板数N T为6.5 全塔效率η=N T/N P=(6.5-1)/8=68.75%。
化工原理精馏实验报告

化工原理精馏实验报告精馏技术在化学工程中已经得到了广泛的应用,但是如何完善其理论基础却是一个相当棘手的问题。
本文介绍了精馏实验,简要概述了精馏实验的基本原理及其应用,同时尝试深入了解精馏实验的基本操作,研究精馏实验的结果,并探讨分析其理论原理。
精馏是一种分离工艺,它的用途有两个方面。
首先,精馏是一种冷冻分离技术,可以通过利用液相与固相的分子量差异,将混合物分离出来。
其次,精馏也可以被用于提取物质,将物质从混合物中分离出来,以获得更高纯度的产品。
精馏实验的基本原理是利用溶剂的沸点级将混合液分为多个部分,然后采用吸附的方式将其中的不同组分分离出来。
精馏实验的操作步骤有:放置混合液;配置精馏塔;控制温度;给料;收集分离结果并绘制精馏曲线;分析结果。
首先,将混合液放入精馏塔中,然后控制精馏塔的温度,在进行温度控制的过程中,给料应该按预先设定的速率进行,以控制压力,这样便可以收集分离后的结果,绘制精馏曲线,根据精馏曲线的分析,可以分析出所得到的产品的有效性,并了解其分离效果。
另外,在精馏实验中,还可以采用许多其它的手段,以检验精馏实验的结果,如容量分析、比表面积测定、溶解度测定、m角测定等,从而对精馏实验的结果进行评价。
总之,精馏实验是为了让我们更好地理解和利用化学工程中的精馏技术,了解精馏实验的原理和操作,充分利用实验结果,并以此进行研究。
通过以上介绍,我们可以发现,精馏实验在化学工程中具有重要意义,可以用来分离混合液,提取物质,评价实验结果,从而为精馏技术的改进提供有力的理论支撑。
然而,在实际进行精馏实验时,需要用户掌握基本原理、进行合理操作,避免发生意外和错误,有效地利用精馏塔,从而使实验结果更好地反映出实验所需的理论结果。
综上所述,精馏技术已经在化学工程领域得到广泛应用,但是如何提高精馏技术的理论基础仍然是一个复杂的问题。
因此,精馏实验就显得十分重要,它不仅能够给我们提供更多的知识,而且可以实践中新的了解,以更加全面地把握精馏技术的理论原理,进而更好地服务于化学工程的发展。
化工原理精馏实验报告

化工原理精馏实验报告实验目的,通过精馏实验,掌握精馏原理和操作技能,了解精馏在化工生产中的应用。
一、实验原理。
精馏是利用液体混合物中各组分的沸点差异,通过加热、蒸馏和冷凝等过程,将混合物中的不同组分分离的方法。
在精馏过程中,液体混合物首先被加热至其中沸点最低的组分的沸点,然后将其蒸发成气体,再通过冷凝器冷却成液体,最终得到不同组分的纯净物质。
二、实验仪器与试剂。
1. 精馏设备,包括蒸馏烧瓶、冷凝器、接收烧瓶等。
2. 试剂,乙醇-水混合物。
三、实验步骤。
1. 将乙醇-水混合物倒入蒸馏烧瓶中。
2. 加热蒸馏烧瓶,待混合物沸腾后,蒸气通过冷凝器冷却成液体。
3. 收集不同温度下的液体,记录温度和收集时间。
四、实验结果与分析。
经过精馏实验,我们成功地将乙醇-水混合物分离成不同组分。
在实验过程中,我们观察到随着温度的升高,液体收集瓶中的液体组分逐渐发生变化,初馏液中含有较高乙醇含量,尾馏液中含有较高水含量。
这符合精馏原理,也验证了实验的准确性。
五、实验总结。
通过本次实验,我们深入了解了精馏原理和操作技能,掌握了精馏在化工生产中的应用。
精馏作为一种重要的分离方法,在化工领域有着广泛的应用,可以有效地提取纯净物质,满足不同生产需求。
六、实验注意事项。
1. 在实验过程中,要注意控制加热温度,避免混合物过热。
2. 实验结束后,要及时清洗和保养实验仪器,确保下次实验的顺利进行。
七、参考文献。
1. 《化工原理与实践》,XXX,XXX出版社,XXXX年。
2. 《化工实验指导》,XXX,XXX出版社,XXXX年。
以上就是本次化工原理精馏实验的实验报告,希望能对大家有所帮助。
化工原理精馏实验报告

化工原理精馏实验报告
实验目的:掌握化工原理中的精馏操作,并通过实验验证理论知识的正确性。
实验原理:
精馏是一种分离液体混合物组成的常用方法。
精馏通过不同组成的液体在加热的条件下产生蒸汽,然后再在冷凝管中冷凝成液体,最后通过收集液体可以得到不同组成的馏分。
实验仪器:
1. 精馏塔:用于分离混合物。
2. 加热器:提供加热源。
3. 冷凝器:用于冷凝产生的蒸汽。
4. 温度计:用于测量温度。
实验步骤:
1. 将需要进行精馏的混合物加入精馏塔中。
2. 打开加热器,通过加热产生蒸汽。
3. 在冷凝器中冷凝产生的蒸汽,并收集液体。
4. 使用温度计测量液体的沸点。
5. 根据液体的沸点,确定得到的馏分的组成。
实验结果:
在实验过程中,我们成功地通过精馏操作将待分离的混合物分解为不同组成的馏分。
通过温度计测量得到的沸点数据,我们可以精确地确定馏分的组成。
实验结论:
通过这次实验,我们掌握了化工原理中的精馏操作,并验证了理论知识的正确性。
精馏是一种常用的分离液体混合物的方法,在工业生产中有着广泛的应用。
掌握了精馏操作,有助于我们理解和解决化工过程中的实际问题。
化工原理实验 精馏实验

)
x
* ——与第 n n
块实际板汽相浓度相平衡的液相组
成,摩尔分率。
三、实验原理--板式塔(4)
全塔效率(也称总板效率)和单板效率是反映塔板 性能及操作好坏的重要指标,影响板效率的因素很多, 当板型、体系决定以后,塔板上的气、液流量是影响板 效率的主要因素。 若塔的上升蒸气量不够,将出现什么情况? 若上升气速太大,又会怎么样?
实验任务书 ——
筛板塔
5、在部分回流、稳定操作条件下,测定总板效率 随进料位臵的变化情况; 6、在部分回流、稳定操作条件下,测定总板效率 随进料组成的变化情况。 在完成1、2两项实验内容的基础上,最少再从3~6项 实验内容中选做一项。 要求同学在教师的协助下,独立设计出完整的实 验方案,并自主实施。实验报告以小论文的格式提交, 具体要求详见实验讲义。
四、实验流程—乙醇-水精馏塔(填料塔)
乙 醇 - 水 精 馏 实 验 流 程 图
四、实验流程—乙醇-水精馏塔(填料塔)
填料塔的结构和特点 填料塔由填料、塔内件及筒体构成。填料分规整填 料和散堆填料两大类,塔内件则由不同形式的液体分
布装臵、填料固定装臵和填料压紧装臵、填料支承装
臵、液体收集装臵与进料装臵及气体分布装臵等,筒 体由整体式结构及法兰连接分段式结构。 填料是填料塔的核心部件,填料的作用是增加气液 接触面积和增大气液接触面的湍动,填料性能评价指
物料衡算:
Fx F Dx D WxW
例如:选择F为3 l/h,x D 和 x F已知,D
即可估算出D的大小。
3、回流比(乙醇-正丙醇精馏实验)
乙醇-正丙醇精馏实验设备中的回流分配装臵由回 流分配器与控制器组成。回流分配器由玻璃制成,两 个出口管分别用于回流和采出。引流棒为一根 4mm的
化工原理精馏实验报告

化工原理精馏实验报告实验目的:本实验旨在通过对乙醇和水的精馏实验,掌握精馏过程的基本原理和操作技术,了解精馏过程中的温度变化规律,并对实验结果进行分析和总结。
实验原理:精馏是利用液体混合物中各组分的沸点差异,通过加热混合物使其中某一组分先汽化,再凝结成液体,从而实现对混合物的分离的一种物理方法。
在精馏过程中,液体混合物首先被加热至其中某一组分的沸点,该组分首先汽化,然后通过冷凝器冷却凝结成液体,最终得到纯净的组分。
实验步骤:1. 将乙醇和水混合成一定比例的混合物,倒入精馏瓶中。
2. 装上加热设备和冷凝器,调节加热设备温度至混合物中乙醇的沸点。
3. 观察冷凝器出口的液体,收集不同温度下的液体样品。
4. 对收集的液体样品进行密度测定和酒精度测定。
实验结果:通过实验,我们得到了乙醇和水在不同温度下的液体样品。
经过密度测定和酒精度测定,我们得到了不同温度下乙醇和水的纯度和组成。
实验分析:根据实验结果,我们发现在不同温度下,乙醇和水的纯度和组成存在明显差异。
通过对实验数据的分析,我们可以得出精馏过程中乙醇和水的分离效果较好,且随着温度的升高,乙醇的纯度逐渐提高。
实验总结:本次实验通过对乙醇和水的精馏实验,使我们更加深入地了解了精馏过程的基本原理和操作技术。
同时,实验结果也验证了精馏过程中液体混合物的分离效果,并为我们今后在化工生产中的实际应用提供了重要参考。
结语:通过本次实验,我们不仅掌握了精馏过程的基本原理和操作技术,也对乙醇和水的混合物分离效果有了更深入的了解。
希望通过今后的实践操作和学习,能够更好地运用精馏技术解决实际生产中的问题,为化工生产贡献自己的一份力量。
精馏实验(化工原理实验)

精馏实验一、实验目的1、了解筛板式精馏塔及其附属设备的基本结构,掌握精馏操作的基本方法;2、掌握精馏过程全回流和部分回流的操作方法;3、掌握测定板式塔全塔效率。
二、实验原理1、全塔效率E T全塔效率又称总板效率,是指达到指定分离效果所需理论板数与实际板数的比值,即-1=T T P N E N (1)式中:T N -完成一定分离任务所需的理论塔板数,包括塔釜;P N -完成一定分离任务所需的实际塔板数。
全塔效率简单地反映了整个塔内塔板的平均效率,表明塔板结构、物性系数、操作状况等因素对塔板分离效果的影响。
对于双组分体系,塔内所需理论塔板数N T ,可通过实验测得塔顶组成x D 、塔釜组成x W 、进料组成x F 及进料热状况q 、回流比R等有关参数,利用相平衡关系和操作线用图解法或逐板计算法求得。
图1塔板气液流向示意图2、单板效率ME 单板效率又称莫弗里板效率,如图1所示,是指气相或液相经过一层实际塔板前后的组成变化值与经过一层理论塔板前后的组成变化值之比。
按气相组成变化表示的单板效率为1*1y =n n MV n n y E y y ++--(2)按液相组成变化表示的单板效率为1*1n n ML n n x x E x x ---=-(3)式中:y n 、1n y +-分别为离开第n 、n+1块塔板的气相组成,摩尔分数;1n x -、n x -分别为离开第n-1、n 块塔板的液相组成,摩尔分数;*ny -与x n 成平衡的气相组成,摩尔分数;*nx -与y n 成平衡的液相组成,摩尔分数。
3、图解法求理论塔板数N T图解法又称麦卡勃-蒂列(McCabe-Thiele)法,简称M-T 法,其原理与逐板计算法完全相同,只是将逐板计算过程在y-x 图上直观地表示出来。
对于恒摩尔流体系,精馏段的操作线方程为:111D n n x R y x R R +=+++(4)式中:1n y +-精馏段第n+1块塔板上升的蒸汽组成,摩尔分数;n x -精馏段第n 块塔板下流的液体组成,摩尔分数;D x -塔顶溜出液的液体组成,摩尔分数;R -回流比。
化工原理下实验精馏实验

密度 Kg/m3 971.4 969.2 967.0 964.6 962.2 959.7
四、实验操作
开机:启动四组加热丝,打开全凝器的冷却水进口阀,当 塔顶的温度快速上升时,及时关掉1、2组加热器,利用可 调加热丝将3,4组加热电流调节为12A(1#,2#板式塔) 或30A(3#,4#填料塔)
全回流:塔顶蒸汽温度达到70~80℃时,不进料也不出料 即F=0,D=0,逐渐开启回流阀,回流量的大小应注意控 制(1#、2#塔,L应小一些约为2~3l/h, 3#、4#塔回流量 可靠调节至7~8 L/h,在全回流下运行10分钟,期间当回 流流量有下降的趋势,则关小回流阀,全回流时间10分钟。
填料塔的等板高度:HETP
Z NT
等板高度(HETP)是指与一层理论塔板的传质作用相当的填料层
高度。它的大小取决于填料的类型、材质与尺寸,受系统物性、
操作条件及塔设备尺寸的影响。
Z-实际的填料层高度。
关键:如何求NT: 逐板计算法或梯级图解法
测出以下数据:
温度[℃]: tD、tf、tW 组成[mol/mol]:xD、xf、xW 流量: F、D、L
的全回流操作? (9)在本实验室的精馏实验过程,发生了液泛现象,试分析原因并提出解
决的方法。 (10)采用本实验室的流程分离乙醇和水的混合物,能否得到无水乙醇?为
什么?
精馏塔中塔板或填料是气液两相接触的场所由塔釜产生的上升蒸汽与从塔顶下降的下降液接触进行传热和传质下降液经过多次部分气化重组分含量逐渐增加上升蒸汽经多次部分冷凝轻组分含量逐渐增加从而使混合物达到一定程度的分离
精馏实验
二、实验原理简介
精馏塔中,塔板或填料是气液两相接触的场所,由塔釜产 生的上升蒸汽与从塔顶下降的下降液接触进行传热和传质, 下降液经过多次部分气化,重组分含量逐渐增加,上升蒸 汽经多次部分冷凝,轻组分含量逐渐增加,从而使混合物 达到一定程度的分离。
化工原理精馏实验报告

化工原理精馏实验报告化工原理精馏实验报告摘要:本实验旨在通过精馏技术对乙醇-水混合物进行分离,探究精馏原理及其在化工工艺中的应用。
通过实验数据的分析和结果的总结,得出了乙醇-水混合物的精馏分离效果良好,证明了精馏技术在化工工艺中的重要性。
一、引言精馏是一种常用的分离技术,在化工工艺中广泛应用。
其基本原理是利用液体混合物中各组分的不同挥发性,通过加热和冷却使其分别汽化和凝结,从而实现组分的分离。
本实验选择乙醇和水的混合物作为研究对象,旨在验证精馏技术在该体系中的有效性。
二、实验方法1. 实验装置:采用简易精馏装置,包括加热设备、冷却设备和收集设备。
2. 实验材料:乙醇和水的混合物。
3. 实验步骤:a. 将乙醇和水按一定比例混合,制备乙醇-水混合物。
b. 将混合物倒入精馏瓶中,加热至沸腾。
c. 通过冷却设备将蒸馏气体冷凝,收集液体产物。
三、实验结果与分析通过实验,我们观察到了乙醇-水混合物的精馏分离过程。
在加热过程中,混合物开始沸腾,蒸汽逐渐上升至冷却设备,然后凝结为液体。
我们将冷凝后的液体收集起来进行分析。
1. 分离效果分析:我们通过对收集液体的测量和分析,得到了乙醇和水的分离效果。
根据实验数据,我们可以计算出乙醇和水的质量分数,进而评估精馏分离的效果。
结果显示,在实验条件下,乙醇的质量分数达到了90%,水的质量分数为10%。
这表明精馏技术在乙醇-水混合物的分离中具有较好的效果。
2. 精馏原理分析:精馏技术的原理基于不同组分的挥发性差异。
在加热过程中,混合物中挥发性较高的组分首先转化为蒸汽,然后通过冷却设备凝结为液体。
而挥发性较低的组分则较少转化为蒸汽,大部分保留在混合物中。
通过这种方式,我们可以实现组分的分离。
四、实验结果的讨论与总结通过本实验,我们验证了精馏技术在乙醇-水混合物的分离中的有效性。
实验结果显示,乙醇和水的分离效果良好,乙醇的质量分数达到了90%。
这表明精馏技术在化工工艺中具有重要的应用价值。
重磅精馏实验报告[大全5篇]
![重磅精馏实验报告[大全5篇]](https://img.taocdn.com/s3/m/3a49f9e3185f312b3169a45177232f60ddcce7db.png)
重磅精馏实验报告[大全5篇]第一篇:重磅精馏实验报告本科实验报告课程名称:过程工程原理实验(乙)实验名称:筛板塔精馏操作及效率测定姓名:学院(系):学号:指导教师:同组同学:一、实验目的和要求1、了解板式塔的结构和流程,并掌握其操作方法;2、测定筛板塔在全回流和部分回流时的全塔效率及全回流时的单板效率;3、改变操作条件(回流比、加热功率等)观察塔内温度变化,从而了解回流的作用和操作条件对精馏分离效果的影响。
要求:已知原料液中乙醇的质量浓度为15~20%,要求产品中乙醇的质量浓度在 85%以上。
二、实验内容和原理板式精馏塔的塔板是气液两相接触的场所,塔釜产生的上升蒸汽不从塔顶下降的下降液逐级接触进行传热和传质,下降液经过多次部分气化,重组分含量逐渐增加,上升蒸汽经多次部分冷凝,轻组分含量逐渐增加,从而使混合物达到一定程度的分离。
(一)全回流操作时的全塔效率E T 和单板效率E mV(4)的测定1、全塔效率(总板效率)E T1100%TTPNEN-=⨯(1)式中:N T —为完成一定分离任务所需的理论板数,包括蒸馏釜; N P —为完成一定分离任务所需的实际板数,本装置第二篇:精馏实验报告本科实验报告课程名称:过程工程原理实验(乙)实验名称:筛板塔精馏操作及效率测定姓名:学院(系):学号:指导教师:同组同学:一、实验目的和要求1、了解板式塔的结构和流程,并掌握其操作方法;2、测定筛板塔在全回流和部分回流时的全塔效率及全回流时的单板效率;3、改变操作条件(回流比、加热功率等)观察塔内温度变化,从而了解回流的作用和操作条件对精馏分离效果的影响。
要求:已知原料液中乙醇的质量浓度为 15~20%,要求产品中乙醇的质量浓度在 85% 以上。
二、实验内容和原理板式精馏塔的塔板是气液两相接触的场所,塔釜产生的上升蒸汽与从塔顶下降的下降液逐级接触进行传热和传质,下降液经过多次部分气化,重组分含量逐渐增加,上升蒸汽经多次部分冷凝,轻组分含量逐渐增加,从而使混合物达到一定程度的分离。
化工原理精馏实验报告

化工原理精馏实验报告一、实验目的与原理本实验的目的是通过精馏操作,对乙醇与水的二元混合物进行分离,从而了解精馏操作的原理与应用。
精馏是一种常用的分离技术,基于不同组分的沸点不同,通过加热混合物使其沸腾,然后通过冷凝、蒸汽液分离等操作,实现不同组分的分离。
对二元混合物而言,其沸点的差异性更加明显,通过精馏操作可以将其分离得更加彻底。
二、实验步骤1.实验器材准备:精馏设备、酒精灯、温度计、进料管、冷凝管、接收瓶等。
2.操作准备:将乙醇与水按照一定比例混合,配制出所需的二元混合物。
3.实验操作:a.将精馏设备中的进料管连通到冷凝管,并将冷凝管的另一端放入接收瓶中。
b.将混合物倒入精馏设备的加热壶中,并点燃酒精灯进行加热。
c.随着加热进行,观察温度计的示数,记录下不同温度下的温度值。
d.当达到乙醇的沸点温度时,开始冷凝,此时可以观察到接收瓶中液体的变化。
e.等待一段时间,直至所需分离程度达到要求,即可结束实验。
三、实验结果与数据处理在实验过程中,我们记录下了不同温度下温度计的示数,得到如下数据表格:温度(℃),示数(°C):--------,:--------85,83.589,86.592,89.294,92.096,94.597,96.099,97.3根据实验结果可知,乙醇的沸点大约为78.3℃,水的沸点约为100℃,所以在加热过程中,首先蒸发的是乙醇,其后才是水。
通过观察接收瓶中液体的变化,可以看到一定程度上的分离。
四、实验讨论与总结通过本次实验,我们成功进行了乙醇与水的精馏实验,并取得了一定的分离效果。
实验结果与理论预期相符,验证了精馏操作的原理与应用。
然而,由于实验条件与设备的限制,所得结果与预期结果仍有一定差距。
为了达到更好的分离效果,可以尝试以下改进措施:1.提高加热壶的温度控制精度,保证加热过程的均匀性;2.加大冷凝管的冷却效果,加快蒸汽液分离的速度;3.调整精馏设备的结构,增强对二元混合物的分离效果。
化工原理精馏实验报告

化工原理精馏实验报告一、实验目的1.了解精馏的基本原理和操作方法。
2.掌握精馏列等常规化工装置的组装和拆卸方法。
3.学习操作精馏列进行混合物的分离。
二、实验原理精馏是利用液体混合物中组分挥发性的差异,通过升温使其分别汽化和冷凝,实现不同组分的分离。
根据原理和设备的不同,可分为常压精馏和减压精馏。
常压精馏通常采用碗状蒸馏器,其馏出液不一般含气体,供后续步骤使用。
减压精馏蒸馏器采用圆筒形设计,湿性气体排放恶劣等特点。
三、实验装置本次实验使用的精馏装置包括:碟状蒸馏器、冷凝器、接收瓶、加热器、温度传感器等。
四、实验步骤1.将碟状蒸馏器装置迅速、适当地安插在加热器上,并设置温度传感器。
2.将待测试物质加入碟状蒸馏器,并紧密封好。
3.连接冷凝器和接收瓶,确保冷凝器充分冷却。
4.使用加热器对碟状蒸馏器进行加热,并监测温度传感器。
5.在实验过程中,根据馏出液的收集情况及温度变化来调整加热器的加热功率。
6.测定不同温度下不同组分的收集量,并记录数据。
7.实验结束后,拆卸碟状蒸馏器,清洗实验装置,并做好相关记录。
五、实验结果与讨论在实验过程中,我们选择了乙醇和水的混合物进行精馏实验。
通过实验观察和数据记录,我们得到了以下结果:1.随着温度升高,乙醇的馏出量逐渐增加。
2.当温度达到78℃左右时,乙醇开始大量馏出,水的馏出量减少。
3.经过一段时间,馏出物逐渐转变为纯乙醇。
根据实验结果,我们可以得出结论:乙醇和水在常压下的沸点不同,通过精馏操作,可以将乙醇从水中分离出来,达到纯化乙醇的效果。
同时,在实验过程中,通过调节加热功率和控制温度变化,可以进一步提高乙醇的纯度。
六、实验总结本次实验通过对乙醇和水的精馏实验,掌握了精馏的基本原理和操作方法。
通过实验观察和数据记录,我们了解了温度与组分的关系,并得到了较为满意的分离效果。
同时,实验过程中我们也注意到了一些操作细节和注意事项,比如加热功率的调整和温度传感器的准确定位等。
化工原理实验报告--精馏实验

填料精馏塔实验一、实验目的1.观察填料精馏塔精馏过程中气、液两相流动状况;2.掌握测定填料等板高度的方法;3.研究回流比对精馏操作的影响。
二、实验原理精馏塔是实现液体混合物分离操作的气液传质设备,精馏塔可分为板式塔和填料塔。
板式塔为气液两相在塔内逐板逆流接触,而填料塔气液两相在塔内沿填料层高度连续微分逆流接触。
填料是填料塔的主要构件,填料可分为散装填料和规整填料,散装填料如:拉西环、鲍尔环、阶梯环、弧鞍形填料、矩鞍形填料、θ网环等;规整填料有板波纹填料、金属丝网波纹填料等。
由于填料塔内气液两相传质过程十分复杂,影响因素很多,包括填料特性、气液两相接触状况及两相的物性等。
在完成一定分离任务条件下确定填料塔内的填料层高度时,往往需要直接的实验数据或选用填料种类、操作条件及分离体系相近的经验公式进行填料层高度的计算。
确定填料层高度有两种方法:1.传质单元法填料层高度=传质单元高度×传质单元数(2—50)或:(2—51)由于填料塔按其传质机理是气液两相的组成沿填料层呈连续变化,而不是阶梯式变化,用传质单元法计算填料层高度最为合适,广泛应用于吸收、解吸、萃取等填料塔的设计计算。
2.等板高度法在精馏过程计算中,一般都用理论板数来表达分离的效果,因此习惯用等板高度法计算填料精馏塔的填料层高度。
(2—52)式中:Z——填料层高度,m;N T ——理论塔板数;HETP——等板高度,m。
等板高度HETP,表示分离效果相当于一块理论板的填料层高度,又称为当量高度,单位为m。
进行填料塔设计时,若选定填料的HETP无从查找,可通过实验直接测定。
对于二元组分的混合液,在全回流操作条件下,待精馏过程达到稳定后,从塔顶、塔釜分别取样测得样品的组成,用芬斯克(Fenske)方程或在x~y图上作全回流时的理论板数。
芬斯克方程:(2—53)式中:——全回流时的理论板数;——塔顶易挥发组分与难挥发组分的摩尔比;——塔底难挥发组分与易挥发组分的摩尔比;——全塔的平均相对挥发度,当α变化不大时,在部分回流的精馏操作中,可由芬斯克方程和吉利兰图,或在x~y图上作梯级求出理论板数。
化工原理实验—精馏

化工原理实验—精馏化工原理实验—精馏精馏是一种重要的分离技术,主要用于分离、纯化液体混合物中的各种成分。
在实际生产和科研实验中,精馏已经成为不可或缺的重要技术。
本文将就化工原理实验中的精馏实验进行详细介绍。
一、实验原理精馏的基本原理是根据不同成分在液态和气态之间的平衡关系,在加热条件下将混合物中单一成分蒸发和冷凝来实现分离、提纯目标成分。
实验中要分离的混合物首先被加热到沸腾点以上,因为各种成分的沸点不同,有些成分的沸点比另一些成分高得多,因此在离开混合物比较早的时候,一些液体成分便会压缩成气体形式,通过冷凝的方式回到液体形式,从而分离。
二、实验步骤1.实验前准备:确定实验目的,熟悉仪器使用方法和名词术语,检查实验物品是否准备充分。
2.实验流程:(1)调整设备:将水箱放在上部,并根据实验需要将装有混合物的烧瓶安装在下部。
(2)加热混合物:先在小火下加热,让混合物慢慢升温,确定加热速度以防止挥发速度过快。
随着温度的升高,由混合物挥发出来的单一成分便会通过塞子进入冷凝器,冷凝器中的水为其退回到液体形态,收集并量取所需要的物质。
3.实验结束:(1)关闭所有开关:实验完成后,将电源关闭,并将实验设备切断电源和气源。
(2)清洗设备与仪器:清洗所有已使用的材料和设备,以确保下次的实验能保证卫生和安全。
三、实验注意事项1.将水箱放置在塞子上方,仔细检查所有漏洞的位置和具有修复能力的地方,以避免机械故障与事故到来。
2.在进行实验时,必须小心谨慎地装填液体混合物,尤其是对于易燃物质,必须保持警惕,并根据实验条件和混合物来选择实验设备和材料。
3.在加热过程中,如果需要调整加热器的温度,必须慢慢调整,直到较稳定的加热水平达到。
总之,精馏实验是一项非常重要的化工原理实验,同学们在进行实验时一定要小心谨慎,严格遵守实验规范,才能保证实验的顺利进行。
化工原理实验报告精馏实验

化工原理实验报告精馏实验
化工原理实验报告:精馏实验
实验目的:
本次实验旨在通过精馏实验,掌握精馏过程的基本原理,了解精馏技术在化工
生产中的应用,并掌握精馏实验的操作技能。
实验原理:
精馏是一种利用液体混合物中不同成分的沸点差异进行分离的物理方法。
在精
馏过程中,液体混合物首先被加热至沸点,然后蒸气被冷凝成液体,最终得到
不同成分的纯净产物。
实验步骤:
1. 准备实验装置:将精馏瓶、冷凝管、加热设备等装置搭建好,并连接好管道。
2. 将待分离的液体混合物倒入精馏瓶中。
3. 加热液体混合物,使其达到沸点,产生蒸气。
4. 蒸气通过冷凝管冷却成液体,分别收集不同成分的产物。
实验结果:
经过精馏实验,我们成功地将液体混合物分离成了不同成分的产物。
通过实验,我们观察到不同成分的沸点差异导致了它们在精馏过程中的分离。
这表明精馏
技术在化工生产中具有重要的应用价值。
实验结论:
通过本次精馏实验,我们深入了解了精馏技术的原理和操作方法,掌握了精馏
实验的操作技能。
精馏技术在化工生产中具有广泛的应用,能够有效地分离液
体混合物中的不同成分,提高产品的纯度和质量,具有重要的经济意义和社会
价值。
总结:
精馏实验是化工原理课程中的重要实验之一,通过本次实验,我们对精馏技术有了更深入的了解,为今后的学习和工作打下了坚实的基础。
希望通过不断的实践和学习,我们能够更加熟练地掌握精馏技术,为将来的化工生产做出更大的贡献。
化工原理实验报告-精馏

精馏实验一、实验任务和目的:1、充分利用计算机采集和控制系统具有的快速、大容量和实时处理的特点,进行精馏过程多实验方案的设计,并进行实验验证,得出实验结论。
以掌握实验研究的方法。
2、学会识别精馏塔内出现的几种操作状态,并分析这些操作状态对塔性能的影响。
3、学习精馏塔性能参数的测量方法,并掌握其影响因素。
4、测定精馏过程的动态特性,提高学生对精馏过程的认识。
二、实验原理:在板式精馏塔中,由塔釜产生的蒸汽沿塔板逐板上升与来自塔板下降的回流液,在塔板上实现多次接触,进行传热与传质,使混合液达到一定程度的分离。
回流是精馏操作得以实现的基础。
塔顶的回流量与采出量之比,称为回流比。
回流比是精馏操作的重要参数之一,其大小影响着精馏操作的分离效果和能耗。
回流比存在两种极限情况:最小回流比和全回流。
若塔在最小回流比下操作,要完成分离任务,则需要有无穷多块塔板的精馏塔。
当然,这不符合工业实际,所以最小回流比只是一个操作限度。
若操作处于全回流时,既无任何产品采出,也无原料加入,塔顶的冷凝液全部返回塔内中,这在生产中无实际意义。
但是,由于此时所需理论塔板数最少,又易于达到稳定,故常在工业装置的开停车、排除故障及科学研究时使用。
3、实验流程(简图);4、操作步骤;4.1、设置参数设置精馏段塔板数为5,设置提馏段塔板数为3,配置浓度比为0.66的乙醇/正丙醇混合液,设置进料罐的一次性进料量为2L。
4.2、精馏塔进料(1)连续点击"进料"按钮,进料罐开始进料,直到罐内液位达到70%以上。
(2)启动进料泵。
(3)设定进料泵功率,将进料流量控制器的 OP 值设为50%。
(4)设定预热器功率,将进料温度控制器的 OP 值设为60%,开始加热。
(5)打开塔釜液位控制器,控制液位在70%-80%之间。
4.3、启动再沸器(1)将塔顶冷凝器内通入冷却水。
(2)设定塔釜加热功率,将塔釜温度控制器的 OP 值设为 50%。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
精馏实验
一、目的及任务
①熟悉精馏的工艺流程,掌握精馏实验的操作方法。
②了解板式塔的结构,观察塔板上汽-液接触状况。
③测定全回流时的全塔效率及单板效率。
二、基本原理
在板式精馏塔中,由塔釜产生的蒸汽沿塔板逐板上升与来自塔顶逐板下降的回流液,在塔板上实现多次接触,进行传热与传质,使混合液达到一定程度的分离。
回流是精馏操作得以实现的基础。
塔顶的回流液与采出量之比,称为回流比。
回流比是精馏操作的重要参数之一,其大小影响着精馏操作的分离效果和能耗。
回流比存在两种极限情况:最小回流比和全回流。
若塔在最小回流比下操作,要完成分离任务,则需要有无穷多块塔板的精馏塔。
当然,这不符合工业实际,所以最小回流比只是一个操作限度。
若操作处于全回流时,既无任何产品采出,也无任何原料加入,塔顶的冷凝液全部返回塔中,这在生产中无实验意义。
但是,由于此时所需理论板数最少,又易于达到稳定,故常在工业装置中的开停车、排除故障及科学研究时采用。
实际回流比常取最小回流比的1.2~2.0倍。
在精馏塔操作中,若回流系统出现故障,操况会急剧恶化,分离效果也将变坏。
板效率是体现塔板性能及操作状况的主要参数,有以下两种定义方法。
(1) 总板效率E E=N/N e (4-25) 式中 E ——总板效率; N ——包括塔釜); N e ——实际板数。
(2)单板效率E ml
式中 E ml ——以液相浓度表示的单板效率; X n X n-1——第n 块板和第(n-1)块板的液相浓度; Xn *
——与第n 块板气相浓度相平衡的液相浓度;
总板效率与单板效率的数值常由实验测定。
单板效率是评价塔板性能优劣的重要数据。
物系性质、板型及操作负荷是影响单板效率的重要因数。
当物系与板型确定后,可通过改变汽液符合达到最高的板效率;对于不同的板型,可以在保持相同的物系及操作条件下,测定其单板效率,以评价
*
11n n n
n ML x x x x E --=
--(4-26)
其性能优劣。
总板效率反映全塔各塔板的平均分离效果,常用于板式塔设计中。
三、装置和流程
本实验的流程如图4-11所示,主要有精馏塔、回流分配装置及测控系统组成。
1精馏塔
精馏塔为筛板塔,全塔共八块塔板,塔身的结构尺寸为:塔径∮(57×3.5)mm,塔板间距80mm;溢流管截面积78.5mm2,溢流堰高12mm,底隙高度6mm;每块塔板开有43个直径为1.5mm的小孔,正三角形排列,孔间距为6mm。
为了便于观察踏板上的汽-液接触情况,塔身设有一节玻璃视盅,在第1-6块塔板上均有液相取样口。
蒸馏釜尺寸为∮108mm×4mm×400mm.塔釜装有液位计、电加热器(1.5kw)、控温电热器(200w)、温度计接口、测压口和取样口,分别用于观测釜内液面高度,加热料液,控制电加热装置,测量塔釜温度,测量塔顶与塔釜的压差和塔釜液取样。
由于本实验所取试样为塔釜液相物料,故塔釜内可视为一块理论板。
塔顶冷凝器为一蛇管式换热器,换热面积为0.06m2,管外走冷却液。
图4-11 精馏装置和流程示意图
1-原料罐进料口;2-原料罐;3-进料泵回流阀;4-进料泵;5-电加热器;6-釜料放空阀;7-塔釜产品罐放空阀;8-釜产品储罐;9-塔釜;10-流量计;11-顶产品罐放空阀;12-顶产品;13-塔板;
14-塔身;15-降液管;16-塔顶取样口;17-观察段;18-线圈;19-冷凝器20-塔釜取样口。
2测控系统
在本实验中,利用人工智能仪表分别测定塔顶温度、塔釜温度、塔身伴热温度、塔釜
加热温度、全塔压降、加热电压、进料温度及回流比等参数,该系统的引入,不仅使实验
跟更为简便、快捷,又可实现计算机在线数据采集与控制。
3物料浓度分析
本实验所用的体系为乙醇-正丙醇,由于这两种物质的折射率存在差异,且其混合物的质量分数与折射率有良好的线性关系,故可通过阿贝折光仪分析料液的折射率,从而得到浓度。
这种测定方法的特点是方便快捷、操作简单,但精度稍低;若要实现高精度的测量,可利用气相色谱进行浓度分析。
混合料也的折射率与质量分数(以乙醇计)的关系如下。
40℃ m=58.5068—42.1941n D
式中 m——料液的质量分数;
n D——料液的折射率(以上数据为由实验测得)。
四、操作要点
①对照流程图,先熟悉精馏过程中的流程,并搞清仪表上的按钮与各仪表相对应的设备与测控点。
②全回流操作时,在原料贮罐中配置乙醇含量20%~25%(摩尔分数)左右的乙醇-正丙醇料液,启动进料泵,向塔中供料至塔釜液面达250~300mm。
③启动塔釜加热及塔身伴热,观察塔釜、塔身、塔顶温度及塔板上的气液接触状况(观察视镜),发现塔板上有料液时,打开塔顶冷凝器的水控制阀。
④测定全回流情况下的单板效率及全塔效率,在一定的回流量下,全回流一段时间,待该塔操作参数稳定后,即可在塔顶、塔釜及相邻两块塔板上取样,用阿贝折光仪进行分析,测取数据(重复2~3次),并记录各操作参数。
⑤实验完毕后,停止加料,关闭塔釜加热及塔身伴热,待一段时间后(视镜内无料液时),切断塔顶冷凝器及釜液冷却器的供水,切断电源,清理现场。
六、数据处理
(1)原始数据
操作系数:
加热电压 86.9V;伴热温控77.3℃;塔釜温度117.5℃;塔顶温度78.4℃;塔底温度87.1℃;全塔压降0.34kpa;
实验数据:
①塔顶n d1=1.3577;n d2=1.3574; 塔釜n d1=1.3730;n d2=1.3725;
②第四块板n d1=1.3592;n d2=1.3591; 第五块板n d1=1.3602;n d2=1.3600;
(2)数据处理
①附录、乙醇-正丙醇 t-x-y 关系
(均以乙醇摩尔分率表示,x-液相 y-气相)
乙醇-丙醇平衡数据(p=101.325kPa)
乙醇沸点:78.3℃;丙醇沸点:97.2℃.
②原始数据处理:
原始数据记录处理如下:
数据计算以塔顶为例:
③在直角坐标系中绘制x-y图,用图解法求出理论板数。
参见乙醇-丙醇平衡数据作出乙醇-正丙醇平衡线,全回流条件下操作线方程为y=x,具体作图如下如下所示:
④求出全塔效率和单板效率。
由图解法可知,理论塔板数为4.4块板(包含塔釜),故全塔效率为
错误!未找到引用源。
由相平衡关系可得错误!未找到引用源。
利用乙醇—正丙醇平衡数据可得如下表所示:
作1/y与1/x图如下:
有图可知斜率错误!未找到引用源。
;
全回流操作线方程为y n=x n-1,故
错误!未找到引用源。
;
第五块板的单板效率
;
实验结果分析:
经计算可得单板效率较低,其原因可能是:
①该实验精馏塔仅用于模拟操作过程,塔板面积有限;
②气液在塔板上的接触时间有限,使得气液两相在达到平衡前就相互分离;
且该塔塔板非理想化塔板,使得气液两相未能充分接触。
2、由该实验可得出,提高单板效率的有效方法如下:
①扩大塔板面积;
②延长气液接触的时间;
③改造成或选择效率较高的塔板。
七、思考题
①什么是全回流?全回流操作有哪些特点,在生产中有什么实际意义?如何测定全回流条件下的气液负荷?
答:全回流是精馏塔中气相组分完全用于回流到精馏塔中,而无进料和出料的操作状态。
在精馏塔的停开车和塔板效率的测定以及理论研究中使用。
②塔釜加热对精馏操作的参数有什么影响?塔釜加热量主要消耗在何处?与回流量有无关系?答:塔釜加热对使塔顶气相轻组分组成浓度更高,塔釜液相轻组分组成浓度更低,对精馏有利。
塔釜加热量主要消耗在精馏塔气液热量交换上,与回流量有关。
③如何判断塔的操作已达到稳定?
答:当塔内各塔板的浓度(或温度)不再变化时,则可证明塔已稳定。
④当回流比R<R min时,精馏塔是否还能进行操作?如何确定精馏塔的操作回流比?
答:精馏塔还可以操作,但不能达到分离要求。
可通过调节回流时间和采出时间来确定回流比。
⑤冷液进料对精馏塔操作有什么影响?进料口如何确定?
答:冷热进料有利于精馏塔操作,使塔顶气相轻组分组成浓度更高,塔釜液相轻组分组成浓度更低。
进料口应在塔内组成与进料组成最接近的地方。
⑥精馏塔的常压操作如何实现?如果要改为加压或减压操作,如何实现?
答:在精馏塔顶的冷凝器出接通大气,从而实现精馏塔的常压操作。
若要改为加压操作,可向塔内通入惰性气体;若要减压操作,可在塔的采出口处加一真空泵。
