单克隆抗体的重链和轻链在体积排阻色谱柱上的检测
糖蛋白药物的多糖结构解析进展

糖蛋白药物的多糖结构解析进展刘艳玲;刘晓志;赵伟;王志明【摘要】细胞表达的治疗性单克隆抗体多数是糖蛋白.附着在蛋白质上的多糖直接影响蛋白质药物的稳定性、生物活性及免疫原性.因此,应对糖蛋白产品上的多糖进行充分分析,以控制产品质量.然而,糖蛋白上多糖的复杂性对检测带了艰巨挑战.介绍了糖蛋白上多糖分析的最新进展,以及利用凝集素芯片技术的高通量多糖分析法,重点介绍了用于检测糖基化位点、糖链结构和含量的测定分析方法,以期为糖蛋白药物的研发提供参考.【期刊名称】《生物技术进展》【年(卷),期】2016(006)004【总页数】5页(P244-248)【关键词】治疗性糖蛋白药物;多糖分析;凝集素芯片技术【作者】刘艳玲;刘晓志;赵伟;王志明【作者单位】华北制药集团新药研究开发有限责任公司,抗体药物研制国家重点实验室,石家庄050015;华北制药集团新药研究开发有限责任公司,抗体药物研制国家重点实验室,石家庄050015;华北制药集团新药研究开发有限责任公司,抗体药物研制国家重点实验室,石家庄050015;华北制药集团新药研究开发有限责任公司,抗体药物研制国家重点实验室,石家庄050015【正文语种】中文细胞表达的生物技术药物多数是糖蛋白,包括单克隆抗体、重组蛋白、融合蛋白、生长因子、细胞因子、酶和激素。
这些药物被用于癌症、自身免疫性疾病及其他危及生命的疾病的治疗。
适度糖基化对药物的溶解性、稳定性、生物活性、安全性、药代动力学和药效动力学等特征具有重要影响。
药物糖基化不但可以增加药物体外稳定性,还可以保护蛋白药物免受体内蛋白酶的降解。
非糖基化促红细胞生成素(erythropoietin,EPO)较糖基化EPO,更易受到化学物质、pH变化或是加热引起的变性或降解。
蛋白质糖基化可以影响蛋白药物PK/PD特征,研究显示,末端半乳糖部分糖基化蛋白,较末端唾液酸完成糖基化蛋白具有更短的循环寿命。
由于肝细胞表达的唾液酸糖蛋白受体同半乳糖结合,促进了肝脏对部分糖基化蛋白的清除。
单克隆抗体及其高聚体的体积排阻色谱分析方法开发-Waters

抗体的SEC分析方法开发
5
[ 应用纪要 ]
0.030 0.025 0.020
0.4 mL/min 聚集体 = 3.14% USP分离度 = 2.0
0.015
0.010
0.005
0.000
1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 6.0 6.5 7.0 7.5 min
0.030 0.025 0.020
为了展示这些影响,我们在4.6 x 150 mm以及4.6 x 300 mm的色谱柱上运行了一组蛋白标准品。 校准曲线的对比结果显示,与150 mm色谱柱相比,300 mm色谱柱的校准曲线斜率更加平缓, 说明增加色谱柱长度可增强其分离能力(图6)。
150 mm
蛋白质
分子量
6.5
300 mm
甲状腺球蛋白 670000
除了蛋白质标准品外,我们还评估了溶于50-250 mM氯化钠中的小鼠单克隆抗体(mAb) 的SEC分离情况(图2)。正如通常会在凝胶过滤填料上观察到的一样2,较大的离子强度 可减少mAb单体的峰拖尾现象并使峰形更窄。当氯化钠浓度从50升至200 mM时,mAb的 峰高从0.189升至0.289。USP拖尾因子也从1.64降至1.22。而当流动相离子强度从200升 至250 mM氯化钠时,上述变化不再明显(USP拖尾因子 = 1.20)。
200 mM 聚集体 = 5.27% USP分离度 = 1.57 USP拖尾因子 = 1.22
0.0
0.3
250 mM
聚集体 = 5.39%
0.2
USP分离度 = 1.58
USP拖尾因子 = 1.20
0.1
0.0
0.5
1.0
1.5
免疫亲和柱净化柱前衍生化-高效液相色谱荧光检测法测定粮谷中的T-2毒素

( ! $ %&’()&)* +),-. / " +0&, 1)2345,&() ’)6 78’-’),&)4 98-4’8 ,:’;&’) !!#$$! ,<=&)’ ; % $ !=4).’)* >*-&58;,8-4 ?)&@4-2&,. ,!=4).’)* !!$!#! ,<=&)’ )
! ! 自然界中多种农作物的致病菌可以产 生 #"# 毒 素, 其中大部分来自镰孢菌属, 产毒能力随真菌种类 不同而异, 并受 到 环 境 因 素 的 影 响。 玉 米 和 黑 麦 中 的致病菌产毒能 力 较 强, 其 次 为 大 麦、 大 米 和 小 麦。 #"# 毒素的毒 性 主 要 作 用 于 增 殖 活 跃 的 细 胞, 如骨 髓、 肝、 黏膜上皮和 淋 巴 细 胞 等, 而对淋巴细胞的损 呕 害最为严重。 #"# 毒 素 的 中 毒 症 状 主 要 为 恶 心、 吐、 食欲减退或拒 食、 倦 怠 和 体 重 减 轻 等, 同时还具 有致畸性和弱的致癌性。在动物实验中发 现 #"# 毒 素对动 物 的 小 肠、 脾、 胸 腺、 肠 黏 膜、 淋 巴 器 官、 造血 器官和睾丸都有损 伤, 过量时可导致骨髓和淋巴组 织坏死、 溶解、 外周 血 粒 细 胞 减 少, 淋巴细胞严重缺 乏。同时 #"# 毒素 进 入 机 体 后, 迅速经酯酶代谢成 $#"# 毒素等多 种 代 谢 物[ ( ]。 国 际 上 对 #"# 毒 素 非 常重视, 前苏联已 提 出 国 家 的 食 品 卫 生 限 量 标 准 为 ()) ! % ! &% 。我国小麦 中 #"# 毒 素 的 污 染 率 和 含 量 是比较高的, 据对 "") 份小麦样品的调查结果 表明, 正常小麦中 #"# 毒 素 的 污 染 阳 性 率 为 *) ’ , 平均含 量为 ’"& " ! % ! &% , 最高含量可达( (##& ) ! % ! &%[ # ]。 ! ! #"# 毒 素 的 测 定 方 法 主 要 有: 薄层色谱法
毛细管电泳技术在单克隆抗体药物分析中的应用

毛细管电泳技术在单克隆抗体药物分析中的应用陈泓序;屈锋【摘要】单克隆抗体药物在生物制药行业占有重要地位,是生物医药领域发展的主要方向.因此,单克隆抗体药物的质量控制已成为全球生物制药企业及法规机构关注的热点,对单克隆抗体药物精确表征的需求日益增加.毛细管电泳技术具有分离效率高、分析速度快、分离模式多、样品用量少等特点,已成为单克隆抗体药物分析和质量控制的重要手段.该文对毛细管凝胶电泳、毛细管等电聚焦、毛细管区带电泳等模式在单克隆抗体药物的纯度分析、等电点测定、电荷异质性分析和 N-寡糖分析的应用进行综述,以期为国内单克隆抗体研究开发和生产的企事业单位提供技术参考.%Therapeutic monoclonal antibodies play an important role in biopharmaceuticals, and gradually become one of the main directions of the development of biological medicine. The quality control of monoclonal antibodies has also become the focus of global biopharma compa-nies and regulatory agencies. Capillary electrophoresis has become an important tool in the analysis of monoclonal antibodies with multi-modes and high resolution. In this paper,we reviewed the application of capillary gel electrophoresis,capillary isoelectric focusing and capil-lary zone electrophoresis on the analysis of purity,isoelectric point/charge heterogeneity and N-glycan profiling of therapeutic monoclonal antibodies.【期刊名称】《色谱》【年(卷),期】2018(036)003【总页数】14页(P195-208)【关键词】毛细管电泳;毛细管凝胶电泳;毛细管区带电泳;毛细管等电聚焦;单克隆抗体药物;纯度;电荷异质性;N-寡糖;综述【作者】陈泓序;屈锋【作者单位】北京理工大学生命学院,北京100081;北京理工大学生命学院,北京100081【正文语种】中文【中图分类】O658随着单克隆抗体技术近40年的发展,其在生物医学研究和生物制药以及临床治疗中的应用发展迅速,已占有重要地位。
(仅供参考)治疗用单克隆抗体质量控制 讲义

Fab:fragment antigen binding Fc: fragment crystallizable
免疫球蛋白的水解片段示意图
治疗性抗体发展史
第一代抗体药物:来源于动物的多价抗血清 早年制备抗体的方法是以相应抗原免疫动物,获得抗血清。 抗原通常含有不同的表位,加之所获得的抗血清也未经免疫纯
4 应对标准物质进行稳定性考察,以确定标准物质 在特定条件下保持正常结构及适宜效价的时间。
抗体药物的质量控制
理化对照品的结构验证: 重组抗体药物空间结构复杂,正确的结构是其生物
学活性的前提和基础,因此要对抗体的结构进行验 证。 在抗体药物的常规质控中,对每批产品均进行全面 的结构分析,不仅成本昂贵,而且工作量巨大,难 以完成。 在这种情况下,理化对照品显得尤为必要,只需对 对照品进行充分的结构分析,证明其结构正确;同 时在常规质控中将待测产品与之同时测定,如果结 果一致,可基本说明待测样品结构正确。
抗体药物的质量控制
理化对照品的结构分析包括以下内容: 1 一级结构验证 1.1 质谱分子量测定:可以直接测定完整抗体的分子量,
也可以用糖苷酶将糖基切除后再测定抗体蛋白部分的分子 量,还可以用还原剂将抗体的二硫键打开,分别测定轻、 重链的分子量。测得抗体的分子量后,将其与理论分子量 进行比较,以初步判断蛋白的氨基酸序列是否正确。
免疫球蛋白的分类:根据免疫球蛋白重链 C区的氨基酸组成和抗原特异性不同,将 免疫球蛋白分为IgG 、IgA、IgM、IgD、 IgE五类。
IgG中,根据其重链抗原性和二硫键的数 目和位置的不同,又可分为IgG1~ IgG4四 个亚类。
抗体及其结构
分子体积排阻高效液相色谱法测定低浓度重组人源化抗BCMA/CD3双特异性抗体药物的浓度

药物分析杂志Journal of Pharmaceutical Analysis药物分析杂志 线性关系考察 精密吸取混合对照品储备液、4、6、8、10 mL ,分别置10 mL 量瓶中,用70%甲醇水溶液定容至刻度,即得系列混合对照品溶液。
分别精密吸取上述系列混合对照品溶液10 μL ,按“2.1”项下色谱条件进样分析,测定峰面积。
以峰面积(Y )葛根素(puerarin ) 2. 连翘酯苷A (forsythiaside A ) 3. 黄芩苷(baicalin 牛蒡苷(arctiin )混合对照品(mixed reference substances ) B. 样品(sample ) C. 缺葛根阴性样品(negative sample of Puerariae Lobatae Radix ) D. 缺连翘阴性样negative sample of Forsythiae Fructus ) E. 缺黄芩阴性样品(negative sample of Scutellariae Radix ) F. 缺炒牛蒡子阴性样品(negative sample ofArctii Fructus ) 小儿解表颗粒HPLC 色谱图 HPLC chromatograms of Xiao ’er Jiebiao granules表2 4个成分的线性回归方程、相关系数(r )及线性范围Tab. 2 The regression equation ,correlation coefficients and linear ranges of 4 components成分(component )回归方程(regression equation )r线性范围(linear range )/(μg ·mL -1)葛根素(puerarin )Y =45.19X +7.5460.999 9 4.799~47.99连翘酯苷A forsythiaside A )Y =16.61X +1.3590.999 93.968~39.68黄芩苷(baicalin )Y =32.55X +13.430.999 916.76~167.6牛蒡苷(arctiin )Y =5.843X +0.992 80.999 97.082~70.82药物分析杂志药物分析杂志药物分析杂志药物分析杂志。
高效分子排阻色谱法测定注射用头孢匹胺钠中聚合物的含量

高效分子排阻色谱法测定注射用头孢匹胺钠中聚合物的含量郭艳娟;郭福庆【摘要】目的:建立高效分子排阻色谱法测定注射用头孢匹胺钠中聚合物的含量.方法:采用TSK-GEL G2000SWXL色谱柱(7.8 mm ×300 mm);以磷酸盐缓冲液(pH 7.0) [0.01 mol/L磷酸氢二钠-0.01 mol/L磷酸二氢钠溶液(61∶ 39)]-乙腈(97.5:2.5)为流动相;检测波长231 nm;柱温30℃;流速0.8 ml/min;进样量10μl.结果:头孢匹胺在1.962 5~19.624 5μg/ml范围内与峰面积呈良好的线性关系(r=1.0000),最低检出浓度0.08 μg/ml.结论:建立的方法简单、快速、灵敏度高,可有效控制产品的质量.【期刊名称】《天津药学》【年(卷),期】2015(027)002【总页数】4页(P21-24)【关键词】注射用头孢匹胺钠;高分子聚合物;TSK-GEL G2000SWXL凝胶色谱柱【作者】郭艳娟;郭福庆【作者单位】天津市药品检验所,天津300070;天津市药品检验所,天津300070【正文语种】中文【中图分类】R927.2注射用头孢匹胺钠(cefpiramide sodium)近年来广泛应用于临床,对革兰阳性菌有很强的抗菌作用,对革兰阴性菌在内的细菌亦有广谱抗菌活性。
同时,对绿脓杆菌等葡萄糖非发酵革兰阴性杆菌有很强的抗菌活性,本药作用为杀菌,并对各种细菌产生的β-内酰胺酶稳定。
研究证实,β-内酰胺类抗生素中的高分子聚合物是引发速发型过敏反应的过敏原[1,2],且药品中高分子聚合物的含量直接影响过敏反应的发生率。
故控制产品中的高分子聚合物的含量,对减少此类抗生素过敏具有重要意义[3]。
在传统的聚合物控制中,多采用葡聚糖凝胶G10色谱柱分析。
有文献报道[4],注射用头孢匹胺钠也采用葡聚糖凝胶柱进行聚合物的测定,但该法专属性差,分离效率低,灵敏度低,分析时间长。
单克隆抗体及其高聚体的体积排阻色谱分析方法开发-Waters

2
抗体的SEC分析方法开发
50 mM
蛋白质
分子量
6.5
200 mM
甲状腺球蛋白 670000
250 mM
γ-球蛋白
158000
5.5
卵清蛋白
44000
肌红蛋白
17000
维生素B12 1350
4.5
AU Log MW
3.5
2.5
1.5
0.5
1.0
1.5
2.0
2.5
洗脱体积(mL)
图1.氯化钠对SEC校准曲线的影响。 注:由于蛋白质在溶液中的形状不同,校准点并非呈一条直线。
200 mM 聚集体 = 5.27% USP分离度 = 1.57 USP拖尾因子 = 1.22
0.0
0.3
250 mM
聚集体 = 5.39%
0.2
方法条件 LC条件: 系统:
波长: 色谱柱:
柱温: 样品温度: 进样体积: 流速: 流动相: 最终组成:
数据管理 软件:
配备TUV和钛合金流通池 的ACQUITY UPLC H-Class Bio 系统
214和280 nm
ACQUITY UPLC BEH200 SEC 1.7 µm, 4.6 x 150 mm, 部件号186005225
0.3 0.2 0.1 0.0 0.3 0.2
0.2 0.1 0.0
0.2 0.1 0.0
0.2 0.1 0.0
1.2 1.4 1.6 1.8 2.0 2.2 2.4 2.6 2.8 3.0 3.2 3.4 3.6 3.8 4.0 min
0.1
50 mM 聚集体 = 1.19% USP分离度 = 0.92 USP拖尾因子 = 1.64
scfv名词解释(一)

scfv名词解释(一)SCFV名词解释SCFV(Single-Chain Fragment Variable)是一种在蛋白质工程中常用的单链抗体分子,由抗体的轻链变量区和重链变量区通过肽链连接起来形成。
SCFV拥有小分子量、高亲和力和较高的稳定性,因此被广泛应用于抗体工程、免疫治疗和生物药物研发等领域。
以下是与SCFV相关的名词解释:1. 重链和轻链•重链:抗体分子中较为重的一条多肽链,通过二硫键连接形成抗体的抗原结合区。
在SCFV中,重链变量区主要负责与抗原结合。
•轻链:抗体分子中较为轻的一条多肽链,通过二硫键连接形成抗体的抗原结合区。
在SCFV中,轻链变量区也负责与抗原结合,并与重链变量区通过肽链连接。
2. 亲和力•亲和力:指抗体与抗原结合的结合力强度。
亲和力越高,抗体与抗原的结合越牢固。
SCFV经过优化设计后具有较高的亲和力,能够更有效地与特定抗原结合。
3. 抗体工程•抗体工程:利用基因工程技术对抗体进行改造和优化的过程。
在抗体工程中,SCFV常被用作基础模块,通过引入不同的CDR序列(亮链和重链变量区间)或其他改变,以获得更高亲和力或特定特性的抗体。
4. 免疫治疗•免疫治疗:利用抗体或其他免疫分子来治疗疾病的方法。
SCFV作为一种小分子抗体,具有较好的穿透性和渗透性,使其在免疫治疗中具有优势。
5. 生物药物研发•生物药物研发:开发和生产利用生物技术制造的药物。
SCFV由于其较小的分子量和优良的稳定性,成为生物药物研发的理想选择,可以用于制备高效、安全的药物。
以上是对SCFV相关名词的解释。
SCFV作为一种重要的蛋白质工程工具,持续推动着抗体工程、免疫治疗和生物药物研发领域的发展。
单克隆抗体

单克隆抗体技术【原理及意义】单克隆抗体技术(The technique of monoclonal antibody)是由Kǒhler与Milstein于1975年创立的。
他们发现将小鼠骨髓瘤细胞与绵羊红细胞免疫的小鼠脾细胞进行融合,形成的杂交细胞既可产生抗体,又可无限增殖,从而创立了单克隆抗体杂交瘤技术。
单克隆抗体(monoclonal antibody,M cAb)具有结构均一、纯度高、特异性强、效价高、交叉反应少或无等优点,缺点是其鼠源性对人具有较强的免疫原性,反复人体使用后可诱导产生人抗鼠的免疫应答,从而削弱其作用,甚至导致免疫病理损伤。
制备单克隆抗体包括动物免疫、细胞融合、选择杂交瘤、检测抗体、杂交瘤细胞的克隆化、冻存以及单克隆抗体的大量生产等一系列实验步骤。
下面按照制备单克隆抗体的流程顺序,逐一介绍其实验方法。
一、细胞融合前的准备(一)免疫方案选择合适的免疫方案对于细胞融合的成功,获得高质量的M cAb 至关重要。
一般要在融合前两个月左右确立免疫方案开始初次免疫,免疫方案应根据抗原的特性而定。
1.颗粒性抗原免疫性较强,不加佐剂就可获得很好的免疫效果。
下面以细胞性抗原为例:免疫细胞数为每只小鼠1×107/0.5 m L生理盐水,腹腔注射。
1)初次免疫,间隔2~3周。
2)第二次免疫,间隔3周。
3)第三次免疫10天后,取血测效价。
4)加强免疫3天后,取脾融合。
2.可溶性抗原免疫原性弱,一般要加佐剂。
将抗原与佐剂等体积混合在一起,研磨成油包水的乳糜状(放一滴在水面上不易马上扩散呈小滴状表明已达到油包水的状态)。
1)初次免疫,Ag5~50微克/只,加弗氏完全佐剂皮下多点注射,一般0.2毫升/点,间隔3周。
2)第二次免疫,剂量途径同上,加弗氏不完全佐剂,间隔3周。
3)第三次免疫,剂量同上,不加佐剂,于生理盐水中腹腔注射,7~10天后采血测其效价,检测免疫效果,间隔2~3周。
4)加强免疫,剂量50μg为宜,腹腔或静脉注射。
IgG1型单克隆抗体对照品的一级结构解析

IgG1型单克隆抗体对照品的一级结构解析崔新玲; 胡志上; 孟晓光; 钱小红; 朱涛; 应万涛【期刊名称】《《分析测试学报》》【年(卷),期】2019(038)008【总页数】7页(P939-945)【关键词】抗体对照品; 分子量; 等电点; 电荷异质性; 肽图【作者】崔新玲; 胡志上; 孟晓光; 钱小红; 朱涛; 应万涛【作者单位】天津科技大学生物工程学院天津300457; 北京蛋白质组研究中心蛋白质组学国家重点实验室国家蛋白质科学中心(北京) 北京102206; 中国计量科学研究院北京100013; 北京正旦国际科技有限责任公司北京102206; 天津康希诺生物股份有限公司天津300457【正文语种】中文【中图分类】O65721世纪以来,单克隆抗体的研发技术快速发展,推进了其在生物医学研究、生物制药以及临床治疗中的应用[1]。
单克隆抗体药物(mAb)是通过基因工程生产的蛋白质药物,具有特异性高、作用机制明确、效果显著、经济效益大等优势,已成为近年来生物医药产业的重要增长点。
与小分子药物不同,抗体类药物不仅分子质量大[2],结构复杂,而且可经糖基化或其它翻译后修饰[3],导致其结构具有高度不均一性(异质性)[3-4],这对单克隆抗体类药物的表征分析和质量控制提出了新的要求和挑战。
先进的分析方法,比如质谱技术[5-11],可提供非常详细的表征过程和产品信息[5,12-13],其提供的丰富的结构信息对产品质量至关重要,而这些技术自身的准确性、精确性、稳健性和适用性也同样重要。
产品质量标准是根据产品而设定的,并且要持续适用于内部参考标准品[14]。
具有代表性且应用广泛的mAb标准品[15-17],加之详细的表征数据,可极大地保证整个药品生命周期中的质量控制[18-23]。
本文主要对中国计量科学研究院提供的抗体对照品(IgG1型单克隆抗体)的关键参数进行研究分析(主要是一级结构),为后续进行深入的质量研究与计量学溯源技术标准提供参考。
BioVendor游离轻链(κ和λ)Elisa试剂盒检测步骤

BioVendor游离轻链(κ和λ)Elisa试剂盒检测步骤人免疫球蛋白(Ig)分子由两个相同的重链和两条相同的轻链组成,重链有α、δ、ε、γ和μ这5种类型,这些重链分别决定了免疫球蛋白IgA,IgD,IgE,IgG和IgM这5类;轻链分为 k (kappa)链和λ (lambda)链2种类型,每个Ig分子上只有一个型别的轻链。
FLC是B淋巴细胞的天然产物,因此代表了肿瘤和反应性B细胞相关疾病的独特生物标志物。
FLC的增加与恶性血浆失调和其他淋巴结性免疫增生性疾病有关。
同时,FLC的检测也是各种单克隆球蛋白病的重要诊断辅助,例如多发性骨髓瘤,巨球蛋白血症,非分泌性骨髓瘤,雾化多发性骨髓瘤,单克隆肺炎,单克隆性颅脑病。
较精确测量血清尿液中的单克隆游离轻链在轻链疾病中尤其重要,例如轻链骨髓瘤,原发全身性淀粉样变性和轻链沉积疾病。
定量单克隆FLC的能力可能有助于监测该疾病。
在轻链骨髓瘤的患者中,在疾病早期阶段导致FLC κ/λ比的明显变化。
免疫球蛋白的尿液单克隆kappa或Lambda游离轻链的检测,也称为Bence Jones 蛋白(BJP,本周蛋白),对于识别和监测BCELL恶性肿瘤也很重要。
来看看接下来要介绍的人免疫球蛋白游离轻链(κ和λ)Elisa试剂盒(适用样本类型:血清、血浆-EDTA、血浆-肝素、血浆-柠檬酸盐、尿液):游离轻链(κ和λ)Elisa 试剂盒检测步骤:FLC kappa和FLC λ的检测范围和灵敏度分别是:检测范围灵敏度10–320ng/ml 6ng/ml17.5–560ng/ml 5ng/mFLC kappa和FLC λ的较精确度分别是:组间差异:FLC kappa(n=6) FLC λ(n=6)CV=7.0% CV=6.4%组内差异:FLC kappa(n=8) FLC λ(n=8)CV = 3.0% CV = 4.5%BioVendor人免疫球蛋白游离轻链(κ和λ)Elisa试剂盒部分引文结果展示:1、Hantavirus infection-induced B cell activation elevates free light chains levels in circulation.2、Randomized controlled trial of medium cut-off versus high-flux dialyzers on quality of life outcomes in maintenance hemodialysis patients.3、Assessment of Intrathecal Free Light Chain Synthesis: Comparison of Different Quantitative Methods with the Detection of Oligoclonal Free Light Chains by Isoelectric Focusing and Affinity-Mediated Immunoblotting。
治疗性单克隆抗体类制品质量控制标准的思考_张峰

同参比品一致 b 同参比品一致 b 电泳图谱同参比品一致,且样品主峰迁移时间应位于规定范围内 酸性区、主峰、碱性区峰面积百分比位于规定范围内 阳性(同参考图谱比较,有所有 / 部分特定色谱峰,且无明显新峰) 同理到期,如:赫塞汀 (曲妥珠单抗)、美罗华(利妥昔单抗)、爱必妥(西 妥昔单抗)和类克(英利西单抗)等,许多医药企业 通过生物仿制药的方式加入到单抗制品的开发和 生产中。随之而来的问题是,由于缺乏对单抗结构 与其安全性和有效性间关系的深入了解,新加入 企业和生物仿制药企业在单抗制品的质量控制方
总体上看,单抗的质量控制项目(见表 1)主 要包括一般项目、理化检测、含量、鉴别、纯度、活 性 、安 全 性 等 几 个 方 面[5],其 中 安 全 性 方 面 检 测 包 括 :DNA 残 留 、宿 主 细 胞 蛋 白 残 留 、生 产 过 程 相 关 外源因子和异常毒性检测。 作为对纯化工艺去除 外 源 因 子 能 力 的 验 证 , 宿 主 细 胞 DNA、 宿 主 细 胞 蛋白残留和生产过程相关外源因子的检测主要在 注册阶段的原液样品中进行,考虑到最适样本的 问题,这些项目在成品检测中可以不检测。在产品 质量标准设定和检测方法选择的过程中,应根据 制品的具体情况选择合适的检测方法,并根据工 艺的稳定性、产品的安全性和有效性以及方法本 身的变异情况设定合适的质量标准。 由于对结构 与功能间关系认识的不断深入和检测技术的不断 发展,产品的检定方法和质量标准是一个不断发 展提高的过程,下面就当前单抗制品的检测方法 和质量标准进行说明和论述。 3 单抗质量方法研究现状及其标准制定的注意事项
从表 1 可以看出,对于一个质量控制项目可 能会采用不同的方法,从不同的侧面反映单抗的 质量,特别是近年来一些新技术应用于单抗的质 量控制,对单抗制品的质量控制提供了更高的保 障。 但同时也需考虑到,对于单抗,表 1 中所列出 的项目只是一个较为普遍的原则,但并不是所有 的检测方法都适用于每一种单抗制品,表中所规 定的标准也并非适用于所有的制品,针对于某一 个特定单抗来说, 都会有一些特殊的因素需要考 虑, 下面就不同检测方法在单抗质量控制中的作 用及其标准制定时需要考虑的问题作简单分析。
抗体的结构
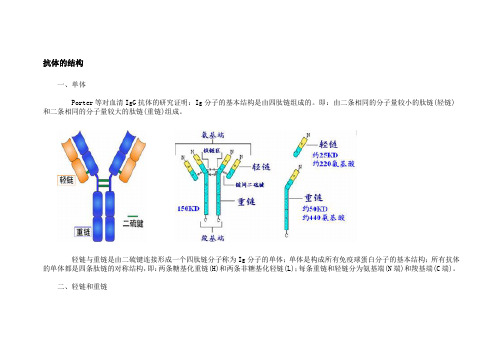
抗体的结构一、单体Porter等对血清IgG抗体的研究证明:Ig分子的基本结构是由四肽链组成的。
即:由二条相同的分子量较小的肽链(轻链)和二条相同的分子量较大的肽链(重链)组成。
轻链与重链是由二硫键连接形成一个四肽链分子称为Ig分子的单体;单体是构成所有免疫球蛋白分子的基本结构;所有抗体的单体都是四条肽链的对称结构,即:两条糖基化重链(H)和两条非糖基化轻链(L);每条重链和轻链分为氨基端(N端)和羧基端(C端)。
二、轻链和重链1、轻链(light chain,L链)由214个氨基酸残基组成,通常不含碳水化合物,分子量为24kD,有两个由链内二硫键组成的环肽,L链可分为:Kappa(κ)与 lambda(λ)2个亚型。
2、重链(heavy chain,H链)由450-550个氨基酸残基组成,分子量55-75kD,含糖数量不同,4-5个链内二硫键,可分为5类,μ、γ、α、δ、ε链,不同的H链与L链(κ或λ)组成完整的Ig分子。
分别称为:IgM,IgG,IgA,IgD和IgE。
三、可变区和恒定区通过对H链或L链的氨基酸序列比较分析,发现:其N-末端序列变化很大,称此区为可变区(V区);C-末端氨基酸则相对稳定,变化很小,称此区为恒定区(C区)。
1、可变区(Variable region,V区)L链N端1/2处(VL)108-111个氨基酸残基,H链N端1/5-1/4处(VH)118个氨基酸残基,V区有一个肽环65-75个氨基酸残基。
可变区可分为高变区(hypervariable region,HVR)和骨架区(framework region,FR),VL的HVR在24-34,50-56,89-97氨基酸位置。
VH的HVR在31-35,50-56,95-102氨基酸位置。
分别称为VL和VH的HVR1,HVR2,HVR3。
高变区为抗体与抗原的结合位置,称为决定簇互补区(complementarity- determining region,CDR),VL和VH的HVR1,HVR2,HVR3又分别称为CDR1,CDR2,CDR3,其中CDR3具有更高的高变程度,H链在与抗原结合中起重要的作用。
常用的单克隆抗体检测方法

常用的单克隆抗体检测方法通过杂交瘤技术制备单克隆抗体,在杂交瘤制备完成后,需要对抗体进行一个检测,本文介绍了几种常用的抗体检测的方法(1)免疫酶技术免疫酶技术是将抗原抗体反应的特异性和酶对底物显色反应的高效催化作用有机结合而成的免疫学技术。
由于它特异性强,灵敏度高,现已广泛用于筛选和鉴定单抗。
①器材和试剂a、包被缓冲液:碳酸盐缓冲液:取0.2mol/L Na2CO3 8ml,0.2mol/L NaHCO3 17ml 混合,再加75ml蒸馏水,调PH至9.6。
Tris-HCl缓冲液(PH8.0,0.02mol/L):取0.1mol/L Tris 100ml,0.1mol/L HCl 58.4ml混合,加蒸馏水至1000ml。
b、洗涤缓冲液(PH7.2的PBS):KH2PO4 0.2g,KCl 0.2g,Na2HPO4·12H2O 2.9g,NaCl 8.0g,Tween-20 0.5ml,加蒸馏水至1000ml。
c、稀释液和封闭液:牛血清白蛋白(BSA)0.1g,加洗涤液至100ml;或用洗涤液将小牛血清配成5-10%使用。
d、酶反应终止液(2mol/LH2SO4):取蒸馏水178.3ml,滴加浓硫酸(98%)21.7ml。
e、底物缓冲液(PH5.0,磷酸盐-柠檬酸缓冲液):取0.2mol/L Na2HPO4 25.7ml,0.1ml/L柠檬酸24.3ml,再加50ml蒸馏水。
柠檬酸溶液及配成的底物缓冲液不稳定,易形成沉淀,因此一次不宜配制过多。
f、底物使用液:OPD底物使用液(测490nm的OD值):OPD 5mg,底物缓冲液10ml,3% H2O20.15ml。
TMBS或TMB底物使用液(测450nm的OD值):TMBS或TMB(1mg/ml)1.0ml,底物缓冲液10ml,1% H2O2 25ul。
ABTS底物使用液(测410nm的OD值):ABTS 0.5mg,底物缓冲液1ml,3% H2O2 2ul。
抗体重链 跑胶-概述说明以及解释

抗体重链跑胶-概述说明以及解释1.引言1.1 概述概述抗体重链是构成抗体分子的关键组成部分之一,对于抗体的结构和功能具有重要的影响。
抗体是机体在抵御入侵的病原体时产生的一种具有特异性的免疫蛋白质,在免疫系统中发挥着重要的作用。
抗体重链是由多个氨基酸序列组成的多肽链,主要分为两种类型:重链和轻链。
其命名来源于它们相对分子质量的大小,重链相对较大,轻链相对较小。
抗体重链的作用是通过与抗原结合,从而激活免疫系统,诱导免疫应答,以清除病原体或异常细胞。
在本文中,我们将详细探讨抗体重链的结构和功能,以及它在医学和生物学领域中的应用。
我们还将讨论抗体重链研究的前景和挑战,展望未来的发展方向。
通过深入了解抗体重链,我们可以更好地理解免疫系统的工作原理,并为疾病的防治提供更有效的策略和方法。
了解抗体重链的相关知识对于研究和开发新型药物、诊断工具以及免疫治疗手段都具有重要的意义。
本文旨在系统地介绍抗体重链的定义、结构、功能以及其在医学和生物学中的应用。
通过对相关研究领域的总结和分析,我们希望为抗体重链研究提供更深入的见解,并为进一步推动相关领域的发展贡献一份力量。
1.2文章结构文章结构部分的内容可以是以下内容:文章结构部分是对整篇文章的整体框架进行介绍和概述。
本文旨在探讨抗体重链及其在医学和生物学中的应用,下面将详细介绍文章的各个章节内容。
第一章为引言部分,主要包括概述、文章结构和目的。
概述部分将简要介绍抗体重链的背景和意义,为读者提供一个整体的了解。
文章结构部分将详细说明文章的各个章节及其内容安排。
目的部分将明确本文的研究目的和意义。
通过引言部分,读者可以预览文章的内容和结构,了解本文的主要研究内容和意义。
第二章为正文部分,将从抗体重链的定义和作用以及其结构和功能两方面进行论述。
首先,将介绍抗体重链的定义和作用,包括其在免疫系统中的作用、分子结构和基本特征等方面的内容。
其次,将详细讨论抗体重链的结构和功能,包括不同类型抗体重链的特点、功能以及其在免疫应答中的作用机制等。
抗红细胞H抗原单链抗体中可变区重链和轻链顺序对其活性的影响

间插入 1段连接肽 ( linker), 即 ( G ly4 Ser) 3, 扩增得 到的 1条 VH linker VL 或 VL linker VH 基因 后, 表 达 出具有一定活性的蛋白质, 它所具有的分子量小、组 织穿透能力强及免疫原性低等特点, 使得其在疾病 的诊断及治疗应 用方面具有很大 潜力 [ 1] 。 scF v 的 构建中, 除连接肽 序列的设计是 一个重要环节外, VL 在前或 VH 在前的顺序不同也对其空间构象产生
! ! 摘要: 目的 ! 探讨抗红细胞 H 抗原单链抗体 ( scF v)中可变区重链 ( VH )和轻 链 ( VL )顺序对 该单链抗 体活性的 影响。方法 ! 采用 PCR 方法从质粒 pM D 18T 2E8scF v( VH linker VL 型 )中克隆出 VL 和 VH 可变区 基因, 通过重叠 引物延伸法将这 2种基因连接, 并引入连接肽 ( linker)编码序列, 构建 VL linker VH 型的单链抗体基因, 将 VL linke r VH 和原有的 VH linke r VL 2种形式的单链抗体基因分别插入到原核表达 载体 pET h is中, 转化 BL 21( DE3) plysS细 胞, 异丙基硫代 D 半乳糖 苷 ( IPTG )诱导表达, 表达产物 用镍亲和层析柱纯化; 免疫荧光法、竞争 EL ISA 和低离子 聚凝胺法检测纯化后 scF v活性。结果 ! 酶切 及测序 表明 VL linke r VH 型 单链抗 体表达 载体构 建成 功, SDS PAGE 和 W estern blot分 析表明 V L linke r VH 和 VH linker VL 2型抗人红 细胞 scF v均在 BL21菌中 获得高效表达, 重组蛋白 的相对分子质量 (M r )为 27kD, 表达产物以包涵体形式存在, 分别占菌体总蛋白的 26. 8% 和 27. 6% , 纯化 后获得了 高纯度的 scF v; 免疫荧光、竞争 EL ISA 和低离子聚凝胺试验分析证明 2种 单链抗体均 可特异结 合红细胞表 面 H 抗 原, VH linke r VL 结合活 性高于 VL linker VH。结论 ! 成功制备了 VL linker VH 型 2E8scF v; VH linker VL 型 2E8scFv 抗原的纯合活性高于 VL linker VH 型 2E8scFv。
