用薄层色谱法鉴定咖啡因
咖啡中咖啡因的紫外线分光光度测定法

咖啡中咖啡因的紫外线分光光度测定法作者:李华峰赵士峰吕秀明来源:《品牌与标准化》2014年第12期咖啡因含量是咖啡的一项重要测试指标。
咖啡因的测定方法有薄层色谱法、紫外分光光度法、气相色谱法和高效液相色谱法。
为适应一般实验室的需要,本文用紫外分光光度法对速溶咖啡、普通咖啡及咖啡豆中咖啡因的测定方法进行了试验,结果较为满意。
本法操作简单、迅速、不需要特殊的试剂及仪器,方法添加回收率为95%~105%,精密度良好,变异系数为2.0%~2.8%,准曲线相关系数为0.999。
1 试验方法原理咖啡经加水煮沸,是咖啡因溶于水,用三氯甲烷提取后在276nm波长下测其吸光值与标准比较定量。
仪器与试剂755紫外分光光度计;氧化镁,A[⋅]R;三氯甲烷,A[⋅]R;无水硫酸钠,A[⋅]R;咖啡因,生化试剂;咖啡因标准溶液:咖啡因在80℃干燥4h,精确称取50mg溶于水成100ml。
取此液20ml移入分液漏斗中,加10%氢氧化钠溶液2ml,氯化钠2g溶解后用三氯甲烷提取三次,每次20ml,合并提取液,经无水硫酸钠脱水过滤于100ml容量瓶中,用三氯甲烷洗涤,合并,定容至刻度。
此溶液1ml=100μg咖啡因。
操作方法:样品处理及提取咖啡豆、普通咖啡,称取样品(咖啡豆研磨成粉状)1.0g~2.0g;速溶咖啡取0.5g,于250ml烧杯中,加150ml水,盖表面皿,在电炉上煮沸,保持微沸30min,加氧化镁2g,移入250ml容量瓶中,用水冲洗烧杯合并于容量瓶中,放冷后加水至刻度,混匀,过滤。
取滤液10ml于分液漏斗中,用三氯甲烷20ml、20ml、10ml提取,提取液经无水硫酸钠(约2g)脱水,并滤于50ml容量瓶中,加三氯甲烷至刻度。
同时做空白试验。
测定取上述样品的三氯甲烷提取液,用1cm石英杯,以试剂空白调节零点,于波长276nm处测其吸光值,查咖啡因标准曲线,计算其含量。
标准曲线取咖啡因标准溶液(1ml=100μg)0.4ml、0.8ml、1.2ml、1.6ml、2.0ml于10ml容量瓶中,加三氯甲烷至刻度。
中药执业药师中药学专业知识(一)-2

中药执业药师中药学专业知识(一)-2(总分:100.00,做题时间:90分钟)一、最佳选择题(总题数:45,分数:100.00)1.茶叶中咖啡因的提取方法是(分数:2.00)A.回流法B.渗漉法C.浸渍法D.升华法√E.连续回流法解析:[解析] 本题考查升华法的应用。
固体物质在受热时不经过熔融直接转化为蒸气,蒸气遇冷后又凝结成固体的现象称为升华。
中药中具有升华性的成分利用升华法直接从中药中提取出来,如樟木中的樟脑、茶叶中的咖啡因。
2.下列溶剂中极性最大的是(分数:2.00)A.三氯甲烷B.石油醚C.甲醇√D.乙醇E.丙酮解析:[解析] 本题考查溶剂极性强弱的判断。
常用于中药化学成分提取的溶剂按极性由强到弱的顺序:水>甲醇>乙醇>乙酸乙酯>三氯甲烷>乙醚(无水)>苯>己烷。
3.不宜用煎煮法提取的中药化学成分是(分数:2.00)A.蒽醌苷B.挥发油√C.黄酮苷D.多糖E.皂苷解析:[解析] 本题考查煎煮法的适用范围。
煎煮法是中药材加入水浸泡后加热煮沸,将有效成分提取出来的方法。
含挥发性成分或有效成分遇热易分解的中药材不宜用此法。
4.硅胶作为吸附剂用于吸附色谱时是(分数:2.00)A.非极性吸附剂B.极性吸附剂√C.两性吸附剂D.化学吸附剂E.半化学吸附剂解析:[解析] 本题考查硅胶的特点。
硅胶、氧化铝属于物理吸附剂中的极性吸附剂,而活性炭属于非极性吸附剂。
5.最常用的超临界流体是(分数:2.00)A.二氧化碳√B.乙烷C.庚烷D.一氧化二氮E.六氟化硫解析:[解析] 本题考查超临界流体萃取法常用流体种类。
超临界流体萃取法是采用超临界流体为溶剂对中药材进行萃取的方法。
物质处于其临界温度和临界压力以上状态时,成为单一相态,将此单一相态下的物质称为超临界流体。
已知可作为超临界流体的物质很多,如二氧化碳、一氧化二氮、六氟化硫、乙烷、庚烷、氨、二氯二氟甲烷等,其中以二氧化碳最为常用。
6.水蒸气蒸馏法主要用于提取(分数:2.00)A.挥发油√B.黄酮苷C.强心苷D.糖类E.生物碱解析:[解析] 本题考查水蒸气蒸馏法的适用范围。
咖啡因药典标准2010版
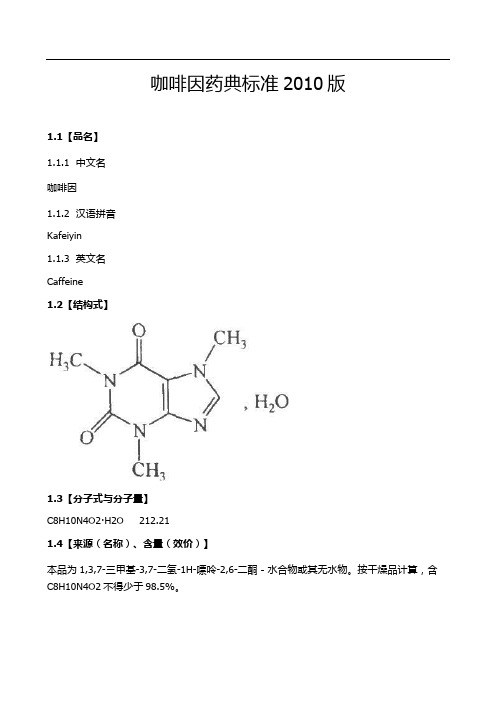
咖啡因药典标准2010版1.1【品名】1.1.1 中文名咖啡因1.1.2 汉语拼音Kafeiyin1.1.3 英文名Caffeine1.2【结构式】1.3【分子式与分子量】C8H10N4O2·H2O 212.211.4【来源(名称)、含量(效价)】本品为1,3,7-三甲基-3,7-二氢-1H-嘌呤-2,6-二酮-水合物或其无水物。
按干燥品计算,含C8H10N4O2不得少于98.5%。
1.5 【性状】本品为白色或带极微黄绿色、有丝光的针状结晶;无臭,味苦;有风化性。
本品在热水或三氯甲烷中易溶,在水,乙醇或丙酮中略溶,在乙醚中极微溶解。
1.5.1 熔点本品的熔点(2010年版药典二部附录Ⅵ C)为235~238℃。
1.6【鉴别】(1)取本品约10mg,加盐酸1ml与氯酸钾0.1g,置水浴上蒸干,残渣遇氨气即显紫色;再加氢氧化钠试液数滴,紫色即消失。
(2)取本品的饱和水溶液5ml,加碘试液5滴,不生成沉淀;再加稀盐酸3滴,即生成红棕色的沉淀,并能在稍过量的氢氧化钠试液中溶解。
(3)本品的红外光吸收图谱应与对照的图谱(《药品红外光谱集》250图)一致。
1.7【检查】1.7.1 溶液的澄清度取本品1.0g,加水50ml,加热煮沸,放冷,溶液应澄清。
1.7.2 有关物质取本品,加三氯甲烷-甲醇(3:2)溶解制成每1ml中约含20mg的溶液,作为供试品溶液;精密量取适量,加上述溶剂定量稀释成每1ml中约含0.10mg的溶液,作为对照溶液。
照薄层色谱法(2010年版药典二部附录Ⅴ B)试验,吸取上述两种溶液各10μl,分别点于同一硅胶GF254薄层板上,以正丁醇-丙酮-三氯甲烷-浓氨溶液(40:30:30:10)为展开剂,展开,晾干,在紫外光灯(254nm)下检视。
供试品溶液如显杂质斑点,与对照溶液的主斑点比较,不得更深。
1.7.3 干燥失重取本品,在105℃干燥至恒重,减失重量不得过8.5%;如为无水咖啡因,减失重量不得过0.5%(2010年版药典二部附录Ⅷ L)。
绿茶的化学实验报告

实验名称:绿茶提取物的化学分析一、实验目的与摘要本实验旨在通过化学分析的方法,对绿茶提取物进行定性分析和定量测定,了解绿茶中的主要化学成分及其含量,探讨绿茶的保健作用。
实验过程中,我们将提取绿茶中的茶多酚、咖啡因等活性成分,并通过化学分析方法进行定性和定量分析。
二、实验器材1. 电子天平2. 烧杯3. 漏斗4. 玻璃棒5. 滤纸6. 水浴锅7. 紫外可见分光光度计8. pH计9. 精密移液管10. 茶叶样品三、实验原理绿茶中含有多种生物活性成分,如茶多酚、咖啡因、氨基酸等。
本实验主要采用以下方法进行提取和分析:1. 茶多酚的提取:采用乙醇提取法,利用茶多酚在乙醇中具有较高的溶解度,从绿茶中提取茶多酚。
2. 茶多酚的定性分析:采用紫外-可见分光光度法,通过测定茶多酚在特定波长下的吸光度,判断茶多酚的存在。
3. 茶多酚的定量分析:采用标准曲线法,以已知浓度的茶多酚溶液为标准,绘制标准曲线,根据样品的吸光度计算茶多酚的含量。
4. 咖啡因的提取:采用酸碱中和法,利用咖啡因在酸性条件下溶解度较高的特性,从绿茶中提取咖啡因。
5. 咖啡因的定性分析:采用薄层色谱法,通过比较样品与标准样品在薄层色谱板上的色斑,判断咖啡因的存在。
6. 咖啡因的定量分析:采用紫外-可见分光光度法,测定咖啡因在特定波长下的吸光度,根据标准曲线计算咖啡因的含量。
四、实验步骤1. 茶多酚的提取:称取5g绿茶样品,加入50mL 70%乙醇溶液,超声提取30分钟,过滤,滤液备用。
2. 茶多酚的定性分析:取适量滤液,在紫外-可见分光光度计上测定其在275nm处的吸光度,与标准曲线对照,判断茶多酚的存在。
3. 茶多酚的定量分析:取适量滤液,在紫外-可见分光光度计上测定其在275nm处的吸光度,根据标准曲线计算茶多酚的含量。
4. 咖啡因的提取:称取5g绿茶样品,加入50mL 1M盐酸溶液,煮沸10分钟,冷却,过滤,滤液备用。
5. 咖啡因的定性分析:取适量滤液,滴加苯酚-硫酸溶液,观察色斑变化,与标准样品对照,判断咖啡因的存在。
实验3 柱色谱分离染料和薄层色谱鉴定阿司匹林与咖啡因

实验三、柱色谱分离染料和薄层色谱鉴定阿司匹林与咖啡因自我实践实验:旋光度的测定一、目的1. 了解柱色谱和薄层色谱的原理2. 练习柱色谱和薄层色谱的操作二、原理 (略,见实验指导。
P72-74, P53-60)三、实验仪器色谱柱,50ml 烧杯(二只),10ml 量筒,短颈漏斗,长颈滴管(二支),铁架台,烧瓶夹,双联球,高效薄层板(每组二块),层析缸,毛细管,镊子,紫外分析仪。
四、药品石英砂,氧化铝,95%乙醇,无水乙醇,混合染料(甲基橙、亚甲基蓝),0.2mol/L 盐酸,咖啡因,阿斯匹林。
1,2-二氯乙烷/乙酸(12:1)展开剂。
五、实验操作步骤(一)甲基橙和亚甲基蓝两种染料的分离1.装柱固定色谱柱加约6克氧化铝 用双联球压实 加少量石英砂覆盖 打开活塞 2.加样加6滴混合染料 打开活塞 加少量乙醇 淋洗 (重复2-3次)(用长滴管) (短滴管约1管)3.洗脱用乙醇洗脱(速度慢可用双联球压出)直到蓝色物质全部洗出 小烧杯接收。
(约10mL )待蓝色带完全洗脱后加少量0.2mol/L 盐酸 淋洗 (重复2-3次)用0.2mol/L 盐酸洗脱 (短滴管约1管) (约25mL )小烧杯接收,直到红色物质全部洗出,速度慢用双联球压出。
4.注意事项:(1)柱要装的均匀,石英砂少量即可(约2-3毫米厚度)(2)缓慢加样,尽量不要碰在柱壁上。
(3)洗脱时,洗脱剂加入速度要慢,每次加入的量不要太多(二)薄层色谱1.点样距薄板一端约0.5cm处,用毛细管在一块薄层板上等距离分别点上乙酰水杨酸标样、咖啡因标样和阿加片提取液(乙酰水杨酸与咖啡因的混合样液)。
如图所示2.展开在层析缸中加入约5ml展开溶剂(1,2-二氯乙烷/乙酸(12:1))后,将薄板放入层析缸中,展开剂液面不得超过点样线。
当溶剂前缘距薄板顶端0.5cm时,取出薄板,作好标记,放在空气中自然晾干。
3.检出在紫外分析仪上,观察荧光的斑点,并描出斑点的位置,计算各样品的R f值。
薄层层析实验报告

薄层层析实验报告篇一:薄层色谱法实验报告有机化学第二课堂实验报告一,基本信息姓名:年级:XX级专业层次:队别:日期:XX年5月23日实验室:有机化学实验室二二、实验报告正文实验题目:薄层板的制作及薄层色谱的应用实验目的掌握薄层色谱的基本原理及其在有机物分离中的应用。
实验原理1.有机混合物中各组分对吸附剂的吸附能力不同,当展开剂流经吸附剂时,有机物各组分会发生无数次吸附和解吸过程,吸附力弱的组分随流动相迅速向前,而吸附力弱的组分则滞后,由于各组分不同的移动速度而使得她们得以分离。
物质被分离后在图谱上的位置,常用比移值Rf表示。
Rf?原点至层析斑点中心的距离原点至溶剂前沿的距离实验仪器与药品实验仪器:硅胶层析板两块,卧式层析槽一个,点样用毛细管,紫外荧光灯,铅笔暖风机、载玻片、钢勺、镊子等药品:碱性湖蓝与荧光黄混合样品、咖啡因与阿司匹林混合样品、阿司匹林纯样品二氯乙烷层析液、95%的乙醇溶液,硅胶粉、5%的羧甲基纤维素钠(CMC)的水溶液等仪器装置图“浸有层析板的层析槽”图1-层析缸(广口瓶),2-薄层板,4-层析液实验步骤(1)薄层板的制备:(本文来自: 小草范文网:薄层层析实验报告)取3g 硅胶G粉于研钵中,加相当于8ml左右的用5%的羧甲基纤维素钠(CMC)的水溶液,用力研磨1-2分钟,至成糊状后立即倒在准备好的薄层板中心线上,快速左右倾斜,使糊状物均匀地分布在整个板面上,厚度约为0.25mm,然后平放于平的桌面上干燥15分钟,再放入100℃的烘箱内活化2小时,取出放入干燥器内保存备用。
(2)点样。
在层析板下端1.0cm处,(用铅笔轻化一起始线,并在点样出用铅笔作一记号为原点。
)取拉好的毛细点样管,分别蘸取咖啡因与阿司匹林混合样品、阿司匹林纯样品,点于原点上(注意点样用的毛细管不能混用,毛细管不能将薄层板表面弄破,样品斑点直径在1到2mm为宜!斑点间距稍大一点。
点样次数5到7次)另取一块薄层板,点碱性湖蓝与荧光黄混合样品。
咖啡因实验报告

咖啡因的提取分离及鉴定一实验目的(1)学习天然物的提取技术和鉴定知识(2)掌握从茶叶中提取咖啡因的方法的原理和操作(3)掌握波层色谱和紫外光谱的操作方法(4)巩固回流、蒸馏、升华等基本操作(5)了解生物碱的应用及定性经验方法二基本原理咖啡因是一种黄嘌呤生物碱化合物,是一种中枢神经兴奋剂,能够暂时的驱走睡意并恢复精力。
有咖啡因成分的咖啡、茶、软饮料及能量饮料十分畅销,因此,咖啡因也是世界上最普遍被使用的精神药品。
茶叶中含有多种生物碱,其中咖啡因(也叫咖啡碱,caffeine)含量为1 % ~ 5 %,单宁酸含量为11 % ~ 12 %,色素、纤维素、蛋白质等含量为 %,咖啡因是弱碱性化合物,易溶于氯仿( %)、水(2 %)及乙醇(2 %)、热苯(5 %)等。
单宁酸易溶于水和乙醇,不溶于苯。
咖啡因为嘌呤的衍生物,化学名为1,3,7- 三甲基-2,6-二氧嘌呤,其结构式如下:近年来从茶中提取药用咖啡因方法的研究进展,包括升华法、溶剂法、吸附法和超临界CO2气提法。
三实验所用试剂、仪器实验试剂:氯仿无水硫酸钠纯净水茶叶无水乙醇实验仪器:电磁炉锅烧杯蒸发皿玻璃棒分液漏斗球形冷凝器铁架台滤纸玻璃漏斗蒸馏头接收管锥形瓶四分离方法创新之处首先用水煎煮茶叶,然后再用氯仿将咖啡因从水中萃取出来,使用旋转蒸发仪将氯仿蒸出,可以得到咖啡因粗品,颜色为淡绿色。
然后将粗品溶于乙醇当中用蒸发皿蒸出乙醇可以得到交纯的咖啡因。
五自制或创造了那些实验条件条件在做咖啡因的纯化时,将咖啡因粗品溶于乙醇中,在用蒸发皿将乙醇蒸出此时给蒸发皿上面盖上一层滤纸可以回收一部分升华的咖啡因六实验流程及操作方法实验步骤1、称取300g市售茶叶,用纱布包起,加入到盛有 3L蒸馏水的烧杯中,加热煮沸3h把茶叶提出水面,并用玻璃棒把残留在其中水赶出来。
2、冷却至室温,转移至分液漏斗,用600mL氯仿分两次萃取,收集萃取液于一干燥的锥形瓶中,用无水硫酸钠干燥。
从茶叶中提取咖啡因实验报告

从茶叶中提取咖啡因及薄层色谱法对APC各组分的分离鉴定实验课程基础合成实验-有机化学实验实验项目从茶叶中提取咖啡因薄层色谱法对APC各组分的分离专业化学工程与工艺班级学号姓名指导教师开课学期至学年二学期实验时间一、实验目的1、学习索氏提取器的原理和方法,掌握从茶叶中提取咖啡因的原理和操作。
2、了解咖啡因的一般性质及掌握利用升华方法纯化固体产物的原理和基本操作3、巩固复习有机化合物熔点的测定方法。
4、了解并分离鉴定解热镇痛药复方阿司匹林的主要成分。
5、掌握薄层色谱法分离鉴定药物的原理和方法。
二、药品简介◆咖啡因分子结构式◆咖啡因的物理性质:纯的咖啡因是白色的,强烈苦味的白色粉末或六角棱柱状结晶。
化学式为C8H10N4O2 ,化学名称1,3,7-三甲基-2,6-二氧嘌呤,分子量194.19,相对密度:1.2g/cm*3,熔点:234.5℃,沸点:178℃,纯品熔点235~236℃,味苦,易溶于氯仿(12.5%),水及乙醇(2%)等。
含结晶水的咖啡因为无色针状晶体, 在100 ℃时失去结晶水, 并开始升华,120 ℃时显著升华,178℃时迅速升华◆来源食品工业中咖啡因的主要来源是咖啡豆、可可、茶叶,冬青等,但咖啡豆的咖啡因含量会因品种不同也有不同。
也存在于自然界中100种植物的叶子,根和果实中。
◆用途:①对中枢神经系统有较强的兴奋作用,对大脑皮层具有选择性兴奋作用。
②医药上可用作心脏和呼吸兴奋剂,也是一种重要的解热镇痛剂,是复方阿司匹林和氨非加的主要成分之一,还有一定的利尿作用。
③咖啡因作为兴奋剂、苦味剂、香料,主要供可乐饮料及含咖啡、饮料使用。
小剂量:振奋精神,减少疲劳。
大剂量:则有兴奋延脑生命中枢的作用,可使呼吸加深、加快,血压回升及血循环改善。
◆茶叶化学组成的一般含量:水分(75%)鲜茶叶无机化合物(3.5%--7%)干物质(25%)有机化合物(93%--96%)水溶性部分:2%--4%无机化合物(3.5%--7%)(茶叶高温灼烧、碳水不溶性部分:1.5%--3%化后剩下的灰烬)氨基酸:1--7%蛋白质:20--30%含N化合物生物碱:2--5%酶茶多酚:20--35%有机化合物(93%--96%)芳香物质:0.02%类脂:8%含C有机物糖类:20--30%有机酸:3%色素:1%维生素:0.6--1%◆茶叶中的主要成分及其作用:1、氨基酸:氨基酸是构建生物机体的众多生物活性大分子之一,是构建细胞、修复组织的基础材料对纺织早衰,促进生长和智力发育,增强造血功能,有着重要的作用。
咖啡因检验操作规程

咖啡因检验操作规程范围:本标准规定了咖啡因的检测方法和操作要求;适用于本公司咖啡因的质量检测。
二、引用标准:中华人民共和国药典(2000年版一部)三、质量标准:四、试剂:1、氯仿(AR)2、甲醇(AR)3、醋酐(AR)4、冰醋酸(AR)5、高氯酸(AR)五、仪器和用具1、熔点测定仪2、红外分光光度计3、紫外灯六、结构式和分子量 O H 3C 8H 10N 4O 2·H 2O 212.21七、操作步骤:1、性状 本品为1,3,7-三甲基-3,7二氢-1H-嘌呤-2,6-二酮-水合物。
按干燥品计算,含C 8H 10N 4O 2不得少于98.5%。
1.1 物理外观 本品为白色或带极微黄绿色、有丝光的针状结晶,无臭,味苦,有风化性。
1.2 熔点 本品的熔点(见熔点测定操作规程)为235~238℃。
2、鉴别2.1 取本品约10mg ,加盐酸1ml 与氯酸0.1g ,置水浴上蒸干,残渣遇氨气即显紫色;再加氢氧化钠试液数滴,紫色即消失。
2.2 取本品的饱和水溶液5ml ,加碘试液5滴,不生成沉淀;再加稀盐酸3滴,即生成红棕色的沉淀,并能在稍过量的氢氧化钠试液中溶解。
2.3 本品的红外光吸收图谱应与对照的图谱(光谱集250图)一致。
3、检查3.1 溶液的澄清度 取本品1.0g ,加水50ml ,加热煮沸,放冷,溶液应澄清。
3.2 有关物质 取本品,加氯仿-甲醇(3:2)制成每1ml 中含20mg 的溶液,作为供式品溶液;精密量取适量,加上述溶剂稀释成每1ml 中含0.10mg 的溶液,作为对照溶液。
照薄层色谱法(见薄层色谱法检验操作规程)试验,吸取上述两种溶液各10ul ,分别点于同一硅CH 3H 2O胶GF薄层板上,以正丁醇-丙酮-氯仿-浓氨溶液(40:30:30:10)为展开剂,展开后,取出,254晾干,在紫外光灯(254nm)下检视。
供试品溶液如显杂质斑点,与对照溶液的主斑点比较,不得更深。
茶叶中提取咖啡因和薄层色谱(最全版)PTT文档

占1~5%,与茶碱和可可碱共存于茶叶中,另外还 7、本实验在制备薄层色谱用的试样溶液时,如何确定粗
9、薄层板上点样时,需使用平口毛细管与薄层轻轻接 小心取下漏斗,揭开滤纸,用刮刀将纸上和器皿周围的咖啡因刮下。
含 有 回答思考题2、 3、
定性分析的原理。
棉花团
滤纸筒高度要 高于虹吸管低 于蒸气上升管
2、升华提纯
四分法取出1/4粗产品,其余置蒸
发皿中,将口径合适的玻璃漏斗(颈 部塞一小团棉花)罩在隔以刺有许多
滤纸上的 孔刺向上
小孔滤纸的蒸发皿上,用酒精灯小心
加热升华。当滤纸上出现许多白色毛
状结晶时,停止加热,让其自然冷却
至100℃左右。
小心取下漏斗,揭开滤纸,用刮 刀将纸上和器皿周围的咖啡因刮下。 残渣经拌和后用较大的火再加热片刻, 使升华完全。合并两次收集的咖啡因, 称重,计算产率。
试剂:
干茶叶,碳酸钠,氯仿,95%乙醇, 酸性碘-碘化钾溶液,乙酸乙酯。
材料:
毛细管,沸石,滤纸,脱脂棉 。
脂肪提取器
冷凝管
提取咖啡因的实验流程
提取器的滤纸筒 中:10g茶叶 圆底烧瓶中: 120mL 95%乙醇 和沸石3~3粒
提取2~3h
至提取液 颜色很浅
常压蒸馏 补加沸石
乙醇
烧瓶内 残留物
回收
操作注意事项
1、提取和常压蒸馏时要加入沸石,防止暴沸;先通入冷 却水,再加热。 2、滤纸筒直径略小于抽提筒,其高度要高于虹吸管,但 圆底烧瓶中:120mL 95%乙醇 和沸石3~3粒
5℃,味苦,在100℃时即失去结晶水,并开始升华,随温度升高升华加快。
低于蒸气上升管。 3、升华装置上盖的滤纸直径应大于蒸发皿,所用的玻璃
薄层色谱法实验报告

实验结果记录及分析
实验结果图
项目
组一
组二
药品
阿司匹林咖啡因混合样品
阿司匹林
荧光黄
碱性湖蓝
斑点移动距离a(cm)
溶剂移动距离b(cm)
Rf
实验注意事项
1、铺板时一定要铺匀,特别是边、角部分,晾干时要放在平整的地方。
2、点样时点要细,直径不要大于2mm,间隔0.5cm以上,浓度不可过大,以免出现拖尾、混杂现象。
(3)定位及定性分析
将点好样的薄层板分别放入装有二氯乙烷层析液和5%的乙醇溶液的两个广口瓶中,盖上盖子,待层析液上行至距薄层板上沿1cm左右时,有镊子取出,铅笔将各斑点框出,并找出斑点中心,用小尺量出各斑点到原点的距离和溶剂前沿到起始线的距离(点有阿司匹林的薄层板需用暖风机吹干),算各样品的比移值并定性确定混合物中各物质名称。
1-层析缸(广口瓶),2-薄层板,4-层析液
实验步骤
(1)薄层板的制备:
取3g硅胶G粉于研钵中,加相当于8ml左右的用5%的羧甲基纤维素钠(CMC)的水溶液,用力研磨1-2分钟,至成糊状后立即倒在准备好的薄层板中心线上,快速左右倾斜,使糊状物均匀地分布在整个板面上,厚度约为0.25mm,然后平放于平的桌面上干燥15分钟,再放入100℃的烘箱内活化2小时,取出放入干燥器内保存备用。
有机化学第二课堂实验报告
咖啡因检验操作规程

咖啡因检验操作规程1. 目的建立咖啡因检验标准操作规程,使咖啡因检验操作规范化。
2. 范围适用于咖啡因的质量检验。
3. 术语或定义N/A4. 职责质量控制部对本规程的实施负责。
5. 程序5.1 检验依据5.1.1 《中国药典》2020年版二部(第797页)。
5.1.2 咖啡因质量标准(质量标准编号)。
5.1.3 《中国药典》2020年版四部。
1.【性状】1.1本品为白色或带极微黄绿色、有丝光的针状结晶或结晶性粉末;无臭;有风化性。
本品在热水或三氯甲烷中易溶,在水、乙醇或丙酮中略溶,在乙醚中极微溶解。
1.2熔点依熔点测定法检验操作规程进行测定。
本品的熔点应为235~238℃。
2.【鉴别】2.1鉴别⑴2.1.1试药与试液盐酸、氯酸钾、浓氨溶液、氢氧化钠试液2.1.2仪器与用具天平(感量0.1g、0.1mg)、电热恒温水浴锅、蒸发皿、刻度吸管(1ml)2.1.3操作方法取本品约10mg,加盐酸1ml与氯酸钾0.1g,置水溶上蒸干,残渣遇氨气即显紫色;再加氢氧化钠试液数滴,紫色即消失。
2.2鉴别⑵2.2.1试药稀盐酸、碘试液、氢氧化钠试液2.2.2操作方法取本品的饱和水溶液5ml,加碘试液5滴,不生成沉淀,再加稀盐酸3滴,即生成红棕色的沉淀,并能在稍过量的氢氧化钠试液中溶解。
2.3鉴别⑶2.3.1仪器双光束红外分光光度计、压片机。
2.3.2操作方法取供试品约1mg,置入玛瑙研钵研细,再取溴化钾粉(约200mg),在玛瑙研钵中充分研磨混匀,移置于直径13mm的压模中,使铺布均匀,加压至20MPa,约60秒取出。
目视检查应均匀,无明显颗粒。
将供试片置于仪器的样品光路中,进行光谱扫描。
供试品的红外光吸收图谱应与对照的图谱(光谱集1289图)一致。
3.【检查】3.1溶液的澄清度3.1.1仪器与用具天平(感量0.1g)、电炉、烧杯(100ml)、量筒(50ml)3.1.2操作方法取本品1.0g加水50ml,加热煮沸,放冷,溶液应澄清。
用薄层色谱法鉴定咖啡因

用薄层色谱法鉴定咖啡因
2、薄层色谱法对APC各组分的分离鉴定实验操作及现象
(1)点样:点样前,先用铅笔在薄层板上距末端0.6~1cm处轻轻画一横线,等距点上三点,再在薄板的另一端距末端约1cm处轻轻画上一横线,然后用毛细管依次分别吸取咖啡因、阿司匹林、乙酰水杨酸轻轻点样在已画好的点上,干燥后可进行色谱展开。
(2)展开:将事先选好的展开剂(苯:乙醚:冰醋酸:甲醇=120:60:18:1)放入干净小烧杯内展开剂的深度达0.5~1cm即可,再放入点好样品的薄层板,用表面皿盖好烧杯,使样品在杯内进行展开分离。
当展开剂上升到预定的位置时(上步中画好的横线),立即取出薄层板并尽快用铅笔在展开剂上升的前沿处画一横线作标记,在水平位置上风干,然后在红外灯下烘干冰醋酸。
(3)鉴定:a.显色:将烘干的薄层板放入254nm紫外分析仪中照射显色,可清晰地看到展开得到粉红色斑点。
b.定位:定出多点的相对位置,量出斑点中心到原始点的距离及展开剂前沿到原始点中心的距离,计算Rf值。
c.确定镇痛药APC的成分:通过Rf值的分析结果,课确定相应的组分。
展开剂液面要在点样线一下,不能超过;薄层板取出后要及时标记展开剂的前沿,否则展开剂挥发后难以确定;其中APC是三个点。
Rf=物质移动距离/溶剂移动距离。
CMOS法测定咖啡因含量的探究

第42卷第2期肇庆学院学报V ol.42,No .22021年3月JOURNAL OF ZHAOQING UNIVERSITYMar.2021CMOS 法测定咖啡因含量的探究郑静,涂雪元,马德运(肇庆学院食品与制药工程学院,广东肇庆526061)摘要:本实验利用薄层色谱分离咖啡因,在紫外灯254mm 条件照射下,反射不同程度的荧光强度,然后再利用CMOS 设备如手机摄像头把光信号转化为电信号,Photoshop 软件按照畸变矫正—灰度模式—抠选样品点—反相处理—导出数据的流程处理,尽量排除其它因素的影响,用样品点的灰度参数反应咖啡因的含量.实验证明,样品点经过处理后的灰度与咖啡因的含量呈良好的线性关系,R 2=0.9906,由线性拟合曲线可得出待测品中咖啡因的含量.本实验方法实验条件要求简单,操作简便,可现场快速测定咖啡因的含量.关键词:咖啡因;薄层色谱;UV ;CMOS ;灰度中图分类号:O652.1文献标志码:A文章编号:1009-8445(2021)02-0057-05收稿日期:2020-11-29基金项目:肇庆学院青年科研项目(201913)作者简介:郑静(1989-),女,河南商丘人,肇庆学院食品与制药工程学院教师,硕士.通信作者:马德运(1980-),男,广东梅州人,肇庆学院食品与制药工程学院副教授,博士.咖啡因的定量检测最早采用滴定法,该方法对于操作者的要求高且操作条件复杂,稍不注意就会引起误差,测定结果准确性低.而薄层层析-紫外分光光度法的缺点是不同人员操作结果不同,人为的干扰因素较大,还有就是刮板的干净度,洗脱程度,会造成偏差较大,降低准确度[1-4].高效液相色谱法是目前准确判定咖啡因含量的国际通用方法,但需要特殊的昂贵仪器,且前处理过程繁琐,不适用于现场快速测定咖啡因含量[5-9].薄层色谱法是一种微量分离方法,与高效液相色谱法相比,薄层色谱法具有相对操作程序简单、分析速度快、成本低、溶剂消耗少等优点[9-13].CMOS (Complementary Metal Oxide Semiconductor )是互补金属氧化物半导体的缩写,可应用于数字影像领域.现在手机摄像头都为CMOS ,可把光信号转化为电信号的形式.为了把电信号量化,我们引入一个灰度的概念.由于景物各点的颜色及亮度不同,摄成的黑白照片上或电视接收机重现的黑白图像上各点呈现不同程度的灰色,把白色与黑色之间按对数关系分成若干级,称为“灰度等级”,范围一般从0到255,白色为255,黑色为0,故黑白图片也称灰度图像.在本实验中,图片处理后选用灰度作为参考数据.图片可以用由0-255的灰度像素组成,并且每个灰度都有一定数量的像素,即频数.总灰度=∑0255像素个数由于现有的咖啡因检测手段存在着操作复杂,或者仪器昂贵,费时费力的问题,本实验将咖啡因通过薄层色谱分离出来,在紫外灯254mm 照射下,产生荧光,利用CMOS 拍摄,Photoshop 软件处理图片,导出相关数据,探究咖啡因含量与各参数之间的关系[13-16].本实验方法准确度较现有方法稍差,但是操作简便,设备普通,成本低廉,省时省力,因此适用于现场快速检测咖啡因含量.1实验部分1.1仪器与试剂电子天平(AG135、AB204-N 、CPA3245),玻璃点样毛细管(内径0.3mm ),硅胶板(GF245),紫外分析仪58肇庆学院学报第42卷(ZW-3),计算机(Adobe Photoshop软件CS6).甲醇(分析纯/500mL,西陇化工股份有限公司);三氯甲烷(分析纯/500mL,广州化学试剂厂);咖啡因(纯度99.9%,广州化学试剂厂)1.2咖啡因标准品溶液的配制用电子天平称取0.01g咖啡因,置于烧杯中,加蒸馏水溶解.再转移到10mL的容量瓶中定容,得到0.001g/mL的咖啡因标准品.按照上述方法分别配制出0.005g/m、0.0025g/mL、0.002g/mL、0.001g/mL、0.0005g/mL的咖啡因标准品.1.3实验条件探究将咖啡因样品点于硅胶板,用展开剂展开.将展开的硅胶板置于254mm紫外分析仪下,利用手机摄像头拍摄,把咖啡因的光信号转化为电信号,储存于电脑,利用Photoshop软件打开该样品图片进行处理.1.3.1探究GF板摆放位置的影响截取一段2cm的玻璃点样毛细管,吸取2mL浓度为0.001g/mL的咖啡因,点于6cm×5cm的GF板上,等距点5个样品点,命名为板1.待样品点干燥后,置于展开液(三氯甲烷:甲醇=9:1)中展开.展开完成后晾干做下一步处理.鉴于紫外分析仪的光源,造成紫外光度不一样,就会导致薄层板上样品点对光的吸收强度或者被光激发后产生的荧光强度不同,会对实验结果造成影响.在摆放台上找到一个光源最集中的位置,标为光源焦点位置;除此之外的其余位置为光源焦点外位置.将板1置于光源焦点位置,拍摄照片.将板1置于光源焦点外位置,拍摄照片.按照灰度模式—抠选样品点—分析记录的流程处理分析图片.1.3.2探究样品点于不同板与同块板的影响截取一段2cm的玻璃点样毛细管,吸取2mL浓度为0.001g/mL的咖啡因,点于1cm x5cm的GF板上,分别点5块.5块分开板命名为板1’.待样品点干燥后,置于展开液三氯甲烷:甲醇为9:1中展开.展开完成后晾干做下一步处理.将板1’和板1置于光源焦点位置拍摄.按照灰度模式—矩形工具抠选样品点—分析记录的流程处理分析图片.1.3.3探究不同抠图工具的影响将板1于1.3.1拍摄图片调为灰度模式,用矩形工具处理抠取选取样品点,导出数据分析;将板1于1.3.1拍摄图片调为灰度模式,用魔棒工具(容差值30)抠选样品点,导出数据分析.1.3.4探究畸变矫正对于实验的影响将板1于1.3.1拍摄图片利用透视剪裁工具进行图片的畸变矫正,调为灰度模式,用矩形工具抠选样品点,导出数据分析.与未做畸变矫正处理的实验数据对比.1.3.5探究反相处理对于实验的影响将板1于1.3.1拍摄图片利用透视剪裁工具对图片做畸变矫正处理,调为灰度模式,用矩形工具抠选样品点,图片进行反相处理,导出数据分析.与未做反相处理的实验数据对比.1.3.6探究环境光对于实验的影响把板1置于光源聚焦位置,打开实验室日光灯的条件下拍摄;把板1置于光源聚焦位置,在黑暗环境的条件下拍摄.把两组照片在Photoshop软件中打开,做畸变矫正处理,调为灰度模式,矩形工具抠选样品点,反相处第2期郑静等:CMOS法测定咖啡因含量的探究理,导出数据分析处理.1.3.7探究不同曝光参数对于咖啡因含量测定的影响把板1置于光源聚焦位置,在黑暗环境的条件下拍摄2次.把两组照片在Photoshop软件中打开,做畸变矫正处理,调为灰度模式,矩形工具抠选样品点,反相处理,导出数据分析处理.1.4探究不同参考标准的区别把板1置于光源聚焦位置拍摄的图片打开,做畸变矫正处理,调为灰度模式,用矩形工具处理抠取选取样品点,反相处理后导出数据总灰度、灰度中间值,灰度峰总值分析.以总灰度、中间灰度值、灰度峰总值为参数之间的差异.1.5测试茶叶中咖啡因的含量用电子天平称取8.0043g茶叶,泡于50mL的蒸馏水中,煮沸,过滤,待茶水冷却至室温时,用毛细玻璃管取2mL滤液,点于硅胶板.用玻璃点样毛细管分别取2mL浓度为0.0005g/ml、0.002g/mL、0.005g/mL的咖啡因标准溶液点于同一块硅胶板,样品点之间间隔1cm.置于展开液展开,在黑暗条件下拍摄,按实验流程处理图片,利用咖啡因标准溶液绘制标准曲线,再求出滤液中咖啡因含量.2实验结果与分析2.1实验的影响因素影响实验的因素以及显著性可以归纳为表1:表1影响因素的显著性影响因素显著性位置**板块**抠图工具**畸变矫正处理**反相处理**环境光*曝光系数-通过实验结果发现,GF板摆放位置、分开板与同块板、抠图工具、畸变矫正、反相处理、环境光等因素对于样品点的总灰度有显著影响;但在相同的拍摄条件下,拍摄的参数对最终的总灰度无显著影响.P值为0.9052,拒绝原假设曝光系数对于实验结果的影响显著的概率为0.9052,所以曝光系数对于样品点总灰度影响不列入统计范围.因此,拍摄时无需特别调试拍摄参数.2.2探究不同参数对于实验结果的适用范围影响实验选取灰度峰总值、中间灰度值、总灰度值为参数,论证咖啡因的含量和不同参数之间的关系.灰度峰总值=像素max×灰度值中间灰度值=灰度的中位数总灰度=∑0255像素数量按照1.4的实验操作流程得到表2.表2不同参数数据影响因素灰度峰值中间灰度值总灰度平均值19658148.2692730方差473564685.279731832.22RSD35.01%1.54%1.29%F18354.88P-value1.2177E-21如果从方差的角度分析,灰度中间值<灰度峰总值<总灰度,灰度中间值的波动最小.如果从变异系数的59肇庆学院学报第42卷角度分析,总灰度<灰度中间值<灰度峰总值,且灰度峰总值的变异系数大于15%,数据不稳定,可重复性弱,不适宜用作定量依据.中间灰度值和总灰度作为参数,从RSD值来分析,都是可取的.因此需对2个参数进行线性拟合分析. 2.3探究不同参数下的标准曲线2.3.1探究同浓度不同体积的不同参数的标准曲线根据实验操作流程,得到同浓度不同体积的不同参数的数据.1)用物质的量作为横坐标,灰度平均值作为纵坐标,绘制出标准曲线,得y=96249x+129.8,R2=0.9906,接近1,表明中间灰度值与物质的量存在一定的线性关系.2)用物质的量作为横坐标,总灰度值作为纵坐标,绘制出标准曲线,得y=5E+08x+991105,R2=0.9959,接近1,表明总灰度值与物质的量存在一定的线性关系.对比2个以不同参数绘制的标准曲线,总灰度—物质的量的回归线方程斜率大于中间灰度值—物质的量的回归线方程斜率,相同单位的浓度变化,总灰度的变化值更大.以总灰度作为咖啡因含量参数的参考标准,响应更为灵敏,提高实验结果的精度.2.3.2探究总灰度值与咖啡因物质的量标准曲线根据实验操作流程,得到同体积不同浓度的不同参数的数据.用物质的量作为横坐标,总灰度值作为纵坐标,绘制出标准曲线,得y=5E+08x+893587,R2=0.9817,接近1,表明总灰度值与物质的量存在一定的线性关系.在实际检测中,我们需要用咖啡因标准品的物质的量和总灰度建立标准曲线,再求出待测咖啡因样品的总灰度,代入回归方程,即可求出待测品的咖啡因物质的量.2.3.3测试茶叶中咖啡因的含量根据1.5的实验操作流程,得到以下数据如表3所示.表3滤液中咖啡因含量测定数据样品点滤液C/(g∙mL-1)未知L/cm2m/g未知S/cm27520平均灰度值129.2428总灰度971905根据表3中的数据,由线性拟合曲线y=5E+08x+893587可得,滤液中咖啡因含量为0.000144g,由物质的量=浓度×毛细管长度×毛细管横截面积可得,茶水中咖啡因的浓度为0.001g/mL,再根据1.5中的取样可得每克茶叶含咖啡因0.0062g.3总结本实验的操作条件为黑暗的环境,标准品点于同一块硅胶板,样品点也同样点于同一块硅胶板,做好数据记录.在紫外分析仪下有荧光现象.寻找光源聚焦位置拍摄,再用Photoshop软件处理,畸变矫正,灰度模式,样品点区域的抠取,反相处理,分析测量样品点的总灰度值,便可以绘制相应的标准曲线.把待测样品点总灰度求出,代入标准曲线,就可以粗略求出样品点咖啡因的含量.现今检测手段多种多样,每种检测手段存在着各自的优势以及劣势.本检测手段的优点是设备简便,省时省力,可现场快速检测咖啡因含量.而缺点就是准确度较一般,若需要准确测量样品中咖啡因的含量,则需要与其他检测方法配合使用.60第2期郑静等:CMOS法测定咖啡因含量的探究61参考文献:[1]LONGGANG G,SHUAI S,HE L,et al.,primary study of novel method for determination of saponin in ziziphi spinosae se-men(Suan-Zao-Ren)by digitally scanning the photo of the HPTLC image without configuration of TLC scanner facility[J].Chinese Medicine,2014,5:211-217.[2]赵卫星,姜红波,冯国栋.茶叶中咖啡因的提取研究进展[J].化学与生物工程,2010,27(9):17-20.[3]罗由萍,邓鹏飞.薄层色谱及其在药用植物研究中的应用[J].安徽农业科学,2011,39(6):3309-3312.[4]张凤,迟逸仙,张景如,等.茶叶中咖啡因含量的薄层色谱扫描测定方法的建立[J].食品科技,2011,36(2):265-269.[5]高玲,胡克勤,高志华.分光光度法测定溴咖合剂中咖啡因含量[J].遵义医学院学报,2007,30(4):527-529.[6]刘臣,唐长波,姚丽萍,等.高效液相色谱法测定碧螺春茶叶中的咖啡因含量[J].江苏农业学报,2012,28(4):877-879.[7]徐学笛.高效液相色谱法测定咖啡因含量的研究与探讨[J].科技成果纵横,2008(6):60-61.[8]卢金清,戴艺,梁欢,等.可可粉中可可碱和咖啡因的TLC鉴别及HPLC法含量测定[J].食品工业,2013,34(12):185-188.[9]刘清华.紫外分光光度法测可乐中咖啡因的含量[J].广东轻工,2013,19(261):158-167.[10]孙延春,张英.紫外光谱法测定饮料中的咖啡因含量[J].化学研究,2011,22(1):77-79.[11]姜彬.蛋白质免疫印记分析法实验条件的研究[J].实验技术与管理,2008(5):53.[12]金茂俊,邵华,金芬,等.化学发光免疫分析方法的研究及应用[J].农产品质量与安全,2012(2):42-46.[13]汪晨,吴洁,宗晨,等,化学发光免疫分析方法与应用进展[J].分析化学,2012,1(40):3-10.[14]宗晓明,李继峰,肖伯涛.基于Image J的球铁石墨定量分析[J].铸造设备与工艺,2013,10(5):21-24.[15]方会龙,曾庆仁,王俊杰,等.运用QuantityOne软件分析日本血吸虫不同发育时期蛋白组分差异[J].中国血吸虫病防治,2010,22(4):320-323.[16]舒锡婷,欧阳娜,江昌俊,等.茶树叶片类脱水素蛋白的Western-blot分析[J].西北植物学报,2015,35(12):2448-2454.Study on the Determination of Caffeine by CMOS MethodZHENG Jing,TU Xueyuan,MA Deyun(School of Food and Pharmaceutical Engineering,Zhaoqing University,Zhaoqing,Guangdong526061,China) Abstract:In this study,caffeine was separated by thin-layer running board,and the fluorescence intensity was reflected at different wavelengths of254mm.In the use of CMOS devices such as mobile phone camera to convert optical signals into electrical signals,Photoshop software exported data in accordance with the distortion correction-gray mode-pull the sample point-reverse processing,the process of which tried to exclude the im-pact of other factors.The grayscale parameter responded to the content of caffeine.Experiment results show that the sample gray and caffeine content after the treatment revealed a good linear relationship,R2=0.9906.And the content of caffeine can be obtained by linear fitting curve.The condition requirements of this experiment are sim-ple,and it is easy to operate,and the on-site caffeine content can be quickly measured.Keywords:caffeine content;thin layer chromatography;UV;CMOS;grayscale(责任编辑:张宝杰)。
从茶叶中提取咖啡因及薄层色谱法对APC各组分的分离鉴定

广州大学化学化工学院本科生综合实验报告实验课程有机化学基础实验合成实验项目从茶叶中提取咖啡因及薄层色谱法对APC各组分的分离鉴定专业化学工程与工艺班级12化工2学号1205200087 姓名王伟指导教师刘莹开课学期2012 至2013 学年第二学期实验时间2013年4月12日.目录从茶叶中提取咖啡因 (2)∙实验目的 (2)∙实验原理 (2)∙实验仪器及装置图 (4)∙实验步骤及现象 (4)∙注意事项 (5)∙实验试剂及相关物理常数 (5)∙祖产品纯化流程图 (6)∙实验结果分析结果分析与讨论 (7)∙思考题 (7)薄层色谱法对APC各组分的分离鉴定 (9)∙实验目的 (9)∙实验原理 (9)∙实验仪器及装置图 (11)∙实验试剂及相应化合物的物理常数 (11)∙实验步骤及现象 (11)∙实验结果与数据处理 (12)∙参考文献 (12)从茶叶中提取咖啡因一、实验目的1.学习天然物的提取技术和鉴定知识;2.掌握从茶叶中提取咖啡因的方法、索氏提取器的原理和操作;3.掌握利用升华方法纯化固体产物的原理和基本操作。
二、实验原理咖啡因咖啡因的分子结构式性质描述:咖啡因属于甲基黄嘌呤的生物碱。
纯的咖啡因是白色的,强烈苦味的白色粉末或六角棱柱状结晶。
它的化学式是C8H10N4O2。
它的化学名是1,3,7-三甲基黄嘌呤或3,7-二氢-1,3,7三甲基-1H-嘌呤-2,6-二酮。
分子量,194.19。
熔点238°C,178°C 升华。
1g咖啡因溶于46ml水、5.5ml 80°的水、1.5ml沸水、66ml乙醇、22ml 60°的乙醇、50ml 丙酮及5.5ml 氯仿等。
作用与应用:咖啡因是从茶叶、咖啡果中提炼出来的一种生物碱,适度地使用有祛除疲劳、兴奋神经的作用,临床上用于治疗神经衰弱和昏迷复苏。
咖啡因有时也与其他药物混合提高它们的功效。
咖啡因能够使减轻头痛的药的功效提高40%,并能使身体更快的吸收这些药品缩短起作用的时间。
有机化学综合性实验(咖啡因的提取及鉴定)

注意事项 提取时间主要依据萃取 溶剂的颜色判断,当颜 色较淡时,即大部分物 质已被萃取到溶剂内 了,此时可停止萃取。
安装好蒸馏装置, 重新加入几粒沸石, 进行蒸馏,蒸出大部分乙醇(要回收)。 残液(约 5~10ml)趁热倒入蒸发皿中, 加入 4g 研细的生石灰粉, 在玻璃棒不 断搅拌下将溶剂蒸干。
有无色液体经冷凝器流入锥形 瓶中。 墨绿色液体渐渐变得粘稠, 至干 爽的绿色粉末,并伴有茶香。
复方阿司匹林研细后用二氯甲烷与水 层析液不断上升; 混合搅拌, 分液后用无水硫酸镁干燥, 显色时有五个斑点在层析板上。 取清液用毛细管点样。阿司匹林与咖 啡因用二氯甲烷溶解后点样。 在展开缸中倒入少量展开液,盖好玻 璃盖,待展开液上升至一定高度记录 风干。 显色,定位。
点样前,用铅笔在层析 板据末端 1cm 处轻轻画 一条横线;用毛细管点 样,动作须轻快敏捷, 若需重新点样,要等前 次溶液挥发后; 样与样、 样与薄层板边缘保持一 定距离。
1
六、粗产物纯化流程
2
七、结果分析与讨论 1.产品分析及产率计算 咖啡因实际产量:0.11g; 理论产量:0.25g; 产率:44.00% R 咖啡因=0.43 R 乙酰水杨酸=0.84 复方 APC:R1=0.34,R2=0.67, R3=0.85
2.对实验现象、实验结果的分析及其结论
咖啡因晶体呈白色针状,大小均匀,在收集的滤纸上呈放射状分布。 层析时分离的五个斑点分离明显,较成功。 3.本实验的成败、关键环节及改进措施 总的来说,这次试验是成功的,所制咖啡因晶体为白色针状,质量 0.11g,产率为 44%;Rf 值与理论相差不大。产率较低,原因可能是升华不完全,有一些近晶体没有升 华出来留在了蒸发皿里,蒸干溶剂时有部分咖啡因流失,并漏斗覆盖不严密至一些咖啡 因流失。在做层析时,点样量过少,以至显色时不是很明显。 改进措施:加入石灰粉后蒸发时,应严格控制反应温度,以防部分晶体升华造成的 产率过低;点样时在注意快捷迅速的同时,要注意留在层析板上的溶质的量,量少时须 多次点样。
薄层层析—紫外分光光度法测定抗感灵片中咖啡因的含量

薄层层析—紫外分光光度法测定抗感灵片中咖啡因的含量曾仁乾;陆星;章小力;王益平
【期刊名称】《华西药学杂志》
【年(卷),期】1989(4)2
【摘要】解热镇痛药中一些复方制剂含有咖啡因和扑尔敏。
咖啡因的含量测定多采用剩余碘量法,由于扑尔敏有干扰,碘量法测定结果。
【总页数】3页(P108-110)
【关键词】抗感灵片;咖啡因;薄层层析
【作者】曾仁乾;陆星;章小力;王益平
【作者单位】万县地区药品检验所
【正文语种】中文
【中图分类】R927
【相关文献】
1.薄层析-紫外分光光度法测定川芎中阿魏酸含量 [J], 苏秀兰;杨倚麟
2.薄层层析-紫外分光光度法测定蒙药三子散中栀子甙含量 [J], 王烈群;屈爱桃;马彦彪;杨冬丽;朱庆玲
3.采用薄层层析—紫外分光光度法测定广西不同产地黄花蒿中青蒿素含量 [J], 李典鹏;梁小燕;陈秀珍
4.薄层层析-紫外分光光度法测定延胡索中延胡索乙素含量 [J], 徐丹丹;偶志红;曲婷丽;刘锐玲
5.薄层层析-紫外分光光度法测定延胡索中延胡索乙素含量 [J], 徐丹丹; 偶志红; 曲婷丽; 刘锐玲
因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2、薄层色谱法对APC各组分的分离鉴定实验操作及现象
(1)点样:点样前,先用铅笔在薄层板上距末端0.6~1cm处轻轻画一横线,等距点上三点,再在薄板的另一端距末端约1cm处轻轻画上一横线,然后用毛细管依次分别吸取咖啡因、阿司匹林、乙酰水杨酸轻轻点样在已画好的点上,干燥后可进行色谱展开。
(2)展开:将事先选好的展开剂(苯:乙醚:冰醋酸:甲醇=120:60:18:1)放入干净小烧杯内展开剂的深度达0.5~1cm即可,再放入点好样品的薄层板,用表面皿盖好烧杯,使样品在杯内进行展开分离。
当展开剂上升到预定的位置时(上步中画好的横线),立即取出薄层板并尽快用铅笔在展开剂上升的前沿处画一横线作标记,在水平位置上风干,然后在红外灯下烘干冰醋酸。
(3)鉴定: a.显色:将烘干的薄层板放入254nm紫外分析仪中照射显色,可清晰地看到展开得到粉红色斑点。
b.定位:定出多点的相对位置,量出斑点中心到原始点的距离及展开剂前沿到原始点中心的距离,计算Rf值。
c.确定镇痛药APC的成分:通过Rf值的分析结果,课确定相应的组分。
展开剂液面要在点样线一下,不能超过;薄层板取出后要及时标记展开剂的前沿,否则展开剂挥发后难以确定;其中APC是三个点。
Rf=物质移动距离/溶剂移动距离。
