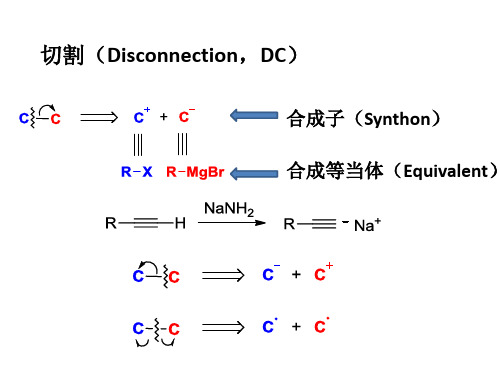
合成子
常用于有机合成的反应
O N CH3 + CH3OH
羰基化合物的亲核加成
3. Sandmeyer反应
2.
利用分子的对称性,最大程度简化分子的结构;
3. 借助官能团转化,导向已知的反应; Functional Group Interchange, FGI
4. 添加合适官能团,导向已知的反应; Functional Group Addition, FGA
试推测A和C的结构。
从鱼油中分离得到一种天然化合物A,其分子式为C19H38。 A经催化氢化生成2,6,10,14-四甲基十五烷,经臭氧化-还
原生成丙酮和一种16个碳的醛B。试推测A和B的结构。
化合物A分子式为C6H13Br,在制成格氏试剂后与丙酮反应水 解得到2, 4-二甲基-3-乙基-2-戊醇。A在CH3ONa作用下生成分 子式为C6H12的烯烃B;B在OsO4作用下生成C;C与高碘酸反应 得到一个醛D和一个酮E,写出A,B,C,D,E的结构式。
有一种芳香醛和丙酮可在碱作用下,生成化合物A(C12H14O2)。 A经碘仿反应后生成化合物B(C11H12O3)。B经催化下加氢可 生成C。B、C经氧化均可生成化合物D(C9H10O3)的。D经HI处 理后可生成邻羟基苯甲酸。推测A、B、C、D的结构。
试画出下列各反应的机理
CO2CH3 + O CH3NH2 O
5. 重组碳骨架,导向已知的反应 Reconnection, RC
6. 重新分布碳骨架,导向已知的反应 Redistribution, RD
重要反应
1. Diels-Alder [2+4] cycloaddition:产物:环己烯
立体选择性:同面加成
立体选择性:endo为主
区域选择性:
药物合成反应习题及答案

药物合成反应习题及答案一、举例解释下列概念:1, 官能团保护;为什么保护?当分子中有多个官能团,想在某一官能团进行转换反应,为了不使其他官能团影响反应,需对这些官能团进行衍生化,这就是官能团的保护。
达到反应目的后再还原这些官能团。
理想保护基:试剂易得、无毒,保护基稳定,引入和脱去反应选择性好,收率高。
2, 相转移催化剂; 一种与水相中负离子结合的两性物质,可以把亲核试剂转移到有机相进行亲核反应。
相转移催化剂优点:克服溶剂化作用;不需无水操作;可用无机碱代替有机金属碱;降低反应温度。
3,重排反应;重排反应是指在同一分子内,某一原子或基团从一个原子迁移至另一原 子而形成新分子的反应。
按反应机理可分为亲电重排、亲核重排、自由基重排和协同重排。
4,合成子;合成子:组成靶分子或中间体骨架的各个单元结构的活性形式. 包括:离子合成子、自由基或周环反应所需的中性分子。
离子合成子:包括 d 合成子和 a 合成子d 合成子: 亲核性的离子合成子 d---donor of electrond 合成子CN KCNCH 2-CHO CH3CHOMeSHMeS RCH C RCH CHBu BuLi等价试剂a 合成子:氧化性或亲电性的离子合成子 a 合成子:Me 2C-OH Me 2C=OCH 2COCH 3BrCH 2COCH 3CH 2-CH-COOR CH 2=CH-COOR等价试剂5,协同反应协同反应:在反应过程中,若有两个或两个以上的化学键破裂 和形成时,都必须相互协调地在同一步骤中完成。
6, 非均相催化氢化: 催化剂、反应物、试剂和氢供体在两项或多项中反应,催化剂自成一相,称为非均相催化氢化。
催化剂自成一相称为非均相催化剂如Pd/C 为催化剂, 氢气为氢供体,在反应液中还原双键的反应。
1) DMAP 2) DMF 3) DCC 4) TBAF1) Aromatic Electrophilic Substitution; 芳香亲电取代2) Phase-transfer catalyst; 相转移催化剂 3) Carbocations; 碳负离子4) trifluoroacetic anhydride.三氟乙酸酐Ryoji Noyori was awarded the Nobel Prize in 2001, What did he discover?Ryoji Noyori 日本名古屋大学的野伊良治因在手性催化氢化反应方面做出了突出贡献而被授予2001年Nobel 化学奖。
合成化学第七章

d2 RCH2CHO
不对称酮:区域选择性
O
低温、强碱
O
OH
-
O
OH-
高温、弱碱
② a合成子
RCl
O O
R+ + Cl-
a1
RCCl
O
RC+
OH
RCH a2 RCHClCOR
O
RCH
+
RCHCOR
+
OH
RCHCHR'
R R'
+
a3
RCH=CHCOR'
RCHCH2COR'
O FGI
O
O
OH
O
③ 官能团引入
FGA
COOCH3 COOCH3 FGA Ph COOCH3
Ph
OHC FGA O O COOCH3 O O COOCH3
OHC
+
O
O COOCH3
④ 官能团消去
O
FGR
O
FGR t Bu
t Bu
O
2 3 1 O Reaar NH 4 5 6 N-OH
FGI
O
例1
O
例5
CO2H
O
O
+ CO2H
CH2CO2H
H2CBr
C
CH
CH2(CO2Et)2
综合练习:试设计合成
O CO2Et Ph Ph
O CO2Et Ph Ph Ph O
O CO2Et Ph
O CO2Et + Ph
O Ph
O Ph
+
合成子的定义

合成子的定义
合成子是指在生物体内或外部产生的一种人工合成的化合物,具有相似或相同的结构和化学活性,可以替代天然化合物,在医学、化工、生物学等领域具有重要的应用价值。
合成子一般可以通过化学合成、生物合成等方法获得,属于一种纯粹的人工化合物。
合成子主要的应用是在药物研发和农业领域。
在药物研发方面,合成子是一种有益的工具,能够用于药物的设计、开发和优化。
由于生物活性的高度可控性和改性的灵活性,合成子可以通过结构上的设计来提高药物的特异性、抗药性和生物利用度。
特别是在疾病治疗中,合成子已成为一种重要的工具,被广泛应用于癌症、感染病、心血管病等疾病的治疗。
在农业领域,合成子也发挥了重要作用,其主要应用于化学农药和生物农药的研发。
合成子能够通过改良和完善原有的化学结构,来提高农药的防治效果和作用时间,同时还能够增加农作物抗逆性和耐胁迫性。
与此同时,生物农药可以通过合成子来加强作用力和拓展杀虫范围,从而更好地实现生物防治。
总的来说,合成子的定义是一个比较广泛的概念,其含义不仅限于化学合成物,也包括天然的有机物、酶和蛋白质。
合成子的应用十分广泛,既用于药物开发,也逐渐应用到农业和其他工业领域。
这从一个侧面也反映了合成子技术在各个领域的应用前景非常广阔。
有机合成中的合成子

例1:苯基与氧处于交叉构象的位置
位阻小
O S O
大 S
CH3
O S
S
CH3
S
CH3
S
M eLi (T H F ,-5 0 o C )
Li
中
H
小
+
H
H
H
Li
S
Ph Ph Ph
R (S , S ) 94% (R , S ) 6%
(S )-(+ )苄 基 , 甲 基 亚 砜
例2 叔丁基和苯处于对位。去质子发生在亚甲基上位阻最小 的部位。
空间位阻大的碱:
(CH3)3C OK
(CH3CH )2 NLi CH3
KOBut
特丁醇钾
(LDA)
二异丙基氨化锂
Me3Si Me3Si
N Li
双(三甲硅烷基)氨化锂
H2N
NH K
KAPA
3-氨基丙氨钠
O Li
1,1-二(三甲基硅烷基)-3-甲基丁醇锂
SiMe3 SiMe3
N M e2
CH2
CH
d
COOR
C C
2 3
COOR
H C C COOR
LDA
Li
C C COOR
1
O
ButLi
OSiR3
d
OSiR3
三、接受电子合成子及等效试剂
等效试剂
a
R
R X
(X= Cl, Br,I, OTs, OMe3 等)
烷基合成子
M e 3S X
硫鎓盐
M e3O B F4
R A lC l 4
(F rie d e l-C ra fts 烷 基 化 )
药物合成重要反应

药合名词解释和重要反应(广医药学)一、名词解释1、靶分子:(Target Molecule):就合成设计而言,凡是所需合成的有机分子均可成为“靶分子”,或者是最终产物,或者是有机合成中的某一个中间体。
2、合成子(Synthons):反合成分析时,目标分子切割成的片段(Piece)叫合成子3、逆合成分析:也称为反合成分析,即由靶分子出发,用你想切断、连接、重排和官能团互换、添加、除去等方法,将其变换成若干中间产物或原料,然后重复上述分析,直到中间体变换成所有价廉易得的和橙子等价试剂为止。
4、化学选择性:取决丁不同官能团的反应差异。
区域选择性:取决丁活性基团周围不同位置的反应性差异。
5、立体选择性:涉及产物分子的相对或绝对立体化学问题。
6、逆向切断(dis):用切断化学键的方法把靶分子骨架剖析城不同性质的合成子,成为逆向切断。
7、逆向官能团转化(con):在不改变靶分子基本骨架的前提下变换官能团的性质或所处位置的方法,包括逆向官能团转换(FGI)、逆向官能团添加(FGA)和逆向官能团除去(FGR)。
8、等价物(Equivalent):与合成子相对应的化合物。
9、切断(disconnection):目标化合物剖析的一种处理方法,想象在目标分子中有价键被打断,形成碎片,进而推出合成所需要的原料。
二、重要的化学反应(包括名解)1、卤化反应:在有机化合物分子中简历碳-卤键的反应称为卤化反应。
2、轻化反应:用轻基取代有机分子中的氢原子,包括在某些官能团或碳架上的氢原子,均称轻化反应。
3、酰化反应:在有机化合物分子中的碳、氧、氮、硫等原子上引入酰基的反应。
4、缩合反应:两个或多个有机化合物分子通过反应形成一个新的较大分子的反应或同一个分子发生分子内的反应形成新分子都可称为缩合。
5、重排反应:在同一分子内,某一原子或基团从一个原子迁移至另一个原子而形成新分子的反应。
6、氧化反应:有机物分子中氧原子的增加,氢原子的活除,或者两者兼而有之,不包括形成C-X、C-N、C-S的反应。
合成子与极性转换

不饱和吸电子基团影响α-碳上碳氢键的活化
a合成子,产物无官能团。
合成子的加合——a合成子与d合成子的反应
烷基a + 烷基d:
CH3Li
+ (CH3)3SBr
(a)
CH3CH3
+
(CH3)2S +
LiBr
(d)
产物为无官能团化合物。
a1 + d1:
R H OH OH
[H]
+
HCN
R
CN
H
R
NH2
(a1)
(d1)
产物为1,2-双官能团化合物。
反应机理:
因此:
CN
HO
C
-
O
是
的等价物
Example 2:二噻烷碳负离子的形成
醛(如乙醛)可以和1,3-丙二硫醇形成二噻烷。由 于硫对碳负离子具有特殊的稳定性,故邻位的碳有
酸性,用正丁基锂在低温四氢呋喃中处理,得到相
应的亲核性碳负离子。该锂化的碳负离子作为亲核 试剂,可以和卤代烃(溴化苄)、其他羰基化合物 (环己酮)以及环氧乙烷衍生物(苯基环氧乙烷) 等合成子发生亲核取代,生成的产物水解,又得回
的等价物。
合成子极性转换的具体应用
Example 1:安息香缩合反应
安息香缩合是羰基极性转换的代表,也是人们最早知道的极性转 换的例子。反应物苯甲醛中的羰基碳原子是亲电性的。首先发生 氰离子对羰基碳的亲核加成,然后质子由碳转移到氧上,形成一 个碳负离子,其中的碳发生了极性转换,是亲核性的。然后该碳 原子亲核进攻另一分子的苯甲醛的亲电性羰基碳,质子转移,氰 离子离去,得到产物安息香。
O H 3C H O
药物合成名词解释

药物合成名词解释 TYYGROUP system office room 【TYYUA16H-TYY-TYYYUA8Q8-名词解释1、苄位卤取代: 苄位氢原子被卤素原子取代2、烯丙位卤取代:烯丙位氢原子被卤素原子取代3、缺电子体系:含有空轨道的体系4、富电子体系:电子云密度高或含有未共用电子对的体系5、脱羧卤置换反应:羧酸脱去二氧化碳,生成比原产物少一个碳原子的卤代烃的反应6、卤交换反应:有机卤化物和无机卤化物之间进行卤素交换的反应7、S1反应:单分子亲核取代反应N2反应:双分子亲核取代反应8、SN9、NBA:N-溴代乙酰胺10、t-BuOH:叔丁醇11、t-BuOCl:次氯酸叔丁酯12、n-BuLi:正丁基锂B(p-2):在乙醇溶液中制备的硼化镍13、N i214、T sCl:对甲苯磺酰氯15、s-BuLi:仲丁基锂16、i-PrOH:异丙醇17、释电子基:能增加相邻基团电子云密度的基团18、还原胺化反应:羰基与胺加成脱水成亚胺,再还原为胺类化合物19、吸电子基:能减少相邻基团电子云密度的基团20、反应机理:反应发生的机制和道理21、邻苯二甲酰亚胺制胺法:邻苯二甲酰亚胺和卤代烃在碱性条件下反应,然后肼解得伯胺的反应22、α-羟烷基化反应:含有活性α-氢原子的醛酮,在碱或酸的催化下发生缩合,生成β-羟基醛或酮类化合物的反应23、B lanc反应:芳烃在甲醛、氯化氢和路易斯酸或质子酸的存在下,在芳环上引入卤烷基的反应24、β-羟烷基化反应:活性化合物与环氧乙烷发生反应,生成β-羟烷基化产物25、羰基烃化反应:醛、酮的羰基还原为亚甲基的反应26、β-羰烷基化反应:α,β不饱和羰基化合物在碱性催化剂存在下与亲核试剂发生缩合生成β-羰烷基化类化合物27、双烯合成:1,3-丁烯衍生物和乙烯衍生物在加热情况下生成环己烯骨架的反应28、活性亚甲基:邻位具有羰基或其他强吸电子基的亚甲基结构29、单线态:两个价电子自旋方向相反时,此种分子状态为单线态30、三线态:两个价电子自旋方向相同时,此种分子状态为三线态31、W ittig试剂:卤代物与三苯膦在碱作用下形成磷内盐32、化学氧化:利用化学试剂进行氧化O:乙酸酐33、A c234、(phCO)O:苯甲酸酐235、A cCl:乙酰氯36、B n2O2:过氧苄基醚37、A rOH:芳香酚38、S OCl2:二氯亚砜39、P E:石油醚40、E t3N:三乙胺41、C ollins氧化法:以三氧化铬吡啶复合物的二氯甲烷溶液作为氧化剂的方法42、J ones氧化法:以三氧化铬硫酸的丙酮溶液作为氧化剂的方法43、D DQ氧化法:以二氯二氰苯醌作为氧化剂的方法44、A g2CO3氧化法:以碳酸银作为氧化剂的方法45、A l(O-i-Pr)3:三异丙氧基铝46、D MSO氧化法:以二甲亚砜作为氧化剂的方法47、L AH还原法:以四氢铝锂作为还原剂的方法48、极性倒置:通过杂原子的交换、引入或添加,将某一合成子的正常极性转化成其相反的性质的过程49、C lemmensen还原法:锌汞齐盐酸反应将羰基还原成亚甲基的反应50、W olff还原法:肼在碱性条件下还原羰基成亚甲基的反应51、多相催化氢化:使用过渡金属等催化剂,使得不饱和烃加氢形成饱和烃的过程52、催化转移氢化:在催化剂的作用下,氢由氢的给体转移到有机化合物反应底物的反应53、R osenmund反应:酰卤用催化氢化或金属氢化物选择性地还原为醛的反应54、D ieckmann反应:指二元羧酸的酯类在金属钠或醇钠作用下发生分子内的克莱森缩合反应,形成环状的β-酮酯55、质子酸:水溶液中能电离出质子的酸56、脱氢芳构化:使用氧化脱氢的方法使得脂肪族化合物转变成芳香族化合物的反应57、B irch还原:芳香族化合物在液氨中用钠还原,生成非共轭二烯的反应58、亲电重排:正性取代基向富电子原子上迁移的反应59、亲核重排:负性取代基向缺电子原子上迁移的反应60、单酐:相同酸脱水得到的酸酐61、混酐:不同种酸脱水形成的酸酐62、单醚:单一醇脱水生成的醚63、混醚:不同的烃基形成的醚64、酯交换反应:不同种酸脱水形成的酸酐65、Oppenauer氧化66、Darzens缩合67、Knoevenagel反应68、羰基烯化反应(Wittig反应)69、DMSO:二甲基亚砜70、THF:四氢呋喃73、靶分子:凡是需要合成的有机分子。
合成化学第七章

CHO CHO
第七章 合成路线设计技巧(11学时)
第一节 逆向合成法常用术语(1学时)
三、逆向官能团交换
定义:所谓逆向官能团变换就是在不改变目标分子基本骨架的 前提下变换官能团的性质或位置的方法。一般包括下面三种变 换。 1. 逆向官能团互换(Antithetical Functional Group Interconversion 简称FGI)
第七章 合成路线设计技巧(11学时)
有机合成就是利用易得的“廉价”原料,通过化学方法来合 成有用的新产品或具有特殊结构的新化合物。 1967年,Corey首先提出了合成设计的概念和原则。 Corey 在提出了合成设计的概念和原则后,又发展了电子计 算机辅助合成分析,并已取得了一定的成绩,但距实际应用还有 一段距离。
合成:
CH2(CO2Et)2 Br LiAlH4 HO EtONa (EtO2C)2HC 1.H /H2O 2.EtOH/H
EtO2C
PBr3
Br
C6H5ONa
目标分子
第七章 合成路线设计技巧(11学时)
第二节 逆向切断技巧(4学时)
设计
O
OH
OH
的合成路线。
O
分析:
OH
CHO + HCN
O
O OH HCHO +
1.NaBH4 2.PBr3
1.Mg, Et2O 2.CO2 3.水解
目标分子
第七章 合成路线设计技巧(11学时)
第二节 逆向切断技巧(4学时)
CH3
设计
CH3CH OH C C2H5
CH3 FGI CH3CH OH C C2H5 CH2OH CH3C O C C2H5 C2H5Br COOEt
超分子化学

分子受体设计
设计原则(1)大的接触面积,如空腔,互补.大 环配体受体. (2)刚性与柔性的平衡.a受体的稳定性需要 刚性分子结构b识别过程的变换,调控,协 同作用等需要柔性 (3)氢键的作用在分子识别过程中非常重要 (4)π堆积提供了平面杂环低物的识别 (5)酶催化依赖于配位作用与过渡态的稳定 性
球形识别特点
1.强的作用,如氧对碱金属离子(AC)的作用 2.结构互补,空穴等 3.立体比平面有更强的选择性,二,三,四环 选择性不同
多氮杂、多硫杂配体、过渡金属离子识别
特点:1.配位作用N 、S对过渡金属的配 位,具有更强的选择性
2.结构互补,穴状配合物。谱学,磁学。
3.立体选择性
分子产物中的结构单位,而不等同于反应物的作用基团。
超分子合成子把分子片的化学特征和几何识别特征结合在 一起,即把明确的含蓄的分子间相互作用的内容包含在内。
合成子:用已知的或想象的合成操作所能形 成或组装出来的分子中的结构单位。
超分子合成子:用已知的或想像的、包含分 子间相互作用的合成操作所能形成的超分 子中的结构单位。 利用氢键的识别,设计超分子合成子是超分 子化学的重要内容。
下面列出几个以氢键结合的合成子:
一 些 有 代 表 性 的 超 分 子 合 成 子
分子识别:受体对底物的作用 受体结构储存信息(1)尺寸,形状等(2)构象, 手性(3)结合点性质,电子性质(电荷,极性, 极化力,范德华力)等 识别过程----信息的储存和读取过程
识别条件:受体和底物 (1) 结构互补 (2)作用力互补 (3) 有较大的接触区域 A:多个作用点,B:大区域的强结合 (4)介质效应,疏水,亲水作用 (5)作用力协同作用
分子间的三点作用类型包括氢键,偶极相互
第7章逆合成分析法与合成路线设计

7.1.1 逆合成分析法概念
1.合成子
C M+ X C
C MgX + O
O C
OEt COOEt
C C + MX
C C OH O
COOEt
7.1 逆合成分析法
7.1.1 逆合成分析法概念
1.合成子
C:+ C C: + O C
CC C CO
O C
COOEt
O COOEt
7.1 逆合成分析法
7.1.1 逆合成分析法概念
CH2CH2COOCH3
(e) CH2CH2COOCH3
(f) CH3OCOCH2 (g) OCH3 CH2 CHCOOCH3
在这些结构单元中,只有(d)和(e)是有效的,叫有效合成子。因为(d)可以
修饰为C6H5COC-HCOOCH3,(e)可以修饰为 。
CH2
CH2COOCH3
7.1 逆合成分析法
逆向合成分析过程图
合成子:在切断时所 得出的概念性的分子 碎片,通常是个离子
6
7.1 逆合成分析法
7.1.1 逆合成分析法概念
反应
反应
原料
中间物
目标分子 ( 产物 )
官能团转换
目标分子
逆合成转变
另外的目标分子
逆合成转变
前体的前体
原料
前体(合成子)
目标分子
A
B
CO
D E
F GJ K L
H
M
N
多路线逆合成分析示意图
X
1
C
2
C
3
C
C4
C5
C
FG
X=杂原子 FG=官能团
有机合成
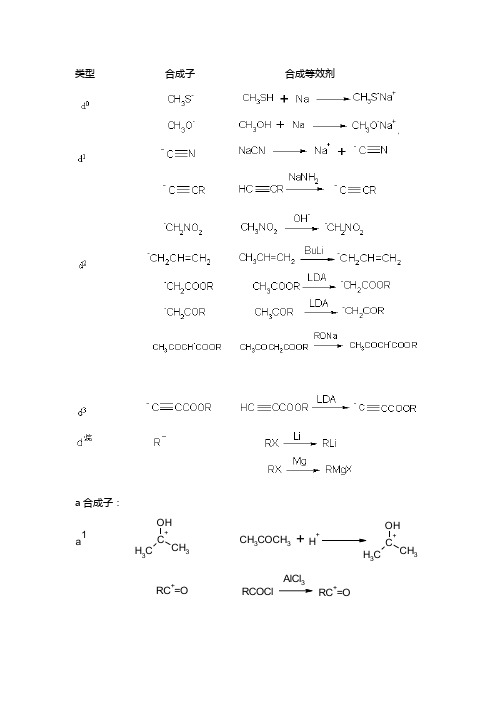
类型 合成子 合成等效剂a 合成子:C+OH CH 3CH 3CH 3COCH 3H +C+OHCH3CH 3RC+=ORCOClAlCl 3RC +=O+CH 2COCH 3BrCH 2COCH 3BrC -HCOCH 3+CH 2CHOHCH 3OCH 3H++CH 2CHOHCH3R(H)OCNXX=Cl,Br,IR+RXR 2SO 48.1.2.2合成子的作用规律一个d 合成子与一个a 合成子在适当的条件下化合,得到一个加合的C -C 键(d 0合成子除外)。
下述的一些规律,可以用来设计产物(目标分子)中的官能团的位臵。
d 烷+a 烷,反应产物是无官能团产物 a 烷+d 1,a 1+d 烷,反应产物是单官能团化合物 a 1+d 1, 反应产物是1,2-双官能团化合物 a 1+d 2,a 2+d 1,反应产物为1,3-双官能团化合物等等。
例如:烷基a +烷基d :CH 3LiCH 3Br CH 3-CH 3a 1+d 1:RC=OHHCNRCH OHCNa 1+d 2:CH 3COCH 3CH 3CHOC OHCH 2CHOCH 3C H 3a2+d2:OCOOCH3BrO COOCH3OCOOCH3O COOCH3a3+d2:OOHO注意:目标分子是合成子就必须由一个以上官能团。
如果在开链化合物分子中,含有一个电子接受体部位和一个供电子中心,则这两个原子间可进行分子内键合。
相应地生成单环化合物。
例如:O OMeO8.2供电子合成子8.2.1烷基(烃基)d合成子碳负离子是带一对电子的有机负离子,电荷主要集中在碳原子上。
烷基、烯基、炔基负离子中,非键合的电子总是定域在碳原子上,它们具有高度的反应活性。
形成碳负离子的难易程度:与碳氢键中的S成分有关,S成分增加,则越易形成碳负离子。
C CH C CH C CH当碳原子上的取代基数目不同时,饱和烷基负离子的稳定性顺序为3o<2o<1o,但他们的稳定性都很小。
合成子分类

– 离子合成子: a-合成子——正离子 d-合成子——负离子
– 自由基合成子: r - 合成子—— 自由基 • R – 周环反应合成子: e - 合成子 —— 分子
a-合成子——正离子 ,亲电性
合成子
Ra
Me +
a0
Me2P +
等价物
Me3SBr Me2PCl
a1
+ Me2C-OH
R1 COOH
• Wittig反应的反合成子
R1
R3
R1
R3
O (C6H5)3P
R2
R4
R2
R4
MeCoMe
a2
+ MeCOCH2
MeCOCH2Br
OH
a3
+CH2-CH=C-OR CH2=CHCOOR
官能团
Me2P--O O
-COOR
d-合成子——负离子 ,亲核性
合成子
Rd
Me -
d0 d1,2
MeS -
R-CH=CH
等价物
MeLi
官能团
MeSH R-CH=CH-X / M
-SH
d1 -C N
目标分子中宜转化的结构单元
—经典反应为依据的反合成子
Diels-Alder反应反合成子
R
CH2
R
+
CH2
CH2
Claisen重排反应反合成子
R1
O R2
R3
H2C
R1
CH2
O R2
R3
H2C
R1
CH2
O C2H5
OH R2
R3
Robinson增环反应反合成子
好字合成子女的句子

好字合成子女的句子
1、儿女双全,何其幸运拼了两次命凑成了一个好字,从此封肚陪你们一起长大。
2、儿女双全,何其幸运,老婆拼了两次命,为我们凑成一个好字,愿此生三餐四季,温暖有趣,愿你们两个,拥之则安,伴之则暖!
3、真羡慕儿女双全的啊,凑成一个好字了,而且长得都好看。
4、明天剖宫产了,希望能凑成好字,儿女双全,一切顺利。
5、女+子=好!儿女双全,何其幸运,拼了两次命,终于凑成了一个好字,愿此生三餐四季,温暖有趣,愿你们兄妹两个拥之则安,伴之则暖!
6、儿女双全,何其幸运拼了两次命,凑成了一个好字陪伴你们一起长大,愿你们两拥之则安,伴之则暖,健康快乐成长。
7、不管怎么说,2021年我儿女双全了,好字凑成了,希望未来的我们,能事事顺心!
8、希望肚子里怀的是女孩,大宝是男孩,愿儿女双全,凑成好字。
9、在2021年儿女双全,凑成好字,一家四口,健健康康,快快乐乐。
10、希望是两个弟弟,儿女双全,凑成好字,你值得拥有也一定要是全世界最幸福。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
d0: 也可能在C之前,官能团(FG)或杂原子X0有活性,就是d0合成子
相似地,也有因极性转换使碳原子有受电子能力而形成活 性中心的,受电子合成子就合成子
思考:
CH3Li
CH3- + Li+ 中, CH3-属于哪一类合成子?
CH3Li中不含有任何官能团,在反应中只起到烷基化的作 用,因此,我们把这种合成子称为烷基d合成子。 由于烷基 d合成子在反应中只起到烷基化的作用,因此, 产物不会增加官能团。
(三)d3合成子
H2C O
等效试剂制备
CH2 OSiR3
t-BuLi
H2C OSiR3
CH2
COOR
等效试剂制备
COOR
COOR
t-BuOK
COOR
COOR
HO
OR
(四)>3的dn合成子
如果参与反应的官能团和不参与反应的官能团相隔较远,大多数情 况互相不起作用,不再形成一个整体。例如:
O O
(1)KH-H2,THF (2)t-BuLi,TMEDA
R X R + Nu X R Nu MgX R E
RMgX
R
+ E
像这种,卤代烷分解时产生R+离子,而通过格式剂再分解时, 烷基就成了负离子。这就叫极性转换。 有了极性转换,同一基团既可以成为正离子也可以成负离子, 这就扩大了可能进行的有机合成的范围。
O
O
O
+
H3COC
CH3C
极性转换: 途径:
O
O
CH3C
CH3C
如何选用A和B? 选用亲核能力强的B,利于第一步的反应;选择离去能力 强的A,利于对后一步的反应。 具体合成路线:
合成子与稳定性
是否所有分子都可以按下列形式拆分?
不是 !!!
当X=CN时:
氰基(CN-)是很稳定的负离子,易与羰基发生亲核加成反应
HCN有剧毒,且挥发性较大(沸点26.5℃),故在羰基化合物与氰化氢加成时,通 常是把无机酸加入醛(酮)和氰化钠水溶液的混合物中,HCN一生成就立即与醛 (酮)作用,但在加酸时应注意控制溶液的pH值,使之始终偏于碱性(pH约为8), 以利于反应的进行。
利用Si,S,P及过渡金属也可生成d1合成子。
烷基硅叶立德:(Si)
还有之前介绍过的二噻烷负离子:(S)
S R S S
+
n-BuLi
- BuH
R S
Li
磷叶立德:(P)
(三)d2合成子
(1)如α -碳原子旁有不饱和吸电子基团,α -碳上的碳氢 键就会被活化,使α -碳成为d2合成子。
不饱和吸电子基团影响α -碳上碳氢键的活化能力,其大小有如下顺序:
O
和
前面提到,酰基负离子是不稳定的,因此我们需要寻找一种等价物:
O
CN
HCN
OH
安息香缩合反应机理:
除了用HCN,利用有机金属化合物引起极性转换也可以得到酰基负离 子:
OCH3
+ t - Bu Li
利用烯醚结构使得带负电的酰基合成子更稳定:
OCH3
H
例:
Li
OCH3
O
OCH3 OH
O OH
+
1 2
产物是单官能团化合物
(4)a1+d2
+
1 2
产物α,β-不饱和醛,是1,3双官能团化合物。
(5)a2+d2
-
+
产物是1,4-双官能团化合物。另外,a1+d3、a3+d1的产物也都是1,4双官能团化合物。
(6)a3+d2
+ 1
5
+
(d2 + a1)
1,3双官能团化合物
-
产物是1,5-双官能团化合物
上述反应可以很容易的进行,但若X=C2H5时,则不可以。
Et-是一个不稳定的负离子,不能直接用于和羰基的反应,但通过格 式剂就能将它稳定起来,这是的格式剂就起到一个合成子等价物的作 用。反应如下:
5.2 合成子极性转换的具体应用
(一)安息香缩合:
苯甲醛双分子缩合的产物是 是:
O H
它的“合成子”应该
规律:合成子(非烷基合成子及0合成子)上标 之和为n,则可得到1,n-双官能团化合物。
供电子合成子
大多通过有机金属卤化物制得,由C-Na,C-Li通过金属交换而得C-M, 反应如下:
(一)烃基d合成子
或者通过格式剂制备烃基d合成子:
THF
Cl
+
Mg
MgCl
(二)d1合成子
在C1-X0(杂原子)中,碳的电子对可离域到杂原子上去,就形成较 稳定的碳负离子,即d1合成子。HCN(及钾盐、钠盐)以及CH3NO2都能 在水溶液中生成d1合成子。
注意:区分d合成子和d1合成子,关键在于有无官能团。
相似的,也存在烷基a合成子,同样只在反应中起到烷基化 的作用
合成子的加合——a合成子与d合成子的反应 下面列举六种合成子的加合反应 (1)烷基a + 烷基d
烷基d
烷基a
产物为无官能团化合物。
(2)a1+d1
+
产物是1,2-双官能团化合物。
(3)烷基a + d2
合成子的有效性
有机分子的拆分:
O O
1
4
5
OCH3
2
H3CO
3
O
这些碎片不一定都能反过来键接而成分子,即并不是所有的碎片是合成子。 合成子是分子拆开后在有机合成中确实有效的碎片。
上述分子中只有下列两个碎片是有效的
O O
OCH3
H3CO O
O
O
O
+ H+
H3CO O
OCH3
OCH3
二者通过Michael加成得到原分子:
5.合成子与极性转换
5.1 关于合成子的基本概念
合成子的概念
Corey E.J. :凡是能用已知的,或合理的操作
连接成分子的结构单元均称为合成子。
——1967
合成子是有机合成反应中的基本单元
A电子供体
+
B+
电子受体
A-B
中性产物分子
A.
+
自由基
B.
A-B
中性产物分子
这里的A- 和B+ 、A.和B.以合理的操作连接成分子A-B,可称为合成子。它 们是合成反应中的基本单位。
O O
O O
+
OCH3 H3CO O
EtONa
OCH3
H3CO
O
O
O
因此只有
H3CO O
和
OCH3
O O
两个碎片才
是 分子
H3CO O
OCH3
的合成子
当然,有的拆开的地方在今天看来是不可能键接的,但随着有机 合成化学的不断发展,这个地方就有可能成为可行的键接处,到 那时就会有新的合成子出现。
合成子不一定实际存在
d2合成子的形成与C-H的pKa,即该H的酸性,有很大关系,也与所用试 剂的碱性有很大关系。
(2)如果羰基化合物是一个不对称酮,左右两边的α -碳上都有碳氢 键,这就会有区域选择性
动力学控制
O
28%
LiO
72%
OLi
Ph3CLi DMF
+
热力学控制
94%
6%
动力学控制:中间体稳定性,倾向于生成稳定的碳负离子; 热力学控制:倾向于生成稳定的产物。
Li
H3 O 86%
(二)二噻烷碳负离子的生成
S
O
这里
S
,也相当于
,也是县酰基负离子的等价物。
5.3 合成子的分类和加合
合成子的分类
极性转换中的合成子可分为供电子合成子d(donor)与受电子合成 子a(acceptor)两大类。 见下列有机分子的基本结构:
FG: 官能团 X0: 促使分子发生极性转换的金属原子或杂原子(Li,Mg等,或-O,-N,S等)。 C1C2C3…… : 碳原子的顺序编号,由于极性转换而使C1有供电子能力形 成活性中心,就是d1合成子;C2有活性,就是d2合成子,依次类推。
Ph
这个结构不以稳定,两个负电荷可能分开,形成一个二负离子,分 别起反应。
受电子合成子 a合成子在反应中作为亲电试剂,情面已经讲过,这里再补充一些 例子:
烷基a合成子
a1合成子
,
如:
,
a2合成子
a3合成子
a4合成子
如:
X=OH2,Cl,Br,I,OMes
+
用合成子的观点解决路线设计中的具体问题。
合成子是一个人为的、概念化了的名词。
O O O
+
O
碱
碎片是
O
与
O
这里两个碎片,后一个是实际且稳定存在的。但是,环己酮负离子是 很不稳定的,它只在反应过程中瞬间存在并立即起反应。
O
O
H3COC
O
O
对于这个产物分子来讲 它的合成子应是 前者是不存在的。 问题:如何合成?
CH3C
和
。
然而 在思考合成路线或进行逆合成分析时,仍然认为它是 一个合理的合成子,因为它存在一个对等的等价物。
什么是合成等价物呢?
合成等价物:一种能起合成子作用的试剂。合成 子通常由于其本身的不太稳定而不能直接使用。 : Me+
合成子
