2018-2019学年度北京市朝阳区高三一模化学试卷及答案(word版)
2018-2019北京市朝阳化学一模
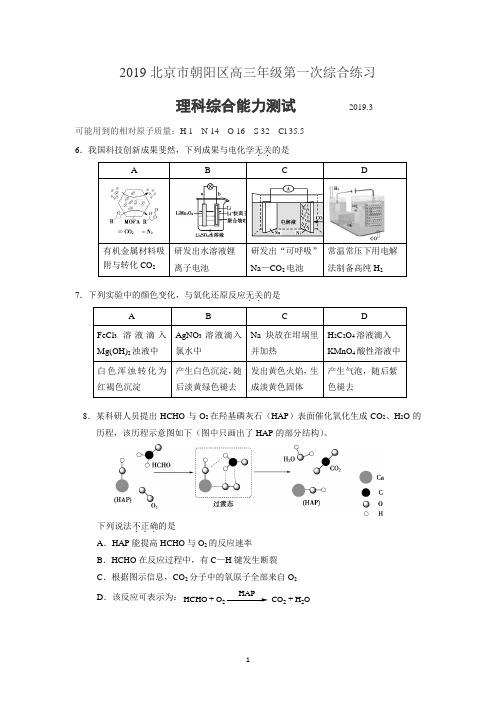
2019北京市朝阳区高三年级第一次综合练习理科综合能力测试2019.3可能用到的相对原子质量:H 1 N 14 O 16 S 32 Cl 35.56.我国科技创新成果斐然,下列成果与电化学无关..的是7.下列实验中的颜色变化,与氧化还原反应无关..的是8.某科研人员提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如下(图中只画出了HAP的部分结构)。
下列说法不.正确..的是A.HAP能提高HCHO与O2的反应速率B.HCHO在反应过程中,有C—H键发生断裂C.根据图示信息,CO2分子中的氧原子全部来自O2D.该反应可表示为:HCHO + O HAP CO+ H2O29.我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如下图所示。
下列说法不.正确..的是A.该装置可将太阳能转化为化学能B.催化剂a表面发生还原反应,产生H2C.催化剂b附近的溶液pH增大D.吸收1 mol SO2,理论上能产生1 mol H210.2019年是“国际化学元素周期表年”。
1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。
下列说法不正确...的是A.元素甲位于现行元素周期表第四周期第ⅢA族B.原子半径比较:甲>乙>SiC.元素乙的简单气态氢化物的稳定性强于CH4D.推测乙可以用作半导体材料11.一种高分子可用作烹饪器具、电器、汽车部件等材料,其结构片段如下图。
下列关于该高分子的说法正确的是A.该高分子是一种水溶性物质B.该高分子可由甲醛、对甲基苯酚缩合生成C.该高分子的结构简式为D.该高分子在碱性条件下可发生水解反应12.探究铝片与Na2CO3溶液的反应。
下列说法不.正确..的是A.Na2CO3溶液中存在水解平衡:CO32- + H2O ⇌ HCO3- + OH-B.对比Ⅰ、Ⅲ,说明Na2CO3溶液能破坏铝表面的保护膜C.推测出现白色浑浊的原因:AlO2- + HCO3- + H2O = Al(OH)3↓+ CO32- D.加热和H2逸出对CO32-水解平衡移动方向的影响是相反的25.(17分)药物中间体Q、医用材料PV A的合成路线如下。
2019届北京市朝阳区高三一模理综化学试卷【含答案及解析】
2019届北京市朝阳区高三一模理综化学试卷【含答案及解析】姓名___________ 班级____________ 分数__________一、选择题1. 中国传统文化对人类文明贡献巨大,古化文献中充分记载了古代化学研究成果.下列关于 KNO 3 的古代文献,对其说明不合理的是(________ )2. N 2 (g) 与 H 2 (g) 在铁催化剂表面经历如下过程生成 NH 3 (g) :下列说法正确的是(________ )A .Ⅰ中破坏的均为极性键B .Ⅳ中 NH 3 与 H 2 生成 NH 3C .Ⅱ、Ⅲ、Ⅳ均为放热过程D .3. 下列检测方法不合理的是(________ )4. 某厂用 Na 除掉苯中的水分。
某次生产误将甲苯当做苯投进反应釜中,由于甲苯中含水量少,最后反应釜还残留大量的 Na 。
下列处理方法更合理、更安全的是(________ )A .打开反应釜,将 Na 暴露在空气中与氧气反应B .向反应釜通入 Cl 2 , Na 在 Cl 2 中燃烧生成 NaClC .向反应釜加大量 H 2 O ,通过化学反应“ 除掉” 金属钠D .向反应釜滴加 C 2 H 5 OH ,并设置放气管,排出氢气和热量5. 《常用危险化学用品贮存通则》规定:“ 遇火、遇热、遇潮能引起燃烧、爆炸或发生化学反应,产生有毒气体的化学危险品不得在露天或在潮湿、积水的建筑物中贮存” 。
下列解释事实的方程式中,不合理的是(________ )A .贮存液氮的钢瓶防止阳光直射:B .硝酸铵遇热爆炸:C .干燥的 AlCl 3 遇水产生气体:D .火灾现场存有电石,禁用水灭火:6. 下列“ 试剂” 和“ 试管中的物质” 不能完成“ 实验目的” 的是(________ )7. 某同学做如下实验:下列说法正确的是(________ )A .“ 电流计指针未发生偏转” ,说明铁片Ⅰ、铁片Ⅱ均未被腐蚀B .用 K 3 [Fe(CN) 3 ] 溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断电池的正、负极C .铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,二者的腐蚀速率相等D .铁片Ⅳ的电极反应式为 Fe-3e - =Fe 3+二、推断题8. 有机物 A 为缓释阿司匹林的主要成分。
朝阳区高三化学一模试题(附答案)

2019 朝阳区高三化学一模试题(附答案)7. 已知:下列说法不正确的是A. ①和②变化过程中都会放出热量B. 氯原子吸引电子的能力强于钠原子和氢原子C. ①和②中的氯原子均得到1 个电子达到8 电子稳定结构D. NaCl 中含有离子键,HCl 中含有共价键8. 综合下图判断,下列叙述不正确的是A. I、H的反应原理均是Zn + Cu2+ = Zn2+ + CuB. I、H中均有电子转移,均是把化学能转化为电能利用C. 随着反应的进行,1、□中CuSO4溶液颜色均渐渐变浅D. 取a 中溶液,加足量Ba(NO3)2 溶液,过滤后向滤液中加AgN03容液,有沉淀产生9. 下列解释事实的方程式不准确的是A. 氨水使湿润的红色石蕊试纸变蓝:NH3H2O NH4+ + OH-B. 工业上用过量的NaOH容液吸收SO2 SO2+ OH- == HSO3-C. 用烧碱溶液清洗铝表面的氧化膜:2OH- + Al2O3 = 2AlO2- + H2OD. 用石灰乳吸收泄漏的氯气:2Ca(OH)2 + 2Cl2== CaCl2 + Ca(ClO)2 + 2H2O10. 下列实验事实不能用平衡移动原理解释的是温度/ C 20 100FeCl3 饱和溶液棕黄色红褐色A. B.c( 醋酸) / (molL-1) 0.1 0.01pH 2.9 3.411. 右图为实验室制取乙炔并验证其性质的装置图。
下列说法不合理的是A. 逐滴加入饱和食盐水可控制生成乙炔的速率B. KMnO4酸性溶液褪色,说明乙炔具有还原性C. 用Br2 的CCl4 溶液验证乙炔的性质,不需要除杂D. 将纯净的乙炔点燃,有浓烈的黑烟,说明乙炔不饱和程度高12. 在100C时,将N2O4 N02分别充入两个各为1 L的密闭容器中,反应过程中浓度变化如下:[2NO2(g) N2O4(g)△ H0]容器物质起始浓度/(molL-1) 平衡浓度/(molL-1)I N2O4 0.100 0.040NO2 0 0.120II N2O4 0 0.014NO2 0.100 0.072下列说法正确的是A. 平衡时,I、I中反应物的转化率 a (N2O4) a (NO2)B. 平衡时,I、I中上述正反应的平衡常数K( I ) = 2K( I)C. 平衡后,升高相同温度,以N2O4表示的反应速率V ( I)V(n)D. 平衡后,升高温度,i、n中气体颜色都将变深25. (16 分)对羟基扁桃酸、香豆素-3-羧酸用于制备药物、香料,二者合成路线如下( 部分产物及条件未列出) :(1) A 的结构简式是______ 。
2019年北京市朝阳区高考化学一模试卷解析版

2019年北京市朝阳区高考化学一模试卷一、选择题(共7小题,每小题6分,满分42分)1.(6分)我国科技创新成果斐然,下列成果与电化学无关的是( )A .AB .BC .C D .D2.(6分)下列实验中的颜色变化,与氧化还原反应无关的是( )A .AB .BC .CD .D3.(6分)某科研人员提出HCHO 与O 2在羟基磷灰石(HAP )表面催化氧化生成CO 2、H 2O 的历程,该历程示意图如下(图中只画出了HAP 的部分结构)。
下列说法不正确的是( )A .HAP 能提高HCHO 与O 2的反应速率B .HCHO 在反应过程中,有C ﹣H 键发生断裂C .根据图示信息,CO 2分子中的氧原子全部来自O 2D .该反应可表示为:HCHO+O 2CO 2+H 2O4.(6分)我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如下图所示。
下列说法不正确的是()A.该装置可将太阳能转化为化学能B.催化剂a表面发生还原反应,产生H2C.催化剂b附近的溶液pH增大D.吸收1molSO2,理论上能产生1molH25.(6分)2019年是“国际化学元素周期表年”。
1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。
下列说法不正确的是()A.元素甲位于现行元素周期表第四周期第ⅢA族B.原子半径比较:甲>乙>SiC.元素乙的简单气态氢化物的稳定性强于CH4D.推测乙可以用作半导体材料6.(6分)一种高分子可用作烹饪器具、电器、汽车部件等材料,其结构片段如下图。
下列关于该高分子的说法正确的是()A.该高分子是一种水溶性物质B.该高分子可由甲醛、对甲基苯酚缩合生成C.该高分子的结构简式为D.该高分子在碱性条件下可发生水解反应7.(6分)探究铝片与Na2CO3溶液的反应。
北京市朝阳区2019届高三第一次(3月)综合练习(一模)化学试卷 含解析

北京市朝阳区高三年级第一次综合练习理科综合能力测试可能用到的相对原子质量:H 1 N 14 O 16 S 32 Cl 35.51.我国科技创新成果斐然,下列成果与电化学无关..的是A. 有机金属材料吸附与转化CO2B. 研发出水溶液锂离子电池C. 研发出“可呼吸”Na—CO2电池D. 常温常压下用电解法制备高纯H2【答案】A【解析】【详解】电化学指的是研究电能和化学能相互转化的的化学,高中阶段最常见的两个装置为原电池和电解池。
A.环氧烷烃被有机金属材料吸附与CO2生成碳酸酯,无电流产生,与电化学无关,A项符合题意;B.锂电池,能够发生自发的氧化还原反应,属于原电池,与电化学有关,B项不符合题意;C.Na-CO2电池,属于原电池,与电化学有关,C项不符合题意;D.用电解法制备H2,属于电解池,与电化学有关,D项不符合题意;本题答案选A。
2.下列实验中的颜色变化,与氧化还原反应无关..的是A. FeCl3溶液滴入Mg(OH)2浊液中,白色浑浊转化为红褐色沉淀B. AgNO3溶液滴入氯水中,产生白色沉淀,随后淡黄绿色褪去C. Na块放在坩埚里并加热,发出黄色火焰,生成淡黄色固体D. H2C2O4溶液滴入KMnO4酸性溶液中,产生气泡,随后紫色褪去【答案】A【解析】【详解】A.难溶电解质之间的转化,3Mg(OH)2+2FeCl3=2Fe(OH)3+3MgCl2,化合价没有变化,与氧化还原反应无关,A项符合要求;B.Cl2与水反应,生成HCl和HClO,氯元素化合价发生变化,与氧化还原反应有关,B项不符合题意;C.Na在空气中与氧气反应,2Na+O2Na2O2,化合价发生变化,与氧化还原反应有关,C项不符合题意;D.草酸与高锰酸钾溶液发生,紫红色褪去,生成CO2,化合价变化,属于氧化还原反应,D项不符合题意;本题答案选A。
【点睛】氧化还原反应与非氧化还原反应的本质区别在于是否有电子的转移,可以从是否有化合价的变化来判断是否为氧化还原反应。
北京市朝阳区2018~2019学年度(1月)高三第一学期化学期末练习(含答案)

北京市朝阳区2018~2019学年度第一学期期末质量检测高三化学试卷(考试时间90分钟 满分:100分) 2019.1可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Fe 56第一部分 (选择题 共42分)每小题只有一个选项符合题意,每小题3分,共14道小题,共42分。
1.电动汽车(标志为“”)在改善城市交通、保护环境等方面的作用至关重要。
下列说法不正确...的是A .电动汽车的使用有助于减少氮氧化物的排放B .燃油汽车也可以悬挂该标志C .电动汽车使用时涉及化学能与电能的转换D .电动汽车充电、放电过程均有电子转移2.下列物质的用途是基于其氧化性的是A .氨用作制冷剂B .次氯酸钙用于生活用水的消毒C .氧化铝透明陶瓷用于防弹汽车的车窗D .生石灰用于废气的脱硫 3.下列化学用语表达不.正确..的是 A .CH 4的比例模型:B .NH 3的电子式:C .Na 2CO 3溶液呈碱性的原因:CO 32﹣+ 2H 2H 2CO 3+ 2OH -D .NH 3遇氯化氢迅速产生白烟:NH 3 + HCl = NH 4Cl4.学习和研究化学,经常要进行实验。
安全是顺利进行实验及避免伤害和事故的保障。
下列说法不正确...的是 A .将剩余的钠块直接投进垃圾箱B .电石(主要成分为CaC 2)在干燥环境中密封存放 C .用CCl 4萃取碘,振荡分液漏斗后要打开活塞放气D .电器失火要先切断电源5.下列关于物质性质的比较,不正确...的是 A .沸点:C 2H 5OH >CH 3CH 3 B .水的电离程度:100℃>25℃C .溶解度:AgI >AgClD .完全燃烧放出的热量:1mol C >1mol CO6.常温时,能证明乙酸是弱酸的实验事实是 A. CH 3COOH 溶液与Fe 反应放出H 2B. 0.1 mol/L CH 3COOH 溶液的pH 大于1C. CH 3COOH 溶液与NaHCO 3反应生成CO 2D. 0.1 mol/L CH 3COOH 溶液可使紫色石蕊变红7.根据元素周期律判断,不正确...的是 A .铍(Be )原子失电子能力比Ca 弱 B .K 与水反应比Mg 与水反应剧烈C .HCl 的稳定性强于HBrD .硼酸(H 3BO 3)的电离程度强于H 2SO 48.阿伏加德罗常数的值为N A 。
最新-2018年4月北京市朝阳区理综一模化学部分(含答案)

2018年北京市朝阳区高三 理综一模(化学部分)2018年4月5. 下列说法不正确的是A. 60C 与金刚石互为同素异形体B. 114号元素的一种同位素中子数为184,则该原子的质量数为298C. 酒精可以和钠发生置换反应,所以酒精属于电解质D. 分子式Cl H C 52只表示一种物质6. 下列离子方程式正确的是A. 2MgCl 溶液中滴加氨水 ↓=+-+22)(2OH Mg OH MgB. 醋酸和氢氧化钠溶液反应 O H OH H 2=+-+C. 铝和氢氧化钠溶液反应 ↑+=++--22232222H A l O O H OH AlD. 铁和氯化铁溶液反应 ++=+232Fe Fe Fe7. “泰诺林”是治疗感冒发烧的一种药物。
其主要成份的结构简式如下:3COCH NH HO --下列关于该物质的描述不正确的是A. 该化合物分子式为N O H C 298工资B. 能和银氨溶液发生银镜反应C. 能和氢氧化钠溶液发生反应D. 其分子中的原子不可能都在同一平面上8. 已知热化学方程式)(23g SO )()(222g O g SO +;mol kJ H /1971+=∆和热化学方程式)()(222g O g SO +)(23l SO ;mol akJ H /2-=∆则下列说法正确的是 A. a>197 B. a<197C. a=197D. 热化学方程式中化学计量数可表示分子个数9. 在密闭容器内,下列已达到平衡的化学反应中,当升高温度并同时减小压强时,平衡一定向右移动的是A. )(2)(g B g A +)(2g C ;01>∆H B. )()(g B g A +)()(g D g C +;02>∆HC. )(2)(g B s A +)(g C ;03>∆H D. )(s A )()(g C g B +;04<∆H10. 已知3NaHCO 溶液呈碱性,在0.1 mol/L NaHCO 3溶液中,下列关系正确的是A. )()()()(3--+++=+OH c HCO c H c Na cB. L mol CO c HCO c /1.0)()(233=+-- C. )()(2332->CO c CO H c D. )()()(332-++=HCO c CO H c Na c11. 某温度下,VmL 不饱和3NaNO 溶液a g ,蒸发掉b g 水或加入b g 3NaNO 固体(恢复到原温度)均可使溶液达到饱和,则下列量的计算结果正确的是A. 该温度下3NaNO 的溶解度为100gB. 原不饱和溶液中3NaCO 质量分数为%)(500ab a - C. 原不饱和溶液中3NaNO 物质的量浓度为L mol b a /17)(100- D. 原不饱和溶液的密度为mL g Vba /+12. 为提纯下列物质(括号内为少量杂质),有关除杂试剂和分离方法的选择均正确的是25. (15分)图中A ~J 分别代表一种反应物或生成物,已知A 受热分解得到等物质的量的B 、C 、D 气态物质,图中部分生成物未列出请回答(1)B 的电子式___________,C 是___________(极性、非极性)分子,D 分子的空间构型为______(2)写出反应①、②的化学方程式①____________________________________________②____________________________________________ (3)写出反应③的离子方程式______________________________________________26. (15分)已知(1),产物不发生银镜反应(2)烃A 有下图转化关系,图中每个字母表示一种有机物,D 的结构简式为,G与M 是由不同方式形成的高分子化合物。
朝阳区2018届高三一模化学试题及答案(word版)

N (C 4H 8O2)
Br2 PBr3
ⅰ .NaOH X
ⅱ .H+
Y
O2
催化剂
F (C4H 6O 3)
CH3
N COOH
有机物 P
已知:
O
RNH 2 +
C
一定条件
RN C
+ H2O
O C H+
O CH 2 C
一定条件
O CH C C
+ H2O
( 1) A 为芳香化合物,其结构简式是
。
( 2) A → B 的化学方程式是
C.反应④的颜色变化是由化学平衡移动引起的
D .反应①可由右图所示装置实现
水
11. 测溶液 pH 可研究反应过程。用盐酸分别滴定 Na2CO3、 NaHCO 3溶液,测得 pH 随加
入盐酸体积的变化如下图所示(曲线②从
B1 点开始滴定) 。下列判断不.正.确.的是
A .曲线①表示用盐酸滴定 Na2CO 3 的过程
的氧化率。反应如下:
6Fe2+
+
Cr
2O
27
+
14H +
=2Cr 3+ + 6Fe3+ + 7H 2O
第一部分(选择题 共 120 分)
本部分共 20 小题,每小题 6 分,共 120 分。在每小题列出的四个选项中,选出最符合 题目要求的一项。 6. 吉州窑黑釉木叶纹盏是中华名瓷,传统制作过程如下。其中以化学反应为主的是
A. 踩泥
B . 拉坯
C. 上釉
D. 烧制
7. 下列事实不.能.用元素周期律解释的是
专业 K12 教研共享平台
朝阳2018-2019学年度第一学期期末高三化学参考答案

参考答案第一部分(选择题共42分)第二部分(非选择题共58分)15.(14分)(1)① 22222CH CH Br CH Br CH Br =+→-②NaOH/CH 3CH 2OH ③ 碳碳双键、醛基 ④3222CH CH CH CH OH(2)① Cu 3222232222CH CH CH CH OH O 2CH CH CH CHO 2H O +−−→+ ②OO③COOHCOOCH 2CH(CH 2)3CH 32H 5酯化反应16.(10分) (1)① c②CH 4(g) + 2H 2O ⇌CO 2(g) + 4H 2(g) ∆H =+169kJ· mol -1 ③ 1(2)① CaO 可吸收2CO ,c (2CO )减小,使生成2H 的反应正向移动,2H 百分含量增大 ②纳米CaO 颗粒小,表面积大,使反应速率加快 (3)① 降低温度、增大压强 ② C + H 2O =CO + H 217.(12分)(1)22Cl 2OH Cl ClO H O ---+=++(其它答案合理均可) (2)① 2Fe +、Br - ② 铁粉(3)322BrO 5Br 6H 3Br 3H O --+++=+(4)①Br 2② 理由:22224SO Br 2H O H SO 2HBr ++=+方案:用4CCl 萃取颜色很浅的溶液,观察溶液下层是否呈棕红色 ③ 稀硫酸 18.(10分) (1)KSCN 溶液(2)I .23224Fe 4H O 4Fe 2H O +++++=+II .①试纸变蓝②()33432212Fe OH NO 4Fe O NH OH 10H O --+=+↑++(3)ab (4)① 24H PO -② pH = 5时,34Fe O 带正电荷,含磷的主要微粒是24H PO -;pH = 9时,34Fe O 带负电荷,含磷的主要微粒是24HPO -。
因此在pH = 9时,吸附剂和含磷的主要微粒之间的静电排斥作用强于pH = 5时。
化学#高三#北京市#高三一模#2018-2019学年度北京市朝阳区高三一模化学试卷

【题干序号】1我国科技创新成果斐然,下列成果与电化学无关..的是()A.有机金属材料吸附与转化CO2B.研发出水溶液锂离子电池C.研发出“可呼吸”Na—CO2电池D.常温常压下用电解法制备高纯H2【答案序号】【来源】2018-2019学年度北京市朝阳区高三一模化学试卷【答案】A【解析】A.环氧烷烃被有机金属材料吸附与CO2生成碳酸酯,无电流产生,与电化学无关,A项符合题意;B.锂电池,能够发生自发的氧化还原反应,属于原电池,与电化学有关,B项不符合题意;C.Na-CO2电池,属于原电池,与电化学有关,C项不符合题意;D.用电解法制备H2,属于电解池,与电化学有关,D项不符合题意;【题干序号】2下列实验中的颜色变化,与氧化还原反应无关..的是()A.FeCl3溶液滴入Mg(OH)2浊液中,白色浑浊转化为红褐色沉淀B.AgNO3溶液滴入氯水中,产生白色沉淀,随后淡黄绿色褪去C.Na块放在坩埚里并加热,发出黄色火焰,生成淡黄色固体D.H2C2O4溶液滴入KMnO4酸性溶液中,产生气泡,随后紫色褪去【答案序号】【答案序号】【来源】2018-2019学年度北京市朝阳区高三一模化学试卷【答案】A【解析】A.难溶电解质之间的转化,3Mg(OH)2+2FeCl3=2Fe(OH)3+3MgCl2,化合价没有变化,与氧化还原反应无关,A项符合要求;B.Cl2与水反应,生成HCl和HClO,氯元素化合价发生变化,与氧化还原反应有关,B 项不符合题意;C.Na在空气中与氧气反应,2Na+O2Na2O2,化合价发生变化,与氧化还原反应有关,C项不符合题意;D.草酸与高锰酸钾溶液发生,紫红色褪去,生成CO2,化合价变化,属于氧化还原反应,D项不符合题意。
【题干序号】3某科研人员提出HCHO(甲醛)与O2在羟基磷灰石(HAP)表面催化生成H2O的历程,该历程示意图如下(图中只画出了HAP的部分结构):下列说法不正确的是()A.HAP能提高HCHO与O2的反应速率B.HCHO在反应过程中,有C-H键发生断裂C.根据图示信息,CO2分子中的氧原子全部来自O2D.该反应可表示为:HCHO+O2CO2+H2O【答案序号】【来源】2018-2019学年度北京市朝阳区高三一模化学试卷【答案】C【解析】A.根据图知,HAP在第一步反应中作反应物,在第二步反应中作生成物,所以是总反应的催化剂,催化剂能改变化学反应速率,因此该反应中HAP作催化剂而提高反应速率,A正确;B.HCHO在反应中有C-H断裂和C=O键形成,所以甲醛被氧化生成二氧化碳和水,B正确;C.根据图知,CO2分子中的氧原子一部分还来自于甲醛,C错误;D.该反应中反应物是甲醛和氧气,生成物是二氧化碳和水,HAP为催化剂,反应方程式为HCHO+O2CO2+H2O,D正确;【题干序号】4我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如图所示。
【区级联考】北京市朝阳区2019届高三下学期一模考试化学试题-89332b5105a84d2aa0e57b5bcfecfd7f
…外…………○…………装…………○……学校:___________姓名:___________班级:_…内…………○…………装…………○……绝密★启用前 【区级联考】北京市朝阳区2019届高三下学期一模考试化学试题 试卷副标题 注意事项: 1.答题前填写好自己的姓名、班级、考号等信息 2.请将答案正确填写在答题卡上 第I 卷(选择题) 请点击修改第I 卷的文字说明 一、单选题 1.我国科技创新成果斐然,下列成果与电化学无关..的是 A .有机金属材料吸附与转化CO 2 B .研发出水溶液锂离子电池 C .研发出“可呼吸”Na —CO 2电池 D .常温常压下用电解法制备高纯H 2 2.下列实验中的颜色变化,与氧化还原反应无关..的是 A .FeCl 3溶液滴入Mg(OH)2浊液中,白色浑浊转化为红褐色沉淀 B .AgNO 3溶液滴入氯水中,产生白色沉淀,随后淡黄绿色褪去 C .Na 块放在坩埚里并加热,发出黄色火焰,生成淡黄色固体…………外……………○……………线………※在※※装※※订※※线…………内……………○……………线………D .H 2C 2O 4溶液滴入KMnO 4酸性溶液中,产生气泡,随后紫色褪去 3.某科研人员提出HCHO 与O 2在羟基磷灰石(HAP )表面催化氧化生成CO 2、H 2O 的历程,该历程示意图如下(图中只画出了HAP 的部分结构)。
下列说法不正确...的是 A .HAP 能提高HCHO 与O 2的反应速率B .HCHO 在反应过程中,有C —H 键发生断裂C .根据图示信息,CO 2分子中的氧原子全部来自O 2D .该反应可表示为:HCHO+O 2CO 2+H 2O4.我国科研人员借助太阳能,将光解水制H 2与脱硫结合起来,既能大幅度提高光解水制H 2的效率,又能脱除SO 2,工作原理如图所示。
下列说法不正确...的是A .该装置可将太阳能转化为化学能B .催化剂a 表面发生还原反应,产生H 2C .催化剂b 附近的溶液pH 增大D .吸收1 mol SO 2,理论上能产生1 mol H 25.2019年是“国际化学元素周期表年”。
北京市朝阳区2019年高考第一次模拟化学试题及答案

北京市朝阳区2019年高考第一次模拟化学试题及答案一、选择题共42分)本部分共7小题,每小题6分,共42分。
在每小题列出的四个选项中,选出最符合题目要求的一项。
题号 6 7 8 9 10 11 12答案 D C B B A C D第二部分(非选择题共58分)(答案合理均给分)25. (16分)(1)CH 3COOH(2)取代反应(3)羟基羧基(4)(5)2CH 3CH 2OH + HOOC —CH 2—COOH C 2H 5OOC —CH 2—COOC 2H 5+2H 2O(6)ab(7)(8)26.(12分)(1)ab(2)CO 2 + Li 4SiO 4 Li 2CO 3 + Li 2SiO 3(3)①吸热反应物总能量低于生成物总能量(或ΔH >0)② CO 2(g) + H 2O(g) ==CO(g) + H 2(g) +O 2(g) ΔH = +524.8 kJ ·mol -1(4)①氧化② CO 2 + 2e -== CO+O 2-(5)增大压强或及时将生成的C 5H 12分离出去或降低温度27.(14分)(1)SiO 2 + 2NaOH == Na 2SiO 3 + H 2O(2)CaSO 4在水中存在平衡CaSO 4(s)Ca 2+(aq)+ SO 42-(aq),用Na 2CO 3溶液浸泡后,Ca 2+与CO 32-结合成更难溶的CaCO 3,使上述平衡右移,CaSO 4转化成CaCO 3,然后用盐酸除去。
(3)① CaCO 3、Mg(OH)2、SiO 2500℃700℃HO CH —COOHOH △浓H 2SO 4—OH—CH=C —COOC 2H 5COOC 2H 5O C=O CH COOC 2H 5C+ 3NaOH —ONa —CH=C —COONaCOONa+ C 2H 5OH + H 2O② 2Fe3+ + Fe == 3Fe2+(4)将Fe3+还原成Fe2+,防止Fe3+腐蚀锅炉(5)① 2 2 1 1 1Fe2O3 2OH-② bc28. (16分)(1)SO2(2)将反应后的混合物倒入装有冷水的烧杯中,冷却后过滤(3)黑色沉淀中不含有CuO(4)①还原性② 2NO +O2==2NO2③ B试管中出现白色沉淀NO2 + SO2 + Ba2+ + H2O == BaSO4↓+ NO↑+ 2H+④取冷却后A装置答案(5)CuS + 4H2SO4(浓)== CuSO4 + 4SO2↑+ 4H2O△。
2018年北京朝阳高三一模理综化学试题与答案

市区高三年级第一次综合练习理科综合测试(化学)2018.3(考试时间150分钟满分300分)本试卷共17页,共300分。
开始时长150分钟。
考生务必将答案答在答题卡上,在试卷上作答无效。
考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H1 N14 O16 K39 Ar40第一部分(选择题共120分)本部分共20小题,每小题6分,共120分。
在每小题列出的四个选项中,选出最符合题目要求的一项。
6.吉州窑黑釉木叶纹盏是中华名瓷,传统制作过程如下。
其中以化学反应为主的是A.踩泥B.拉坯C.上釉D.烧制7.下列事实不能..用元素周期律解释的是A.碱性:NaOH>Al(OH)3B.相对原子质量:Ar>KC.酸性:HClO4>HIO4D.稳定性:H2O>H2S8. NaCl溶液的电解产物可用于生产盐酸、漂白粉、氢氧化钠等产品。
下列说法不正确...的是A.HCl的电子式:B. NaOH中既含离子键又含共价键C. 电解NaCl溶液时,阴极区pH增大的原因:2H2O + 2e–= 2OH–+ H2↑D.漂白粉露置在空气中:Ca(ClO)2 + CO2 + H2O = CaCO3 + 2HClO9.屠呦呦率领的团队先后经历了用水、乙醇、乙醚提取青蒿素的过程,最终确认只有采用低温、乙醚冷浸等方法才能成功提取青蒿素。
研究发现青蒿素中的某个基团对热不稳定,该基团还能与NaI作用生成I2。
下列分析不正确...的是A.推测青蒿素在乙醚中的溶解度大于在水中的溶解度B.通过元素分析与质谱法可确认青蒿素的分子式C.青蒿素中能将NaI氧化为I2的基团是酯基D.青蒿素中对热不稳定的基团是“”10.液态N2O4是火箭推进系统的有效氧化剂。
实验室制备少量N2O4的流程如下:NH4Cl固体Ca(OH)2NH3NO催化氧化N2O4液体O2NO2降温(红棕色)(无色)下列分析不正确...的是A.反应②、③中氮元素的化合价发生了变化B.反应②利用了NH3的还原性C.反应④的颜色变化是由化学平衡移动引起的D.反应①可由右图所示装置实现11.测溶液pH可研究反应过程。
朝阳区2018~2019学年度第一学期期中高三化学检测
北京市朝阳区2018~2019学年度第一学期高三年级期中统一考试化学试卷(考试时间:90分钟满分:100分)2018.11可能用到的相对原子质量:H 1 C 12 O 16 Na 23 Fe 56第一部分(选择题共42分)每小题只有一个选项符合题意,每小题3分,共14道小题,共42分。
1.垃圾分类并回收利用,符合可持续发展的要求。
下列垃圾归类合理的是2.下列物质的用途利用了水解原理的是A.明矾用作净水剂B.纯碱用于除去粗盐中的钙离子C.四氧化二氮用作火箭燃料的氧化剂D.氢氧化铝用于中和过多的胃酸3.2018年国家文物局对北洋海军军舰“经远舰”进行海上考古,考古队为舰体焊接锌块以实施保护。
下列判断不合理...的是A.焊接锌块后的负极反应:Fe﹣2e- = Fe2+B.上述保护方法中可用镁合金块代替锌块C.腐蚀的正极反应:2H2O + O2 + 4e- = 4OH-D.考古队采用的是牺牲阳极的阴极保护法4.最新版元素周期表已全部填满,联合国将2019年定为国际化学元素周期表年。
鉨(Nh)是113号主族元素,其原子核外最外层电子数是3。
下列说法不正确...的是A.Nh的金属性强于Al B.Nh是第七周期第ⅢA族元素C.Nh的原子半径小于同族元素原子D.Nh在其化合态中主要呈+3价5.下列实验未涉及...氧化还原反应的是6.下列关于元素化合物的化学用语不正确...的是 A .氟离子的结构示意图:B .H 和Cl 形成共价键的过程:H +﹣C .铅蓄电池放电时的负极反应:Pb(s) + SO 2-4(aq) -2e - = PbSO 4(s)D . SO 2氧化H 2S 生成单质硫: 22 + 2H 2O -7. 龋齿是有机酸使牙齿中的Ca 5(PO 4)3(OH)溶解造成的。
饮水、食物里的F - 会将其转化为Ca 5(PO 4)3F ,后者更能抵抗酸的腐蚀。
下列分析不正确...的是 A .溶解度:Ca 5(PO 4)3(OH)<Ca 5(PO 4)3FB .Ca 5(PO 4)3(OH)电离出来的OH -、PO 43- 均能与H + 反应C .牙膏中添加NaF 可发生反应:Ca 5(PO 4)3(OH) + F - = Ca 5(PO 4)3F + OH -D .上述过程涉及的反应类型只有复分解反应 8.下列指定微粒数目一定相等的是A .等质量纯水在25℃、100℃时的H + 数B .等体积等浓度的醋酸与盐酸中的H + 数C .等质量的Fe 与Na 分别与足量Cl 2反应时转移的电子数D .等物质的量的 Na 2O 与 Na 2O 2中含有的阴离子数 9.下列解释事实的方程式不正..确.的是 A .铝热法炼铁:2Al + Fe 2O 32Fe + Al 2O 3B .常温时,0.1 mol ·L -1氨水的pH = 11.1:NH 3·H 2ONH 4++ OH ﹣C .“NO 2球”浸泡在热水中,颜色变深:2NO 2(g)N 2O 4(g) ∆H >0(红棕色) (无色)D .用酸化的H 2O 2溶液从灰化的海带中提碘:H 2O 2 + 2H + + 2I - = I 2 + 2H 2O10.某科研团队研制出“TM—LiH(TM表示过渡金属)”双催化剂体系,显著提高了在温和条件下氮气和氢气合成NH3的效率,原理示意如下:NHLiHLiH状态Ⅰ状态Ⅱ状态Ⅲ下列分析不.合理..的是A.状态Ⅰ,吸收能量并有N≡N键发生断裂B.合成NH3总反应的原子利用率是100%C.“TM—LiH”能降低合成氨反应的∆HD. 生成NH3:2LiNH +3H2=2LiH + 2NH311. CO2催化加氢制取甲醇的研究,对于环境、能源问题都具有重要的意义。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
北京市朝阳区高三年级第一次综合练习理科综合能力测试2019.3可能用到的相对原子质量:H 1 N 14 O 16 S 32 Cl 35.56.我国科技创新成果斐然,下列成果与电化学无关..的是7.下列实验中的颜色变化,与氧化还原反应无关..的是8.某科研人员提出HCHO与O2在羟基磷灰石(HAP)表面催化氧化生成CO2、H2O的历程,该历程示意图如下(图中只画出了HAP的部分结构)。
下列说法不.正确..的是A.HAP能提高HCHO与O2的反应速率B.HCHO在反应过程中,有C—H键发生断裂C.根据图示信息,CO2分子中的氧原子全部来自O2D.该反应可表示为:HCHO + O HAP CO+ H2O29.我国科研人员借助太阳能,将光解水制H2与脱硫结合起来,既能大幅度提高光解水制H2的效率,又能脱除SO2,工作原理如下图所示。
下列说法不.正确..的是A.该装置可将太阳能转化为化学能B.催化剂a表面发生还原反应,产生H2C.催化剂b附近的溶液pH增大D.吸收1 mol SO2,理论上能产生1 mol H210.2019年是“国际化学元素周期表年”。
1869年门捷列夫把当时已知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。
下列说法不正确...的是A.元素甲位于现行元素周期表第四周期第ⅢA族B.原子半径比较:甲>乙>SiC.元素乙的简单气态氢化物的稳定性强于CH4D.推测乙可以用作半导体材料11.一种高分子可用作烹饪器具、电器、汽车部件等材料,其结构片段如下图。
下列关于该高分子的说法正确的是A.该高分子是一种水溶性物质B.该高分子可由甲醛、对甲基苯酚缩合生成C.该高分子的结构简式为D.该高分子在碱性条件下可发生水解反应12.探究铝片与Na2CO3溶液的反应。
下列说法不.正确..的是A.Na2CO3溶液中存在水解平衡:CO32- + H2O ⇌ HCO3- + OH-B.对比Ⅰ、Ⅲ,说明Na2CO3溶液能破坏铝表面的保护膜C.推测出现白色浑浊的原因:AlO2- + HCO3- + H2O = Al(OH)3↓+ CO32-D.加热和H2逸出对CO32-水解平衡移动方向的影响是相反的25.(17分)药物中间体Q、医用材料PV A的合成路线如下。
NH C OH已知:NH2+O C(1)A的分子式是C6H6,A→B的反应类型是。
(2)B→C是硝化反应,试剂a是。
(3)C→D为取代反应,其化学方程式是。
(4)E的结构简式是。
(5)F含有的官能团是。
(6)G→X的化学方程式是。
(7)W能发生聚合反应,形成的高分子结构简式是。
(8)将下列E + W→Q的流程图补充完整(在虚线框内写出物质的结构简式):26.(13分)脱除烟气中的氮氧化物(主要是指NO和NO2)可以净化空气、改善环境,是环境保护的主要课题。
(1)以漂粉精溶液为吸收剂脱除烟气中的NO,相关热化学方程式如下:ⅰ.4NO(g) + 3O2(g) + 2H2O(l) = 4HNO3(aq) ∆H1 =﹣423 kJ·mol-1ⅱ.Ca(ClO)2(aq) = CaCl2(aq) + O2(g) ∆H2 =﹣120 kJ·mol-1ⅲ.3Ca(ClO)2(aq) + 4NO(g) + 2H2O(l) =4HNO3(aq) + 3CaCl2(aq) ∆H3①∆H3 = kJ·mol-1。
②反应ⅲ的平衡常数随温度升高的变化趋势是。
(2)HClO可有效脱除NO,但HClO不稳定,实际应用中常用其盐。
C12和Ca(OH)2制取漂粉精的化学方程式是。
(3)次氯酸盐脱除NO的主要过程如下:a.NO+HClO = NO2+HClb.NO + NO2+H2O ⇌2HNO2c.HClO+ HNO2= HNO3+HCl下列分析正确的是。
A.烟气中含有的少量O2能提高NO的脱除率B.NO2单独存在时不能被脱除C.脱除过程中,次氯酸盐溶液的pH下降(4)研究不同pH、不同温度下漂粉精溶液对NO脱除率的影响,结果如图1、图2。
图1图2①图1中,pH降低NO脱除率增大的原因:。
②脱除过程中往往有Cl2产生,原因是(用离子方程式表示)。
③图2中,60~80℃NO脱除率下降的原因:。
(至少答出两点)27.(13分)以废旧锌锰电池中的黑锰粉(MnO2、MnO(OH)、NH4Cl、少量ZnCl2及炭黑、氧化铁等)为原料制备MnCl2,实现锰的再利用。
其工作流程如下:(1)过程Ⅰ,在空气中加热黑锰粉的目的是除炭、氧化MnO(OH)等。
O2氧化MnO(OH)的化学方程式是。
(2)溶液a的主要成分为NH4Cl,另外还含有少量ZnCl2等。
①溶液a呈酸性,原因是。
②根据右图所示的溶解度曲线,将溶液a(填操作),可得NH4Cl粗品。
③提纯NH4Cl粗品,有关性质数据如下:根据上表,设计方案提纯NH4Cl:。
(3)检验MnSO4溶液中是否含有Fe3+:取少量溶液,加入(填试剂和现象),证明溶液中Fe3+沉淀完全。
(4)探究过程Ⅱ中MnO2溶解的适宜条件。
ⅰ.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
ⅱ.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
①用化学方程式表示ⅱ中MnO2溶解的原因:。
②解释试剂加入顺序不同,MnO2作用不同的原因:。
上述实验说明,试剂加入顺序不同,物质体现的性质可能不同,产物也可能不同。
28.(15分)某小组探究Na2SO3溶液和KIO3溶液的反应。
实验I:向某浓度的KIO3酸性溶液(过量)中加入Na2SO3溶液(含淀粉),一段时间(t秒)后,溶液突然变蓝。
资料:IO3-在酸性溶液氧化I-,反应为IO3- + 5I- + 6H+ = 3I2 + 3H2O(1)溶液变蓝,说明Na2SO3具有性。
(2)针对t秒前溶液未变蓝,小组做出如下假设:i.t秒前未生成I2,是由于反应的活化能(填“大”或“小”),反应速率慢导致的。
ii.t秒前生成了I2,但由于存在Na2SO3,(用离子方程式表示),I2被消耗。
(3)下述实验证实了假设ii合理。
实验II:向实验I的蓝色溶液中加入_______,蓝色迅速消失,后再次变蓝。
(4)进一步研究Na2SO3溶液和KIO3溶液反应的过程,装置如下。
实验III:K闭合后,电流表的指针偏转情况记录如下表:①K闭合后,取b极区溶液加入盐酸酸化的BaCl2溶液,现象是。
②0~t1时,从a极区取溶液于试管中,滴加淀粉溶液,溶液变蓝;直接向a极区滴加淀粉溶液,溶液未变蓝。
判断IO3-在a极放电的产物是。
③结合反应解释t2~t3时指针回到“0”处的原因:。
(5)综合实验I、II、III,下列说法正确的是。
A.对比实验I、II,t秒后溶液变蓝,I中SO32-被完全氧化B.对比实验I、III,t秒前IO3- 未发生反应C.实验III中指针返回X处的原因,可能是I2氧化SO32-北京市朝阳区高三年级第一次综合练习理科综合能力测试 2019.325.(17(1)取代反应(2)浓硫酸、浓硝酸 (3)+ 2NH 3NO 2ClNO 2NH 2+ 2NH 4Cl(4)NH 2NH 2(5)碳碳双键、酯基(6)CH 2CHOC CH 3n +n H 2O +CH 2CHOHn+n CH 3COOH(7)HNHCH 2COOH n(8)NH 2NHC OCH 2NH 2NHNHCOH CH 2NH 226.(13分)(1)① 1783 kJ mol --⋅② 变小(2)()()222222Cl 2Ca OH CaCl Ca ClO 2H O +==++(3)AC(4)① pH 降低,ClO - + H + = HClO ,溶液中()HClO c 增大② HClO + Cl + + H + = Cl 2↑+ H 2O (或22ClO Cl 2H Cl H O --+++=↑+)③ HClO 受热分解,()HClO c 浓度减小;气体溶解度降低;反应b 平衡逆向移动;反应ⅲ平衡逆向移动等(合理即可)27.(13分)(1)()2224MnO OH O 4MnO 2H O +==+(2)① 42NH H O ++⇌32NH H O H +⋅+(或4NH +水解产生H +)② 蒸发浓缩,冷却结晶,过滤③ 加热4NH Cl 粗品至340℃左右,NH 4Cl = NH 3 + HCl ;收集产物并冷却, NH 3 + HCl=NH 4Cl ,得到纯净NH 4Cl 。
(3)KSCN 溶液,不变红(4)① 22224422MnO H O H SO MnSO 2H O O ++==++↑② i 中2MnO 作催化剂,反应快, 2MnO 只催化分解22H O ;ii 中2MnO 作氧化剂,加入稀24H SO 后,2MnO 的氧化性增强,被22H O 还原为 4MnSO 。
28.(15分)(1)还原(2)i .大 ii .222324I SO H O 2I SO 2H ---+++=++ (3)少量23Na SO(4)① 生成白色沉淀 ② I -③ 此时,a 极区发生反应IO 3- + 5I - + 6H + = 3I 2 + 3H 2O ,IO 3- 不再与SO 32-发生反应,外电路无电流通过(5)A C。
