中考化学计算题专题含答案
九年级化学化学计算题题20套(带答案)及解析
九年级化学化学计算题题20套(带答案)及解析一、中考化学计算题1.小王同学为了测定某Na2CO3溶液中溶质的质量分数,取10g该溶液于烧杯中,然后将400g澄清石灰水分四次加入,烧杯中沉淀的质量与每次加入澄清石灰水的质量关系如表。
请计算:第一次第二次第三次第四次加入澄清石灰水100100100100的质量/g生成沉淀的质量0.4m 1.0 1.0/g(1)表中m的值为_____。
(2)Na2CO3溶液中溶质的质量分数_____(写出计算过程)。
【答案】0.8 10.6%【解析】【分析】第一次生成沉淀0.4g,而第三次不到0.4g的3倍,则第二次应该为0.4g的二倍,所以m=0.4g×2=0.8g,根据碳酸钙的质量和对应的化学方程式求算碳酸钠溶液中溶质的质量分数。
【详解】由分析可知,m=0.4g×2=0.8g设原Na2CO3溶液中溶质的质量分数为x。
106100=10g?x 1.0gx=10.6%答:(1)表中的m的值为 0.8。
(2)原Na2CO3溶液中溶质的质量分数是10.6%。
2.将含有杂质(不溶于水)的氯化钡样品12.5g放入39.6g水中充分搅拌,完全溶解后过滤。
取20g滤液与足量的稀硫酸完全反应,得到4.66g沉淀。
请计算:①配制的氯化钡溶液中溶质的质量分数。
②样品中氯化钡的质量分数。
【答案】20.8%;83.2%【解析】【详解】①设参加反应的氯化钡的质量为x 。
2244BaCl +H SO =BaSO +2H 208233x4Cl.66g208233=x 4.66gx= 4.16g则配制的氯化钡溶液中溶质的质量分数为 :4.16g20g×100%=20.8% ②由于20g 溶液中含有4.16g 氯化钡,则可设样品中氯化钡的质量为y 。
则4.16g y=20g-4.16g 39.6gy=10.4g样品中氯化钡的质量分数为:10.4g12.5g×100%=83.2%答:①氯化钡溶液中溶质的质量分数为20.8% ②样品中氯化钡的质量分数为83.2%。
中考化学化学计算题100篇及答案

中考化学化学计算题100篇及答案一、中考化学计算题1.某混合溶液中含有硫酸和盐酸,取该混合溶液20g 于烧杯中,不断滴加氢氧化钡溶液,反应过程中烧杯中产生沉淀的质量、溶液pH 的变化如图所示(BaCl 2溶液呈中性)。
求:(1)完全反应后生成沉淀的质量为_____g ;(2)氢氧化钡溶液的质量分数为_____;(3)计算20g 混合溶液中HCl 的质量为多少?_____【答案】4.66 17.1% 2.92g【解析】【分析】根据图可知,生成4.66g 沉淀消耗的氢氧化钡溶液的质量为20g ,而总消耗的氢氧化钡的溶液的质量为60g ,则与盐酸反应的氢氧化钡溶液的质量为60g ﹣20g =40g ,据此结合对应的化学方程式求算。
【详解】由图可知生成沉淀的质量为4.66g ,与硫酸反应的氢氧化钡溶液的质量为20g 设氢氧化钡溶液的质量分数为x22442Ba(OH)+H SO BaSO +2H O 17123320gx 4.66g ↓=171233=20g 4.66gx x =17.1%与盐酸反应的氢氧化钡溶液的质量为60g ﹣20g =40g设20g 混合溶液中HCl 的质量为y222()1717317.1%40g yBa OH +2HCl BaCl +2H O ⨯=17173=17.1%40g y ⨯y=2.92g故填:(1)4.66;(2)17.1%;(3)2.92g【点睛】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
2.我国化工专家侯德榜发明了侯氏制碱法,为世界制碱工业作出了突出贡献。
(1)主产品Na2CO3的俗名是_____,副产品氯化铵中阳离子符号为_____。
(2)在实际生产中,产品Na2CO3中常混有少量的NaCl,现有样品11.0g,将其放入干净的烧杯中,向烧杯中逐滴加入溶质质量分数为7.3%的稀盐酸,反应后烧杯中物质的质量与滴入稀盐酸的质量关系如图所示。
中考化学计算题及答案(精选)

中考化学计算题及答案(精选)1.用氯酸钾和二氧化锰的混合物16g,加热制取氧气,待完全反应,冷却后称量,得到11.2g固体物质,计算原混合物中二氧化锰的质量(计算结果保留二位小数).2.刘彬同学的姑父从三峡搬迁到我们家乡后,准备兴建一座碳酸钙精粉厂.为检测当地石灰石中碳酸钙的纯度,他在实验室用6g石灰石样品(杂质不参加反应)与19g稀盐酸恰好完全反应,测得残留物为22。
8g。
求:(1)依椐质量守恒定律,生成二氧化碳g;(2)样品中碳酸钙的质量分数;(3)所用稀盐酸溶液中溶质的质量分数。
3.(5分)由硫元素和铜元素组成的一种化合物(硫化物)4.0g,高温条件下在空气中充分煅烧,只得到气体SO2和4。
0g固体CuO .(1)要使煅烧后的固体CuO完全溶解,可加入适量稀硫酸.计算至少需要溶质质量分数为10%的稀硫酸多少克?(要求写出计算所需的化学方程式)(2)运用所学知识和上述数据进行分析,这种硫化物的化学式为。
4.(1)曲酸(C6H6O4)是一种新型添加剂,它具有广泛的抗菌作用,作为防腐剂添加于食品中,具有非常好的效果.曲酸的相对分子质量是,曲酸中碳、氢、氧三种元素的质量比是(2)某工厂的废料中含铁和铜,需回收此废料中的铜.现取铁和铜的混合物样品l0g,向其中加入废弃的稀硫酸50g恰好完全反应,产生0.1gH2.求:①废料中铜的质量分数。
②废弃稀硫酸中硫酸的质量分数。
5.侯德榜是我国著名的化学家。
由他发明的侯氏制碱法制得的纯碱中可能含有少量氯化钠。
现取仅含氯化钠杂质的纯碱样品33.2g,加入130g稀盐酸中,恰好完全反应,得氯化钠溶液150g。
求:(1)该纯碱样品中Na2CO3的质量;(2)反应后所得溶液中溶质的质量分数。
6.(10分)某矿井采出的食盐(俗称井盐)中含有CaCl2,为设计除杂方案需测定CaCl2的含量;取上述井盐22.8g,向其中加入100g 质量分数为10.69%的Na2CO3溶液恰好完全反应.若样品检测过程在露℃的恒温下进行,此时NaCl的溶解度为36g。
中考化学计算题及详细答案

有关化学式的计算题1、计算CuSO4·5H2O的式量______________________________2、计算NH4NO3中所含各元素的质量比_________________________________3、某黄铁矿中含FeS2为72%,计算该黄铁矿中硫元素的质量分数是()A.36%B.38.4%C.42.6%D.48%4、某元素R的单质跟氧气化合生成的氧化物中,R元素跟氧元素的质量比为21:8,原子个数比为3:4,又知氧元素的相对原子质量为16,则元素R的相对原子质量为()A.24B.27C.56D.655、在SO3和SO2的两种物质中,相同的是()A.氧元素的质量分数B.硫元素的质量分数C.元素种类D.原子个数比6、A、B两种化合物均由R和氧两种元素组成的,在化合物A和B中,R元素的质量分数分别为50%和40%,若A的化学式为RO2,则B的化学式为() A.R2O B.RO C.R2O3 D.RO37、在FeSO4和Fe2 (SO4) 3的混合物中,氧元素的质量分数为a%,则该混合物中铁元素的质量分数为()A.2a%B.1-a%C.1-0.5a%D.1-1.5a%8、甲、乙两种化合物x2y和yz2中,y元素的质量分数分别约为40%和50%,则在丙化合物x2yz3中y 元素的质量分数约为()A.20% B.25% C.30% D.35%(一)标签型化学式计算题:1、锌是人体健康必需的元素,锌缺乏容易造成发育障碍,易患异食癖等病症,使人体免疫功能低下。
市售的葡萄糖酸锌口服液对治疗锌缺乏病具有较好的疗效。
下图是某品牌葡萄糖酸锌口服液的标签,请根据标签信息回答:(1)葡萄糖酸锌中各元素的质量比;(3)某患者除正常饮食吸锌元素外,还需服用该品牌葡萄糖酸锌口服液。
若治疗一个疗程需补充104mg锌元素,而这些锌有75%来自该口服液,则患者共需服用支葡萄糖酸锌口服液?(简写出解题过程)(二)叙述型化学式计算题:1、蛋白质是由多种氨基酸[丙氨酸:CH3CH(NH2)COOH等]构成的极为复杂的化合物,人体通过食物获得蛋白质,在胃肠道里与水发生反应,生成氨基酸,试计算:(1)丙氨酸分子中氮原子与氧原子的个数比。
最新中考化学化学计算题专项训练及答案.docx

最新中考化学化学计算题专项训练及答案一、中考化学计算题1.将 20.0g 稀盐酸逐滴加入到10.0g 溶质质量分数为40%的氢氧化钠溶液中,边滴加边搅拌,随着稀盐酸的滴加,溶液的 pH 变化情况如图所示,溶液的温度变化如表所示(不考虑反应过程中热量散失)反应时间0102030405060(s)溶液温度20.520.620.720.820.920.820.7(℃)_____℃(1)当稀盐酸与氢氧化钠溶液恰好完全反应时,溶液的温度是(2)计算稀盐酸中溶质的质量分数_________(精确到0.1%)【答案】 20.9 36.5%【解析】【分析】根据图表可知当反应时间为40 秒时,溶液的温度最高,所以当40 秒时,反应恰好完全反应。
当 pH 为 7 的时候,恰好完全反应,根据氢氧化钠的质量可以求出盐酸的质量分数。
【详解】(1)因为中和反应是放热反应,所以温度最高时恰好完全反应,所以恰好完全反应时的温度从表上可知为 20.9 ℃(2)设参加反应的盐酸的质量为xx=3.65g36.5%所以参加反应的盐酸的质量是36.5%。
2.某混合溶液中含有硫酸和盐酸,取该混合溶液20g 于烧杯中,不断滴加氢氧化钡溶液,反应过程中烧杯中产生沉淀的质量、溶液pH 的变化如图所示(BaCl2溶液呈中性)。
求:(1)完全反应后生成沉淀的质量为_____g;(2)氢氧化钡溶液的质量分数为 _____;(3)计算 20g 混合溶液中 HCl 的质量为多少? _____【答案】 4.66 17.1% 2.92g【解析】【分析】根据图可知,生成 4.66g 沉淀消耗的氢氧化钡溶液的质量为液的质量为60g,则与盐酸反应的氢氧化钡溶液的质量为化学方程式求算。
20g,而总消耗的氢氧化钡的溶60g﹣20g=40g,据此结合对应的【详解】由图可知生成沉淀的质量为 4.66g,与硫酸反应的氢氧化钡溶液的质量为20g 设氢氧化钡溶液的质量分数为xBa(OH) 2+H2SO4=BaSO4+2H 2O17123320gx 4.66g171 =23320gx 4.66gx= 17.1%与盐酸反应的氢氧化钡溶液的质量为60g﹣ 20g= 40g设 20g 混合溶液中HCl 的质量为 yBa(OH)2+2HCl=BaCl2+2H 2O1717317.1% 40g y171=73 17.1% 40g yy=2.92g故填:( 1) 4.66;( 2) 17.1%;( 3) 2.92g【点睛】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整。
(化学) 中考化学化学计算题专项训练100(附答案)

(化学)中考化学化学计算题专项训练100(附答案)一、中考化学计算题1.将含有NaCl杂质的某烧碱样品10 g完全溶于90 g水中,再向所得溶液中慢慢滴入溶质质量分数为7.3%的稀盐酸。
在实验过程中,溶液的pH与滴入稀盐酸的质量关系如图所示。
(1)求10 g该样品中氢氧化钠的质量。
(2)求a点时,溶液中溶质的质量分数(计算结果精确到0.1%)。
【答案】(1)8 g (2)6.9%【解析】当恰好完全反应时消耗的盐酸溶液的质量为100g,对应的HCl的质量为100g×7.3%=7.3g设氢氧化钠的质量为x,生成的氯化钠的质量为yNaOH+HCl═NaCl+H2O40 36.5 58.5x 7.3g y==x=8gy=11.7ga点时,溶液中溶质的质量分数为×100%≈6.9%答:(1)l0g该样品中氢氧化钠的质量为8g.(2)a点时,溶液中溶质的质量分数约为6.9%2.化学兴趣小组取26g石灰石样品(杂质不参加反应,也不溶于水)放在烧杯中,向其中加入90g稀盐酸,恰好完全反应,反应后烧杯中物质的总质量为105g,计算:(1)生成二氧化碳的质量是____。
(2)反应后所得溶液的溶质质量分数是____。
【答案】(1)11克(2) 26.7%【解析】试题解析:由质量守恒定律可以知道反应前的各物质的总质量等于反应后各物质的总质量的,所以二氧化碳的质量=26+90-105=11克,反应后的溶质是CaCl2,而溶液的质量等于105克减去石灰石中的不反应的杂质的质量,设:石灰石中CaCO3质量为X,生成的CaCl2质量为Y,CaCO3+ 2HCl==CaCl2 + CO2↑ + H2O100 111 44X Y 11克列比例式:100:X=44::11克解得:X=25克111:Y=44:11克解得:Y="27.75" 克反应后所得溶液的溶质质量分数=27.75/105-(26-25)×100%≈26.7%考点:质量守恒定律及其根据化学方程式的计算溶液的相关计算3.徐州地区石灰石资源丰富。
初中化学计算题大全(含答案及解析)

2024年中考化学《必考经典》计算题大全(含答案及解析)1.实验室欲测定一瓶标签破损的稀硫酸中溶质的质量分数,现取10g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液pH的变化情况如图所示。
分析并计算:(1)a点溶液中含有的离子是_____。
(2)当pH=7时,消耗氢氧化钠溶液中NaOH质量为_____g。
(3)计算稀H2SO4中溶质的质量分数。
_____(4)计算恰好完全反应时所得溶液的溶质质量分数。
_____【答案】Na+、H+、SO42- 0.8 稀H2SO4的溶质质量分数是9.8%;恰好完全反应时所得溶液的溶质质量分数是5.5%。
【解析】【详解】(1)由图示可知,在a点时溶液的pH小于7,说明加入的NaOH完全反应,有剩余的硫酸,所以,溶液中含有的离子为:Na+、H+、SO42-;(2)由图示可知,在溶液的pH等于7,消耗的NaOH溶液的质量为16g,溶质的质量为:16g×5%=0.8g;(3)10g稀硫酸样品含有H2SO4的质量为x,生成的硫酸钠的质量为y2NaOH+H SO=Na SO+2H O2424280981420.8g x y解得:x=0.98g y=1.42g稀H2SO4的溶质质量分数为:×100%=9.8%;(4)恰好完全反应时所得溶液的溶质质量分数:×100%≈5.5%。
2.某小组同学将530 g碳酸钠溶液加入到280 g石灰乳(水和氢氧化钙的混合物)中,使之恰好完全反应,所得溶液中溶质的质量分数为1%,计算加入的碳酸钠溶液中溶质的质量分数。
【答案】2%【解析】【详解】设原碳酸钠溶液中溶质的质量为xNa2CO3+ Ca(OH)2=CaCO3↓+ 2NaOH106 100 80X则解得x =10.6g所以加入的碳酸钠溶液中溶质的质量分数为答:加入的碳酸钠溶液中溶质的质量分数为2%。
3.取一定量的氯化钠与氢氧化钠的混合物,加一定量的水配成溶液,然后向其中滴加溶质质量分数为7.3%稀盐酸,直至恰好反应,共消耗稀盐酸50g。
(word完整版)初三中考化学专题练习--计算题(含参考答案最新)
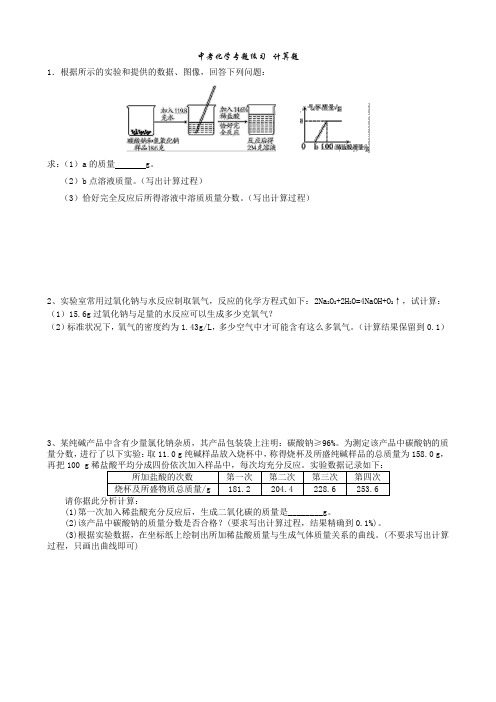
中考化学专题练习--计算题1.根据所示的实验和提供的数据、图像,回答下列问题:求:(1)a的质量 g。
(2)b点溶液质量。
(写出计算过程)(3)恰好完全反应后所得溶液中溶质质量分数。
(写出计算过程)2、实验室常用过氧化钠与水反应制取氧气,反应的化学方程式如下:2Na2O2+2H2O=4NaOH+O2↑,试计算:(1)15.6g过氧化钠与足量的水反应可以生成多少克氧气?(2)标准状况下,氧气的密度约为1.43g/L,多少空气中才可能含有这么多氧气。
(计算结果保留到0.1)3、某纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%。
为测定该产品中碳酸钠的质量分数,进行了以下实验:取11.0 g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0 g,再把100 g(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是________g。
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)。
(3)根据实验数据,在坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线。
(不要求写出计算过程,只画出曲线即可)4.工业盐酸中通常溶有少量的FeCl3而呈黄色,小红为测定某工业盐酸中HCl的含量进行如下实验:取某工业盐酸l00g,滴加一定溶质质量分数的NaOH溶液,测得加入NaOH溶液质量与反应生成的沉淀质量关系如图所示。
请回答下列问题:(1)FeCl3与NaOH恰好完全反应时,生成沉淀的质量是________g。
(2)计算氢氧化钠溶液的溶质质量分数。
(写出计算过程)(3)该工业盐酸中HCl的质量分数是_________。
5、钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。
某补钙药剂主要成分为碳酸钙,现将100g盐酸分成5等份,逐次加到用40g该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象。
请根据有关信息回答问题:序号第1次第2次第3次第4次第5次加入盐酸的质量/g 20 20 20 20 20剩余固体的质量/g 35 30 25 20 a(1)a的数值为________,该品牌补钙药剂中CaCO3的质量分数是_________。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学计算题专题一、计算题(共29题;共121分)1.某碳酸钠样品含有少量的氯化钠,取12.5g的该样品,完全溶解在水中配制成60g溶液,将其全部加入到50g一定质量分数的盐酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质量是105.6g,计算:(1)生成气体的质量为________ g。
(2)求所得溶液中溶质质量分数(计算结果精确到0.1%)。
【答案】(1)4.4g(2)解:设样品中Na2CO3的质量为x,生成NaCl的质量为yNa2CO3+ 2HCl= 2NaCl+H2O+ CO2↑106 117 44x y 4.4g则所设溶液中溶后的质量分数为:答:所得溶液溶后质量分数为12.9%。
2.镁条具有抗腐蚀性,是因为表面生成了一层氧化物膜,化学实验小组同学为研究镁条表面氧化程度,将3.2g镁条放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图所示(假设镁条除有MgO外,不含其他杂质)。
(1)生成氢气的质量为________g。
(2)该镁条中MgO的质量分数为________。
(3)所用稀盐酸中溶质的质量分数为多少?(写出计算过程)【答案】(1)0.2(2)25%(3)解:设用于产生氢气消耗的盐酸中溶质的质量为xMg + 2HCl = MgCl2+ H2↑73 2x 0.2gX=7.3g稀盐酸中溶质的质量分数为:7.3g÷(125.0g-20.0g)*100%=7.3%答:所用稀盐酸中溶质的质量分数为7.3%。
3.在含少量NaCl的某纯碱样品23g中加入盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。
(提示:相关反应为:Na2CO3+2HCl=2NaCl+H2O+CO2↑)计算当恰好完全反应时:(1)产生的二氧化碳的质量是________克。
(2)此纯碱样品中碳酸钠的质量分数________(写出必要的计算过程,结果保留到0.1%)。
【答案】(1)8.8(2)解:设纯碱样品中碳酸钠的质量分数为xx≈92.2%答:纯碱样品中碳酸钠的质量分数为92.2%。
4.向氯化钠和氯化钡的混合溶液中加入碳酸钠溶液。
反应过程中滴加碳酸钠溶液的质量与生成沉淀的质量关系如图所示,请计算:(1)m的值是________g。
(2)碳酸钠溶液的质量分数是多少?【答案】(1)5.91(2)解:设20g碳酸钠溶液中含溶质质量为xBaCl2+ Na2CO3=BaCO3↓+2NaCl106 197x 1.97gx=1.06g碳酸钠溶液的质量分数是×100%=5.3%答:碳酸钠溶液的质量分数是5.3%。
5.为防止汶川地震灾区的病菌传播,防疫人员大量使用了“漂白粉”来杀菌消毒,“漂白粉”的有效成分为次氯酸钙[化学式为:Ca(ClO)2]。
请回答:(1)钙、氧、氯三种元素的质量比为________ 。
(2)次氯酸钙中氯元素的质量分数是________(精确到0.1%)。
【答案】(1)40:71:32(2)49.76.某纯碱样品中混有少量的氯化钠,为了测定样品的纯度,做如下实验:准确称取样品12.0 g ,向其中加入57.9 g稀盐酸,恰好完全反应,共产生气体4.4 g ,求:所得溶液溶质的质量分数是多少?(精确到0.1%)【答案】解:设生成的氯化钠质量为x,碳酸钠质量为yNa2CO3+2HCl=2NaCl+H2O+CO2↑10611744y x 4.4gx=11.7g y=10.6g所得溶液溶质质量分数为.7.长久使用的热水壶底部有一层水垢,主要成分是碳酸钙(CaCO3),某化学兴趣小组为了测定水垢中碳酸钙的质量分数,取25g水垢放入过量的稀盐酸的烧杯中,立即将烧杯放在天平上,称其质量。
在以后的5min内,每一分钟读一次数。
结果如下表,试回答下列问题:(1)反应生成的二氧化碳的质量为多少?(2)该水垢中CaCO3的质量分数为多少?【答案】(1)反应生成的二氧化碳的质量为100g-91.2g=8.8g(2)80%8.化学兴趣小组为测定某铜锌合金中成分金属的含量,称取10g样品放入烧杯中,向其中加入100g稀硫酸,样品中的锌恰好完全反应,此时测得烧杯内物质的总质量为109.8g。
请完成下列分析及计算:(1)硫酸(H2SO4)中硫元素的质量分数为________(计算结果精确到0.1%)。
(2)反应中共生成气体________g。
(3)计算样品中铜的质量分数。
【答案】(1)32.7%(2)0.2(3)解:设参加反应的锌的质量为xZn+H2SO4= ZnSO4+ H2↑65 2x 0.2gx=6.5g铜锌合金中铜的质量分数×100%=35.0%答:铜锌合金辆的质量分数为35.0%.9.小文同学取瑞金市石灰石样品20g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量如表所示。
试求:(1)m的值为________;(2)第________次为恰好完全反应:(3)计算该石灰石样品中碳酸钙的质量分数。
(写出计算过程)【答案】(1)3.3(2)4(3)解:设石灰石样品中碳酸钙的质量为x。
CaCO3+2HCl=CaCl2+ CO2↑+H2O100 44x 4.4gx=10g石灰石样品中碳酸钙的质量分数= ×100%=50%答:石灰石样品中碳酸钙的质量分数为50%10.为测定某石灰石样品中碳酸钙的质量分数,取26g石灰石样品放在烧杯中,然后向其中逐渐加入稀盐酸,使之与样品充分反应,恰好完全反应(杂质不参加反应)时,加入稀盐酸的质量为90g,反应后烧杯中物质的总质量为107.2g。
请计算:(1)计算生成二氧化碳的质量________;(2)样品中碳酸钙的质量分数________(结果保留到0.1%)。
【答案】(1)8.8g(2)76.9%11.已知一个氧原子的质量为2.657×10﹣26kg,一个碳﹣12原子的质量为1.993×10﹣26kg,则氧原子的相对原子质量为________.(最后结果保留整数)【答案】1612.现有10克混合气体,其成分为CO和CO2,将该混合气体通入足量的澄清石灰水中,充分反应后得到10克白色沉淀。
则原混合气体中CO的质量分数是________。
【答案】56%13.向10g大理石样品(杂质不溶于水,也不与盐酸反应)分两次加入一定溶质质量分数的稀盐权,充分反应后烧杯内物质内物质总质量变化如图所示。
请计算:(1)生成的二氧化碳的质量是________;(2)大理石中碳酸钙的质量分数是多少?【答案】(1)3.3g(2)75%14.为防治碘缺乏病,我国正推广食用加碘盐,即在食盐中加入适量碘酸钾(化学式为KIO3),严禁出售不含碘的工业盐.下面请按要求解题(1)KIO3中碘元素的化合价为A.+1B.+3C.+4D.+5(2)KIO3中碘元素的质量分数是多少?(结果保留三位数字)(3)正常人每天需要补充大约0.1mg碘元素.若1000g碘盐中约含33.7mg碘酸钾,那么一个正常人一天大约需要吃多少克这种含碘盐?(结果取整数)【答案】(1)D(2)59.3%(3)5g15.甲醇是一种无色、有特殊香味、易挥发的液体,可用于制造甲醛和农药等。
已知:甲醇由碳、氢、氧三种元素组成,其中氢元素的质量分数为12.5%、氧元素的质量分数为50%;一个甲醇分子中含有4个氢原子。
请通过计算回答下列问题(1)甲醇的化学式量(即相对分子质量)是________;(2)一个甲醇分子中含氧原子的个数是________ 。
(3)64g甲醇中碳元素的质量为________ g。
【答案】(1)32(2)1(3)2416.某纯碱样品中含有少量氯化钠。
现称量该样品15.4g放入烧杯中,再向其中加入一定溶质质量分数的稀盐酸至100g时恰好完全反应。
此时烧杯内的物质质量为111g。
试计算:(1)碳酸钠中钠元素、碳元素、氧元素的质量比为________;(化为最简比)(2)反应后生成的气体质量为________g;(3)恰好完全反应时所得溶液中溶质的质量分数________。
(计算结果精确到0.1%)【答案】(1)23:6:24(2)4.4(3)14.9%17.把干燥纯净的氯酸钾和二氧化锰混合物16克装入大试管后,给试管加热至完全反应后冷却称量,试管中固体物质质量为11.2克。
请计算:(1)氯酸钾中氧元素的质量分数是________(保留一位小数);(2)反应产生的氧气的质量是________克;(3)试管中残留固体物质有哪些?其质量各是多少?________(写出计算过程)【答案】(1)39.2%(2)4.8(3)氯化钾和二氧化锰;氯化钾的质量为7.45g,二氧化锰的质量为3.75g18.将4.0 g Cu-Zn合金粉末放到盛有10g稀硫酸的烧杯中,恰好完全反应,Cu不与硫酸反应。
相关实验数据如下:(1)生成氢气的质量是________;(2)若不考虑该合金中除Cu、Zn以外的其他成分,请计算原Cu-Zn合金中Zn的质量。
写出要的计算过程。
【答案】(1)0.04g(2)1.3g19.为了减缓温室效应,改善人类居住环境,人类发明了一种“ 人造树叶”,可吸收二氧化碳并转化为乙解(C2H5OH)燃料,化学方程式为。
研究表明,一升“人造树叶”每天可从空气中吸收968gCO2。
请问:(1)一升“人透树叶”工作一天可得到乙醇的质量是多少________?(2)若每天一棵树平均可吸收48.4gC O2 ,则一升“人造树叶” 每天吸收的CO2相当于________棵树吸收的CO2。
【答案】(1)506g(2)2020.某补钙药剂的标签主要内容如图所示,现测定该钙片含量是否符合标注,做如下实验:取10片该钙片,放入干燥、洁净的烧杯中,再向烧杯中加入50g某浓度稀盐酸,恰好完全反应(钙片中其他成分不溶于水,也不和稀盐酸反应,反应中产生的气体全部放出),反应后称量烧杯内剩余物质的质量为64.5g.(1)反应中生成多少克二氧化碳________?(2)通过计算说明实际钙含量是否与标注相符________?(3)试计算所用稀盐酸的溶质质量分数________。
【答案】(1)5.5g(2)不相符(3)18.25%21.鸡蛋壳的主要成分是碳酸钙(其他成分不与水和盐酸反应)。
为了测定鸡蛋壳中碳酸钙的含量,进行如下实验:请回答下列问题:(1)生成二氧化碳的质量为________ g;(2)计算鸡蛋壳中碳酸钙的质量分数;________。
【答案】(1)8.8(2)80%22.某炼铁厂月产含铁97%的生铁23072 t , 该厂需储备含氧化铁80%的赤铁矿原料至少不低于________吨?【答案】39964t23.某钢铁厂每周计划生产生铁(含Fe 97%)30000t。
