平衡常数K专题解析
平衡常数

高考热点—四大平衡常数自从新课程引人平衡常数以后,化学平衡常数、电离平衡常数、溶度积常数以及水的离子积常数等四大平衡常数就成为高考的热点,倍受命题者的青睐.一、化学平衡常数1.概念:对于一定温度下的可逆反应,无论反应物的起始浓度如何,反应达平衡状态后,生成物浓度的幂之积与反应物浓度幂之积的比值是一个常数,这个常数即该反应的化学平衡常数.用符号K表示. 2.书写: (l)同一化学反应,可以用不同的化学反应式来表示,每个化学方程式都有自己的平衡常数关系式及相应的平衡常数. (2)稀溶液中进行的反应,如有水参加,水的浓度也不必写在平衡关系式中. (3)非水溶液中的反应,如有水生成或有水参加反应,此时水的浓度不可视为常数,必须表示在平衡关系式中. (的若干方程式相加(减),则总反应的平衡常数等于分步平衡常数之乘积(商). 3.注意点(l)化学平衡常数K只与温度有关;固体或纯液体的浓度看作“1”,不代人公式. (2)化学平衡常数表示可逆反应进行的程度.K值越大,表示反应进行得越完全;K值越小,表示反应进行得越不完全. (3)反应的平衡常数是指某一指定的反应,若反应方向改变,则K改变.若反...... (专题8·化学平衡常数解题策略化学平衡常数与化学平衡及其影响因素的关系是高考命题的趋势之一。
化学平衡常数的引入,对判断化学平衡移动方向带来了科学的依据。
平衡常数是表征反应限度的一个确定的定量关系,是反应限度的最根本的表现。
平衡常数的使用,从定量的角度解决了平衡的移动。
一、化学平衡常数在一定温度下,可逆反应无论从正反应开始还是从逆反应开始,无论反应混合物的起始浓度是多少,当反应达到平衡状态时,正反应速率等于逆反应速率,反应混合物中各组成成分的含量保持不变,即各物质的浓度保持不变。
生成物浓度的幂次方乘积与反应物浓度的幂次方乘积之比是常数,这个常数叫化学平衡常数,用K表示。
化学平衡常数的计算公式为:对于可逆反应:mA(g)+nB(g)pC(g)+qD(g)二、化学平衡常数意义1、化学平衡常数K表示可逆反应进行的程度。
高一化学 专题15 化学平衡常数及反应自发性 含解析

专题15 化学平衡常数及反应自发性【知识回顾】一、化学平衡常数1.概念:在一定温度下,一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数比值,用符号K 表示。
2.表达式:对于一般的可逆反应:m A(g)+n B(g)p C(g)+q D(g),在一定温度下达到平衡时:K =()()()()p q m n c C c D c A c B 。
3.注意事项:(1)表达式中各物质的浓度是平衡时的浓度,不是起始浓度也不是物质的量。
(2)对于一个具体的可逆反应,平衡常数K 只与温度(T )有关,与反应物或生成物的浓度无关。
(3)正逆反应的化学平衡常数不一样,互为倒数关系。
(4)反应物或生成物中有固体或纯液体存在时,由于其浓度看视为常数,是固定不变的,不能代入平衡常数表达式中。
(5)化学平衡常数是指某一具体反应的平衡常数。
若化学方程式中各物质的化学计量数等倍扩大或缩小,尽管是同一反应,平衡常数也会改变。
(6)稀溶液中进行的反应,如有水参加,水的浓度不必写在平衡常数表达式中。
4.化学平衡常数K 的应用(1)化学平衡常数值的大小是可逆反应进行程度的标志。
K 值越大,说明平衡时生成物的浓度越大,反应物的浓度越小,它的正向反应进行的程度越大,即该反应进行得越完全,反应物转化率越高。
反之,则相反。
一般地,K >105时,该反应就进行得基本完全了。
可以说,化学平衡常数是在一定温度下一个反应本身固有的内在性质的定量体现。
(2)可以利用K 值做标准,判断正在进行的可逆反应是否平衡及不平衡时向何方进行建立平衡。
(Q :浓度积)对于可逆反应a A(g)+b B(g)c C(g)+d D(g),在一定温度下的任意时刻,反应物与生成物浓度有如下关系:()()()()p q m n c C c D c A c B =Q c , Q c ⎩⎪⎨⎪⎧ <K 反应向正反应方向进行,v 正>v 逆=K 反应处于化学平衡状态,v 正=v 逆>K 反应向逆反应方向进行,v 正<v 逆。
C3H3化学微专题—化学平衡常数

温度下,反应 2HI(g) H2(g)+I2(g)的平衡常数为K11,故反应
HI(g) 12H2(g)+12I2(g)的平衡常数 K2=
K11,故 K1=K122。
2.某温度下 2 L 密闭容器中 3 种气体起始状态和平衡状态时 的物质的量(n)如表所示,下列说法正确的是 ( )
n(起始状态)/mol n(平衡状态)/mol
n衡(H常2O数)=减0小.2,0 故mo正l,反说应明为放t1 m热i反n 时应反,B应项已错经误达;到保平持衡其状他态条,件根
据不化变学,方向程平式衡可体知系,中达再到通平入衡0时.20nm(CoOl H2)2=O0(g.4)和0 m0o.4l,0 Dmo项l 正确。
6.在一定温度下,1 L 的密闭容器中发生反应:C(s)+H2O(g) CO(g) +H2(g),平衡时测得 C、H2O、CO、H2 的物质的量都为 0.1 mol。 (1)该反应的平衡常数 K=___0_._1___。 (2)若升高平衡体系的温度,该反应的平衡常数会增大, 则该反应的 ΔH____>____0(填“>”或“<”)。 (3)相同条件下,向该密闭容器中充入各物质的起始量如下: ①均为 0.2 mol ②C(s)、H2O 为 0.2 mol,CO、H2 为 0.1 mol,判断该反应进行的方向:①_向__逆__反__应__方__向_____, ②_向__正__反__应__方__向_____。
起始(mol)
ab
00
变化(mol) mx nx
px qx
平衡(mol) a-mx b-nx
px qx
对于反应物:n(平)=n(始)-n(变)
对于生成物:n(平)=n(始)+n(变)
则有:(1)平衡常数:K=
第八章-水溶液中的离子平衡热点专题(五)四大平衡常数的重要应用资料讲解

第八章水溶液中的离子平衡热点专题(五)四大平衡常数的重要应用第八章水溶液中的离子平衡热点专题(五)四大平衡常数的重要应用四大平衡常数的比较 对于一般的可逆反应: m A(g)+n B(g)p C(g)+q D(g),在一定温度下达到平衡时:K =c p C ·c q D c m A ·c n B(1)对于一元弱酸HA : HAH ++A -,电离常数K a =c H +·c A -c HA(2)对于一元弱碱BOH : BOHB ++OH-,电离常数K b =错误!影响因素只与温度有关只与温度有关,升高温度,K 值增大只与温度有关,升高温度,K w 增大只与难溶电解质的性质和温度有关考点一 化学平衡常数常考题型1.求解平衡常数;2.由平衡常数计算初始(或平衡)浓度; 3.计算转化率(或产率);4.应用平衡常数K 判断平衡移动的方向(或放热、吸热等情况)。
对 策从基础的地方入手,如速率计算、“三阶段式”的运用、阿伏加德罗定律及其推论的应用、计算转化率等,这些都与化学平衡常数密不可分(严格讲电离平衡、水解平衡、沉淀溶解平衡也是化学平衡,只是在溶液中进行的特定类型的反应而已),要在练习中多反思,提高应试能力。
[应用体验]1.高炉炼铁过程中发生的主要反应为13Fe 2O 3(s)+CO(g)23Fe(s)+CO 2(g)。
已知该反应在不同温度下的平衡常数如下:温度/℃ 1 000 1 150 1 300 平衡常数4.03.73.5请回答下列问题:(1)该反应的平衡常数表达式K =________,ΔH ________0(填“>”“<”或“=”); (2)在一个容积为10 L 的密闭容器中,1 000 ℃时加入Fe 、Fe 2O 3、CO 、CO 2各 1.0 mol ,反应经过10 min 后达到平衡。
求该时间范围内反应的平均反应速率v (CO 2)=________,CO 的平衡转化率=________。
2020高考化学冲刺核心素养专题 四大平衡常数(Ka、Kh、Kw、Ksp)的综合应用含解析
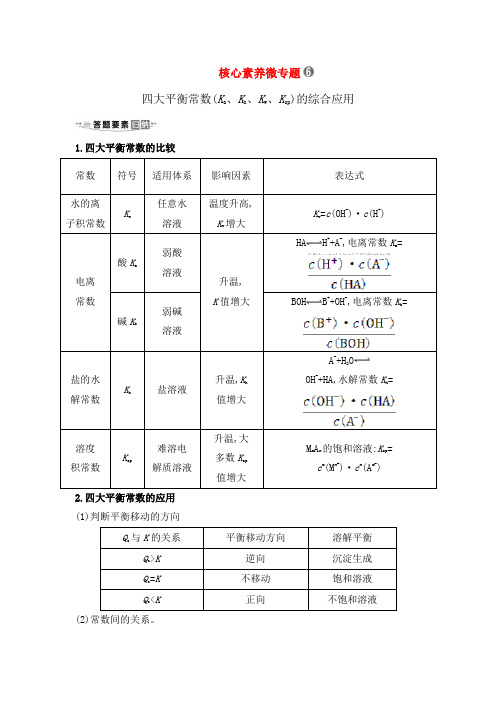
核心素养微专题四大平衡常数(K a、K h、K w、K sp)的综合应用1.四大平衡常数的比较常数符号适用体系影响因素表达式水的离子积常数Kw任意水溶液温度升高,Kw增大Kw=c(OH-)·c(H+)电离常数酸K a弱酸溶液升温,K值增大HA H++A-,电离常数K a= 碱K b弱碱溶液BOH B++OH-,电离常数K b=盐的水解常数Kh盐溶液升温,K h值增大A-+H2OOH-+HA,水解常数K h=溶度积常数Ksp难溶电解质溶液升温,大多数K sp值增大M m A n的饱和溶液:K sp=c m(M n+)·c n(A m-)2.四大平衡常数的应用(1)判断平衡移动的方向Qc与K的关系平衡移动方向溶解平衡Qc>K逆向沉淀生成Qc=K不移动饱和溶液Qc<K正向不饱和溶液(2)常数间的关系。
①K h=②K h=(3)判断离子浓度比值的大小变化。
如将NH3·H2O溶液加水稀释,c(OH-)减小,由于电离平衡常数为,此值不变,故的值增大。
(4)利用四大平衡常数进行有关计算。
【典例】(2019·武汉模拟)(1)用0.1 mol·L-1 NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 mol·L-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
①滴定醋酸的曲线是________(填“Ⅰ”或“Ⅱ”)。
②V1和V2的关系:V1________V2(填“>”“=”或“<”)。
(2)25 ℃时,a mol·L-1的醋酸与0.01 mol·L-1的氢氧化钠溶液等体积混合后呈中性,则醋酸的电离常数为________。
(用含a的代数式表示)。
【审题流程】明确意义作判断,紧扣关系解计算【解析】(1)①醋酸为弱酸,盐酸为强酸,等浓度时醋酸的pH大,曲线Ⅱ为滴定盐酸曲线,曲线Ⅰ为滴定醋酸曲线,答案填Ⅰ;②醋酸和氢氧化钠恰好完全反应时,得到的醋酸钠溶液显碱性,要使溶液pH=7,需要醋酸稍过量,而盐酸和氢氧化钠恰好完全反应,得到的氯化钠溶液显中性,所以。
2020高考化学冲刺核心素养微专题: 6 四大平衡常数(Ka、Kh、Kw、Ksp)的综合应用
温馨提示:此套题为Word版,请按住Ctrl,滑动鼠标滚轴,调节合适的观看比例,答案解析附后。
关闭Word文档返回原板块。
核心素养微专题四大平衡常数(K a、K h、K w、K sp)的综合应用1.四大平衡常数的比较常数符号适用体系影响因素表达式水的离子积常数K w任意水溶液温度升高,K w增大K w=c(OH-)·c(H+)电离常数酸K a弱酸溶液升温,K值增大HA H++A-,电离常数K a=碱K b弱碱溶液BOH B++OH-,电离常数K b=盐的水解常数K h盐溶液升温,K h值增大A-+H2OOH-+HA,水解常数K h=溶度积常数K sp难溶电解质溶液升温,大多数K spM m A n的饱和溶液:K sp=c m(M n+)·值增大c n(A m-)2.四大平衡常数的应用(1)判断平衡移动的方向Q c与K的关系平衡移动方向溶解平衡Q c>K逆向沉淀生成Q c=K不移动饱和溶液Q c<K正向不饱和溶液(2)常数间的关系。
①K h=②K h=(3)判断离子浓度比值的大小变化。
如将NH3·H2O溶液加水稀释,c(OH-)减小,由于电离平衡常数为,此值不变,故的值增大。
(4)利用四大平衡常数进行有关计算。
【典例】(2019·武汉模拟)(1)用0.1 mol·L-1NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 mol·L-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
①滴定醋酸的曲线是________(填“Ⅰ”或“Ⅱ”)。
②V1和V2的关系:V1________V2(填“>”“=”或“<”)。
(2)25 ℃时,a mol·L-1的醋酸与0.01 mol·L-1的氢氧化钠溶液等体积混合后呈中性,则醋酸的电离常数为________。
(用含a的代数式表示)。
2023届高考化学小专题:《“三段式”在平衡常数、转化率计算中的完美应用》

1.O3是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O3可溶于 水,在水中易分解,产生的[O]为游离氧原子,有很强的杀菌消毒能力。常温
常压下发生的反应如下:
反应① O3 O2+[O] ΔH>0 平衡常数为K1; 反应② [O]+O3 2O2 ΔH<0 平衡常数为K2; 总反应:2O3 3O2 ΔH<0 平衡常数为K。 下列叙述正确的是
“三段式”突破平衡常数(K)、转化率的相关计算
1.一个模式——“三段式”
如mA(g)+nB(g) pC(g)+qD(g),令A、B起始物质的量浓度分别为a mol·L -1、b mol·L-1,达到平衡后消耗A的物质的量浓度为mx mol·L-1。
mA(g)+nB(g) pC(g)+qD(g)
c始/mol·L-1 a
(1)该反应正反应为__吸___(填“吸”或“放”)热反应,温度为T5 ℃时,该反应 耗时40 s达到平衡,则T5℃时,该反应的平衡常数数值为__0_.2__。 解析:T5 ℃时,c(CO2)=0.20 mol·L-1,K=c(CO2)=0.20。
(2)如果该反应的平衡常数K值变大,该反应__b_c_(选填字母)。 a.一定向逆反应方向移动 b.在平衡移动时正反应速率先增大后减小 c.一定向正反应方向移动 d.在平衡移动时逆反应速率先减小后增大
b
0
0
c转/mol·L-1 mx
nx
px qx
c平/mol·L-1 a-mx b-nx px
qx
K=a-mpxxpm··qbx-q nxn。
2.明确三个量的关系 (1)三个量:即起始量、变化量、平衡量。 (2)关系 ①对于同一反应物,起始量-变化量=平衡量。 ②对于同一生成物,起始量+变化量=平衡量。 ③各转化量之比等于各反应物的化学计量数之比。
化学平衡常数在高考试题中的考查视角及解题策略
水蒸气呢? 因 为 乙 烯 和 水 蒸 气 的 化 学 计 量 数 之 比 为
1∶4,两者物质 的 量 的 比 值 始 终 为1∶4,如 果 是 乙 烯 的
物质 的 量 分 数 为 0
39,则 水 蒸 气 的 物 质 的 量 分 数 为
所 以,该 条 件 下,水 蒸
0
39 的 4 倍,显 然 是 不 合 理 的 .
极其独特的 作 用 .
因 此,化 学 平 衡 常 数 作 为 考 查 学 生
知识和能力的载体,成为近几年高考试题中的新宠儿 .
1 2020 年高考化学平衡常数题统计
随着新课程改革的不断 推 进,全 国 高 考 呈 现 了 多
元化的命题方式,在 2020 年 全 国 高 考 中,化 学 学 科 共
有 10 套 试 卷,其 中 教 育 部 考 试 中 心 命 制 5 套,分 别
×
4 0
0393
该题把图象和 计 算 有 机 地 结 合 起 来,考 查 了
图1
根据图中点 A (
440K,
0
39),计算该温度时反应
学生从化学平衡移动的视角分析曲线变化
的平衡常数 Kp =
和利用“三段式”计 算 A 点 平 衡 时 各 反 应 物 和 生 成 物
方法 1 假设 n(
CO2 )和 n(H2 )的物质的 量
n(
N2O4),则2-
2
α=3
α,求出 NO2 转化率α=0
4,平衡时 n(
NO2 )=
93
方法与技巧
需 要 特 别 注 意 的 是,由
1
2 mo
l,n(
N2O4)=0
4 mo
l.
于 恒 温 恒 容 条 件,平 衡 时 的 压 强 发 生 了 变 化 不 再 是
微专题2 全面突破化学反应速率、化学平衡常数及转化率的判断与计算

v(N2O5)=2×10-3×30.0 kPa·min-1=6.0×10-2 kPa·min-1。
123456
解析 答案
③若提高反应温度至35 ℃,则N2O5(g)完全分解后体系压强p∞(35 ℃)_大__于__ 63.1 kPa(填“大小”“等于”或“小于”),原因是温__度__提__高__,__体__积__不__变__, _总__压__强__提__高__;__N_O_2_二__聚__为__放__热__反__应__,__温__度__提__高__,__平__衡__左__移__,__体__系__物__质__的__ _量__增__加_,__总__压__强__提__高___。
(3)依据化学方程式计算平衡常数 ①同一可逆反应中,K正·K逆=1。 ②同一方程式中的化学计量数等倍扩大或缩小 n 倍,则新平衡常数 K′与
原平衡常数 K 间的关系是 K′=Kn 或 K′=n K。 ③几个可逆反应方程式相加,得总方程式,则总反应的平衡常数等于各 分步反应平衡常数之积。
2.转化率、产率及分压的计算
微专题2 全面突破化学反应速率、化学平衡 常数及转化率的判断与计算
核心知识透析
1.化学平衡常数 (1)意义:化学平衡常数K表示反应进行的程度,K越大,反应进行的程 度越大。K>105时,可以认为该反应已经进行完全。K的大小只与温度 有关。 (2)化学平衡常数表达式:对于可逆化学反应 mA(g)+nB(g) pC(g)+ qD(g)在一定温度下达到化学平衡时,K=ccmpCA··ccqnDB。另可用压强平衡常 数表示: Kp=ppmpCA··ppqnDB[p(C)为平衡时气体 C 的分压]。
【化学专题复习】化学平衡常数的应用

化学平衡常数(K值)的应用一、化学平衡常数的定义化学平衡常数是在一定温度下,可逆反应无论从正反应开始,还是从逆反应开始,也无论反应物起始浓度是大还是小,最后都能达到平衡,这时各生成物浓度幂的乘积除以各反应物浓度幂的乘积所得的比值是个常数,用K表示。
例如:mA(g) + nB(g) pC(g) + qD(g),K =c p(C)·c q(D)c m(A)·c n(B)(式中个浓度均为平衡浓度)。
化学平衡常数是一个常数,只要温度不变,对于一个具体的可逆反应就对应一个具体的常数值。
二、应用平衡常数应注意的问题(1)化学平衡常数只与温度有关,与反应物或生成物的浓度无关。
(2)反应物或生成物中有固体和纯液体存在时,其浓度可看做“1”,因而不用代入公式(类似化学反应速率中固体和纯液体的处理)。
(3)化学平衡常数是指某一具体反应的平衡常数。
若反应方向改变,则平衡常数改变。
若化学方程式中各物质的化学计量系数等倍扩大或缩小,尽管是同一反应,化学平衡常数也会改变。
三、化学平衡常数的应用(有4条)(1)化学平衡常数值的大小是可逆反应进行程度的标志。
它能够表示出可逆反应进行的完全程度。
一个可逆反应的K值越大,说明平衡时生成物的浓度越大,反应物转化率也越大。
可以说,化学平衡常数是一定温度下一个可逆反应本身固有的内在性质的定量体现。
【例1】一元弱酸的电离方程式的通式:HA H+ + A—K= c(H+)c(A—)/c(HA) 此时的K值用Ka来表示,专指弱酸的电离常数。
Ka值越大,正向(电离)的程度就越大,该弱酸的酸性就越强。
反之,Kb代表弱碱的电离常数,Kb 值越大,该弱碱的碱性就越强。
如:CH3COOH 1.8×10—5 ;H2CO3 4.5×10—7(Ka1)说明CH3COOH的酸性比H2CO3强。
(2)可以利用平衡常数的值作标准,判断正在进行的可逆反应是否平衡及不平衡时向何方进行建立平衡。
化学平衡计算的专题试题 答案解析

化学平衡计算1.在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:已知容器甲乙丙反应物的投入量、的浓度反应的能量变化放出akJ 吸收bkJ 吸收ckJ体系的压强反应物的转化率下列说法正确的是A. B. C. D.【答案】B【解析】分析:甲容器内的平衡与乙容器内平衡是等效平衡, 所以平衡时NH3的浓度相等,即c1=c2,丙容器反应物投入量4molNH3,是乙的二倍,相当于增大压强,平衡正移,所以丙中氨气的浓度大于乙中氨气浓度的二倍,即c3>2c2,即c3>2c1,2P2>P3,,所以.详解:A.甲容器内的平衡与乙容器内平衡是等效平衡, 所以平衡时NH3的浓度相等,即c1=c2,丙容器反应物投入量4molNH3,是乙的二倍,相当于增大压强,平衡正移,所以丙中氨气的浓度大于乙中氨气浓度的二倍,即c3>2c2,即c3>2c1,A错误;B.乙中开始投入2molNH3,则甲与乙是等效的,甲与乙的反应的能量变化之和为92.4kJ,故a+b=92.4,B正确;C.丙容器反应物投入量4molNH3,是乙的二倍,反应起始时2P2=P3,由于合成氨的反应是气体体积减小的反应,故2P2>P3,C错误;D.丙容器反应物投入量4molNH3,是乙的二倍,相当于增大压强,平衡向右移动,所以丙中氨的转化率比乙小,因为,所以,D错误。
本题选B .2.一定温度下在甲、乙、丙三个体积相等且恒容的密闭容器中发生反应:NO 2(g)+SO2(g) SO3(g)+NO(g)。
投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列说法正确的是起始浓度甲乙丙c(NO2)/(mol·L-1) 0.10 0.20 0.20c(SO2)/(mol·L-1) 0.10 0.10 0.20A. 容器甲中的反应在前2min的平均速率v(NO)=0.05mol·L-1·min-1B. 容器乙中若起始时改充0.10mol·L-1NO2和0.20mol·L-1SO2,达到平时c(NO)与原平衡相同C. 达到平衡时,容器丙中SO3的体积分数是容器甲中SO3的体积分数的2倍D. 达到平衡时,容器乙中NO2的转化率和容器丙中NO2的转化率相同【答案】B【解析】分析:甲经2min达平衡时,NO2的转化率为50%,其平衡浓度为0.05mol/L,NO2(g)+SO2(g)⇌SO3(g)+NO(g)开始(mol/L):0.1 0.1 0 0转化(mol/L):0.05 0.05 0.05 0.05平衡(mol/L):0.05 0.05 0.05 0.05故该温度下平衡常数K=,各容器内温度相同,平衡常数均相同。
四大平衡常数

专题三十九四大平衡常数的专题K a/K b/K W、K h、k sp【2018年高考考纲解读】了解四大平衡常数【重点、难点剖析】一、四大平衡常数的比较对于一般的可逆反应:m A(g)+n B(g)p C(g)+q D(g),在一定温度下达到平衡时:K=c p(C)·c q(D)c m(A)·c n(B)以一元弱酸HA为例:HA H++A-,电离常数K a=c(H+)·c(A-)c(HA)二、高考题型示例【变式训练1】(2018全国III卷)用0.100 mol·L-1 AgNO3滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。
下列有关描述错误的是()A.根据曲线数据计算可知K sp(AgCl)的数量级为10-10B.曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=K sp(AgCl)C.相同实验条件下,若改为0.0400 mol·L-1 Cl-,反应终点c移到aD.相同实验条件下,若改为0.0500 mol·L-1 Br-,反应终点c向b方向移动【解析】A.选取横坐标为50mL的点,此时向50mL 0.05mol/L的Cl-溶液中,加入了50mL 0.1mol/L的AgNO3溶液,所以计算出此时溶液中过量的Ag+浓度为0.025mol/L(按照银离子和氯离子1:1沉淀,同时不要忘记溶液体积变为原来2倍),由图示得到此时Cl-约为1×10-8mol/L(实际稍小),所以K SP(AgCl)约为0.025×10-8=2.5×10-10,所以其数量级为10-10,选项A正确。
B.由于K SP(AgCl)极小,所以向溶液滴加硝酸银就会有沉淀析出,溶液一直是氯化银的饱和溶液,所以c(Ag+)·c(Cl-)=K SP(AgCl),选项B正确。
C.滴定的过程是用硝酸银滴定氯离子,所以滴定的终点应该由原溶液中氯离子的物质的量决定,将50mL 0.05mol/L的Cl-溶液改为50mL 0.04mol/L的Cl-溶液,此时溶液中的氯离子的物质的量是原来的0.8倍,所以滴定终点需要加入的硝酸银的量也是原来的0.8倍,因此应该由c点的25mL变为25×0.8=20mL,而a点对应的是15mL,选项C错误。
四大平衡常数的计算与应用--2024年高考化学考点微专题(解析版)

微专题四大平衡常数的计算与应用1(2023·辽宁·统考高考真题)某废水处理过程中始终保持H2S饱和,即c H2S=0.1mol⋅L-1,通过调节pH使Ni2+和Cd2+形成硫化物而分离,体系中pH与-lg c关系如下图所示,c为HS-、S2-、Ni2+和Cd2+的浓度,单位为mol⋅L-1。
已知K sp NiS>K sp(CdS),下列说法正确的是 A.K sp(CdS)=10-18.4B.③为pH与-lg c HS-的关系曲线C.K a1H2S=10-14.7=10-8.1 D.K a2H2S【答案】D【解析】已知H2S饱和溶液中随着pH的增大,H2S的浓度逐渐减小,HS-的浓度增大,S2-浓度逐渐增大,则有-lg c(HS-)和-lg(S2-)随着pH增大而减小,且相同pH相同时,HS-浓度大于S2-,即-lg c(HS-)小于-lg(S2-),则Ni2+和Cd2+浓度逐渐减小,且K sp NiS>K sp(CdS),即当c(S2-)相同时,c(Ni2+)>c(Cd2+ ),则-lg c(Ni2+)和-lg(Cd2+)随着pH增大而增大,且有-lg c(Ni2+)小于-lg(Cd2+),由此可知曲线①代表Cd2+、②代表Ni2+、③代表S2-,④代表HS-,据此分析结合图像各点数据进行解题。
A.由分析可知,曲线①代表Cd2+、③代表S2-,由图示曲线①③交点可知,此时c(Cd2+)=c(S2-)=10-13mol/L ,则有K sp CdS =c Cd 2+ ∙c S 2- =10-13mol/L ×10-13mol/L =10-26,A 错误; B .由分析可知,③为pH 与-lg c S 2- 的关系曲线,B 错误;C .由分析可知,曲线④代表HS -,由图示曲线④两点坐标可知,此时c (H +)=10-1.6mol/L 时,c (HS -)=10-6.5mol/L ,K a 1H 2S =c H + ∙c HS - c H 2S =10-1.6mol/L ×10-6.5mol/L 0.1mol/L =10-7.1或者当c (H +)=10-4.2mol/L 时,c (HS -)=10-3.9mol/L ,K a 1H 2S =c H + ∙c HS - c H 2S=10-4.2mol/L ×10-3.9mol/L 0.1mol/L =10-7.1,C 错误;D .已知Ka 1Ka 2=c (H +)c (HS -)c (H 2S )∙c (H +)c (S 2-)c (HS -)=c 2(H +)∙c (S 2-)c (H 2S ),由曲线③两点坐标可知,当c (H +)=10-4.9mol/L 时,c (S 2-)=10-13mol/L ,或者当c (H +)=10-6.8mol/L 时,c (S 2-)=10-9.2mol/L ,故有Ka 1Ka 2=c 2(H +)c (S 2-)c (H 2S )=(10-4.9mol/L )2×10-13mol/L 0.1mol/L =(10-6.8mol/L )2×10-9.2mol/L0.1mol/L =10-21.8,结合C 项分析可知Ka 1=10-7.1,故有K a 2H 2S =10-14.7,D 正确;故答案为D 。
2024-2025学年高二化学选择性必修1(配苏教版)教学课件专题2第2单元第3课时化学平衡常数

B.40%
C.50%
D.65%
D
)
解析 假设X和Y的物质的量均为1 mol,达到平衡时消耗X的物质的量为a
mol,则:
X + 2Y
2Z
起始量/mol
1
1
转化量/mol
a
2a
2a
平衡量/mol
1-a
1-2a
2a
1×2 mol
1
根据题意有:(1-a+1-2a)∶2a =3∶2,解得 a= ,Y 的转化率=3
10-2 mol·L-1。已知37 ℃时,平衡常数K=220,此时Hb·CO的浓度
大于
(填“大于”“等于”或“小于”)Hb·O2浓度的百分之二。
解析
(Hb·CO)
(2)
(Hb·O2 )
=
·(CO)
(O2 )
=
220×10-6 mol·L-1
10-2 mol·L-1
=2.2×10-2。
2.已知相同条件下:(1)2H2O(g)
D.K= (NH )·(Cl )
3
2
解析 根据反应 8NH3(g)+3Cl2(g)
数表达式为
(N2 )
K=8 (NH )·3 (Cl )。
3
2
6NH4Cl(s)+N2(g),该
6NH4Cl(s)+N2(g)可知,该反应的平衡常
视角2平衡常数的理解及计算
(A)·2()
4.一定温度下,某气体反应达到化学平衡,平衡常数 K= 2
(2)举例分析:
以反应mA(g)+nB(g)
pC(g)+qD(g)为例,若A、B起始物质的量浓度分别
为a mol·L-1、b mol·L-1,达到平衡后消耗A的物质的量浓度为mx mol·L-1。
高中化学第3讲 化学平衡常数

第3讲化学平衡常数课程标准知识建构1.能书写平衡常数表达式,能进行平衡常数、转化率的简单计算。
2.能利用平衡常数和浓度商的关系判断化学反应是否达到平衡及平衡移动的方向。
3.了解浓度商和化学平衡常数的相对大小与反应方向间的联系。
4.知道化学反应是有方向的,知道化学反应的方向与反应的焓变和熵变有关。
一、化学平衡常数1.概念在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常数,用符号K表示。
2.数学表达式(1)一般形式:对于反应m A(g)+n B(g)p C(g)+q D(g),K=c p(C)·c q(D)c m(A)·c n(B)(固体和纯液体的浓度视为常数,通常不计入平衡常数表达式中)。
(2)实例如:①C(s)+H2O(g)CO(g)+H2(g)的平衡常数表达式K=c(CO)·c(H2) c(H2O)。
②Fe3+(aq)+3H2O(l)Fe(OH)3(s)+3H+(aq)的平衡常数表达式K=c3(H+)c(Fe)。
(3)化学平衡常数与化学方程式的关系化学平衡常数是指某一具体反应的平衡常数。
若反应方向改变,则平衡常数改变。
若化学方程式中各物质的化学计量数等倍扩大或缩小,尽管是同一反应,平衡常数也会改变。
如:化学方程式 平衡常数 关系式N 2(g)+3H 2(g)2NH 3(g)K 1=c 2(NH 3)c (N 2)·c 3(H 2)K 2=K 1 (或K 121) K 3=1K 112N 2(g)+32H 2(g)NH 3(g) K 2=c (NH 3)c 12(N 2)·c 32(H 2)2NH 3(g)N 2(g)+3H 2(g) K 3=c (N 2)·c 3(H 2)c 2(NH 3)3.意义平衡常数表示可逆反应正向进行的程度,K 值越大,反应进行的程度越大。
4.影响因素K 只受温度影响,与反应物或生成物的浓度变化无关。
新教材高中化学二轮精品 专题六 题型专攻(八) 化学反应速率、化学平衡的综合计算

题型专攻(八) 化学反应速率、化学平衡的综合计算1.化学平衡常数(1)意义:化学平衡常数K 表示反应进行的程度,K 越大,反应进行的程度越大。
K >105时,可以认为该反应已经进行完全。
K 的大小只与温度有关。
(2)化学平衡常数表达式:对于可逆化学反应m A(g)+n B(g)p C(g)+q D(g)在一定温度下达到化学平衡时,K =c p (C )·c q (D )c m (A )·c n (B )。
另可用压强平衡常数表示:K p =p p (C )·p q (D )p m (A )·p n (B )[p (C)为平衡时气体C 的分压]。
(3)依据化学方程式计算平衡常数 ①同一可逆反应中,K 正·K 逆=1。
②同一方程式中的化学计量数等倍扩大或缩小n 倍,则新平衡常数K ′与原平衡常数K 间的关系是K ′=K n 或K ′=nK 。
③几个可逆反应方程式相加,得总方程式,则总反应的平衡常数等于各分步反应平衡常数之积。
2.转化率、产率及分压的计算 反应物转化率=反应物的变化量反应物的起始量×100%产物的产率=生成物的实际产量生成物的理论产量×100%分压=总压×物质的量分数 3.常用的气体定律同温同体积:p (前)∶p (后)=n (前)∶n (后) 同温同压强:ρ(前)ρ(后)=M (前)M (后)=V (后)V (前)=n (后)n (前)1.(2021·山东,20)2-甲氧基-2-甲基丁烷(TAME)常用作汽油原添加剂。
在催化剂作用下,可通过甲醇与烯烃的液相反应制得,体系中同时存在如图反应:反应Ⅰ:反应Ⅱ:反应Ⅲ:回答下列问题:(1)反应Ⅰ、Ⅱ、Ⅲ以物质的量分数表示的平衡常数K x与温度T变化关系如图所示。
据图判断,A和B中相对稳定的是_____________________________________(用系统命名法命名);ΔH1ΔH2的数值范围是________(填标号)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
平衡常数K专题解析平衡常数K 专题化学平衡常数统领化学平衡移动的结果分析,堪称化学平衡的精灵,是高考试题的宠儿。
纵观各地高考试题,放在一起,经过排序之后,发现很美妙的一件事情,平衡常数的不同层面像一首美妙的歌曲呈现在考试题中。
一、序曲----化学平衡常数的常规考查1、前奏---化学平衡常数的常规计算例1.(2014·重庆理综化学卷,T11节选)氢能是最重要的新能源。
储氢作为氢能利用的关键技术,是当前关注的热点之一。
储氢可借助有机物,如利用环已烷和苯之间的可逆反应来实现脱氢和加氢。
(g)+3H 2(g)在某温度下,向恒容容器中加入环己烷,其起始浓度为amol ·L -1,平衡时苯的浓度为bmol ·L -1,该反应的平衡常数K =解析:利用三段式解题(g)+3H 2(g)高温 FeSO 4/Al 2O 3高温 FeSO 4/Al 2O 3起始(mol/L) a 0 0转化(mol/L) b b 3b平衡(mol/L) a-b b 3b化学平衡常数K= =mol3/L3;2、小插曲---固体物质在平衡常数表达式中处理的技巧例2.(2014·福建理综化学卷,T24节选)铁及其化合物与生产、生活关系密切。
已知t℃时,反应FeO(s)+CO(g)Fe(s)(g)的平衡常数K=0.25。
+CO2①t℃时,反应达到平衡时n(CO):n(CO2)=。
②若在1 L密闭容器中加入0.02 molFeO(s),并通入xmolCO,t℃时反应达到平衡。
此时FeO(s)转化率为50%,则x=。
解析:根据反应FeO(s)+CO(g)Fe(s)+CO(g),平衡常数K为0.25,因为固体的浓度为2)/c(CO)=0.25,体积相同,所以反1,则k=c(CO2应达到平衡时n(CO):n(CO2)=4:1,若在1 L密闭容器中加入0.02 mol FeO(s),并通入xmolCO,t℃时反应达到平衡。
此时FeO(s)转化率为率为50%,FeO(s)+CO(g)Fe(s)+CO(g)2起始 0.02 x 0 0变化 0.01 0.01 0.01 0.01 平衡时 0.01 x-0.01 0.01 0.01 因为温度不变,所以平衡常数K=0.25得:0.0.1/(x-0.01)=0.25 解得x=0.05。
二、深入考查-----化学平衡常数与平衡移动因素的辩证思维1、平衡移动因素与化学平衡常数的辩证关系例3.(2014·上海单科化学卷,T14)只改变一个影响因素,平衡常数K与化学平衡移动的关系叙述错误的是A.K值不变,平衡可能移动B.K 值变化,平衡一定移动C.平衡移动,K值可能不变D.平衡移动,K值一定变化解析:A、K值代表化学平衡常数,平衡常数只与温度有关系,K值不变只能说明温度不改变,但是其他条件也可能发生改变,平衡也可能发生移动,A正确;B、K值变化,说明反应的温度一定发生了变化,因此平衡一定移动,B正确;C、平衡移动,温度可能不变,因此K值可能不变,C正确;D、平衡移动,温度可能不变,因此K值不一定变化,D错误。
所以,答案为D2、再强调----温度与化学平衡常数的关系例4.(2014·北京理综化学卷,T26节选)NH3经一系列反应可以得到HNO3,2NO(g)+O22NO2(g)。
在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如图)。
1、比较P1、P2的大小关系:________________。
2、随温度升高,该反应平衡常数变化的趋势是________________。
解析:1、控制单一变量,可以选取600℃,看纵坐标,P2对应的纵坐标大于P1对应的纵坐标,纵坐标为NO的平衡转化率,即P2时NO的平衡转化率大于P1时NO的平衡转化率。
分析反应的特点由2NO(g)+O2(g) 2NO2(g)可知该反应为气体体积减小的反应,温度相同,增大压强,平衡正向移动,NO的平衡转化率增大,所以,p1<p2。
2、再看同一压强线,温度升高,NO的平衡转化率降低,平衡向逆反应方向移动,则正反应为放热反应,温度升高,平衡常数减小。
3、当用平衡移动原理解释相互矛盾时,平衡常数的妙用例5(2014·海南单科化学卷,T12)将BaO 2放入密闭真空容器中,反应2BaO2(s)2BaO(s)+O2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是()A、平衡常数减小B、BaO量不变C、氧气压强不变D、BaO2量增加解析:A、化学平衡常数只与温度有关,温度不变,化学平衡常数不改变,A错误;B、由于该反应2BaO 2(s) 2BaO(s)+O2(g)的正反应是气体体积增大的反应,当温度保持不变时,缩小容器体积(相当于加压),平衡会向体积减小的方向即逆方向移动,所以BaO量减小,B错误;C、缩小容器的体积,氧气的压强增大,平衡逆向移动,氧气的压强减小,到底增大的多,还是减少得多?用平衡移动原理无法判断,可借助平衡常数。
温度不变,则化学平衡常数(k=()cO)2不变,所以()cO不变,所以氧气压强不变,C正2确;D、由于该反应2BaO 2(s) 2BaO(s)+O2(g)的正反应是体积增大的反应,当温度保持不变时,缩小容器体积(相当于加压),平衡会向体积减小的方向即逆方向移动,所以BaO2量增加,D正确。
【答案】CD三、平衡常数在盖斯定律运用中的华丽变形例6.(2014·山东理综化学卷,T29节选)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g) K1∆H < 0 ①2NO(g)+Cl2(g)2ClNO(g)K2∆H < 0 ②(1)4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示)。
解析:(1)①×2-②即可得到4NO2(g)+2NaCl(s)2NaNO 3(s)+2NO(g)+Cl2(g)。
此方程式的平衡常数表达式为k总=c(Cl)·c(NO)2/c(NO2)4请看平衡常数的变形过程:如果①×2,则方程式变为4NO2(g)+2NaCl(s)2NaNO3(s)+2ClNO(g),此时的平衡常数变为,方程式② 2NO(g)+Cl2(g)2ClNO(g)的K2=c(ClNO)2/c(NO)2。
C(Cl2),由K和K2相比,可得到K总,所以平衡常数K=212KK;四、高潮-----丰富多彩的化学平衡常数表达方式变形例7.(2014·全国理综I化学卷,T28节选)乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产。
回答下列问题:下图为气相直接水合法乙烯的平衡转化率与温度、压强的关系(其中224(H O)(C H):n n=1:1)①列式计算乙烯水合制乙醇反应(CH2=CH2+H2O催化剂 C2H5OH)在图中A点(对应的转化率为20%)的平衡常数Kp=_______(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
解析:A点乙烯的平衡转化率是20%。
根据反应:CH2=CH2+H2O催化剂 C2H5OH起始 1mol 1mol 0转化 0.2mol 0.2mol 0.2mol平衡 0.8mol 0.8mol 0.2mol则平衡时乙烯的分压:P(C2H4)=7.85Mpa×0.8mol/1.8mol=7.85Mpa×4/9水蒸气的分压:P(H2O)=7.85Mpa×0.8mol/1.8mol=7.85Mpa×4/9乙醇的分压:P(C2H5OH)=7.85Mpa×0.2mol/1.8mol=7.85Mpa×1/9则平衡常数例8.(2014·浙江理综化学卷,T27节选)煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。
采用一定的脱硫技术可以把硫元素以CaSO 4的形式固定,从而降低SO 2的排放。
但是煤炭燃烧过程中产生的CO 又会与CaSO 4发生化学反应,降低脱硫效率。
相关反应的热化学方程式如下: CaSO 4(s)+CO(g) CaO(s) + SO 2(g) + CO 2(g)ΔH 1=218.4kJ·mol -1(反应Ⅰ)CaSO 4(s)+4CO(g)CaS(s) + 4CO 2(g)ΔH 2= -175.6kJ·mol -1(反应Ⅱ)请回答下列问题:对于气体参与的反应,表示平衡常数K p 时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c (B),则反应Ⅱ的K p = (用表达式表示)。
解析:根据固体的浓度为常数,则反应的平衡常数为Kp=44p p 2CO CO ()();练习:1.(2014·广东理综化学卷,T31)(16分)用CaSO 4代替O 2与燃料CO 反应,既可提高燃烧效率,又能得到高纯CO 2,是一种高效、清洁、经济的新型燃烧技术,反应①为主反应,反应②和③为副反应。
①14CaSO4(s)+CO(g) 14CaS(s)+CO2(g)∆H1= —47.3kJ∙mol-1② CaSO4(s)+CO(g) CaO(s)+CO2(g) +SO2(g)∆H2= +210.5kJ∙mol-1③ CO(g) 12C(s)+ 12CO2(g)∆H3= —86.2kJ∙mol-1(1)反应2CaSO4(s)+7CO(g)CaS(s)+CaO(s)+6CO2(g)+ C(s)+SO2(g)的∆H=___________(用∆H1、∆H2和∆H3表示)(2)反应①-③的平衡常数的对数lgK随反应温度T的变化曲线见图18,结合各反应的∆H,归纳lgK-T曲线变化规律:a)_______________________________;b)____________________________。
【解析】(1)根据盖斯定律,①×4+②+③×2得:2CaSO 4(s)+7CO(g) CaS(s)+CaO(s)+6CO2(g)+ C(s) +SO2(g),所以∆H=4∆H1+∆H2+2∆H3;(2)结合图像及反应的∆H可知,反应①③为放热反应,温度升高K值减小,lgK也减小,反应②为吸热反应,温度升高K值增大,lgK 也增大。
(2)a)反应②为吸热反应,温度升高K 值增大,lgK也增大(2分)b)反应①③为放热反应,温度升高K值减小,lgK也减小(2分)2.(2014·全国理综II化学卷,T26节选)在容积为100L的容器中,通入一定量的N2O4,发生反应N2O4g) 2NO2(g),随温度升高,混合气体的颜色变深。
