a02.“吡啶-2,6-二甲酸二甲酯”的合成
重金属离子捕集剂水杨醛双Schiff碱的合成及应用

S hf 碱 配体 的合成 路线 见 图 1 ci f 。
多新 的方 法 , 如螯合 沉 淀 法 、 剂 萃取 法 、 溶 天然 沸 石 吸 附一 离 子交 换法 、 腐殖 酸 类 பைடு நூலகம் 附法 、 聚 糖类 吸 附 法 、 壳
微生 物 吸附法 及纳米 材料 催化 还原 法等 。 螯合 沉淀 法 , 因其能 克服传 统化学 沉 淀法 的不 足 , 操作 简单 , 已成 为重 金 属 废 水 处理 研 究 的热 点 。作 者 在此 以 2 6吡 啶二 甲酸 、 二胺 及 水 杨醛 等 为 原 料合 ,一 乙
C 什 等 ) 行 螯 合 反 应 , 成 了 稳 定 的 絮 状 沉 淀 , 而 r 进 生 从 可 以去 除废水 中的重金 属离 子 。
图 1 配 体 的 合 成 路 线
Fi .1 S nt e i o e o he l n g y h t c r ut f t i ga d
合反 应 。 结 果表 明 , 体 化 合 物 Ⅱ能 与 重 金 属 离子 生成 稳 定 性 较 高 且 不 溶 于 水 的 螯 合 物 , 以去 除 废 水 中 的 重 金 属 离 配 可
子。
关 键 词 : , 一 啶 二 甲酸 ; 杨 醛 ; c if ; 2 6吡 水 S hf 碱 重金 属 离 子 中 图分 类 号 : 2 . 2 O 6 6 3 文献标识码 : A 文 章 编 号 : 6 2 4 5 2 1 ) 5 0 7 — 0 1 7 —5 2 ( 0 1 0 — 0 4 3
测仪 。
1 2 方 法 .
仪 ; ruyVX 3 0型 核 磁 共 振 仪 ( 0 Hz , r Mec r 0 3 0M ) Vai -
目前 , 去除水 中重 金属 离子 的方法 很 多 , 统 的有 传
4-羟基吡啶-2,6-二甲酸二甲酯合成工艺研究

维普资讯
8 4
化 学 反 应 工 程 与工 艺
20 0 6年 2月
( D 1 溶 剂 ,TMS为 内标 ) E 2 0 C C。为 ;P 一4 0元 素 分 析 仪 ;B 10型 液 相 色 谱 仪 。 吡 啶一 , 一 甲 酸 T8 0 2 6二 ( P ,浙江 九州化 工厂 生产 。其 它试剂 均 为市售化 学纯 或分析纯 试剂 。 D A)
后合成 吡 啶一,一 甲酸 二 甲酯 ,然 后 在酸 性环 境 中质 子 化芳 香 杂环 ,增 强其 与 自由基反 应 的反应 活 2 6二 性 ,又 因烷 氧基 自由基 中 氧原子 的存 在增 强 了 自由基 的亲核性 和稳 定性[ ,最后 合成 得到 4羟 甲基吡 6 ] 一 啶一,一 甲酸 二 甲酯 ( ,其 合成 路线 如 图 l 2 6二 Ⅲ) 所示 。
CH H 0
一
c H
哪 。 c ∞ 。 。 一 H
图 1 - 甲基 吡 啶一 ,一 甲酸 二 甲酯 的 合 成 路 线 4羟 2 6二
F g 1 Th y t e i o t fo i t y 一 ( y r x meh 1 p iie2,- ia b x lt i. es n h ssr u eo fdmeh l 4 h d o y t y) r n - 6dc r o yae d
9 8g (4mmo)吡 啶一 ,- 甲酸二甲酯溶于 6 0 ( . 4 1 2 6二 0mL3 V)硫酸和 7 5mL甲醇混合溶液 中,同时等速
滴 加4 . ( 0 0 8mL 4 0mmo)3 过 氧 化 氢溶 液 和 含 1 . 10mmo) 硫 酸 亚 铁 的饱 和 溶 液 ,反 应 温 度 控 1 0 52g(0 1 制 在 3  ̄5 0 0℃ , 目标 产 物 产率 可 达6 . , 经 液相 色 谱 测 定 产 物 的纯 度 大 于 9 ,其 结 构 经 由核 磁 氢 谱 58 8 ( — H NMR) ,红 外 分 析 (R) 和 元 素 分析 得 以表 征 。 I
吡啶-2,6-二甲酸衍生物及其Tb(Ⅲ)配合物的合成与荧光性能研究的开题报告

吡啶-2,6-二甲酸衍生物及其Tb(Ⅲ)配合物的合成与荧
光性能研究的开题报告
一、研究背景与意义
吡啶是一种重要的有机化合物,在药物、农药、杀虫剂、染料、聚合物等领域都有广
泛的应用。
同时,吡啶也是一种重要的配体,可以与金属离子形成稳定的配合物,具
有广泛的应用前景。
其中,吡啶-2,6-二甲酸二甲酯是一种重要的吡啶衍生物,具有
较好的溶解性和稳定性,可用于生物荧光探针、LED器件和药物配合物等领域。
而Tb (Ⅲ)是一种稀土元素,具有独特的发光性质,可作为生物标记物、发光材料等重要
应用。
因此,本研究旨在合成吡啶-2,6-二甲酸二甲酯及其与Tb(Ⅲ)配位生成的配合物,
并探究其荧光性能,为开发新型荧光材料提供参考。
二、研究内容和方法
1.合成吡啶-2,6-二甲酸二甲酯
将吡啶和甲酸乙酯在碱性条件下反应,得到吡啶-2,6-二甲酸二甲酯。
2.合成Tb(Ⅲ)配合物
将合成的吡啶-2,6-二甲酸二甲酯与Tb(Ⅲ)离子在适当的反应条件下反应,得到Tb (Ⅲ)配合物。
3.荧光性能研究
采用荧光光谱仪测试吡啶-2,6-二甲酸二甲酯及其Tb(Ⅲ)配合物的荧光光谱、荧光
强度、荧光寿命等性能。
三、预期结果
合成吡啶-2,6-二甲酸二甲酯及其Tb(Ⅲ)配合物,并探究其荧光性能。
预期结果为:合成成功的吡啶-2,6-二甲酸二甲酯和Tb(Ⅲ)配合物具有良好的荧光性能,可作为
生物荧光探针、LED器件和药物配合物等重要应用。
同时,本研究对于深入了解吡啶
衍生物的化学性质、荧光性质及其与稀土金属配合物的性质有一定的参考价值。
5-甲基吡啶-2,3-二羧酸二甲酯合成工艺

5-甲基吡啶-2,3-二羧酸二甲酯(简称为“5-MeO-DCM”)是一种重要的有机合成中间体化合物,广泛应用于医药、农药、染料和涂料等领域。
其生产合成工艺对于高效、环保和经济可行非常关键。
本文将深入探讨5-MeO-DCM的合成工艺,并共享个人观点和理解。
1. 介绍5-MeO-DCM是一种含氮的芳香族化合物,其合成工艺的研发和优化对于相关产业的发展至关重要。
我们先来了解一下5-MeO-DCM的结构和性质。
5-MeO-DCM是一种白色固体,可溶于有机溶剂,具有良好的稳定性和反应活性,是一种重要的化学合成中间体。
2. 传统合成工艺分析在过去的研究中,人们通过一系列反应途径来合成5-MeO-DCM,比如甲基吡啶的芳香硝化、重氮化反应和甲醛缩合等。
这些传统的合成方法虽然能够获得5-MeO-DCM,但是存在着反应条件苛刻、产物纯度低、废弃物排放难以处理等问题,导致生产成本高、环境污染严重等不利因素。
3. 现代合成工艺改进基于上述传统合成方法的不足,近年来,许多科研人员致力于改进5-MeO-DCM的合成工艺。
通过催化剂的设计和选择,可以实现反应条件的温和化和产物纯度的提高;采用新型溶剂和循环利用废弃物可以有效减少环境污染。
这些改进使得5-MeO-DCM的合成工艺更加高效、环保和经济可行。
4. 个人观点和理解在我看来,5-MeO-DCM的合成工艺改进是一个充满挑战和机遇的领域。
在实际工作中,我们需要不断学习和探索最新的合成工艺,灵活应用各种新技术和手段,以提高产物质量、减少生产成本,推动产业的发展和创新。
我们也要高度重视环保理念,努力寻求绿色合成工艺,为可持续发展贡献自己的力量。
5. 总结通过对5-MeO-DCM的合成工艺进行全面评估和探讨,我对这一领域的理解更加深入。
经过对传统合成方法和现代工艺改进的对比分析,我认识到合成工艺的优化对于产业发展的重要性。
我坚信,未来定会有更多关于5-MeO-DCM合成工艺的重要突破和创新,为相关领域的发展带来新的活力和机遇。
2_6_二甲基苯甲酸的合成工艺研究

第13卷第16期2013年6月1671—1815(2013)16-4724-03科学技术与工程Science Technology and EngineeringVol.13No.16Jun.2013 2013Sci.Tech.Engrg.化工技术2,6-二甲基苯甲酸的合成工艺研究赵迎春张学楷黄龙江滕大为*(青岛科技大学化工学院,青岛266042)摘要以2,6-二甲基溴苯为原料,经氰基化,两步水解等反应合成了2,6-二甲基苯甲酸,并对氰基水解反应的工艺条件进行了优化。
先将氰基在碱性条件下水解成酰胺,收率:100%;再在酸性条件下水解酰胺,得到最优的酰胺水解条件是:酰胺与65%硫酸的配比为1gʒ10mL ,水解温度110ħ,水解时间12h ,收率达到:85%。
关键词2,6-二甲基苯甲酸合成酰胺水解中图法分类号TQ245.12;文献标志码B2013年2月22日收到,2013年3月18日修改教育部归国留学人员科研基金项目(201000265)资助第一作者简介:赵迎春(1988—),女,硕士研究生。
研究方向:精细化工。
*通信作者简介:滕大为。
E-mail :dtengw@ 。
2,6-二甲基苯甲酸是重要的化工和医药中间体苯甲酸类的一种。
由于苯环上羧基相邻的位置具有两个甲基,其所具有的位阻效应导致该羧基碳原子所形成的酯或酰胺等键在空间上和苯环不再共平面,所形成的产物具有特殊的空间构型而在医药研发中具有某些独特的功用[1,2],有关2,6-二甲基苯甲酸的合成报道很多[2—6],归纳起来可以分成以下三类:(1)以2,6二甲基溴苯经格式试剂反应后与干燥的二氧化碳反应制备[3,4],收率约50%,反应需要-78ħ低温和无水等苛刻的条件,不易用于大量制备;(2)以1,2,3-三甲苯为原料经高锰酸钾氧化制备[5],该制备方法反应收率较低,因为反应中会产生大量的2,3-二甲基苯甲酸,无论是从产率和产物的分离角度,该路线都不适合大量制备;(3)以邻甲基苯甲酸的钾盐或钠盐为原料[6],在Pd 催化下羧基的邻位芳香氢甲基化制备,反应收率50%,反应过程中用到贵金属Pd ,环境不友好;(4)以间二甲苯和干燥的二氧化碳为原料的羰基化反应制备[2],该反应产物收率较低,究其原因是由于两个甲基的位阻效应导致反应选择性在5位发生,从而得到主要产物3,5-二甲基苯甲酸;(5)以2,6-二甲基苯腈为原料水解制备,文献[2]报道收率为50%,另外产生了大量的副产物间二甲苯和未反应完全的原料以及部分水解的中间体2,6-二甲基苯甲酰胺。
2,6-二(对甲氧基苯甲酰乙酰基)吡啶的合成工艺

第2 5卷 第 4期
20 0 8年 4月
应 用 化 学
C N EJ HI ES OURN P I D CHE S RY AL OF AP L E MI T
Vo . 5 1 2 No. 4 Ap . 00 r2 8
2 6 二 ( 甲 氧 基 苯 甲 酰 乙 酰 基 ) 啶 的 合 成 工 艺 ,. 对 吡
相 应 的强酸 酯 , 乙醇 钠或 氢化 钠等 强碱 催化 下 , Casn酯缩 合 反 应 合 成 , 由酮 与酰 氯 反应 , 二 在 经 li e 或 用
异 丙胺基 溴化 镁 做碱性 缩 合剂合 成 (]或 由强 酸 酯 和 酮 , 甲醇 钠 催 化 剂 缩 合 制 备 l 这 些 方 法 多半 1, 2 经 】 , 存 在产 率低 、 副反 应 多 、 应时 间长 及 后 处 理 复 杂 等 缺 点 。Saf n 反 alak等 ¨ r 曾 报道 了一 系 列 含 吡 啶 环 的
2 6吡 啶 二 甲 酸 二 甲 酯 、 甲氧 基 苯 乙 酮 和 金 属 钠 的 摩 尔 比为 12 42 4的 条 件 下 , 对 甲氧 基 苯 乙酮 的 甲苯 ,. 对 :. :. 将
溶液滴加到 2 6吡啶二 甲酸二 甲酯 的甲苯溶 液 ( 有小钠 珠 ) , ,- 含 中 控制前 期反应 温度 10—10℃ , 0 1 后期恒 温
行 了优 化 , 到 了简化 后处 理步 骤 、 达 缩短 反应 时 间 、 高产 率 的效果 。其合 成路 线 如下 : 提
O CH OH CH COC l
。—
3 一
H O
Na o u n /T l e e
H OOC
COO H ∞
Hj COOC
吡啶-2,6-二羧酸的工业用途

吡啶-2,6-二羧酸是一种重要的有机化合物,在工业上有着广泛的用途。
它是一种中间体化合物,可以参与到多种合成反应中,从而产生各种有机化合物,具有很高的应用价值。
下面将对吡啶-2,6-二羧酸的工业用途进行详细介绍。
一、吡啶-2,6-二羧酸在医药领域的应用1. 吡啶-2,6-二羧酸可以作为制药中间体,参与到多种药物的合成中。
它可以被用于合成抗生素、抗肿瘤药物等重要药物,对于医药工业有着重要意义。
二、吡啶-2,6-二羧酸在染料领域的应用2. 吡啶-2,6-二羧酸可以用于染料的合成,产生出各种颜色的有机染料。
这些染料在纺织、皮革等行业都有着广泛的应用,为这些行业提供了丰富的颜色选择。
三、吡啶-2,6-二羧酸在化工领域的应用3. 吡啶-2,6-二羧酸可以被用于吡啶树脂的合成,这种树脂具有优良的化学性能和物理性能,可用于制备各种防腐涂料、油墨、粘合剂等,广泛应用于化工领域。
四、吡啶-2,6-二羧酸在农业领域的应用4. 吡啶-2,6-二羧酸可以用于农药的合成,有些农药的合成过程中需要使用吡啶-2,6-二羧酸作为原料,从而控制病虫害,提高农作物的产量和质量。
五、吡啶-2,6-二羧酸在其他领域的应用5. 吡啶-2,6-二羧酸还可以用于生态环境领域,例如可用于制备螯合剂,用于废水处理,固体废物处理等,能够对环境进行良好的保护和改善。
吡啶-2,6-二羧酸作为一种重要的有机化合物,在工业上有着广泛的用途,不仅在医药领域有着重要的应用,而且在染料、化工、农业、生态环境等领域也发挥着重要作用。
它的应用范围非常广泛,对于各行各业都有着重要的意义。
可以预见,随着科技的不断进步和发展,吡啶-2,6-二羧酸在工业上的应用将会更加广泛。
吡啶-2,6-二羧酸作为一种重要的有机化合物,在工业上有着广泛的用途。
它的多种应用使得吡啶-2,6-二羧酸成为化工行业的重要原料之一。
下面将结合吡啶-2,6-二羧酸的特性和化学性质,继续深入探讨它在工业上的应用。
含吡啶环的双醛腙类试剂的合成及其光谱研究

当紫色褪去时 , 再加入另外 的 5. 3 5gKMn 4 2 0mL水 , O 和 0 由于高锰 酸钾过量 , 溶液略显紫色 ,稍冷后 , 入 1 加 0g亚硫 酸氢钠还原过量 高锰酸银 , 冷却 ,过滤 出二氧化 锰 ,将滤 出
光 波 长 发生 红 移 。
关键词
吡啶 ; 双醛腙 ; 合成 ; 红外光谱 ; 荧光光谱
文献 标 识 码 :A 文 章 编 号 :10 —5 3 20 )711 —4 0 00 9 (0 8 0 —540
中 图分 类 号 :T 7 QO 5
引 言
腙类试剂是一类理想 的荧光分 析试 剂,用其 测定 Al , Z2 n 和 C 2 已显示 出灵 敏度高 、选择 性好 的优点[ ] u 等 1 ,腙
收 稿 日期 :2 0 —10 ,修 订 日期 : 0 70 —0 0 70—8 2 0 —32
基金项 目: 国家 自然科学基金 项 目(970 3和教育部归国留学科研启 动金项 目(06 3 ) 294 1) 20— 1资助 3
作者简介 : 子恺,18 年生 ,长春工业大学生物工程学院硕士研究生 鲁 91 emal uia o u cm - i zki h .o :l @s
板显示技术领域研究 的热点之一 。开发性能优 良的 电子传输材料是提 高有机及 聚合 物 L D 性能 的关键 。双 E 席夫碱类金属配合物同时满足 了电荷平衡和配位 数饱 和两个条 件 ,可 以得 到非 常纯 的荧 光 ,能够成 为 良好 的电致 发光材 料。文章设计并合成 了四种新 的含 吡啶环 的双醛腙类化合物 ,通过红外光谱 、 素分 析、荧光 元
一种2,6-奈二甲酸二甲酯(2,6-NDC)的制备方法

一种 2, 6-奈二甲酸二甲酯( 2, 6-NDC)的制备方法摘要:介绍一种2,6-奈二甲酸二甲酯(2,6-NDC)的制备方法,采取的技术原理,工艺路线。
关键词:2,6-奈二甲酸二甲酯、2,6-NDC、PEN1、概述聚2,6-奈二甲酸乙二醇酯(PEN)由2,6-奈二甲酸二甲酯(2,6-NDC)与乙二醇(EG)缩聚而得,是目前我国尚未广泛应用的高性能聚酯材料。
PEN的热性能、力学性能、化学性能、机械性能、对气体的阻隔性、绝缘性能、以及其他综合性能都比聚对苯二甲酸乙二醇酯(PET)优越,从20世纪90年代以来,全球各大塑料生产和应用公司纷纷投入巨资和大量人力进行PEN的合成和应用研究,先后开发了瓶级、薄膜级、纤维级等系列产品,开拓了PEN的应用领域。
在国内,合成PEN的重要单体2,6-NDC的工业化一直制约着PEN的生产。
2、拟采取的2,6-NDC的制备方法2.1采用技术原理酰化反应:本项目工艺流程分为酰基化和氧化两大部分,酰化反应机理为Friedel-Crafts(傅里德-克拉夫茨反应,简称傅-克反应)亲电取代反应,即在催化剂作用下,酰化剂对萘环进行亲电取代反应。
酰基化反应与烷基化反应不同,酰化基团对萘环具有钝化作用,使得酰化反应不能生成多元取代产物,而且酰化反应不可逆。
酰化剂和催化剂形成的亲电质点具有较大的空间位阻,有利于高选择性的得到2,6-位置产物。
氧化反应:空气液相氧化常用的催化剂都是过渡金属,其中钴和锰是最有效的,加入溴化物可以提高催化能力。
催化剂的作用是促进烷基自由基的生成和烷基过氧化氢的分解。
烃类氧化属于自由基氧化,一般认为反应包括三个阶段,如下所示:(1)链的引发指被氧化物在能量(热能、光辐射等)、可变价金属或游离基的作用下,发生键的均裂而生成游离基的过程。
(2)链的传递指游离基与空气中的氧相作用生成有机过氧化氢物的过程。
在这个阶段烷烃解离形成自由基,进一步转变成为过氧化氢物,过氧化氢物再解离得烷氧基自由基,进一步转化为醇和酮,醇酮被氧化生成酸及其衍生物。
吡啶二甲酸的合成及其应用

硫酸铜为催化剂 , 用浓硝酸在高温氧化异喹啉得到 3, 4 吡啶二甲酸 , 产率为 71 4% , 并讨论了 影响合成的因素。在 钼酸铵存在下 , 采用固相烘焙法 , 2, 3 吡啶二甲酸和 3 , 4 吡啶 二甲酸分别 与尿素和 氯化亚 铜作用得 到了氮 杂铜酞 菁。实验发现 , 以 3 , 4 吡啶二甲酸合成的氮杂铜 酞菁在吡啶中具有较大的溶解度 , 最大吸收波长为 673nm。 关键词 : 喹啉 ; 异喹啉 ; 2 , 3 吡啶二甲酸 ; 3, 4 吡啶二甲酸 ; 氮杂铜酞菁
表 2 硫酸与喹啉物质的量比及硫酸浓 度 对 2 , 3 吡啶二甲酸产率的影响
n ( 硫酸 ) &n ( 喹啉 ) 0 6 1 0 1 5 2 0 2 5 3 0 4 0 6 0 硫酸用量 /m ol 0 12 0 2 0 3 0 4 0 5 0 6 0 7 0 8 硫酸的浓度 / ( m ol /L) 0 55 0 93 1 39 1 85 2 3 2 78 3 24 3 7 产率 /% 44 4 54 1 56 2 55 54 3 52 9 51 6 46 8
由表 3 可见, 滴加硝酸的时间应该 超过 3h ,否 则反应不充分, 影响产率。如反应时间 少于 3h ,不 仅后处理麻烦 , 而且获得的 3 , 4 吡啶二甲酸收率不 高, 且纯度也不高。
*
收稿日期 : 2006 09 11 作者简介 : 陆青青 ( 1981 ), 女 , 在读硕士研究生 , 研究方向为有机色素。
2006 年 12 月 6 日
陆青青 , 等 : 吡啶二甲酸的合成及其应用
# 17#
中的溶解度 , 并测试了其吸收光谱。
220∃ , 在 4h 内滴 加 49 8g ( 0 55m ol) 70 % 硝酸 , 滴 加过程 中温度控 制在 220 ∃ , 加 毕, 把 混合物 倒入 冰 /水中, 用氨水调 p H= 2 , 冷却到 10∃ , 过滤得到 黄色的 3 , 4 吡啶二甲酸粗品。再用 30% 氢氧化钠 将其溶解 , 加入活性炭后加热回流 2h , 过滤除去活 性炭 , 滤液用硝酸调 p H= 1 7 , 析出白色沉淀 , 过滤, 干燥 , 得到白色 的 11 2g ( 0 067m o l) 3 , 4 吡啶 二甲 酸, 产率为 71 4 % 。T m = 259~ 262∃ 。M ass( z/m ): 166( M + , 100 % ) , 167( M + 1 , 10 % )。 2 . 3 氮杂铜酞菁的合成 用研钵把 2 , 3 吡啶 二甲 酸 ( 或 3, 4 吡啶二 甲 酸 )、 尿素、 氯化亚铜 ( 具体的投料量见结果与讨论 ) 充 分 研 细 混 合, 移 至 烧 杯 中 , 加 热。当 加 热 到 110∃ , 烧杯内的固体开始熔化 , 用玻璃棒搅拌使物 料充分混合; 当温度 升至 140∃ 时, 固体全 部熔化, 且开始有氨气放出 , 再在 15m in 内升温到 170∃ ; 加 入钼 酸铵, 搅拌 , 使物 料完 全混合 均匀, 再升 温到 200∃ , 在此过程中放出大量的氨气, 5m in 后反应物 料固化, 保温 5h 以上。加入反应物 10 倍质量的浓 硫酸溶解 , 温度控制在 35∃ 以下 , 倒入 1000mL 水 中, 静置 , 分层 , 分出上层清液 , 再加入清水 , 如此重 复, 直到物 料呈中 性, 过 滤, 滤饼 在 70∃ 干燥。 IR ( KBr , c m
2-氯吡啶和2,6-二氯吡啶合成与应用

22氯吡啶和2,62二氯吡啶合成与应用①韩志伟1,张红波2(11中石化南京化工厂,江苏南京,210038;21焦作鑫达化工有限公司,河南焦作,454001)摘 要:介绍了22氯吡啶和2,62氯吡啶的合成技术,应用,市场与发展。
关键词:22氯吡啶;2,62二氯吡啶;合成;应用;发展中图分类号:TQ25411 文献标识码:A 文章编号:1009-9212(2002)05-0008-02 22氯吡啶和2,62二氯吡啶是一种重要的精细化工中间体,广泛应用于农药、医药和日用化工领域,随着应用研究不断深入,近年来需求快速增加,国外多家公司来中国寻求22氯吡啶和2,62二氯吡啶产品,成为倍受关注的热点产品。
1 合成技术22氯吡啶和2,62二氯吡啶文献报道合成路线较多,其中22氯吡啶国外主要的工业化合成技术按原料路线分有三种,即吡啶N2氧化物法、22羟基吡啶法和吡啶直接氯化法。
2,62二氯吡啶主要是22氯吡啶直接氯化法。
111 吡啶N2氧化法一般是将吡啶与过氧化氢反应,生成吡啶N2氧化物之后,再与氯气反应生成22氯代吡啶N2氧化物,还原后得到22氯吡啶。
该法是传统的合成方法,技术成熟简单,但是路线冗长,有一定三废污染,收率较低。
反应式如下:N H2O2NOCl2NOCl还原N Cl112 22羟基吡啶法22羟基吡啶用氯化亚砜、五氯化磷等氯化剂氯化,羟基与氯原子发生置换反应,得到22氯吡啶,该法工艺简单,但是原料22羟基吡啶来源受到一定限制,国外一般不采用该路线。
反应方程式如下:N OH 氯化剂PCl3或SOCl2溶剂N Cl113 吡啶直接氯化法吡啶与氯气进行光氯化,控制氯化深度,可以得到22氯吡啶和2,62二氯吡啶,而且两种产品可以自由调节比例,产品经分离后分别得到22氯吡啶和2, 62二氯吡啶,反应中氯自由基可以由紫外线引发,也可由加热引发,如22氯吡啶主要生产厂家住友精化就采用该技术,以紫外线为引发剂。
该技术是国外最普遍采用的合成路线,原料易得,工艺过程简单,但是工艺控制比较困难。
新型席夫碱的合成及其抑菌活性

新型席夫碱的合成及其抑菌活性朱万仁;李家贵;陈渊;陈光全;朱宇林;黄肇宇;彭昌顺;林广芝;吴德娟【摘要】The key intermediate, 2,6-pyridinebiformyl hydrazine(3 ), was synthesized from 2,6-dimethyl pyridine. Six novel Schiff bases(la ~ 1f) in yields of 50%~ 97% were prepared by the reaction of 3 with aldehydes or ketones, respectively. The structures were characterized by UV, NMR, IR and MS. The preliminary antibacterial tests showed that 1 exhibited antibacterial activity to staphylococcus aureus, proteus, colibacillus and bacillus, 1d was the best of all.%以2,6-二甲基吡啶为原料合成了关键中间体2,6-吡啶二甲酰肼(3);3分别与醛或酮反应制得了一系列新型席夫碱(la~lf),产率50%~97qo,其结构经UV,NMR,IR和MS表征.初步生物活性测试结果表明,1对金黄色葡萄球菌、变形杆菌,大肠杆菌和芽孢杆菌均具有一定的抑菌活性,其中1d的抑菌活性最高.【期刊名称】《合成化学》【年(卷),期】2011(019)003【总页数】4页(P341-344)【关键词】2,6-吡啶二甲酰胼;席夫碱;合成;抑菌活性【作者】朱万仁;李家贵;陈渊;陈光全;朱宇林;黄肇宇;彭昌顺;林广芝;吴德娟【作者单位】玉林师范学院化学与生物系,广西,玉林,537000;玉林师范学院化学与生物系,广西,玉林,537000;玉林师范学院化学与生物系,广西,玉林,537000;玉林师范学院化学与生物系,广西,玉林,537000;玉林师范学院化学与生物系,广西,玉林,537000;玉林师范学院化学与生物系,广西,玉林,537000;玉林师范学院化学与生物系,广西,玉林,537000;玉林师范学院化学与生物系,广西,玉林,537000;玉林师范学院化学与生物系,广西,玉林,537000【正文语种】中文【中图分类】O625.63Schiff碱及其金属配合物广泛应用于催化、医药、分析、光致变色、腐蚀、农业、海洋、材料等诸多领域[1~6]。
a01.“吡啶-2,6-二甲酸”的合成
5分钟
(2)110℃沸腾回流反应4小时。
产生黑色沉淀,静置后溶液澄清。
紫色褪去
5小时
(3)冷却过滤,减压浓缩至原体积的五分之一,趁热加入10mL 70%硫酸。
搅拌时,溶液有气泡产生ห้องสมุดไป่ตู้大量放热)。
30分钟
(4)自然冷却,过滤,得到粗产品。
溶液呈浅绿色,析出大量的白色晶体。
15分钟
(5)用水重结晶两次,得到白色针状固体。
产量:7.3g;产率:98.6%。
2小时
(6)测熔点。
实测熔点:
七、实验结果
参考文献
[1]谭黎峰、蒋毅民、韦凤仙吡啶—2,6二甲酸合成工艺的研究广西化工第27卷1998年第4期
浓硫酸(18.4mol/L)
98.08
吡啶-2,6-二甲酸
167.12
46
7.69
70%硫酸密度1.6g/cm3
五、仪器装置
六、实验步骤及现象
实验步骤
实验现象
操作目的
操作细节
操作时间
准备:配制70%的硫酸200mL:V98%硫酸=125.30mL;V水=101.14mL
30分钟
(1)将41.0g(261mmol)高锰酸钾一次性加入到盛有388mL水的圆底烧瓶中,再加入5.0g(46mmol)2,6-二甲基吡啶。PS:滴加5滴浓硫酸,加入18-冠醚-6。
270℃分解
溶
浓硫酸
无色液体
溶
溶
吡啶-2,6-二甲酸
白色晶体
228~230℃
248~250℃
5g/L
(20℃)
溶
四、实验试剂
物质名称
式量
物质的量(mmol)
吡啶-2

( 东 省化 学储 能 与新 型 电池 技 术 重 点 实 验 室 ,聊 城 大 学化 学化 工学 院 , 城 2 2 5 ) 山 聊 50 9
摘要
合成 了吡啶一 ,- 甲酸氢钾 ( HD C .利用 x射线单晶衍射仪确定了化合物的晶体结构 .用精密 自 26二 K P)
解 一 应热量 计 ( 反中国科学 院大 连化学 物理研 究所 生产 ) .
1 2 KHD C样 品的合 成 . P
按照 12 : 的摩尔 比取一 定量 的 H:P D C和 K H分 别溶 于蒸馏 水 中 , 电磁搅 拌下将 K H溶液 慢慢 O 在 O 加 入 H D C的溶液 中 , P 加热 回流 约 8h后得 到无色 透 明溶液 , 室温 下静 置 ,得到无 色针 状 晶体 , 滤 , 过 将 产物用 蒸馏 水洗 涤 3次后 真空 干燥 6h 然后 于干 净称量 瓶 中放置备 用 . ,
动绝 热热量计测量 了其在 7 30K温度 区间的低温热容.利用最, - 8— 6 ' -乘法 对配合 物的实验热容 进行拟合 , b-
得到热容 随温度变化 的多项式方程.利用此方 程计算 出温度 区间内的舒平热容 值及相对 于 2 8 1 9 .5K时的热 力学函数值.利用 Hes s 定律设计 合理的热化学循 环 , 在等温环境下利用溶 解一 反应热量计 分别测 定所设 计热 化学反应的反应物和产物在所选溶剂中的溶解焓并计 算 出反应 的反应 焓.最 后 , 计算 出该 化合物 的标准摩
区间 的热容 , 过最 小二 乘法 拟 合 得 到热 容 对 折 合 温 度 的 多项 式 方 程 ,并 利 用 此 方程 计 算 得 到 每 隔 通 5K的舒平 热 容和热 力学 函数 .通 过设 计 合理 的热 化学 循 环 , 择合 适 的量 热溶 剂 , 等 温 环 境下 利 选 在 用溶解 一 应热 量计 得到 了产物 的标 准摩 尔生成 焓 . 反
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(7)常温冷却后,反应瓶置于冰浴中。
得到大量白色固体。
30分钟
(8)过滤,得粗品。
肉色固体;产量:31.0g;产率:83.6%
15分钟
(9)用冷无水乙醇洗涤数次。
(10)测熔点。
实测熔点:
七、实验结果
参考文献
无色液体
–97℃
64.7℃
剧毒
溶
溶
无水乙醇
无色液体
−117.3℃
78.3℃
无毒
溶
溶
吡啶-2,6-二甲酸二甲酯
淡黄色晶体
121~125℃
溶
四、实验试剂物质名称式量物质的量(mmol)
质量(g)
密度(g/ml)
体积(ml)
浓度(mol/l)
吡啶-2,6-二甲酸
162.12
190
31.0g
氯化亚砜
118.97
1656
196.8g
1.630-1.650
120mL
无水甲醇
32.04
4944
158.4g
0.791-0.792
200mL
无水乙醇
46.07
吡啶-2,6-二甲酸二甲酯
195.17
190
37.1g
五、仪器装置
六、实验步骤及现象
实验步骤
实验现象
操作目的
操作细节
操作时间
(1)在500mL圆底烧瓶中加入31.0g(190mmol)吡啶-2,6-二甲酸,在球形冷凝管下端接口处涂上真空硅胶酯,插上球形冷凝管,并从管口倒入120mL(1656mmol)氯化亚砜,插上带无水氯化钙的干燥管。
白色固体微溶于淡黄色液体。
5分钟
(2)加热回流10小时。
溶液从淡黄色变成深红色。
14小时
(3)常压蒸出剩余的氯化亚砜。
红色泥状液体。
1小时
(4)完全冷却后,从球形冷凝管口向残余物中缓慢加入200mL(4944mmmol)无水甲醇。
大量蒸汽向上逸出。
30分钟
(5)加热回流2小时。
淡棕黄色溶液。
4小时
(6)常压蒸出剩余的约120mL甲醇。
“吡啶-2,6-二甲酸二甲酯”的合成
一、实验目的
1.合成“吡啶-2,6-二甲酸二甲酯”
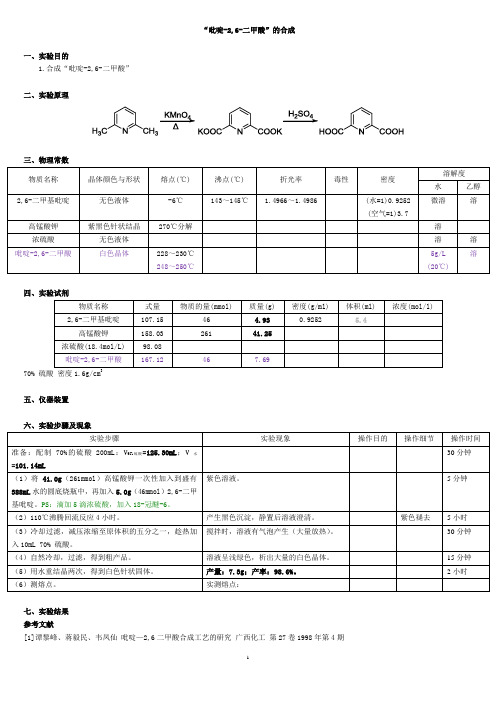
二、实验原理
三、物理常数
物质名称
晶体颜色与形状
熔点(℃)
沸点(℃)
折光率
毒性
密度
溶解度
水
乙醇
吡啶-2,6-二甲酸
针状结晶
228~230℃
难溶
氯化亚砜
淡黄色至红色发烟液体
有强烈刺激气味
-105℃
78.8℃
溶
溶
无水甲醇
