晶型转变及其控制ppt课件
固体药物晶型转化现象以及工艺控制方法PPT文档45页

药物制备过程中引起晶型转变的 因素
• ①温度 药品经干燥或加热灭菌等工艺条 件处理时,当达到某一特定的转变温度, 可能发生晶型转变。
• ②溶剂 多晶型药物的不同晶体可通过不 同的溶剂、不同的结晶条件重结晶获得。 除重结晶时溶剂对晶型的影响外 ,在溶剂存 在的制剂工艺过程 ,如湿法制粒等 ,也可产 生多晶药物的晶形转变。
• 但直接压片又不适用于所有的药物,其中 对水敏感的固体相最好选择干法制粒或熔 化制粒,如无水化合物生成水合物极快,
工艺控制方法
• 极少的水就可转化;若挤压力即可致使药 物相转化,则可制成胶囊,而不压成片剂。 还要控制工艺流程的条件, 对于水合物一 定要控制临界相对湿度、 温度、 湿法制粒、 干燥、 研磨和干法制粒等时的条件;针对 互变体系中的不同晶型,工艺流程温度也 需低于熔点。
• ④溶媒相变:溶媒相变存在于稳态被部分 或完全溶解的过程中,溶解度不同是主要 的驱动力,转化部分不仅限于溶解部分, 只要有溶媒就会发生相转化。此机制只能 完成亚稳态到稳态的转化。由3个连续的步 骤组成,即亚稳态相溶解,产生稳态相晶 核,稳态相结晶增长与亚稳态相的继续溶 解。药物动力学性质受晶核形成和增长的 影响,它反过来 通过溶解度、温度、接触
转化方式
• ②重建式转变: • 当变体结构间差异较大,在转变过程中需
要首先破坏原变体的结构,包括键性,配 位数及堆积方式等的变化,才能重新建立 起新变体的晶体结构。这类转变一般是不 可逆的。
转化方式
• 变体可逆转变与不可逆转变的原理:
• 对于一个单元系统,各种变体的吉布斯自 由能G均服从下列关系式:
影响固态相变的动力学性质,颗粒半径、 表面特征、粒度分布、辅料,杂质对固态 相变的影响较大。
ห้องสมุดไป่ตู้
药物晶型略谈ppt课件

公司: Abbott 药名:利托那韦(Norvir) 剂型:胶囊 教训:1998年,晶型发生变 化,药
品退市,直接经济损失上亿美元
13
晶型专利的重要性
不同层次的专利保护 • New Chemical Entity • Enantiomer • Salt Form • Crystal Form (Polymorph) • Formulation • Process
研发中心----
药物晶型略谈
20**-0*-** ****
1
引言---几个问题
• 何为晶型,其特点? • 晶体如何形成? • 晶型样品的制备? • 药物晶型的稳定性? • 药物晶型检测? • 晶型定性、定量控制?
2
总述
晶型是药物重要属性之一。因为不同的晶型可能有不同的物理化学性 质(比如溶解度,溶出速度,稳定性等)从而影响到药品的有效性、安 全性或质量。当固体药品存在多晶型现象,且不同晶型状态对药品的有 效性、安全性或质量可产生影响时,应对药品固体制剂、半固体制剂、 混悬剂等中的药用晶型物质状态进行定性或定量控制。
enter generic market without undue delay; Enjoy independently protectable IP(intellectual property) right.
14
如何筛选和选择药物新晶型
单晶培养
手动筛选
• 高通量晶型筛选(High throughput screening)
• 常用化学方法主要包括:重结晶法、快速溶剂去除法、沉淀法、种晶 法等;
• 常用物理方法主要包括:熔融结晶法、晶格物理破坏法、物理转晶法 等。
• 晶型样品制备方法可以采用直接方法或间接方法。各种方法影响晶型 物质形成的重要技术参数包括:溶剂(类型、组成、配比等)、浓度、成 核速率、生长速率、温度、湿度、光度、压力、粒度等。鉴于每种药 物的化学结构不同,故形成各种晶型物质状态的技术参数条件亦不同, 需要根据样品自身性质合理选择晶型样品的制备方法和条件。
晶型转变及其控制

对某一特定系统而言,这种相的自由能改变所 伴随的结构改变过程,叫做相转变或相变。英 文phase transition和transformation都用于表述相 变过程。
图3–1 稳定态、介稳态和不稳定态
2
同质异构体(polymorph)或变体(modification)和与同 质多晶或同质多相(polymorphism)现象
C为独立组元(组分)数,Φ为相数,2 代表温度和压力2个变量。
对于凝聚系统来说,压力的影响可以忽 略不计,于是温度成了惟一的外界条件。 在这种情况下,相律可写成
f * = C–Φ + 1, f *被称为条件自由度
4
§3.1 可逆与不可逆晶型转变
从热力学的角度看,一组同质多晶的变体中,吉布斯自由能最低的晶型是稳定的。 对于一个单元系统,各种变体的吉布斯自由能G均服从下列关系式:
晶型转变及其控制方法
2020/4/13
1
相
相变ห้องสมุดไป่ตู้
物质中具有相同化学成分和晶体结构的部分被称为相。相与相之间的转变叫相变。
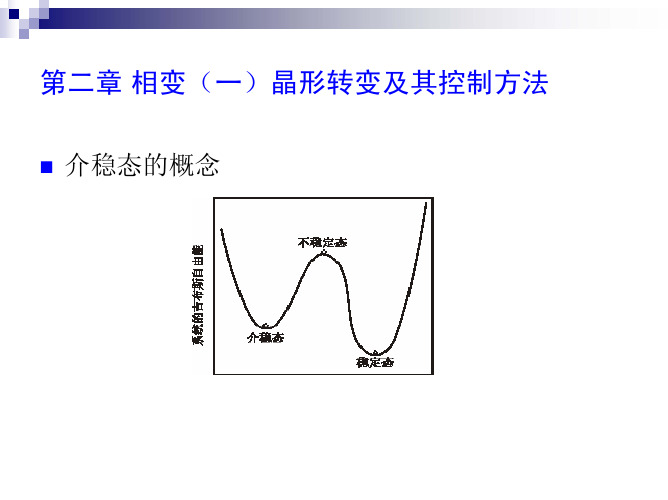
系统中存在的相,可以是稳定、介稳或不稳定的。稳定态指的是系统处在最低的 吉布斯自由能状态。在一定的热力学条件下,如果系统处在一个吉布斯自由能极 小值状态,而不是处在一个最小值状态,它就有可能转变到这个最小值状态;但 也可能会以原状态长期存在, 因为在局部的自由能极小值与最小值之间,存在 着一个势垒,这样的状态称为介稳态,如图2–1所示。当系统的温度、压力或对 系统的平衡发生影响的电场、磁场等条件发生改变时,这种介稳或不稳定状态下 的自由能会发生改变,相的结构(原子或电子分布)也相应地发生变化。
G = U + pV–TS,
(2–1)
式中U为该变体的内能;p是平衡蒸气压
晶形的转变及控制方法
ZrO2的晶型转变
单斜ZrO2
≈1 473K ≈1 273K
四方ZrO2
2 643K
立方ZrO2
立方和四方ZrO2的力学性能和杭热震性能优于单斜 相。 将立方相或四方相ZrO2保待至室温的方法
降低ZrO2的晶粒尺寸。 加入第二相氧化物以稳定ZrO2 。
ZrO2的相变增韧
陶瓷材料产生较大脆性的原因? 相变增韧
σ=
K1C Y L
利用部分稳定ZrO2存在于陶瓷基体里,在一定温度范围内可发 生由四方相向单斜相的晶形转变(伴有3-5%的体积变化), 通过微裂纹机制及应力诱导相变机制来改善陶瓷的强度和韧 性。 微裂纹机制 应力诱导相变机制
2.5 Ca2SiO4 (C2S)和Ca3SiO5 (C3S)的晶型转变 和水泥生产工艺控制
γ -C2 S
798 K
998 K
′ αL -C2 S
943K
1 433 K
′ αH -C2 S
1 K
液相
β–C2S
在硅酸盐水泥熟料烧成时,必须采 取急冷的工艺手段,使高活性的βC2S以介稳的形式保存下来。
表2–1
SiO2晶型转变时的体积变化
计算 采取 的温 度/K 1 273 1 273 1 273 1 273 在该温 度下转 变时的 体积效 应/% 计算 采取 的温 度/K 846 390 436 423 在该温度 下转变时 的体积效 应/% +0.82 +0.2 +0.2 +2.8
重构式转变
位移式转变
重构式转变
会引起化学键的断开以及原子的重新 组合,重新形成新的结构,所需能量 较大,转变过程较慢。
2.3 SiO2的晶型转变和应用
《晶体结构及其变化》课件

THANKS
感谢观看
晶体生长与退火
晶体生长
晶体生长是指晶体从小的结晶核开始,逐渐生长成为较大的 晶体的过程。晶体生长过程中,原子或分子在结晶核上按一 定的规律排列,形成晶体结构。
退火
退火是指将晶体加热至较高温度,然后缓慢冷却的过程。退 火可以消除晶体中的内应力,提高晶体的稳定性。
晶体形变与断裂
晶体形变
晶体形变是指晶体在外力作用下 发生形状改变的现象。晶体形变 过程中,原子或分子的排列发生 变化,导致晶体结构的变化。
分子排列方式对晶体 的物理性质有重要影 响,如密度、溶解度 等。
离子排列
在离子晶体中,离子通过静电 力相互连接,形成离子键。
离子排列方式决定了晶体的离 子导电性、光学性质等。
常见的离子晶体有氯化钠、氧 化镁等。
共价键与金属键
共价键是原子间通过共享电子形 成的化学键,常见于非金属元素
间。
金属键则是金属原子间通过电子 自由运动形成的化学键。
02
晶体结构的组成
原子排列
原子是构成晶体的基本单元,它 们在晶体中按照一定的规律排列
,形成晶格结构。
原子的排列方式决定了晶体的性 质,如硬度、熔点、导电性等。
常见的原子排列方式包括面心立 方、体心立方和密排六方等。
分子排列
在分子晶体中,分子 作为基本单元,通过 分子间作用力相互连 接。
分子排列可以通过X 射线晶体学等方法进 行测定。
晶体断裂
当晶体受到的形变超过其承受极 限时,会发生断裂。断裂过程中 ,晶体的原子或分子的排列被打 乱,形成非晶态物质。
晶体相变与转变
晶体相变
当外部条件发生变化时,如温度、压 力等,晶体的相会发生转变。相变过 程中,晶体的原子或分子的排列发生 变化,形成新的晶体结构。
厦门大学 材料科学基础(二) 第二章-a 相变(一)晶形转变及其控制方法

单元(单组分)系统
f = 0, 最大相数为3
f = 1-Φ+2
Φ=1, 最大自由度为2
2.0 具有多晶转变的单元系统相图
稳定相区 FCD:液相 ;ABE:β 晶型; EBCF:α -晶型;ABCD 以下:气相。 介稳相区
FCGH:过冷液相区
EBGH:过热β-晶型 EBK:过冷α-晶型
特点
晶体的升华曲线(或延长线)与液体的蒸发曲线(或延
长线)的交点是该晶体的熔点。 两种晶型的升华曲线的交点是两种晶型的多晶转变点。 在同一温度下,蒸气压低的相较稳定。 交汇于三相点的三条平衡曲线互相之间另外两条曲线之间。 同一温度时,在三相点附近比容差最大的两相之间的单变 量曲线或其介稳延长线居中间位置。
第二章 相变(一)晶形转变及其控制方法
介稳态的概念
晶型转变
当外界条件改变时,化学组成相同,晶体结构不同的同
质异构体(变体)之间发生的相互转变。
BaTiO3
与相图有关的基本概念
系统
指我们所选择的研究对象 。 系统中具有相同物理性质和化学性质的均匀部分的总和。
相
相与相之间有界面,可以用物理或机械办法分开。 一个相可以是均匀的,但不一定是一种物质。
组元
系统中每个可以单独分离出来并能独立存在的化学均匀物 质。
独立组元
是指独立可变的组元。
独立组元数=组元数-化学反应数
自由度
表示在一定的范围内,可以任意改变而不致引起旧相消失 或新相出现的变数。
独立变数=总变数-非独立变数
平衡状态
在组成、温度、压力一定的情况下,系统的状态长期保持 不变。
控制晶型

第二章晶型转变及其控制方法系统中存在的相,可以是稳定、介稳或不稳定的。
其吉布斯自由能如图2–1所示。
当系统的温度、压力或对系统的平衡发生影响的电场、磁场等条件发生改变时,这种介稳或不稳定状态下的自由能会发生改变,相的结构(原子或电子分布)也相应地发生变化。
此外,在一定的条件下,一种稳定相也可以转变成另一种稳定相,此即下文所说的可逆晶型转变。
对某一特定系统而言,相的自由能改变所伴随的结构改变过程,叫做相转变或相变。
图2–1 稳定态、介稳态和不稳定态化学组成相同的固体,在不同的热力学条件下,常会形成晶体结构不同的同质异构体(polymorph)[1, 2]或称为变体(modification),这种现象叫同质多晶或同质多相(polymorphism)[2]现象。
当温度和压力条件变化时,变体之间会发生相互转变,此称为晶型转变。
显然,晶型转变是相变的一种,也是最常见的一种固–固相变形式。
由于晶型转变,晶体材料的力学、电学、磁学等性能会发生巨大的变化。
例如,碳由石墨结构转变为金刚石结构后硬度超强,BaTiO3由立方结构转变为四方结构后具有铁电性。
可见,通过相变改变结构可达到控制固体材料性质的目的。
相律的表达式是自由度f= C–Φ+ 2,C为独立组元(组分)数,Φ为相数,数字2代表温度和压力2个变量。
对于凝聚系统来说,压力的影响可以忽略不计,于是温度成了惟一的外界条件。
在这种情况下,相律可写成f * = C–Φ+ 1,f * 被称为条件自由度。
对于单元(单组分)系统来说,C = 1,f * = 2–Φ。
由于所讨论的系统至少有1个相,所以单元凝聚系统条件自由度数最多等于1,系统的状态仅仅由温度1个独立变量所决定。
于是,在许多情况下,单元系统相变往往用流程图来表示,例如本章§2.3节对BaTiO3晶型转变所采用的表示法。
在另一些场合下,考虑压力变量的影响对讨论问题是有利的。
由于凝聚系统的平衡蒸气压实际上仍比大气压低得多,所以在讨论单元凝聚系统相图时,往往把压力坐标(纵标)加以夸大,画出来的相图中的曲线仅仅表示温度变化时系统中压力变化的大致趋势,这种情况如在本章§2.4~§2.6中所描述的SiO2、ZrO2和Ca2SiO4(C2S)单元系统带有晶型转变的相图。
第4周-1-晶态结构PPT课件

d. 球晶的生长过程
从中心晶核(多层片晶)开始,然后逐渐向外张开生长, 不断开叉形成捆束形态,最后形成填满空间的球状晶体。
偏光显微镜观察球晶的生长
0s
30s
60s
90s
120s
原子力显微镜观察球晶的生长
• 球晶较小时,呈现球形; • 晶核多并逐渐生长扩大后, 就成为不规则多面体
聚戊二酸丙二酯球晶
(1)单晶:
短程有序性和长程有序性贯穿整块晶体的晶体
a. 形成条件:极稀溶液(浓度<0.1%)中缓慢结晶
• 浓度<0.1%,可得单晶; • 0.1% <浓度< 1% ,多层片晶; • 浓度> 1% ,球晶
b. 结构特点:一定外形,长程有序 判别:衍射图上出现衍射点,而不是衍射环
透射电镜图
电子衍射图
高
固体
晶态 非晶态
分
取向态
子
织态结构
凝
聚
态
液体 液晶态:液晶聚合物
非晶态液体:聚合物熔体or 浓溶液
高分子单链凝聚态
钱人元:高分子单链凝聚态
高分子的凝聚态结构
决 定
材料的性能
获得 控制成型加工条件
高分子链结构
2.1 聚合物内聚能和内聚能密度
表征聚合物分子间的相互作用力的大小
1. 高分子间的相互作用力
所需要的能量E
E HV RT
△Hν: 摩尔蒸发热 RT: 汽化时所做的膨胀功
3. 内聚能密度 (CED):
单位体积凝聚体汽化时所需要的能量
CED E Vm
Vm:摩尔体积
分子间作用力强弱的表征
聚合物内聚能密度测定方法:
• 由于聚合物之间的分子间作用力超过了组成它的化学键 的键能,因此聚合物不能气化,不能直接测定其内聚能 和内聚能密度。
药物晶型转化与控制的研究进展

方法优缺点及应用建议
1、物理方法的优点是可以直接检测药物分子的晶体结构和分子构象,缺点 是对于一些非晶体药物难以准确描述。建议在药物研发和生产中,将物理方法与 其他方法结合使用,以更全面地了解药物多晶型的结构和性质。
2、化学方法的优点是可以提供药物多晶型的化学成分和分子质量信息,缺 点是对于一些化学性质相似的药物难以区分。建议在药物研发和生产中,结合使 用多种化学方法,以提高鉴别的准确性。
研究现状分析
当前,药物晶型转化与控制的研究已经取得了重要进展。在分子设计和高分 子合成方面,越来越多的新技术和新方法被用于药物的研发和制备。在药物晶型 转化方面,通过分子设计和高分子合成技术,可以成功地实现药物的定向输送和 控制释放。在药物晶型控制方面,加热、压力、添加剂等制备方法被广泛应用于 控制药物的晶型和性质。
3、结构方法的优点是可以提供药物多晶型的分子结构和分子动力学信息, 缺点是对于一些大分子药物难以准确描述。建议在药物研发和生产中,将结构方 法与其他方法结合使用,以更全面地了解药物多晶型的结构和性质。
结论
药物多晶型鉴别对于药物研发和生产具有重要意义,因为不同的多晶型可能 具有不同的物理、化学和生物特性,从而影响药物的疗效和安全性。本次演示介 绍了物理、化学和结构等多种鉴别方法,每种方法都有其优点和局限性。在实际 操作中,我们需要根据药物的性质和鉴别的需求,选择合适的方法或方法组合, 以获得更准确的结果。
然而,当前研究仍然存在一些问题,如缺乏系统性和完整性、实验方法和评 价指标的不一致等。因此,未来的研究需要进一步探讨药物晶型转化与控制的机 制和方法,加强跨学科合作,提高研究的系统性和完整性。
结论
本次演示总结了近年来药物晶型转化与控制的研究进展。通过对药物晶型转 化与控制的概念、原理、影响因素和应用进行详细阐述,说明了药物晶型转化与 控制在提高药物的疗效和安全性方面的重要作用。本次演示指出了当前研究的不 足之处和未来研究方向,为相关领域的研究提供了参考。
《药物晶型培训》PPT课件

药物晶型培训
张悦 2011年12月
一、晶体学基础知识
➢ 晶体的概念 ➢ 晶体的特征及共性 ➢ 晶胞及晶系
二、药物晶型
➢ 药物多晶型 ➢ 药物晶型的表征方法 ➢ 结晶问题讨论
药物晶型培训
药物晶型培训
晶体学的意义
1914年 劳厄发现晶体的X射线衍射 诺贝尔物理学奖 1915年 威康·劳伦斯·布拉格用X射线分析晶体结构
药物晶型培训
二、药物晶型
➢ 药物多晶型 ➢ 药物晶型的表征方法 ➢ 结晶问题讨论
药物晶型培训
Spectroscopy
常用固态表征方法
ssNMR,IR,Raman,Terahertz
Microscopy
SEM, Optical, AFM,
Scattering
X-ray, Laser
Thermal analysis
3个晶胞参数 a,b和c 2个晶胞参数 a和α 2个晶胞参数 a和c 2个晶胞参数 a和c 1个晶胞参数 a
药物晶型培训
二、药物晶型
➢ 药物多晶型 ➢ 药物晶型的表征方法 ➢ 结晶问题讨论
药物晶型培训
1.药物多晶型
• Polymorphism(多晶型现象) • The ability of a solid material to exist in more than one form or crystal structure. • Polymorphs(多晶型) • 1. Solid phase • 2. Same chemical composition • 3. Differnet molecular arrangements
药物晶型培训
一、晶体学基础知识
➢ 晶体的概念 ➢ 晶体的特征及共性 ➢ 晶胞及晶系
药物晶型研究讲座PPT课件

➢ 提高药物吸收速度 ➢ 延长血药浓度平台期 ➢ 稳定性差。
第18页/共36页
十、晶型药物的研究方法
常用的检测方法有:
➢ 显微镜技术 分为光学显微镜和电子显微镜。光学显微镜可以用
于观察晶体的形态特征。电子显微镜可用于快捷地鉴别微 小晶型药物样品。
第19页/共36页
➢ X-射线衍射技术 分为单晶X-射线衍射分析和粉末X-射线衍射分析。 单晶X-射线衍射分析技术是以一颗单晶体作为研究对象,
3 药物与溶剂分子作用产生的多晶型现象 当在某种适合溶剂条件下进行重结晶时,药物分子和
溶剂分子产生相互作用力,形成了与之结合的不同种类与不 同数量的溶剂化固体物质状态,这是最多的一种多晶型现象。
与水分子作用,形成结晶水与缔合水;与溶剂分子作 用,存在溶剂种类和数量的变化。
第11页/共36页
4 药物分子成盐产生的多晶型现象 成盐是增加和改善固体化学药物溶解性质的一种国际
三、影响固体化学物质产生多晶型现象的参量
1.固体物质的化学成分(单一成分、混合成分及含量,结 晶水成分及含量,结晶溶剂成分及含量);
2.固体物质的分子结构(构型,构象); 3.固体物质的晶体学参数(晶系,晶胞参数,对称元素); 4.固体物质分子排列规律及周期性(全局有序状态,部分 有序状态,全局无序状态); 5.固体物质分子内与分子间的作用力(氢键,盐键,配位 键)等。
第8页/共36页
7.相同化学药物,在不同的重结晶溶剂条件下,由于晶 体中所含有的药物分子立体手性参数变化而产生不同的晶 型固体物质。
8.相同化学药物,在不同的重结晶溶剂条件下,由于晶 体中所含有的药物分子自身构象参数变化而产生不同的晶 型固体物质。
第9页/共36页
晶型研究方法PPT课件

多晶型的主要分析手段
第13页/共25页
药物晶型的化学分析手段
• 1. Liquid NMR • 2. Mass spectroscropy • 3. Titration • 4. GC • 5. HPLC
第14页/共25页
药物晶型的物理分析手段
• 1. X-ray diffraction(powder and single crystal) • 2.Thermal methods (DSC/TGA..) • 3.Solid state NMR • 4.Raman/IR • 5.Melting point / Microscope method
第11页/共25页
1. 原研药公司对药物分子的晶型申请专利,可以延长药物的专利 保护,从而使自己的产品具有更长时间的市场独享权。
2. 仿制药公司来说,为了确保仿制药和原研药在生物利用度上的等 同性,也需要对原料药的晶型进行研究,以确保原料药和制剂的 质量,正因为如此美国药监局在ANDA申报中也对仿制药多晶型 控制有明确的指南。
第10页/共25页
• 药物分子通常有不同的固体形态,包括盐类,多晶,共 晶,无定形,水合物和溶剂合物;同一药物分子的不同 晶型,在晶体结构,稳定性,可生产性和生物利用度等 性质方面可能会有显著差异,从而直接影响药物的疗效 以及可开发性。如果没有很好的评估并选择最佳的药物 晶型进行研发,可能会在临床后期发生晶型的变化,从 而导致药物延期上市而蒙受巨大的经济损失,如果上市 后因为晶型变化而导致药物被迫撤市,损失就更为惨重。 因此,药物晶型研究和药物固态研发在制药业具有举足 轻重的意义。
3. 开发出药物的新晶型是能够打破原研药公司对晶型的专利保护, 提早将仿制药推向市场,也是近年来仿制药公司一个至关重要的 策略,而且如果能找到在稳定性,生物利用度,以及生产工艺方 面具有优越性的新晶型,还可以申请晶型专利保护,从而大大提 升自己的市场竞争力。
《无机固体材料化学》PPT课件

完整版课件ppt
12
§ 1- 3 晶体的微观特征
• (1)晶体的点阵结构 • 晶体结构=点阵+结构基元 • 一维点阵,结构基元:(-CH2)2
完整版课件ppt
13
二维点阵,结构基元:[B(OH)3]2
点阵参数 a, b,
完整版课件ppt
14
NaCl结构类型的晶胞
点阵参数: a, b, c, , ,
• (a)长程无序 • 无平移对称性
完整版课件ppt
24
• 衍射为弥散的晕 • 和宽化的衍射带
完整版课件ppt
25
(b)短程有序
lim g (r ) 1
r
• 双体概率分布函数: lim g (r ) 0
r 0
g(r) = r/o
完整版课件ppt
26
例:石英玻璃的结构 • r(Si-O) = 1.62Å;r(O-O) = 2.65Å
完整版课件ppt
10
§ 1- 2 晶体的宏观特征 (1)自范性: F(晶面数)+V(顶点数) = E (晶棱数) +2
晶面夹角(或交角)守恒定律
完整版课件ppt
11
• (2)晶体的均匀性,来源于晶体中原子 排布的周期性规则,宏观观察中分辨不 出微观的不连续性。
• (3)物理性质的异向性
• (4)稳定性,晶体有固定的熔点。
• 分子或原子不停地,自由地作长距离运 动即流动性。气体和液体具有流动性。
• 气体:无确定的体积和形状 • 液体:有一定的体积但无确定的形状 • 固体:分子或原子处于完全确定的平衡
位置作热振动。具有确定的形状和稳定 的结构即固体性。
完整版课件ppt
第二章 晶型转变及其控制方法概要
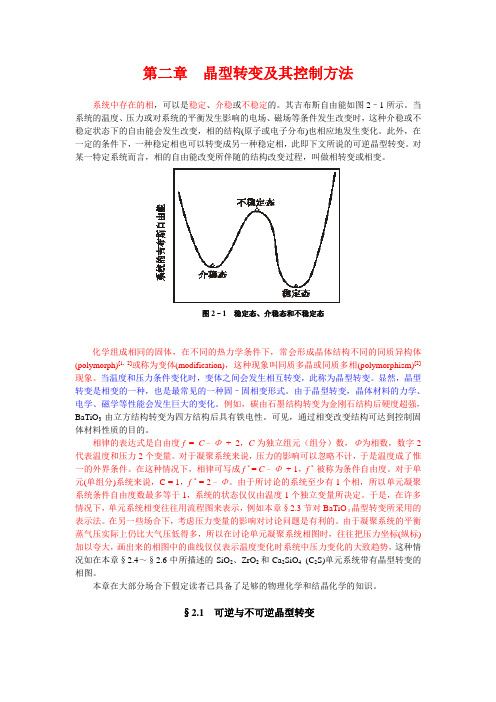
第二章晶型转变及其控制方法系统中存在的相,可以是稳定、介稳或不稳定的。
其吉布斯自由能如图2–1所示。
当系统的温度、压力或对系统的平衡发生影响的电场、磁场等条件发生改变时,这种介稳或不稳定状态下的自由能会发生改变,相的结构(原子或电子分布)也相应地发生变化。
此外,在一定的条件下,一种稳定相也可以转变成另一种稳定相,此即下文所说的可逆晶型转变。
对某一特定系统而言,相的自由能改变所伴随的结构改变过程,叫做相转变或相变。
图2–1 稳定态、介稳态和不稳定态化学组成相同的固体,在不同的热力学条件下,常会形成晶体结构不同的同质异构体(polymorph)[1, 2]或称为变体(modification),这种现象叫同质多晶或同质多相(polymorphism)[2]现象。
当温度和压力条件变化时,变体之间会发生相互转变,此称为晶型转变。
显然,晶型转变是相变的一种,也是最常见的一种固–固相变形式。
由于晶型转变,晶体材料的力学、电学、磁学等性能会发生巨大的变化。
例如,碳由石墨结构转变为金刚石结构后硬度超强,BaTiO3由立方结构转变为四方结构后具有铁电性。
可见,通过相变改变结构可达到控制固体材料性质的目的。
相律的表达式是自由度f= C–Φ+ 2,C为独立组元(组分)数,Φ为相数,数字2代表温度和压力2个变量。
对于凝聚系统来说,压力的影响可以忽略不计,于是温度成了惟一的外界条件。
在这种情况下,相律可写成f * = C–Φ+ 1,f * 被称为条件自由度。
对于单元(单组分)系统来说,C = 1,f * = 2–Φ。
由于所讨论的系统至少有1个相,所以单元凝聚系统条件自由度数最多等于1,系统的状态仅仅由温度1个独立变量所决定。
于是,在许多情况下,单元系统相变往往用流程图来表示,例如本章§2.3节对BaTiO3晶型转变所采用的表示法。
在另一些场合下,考虑压力变量的影响对讨论问题是有利的。
由于凝聚系统的平衡蒸气压实际上仍比大气压低得多,所以在讨论单元凝聚系统相图时,往往把压力坐标(纵标)加以夸大,画出来的相图中的曲线仅仅表示温度变化时系统中压力变化的大致趋势,这种情况如在本章§2.4~§2.6中所描述的SiO2、ZrO2和Ca2SiO4(C2S)单元系统带有晶型转变的相图。
第二章相变(一)晶形转变及其控制方法

ZrO2的晶型转变
单斜ZrO2
≈1 473K ≈1 273K
四方ZrO2
2 643K
立方ZrO2
立方和四方ZrO2的力学性能和杭热震性能优于单斜 相。 将立方相或四方相ZrO2保待至室温的方法
降低ZrO2的晶粒尺寸。 加入第二相氧化物以稳定ZrO2 。
ZrO2的相变增韧
陶瓷材料产生较大脆性的原因? 相变增韧
可逆晶型转变
特点:晶型转变温பைடு நூலகம்低于两 种变体的熔点
不可逆晶型转变
特点:晶型转变温度高于两 种变体的熔点
2.2 位移式与重构式晶型转变
位移式转变
不破坏化学键,可通过原子位置的微小位 移或键角的转动来实现,转变速度较快。 一级配位:最近邻 原子之间的键合 二级配位:次近邻 原子之间的相互作 用
(a)α–方石英;(b)α–鳞石英;(c)β–石英
重构式转变
会引起化学键的断开以及原子的重新 组合,重新形成新的结构,所需能量 较大,转变过程较慢。
2.3 SiO2的晶型转变和应用
SiO2一元相图
由克劳修斯-克拉佩龙方程判断转变时的体积变化
dp ∆H = dT T∆V
ΔH:相变热效应 ; ΔV:体积变化
从低温变体向高温变体转变时,为吸热过程,ΔH为正值,若相图 上曲线的斜率(dp/dT)也为正值,则ΔV为正值,即体积膨胀。
σ=
K1C Y L
利用部分稳定ZrO2存在于陶瓷基体里,在一定温度范围内可发 生由四方相向单斜相的晶形转变(伴有3-5%的体积变化), 通过微裂纹机制及应力诱导相变机制来改善陶瓷的强度和韧 性。 微裂纹机制 应力诱导相变机制
2.5 Ca2SiO4 (C2S)和Ca3SiO5 (C3S)的晶型转变 和水泥生产工艺控制
晶型转变及其控制ppt课件

(2–2)
完整版PPT课件
6
从图2–3可看出,晶型Ⅱ的自由 能在低于熔点的任何温度下均较 晶型Ⅰ高,表明晶型Ⅱ总是处于介 稳状态,随时都有转变成晶型Ⅰ 的可能。但晶型Ⅰ要转变成晶型 Ⅱ则必须先加热到TmⅠ熔融,然 后使熔体过冷到一定的温度(例 如Tx),才能转变成晶型Ⅱ。在 Tx温度时,晶型Ⅰ的自由能是3 个相中最低的,因而最稳定,从
化学组成相同的固体,在不同的热力学条件 下,常会形成晶体结构不同的同质异构体 (polymorph) 或 称 为 变 体 (modification) , 这 种现象叫同质多晶或同质多相 (polymorphism)现象。
完整版PPT课件
ቤተ መጻሕፍቲ ባይዱ
3
相律相关知识
相律的表达式是自由度 f = C–Φ + 2,
对某一特定系统而言,这种相的自由能改变所 伴随的结构改变过程,叫做相转变或相变。英 文phase transition和transformation都用于表 述相变过程。
图3–1 稳定态、介稳态和不稳定态 完整版PPT课件
2
同质异构体(polymorph)或变体(modification)和与 同质多晶或同质多相(polymorphism)现象
p是平衡蒸气压可编辑课件ppt具有不可逆晶型转变的某物质的内能u与自由能g的关系其中uluuslss从图23可看出晶型的自由能在低于熔点的任何温度下均较晶型高表明晶型总是处于介稳状态随时都有转变成晶型的可能
晶型转变及其控制方法
完整版PPT课件
1
相
相变
物质中具有相同化学成分和晶体结构的部分被称为相。相与相之间的转变叫相变。
过冷熔体中先结晶的是介稳的晶 型Ⅱ,然后由晶型Ⅱ再转变成稳 定晶型Ⅰ。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
.
.
感谢亲观看此幻灯片,此课件部分内容来源于网络, 如有侵权请及时联系我们删除,谢谢配合!
化学组成相同的固体,在不同的热力学条件 下,常会形成晶体结构不同的同质异构体 (polymorph) 或 称 为 变 体 (modification) , 这 种现象叫同质多晶或同质多相 (polymorphism)现象。
.
相律相关知识
相律的表达式是自由度 f = C–Φ + 2,
C为独立组元(组分)数,Φ为相数,2 代表温度和压力2个变量。
.
(2–2)
.
从图2–3可看出,晶型Ⅱ的自由 能在低于熔点的任何温度下均较 晶型Ⅰ高,表明晶型Ⅱ总是处于介 稳状态,随时都有转变成晶型Ⅰ 的可能。但晶型Ⅰ要转变成晶型 Ⅱ则必须先加热到TmⅠ熔融,然 后使熔体过冷到一定的温度(例 如Tx),才能转变成晶型Ⅱ。在 Tx温度时,晶型Ⅰ的自由能是3 个相中最低的,因而最稳定,从 过冷熔体中先结晶的是介稳的晶 型Ⅱ,然后由晶型Ⅱ再转变成稳 定晶型Ⅰ。
对某一特定系统而言,这种相的自由能改变所 伴随的结构改变过程,叫做相转变或相变。英 文phase transition和transformation都用于表 述相变过程。
图3–1 稳定态、介稳态和不稳定态
.
同质异构体(polymorph)或变体(modification)和与 同质多晶或同质多相(polymorphism)现象
晶型转变及其控制方法
.
相
相变
物质中具有相同化学成分和晶体结构的部分被称为相。相与相之间的转变叫相变。
系统中存在的相,可以是稳定、介稳或不稳定的。稳定态指的是系统处在最低的 吉布斯自由能状态。在一定的热力学条件下,如果系统处在一个吉布斯自由能极 小值状态,而不是处在一个最小值状态,它就有可能转变到这个最小值状态;但 也可能会以原状态长期存在, 因为在局部的自由能极小值与最小值之间,存在 着一个势垒,这样的状态称为介稳态,如图2–1所示。当系统的温度、压力或对 系统的平衡发生影响的电场、磁场等条件发生改变时,这种介稳或不稳定状态下 的自由能会发生改变,相的结构(原子或电子分布)也相应地发生变化。
对于凝聚系统来说,压力的影响可以忽 略不计,于是温度成了惟一的外界条件。 在这种情况下,相律可写成
f * = C–Φ + 1, f *被称为条件自由度
.
§3.1 可逆与不可逆晶型转变
从热力学的角度看,一组同质多晶的变体中,吉布斯自由能最低的晶型是稳定的。 对于一个单元系统,各种变体的吉布斯自由能G均服从下列关系式:
G = U + pV–TS,
(2–1)
式中U为该变体的内能;p是平衡蒸气压
对于凝聚体系,p-般很小;V是 体积,晶型转变时,体积变化一 般不大;pV项常可忽略不计[2]; T是绝对温度;S是一定晶型的熵, 高温稳定型晶体的熵值比低温稳 定型的大。绝对零度时,吉布斯 自由能G基本由内能项决定[2]。 随着温度增加,TS这一项渐显重 要,不能再轻视。当温度足够高 时,一些具有较大熵值的晶型, 虽然内能也可能较高,其自由能
