无机化工产品典型生产工艺
第三章 无机化工产品典型生产工艺2-硫酸

一段焙烧温度控制为900℃,炉气含20%SO2,经除尘后与渣 同进入二段焙烧。二段温度为800℃,出二段炉气SO2含量约 10%。
四、热能回收及烧渣利用
1、热能回收
焙烧时放出大量的热,炉气温度850~950℃,
若直接通入净化系统→设备要求高;直接冷却 后净化→浪费能量。
通常设置
废热锅炉来回收热量,或产蒸汽发
2、含水多矿与含水少矿适当配合
3、保证燃烧稳定性,含煤硫铁矿不宜太多 4、有无足够之供应量,并兼顾其成本
10.1.2 硫铁矿制二氧化硫炉气
一、焙烧前矿石原料的预处理
主要有3步:粉碎、配矿、干燥。
◆粉碎◆
一般采用二级粉碎,先用腭式压碎机粗碎,再用辊式 压碎机细碎,要求粒度<4mm.
◆配料◆
聚中心,在除雾器可以将其除去。
As2O3 ,SeO2在气体中的饱和浓度
温度/℃ 50 70 As2O3饱和浓度 /mg/Nm3 0.016 0.310 SeO2 饱和浓度 /mg/Nm3 0.044 0.880
热分解
4FeAsS=4FeS+As4
2FeS2=2FeS+S2
4FeAsS+4FeS2=8 FeS+ As4S4
氧化 As4+3O2=2As2O3 1/2 S2+O2= SO2
As4S4+7 O2=2As2O3+4 SO2 3FeS+5 O2 =Fe3O4+3 SO2
在脱砷焙烧中,关键是只能生成磁性氧化铁,避免Fe2O3。
我国硫酸工业发展现状
硫铁矿为 原料/% 硫磺为原 料/% 冶炼烟气 为原料/% 总产量/万t 世界排名
硝酸的生产工艺

硝酸的生产工艺硝酸是一种重要的无机化学品,广泛应用于化工行业和农业生产中。
硝酸的生产工艺主要有亚硝酸氧化法、铵盐法和硝基氧化法等。
1. 亚硝酸氧化法:亚硝酸氧化法是硝酸工业生产中最常用的方法。
该方法以氨为原料,通过两步反应生成硝酸。
首先,通过合成氨制取亚硝酸,然后将亚硝酸氧化为硝酸。
具体工艺如下:(1)合成氨制备亚硝酸反应。
在催化剂存在下,将氨与氧气在高温下反应得到亚硝酸:NH3 + O2 → HNO2 + H2O(2)亚硝酸氧化为硝酸反应。
在催化剂存在下,将亚硝酸与氧气反应得到硝酸:2HNO2 + O2 → 2HNO32. 铵盐法:铵盐法是通过铵盐来制备硝酸的方法。
这种方法主要有铵硫酸法和铵硝酸法两种。
具体工艺如下:(1)铵硫酸法。
将硫酸与氨反应得到硫酸铵,然后将硫酸铵在高温下脱水,生成硝酸:2NH3 + H2SO4 → (NH4)2SO4(NH4)2SO4 → 2NH3 + H2SO4 + H2O2NH3 + H2SO4 + H2O + 1/2O2 → 2HNO3 + (NH4)2SO4(2)铵硝酸法。
将铵硫酸和硝酸反应得到硝酸铵,然后经过脱水处理,生成硝酸:HNO3 + NH4OH → NH4NO3 + H2ONH4NO3 → N2O + 2H2O2NH4NO3 → 2N2O + O2 + 4H2ON2O + 3O2 → 2N2O52N2O5 + H2O → 2HNO33. 硝基氧化法:硝基氧化法是将有机化合物中的氨基或羟基氧化为硝基的方法,然后生成硝酸。
这种方法适用于有机合成过程中的硝化反应。
具体工艺如下:R-NH2 + 2HNO3 → R-NO2 + 2H2O + H2OR-OH + HNO3 → R-ONO2 + H2O以上是硝酸的主要生产工艺,不同的工艺适用于不同情况下的生产需求。
在实际生产中,还需要考虑反应条件、催化剂的选择、产品纯度的控制等因素,以提高生产效率和产品质量。
同时,硝酸的生产过程涉及一些化学反应和氧化,所以在操作过程中需要注意安全措施,以防止事故发生。
硫酸铝制造工艺流程

硫酸铝制造工艺流程硫酸铝,又称硫酸铝明矾,是一种重要的无机化工产品,广泛用于水处理、造纸、皮革、化肥等多个行业。
硫酸铝制造工艺流程通常包括矿石选矿、酸溶浸出、结晶析出、过滤洗涤、干燥、包装等多个步骤。
下面将针对每个步骤进行详细介绍。
一、矿石选矿硫酸铝的主要原料是明矾矿,常见的有黄铁矾石、白铝矾石等。
矿石选矿是指将原矿进行破碎、研磨、浮选等物理化学处理,以获得含铝的矿石。
一般选矿过程包括:原矿破碎、磨矿、洗涤、浮选和脱水等步骤,其目的是将矿石中的杂质物质与有用的矿物质分离开来,为后续的冶炼提供优质的原料。
二、酸溶浸出选矿后的矿石需要进行酸溶浸出,将铝矾土中的铝用酸溶解出来。
一般使用的酸有硫酸、氯化氢等。
酸溶浸出工艺包括浸出槽、搅拌器、过滤等设备,溶解过程需要控制温度、酸浓度、搅拌速度等参数,以提高溶解效率。
三、结晶析出通过酸溶浸出后,获得的溶液需要进行结晶析出,将铝的盐析出成为硫酸铝结晶体。
结晶析出通常是将浸出液加热浓缩,然后在结晶槽内冷却结晶。
结晶过程需要控制温度、pH 值、搅拌速度等参数,以获得均匀的结晶体。
四、过滤洗涤在结晶析出后,生成的硫酸铝晶体需要进行过滤洗涤,去除悬浮的杂质和残留的酸液。
通常使用压滤机、真空过滤机等设备进行过滤,然后用清水进行洗涤。
过程中需要控制滤饼的厚度、滤饼的湿度和洗涤的次数,以确保产品的质量。
五、干燥过滤洗涤后的硫酸铝晶体需要进行干燥处理,去除水分,以获得干燥的硫酸铝成品。
干燥工艺通常采用热风炉、干燥机等设备,控制温度、湿度和转速,保证产品的干燥均匀和质量稳定。
六、包装最后,干燥后的硫酸铝产品需要进行包装,包括袋装、散装等方式,然后进行质检、产品标识、装箱和储存等流程,以待出厂销售。
以上便是硫酸铝制造工艺流程的基本介绍,工艺流程中每一个步骤的参数和设备都需要精确控制,以确保产品质量和生产效率。
同时,还需要关注环保和安全生产,合理处理生产废水和废气,确保生产过程的环保和安全。
无机化工产品典型生产工艺

受限制
特
征
对粘结性煤
受限制 需搅拌装置
0~5
好 受限制
90% 70% <200目 ﹤200 目
不受限制
不受限制
典型煤种
无烟煤 褐煤
褐煤
任何煤种
续表
气化压力,MPa
气化区最高温度, ℃
气化炉出口温度,
操
℃
作
特
耗氧量
征
耗蒸汽
常压 2~3 〈灰软化温度
约100 无低 高高
常压 1.0
常压 3~6.5
850~900 约1100 1350~1600
温度一定、压力升高时, H2及CO含量降低; CO2 CH4等增加
煤气化生产方法及主要设备
⑴生产方法分类
煤气化过程需要吸热和高温,工业上采用燃烧 煤来实现。气化过程按操作方式分为:间歇式 和连续式,前者的工艺较后者落后,现正在被 淘汰。现一般按采用的反应器类型分为:固定 床(移动床)、流化床、气流床和熔融床。前 三种以被工业生产采用,而熔融床处于中试阶 段。
间歇操作是通过控制阀门的开启顺序和开启时 间达到制气的目的-气体组成及热量的利用。
⑶固定床连续式化制水煤气
固定床连续式气化制水煤气法由德国鲁奇公司 开发。燃料块状煤或焦炭由炉顶定时加入,气 化剂为水蒸气和纯氧混合气,在汽化炉中同时 进行碳与氧的燃烧放热反应和碳与蒸汽的气化 吸热反应,调节H2O/O2比例,就可连续制气, 生产强度较高,且煤气质量稳定。但因煤气中 CH4和CO2含量高,CO含量低,一般作城市煤气
34~36 30~40 13~15
31
35
58
45
10
18
N2 %(体积)
约20 0.5
氟硅酸钠生产工艺

氟硅酸钠生产工艺
氟硅酸钠是一种重要的无机化工原料,用于制备氟化物、硅酸盐和玻璃等产品。
下面是氟硅酸钠的生产工艺:
1. 原料准备:将硅酸钠和氢氟酸进行预处理。
硅酸钠经过脱水处理得到无水硅酸钠,氢氟酸则是通过冷冻晶体分离、脱水和干燥处理得到。
2. 配料混合:将无水硅酸钠和氢氟酸按照一定比例混合均匀。
通常情况下,用于制备氟硅酸钠的硅酸钠与氢氟酸的摩尔比为1:3。
3. 反应过程:将混合均匀的配料倒入反应釜中,加热,控制温度在60-80℃。
反应过程中产生的氟硅酸钠会逐渐析出,并进行晶体生长。
4. 晶体筛选:反应完毕后,将产生的氟硅酸钠晶体进行筛选,去除杂质。
5. 湿法处理:将筛选后的氟硅酸钠晶体进行湿法处理,加入适量的水溶解。
溶解过程中需要控制温度和搅拌速度,以保证氟硅酸钠充分溶解。
6. 过滤和干燥:将溶解后的氟硅酸钠溶液进行过滤,除去残渣和杂质。
过滤后的溶液进行干燥处理,通常采用喷雾干燥法或真空干燥法。
7. 成品包装:将干燥后的氟硅酸钠粉末进行包装,通常采用塑料袋或桶装。
氟硅酸钠生产工艺主要有湿法法和干法法两种,以上是湿法法的生产工艺流程。
在实际生产中,还需要根据具体的工艺要求和设备条件进行调整和优化。
无机化工工艺流程

无机化工工艺流程无机化工是指以无机原料为主要原料,在一定的工艺条件下,通过物理或化学方法进行加工、转化、分离等一系列操作,生产各种无机化工产品的工艺过程。
下面将介绍几种常见的无机化工工艺流程。
1.硫酸工艺流程硫酸是一种重要的无机化工产品,广泛应用于冶金、化工、电子、环保等行业。
硫酸的生产工艺主要包括硫磺燃烧工艺和硫铁矿热法工艺两种。
以硫磺燃烧工艺为例,其工艺流程如下:硫磺→磺磺容器→气体先后通过富硝酸钡床和浓硫酸吸收器→去湿塔→浓硫酸。
2.氯碱工艺流程氯碱是指氯气和碱性物质(如氢氧化钠、氢氧化钾、氨水等)产生的化学反应。
氯碱工艺主要包括氨碱工艺和氯碱电解工艺两种。
以氨碱工艺为例,其工艺流程如下:氨气和炼焦气体→炉尾烟气处理装置→煤气→冷凝→硫粉→脱硫装置→制氢→氧化→水神经塔→浓氨碱液。
3.硅酸盐工艺流程硅酸盐是由硅酸盐矿石经过碱熔或盐酸浸取法提取而得的化合物。
硅酸盐的生产工艺主要包括玻璃制造工艺和陶瓷制造工艺两种。
以玻璃制造工艺为例,其工艺流程如下:石英矿石、烟煤→一系列预处理步骤(如破碎、磁选、除铁、煅烧等)→玻璃熔炼炉→玻璃浴→玻璃鼓包→玻璃冷却、切割和加工。
4.硝酸工艺流程硝酸是一种重要的化工原料,广泛应用于农业、化工、煤炭等领域。
硝酸的生产工艺主要包括铵硝酸工艺和硫酸硝酸工艺两种。
天然气→压缩机→压氧体→反应器→分离器→焙烧器→冷却器→分离器→浓硝酸。
5.氧化铝工艺流程氧化铝是一种重要的无机金属材料,主要用于冶金、建筑、电力等领域。
氧化铝的生产工艺主要包括贵金属电解工艺和碳电极电解工艺两种。
以碳电极电解工艺为例,其工艺流程如下:铝石(主要成分为氧化铝)→磨碎→矿石→碳负极→电解池→铝液→铸锭机→铝锭。
以上仅为几种常见的无机化工工艺流程的简单介绍,不同的无机化工产品具体的生产过程可能有所不同。
无机化工工艺的优化和改进将有助于提高产品质量、降低生产成本,并在环保方面做出更多贡献。
液体三氯化铁生产工艺

液体三氯化铁生产工艺
液体三氯化铁是一种常用的无机化工原料,广泛应用于水处理、金属加工、染料合成等领域。
其生产工艺主要包括氯化铁的制备和液态化处理两个步骤。
首先是氯化铁的制备。
氯化铁一般通过氢氧化铁与盐酸反应得到。
具体工艺步骤如下:
1. 原料准备:准备足量的氢氧化铁和盐酸。
氢氧化铁可以通过在氧化铁溶液中滴入氢氧化钠溶液沉淀得到,并经过洗涤、过滤、干燥等处理得到干燥的氢氧化铁。
2. 反应装置准备:将制备好的干燥氢氧化铁加入反应容器中,加入足够的盐酸。
3. 反应过程:控制反应温度在40-60摄氏度之间,搅拌反应溶液,反应一段时间,使氢氧化铁完全与盐酸反应生成氯化铁。
4. 沉淀与分离:反应结束后,放置一段时间,使固体氯化铁沉淀。
然后通过过滤、洗涤等处理,分离固体氯化铁。
通过上述工艺步骤,可以得到氯化铁的产品。
接下来是液态化处理。
1. 溶解固体氯化铁:将得到的固体氯化铁加入适量的水中,搅拌溶解,使其转化为液态。
2. 过滤杂质:通过过滤等工艺,去除溶解中的杂质和不溶于水的固体颗粒,保证液体三氯化铁的纯度。
3. 盐酸调节:根据产品的要求,加入适量的盐酸进行调节,使液体三氯化铁的酸碱度适宜。
4. 包装与贮存:将调节好的液体三氯化铁进行包装,通常使用塑料桶或其他耐腐蚀的容器进行贮存和运输。
通过以上的制备和液态化处理工艺,可以获得高纯度的液体三氯化铁产品。
在实际生产中,还需要注意控制反应条件、操作规范和质量检测等环节,以确保产品的质量和稳定性。
同时,还需要注意安全生产,避免对环境和人身造成损害。
铬酸钠生产工艺

铬酸钠生产工艺
铬酸钠是一种重要的无机化工产品,广泛应用于染料、农药、涂料等行业。
以下是铬酸钠的生产工艺。
铬酸钠的生产主要是通过铬酸三钠和一价铬盐反应生成的。
具体的生产工艺如下:
1. 原料准备:准备一价铬盐(如硫酸亚铬、硫酸铬或氯化铬等)和碳酸钠。
2. 铬酸三钠制备:在反应釜中加入适量的碱液(如氢氧化钠、碳酸钠或碱石灰)溶解,加热至80-90℃,然后加入硫酸铬或
氯化铬等一价铬盐溶液,边加边搅拌,使其完全反应。
反应结束后,过滤得到含有铬酸三钠的溶液。
3. 重结晶:将铬酸三钠溶液加热浓缩至一定浓度,然后静置结晶,使溶液中的铬酸三钠结晶出来。
过滤得到结晶体,将其洗涤干净。
4. 铬酸三钠转化为铬酸钠:将铬酸三钠放入刮板蒸发器中进行干燥,加热至适当温度,使其分解生成铬酸钠。
通过热气流将含有铬酸钠蒸汽输送至冷凝器,使其冷却凝结为固体。
5. 细粉处理和包装:将冷凝器中得到的固体铬酸钠进行研磨,得到所需的细粉。
之后,对细粉进行过筛和干燥处理,最后将其包装称为成品。
需要注意的是,在整个生产过程中,应控制反应温度、反应时间和pH值等参数,以保证产品质量。
此外,还需要对生产过程进行严格的管理和监控,确保生产环境的安全和卫生。
以上就是铬酸钠的生产工艺。
通过合理的操作和控制,可以实现高效、环保的铬酸钠生产,并满足不同行业的需求。
常见无机化工产品的生产过程
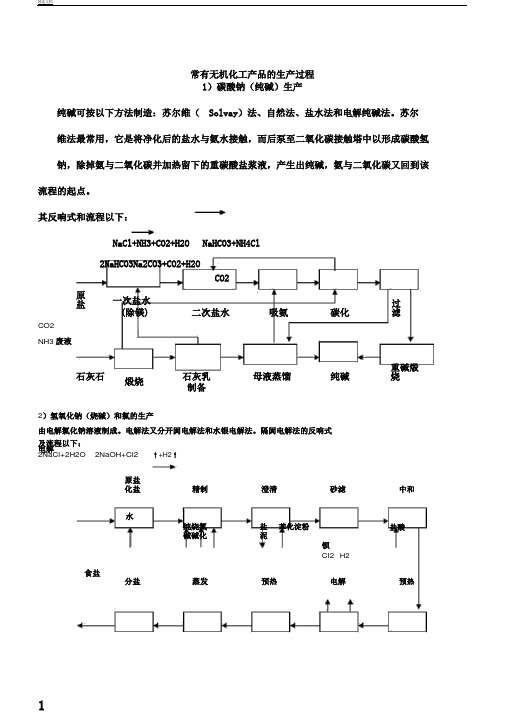
常有无机化工产品的生产过程1)碳酸钠(纯碱)生产纯碱可按以下方法制造:苏尔维(Solvay)法、自然法、盐水法和电解纯碱法。
苏尔维法最常用,它是将净化后的盐水与氨水接触,而后泵至二氧化碳接触塔中以形成碳酸氢钠,除掉氨与二氧化碳并加热留下的重碳酸盐浆液,产生出纯碱,氨与二氧化碳又回到该流程的起点。
其反响式和流程以下:NaCl+NH3+CO2+H2O NaHCO3+NH4Cl2NaHCO3Na2CO3+CO2+H2OCO2原盐一次盐水二次盐水吸氨碳化过滤(除镁) CO2NH3废液石灰石煅烧石灰乳母液蒸馏纯碱重碱煅烧制备2)氢氧化钠(烧碱)和氯的生产由电解氯化钠溶液制成。
电解法又分开阂电解法和水银电解法。
隔阂电解法的反响式及流程以下:电解2NaCl+2H2O 2NaOH+Cl2↑+H2↑原盐化盐精制澄清砂滤中和水纯烧氯碱碱化盐苯化淀粉泥盐酸钡Cl2H2食盐分盐蒸发预热电解预热液体烧碱浓碱液熬浓固体烧碱在隔阂电解槽生产过程中,膜片(石棉隔阂)把生成的气体氢和氯分开。
水银电解法的反响式和流程以下:电解2NaCl+2nHg Cl2↑+2NaHgn2NaHgn+2H2O2NaOH+H2↑+2nHg纯烧氯碱碱化钡苛化淀粉盐酸食盐化盐精制澄清砂滤中和淡盐水H2水银Cl2电解室预热散固体烧碱熬碱解汞室液体烧碱淡盐水(办理后去化盐 )在水银电解槽生产过程中,作为阴极的液态汞与电解生成的碱金属钠形成汞齐,输到另一分开的槽中,与水接触生成氢氧化钠。
3)盐酸生产大部分盐酸是有机氯化过程的副产品,此外,也有由电解食盐水法的氢与氯直接合成制得。
直接合成法的反响式及流程以下:Cl2+H22HCl水H2合成炉冷却器汲取塔冷却器Cl2盐酸成品包装盐酸贮槽4)硫酸生产有接触法、亚硝基法。
主要用接触法生产。
接触法按所用原料不一样,又分硫磺法、硫铁矿法、磷石膏法。
一般以硫铁矿法最常用,该法的反响式及生产流程以下:4FeS2+11O22Fe2O3+8SO22SO2+O22SO3SO3+H2O H2SO4硫铁矿(FeS2)原料办理焙烧净化空气5)硝酸生产主要用氨氧化法生产。
无机化工生产技术

模块一:合成氨生产1、三大步骤:原料气的制取、原料气的净化和氨的合成。
2、合成氨的原料:煤、天然气和重油。
3、半水煤气的组成:CO+H2/N2=3.1—3.2.。
4、为解决供热与制气的矛盾,可采用两种方法解决:间歇制气法和富氧空气或纯氧连续氧化法。
5、间歇式造气炉的工作循环:5个阶段为吹风、一次上吹、下吹、二次上吹和空气吹净。
6、原料气中的硫化物主要分为两大类:无机硫H2S和有机硫,如二硫化碳、硫氧化碳、硫醇和噻吩。
硫化氢含量最多。
7、脱硫方法分为湿法脱硫和干法脱硫。
湿法脱硫主要有栲胶脱硫技术、改良ADA法脱硫技术和PDS法脱硫。
干法脱硫按其性质分为三种类型:加氢转化催化剂型、吸收型或转化吸收型和吸收型;主要技术有:活性炭脱硫技术、有机硫加氢转化脱硫法和氧化锌脱硫法。
8、湿法脱硫三个基本步骤:a、在脱硫塔中脱硫剂的碱性吸收剂将原料气中的硫化氢吸收b、在再生塔中通入空气将吸收到溶液中的硫化氢氧化,以及吸收剂的循环回收c、单质硫的浮选和净化凝固。
9、基本原理:一氧化碳与水蒸气反应生成二氧化碳和氢气的过程。
这是一个需要催化剂参与的可逆、放热、等体积的化学反应。
10、变换反应催化剂:铁镁系催化剂(主要成分是氧化铁,对有机硫有较好的转化能力)、铁铬系催化剂和钴钼耐硫催化剂(不仅能耐高硫原料气,而且对有机硫有70%的转化率,有很宽的活性温度范围)。
11、耐硫变换催化剂的特点:有很好的低温活性、有突出的耐硫和抗毒性、强度高、可再硫化。
主要不足:使用前必须经过硫化处理。
12、中变催化剂的升温还原:氧化铁必须还原为四氧化三铁才具有催化活性。
13、脱碳方法分为湿法脱碳法和干法脱碳法。
湿法脱碳主要有碳酸丙烯酯脱碳法(物理吸收)、NHD脱硫脱碳(物理吸收)和改良热钾碱法(化学法)。
干法脱碳技术有变压吸附和变温吸附。
14、改良热钾碱法基本原理:碳酸钾和二氧化碳反应生成碳酸氢钾。
体积缩小、气液相放热反应;加压、降温操作有利于脱碳反应向右边移动,有利于提高溶液中碳酸钾的转化率。
三氯化硼生产工艺

三氯化硼生产工艺三氯化硼是一种重要的无机化工产品,广泛应用于化工、冶金、玻璃等行业。
以下是三氯化硼的生产工艺的详细介绍。
三氯化硼的生产工艺主要有两种方法:硼酸与盐酸反应法和三氯化钛与硼酸反应法。
硼酸与盐酸反应法:首先将硼酸和盐酸按一定的比例混合,反应生成硼酸盐。
然后将硼酸盐与盐酸浓缩,产生三氯化硼气体。
最后通过冷却、凝固和干燥等步骤,得到三氯化硼的固体产物。
三氯化钛与硼酸反应法:首先将三氯化钛和硼酸按一定的比例混合,反应生成氯化钛酸铵。
然后将氯化钛酸铵溶液与盐酸反应,产生三氯化钛。
最后将三氯化钛与硼酸按一定的比例反应,生成氯化硼。
最后通过冷却、凝固和干燥等步骤,得到三氯化硼的固体产物。
以上两种方法中,硼酸与盐酸反应法是比较常用的生产方法。
具体的生产工艺如下:1. 原料准备:准备所需的硼酸和盐酸,确保原料的纯度和质量。
2. 反应槽:将硼酸和盐酸按一定的比例加入反应槽中,搅拌均匀。
3. 反应:开始反应,反应温度一般控制在60-70℃,反应时间为2-3小时。
反应过程中会产生大量的热量和气体,需要进行循环冷却和排气处理。
4. 浓缩:将反应产生的硼酸盐溶液经过蒸发浓缩,浓缩至一定浓度。
然后将浓缩液以一定的速率加入浓盐酸中,产生三氯化硼气体。
5. 冷却:将三氯化硼气体通过冷却装置冷却,使其转化为三氯化硼固体。
6. 凝固:将冷却后的三氯化硼气体固化成固体颗粒。
固化过程可采用淬湿、滚筒冷却等方式。
7. 干燥:将固化后的三氯化硼颗粒进行干燥,降低其含水量。
干燥过程通常采用旋转干燥器或真空干燥器。
8. 包装:将干燥后的三氯化硼装入合适的包装袋中,进行打包封存。
以上就是三氯化硼的生产工艺的详细介绍,根据具体工艺条件的不同,生产过程中可能还需要进行中间处理步骤和后续处理步骤。
氰化钠生产工艺设计

氰化钠生产工艺设计氰化钠是一种重要的无机化工原料,广泛应用于金属表面镀膜、银镜反射层的制备、制药、冶金等领域。
本文将从原料采购、生产工艺流程、操作条件以及产品质量控制等方面对氰化钠的生产工艺进行设计。
一、原料采购氰化钠的主要原料是氢氧化钠和氢氧化钾。
氢氧化钠优质品是生产氰化钠的关键原料之一,应选用纯碱含量高,杂质含量低的合格产品。
氢氧化钾的选用需考虑纯度、颗粒度等因素,要求纯度在90%以上。
二、生产工艺流程氰化钠的生产工艺可以分为氰氢化反应、加钾熔融、过滤和干燥等步骤。
1.氰氢化反应:在反应釜中加入适量的氢氧化钠溶液,并通过加热使其达到一定温度。
然后将氢氧化钾固体加入反应釜中,控制反应温度在适宜范围内,以促进氰化钠的生成。
反应结束后,升温使反应液沸腾,将反应釜中的氯气彻底去除。
2.加钾熔融:将反应釜中的反应液转移到钾熔融罐中,在加热的条件下使其熔化。
然后搅拌混合,使氰化钠与余下的氢氧化钾反应,生成氰化钠溶液。
3.过滤和干燥:将熔融的氰化钠溶液经过滤器过滤,除去其中的杂质和杂质。
然后将过滤得到的氰化钠溶液进行干燥,得到固态的氰化钠产品。
三、操作条件1.反应温度:氰化钠的生成是在一定温度下进行的,一般考虑到反应速度和产率的影响,反应温度可控制在100-200摄氏度之间。
2.混合速度:在加钾熔融的过程中,搅拌应均匀稳定,避免产生不均匀反应。
混合速度一般应控制在150-300转/分钟。
3.过滤条件:过滤时应选用合适的过滤介质和压力,以确保过滤效果良好,并有效去除杂质。
4.干燥条件:干燥时应掌握适当的温度和时间,以充分除去溶液中的水分,提高产品纯度。
四、产品质量控制对生产得到的氰化钠产品进行质量控制是非常重要的。
其中包括以下几个方面:1.纯度检验:通过抽样取样,使用化学分析方法进行检测,确保产品纯度符合要求。
2.杂质检测:检测氰化钠中的杂质含量,确保产品质量。
3.颗粒度检测:检测产品的颗粒度分布情况,确保产品达到所需的颗粒度要求。
七钼酸铵生产工艺

七钼酸铵生产工艺七钼酸铵(NH4)6Mo7O24)是一种重要的无机化工原料,广泛应用于化肥、染料、电子材料等领域。
下面介绍七钼酸铵的生产工艺。
1. 原料准备七钼酸铵的主要原料包括硝酸铵(NH4NO3)和钼酸铵(NH4)2MoO4)。
首先需要将这两种原料按一定比例准备好。
2. 反应制备将硝酸铵溶解于适量的水中,得到硝酸铵溶液。
同时将钼酸铵溶解于适量的水中,得到钼酸铵溶液。
3. 混合反应将硝酸铵溶液与钼酸铵溶液慢慢混合,同时加热并搅拌。
加热温度一般控制在80-90℃左右,搅拌时间为1-2小时。
在反应过程中,需要保持溶液的pH值稳定在7-8之间,可通过加入碱性物质(如氨水)进行调节。
随着反应的进行,溶液逐渐变为浅黄色。
4. 结晶沉淀在混合反应完成后,将所得的溶液继续加热至沸腾,并保持沸腾状态,持续加热2-3小时。
沸腾过程中会有少量水分蒸发,溶液逐渐浓缩。
当溶液浓度达到一定程度时,开始结晶。
此时关闭加热器,让溶液自然冷却至室温。
5. 过滤与干燥将结晶的七钼酸铵沉淀通过过滤装置进行分离,得到湿沉淀物。
然后将湿沉淀物均匀地分散在干燥器中,通过加热和通风的方式,将湿沉淀物中的水分蒸发干燥,最终得到干燥的七钼酸铵产品。
6. 粉碎与包装将干燥的七钼酸铵产品进行粉碎处理,使其颗粒度均匀。
然后将粉碎后的七钼酸铵产品进行包装,通常采用密封包装,以防止潮湿和氧化。
通过以上工艺步骤,可以生产出高纯度的七钼酸铵产品。
在整个生产过程中,需要注意控制反应温度、pH值和溶液浓度,以及结晶、过滤和干燥等环节的操作条件,以确保产品质量和产量的稳定和高效。
同时,还需要加强安全措施,避免与硝酸铵等化学物品发生反应和产生危险事故。
硼酸锌生产工艺

硼酸锌生产工艺
硼酸锌是一种重要的无机化工产品,广泛用于玻璃陶瓷、电子陶瓷、农药、防腐剂等行业。
以下是硼酸锌的生产工艺介绍,共计700字。
硼酸锌的生产工艺主要包括原料准备、溶液制备、结晶、洗涤和干燥等环节。
1. 原料准备:硼酸锌的主要原料为氧化锌和硼酸。
氧化锌为粉状,硼酸为晶体状。
原料应根据生产需要做好准备。
2. 溶液制备:将一定量的硼酸溶解在适量的水中,形成硼酸溶液。
同时,将氧化锌粉加入一定量的水中,形成氧化锌悬浮液。
两种溶液分别搅拌均匀,保持温度恒定。
3. 结晶:将硼酸溶液和氧化锌悬浮液缓慢混合并搅拌,使二者充分反应。
在搅拌的同时,逐渐加热溶液至65-70摄氏度,保
持一定时间使反应彻底。
随着反应的进行,溶液中产生的硼酸锌逐渐结晶,并逐渐沉积。
4. 洗涤:将反应后的硼酸锌沉淀用冷水洗涤,去除杂质和未反应的物质。
洗涤应反复多次,直到洗涤液中无杂质。
5. 干燥:将洗涤干净的硼酸锌沉淀放入专用干燥器中,进行低温干燥。
干燥温度一般控制在60-70摄氏度,干燥时间根据产
品要求决定。
干燥后的硼酸锌应满足一定的含水量要求。
以上就是硼酸锌的生产工艺介绍。
硼酸锌的生产工艺相对简单,但是每个环节都需要严格控制,以确保产品质量。
同时,在整个生产过程中,需要注意安全生产和环保要求,确保工艺过程的安全性和环境友好。
碱式碳酸锌生产工艺

碱式碳酸锌生产工艺
碱式碳酸锌是一种重要的无机化工产品,广泛应用于电池、橡胶、橡胶带、陶瓷、涂料、塑料等行业。
下面是碱式碳酸锌的生产工艺简介。
碱式碳酸锌的生产工艺主要包括碱式碳酸锌沉淀法和炭酸氢铵法两种。
碱式碳酸锌沉淀法的主要步骤如下:
1. 预处理:将锌盐(如硫酸锌)与水在反应釜中混合,形成锌水溶液。
2. 沉淀反应:向锌水溶液中加入碱性沉淀剂(如氢氧化钠或碳酸钠),控制溶液的pH值,使之适合产生碱式碳酸锌沉淀。
3. 沉淀分离:待溶液中的碱式碳酸锌沉淀充分形成后,通过离心或过滤等方法将沉淀物与溶液分离。
4. 水洗:将分离出的碱式碳酸锌沉淀物进行水洗,去除残留的杂质。
5. 干燥:将水洗后的碱式碳酸锌沉淀物经过脱水和干燥处理,得到成品。
炭酸氢铵法的主要步骤如下:
1. 预处理:将氯化锌与水在反应釜中混合,形成锌水溶液。
2. 中和反应:向锌水溶液中加入炭酸氢铵,使其与锌离子发生反应生成碱式碳酸锌沉淀。
3. 沉淀分离:使沉淀充分形成后,通过离心或过滤等方法将沉
淀物与溶液分离。
4. 水洗:将分离出的碱式碳酸锌沉淀物进行水洗,去除残留的杂质。
5. 干燥:将水洗后的碱式碳酸锌沉淀物经过脱水和干燥处理,得到成品。
以上是碱式碳酸锌的两种常用生产工艺简介,生产过程中需要注意控制反应条件,以确保产品质量的稳定性和合格率。
此外,在生产过程中还需加强环境保护意识,合理处理废水和废气,避免对环境造成污染。
以上是关于碱式碳酸锌生产工艺的简要介绍,希望对您有所帮助。
如需了解更详细的信息,请参考相关专业书籍或咨询相关专业人士。
硫酸生产工艺流程(3篇)

第1篇一、概述硫酸是一种重要的无机化工原料,广泛应用于化肥、农药、冶金、石油、医药、造纸、玻璃、染料等工业部门。
硫酸的生产方法主要有接触法、接触法-转化法、转化法、转化法-转化法等。
本文以接触法为例,详细介绍硫酸的生产工艺流程。
二、原料及设备1. 原料:硫磺、空气、水。
2. 设备:沸腾炉、转化炉、吸收塔、接触室、鼓风机、压缩机、泵、冷却器、加热器、冷凝器、过滤器、分离器、真空泵等。
三、生产工艺流程1. 硫磺燃烧将硫磺送入沸腾炉,在沸腾炉中与空气混合,在高温(800℃-1000℃)下进行燃烧,生成二氧化硫(SO2)。
反应方程式:S + O2 → SO22. 二氧化硫转化将燃烧生成的SO2气体送入转化炉,与水蒸气在催化剂的作用下进行转化反应,生成三氧化硫(SO3)。
反应方程式:2SO2 + O2 → 2SO33. 三氧化硫吸收将转化炉生成的SO3气体送入吸收塔,与水进行反应,生成硫酸。
反应方程式:SO3 + H2O → H2SO44. 硫酸浓缩将吸收塔中生成的硫酸溶液送入接触室,进行浓缩。
浓缩过程中,硫酸溶液与空气混合,加热至沸点,使部分水分蒸发,提高硫酸浓度。
5. 硫酸冷却将浓缩后的硫酸溶液送入冷却器,进行冷却,使其温度降至常温。
6. 硫酸分离将冷却后的硫酸溶液送入分离器,分离出硫酸和未反应的水蒸气。
7. 硫酸储存与输送将分离出的硫酸溶液储存于硫酸储罐中,待使用时通过泵送至用户。
四、生产工艺参数1. 硫磺燃烧温度:800℃-1000℃2. 转化炉温度:450℃-500℃3. 吸收塔温度:50℃-60℃4. 硫酸浓度:98%5. 催化剂活性:95%五、生产工艺特点1. 生产效率高:接触法生产工艺具有生产效率高、设备简单、操作方便等优点。
2. 原料来源广泛:硫磺资源丰富,且价格相对较低。
3. 环保:接触法生产工艺在燃烧过程中,SO2排放量较小,对环境污染相对较小。
4. 产品质量稳定:采用接触法生产工艺生产的硫酸,质量稳定,产品纯度高。
无机化工生产流程详解

无机化工生产流程详解引言无机化工是一门研究无机物质制备和应用的学科,涉及到许多重要的行业和产品,如化肥、玻璃、陶瓷、金属材料等。
无机化工生产过程复杂且多样化,涉及许多工艺和步骤。
本文将详细介绍无机化工生产过程中的一般流程和关键步骤。
原料准备无机化工生产的第一步是原料准备。
不同的生产过程需要不同的原料,如草酸法制备碳酸氢钙,一般需要准备草酸和石灰石作为原料。
原料准备包括原料的选择、储存和预处理。
原料的选择通常基于产品质量的要求和经济考虑。
储存原料需要注意防止受潮、污染和自燃,以保证原料的稳定性和可靠性。
某些情况下,还需要对原料进行预处理,如筛分、干燥等。
反应过程反应是无机化工生产的核心环节。
不同的产品需要不同的反应方式和条件。
反应过程的基本要素包括反应容器、原料投料、控制参数和反应均匀性等。
在有些反应过程中,为了提高反应速率和产率,可能需要添加催化剂或改变反应条件,如温度、压力和PH值等。
在反应过程中,要注意控制反应温度、压力和反应时间,以确保产品的质量和稳定性。
分离和纯化在反应完成后,需要对产物进行分离和纯化,以获取所需的目标产物。
分离和纯化的方法有很多种,如蒸馏、结晶、沉淀、萃取、过滤等。
选择合适的方法要基于产物的性质和要求。
在分离和纯化过程中,还要注意回收和处理废物,以保证环境的安全和可持续发展。
产品包装和储存分离和纯化后的产品需要进行包装和储存,以便于运输和销售。
产品包装要符合国家的标准和法规,并考虑产品的安全性和便捷性。
储存过程中要注意产品的稳定性和防腐措施,以保证产品的质量和有效期。
安全与环保在无机化工生产过程中,安全和环保是非常重要的问题。
涉及到危险化学品和高温高压等因素,容易引发事故和污染。
因此,在生产过程中要严格遵循安全操作规程、配备必要的防护设施,进行安全培训和应急演练。
同时,要建立健全的环保管理体系,控制污染物的排放和处理,减少对环境的影响。
结论无机化工生产流程复杂且多样化,包括原料准备、反应过程、分离和纯化、产品包装和储存等多个环节。
第三章无机化工
工业还原气
3.1.2.1 煤气化的基本化学反应
3.1.2.2
煤气化的分类方法
按制取煤气的热值分类有:
①制取低热值煤气方法,煤气热值低于8374kJ/m3; ②制取中热值煤气方法,煤气热值16747-33494kJ/m3; ③制取高热值煤气方法,煤气热值高于33494kJ/m3. 按气化过程供热方法分类又可分为: ①部分氧化方法,又称自热式气化方法,通过燃烧部分气化用 煤来供热,这种方法目前最普遍;
5-2 鲁奇炉结构示意图 1-煤斗;2-分布器;3-水夹套;4-水斗;5-洗气器
3.气流床连续式气化制水煤气法 条件:一种在常压、高温下以水蒸气和氧气与粉煤反应的气化法。
图3-7 德士古法煤浆气化示意图 1-磨粉机;2-悬浮槽;3-浆液泵; 4-气化炉;5-灰斗;6-冷激器; 7-冷却洗涤塔;8-沉降槽;9-水泵
36
一段转化气体(体积%) CH4 10,CO 10,CO2 10,H2 69, N2 1.
CH4<0.3% (CO+H2)/N2=2.8~3.1
一段转化气不符 合合成氨要求?
合成氨气质要求
①
提高CH4转化率:转化气中 CH4≤ 0.3%,要求T>1000 ℃;但在一段转
化中,目前耐热合金钢工作温度 800~ 900 ℃。(一段转化无法完成)
34
烃类蒸汽转化法:
在催化剂存在条件下,使甲烷等烃类原料在高温下与水蒸气 反应生成 CO和H2
属于强吸热,需供热。
H2/CO=3,CO还可以与H2O变换成H2,适合制纯H2
分两段转化??
35
一段炉转化(管外供热方式)
管内:一段转化(CH4+H2O)
管外:CH4+空气燃烧产生热量
磷酸钠生产工艺

磷酸钠生产工艺
磷酸钠是一种重要的无机化工产品,广泛应用于冶金、玻璃、陶瓷、洗涤剂制造等领域。
以下是磷酸钠的生产工艺简介。
磷酸钠的生产通常采用湿法生产工艺,主要包括磷酸钠溶液的制备、磷酸钠结晶、过滤和干燥等步骤。
首先,制备磷酸钠溶液。
该工艺一般采用磷矿石(如磷灰石、磷酸矿等)作为主要原料,并通过炼焦酸法、硫酸法等方法提取磷酸钠。
首先将磷矿石破碎和磨碎,然后与炼焦酸或硫酸混合,通过反应生成磷酸钠溶液。
该溶液经过澄清、过滤等处理后,得到磷酸钠的溶液。
接下来是磷酸钠结晶。
利用结晶罐进行结晶过程,将磷酸钠溶液加热到一定温度,通过恒温结晶、浓缩结晶等方法使磷酸钠溶液中过饱和度增加,最终形成磷酸钠结晶。
结晶过程中,需要控制温度和浓度,以获得合适的结晶度和结晶纯度。
然后是过滤步骤。
将磷酸钠结晶体与溶液分离,一般采用压滤机进行过滤。
过滤过程中,需要控制过滤速度和过滤效果,以保证分离效果和产品质量。
最后是干燥。
将过滤得到的磷酸钠脱水干燥,以去除水分,提高产品的稳定性和质量。
一般采用干燥机进行脱水干燥,通过加热和排气系统,使磷酸钠在一定的温度和湿度下快速干燥,最终得到磷酸钠的成品。
总结来说,磷酸钠的生产工艺一般包括磷酸钠溶液的制备、磷酸钠结晶、过滤和干燥等步骤。
通过这些步骤,可实现从磷矿石到磷酸钠成品的生产过程。
在生产中,需要控制温度、浓度、过滤速度等参数,以获得合适的产品质量并确保工艺的安全和稳定。
磷酸锌生产工艺

磷酸锌生产工艺
磷酸锌是一种重要的无机化工产品,广泛应用于防腐蚀涂料、防锈剂、陶瓷、橡胶、塑料、油墨等领域。
下面是磷酸锌的生产工艺介绍。
一、原料准备
磷酸锌的主要原料是氧化锌和磷酸。
氧化锌可通过炼锌废水、锌电池废料、锌矿石等多种途径获得;磷酸可通过燧石、磷灰石等磷矿石进行磷酸化反应得到。
二、氧化锌处理
将获得的氧化锌进行研磨,使其粒径均匀细小,增加表面积。
然后将氧化锌与磷酸进行反应,生成磷酸锌。
反应过程需要在一定温度下进行,一般在60-80℃的范围内进行。
反应时间要根据具体情况进行控制,一般为2-3小时。
三、滤液处理
将反应生成的磷酸锌滤出,滤液中除了磷酸锌还有一部分未反应的氧化锌和磷酸。
滤液中的氧化锌可通过再次研磨后,再次与磷酸进行反应,提高产品产量。
滤液中的磷酸可通过酸碱中和、蒸发浓缩等方法进行回收利用。
滤液处理的关键在于减少废品的形成,并将有用的物质回收利用。
四、产品干燥
将滤液过滤后的磷酸锌进行干燥处理,去除多余水分。
常用的干燥方法有喷射干燥、回转干燥等。
干燥的目的是使产品达到一定的水分含量,便于储存和使用。
五、产品包装
干燥后的磷酸锌可以直接包装装袋销售,也可以按照客户要求进行深加工,例如精细分级、表面处理等。
产品包装要注意密封性和防潮性,避免产品受潮和氧化。
以上是磷酸锌的生产工艺介绍,总的来说,磷酸锌的生产过程就是将氧化锌与磷酸进行反应,再经过滤液处理、产品干燥和包装等步骤。
生产工艺的优化和改进可以提高产品质量和产量,降低生产成本,提升企业竞争力。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
空气氮
固氮
Nitrogen
fixation
非生物固氮 生物固氮 人工固氮
其中,人工固氮指通过化学方法,使单质氮气转化为
含氮的化合物。目前工业上最常用、也最经济的是哈伯 法,即氮气(N2)与氢气(H2)在高温高压催化剂(铁)作用 下发生化合反应生成氨(NH3)。
氨的性质和用途
◆ 氨的分子式NH3,分子量17.031,正常沸点 239.65K (-33.5℃,临界温度405.55K(132.4℃),临 界压力11.278 MPa。易溶于水,刺激眼睛和呼吸道, 使人体粘膜迅速脱水,空气中含氨超过5%将使人窒息死 亡。空气中的爆炸范围为15.5~28%。
⑵间歇式制取半水煤气的工作循环及设备
固定床间歇式气化制半水煤气的操作方式为燃烧与 制气分阶段进行,所用设备称煤气发生炉。炉中填满 块状煤或焦炭,首先吹入空气使煤完全燃烧生成CO2并 放出大量的热,使煤层升温,烟道气放空;待煤层温度 达1200℃左右,停止吹风,转吹水蒸气,与高温煤层 反应,生成CO、H2等气体,制成水煤气,送入气柜。 气化吸热使煤层温度下降,当降至950℃时,停止送蒸 汽,重新进行燃烧阶段。如此交替操作,完成制气。
第三章 无机化工产品 典型生产工艺
1
合成氨
2
硫酸
3
纯碱
4
烧碱与氯气
1 合成氨 Synthesis of Ammonia
1
1.1 概 述
2
1.2 原料气的制取
3
1.3 原料气的净化
4
1.4 氨的合成
5 1.5 合成氨发展趋势
1.1 概述 (Preface)
空气中含有大量的游离氮(N2:78.03%),但是只有 极少数农作物(豆科)能够直接吸收空气中的游离氮,大 多数农作物只能吸收化合态氮来供给生长所需养分。固 氮是化学化工研究中既古老又前沿的课题。
⑵间歇式制取半水煤气的工作循环及设备
吹风→ 蒸汽吹净 → 一次上吹制气→下吹制气
(空气↑) (蒸汽↑)
⑵压力 降低压力有利于提高CO和H2的平衡浓 度,但加压有利于提高反应速率并减小反应体 积,目前气化一般采用2.5-3.2MPa,其CH4含量 较常压高些。
⑶水蒸气和氧气的比 氧的作用是与煤燃烧放 热供给水蒸气与煤的气化反应,H2O/O2比值对 温度和煤气组成有影响,其比值要依据采用煤 气化生产方法而定。
CO2 10.8 1.6 0.4 0.2
CO 16.9
N2 a=CO:(CO+CO2)
72.3
61.0
31.9 66.5
95.2
34.1 65.5
98.8
34.4 65.4
99.4
② 以水蒸气为气化剂
C+H2O
CO+H2
C+2H2O(g) CO2+2H2
CO+H2O(g) CO2+H2
C+2H2
CH4
造气
用煤、原油、或天然气作原料, 制备含氮、氢气的原料气。
净化
将原料气中的杂质如CO、 CO2、S等脱除到ppm级(10-6)。
压缩和 合成
净化后的合成气原料气必须经过 压缩到15-30MPa、450℃左右
原油或天然气
煤
空气
造气
蒸汽
氨
CO(g) + H2O(g) = CO2(g) + H2(g)
除尘 合成
◆ 氨是生产尿素、硝酸铵等化学肥料的主要原料,使农 业生产产量大大提高,为人类社会作出巨大贡献。
◆ 氨还是生产染料、炸药、医药、有机合成、塑料、合 成纤维、石油化工等的重要原料。
◆ 首例合成氨厂是1912年在德国建立的30t/d合成氨厂, 目前合成氨厂的规模已达到1000~1500t/d。
合成气的基本过程
脱硫 压缩
CO变换 脱CO2
脱除少量CO与CO2
合成氨的基本过程
焦炭或煤为原料合成氨
天然气为原料合成氨
1.2 煤为原料制合成气
空气煤气 :以空气(实际是空气中的氧气)作气 化剂空气,气体中可燃成份主要为一氧化碳,一般 是高炉生产中的副产物。 水煤气 :水煤气是由水蒸汽和高温碳反应而获得 的。所得煤气中 CO 和 H2 均较高。 混合煤气 :混合煤气综合了空气煤气和水煤气的 特点,以水蒸汽和空气的混合物鼓入发生炉中,制 得比空气煤气热值高,比水煤气热值低的混合发生 炉煤气。
一、化学反应及ቤተ መጻሕፍቲ ባይዱ艺条件
1 化学反应
① 以空气为气化剂
C+O2 = CO2 C+1/2O2 = CO C+CO2 2CO CO+1/2O2 = CO2
∆H0298 KJ/mol -293.777 -110.595 172.284 -283.183
总压0.1MPa时空气煤气的平衡组成,体积%
温度,℃ 650 800 900 1000
温度一定、压力升高时, H2及CO含量降低; CO2 CH4等增加
煤气化生产方法及主要设备
⑴生产方法分类
煤气化过程需要吸热和高温,工业上采用燃烧 煤来实现。气化过程按操作方式分为:间歇式 和连续式,前者的工艺较后者落后,现正在被 淘汰。现一般按采用的反应器类型分为:固定 床(移动床)、流化床、气流床和熔融床。前 三种以被工业生产采用,而熔融床处于中试阶 段。
⑴温度 由上述热力学和动力学分析可知,温 度必须在900℃以上才有满意的气化速度,且 H2、CO含量较高,一般操作温度在1100℃以上 。近年来新工艺采用1500-1600℃进行气化, 使生产强度大大提高。
工艺条件(低压、高温)
由图可知:压力一 定、温度升高时, H2及CO含量增加; CO2及CH4等减小。
∆H0298 KJ/mol 131.390
90.196
-41.194
-74.898
合成氨工业中不仅要求合成气中H2 和CO含量高还要求(CO+H2)/N2=3.13.2(mol),所以需要用适量空气和 水蒸气为气化剂,所得气体为半水煤
气。
煤气化的化学反应速率
固体燃料中的碳和汽化剂在煤气发生炉中 所进行的反应属于气固相系统的多相反应。其 反应速度的大小不仅与碳和汽化剂的化学反应 速度有关,同时还受汽化剂向碳的表面扩散速 度的影响。
①碳和氧的反应
实践证明: Ⅰ、在温度高于1000℃时,燃烧产物主要 是CO、在500℃以下时主要是CO2, Ⅱ、温度低于775℃ ,属动力学控制; Ⅲ、温度高于900℃ ,扩散控制加剧。
②碳和水蒸气的反应
实践证明: Ⅰt=400℃-1100℃ ,属动力学控制; Ⅱt大于1100℃ ,属扩散控制。
煤气化的反应条件
