第六章极端条件下的合成化学
极端环境下的有机化学合成研究

极端环境下的有机化学合成研究在极端环境下进行有机化学合成研究是对化学界的一个重要挑战。
极端环境可以包括高温高压、低温低压、辐射辐射、酸碱溶液、氧化还原条件等。
这些极端环境对有机物分子的稳定性和反应活性造成了巨大的影响,同时也为有机合成提供了新的可能性。
在本文中,我们将探讨在极端环境下进行有机化学合成研究的意义、方法和应用。
极端环境下的有机化学合成研究对于解决一些传统合成方法无法解决的问题具有重要意义。
在高温高压下,一些热力学上不稳定的中间体或过渡态可以形成,从而推动反应向有利方向发展。
这种反应条件可以加速反应速率,提高反应收率。
在低温低压下,有机物分子的反应活性往往会降低,但反应的选择性会增加。
通过调节反应条件,可以控制反应产物的构型和立体选择性。
在极端环境下进行有机化学合成研究的方法有很多种。
其中一种常用的方法是利用强化学反应器,如高压釜和低温冷冻反应器。
这些反应器可以承受高温高压或低温低压条件,并提供适当的反应环境。
另一种方法是利用催化剂,如过渡金属催化剂和酶催化剂。
这些催化剂可以在极端反应条件下提高反应速率和选择性,从而实现特定的有机合成。
极端环境下的有机化学合成研究在许多领域有着广泛的应用。
例如,高温高压条件下的有机合成可以用于制备高分子材料,如塑料和橡胶。
低温低压条件下的有机合成可以用于制备医药中间体,如抗生素和化学药品。
辐射条件下的有机合成可以用于制备特殊的有机小分子,如有机太阳能电池。
极端环境下的有机化学合成研究还具有许多挑战和难点。
一方面,极端环境下的反应条件往往会引起机械设备的磨损和腐蚀。
因此,如何选择和设计适用于极端反应条件的反应器和催化剂成为一个关键问题。
另一方面,极端环境下的有机反应通常需要高能量输入,这对环境保护和能源消耗提出了新的要求。
因此,如何优化反应条件,提高能源利用效率,减少废物排放成为一个重要课题。
综上所述,极端环境下的有机化学合成研究是一项具有重要意义和挑战的研究领域。
第六章低温固相合成

速度极快,无法成为整个固相反应的决速步。再低热固相
化学反应条件下,化学反应也可能是速率的控制步。这一 机理也通过实验得到了证实。
20
3、固相合成方法的适用范围
1、合成原子簇化合物 2、合成新的多酸化合物 固 相 合 成 法 使 用 范 围
3、合成新的配合物
4、 合成固配化合物 5、 合成配合物的几何异构体 6、合成反应中间体 7、 合成非线性光学材料
7
低温固相合成发展
温固相反应那样引起足够的重视,更未能在合成化学领域 中得到广泛应用。然而研究低温固相反应并开发其合成应 用的价值的意义是不言而喻的。1993年Mallouk教授在
《science》上发表评述:“传统固相化学反应合成所得的
是热力学稳定的产物,而那些介稳中间物或动力学控制的
化合物往往只能在较低温度下存在,组装。例如,将Co(bpy) Cl2
和phen· H2O以1:1或1:2摩尔比混合研磨后分别获得了Co(bpy)
(Phen)Cl2和Co(bpy) (Phen)2Cl2;将Co(Phen)2Cl2和bpy按1:2摩
阴离子[Mo13O40]4-,且 都具有Keggin型结构,由中心
25
固相合成方法的适用范围
26
固相合成方法的适用范围
27
固相合成方法的适用范围 4. 合成固配化合物 固相化学反应与液相反应相比,尽管绝大多数得到相同的 产物,但也有很多例外。即虽然使用同样摩尔比的反应物, 但产物却不同,其原因当然是两种情况下反应的微环境的差 异造成的。 低热固相配位化学反应中生成的有些配合物只能稳定地存
29
固相合成方法的适用范围
溶液中无法生成的嵌入化合物。如 Mn(OAc)2· 4H2O 的晶体为层
现代无机合成化学-电解合成

熔盐在无机合成中的应用
• 合成新材料; • 非金属元素的制取; • 氟化物的合成; • 非常规价态化合物的合成;
熔盐在冶金中的应用
• 在电解过程中作为电解质; • 在热还原过程中作为助溶剂; • 各种熔盐制备与处理工艺。
熔盐在能源领域及太阳能领域中 的应用
• 用于金属铀、钍、钚及其它锕系元素的制备;
(可能)由于表面吸附抑制晶核长大而促进新晶核生成;
• 金属离子的配位作用 —— 添加配合物有助于改善产物
沉积状态。
电解装置
1. 阳极
电解提纯:阳极为目标产物的粗制品; 电解提取:使用不溶性阳极。
2. 阴极:
1. 能够高效回收所析出的金属; 2. 面积大于阳极(10 ~ 20 %);
3. 隔膜:用于分隔阳极与阴极。
阳极反应获得目标产物。
具有极强氧化性的物质 —— O3,OF2,等等;
• 应用 普通方法难于合成的高价态化合物 —— 三价Ag,Cu,等等;
特殊高价元素的化合物 —— 过二硫酸,过二硫酸盐,H2O2, 等等。
• 注:所得产物均具有强氧化性,反应活性高且不稳定,应
注意选择电解设备、材质和反应条件。
电还原合成
E槽=E可逆 + ∆E不可逆 + IR1 + IR2
6.1 水溶液中的电解
• 金属电沉积:是指在电场作
用下,金属从电解质中以晶
体形式析出的过程,又称电 结晶。
电解精炼
电镀
电沉积 电提取
要求沉积金属与基体结合牢 固,结构致密,厚度均匀
反应目的
• 获得不易购买的特殊金属; • 比市售品纯度更高的金属; • 粉状或其它特殊形状和性能的金属; • 由废料中回收金属。
精细有机合成化学以及工艺学 第六章 硝化以及亚硝化

15
6.3.6硝化副反应 (1)主要的硝化副反应:氧化、去烃基、置换、 脱羧、开环、聚合等。其中氧化影响最大,生成 硝基酚。 (2)烷基苯硝化时,硝化液颜色发黑变暗,说明 硝酸用量不足或硝化温度过高。 因 为 形 成 了 络 合 物 (C6H5CH3· 2ONOSO3H· 2SO4)。 3H 破坏方法:45~55℃时补加HNO3或混酸 (3)大多数副反应,与体系中存在的氮的氧化物 有关。
-8
1.210
-8
10
结论:苯环上有给电子基,硝化反应速度快,产物 主要是邻、对位 苯环上有吸电子基,硝化速度减慢,产物主要 是间位。 2.芳烃硝化异构产物 带有吸电子的取代芳烃硝化邻位异构体 的生成量比对位异构体多。原因是硝基易同 邻位取代基中带负电荷的原子形成络合物。
CHO 19 72 9 1.3 COOH 18.5 80.5 2.2 CN 17.1 80.7 1 NO 2 9 90 8.2 40.8 NO 2 51 OCH 3
F . N . A. D.V .S . 1 F . N . A. D.V .S . F . N . A. 100 % 1 D.V .S .
22
6.4.2 混算配制 配酸工艺:水、硫酸、硝酸如何混合? 先将浓硫酸先缓慢、后渐快加入到水中, 在40度以下先慢后快加入硝酸。
23
6.4.3硝化操作
(4)非均相混酸硝化
被硝化物和硝化产物在反应温度下都呈液态,且 难溶于混酸时,常采用非均相的混酸硝化。这时 需剧烈搅拌,使有机相充分地分散到酸相中以完 成硝化反应。
(5)有机溶剂中硝化
可避免大量使用硫酸作溶剂。 (6)气相硝化 NO2与苯于80~190℃通过分子筛处理便转化为 硝基苯。
5
6.2硝化理论解释
苛刻条件下合成与制备技术 专题 1.

苛刻条件下合成与制备技术随着社会高科技的迅猛发展,对化合物和材料提出了各种各样的要求,也越来越要求化学家能够合成更多的具有新型结构和新型功能的化合物和材料。
在现代合成中,愈来愈广泛地应用极端条件下的合成方法与技术来实现通常条件下无法进行的合成, 并在这些极端条件下开拓多种多样的一般条件下无法得到的新化合物、新物相与物态。
1.高温合成高温合成技术是化合物和材料合成的一个重要手段。
一般通常的温度都在1000℃以上。
如高熔点金属粉末的烧结、难熔化合物的熔化和再结晶、陶瓷体的烧成等都需要很高的温度。
在实验室中,主要是利用马弗炉来获得高温,根据加热体的不同,可以获得从1000到3000℃的高温,甚至更高。
炉内气氛可以是空气气氛,也可以是其它气氛,炉体可以是箱式,也可以是管式等。
测量高温通常使用热电偶高温计,一般可在室温到2000 ℃之间应用,某些情况下甚至可达3000 ℃。
在更高的温度下可用光学高温计,它的测量范围是700~6000 ℃。
光学高温计只能测量高温,低温段则不准确。
图1.1给出了实验室常见的高温炉和管式炉的结构示意图。
高温下常见的反应是固相反应,它不同于溶液中的反应,他们在常温常压下很难进行。
例如,从热力学角度讲,MgO(s)和Al 2O 3(s)反应生成尖晶石MgAl 2O 4(s)的反应完全可以自发进行。
然而,在实际上,在1200 ℃以下反应几乎不能进行,在1500 ℃时反应也需数天才能完成。
原因有两点:第一,反应的第一阶段,即在反应物晶粒界面上或与界面邻近的晶格中生成MgAl 2O 4晶核,由于产物晶核与反应物结构不同,因而产物晶核的生成很困难;第二,进一步实现在晶核上的晶体生长也有相当的难度,这主要是固相间离子的扩散速率非常慢的缘故。
高温下有利于晶核生成和离子扩散,所以能加速反应。
为了降低固相反应的温度,使反应能在比较温和的条件下进行,有一些方法可以降低固相反应的温度,如将反应物充分破碎和研磨,或通过各种化学途径制备成粒度细、比表面积大、表面具有活性的反应物原料,然后通过加压成片,甚至热压成型使反应物颗粒充分均匀接触;或通过化学方法使反应物组分事先共沉淀;或通过化学反应制成化合物前驱物等。
无机合成简明教程复习笔记(考研+期末)

无机合成简明教程复习笔记一、第一章●无机合成十大热点/前沿领域1.特种结构无机材料的制备2.软化学合成●硬化学:在超高温、超高压、强辐射、无重力、仿地心、仿宇宙等条件下探索新物质合成●软化学:采取迂回步骤,在较温和条件下实现化学反应过程,以制备相关材料的化学领域●方法:前驱体法、溶胶-凝胶法、溶剂热合成法、插入反应、离子交换过程、熔体(助溶剂)法、酶促合成骨骼和人齿反应、拓扑化学过程及一些电化学过程●特点●不需用高纯金属作原料●制成的合金是具有一定颗粒度的粉末,在使用时无需碾碎●产品本身具有高活性●产品具有良好的表面性质和优良的吸放氢性能●合成方法简单●有可能降低成本●为废旧储氢合金的回收再生开辟了新途径3.极端条件下合成4.杂化材料的制备5.特殊聚集态材料合成6.特种功能材料的分子设计●概念:其指开展特定结构无机化合物或功能无机材料的分子设计、裁剪与分子工程学的研究●步骤:以特定的功能为导向➡️在分子水平上实现结构设计和构建➡️研究分子构建的形成和组装规律➡️对特定性能的材料进行定向合成7.仿生合成●概念:其指在分子水平上模拟生物的功能,将生物的功能原理用于化学,借以改善现有的和创造崭新的化学原理和工艺科学●仿生膜●选择性通透作用●低能耗、低成本和单极效率高●适合热敏物质分离●应用广泛、装置简单、操作方便、不污染环境8.纳米粉体材料制备●化学制备方法●水热-溶剂热法●热分解法●微乳液法●高温燃烧合成法●模板合成法●电解法●化学沉淀法●化学还原法●溶胶-凝胶法●避免高温引起相分离9.组合化学●其是一门将化学合成、组合理论、计算机辅助设计及机器人结合为一体的技术●基本思想和主要过程●设想和定义●选择相关元素●构建化合物库●并行处理技术●加工过程●高通量分析●将新材料及合成与分析数据送交用户10.绿色合成●方法和实例●热化学循环分解水●水热-溶剂热合成●超临界二氧化碳和成●绿色电解合成●低热固相合成●固相合成四个阶段●扩散●反应●成核●生长●五个特点●具有潜伏期●无化学平衡●拓扑化学控制原理●分步反应●嵌入反应●定义:指在制造和应用化学产品时有效利用原料(最好可再生),消除废物和避免使用有毒的、危险的试剂与溶剂●核心和主要特点(原子经济反应)●无毒无害原料,可再生资源●环境友好产品,回归自然,废物回收利用●无毒无害催化剂●无毒无害溶剂二、第二章●Ellingham 图1.吉布斯-亥姆霍兹方程2.如何理解:设(x,y)( x,y分别为两种物质),位于金属氧化物线段之下的温度区间,x可用于还原金属氧化物,而本身被还原为y3.应用●古代制铜器●金属锌制备●耦合反应1.概念:原来不能单独自发进行的反应A,在反应B的帮助下合并,合并在一起的总反应可以进行,这种情况称之为耦合反应2.应用实例●单质磷的制备●四氯化钛的制备●氧化法制备硫酸铜●泡佩克斯图1.概念:它是相关电对的电极材料-参加反应各物种浓度-温度-溶液酸度图●电极反应类型●既有氢离子或氢氧根离子参加,又有电子参加,这时的泡佩克斯图为一直线,斜率为(-m/n)*0.059,截距为E池●电极反应只有电子得失,没有氢离子或氢氧根离子参加,其图形为平行于横坐标的直线●电极反应有氢离子或氢氧根离子参加,但没有电子得失,其图形为平行于纵坐标的直线2.性质●直线上方为氧化态的稳定区,下方为还原态的稳定区●直线左边是物种离子的稳定区,右边是沉淀的稳定区3.应用●判断氧化还原反应进行的方向和顺序●对角线规律●两条直线间的距离越大,E池越大,➡️G越负,则反应自发进行的趋势越大●对同时存在的几个反应,氧化还原反应进行的顺序可按直线之间距离的大小排序(从大到小)●确定水的稳定区●如图,凡是泡佩克斯图落在j-k之间的氧化剂或还原剂都不会与水反应●可判断物种在水中存在的区域,或者提供制备的条件●湿法冶金中的应用●在电化学中的应用●热力学相图1.一致熔融化合物2.不一致熔融化合物三、第三章●低温合成1.物态●物质的第四态:等离子态,升高温度(数百万度)●物质的第五态:波色-爱因斯坦凝聚(超导态和超流态),温度低至临界温度2.低温温区划分●普冷区:环境温度到120k●深冷区:120k到绝对零度●普冷与低温的分界线:123k3.低温获得●恒温低温浴●制冷产生低温P78●低温恒温器●储存液化气体装置●高压气体钢瓶●气体钢瓶的颜色●气体钢瓶的安全使用●原因:钢瓶内部填充的气体压力很大,并且有的气体具有可燃性和助燃性,故钢瓶具有一定的易燃易爆性●注意点●气瓶必须连接压力调节器,经降压后,再流出使用●安装调节器,配管一定要用合适的,安装后试接口,不漏气方可使用●保持清洁,防污秽侵入,防漏气●小心使用,不可过度用力●易燃气体钢瓶应装单向阀门,防止回火●避免和电器电线接触,以免产生电弧使气体受热发生危险●瓶内气体不可用尽,即压力表指压不可为0,否则可能混入空气,重装气体时会有危险●气体附近必须有灭火器➡️,且工作场所通风良好4.低温的测量●蒸气压温度计●低温热电偶●低温热电阻温度计5.应用●稀有气体合成●KrF2的低温放电合成● XeO4的低温水解合成●在高氙酸盐中缓慢滴入零下五摄氏度的浓硫酸,生成四氧化氙气体●真空升华得纯品,储存于零下78摄氏度的冷凝容器中●XeF2的低温光化学合成P84●RnF2的光化学合成●金属,非金属同液氨的反应●碱金属及其化合物同液氨的反应●U型汞鼓泡管主要作为液氨蒸发的出口,并在所有的液氨蒸发后,阻止气体进入杜瓦瓶●碱土金属同液氨反应●某些化合物在液氨中的反应●非金属同液氨的反应●液氨中配合物的生成●低温下挥发性化合物的合成●二氧化三碳的合成●氯化氰的合成●磷化氢的合成●实验结束时不断的使氢气通过烧瓶,同时使烧瓶中的物质冷却,直至磷完全凝固。
有机合成化学:第六章 缩合反应
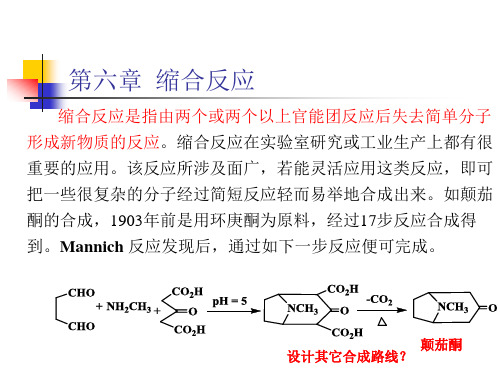
第六章 缩合反应
上例是由于选择不同的起始原料,而选择不同的合成路线,使 产品成本大大降低。如果没有很好的路线选择时,可以通过优化 反应条件,提高产物的收率,降低成本。从产品收率上讲,能提 高1-5%。我们可能认为没什么意义,可对企业讲,产品成本会降 低2-8%左右。如果一个产品产值上亿时,可估算一下其价值了。 所以,一个化工产品刚上市时价格较高,随着生产时间延长,价 格逐渐降低,很大可能是由于生产工艺和生产条件的改变所致。
-CO2
CH3CH CH2CO2H
H3C
O O O
60~76%
CH3NO2 + H3CCH
C H
CO2C2H5
NaOC2H5 CH3CH CH2CO2C2H5
55%
CH2NO2
第六章 缩合反应 CH3
CN
PhCH CO2C2H5 + H2C
C H
CN
KOH 83%
CN
PhC CH2CH2CN CO2C2H5
LDA
H3C
CH3
第六章 缩合反应
羰基化合物烷基化最大负反应是O-烷基化产物。如:
副产物
第六章 缩合反应
LDA CH3(CH2)3CO2CH3 BrCH2CH
CH2
CH3CH2CH2CH CO2CH3 CH2CH CH2
LDA
CH2CH3
C2H5Br CH3CH2Байду номын сангаас CO2CH3
可以分步引入
90%
5. Knoevenagel反应:
这类反应的特点是一个亚甲基上连接两个吸电子基团,使
得其氢活性明显提高,反应较易进行。一般使用弱碱 (有机胺)
第六章 低温固相合成1

传统的固相化学
固体结构和固相化学反应
低热固相化学反应机理 低热固相化学反应的特有规律
低热固相反应在合成化学中的应用
低热固相化学反应在生产中的应用
6.1 传统的固相化学
1、固相化学的确立
1912年,年轻的Hedvall在Berichte杂志上发表了“关 于林曼绿”(CoO和ZnO的粉末固体反应)为题的论文 固相化学反应研究固体物质制备、结构、性质及应用 固相化学反应需要高温的思想 推动技术革命的新型功能材料
固相反应实例
1.
PbO的制备: 溶液反应法: Pb2+盐 + NaOH → Pb(OH)2沉淀 → PbO
2.
传统(高温)固相反应法:
Pb + O2 → PbO
3.
低温固相反应法: Pb2+盐微粉 + NaOH微粉 → PbO
CuCl2· 2H2O + 2AP(a-氨基嘧啶 ) → Cu(AP)2Cl2· 2H2O
2、固体的结构与反应性关系:零维>一维>二维>三维 三维固体:具有致密结构,所有原子都被强化学键所 束缚,晶格组分很难移动,外界物质也难于扩散,反 应性最弱。如金刚石在一定温度范围内几乎对所有试 剂都稳定
低维固体:即二维或一维固体,层间或链间靠分子间 力相连,晶格容易变形,使一些分子容易嵌入层间或 链间,反应性比三维固体强得多。如二维石墨,室温 到450C范围内易发生嵌入反应,生成层状嵌入化合物, 一维聚乙炔,易被掺杂而具有良好的导电性
低温固相反应制备无机纳米材料
直接反应法 氧化法 添加无机盐法 添加表面活性剂法
无机合成化学考点总结

1无机合成化学的内容:1)无机合成化学与反应规律问题2)实验技术与方法问题3)分离问题4)机构鉴定与问题2无机材料合成的思想方法:1开拓新的合成方法2元素的掺杂和置换3突破原有体系4体系杂化5学科交叉3无机合成化学的热点领域:1极端条件合成(模拟宇宙空间条件下高纯度晶体的合成);2软化学合成和绿色化学合成(温和条件下的合成);3特种结构无机材料的制备(特殊聚集态,凝聚态,形貌和尺寸控制);4功能材料的制备(材料的多相复合);5特殊材料集态材料的制备(溶胶—凝胶路线)6特种功能材料的分子设计(新化合物的制备和发现);7生物合成(生物体对血红素的合成)8米粉体材料的制备(纳米级半导体材料Cds)4其他的工业制备N2(低温下的分级冷凝)O2(深度冷凝法)Cl20(电解)CO2(热分解)NH3(化学合成)5气体除杂净化的方法:a化学除杂法-最常用的方法,分离提纯反应必须具有特效性,灵敏性,高选择性b气体的分级分离净化(不能用化学除杂的)—该法是基于气体的沸点,蒸汽压等性能不同对气体进行提纯的一种方法:1)低温下的分级冷凝2)低温下的分级蒸发3)应用分馏柱进行分级蒸发4)气体色谱法c吸附分离和净化—性质极其相似而又缺乏特征化学分离方法的混合气体的分离6气体除杂净化的主要对象:a出去液雾和固体颗粒:b干燥1)低温冷阱2)干燥剂c除氧:通常先初除后细除。
初除方法1)让气体通过铜屑,氨水和氨化铵饱和溶液,2)让气体通过灼热的300——400度的铜3)让气体通过焦性没食子酸溶液4)让气体通过蒽醒- -磺酸钠溶液。
细除方法—最好让气体通过活性铜。
d:除氨:各种碱金属,碱土金属及其合金可直接用作N2的吸收剂,Ca和K,Na.Ba或Si的合金在比较低得温度下就能吸收N2,在高温下用钛粉除N2也是有效的方法。
7、溶剂的主要类型:1、按化学基团—水系(水醇,醛酮)、氨系(氨分子、阱),质子溶剂:包括液氨、液态氟化氢、硫酸、“超酸”溶剂);2:按亲质子性—酸性(卤化氢、发烟硫酸),碱性,两性(水、醇),质子惰性—苯、酚、乙基、环己烷。
05第五次课-特殊材料合成化学

熔盐合成的材料举例
材料:K2Nb8O21 形貌:纳米棒 熔盐:NaCl-KCl
J Am Chem Soc, 2007, 129:15444.
材料:α/β-MnO2 形貌:纳米线 熔盐:LiNO3-NaNO3-KNO3
J Phys Chem C, 2009, 113:8560.
27
常用的熔盐种类
28
(d) (c)
(b) (a)
29
70
(400) (208) (316)
Intensity (a.u.)
20
(004) (112)
BaMoO4的熔盐合成
30
在不同温度下处理前躯体+熔盐的 SEM与XRD图谱
确定出700 oC为最佳合成温度
(202) (114) (211) (200)
2 Theta (Degree)
材料、 稀土发光材料、阴极发射材料和超硬材料、超 低损耗的氟化物玻璃光纤
2.非金属元素F2,B和Si等的制取 如:工业生产氟
气就是通过中温(80~110℃)电解KF· 2HF(低共熔点68.3℃)或 高温 (250~260℃)电解KF· HF(低共熔点229.5℃)来实现 机化合物如CH3· (CH2)n· S02Cl进行电化学氟化反应,而生成所 需氟化物CF3(CF2)n· S02F产品.
第一类为爆轰产物法,它是在瞬时的高温高
压下伴随化学反应,生成物料不同的另一种 物质。 第二类为冲击波瞬态高压高温法,它是利用 冲击压力产生新的结晶结构。
13
高压合成技术的应用
日本油脂株式会社的荒木正任等人,使用冲击波瞬
态高压高温法,在密封容器内装入石墨型氮化硼和 铁粉,成功合成了纤锌矿型(立方)氮化硼。 利用爆炸等方法产生的冲击波,在物质中引起瞬间 的高压高温来合成新材料的动态高压合成法,也称 为冲击波合成法或爆炸合成法。至今,利用这种方 法合成人造金刚石,还有一些其他的新相、新化合 物。
第六章低温固相合成1.

分子固体:零维固体,比所有延伸固体中的作用都弱, 分子可移动性强,物理性质上表现为低熔点和低硬度, 具有最强的反应性
固体结构与固相化学反应
化学键作用仅 在分子范围内 有效
分子固体 ——零维晶体 —— 反应活性最强
固体 延伸固体 化学键作用贯 穿整个晶格 一维固体 低维固体 二维固体 三维固体 —— 稳定性最强 反 应 活 性
1. 2.
低温固相反应:原料粉末研磨混合,5 min完成反应; 液相反应:只能得到Cu(AP)Cl2产物。
固相反应的优势
不使用溶剂
具有高选择性,高产率 简化工艺流程 缩短反应时间
节约能源 降低成本 减少污染
低温固相反应与新材料的发现
传统固相化学反应合成得到的是热力学稳定的产物 低温固相反应可能合成介稳中间物或动力学控制的 化合物(在高温时分解或重组成热力学稳定产物)
2、固相化学对材料科学的贡献
20世纪50年代高纯单晶半导体的固相合成-电子工 业 硅铝酸盐分子筛为基础的催化剂-石油化工
低温固相合成发展
1993年Mallouk教授在《science》上发表评述:“传统固 相化学反应合成所得的是热力学稳定的产物,而那些介稳 中间物或动力学控制的化合物往往只能在较低温度下存在, 它们在高温时分解或重组成热力学稳定的产物。为了得到 介稳固态相反应产物,扩大材料都选择范围,有必要降低 固相反应温度。
低温固相合成发展
我国的一些科学工作者在低温固相合成方面 也作来许多开创性的工作。例如, 1988 年,忻 新泉等开始报道“固态配位化学反应研究”系 列,探讨了室温或近室温条件下固 -固态化学反 应。 1990 年开始合成新的原子簇化合物,并测 定了数以百计的晶体结构。 其中有代表性的[M o8Cu12S32]4-含有20个金属原子,是最大的含
第六章配位化合物的合成化学-PPT文档资料

对Werner型配合物来说,最常用的方法是结晶,其 中包括:
(a)浓缩、蒸发除去溶剂,用冰盐浴等冷却,使产物析出。
(b)缓慢地加入与溶剂有互相混溶,但又不能溶解目标配合物 的溶剂使产物析出。 (c)若目标配合物是配阳离子,可加入能与它生成难溶盐的合 适阴离子将它分离出来,而要制备配阳离子时,可以加入一 种合适的阳离子使其分离出来。当一次结晶不能制得纯目标 化合物时,还需多次结晶,使其纯化。
1. 配体取代
(1)溶剂的作用
即在一定条件下,新配体可以置换 原配合物中的一个,几个或全部配体, 并得到新配合物。选择溶剂及控制反 应条件是提高合成反应产率,减少副 产物的关键。
在配合物合成中,提供中心原子的化合物一般是无机盐(如 含氧酸盐,卤化物等),氧化物或氢氧化物。对溶剂的要求 是反应物在其中能较好的溶解,但碱性要小于目标化合物中 配体的碱性,这样才能保证产物在其中不发生分解(水解、 醇解等),同时还要有利于产物分离。
(1)水溶液中的直接加成 水是最常用,最主要的溶剂之一。水中的直接 加成实际上是用适当的配体去取代水合配离子中 的水分子。合成时溶液的酸度对反应产率和产物 分离有很大影响,控制PH是某些配合物合成的关 键。
很多配体都是有机弱酸,只有将其变为酸根,即 lewis碱后方可配位。因此,合成配合物时需加入些 碱使其转型。例如,由CrCl3和乙酰丙酮(acac)水溶 液合成[Cr(C5H7O2) 3]时,可在反应体系中加入尿素, 通过加热使尿素水解成氨来控制溶液的pH,使产物 很快结晶出来: CO(NH2)+H2O=2NH3+CO2 CrCl3+3C5H8O2+3NH3=[Cr(C5H7O2)3]+3NH4C 1
上述反应就是直接在无水乙醚和乙腈中进行的。
‘无机化学发展前沿’

无机化学发展前沿摘要: 无机化学是化学学科里其它各分支学科的基础学科,在近年来取得较突出的进展,主要表现在固体材料化学、配位化学等方面。
未来无机化学的发展特点是各学科交叉纵横相互渗透,用以解决工业生产与人民生活的实际问题。
当前无机化学的发展趋向主要是新型的无机化合物的合成和应用,以及新的研究领域的开辟和建立。
因此21世纪理论与计算方法的运用将大大加强理论和实验更加紧密的结合。
同时各学科间的深入发展和学科间的相互渗透,形成许多学科的新的研究领域。
例如,生物无机化学就是无机化学与生物学结合的边缘学科;固体无机化学是十分活跃的新兴学科;作为边沿学科的配位化学日益与其它相关学科相互渗透与交叉。
一、无机合成与制备化学研究进展无机合成与制备在固体化学和材料化学研究中占有重要的地位, 是化学和材料科学的基础学科。
发展现代无机合成与制备化学, 不断地推出新的合成反应和路线或改进和绿化现有的陈旧合成方法, 不断地创造与开发新的物种, 将为研究材料结构、性能(或功能) 与反应间的关系、揭示新规律与原理提供基础。
近年来无机合成与制备化学研究的新进展主要表现为以下几个方面:(一)极端条件合成在现代合成中愈来愈广泛地应用极端条件下的合成方法与技术来实现通常条件下无法进行的合成, 并在这些极端条件下开拓多种多样的一般条件下无法得到的新化合物、新物相与物态。
超临界流体反应之一的超临界水热合成就是无机合成化学的一个重要分支。
(二)软化学合成与极端条件下的合成化学相对应的是在温和条件下功能无机材料的合成与晶化, 即温和条件下的合成或软化学合成。
由于苛刻条件对实验设备的依赖与技术上的不易控制性, 减弱了材料合成的定向程度。
而温和条件下的合成化学——即“软化学合成”, 正是具有对实验设备要求简单和化学上的易控性和可操作性特点, 因而在无机材料合成化学的研究领域中占有一席之地。
(三)缺陷与价态控制缺陷与特定价态的控制是固体化学和固体物理重要的研究对象, 也是决定和优化材料性能的主要因素。
课件:第六章 高压合成

如果起始石墨材料添加金属催化剂,则在较低的压 力(5~6)GPa和温度1300~2000K条件下,就可以实现 由石墨到金刚石的转变。这是静高压高温催化剂合成法 成功的一个典型例子。
1957年,Wentorf Jr等人将类似于石墨结构的六角氮 化硼作起始材料,添加金属催化剂(Mg等)在6.2GPa和 1650K的高压高温条件下,合成出与金刚石具有等结构 的立方氮化硼。它是一种由静高压高温催化剂合成法合
高压熔态淬火方法。将起始材料施加高 压,然后加高温,直至全部熔化,保温保压 ,最后在固定压力下.实行淬火,迅速冻结 高压高温状态的结构。这种方法,可以获得 准晶、非晶、纳米晶,特别是可以截获各种 中间亚稳相,是研究和获取中间亚稳相的行 之有效的方法。
第4节 无机化合物的高压合成
4. 1 金刚石和立方氮化硼的合成 1962年,人们将具有六角晶体结构的层状石墨作起
有机金属络合物Pt(DMG)2(6.9GPa)和聚苯胺有机高分 子PAn—H (3.5GPa)材料的电阻—压力极值作为定 标,效果也不错。
2.高温的测量
在高压腔内试样温度的测量中,最常用的方法, 是热电偶直接测量法。
常用的热电偶有Pt30%Rh—Pt6%Rh,Pt—PtlO% Rh,以及镍铬—镍铝热电偶。其中双铂热电偶的热 和化学稳定性很好,对周围有很强的抗污染能力,其 热电动势对压力的修正值很小,可适用于2000K范围 的高压下的高温测量。
常见产生静高压的装置有两类: (1)、是利用油压机作为动力,推动高压装
置中的高压构件,挤压试样,产生高压。 这类高压装置,最常见的有六面顶(高压构 件由六个顶锤组成)高压装置和年轮式两面 顶(高压构件由一对顶锤和一个压缸组成) 高压装置。
(2)、是利用天然金刚石作顶锤制成 的微型金刚石高压装置(diamond anvil cell,简称DAC)。这种装置可以产生几十GPa 到三百多GPa的高压,还可以与同步辐射光源 、X射线衍射、Raman散射等测试设备联用
哈伯法合成氨条件

哈伯法合成氨条件
哈伯法合成氨是德国化学家弗里茨·哈伯于1908年发明的,用于将氢气和氮气转化为氨。
这一过程需要高压和高温,以及铁作为催化剂。
具体来说,哈伯法合成氨的条件包括:
1. 高温:大约需要500℃的高温。
2. 高压:压力至少为20~50MPa,或者更具体地说,至少为200atm (200个标准大气压)。
3. 催化剂:使用铁作为催化剂。
4. 反应物:使用氢气(由天然气热分解提取而成)和大气中的氮气作为反应物。
这些条件是必要的,因为它们允许氢气和氮气在极端的物理条件下有效地反应并形成氨。
然而,值得注意的是,尽管哈伯法在过去被广泛使用,但现代的合成氨方法已经有所改进,以提高效率和减少环境影响。
稀有气体化合物形成过程

稀有气体化合物形成过程
稀有气体化合物是一类非常特殊的化合物,它们由稀有气体元
素组成,如氦、氖、氩、氪、氙和氡。
这些元素在自然界中以气体
的形式存在,非常稳定且不易与其他元素发生化学反应。
然而,科
学家们已经成功合成了一些稀有气体化合物,并研究了它们的形成
过程。
稀有气体化合物的形成过程通常涉及高温高压条件下的化学反应。
其中,最常见的方法是利用强大的激光或电子束来激发稀有气
体元素,使其处于高能态。
在这种高能态下,稀有气体元素会更容
易与其他元素发生化学反应,从而形成稀有气体化合物。
另一种方法是利用低温下的等离子体反应。
在这种反应中,稀
有气体元素首先被激发成等离子体状态,然后与其他元素或分子发
生反应,形成稀有气体化合物。
这种方法通常需要高度控制的实验
条件和精密的设备,但已经被用于合成一些稀有气体化合物。
除了实验室合成,一些稀有气体化合物也可以在自然界中找到,尤其是在极端条件下,如星际空间或地球上的极端环境中。
这些化
合物的形成过程可能涉及宇宙射线、高能粒子或者其他极端条件下
的化学反应。
总的来说,稀有气体化合物的形成过程是一个复杂而又令人着迷的领域。
通过不断的实验和研究,科学家们对这些化合物的形成机制有了更深入的了解,这也为我们认识和利用这些特殊化合物提供了重要的参考和指导。
化学合成中的流动反应技术

化学合成中的流动反应技术化学合成是一项重要的科技产业,应用广泛,涵盖了医药、化妆品、农药、涂料等多个领域。
其中,合成方法的多样性是化学合成的重要特征之一。
现代合成化学通过高效的化学反应来制备需要的化合物。
因此,化学反应的高效性与选择性成为了一个重要的研究方向。
经过长期的发展,化学合成逐渐由传统的试管反应朝向易于大规模工业化生产转变。
这个转变涉及到革命性的科技突破,其中化学反应的微型化和流动反应技术是其中的关键。
很多时候,化学反应的条件要求非常苛刻。
通常需要高温、高压、强酸、强碱等极端条件,需要耗费大量的能源,也对仪器设备有很高的要求。
由于这些原因,传统的化学反应方法已经不能很好地满足现代化学反应的需要。
微型化和流动反应技术是解决这个问题的一个好方案。
微型化技术尤其是微流控技术已经发展成为一项热门的化学研究领域。
微型化技术可以有效降低化学反应的体积和反应时间,从而提高反应效率和产率。
这种技术需要使用微观器件来放置和运输样品,因此需要高精度的微机械加工技术和微型流体技术。
其他技术,如微电化学和微波技术也正在成为流行的研究方向。
在流动反应技术中,液相和气相反应在连续的流体中发生。
这种技术非常适用于快速的反应和高效的反应条件。
流动反应技术最初应用于离子液体和溶剂的反应中。
离子液体具有非常好的溶解性和反应性,可以高效地促进液相的反应。
此外,流动反应技术还被应用于固相反应中。
这些反应可以在晶体或其他固体催化剂表面上进行,这种技术在有机合成中发挥了很大的作用。
流动反应技术被广泛应用于医药、化妆品和涂料工业中。
在医药工业中,流动反应技术可用于制备高品质的药品,因为它可以减少反应时间和化学品的浪费。
化妆品工业中,则可以用该技术制备出色的日化产品。
涂料工业则可以使用这种技术最大限度地提高产品的质量和产量,同时还可以减少环境污染。
流动反应技术还能用于复杂合成领域,包括放射性药物生产和有机太阳能电池等。
总的来说,微型化和流动反应技术已成为当今合成化学界的前沿领域。
海南大学药物合成还原反应课程

Birch
Li K Na(液NH3)
Na NH3 (liq.), EtOH
Na
2020/11/3
NH3 (liq.), EtOH
12
第三节 醛、酮的还原反应
1. 还原成烃的反应 1.1 Clemmensen还原
1.1 Clemmensen还原(酸性条件下反应)
O Zn-Hg/Zn
C
HCl
CH2
Zn-Hg 活性>Zn
b. 载体钯:加入载体(活性炭、CaCO3、BaSO4、硅藻土、Al2O3) 增大比表面,增大活性
c. 钯C(Pd/C)
d. Lindlar(林德拉)催化剂 Pd/BaSO4/
第二节 不饱和烃的还原
1. 炔、烯烃的还原 1.1 多相催化氢化
1.1 多相催化氢化法 (催化剂 Ni , Pd , Pt )
HgCl2+HCl+Zn
Zn-Hg
H H3COCHC C
Hg-Zn
HCl
H3CH2CH2CH2C
PhC
Hg-Zn
C COCH3
HCl
PhHC
C H
CH2CH3
2020/11/3
α,β-不饱和醛酮同时被还原
13
第三节 醛、酮的还原反应
1. 还原成烃的反应 1.1 Clemmensen还原
C O C H 2 C H 2 C O O HH g -Z n H C l
90%
2020/11/3
S CH2 CH CH2
H2
TTC
S CH2CH2CH3 S使催化剂中毒
TTC本身就是络合物不会使催化剂中毒 10
第二节 不饱和烃的还原
2. 芳烃的还原反应 2.1 催化氢化
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
21
PDP 优点:
1). 相对于CRT, 低电压 (< 200 V ) 2). 相对于LCD, 宽视角 3). 超大屏幕显示
PDP 需要改进之处:
电光转换效率低
= Blum / Pelec
Blum – 荧光功率 (lm) Pelec – 输入电功率 (W)
CRT: = 5 lm/W PDP: = 1.5 lm/W
体;大--冷等离子体
4
等离子体分类
按存在分类 1). 天然等离子体 宇宙中99%的物质是以等离子体状态 存在的, 如恒星星系、星云,地球附近的闪 电、极光、电离层等。如太阳本身就是一 个灼热的等离子体火球。 2). 人工等离子体 如:*日光灯、霓虹灯中的放电等离子体。 *等离子体炬(焊接、新材料制备、 消除污染)中的电弧放电等离子体。 *气体激光器及各种气体放电中的电 离气体。
11
等离子体增强CVD (PECVD )
• 以低压下(< 1.3kPa)气体辉光放电产生的等离子
体,来激活气体前驱物发生化学反应,又称作辉光放 电CVD。电子的温度比气体的温度高1~2个数量级, 能有效地降低沉积温度,适合制备大面积薄膜,并且 易于控制薄膜的微结构。
• 而采用PEMOCVD,可进一步降低沉积温度,适用对
第六章 极端条件下的合成
超高压/超高温/超高真空/超低温/强磁场或电场/ 激光/等离子体等条件
新化合物 新价态化合物 化合物的新物相 新合成方法
超高温超高压合成,等离子体化学合成,溅射合成 法,离子束合成法,激光物理气相沉积法,失重合 成
1
6.1 超高温超高压合成
• 举例:课本P216
非晶粉末BCN→块状非晶BCN→
(平面显示器:CRT, LCD, PDP, OLEDs , DLP, E-Paper)
22
6.3 溅射合成法
• 是指利溅射技术,利用经加速的高能粒子轰击靶
材,使靶材原子或分子被溅射出来,并沉积到基 体表面,形成材料的一种方法。
• 按是否发生化学反应,可分为阴极溅射、反应溅
射和吸气溅射三种
23
24
2H2O(g) + 2h
2H2
+
O2
lth
=
495
nm 33
作业:
1、P. 233, 思考题 2,4。 2、5:溅射技术有哪几种?有哪些应用?
34
4. 等离子体环境工程 (燃煤电厂烟气中氮、硫氧化物
脱除,VOC脱除, 汽车尾气中氮氧化物脱除,固体废 料处理,……)
5. 纺织品等材料表面的等离子体改性 (已产业化) 6. 等离子体增强化学气相沉积(PECVD)制备各种
新型材料 (金刚石,类金刚石,碳纳米管,……)
19
等离子体平面显示器 (PDP)
30
分子活化的几种主要手段(二)
3. 光子活化 通过合适波长光子对反应物分子内能态(转动态、
振动态及电子态)的激发提高反应速度,往往也同时 增加新的反应途径。如胶片感光,天然及人工光合 作用,各种光化学反应研究等。
H2O + h → OH + H (DH ~ 242 nm)
(H20 仅吸收短于185 nm 的光,到达地球之太阳光中含此波 段光很少)
MW-PCVD化学气相沉积系统
MW-PCVD微波等离子体化学气相沉积系统。属于 无极放电方法,并且在较低气压下工作,可得到品质 高的透明金刚石膜,应用于场发射等领域。
中国科学院 沈阳科学仪器研制中心
17
等离子体化学气相沉积(PCVD) 应用举例 (课本P223-225)
• 金刚石和特种功能膜的合成
汽化,气态源物质不经化学反应而沉积在衬底上 的方法—LPVD
• 源物质从汽化到沉积过程中发生化学反应者称为
激光诱导化学气相沉积法-- LICVD
• 用于制备金属、合金、金属间化合物、非金属化
合物等超细粉末及薄膜材料等
28
6.5 失重合成(太空合成)
• 太空的特殊环境条件:
微重力,高真空,廉价太阳能,温度条件
负离子、电子和中性粒子的集合体。由于正负电 荷总数相等,宏观上仍呈电中性,所以称为等离 子体。“物质的第四态”
• 分类:按电离度(弱电离体、中电离体、强电离体),
按温度高低(热等离子体和冷等离子体)
• 特性:高导电性,粒子间的特殊集体相互作用,
传播各种振荡波
• 电子温度Te:气体放电等离子体的重要参数 • 冷热等离子体的判据E/p 或 E/n:小--热等离子
磁控与离子束复合溅射系统
沈阳科学仪器研制中心,JL-450B型
主要用于制备CNx等新型功能薄膜材料,还用于金 刚石膜表面金属化,可进行各种金属、化合物的薄膜 沉积研究。
25
溅射合成法的应用(P227-228)
• 钡铁氧体薄膜的合成 • PTC电子陶瓷薄膜的合成 • SnO2气敏薄膜的合成
26
6.4 离子束合成法
2
6.2 等离子体化学合成
也称放电合成,是利用等离子 体的特殊性质进行化学合成的 一种技术 •什么是等离子体(plasma)? •如何获得等离子体? •等离子体化学有何特点? •等离子体在化学合成中的应用
三星PS42S5H等离子电视
3
等离子体的一般概念
• 等离子体是物质高度电离的一种状态,是含有正
5
等离子体的获得
1 热等离子体的获得Байду номын сангаас
•电弧放电法(阳极区、阴极区、弧柱) •射频放电法:电容耦合放电,电感耦合放电 特别适用于等离子体化学反应和等离子体加工 •等离子体喷焰和等离子体炬 一类应用于航天试验,另一类用于化工生产和材 料合成及处理
6
2 冷等离子体的获得
• 低压气体放电 低强度电弧、辉光放电、高频放电(微波、射频) 无电极放电:消除电极与等离子体直接接触而引 起玷污等问题
• 合金和功能无机材料 • 半导体单晶
29
分子活化的几种主要手段(一)
1. 热活化 通过升高反应温度提高分子平动能 k = A exp(-Ea /RT)
2. 催化活化 是经典的但仍是当前工业上应用最广的 促进化学反应的主要手段 1). 通过表面吸附浓缩反应物 (相当于提高 碰撞频率 ) 2). 在催化剂表面形成有利的分子取向 3). 通过形成新的反应途径降低反应活化能 Ea
解离电离 e + AB A+ + B + 2e 解离附着 e + AB A- + B
10
等离子体在化学合成中的应用
热等离子体:
• NO2和CO的生产等 • 超细、超纯耐高温粉末材料的合成 • 亚稳态金属粉末和单晶的制备 • 金属和合金的冶炼
冷等离子体:
•氨、肼、金刚石的合成→较温和的条件下实现
转动、电子态)变化
3) 电离(ionization) 碰撞 e + A A+ + 2e
4) 附着( attachment ) 碰撞 (当A具有正电子亲合势时)
e + A + M A- + M
5) 反应 ( reactive) 碰撞, 如解离反应:
e + AB A + B + e
6) 复杂 碰撞过程, 如:
Glass
MgO (500 nm)
Glass
Address electrode
PbO, Dielectric layer (transp.)
Ag electrode
ITO (In+Tin Oxide, transparent sustained electrode)
Phosphor (RGB: red, green, blue)
Ne (96%) + Xe (4%) , 400 Torr
Ne + e Ne* Ne* + Xe Ne + Xe+ (Penning Ionization) Xe+ + Xe + M Xe2+ + M Xe2+ + e Xe*+ Xe
Xe* Xe* + h
Xe* + Xe + M Xe2* + M
RN Dixon, DW Hwang, XF Yang, …, XM Yang,
Science, 285 (1999) 1249-53. ( h = 121.6 nm)
4. 电子活化 (系等离子体活化之一次过程) 电子与反应分子碰撞产生激发态原子、分子、
自由基和离子等。 31
分子活化的几种主要手段(三)
• 热致电离等离子体 (高平动能原子、分子碰撞导致电离) 高温燃烧、爆炸、冲击波
• 辐射电离等离子体 (光电离) X-射线、紫外光等
7
等离子体化学反应
* 等离子体化学这个名词最早出现:1967年出版 的一本专著 “Plasma Chemistry in Electrical
Discharges ”
* 等离子体化学是研究等离子体中各种粒子之间或这些 粒子与电磁辐射及周围物质间相互化学作用的一门分 支学科
国家标准:化学 → 物理化学 → 高能化学(包括辐射化 学、等离子体化学等)
8
等离子体中各种粒子间的碰撞过程
中性粒子
电子
负离子
正离子
光子
9
电子与中性原子、分子间的 基元碰撞过程
1) 弹性( elastic ) 碰撞过程, 仅有平动能交换 2) 非弹性( inelastic ) 碰撞过程, 包含内能(振动、
• 又称为离子注入,是通过高能离子束轰击固态基
材—靶,而将靶室中已由其他方式汽化的气态源 物质直接强行打入固态基体靶内(即将离子注入靶 内)的非平衡过程。
