常见溶剂的物理性质
常用溶剂的性能介绍及挥发速度

常用溶剂的挥发速度名称-------------- 沸点℃---- 比挥发速度二氯甲烷--------- 40--------- 2750四氯化碳-------- 76.8--------- 1280醋酸甲酯--------- 57.2--------- 1180丙酮------------- 56.2--------- 1120正己烷--------- 65~69 --------- 1000 二氯乙烷--------- 84----------- 750环已烷--------- 80.8------------ 720醋酸乙酯-------- 77.1 --------- 615丁酮------------ 79.6---------- 572四氢呋喃--------- 66---------- 501苯---------------80 ---------- 500正庚烷--------- 98.0---------- 386甲醇----------- 64.5----------- 370甲苯---------- 111.0--------- 240异丙醇--------- 82.5--------- 205乙醇----------- 78.1--------- 203醋酸丁酯--------26.5 --------- 100二甲苯---------135~145-------- 68甲基溶纤剂------ 124.5--------- 55丁醇------------ 117.1--------- 45环已酮--------- 155~156 ------- 25三氯乙烯--------- 86~88--------- 快二氧六环--------- 101~102------- 中二甲基甲酰胺----153------------- 慢醋酸戊酯--------- 130~150 -------慢有机溶剂主要种类及性能介绍有机溶剂主要种类及性能一、烃类溶剂1.烃只含有碳氢两种元素的有机化合物叫烃。
乙二醇、甲醇、乙醇相似相溶-概述说明以及解释

乙二醇、甲醇、乙醇相似相溶-概述说明以及解释1.引言1.1 概述概述部分的内容可以如下编写:在化学领域中,乙二醇、甲醇和乙醇是三种常见的有机溶剂,它们的相似性和相溶性一直是研究的热点。
乙二醇是一种二元醇,也被称为二乙二醇,具有无色、粘稠的液体状态。
甲醇是一种单元醇,常见的有机溶剂,具有无色、易燃的液体状态。
乙醇是一种单元醇,也被称为酒精,是一种常见的溶剂和消毒剂,具有无色、易挥发的液体状态。
这三种有机溶剂具有很多相似性,首先它们在化学结构上都包含一个醇基,即羟基(-OH)。
这使得它们都具有较好的溶解性,能够与许多无机物和有机物发生相互作用。
其次,在物理性质上,它们的密度相近,都是无色的液体,易于分离纯化。
此外,它们的沸点也相对较低,方便在实验室中进行处理。
最重要的是,它们具有与水良好的相溶性,这在很多实际应用中至关重要。
因此,对于乙二醇、甲醇和乙醇的相似性和相溶性的研究具有重要的理论和实际意义。
了解它们的性质和特点,有助于我们更好地选择和应用这些溶剂,并在化学实验和工业生产中取得更好的效果。
本文将重点介绍乙二醇、甲醇和乙醇的性质和特点,以及它们之间的相似性和相溶性的影响因素,以期为相关研究和应用提供一定的参考依据。
1.2 文章结构文章结构部分的内容可以按照以下方式进行编写:文章结构:本文主要包括以下几个部分,分别是引言、正文和结论。
引言部分主要对文章的研究背景和意义进行概述,介绍了乙二醇、甲醇和乙醇相似相溶的相关性质和特点。
接着介绍了本文的结构框架。
正文部分主要包括了乙二醇、甲醇和乙醇的性质和特点的详细介绍。
首先,我们将详细解析乙二醇的化学性质、物理性质以及其在工业领域的应用。
然后,我们将重点介绍甲醇的性质,包括它的化学性质、物理性质以及它在医药、化工等行业的应用情况。
最后,我们将详细探讨乙醇的性质与特点,包括其结构、燃烧性质以及它在日常生活和工业中的应用。
结论部分将总结乙二醇、甲醇和乙醇的相似性。
常见有机溶剂的性质

常见有机溶剂的性质一、溶剂的定义溶剂(solvent)这个词广义指在均匀的混合物中含有的一种过量存在的组分。
狭义地说,在化学组成上不发生任何变化并能溶解其他物质(一般指固体)的液体,或者与固体发生化学反应并将固体溶解的液体。
溶解生成的均匀混合物体系称为溶液。
在溶液中过量的成分叫溶剂;量少的成分叫溶质。
溶剂也称为溶媒,即含有溶解溶质的媒质之意。
但是在工业上所说的溶剂一般是指能够溶解油脂、蜡、树脂(这一类物质多数在水中不溶解)而形成均匀溶液的单一化合物或者两种以上组成的混合物。
这类除水之外的溶剂称为非水溶剂或有机溶剂,水、液氨、液态金属、无机气体等则称为无机溶剂。
二、溶解现象溶解本来表示固体或气体物质与液体物质相混合,同时以分子状态均匀分散的一种过程。
事实上在多数情况下是描述液体状态的。
一些物质之间的混合,金与铜、铜与镍等许多金属以原子状态相混合的所谓合金也应看成是一种溶解现象。
所以严格地说,只要是两种以上的物质相混合组成一个相的过程就可以称为溶解,生成的相称为溶液。
一般在一个相中应呈均匀状态,其构成成分的物质可以以分子状态或原子状态相互混合。
溶解过程比较复杂,有的物质在溶剂中可以以任何比例进行溶解,有的部分溶解,有的则不溶。
这些现象是怎样发生的,其影响的因素很多,一般认为与溶解过程有关的因素大致有以下几个方面:⑴相同分子或原子间的引力与不同分子或原子间的引力的相互关系(主要是范德华引力);⑵分子的极性引起的分子缔合程度;⑶分子复合物的生成;⑷溶剂化作用;⑸溶剂、溶质的相对分子质量;⑹溶解活性基团的种类和数目。
化学组成类似的物质相互容易溶解,极性溶剂容易溶解极性物质,非极性溶剂容易溶解非极性物质。
例如,水、甲醇和乙醇彼此之间可以互溶;苯、甲苯和乙醚之间也容易互溶,但水与苯,甲醇与苯则不能自由混溶。
而且在水或甲醇中易溶的物质难溶于苯或乙醚;反之在苯或乙醚中易溶的却难溶于水或甲醇。
这些现象可以用分子的极性或者分子缔合程度大小进行判断。
乙腈 气相 溶剂-概述说明以及解释

乙腈气相溶剂-概述说明以及解释1.引言1.1 概述乙腈是一种常用的有机溶剂,也是一种重要的气相溶剂。
它具有许多独特的性质和广泛的应用领域。
乙腈化学式为CH3CN,且其分子结构中含有氰基与甲基基团。
与许多其他有机溶剂相比,乙腈具有较低的沸点和良好的挥发性,易于从反应体系中除去。
这使得乙腈成为一种理想的气相溶剂,尤其适用于各种气相色谱、液相色谱和质谱分析技术。
乙腈在化学研究中的应用广泛。
作为溶剂,它可以用于溶解和稀释各种有机和无机化合物,在研究中起到媒介和载体的作用。
由于乙腈具有较高的溶解度和较低的粘度,它在许多反应中具有较好的流动特性,能够加速反应的进行,并且不会对反应产物产生干扰。
此外,乙腈还具有良好的溶解性能,可溶解许多无法在其他溶剂中溶解的化合物,为研究提供了更广泛的选择。
在化学研究中,乙腈还可以作为一个重要的气相溶剂。
由于其挥发性强,乙腈可以迅速转变为气体状态,从而在高温和高压下提供稳定的气相环境。
乙腈的气相溶剂性能使得其在气相色谱、质谱和其他气相分析技术中得到了广泛的应用。
通过使用乙腈作为气相溶剂,研究人员可以更好地理解和分析气相反应的动力学和机理。
总之,乙腈作为一种重要的气相溶剂,在化学研究和分析中扮演着重要的角色。
其独特的性质和广泛的应用使得乙腈成为了科研工作者不可或缺的工具。
通过深入研究乙腈的性质和应用,我们可以更好地利用它在化学领域中的潜力,推动化学科学的发展。
1.2 文章结构本文按照以下结构展开探讨乙腈作为气相溶剂的相关内容。
首先,引言部分将概述乙腈和气相溶剂的基本概念,并阐明文章的目的。
接着,在正文部分,将详细介绍乙腈的性质,包括其物理性质和化学性质,并分析乙腈作为气相溶剂在不同领域的应用。
然后,进一步阐述气相溶剂的定义和作用,通过说明气相溶剂在化学实验和工业生产中的重要性,突出乙腈在其中的独特作用和广泛应用。
最后,在结论部分,总结乙腈作为气相溶剂的应用场景和其在化学研究中的重要性,并展望乙腈作为气相溶剂未来的发展方向。
甲醇、丙酮、乙酸乙酯物理性质[最新]
![甲醇、丙酮、乙酸乙酯物理性质[最新]](https://img.taocdn.com/s3/m/51ca197d571252d380eb6294dd88d0d233d43c6a.png)
丙酮的物理性质(2008-10-10 19:51:35)转载▼标签:丙酮ppm物理性质浓度蒸气杂谈丙酮(Acetone,一般工厂俗称ACE),CH3COCH3,分子量58.08,密度:在25℃时比重0.788,熔点:-94℃,沸点:56.48℃,闪点:-17.78℃(闭杯),又名二甲基甲酮,为最简单的饱和酮。
是一种无色透明液体,有特殊的辛辣气味。
易溶于水和甲醇、乙醇、乙醚、氯仿、吡啶等有机溶剂。
易燃、易挥发,化学性质较活泼。
分极限参数:自燃点:465℃爆炸极限:2.6%~12.8% 最大爆炸压力:87.3牛/平方厘米最易引燃浓度:4.5产生最大爆炸压力浓度:6.3% 最小引燃能量:1.15毫焦(当4.97%浓度时) 燃烧热值:1792千焦/摩尔(液体,25℃) 蒸气压:53.33千帕(39.5℃)。
丙酮主要是对中枢神经系统的抑制、麻醉作用,高浓度接触对个别人可能出现肝、肾和胰腺的损害。
由于其毒性低,代谢解毒快,生产条件下急性中毒较为少见。
急性中毒时可发生呕吐、气急、痉挛甚至昏迷。
口服后,口唇、咽喉烧灼感,经数小时的潜伏期后可发生口干、呕吐、昏睡、酸中度和酮症,甚至暂时性意识障碍。
丙酮对人体的长期损害表现为对眼的刺激症状如流泪、畏光和角膜上皮浸润等,还可表现为眩晕、灼热感,咽喉刺激、咳嗽等。
丙酮,工业上主要作为溶剂用于炸药、塑料、橡胶、纤维、制革、油脂、喷漆等行业中,也可作为合成烯酮、醋酐、碘仿、聚异戊二烯橡胶、甲基丙烯酸、甲酯、氯仿、环氧树脂等物质的重要原料。
毒性:丙酮主要是对中枢神经系统的抑制、麻醉作用,高浓度接触对个别人可能出现肝、肾和胰腺的损害。
由于其毒性低,代谢解毒快,生产条件下急性中毒较为少见。
急性中毒时可发生呕吐、气急、痉挛甚至昏迷。
口服后,口唇、咽喉烧灼感,经数小时的潜伏期后可发生口干、呕吐、昏睡、酸中度和酮症,甚至暂时性意识障碍。
丙酮对人体的长期损害,表现为对眼的刺激症状如流泪、畏光和角膜上皮浸润等,还可表现为眩晕、灼热感,咽喉刺激、咳嗽等。
乙醇---上课用

△
CH3CO18OCH2 CH3+ H2O
• 实质:酸去羟基、醇去氢(羟基上的) • 注意:可逆反应(酯在碱性条件下水解)
“酒是陈的香”
(四)、乙酸的用途
• 是一种重要的化工原料 • 在日常生活中也有广泛的用途
小结:
O
CH3—C—O—H
酸性 酯化
酯类广泛存在于自然界中
酯是有芳香气味的液体,存在于各种水果 和花草中。如:梨里含有 乙酸异戊酯,苹果和香蕉 里含有异戊酸异戊酯等。 酯的密度一般小于水,并 难溶于水,易溶于乙醇和乙 醚等有机溶剂。
C: ② ④
3、把质量为m g的铜丝灼烧变黑,立即放 入下列物质中,能使铜丝变红,而且质 量仍为m g的是( BD ) A: 稀硫酸 B: 酒精 C: 稀硝酸 D: CO 4、能用来检验酒精中是否含有水的试剂 是( B ) A: CuSO4·5H2O B:无水硫酸铜 ·
C:浓硫酸
D: 金属钠
5、在下列物质中加入溴水数滴,振荡,溴 水不褪色的是( B ) A: NaOH溶液 B:酒 精 C: SO2溶液 D:氢硫酸溶液 6、酒精完全燃烧后,生成的产物可用一种 物质完全吸收,这种物质是( C ) A:浓硫酸 B:浓NaOH溶液
2、乙醇分子结构(C2H6O)
结构式
H H H — C—C—O—H H H
结构简式
CH3CH2OH
或C2H5OH
球棍模型
比例模型
【乙烷与乙醇结构的异同】
H H H H
H — C—C—O—H
H H
H — C—C—H
H H
相同点:两个碳原子都是以单键相连
不同点: 1、乙烷中的6个氢原子相同,只有一种等效氢; 2、而乙醇中有三种等效氢。
常见有机溶剂极性表
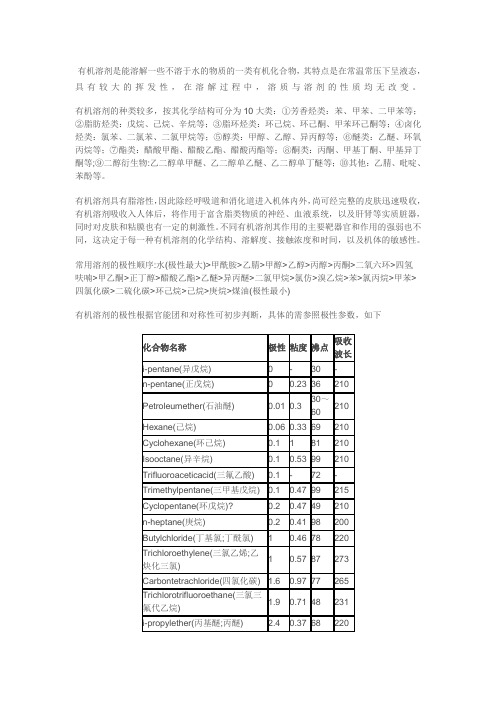
有机溶剂是能溶解一些不溶于水的物质的一类有机化合物,其特点是在常温常压下呈液态,具有较大的挥发性,在溶解过程中,溶质与溶剂的性质均无改变。
有机溶剂的种类较多,按其化学结构可分为10大类:①芳香烃类:苯、甲苯、二甲苯等;②脂肪烃类:戊烷、己烷、辛烷等;③脂环烃类:环己烷、环己酮、甲苯环己酮等;④卤化烃类:氯苯、二氯苯、二氯甲烷等;⑤醇类:甲醇、乙醇、异丙醇等;⑥醚类:乙醚、环氧丙烷等;⑦酯类:醋酸甲酯、醋酸乙酯、醋酸丙酯等;⑧酮类:丙酮、甲基丁酮、甲基异丁酮等;⑨二醇衍生物:乙二醇单甲醚、乙二醇单乙醚、乙二醇单丁醚等;⑩其他:乙腈、吡啶、苯酚等。
有机溶剂具有脂溶性,因此除经呼吸道和消化道进入机体内外,尚可经完整的皮肤迅速吸收,有机溶剂吸收入人体后,将作用于富含脂类物质的神经、血液系统,以及肝肾等实质脏器,同时对皮肤和粘膜也有一定的刺激性。
不同有机溶剂其作用的主要靶器官和作用的强弱也不同,这决定于每一种有机溶剂的化学结构、溶解度、接触浓度和时间,以及机体的敏感性。
常用溶剂的极性顺序:水(极性最大)>甲酰胺>乙腈>甲醇>乙醇>丙醇>丙酮>二氧六环>四氢呋喃>甲乙酮>正丁醇>醋酸乙酯>乙醚>异丙醚>二氯甲烷>氯仿>溴乙烷>苯>氯丙烷>甲苯>四氯化碳>二硫化碳>环己烷>己烷>庚烷>煤油(极性最小)有机溶剂的极性根据官能团和对称性可初步判断,具体的需参照极性参数,如下表示有机溶剂的极性,关系到其物理化学性质、如介电常数、偶极矩或折射率。
这种表示方法把所有的溶剂看作是连续作用的介质,而不是看作由各个分子组成的非连续统一体,并且未考虑到溶剂和溶质之间的特殊的相互作用。
二甲苯溶剂类别

二甲苯溶剂类别摘要:一、二甲苯溶剂的定义与性质二、二甲苯溶剂的分类1.邻二甲苯2.间二甲苯3.对二甲苯三、二甲苯溶剂的应用领域1.涂料工业2.制药工业3.染料工业四、二甲苯溶剂的环保问题与处理方法1.对环境的影响2.我国的相关法规3.处理方法与技术五、二甲苯溶剂的未来发展趋势与展望正文:二甲苯溶剂是一种常见的有机溶剂,具有高溶解力、挥发性和可燃性等特点,被广泛应用于涂料、制药、染料等众多领域。
本文将对二甲苯溶剂的定义、性质、分类、应用及环保问题等方面进行详细阐述。
首先,二甲苯溶剂是一类具有相似结构、性质和用途的有机溶剂,主要包括邻二甲苯、间二甲苯和对二甲苯三种类型。
这三种二甲苯溶剂在物理性质和化学性质上有一定差异,但在很多领域都可以互相替代。
其次,二甲苯溶剂在各个领域有广泛的应用。
在涂料工业中,二甲苯溶剂作为溶剂或稀释剂,可以提高涂料的附着力、流平性和干燥速度。
在制药工业中,二甲苯溶剂可用于提取、精制和储存药物,以及作为制药过程中的反应介质。
在染料工业中,二甲苯溶剂可用于合成和整理染料,提高染料的色牢度和亮度。
然而,二甲苯溶剂在使用过程中对环境和人体健康产生了一定的影响。
挥发的二甲苯溶剂会污染大气,对人体呼吸系统产生刺激作用,长期接触还可能导致癌症。
因此,我国政府制定了一系列法规和标准,限制二甲苯溶剂的生产、使用和排放。
此外,采用吸附、冷凝、燃烧等方法对二甲苯溶剂进行处理,可以有效降低其对环境和人体健康的影响。
总之,二甲苯溶剂在多个领域具有重要作用,但同时也带来了环保问题。
随着科学技术的进步和环保意识的提高,未来二甲苯溶剂的发展趋势将更加注重绿色、环保和可持续发展。
甲醇、丙酮、乙酸乙酯物理性质

丙酮的物理性质(2008-10-10 19:51:35)转载▼标签:丙酮ppm物理性质浓度蒸气杂谈丙酮(Acetone,一般工厂俗称ACE),CH3COCH3,分子量58.08,密度:在25℃时比重0.788,熔点:-94℃,沸点:56.48℃,闪点:-17.78℃(闭杯),又名二甲基甲酮,为最简单的饱和酮。
是一种无色透明液体,有特殊的辛辣气味。
易溶于水和甲醇、乙醇、乙醚、氯仿、吡啶等有机溶剂。
易燃、易挥发,化学性质较活泼。
分极限参数:自燃点:465℃爆炸极限:2.6%~12.8% 最大爆炸压力:87.3牛/平方厘米最易引燃浓度:4.5产生最大爆炸压力浓度:6.3% 最小引燃能量:1.15毫焦(当4.97%浓度时) 燃烧热值:1792千焦/摩尔(液体,25℃) 蒸气压:53.33千帕(39.5℃)。
丙酮主要是对中枢神经系统的抑制、麻醉作用,高浓度接触对个别人可能出现肝、肾和胰腺的损害。
由于其毒性低,代谢解毒快,生产条件下急性中毒较为少见。
急性中毒时可发生呕吐、气急、痉挛甚至昏迷。
口服后,口唇、咽喉烧灼感,经数小时的潜伏期后可发生口干、呕吐、昏睡、酸中度和酮症,甚至暂时性意识障碍。
丙酮对人体的长期损害表现为对眼的刺激症状如流泪、畏光和角膜上皮浸润等,还可表现为眩晕、灼热感,咽喉刺激、咳嗽等。
丙酮,工业上主要作为溶剂用于炸药、塑料、橡胶、纤维、制革、油脂、喷漆等行业中,也可作为合成烯酮、醋酐、碘仿、聚异戊二烯橡胶、甲基丙烯酸、甲酯、氯仿、环氧树脂等物质的重要原料。
毒性:丙酮主要是对中枢神经系统的抑制、麻醉作用,高浓度接触对个别人可能出现肝、肾和胰腺的损害。
由于其毒性低,代谢解毒快,生产条件下急性中毒较为少见。
急性中毒时可发生呕吐、气急、痉挛甚至昏迷。
口服后,口唇、咽喉烧灼感,经数小时的潜伏期后可发生口干、呕吐、昏睡、酸中度和酮症,甚至暂时性意识障碍。
丙酮对人体的长期损害,表现为对眼的刺激症状如流泪、畏光和角膜上皮浸润等,还可表现为眩晕、灼热感,咽喉刺激、咳嗽等。
有机知识整理

有机化学知识点整理与推断专题一、重要的物理性质①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
补充性质【高中化学中各种颜色所包含的物质】1.红色:铜、Cu2O、品红溶液、酚酞在碱性溶液中、石蕊在酸性溶液中、液溴(深棕红)、红磷(暗红)、苯酚被空气氧化、Fe2O3、(FeSCN)2+(血红)2.橙色:、溴水及溴的有机溶液(视浓度,黄—橙)3.黄色(1)淡黄色:硫单质、过氧化钠、溴化银、TNT、实验制得的不纯硝基苯、(2)黄色:碘化银、黄铁矿(FeS2)、*磷酸银(Ag3PO4)工业盐酸(含Fe3+)、久置的浓硝酸(含NO2)(3)棕黄:FeCl3溶液、碘水(黄棕→褐色)4.棕色:固体FeCl3、CuCl2(铜与氯气生成棕色烟)、NO2气(红棕)、溴蒸气(红棕)5.褐色:碘酒、氢氧化铁(红褐色)、刚制得的溴苯(溶有Br2)6.绿色:氯化铜溶液、碱式碳酸铜、硫酸亚铁溶液或绿矾晶体(浅绿)、氯气或氯水(黄绿色)、氟气(淡黄绿色)7.蓝色:胆矾、氢氧化铜沉淀(淡蓝)、淀粉遇碘、石蕊遇碱性溶液、硫酸铜溶液8.紫色:高锰酸钾溶液(紫红)、碘(紫黑)、碘的四氯化碳溶液(紫红)、碘蒸气2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2==CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃)一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)甲乙醚(CH3OC2H5,沸点为10.8℃)环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
常用溶剂的物理性质和纯化

常用溶剂的物理性质和纯化化学合成实验经常会用到溶剂,溶剂不仅作为反应介质,产物的纯化和后处理例如重结晶、萃取、层析等操作也经常用到溶剂。
由于溶剂的用量总是比较大,即使溶剂中微量杂质也会对反应和产物的纯化带来一定的影响。
一些有机反应(如Grignard反应等)对溶剂的要求更高,微量的水和醇都会使反应难以发生。
因此,溶剂在使用前应检验其纯度,需要时将其纯化。
下面介绍常用有机溶剂的物理性质和一般纯化方法。
1.石油醚石油醚为轻质石油产品,是低分子量的烃类(主要是戊烷和己烷)的混合物。
其沸程为30~1500C,收集的温度区间一般为300C,有30~600C、60~900C、90~1200C等沸程规格的石油醚。
石油醚中含有少量不饱和烃,沸点和烷烃相近,用蒸馏法无法分离,必要时可用浓硫酸和高锰酸钾把它除去。
通常将石油醚用其体积十分之一的浓硫酸洗涤两三次,再用10%的硫酸加入高锰酸钾配成的饱和溶液洗涤,直至水层中的紫色不再消失为止,然后再用水洗,经无水氯化钙干燥后蒸馏。
如要绝对干燥的石油醚则再用金属钠进一步干燥(见“无水乙醚”)。
2.苯bp80.10C,mp5.50C,d4200.87865,n D201.5011普通的苯含有少量的水(200C时,苯能溶解0.06%的水),苯和水形成的共沸混合物在69.250C沸腾,含有91.17%的苯。
由煤焦油加工得到的苯还含有少量的噻吩(沸点840C)。
欲除去水和噻吩,可用等体积的15%硫酸洗涤,直至酸层为无色或浅黄色,或检查无噻吩为止(取5滴苯,加入5滴浓硫酸及1~2滴1%α,β-吲哚醌-浓硫酸溶液,振荡,如酸层呈墨绿色或兰色,表示有噻吩存在)。
苯层再依次用水、10%Na2CO3水溶液、水洗涤,无水氯化钙干燥过夜后,蒸馏。
若要高度干燥可加入金属钠进一步除水。
3.甲苯bp110.60C,d4200.8669,n D201.4961甲苯与水形成共沸混合物,在84.10C沸腾,含81.4%的甲苯。
常用溶剂的物理化学性质

1.物质的理化常数:国标编号82503CAS号1336-21-6中文名称氨水英文名称Ammonium hydroxide;Ammonia water别名氢氧化铵;氨溶液[含氨>10%~≤35%]分子式NH4OH 外观与性状无色透明液体,有强烈的刺激性臭味分子量35.05 蒸汽压1.59kPa(20℃)熔点溶解性溶于水、醇密度相对密度(水=1)0.91 稳定性稳定危险标记20(碱性腐蚀品) 主要用途用于制药工业,纱罩业,晒图,农业施肥等2.对环境的影响:一、健康危害侵入途径:吸入、食入。
健康危害:吸入后对鼻、喉和肺有刺激性引起咳嗽、气短和哮喘等;可因喉头水肿而窒息死亡;可发生肺水肿,引起死亡。
氨水溅入眼内,可造成严重损害,甚至导致失明;皮肤接触可致灼伤。
慢性影响:反复低浓度接触,可引起支气管炎。
皮肤反复接触,可致皮炎,表现为皮肤干燥、痒、发红。
二、毒理学资料及环境行为毒性:属低毒类。
急性毒性:LD50350mg/kg(大鼠经口)危险特性:易分解放出氨气,温度越高,分解速度越快,可形成爆炸性气氛。
若遇高热,容器内压增大,有开裂和爆炸的危险。
燃烧(分解)产物:氨。
3.现场应急监测方法:检测管法4.实验室监测方法:纳氏试剂比色法(GB7479-87)水杨酸分光光度法(GB7481-87)5.环境标准:中国(GB/T14848-93) 地下水质量标准(氨氮,mg/L ) I类II类III类IV类V类0.02 0.02 0.2 0.5 0.5以上中国(GB11607-89) 渔业水质标准(非离子氨) 0.02mg/L 中国(GHZB1-1999) 地表水环境质量标准(氨氮,mg/L ) I 类0.5;II类0.5;III类0.5;IV类1.0;V类1.5地表水环境质量标准(非离子氨,mg/L ) I类0.02;II类0.02;III类0.02;IV类0.2;V类0.2中国(GB3097-1997) 海水水质标准(非离子氨) 0.020mg/L中国(GB5048-92) 农田灌溉水质标准(凯氏氮) 水作:12mg/L旱作:30mg/L蔬菜:30mg/L中国(GB8978-1996) 污水综合排放标准(氨氮) 医药原料药、染料、石油化工工业:一级15mg/L;二级50mg/L 其他排污单位:一级15mg/L;二级25mg/L6.应急处理处置方法:一、泄漏应急处理疏散泄漏污染区人员至安全区,禁止无关人员进入污染区,建议应急处理人员戴自给式呼吸器,穿化学防护服。
常用溶剂的物理化学性质

1.物质的理化常数:国标编号82503CAS号1336-21-6中文名称氨水英文名称Ammonium hydroxide;Ammonia water别名氢氧化铵;氨溶液[含氨>10%~≤35%]分子式NH4OH 外观与性状无色透明液体,有强烈的刺激性臭味分子量35.05 蒸汽压1.59kPa(20℃)熔点溶解性溶于水、醇密度相对密度(水=1)0.91 稳定性稳定危险标记20(碱性腐蚀品) 主要用途用于制药工业,纱罩业,晒图,农业施肥等2.对环境的影响:一、健康危害侵入途径:吸入、食入。
健康危害:吸入后对鼻、喉和肺有刺激性引起咳嗽、气短和哮喘等;可因喉头水肿而窒息死亡;可发生肺水肿,引起死亡。
氨水溅入眼内,可造成严重损害,甚至导致失明;皮肤接触可致灼伤。
慢性影响:反复低浓度接触,可引起支气管炎。
皮肤反复接触,可致皮炎,表现为皮肤干燥、痒、发红。
二、毒理学资料及环境行为毒性:属低毒类。
急性毒性:LD50350mg/kg(大鼠经口)危险特性:易分解放出氨气,温度越高,分解速度越快,可形成爆炸性气氛。
若遇高热,容器内压增大,有开裂和爆炸的危险。
燃烧(分解)产物:氨。
3.现场应急监测方法:检测管法4.实验室监测方法:纳氏试剂比色法(GB7479-87)水杨酸分光光度法(GB7481-87)5.环境标准:中国(GB/T14848-93) 地下水质量标准(氨氮,mg/L ) I类II类III类IV类V类0.02 0.02 0.2 0.5 0.5以上中国(GB11607-89) 渔业水质标准(非离子氨) 0.02mg/L 中国(GHZB1-1999) 地表水环境质量标准(氨氮,mg/L ) I 类0.5;II类0.5;III类0.5;IV类1.0;V类1.5地表水环境质量标准(非离子氨,mg/L ) I类0.02;II类0.02;III类0.02;IV类0.2;V类0.2中国(GB3097-1997) 海水水质标准(非离子氨) 0.020mg/L中国(GB5048-92) 农田灌溉水质标准(凯氏氮) 水作:12mg/L旱作:30mg/L蔬菜:30mg/L中国(GB8978-1996) 污水综合排放标准(氨氮) 医药原料药、染料、石油化工工业:一级15mg/L;二级50mg/L 其他排污单位:一级15mg/L;二级25mg/L6.应急处理处置方法:一、泄漏应急处理疏散泄漏污染区人员至安全区,禁止无关人员进入污染区,建议应急处理人员戴自给式呼吸器,穿化学防护服。
几种常用溶剂的物理性质

几种常用溶剂的物理性质丙酮物理性质丙酮结构式[2]外观与性状:无色透明易流动液体,有芳香气味,极易挥发。
熔点(℃):-94.6相对密度(水=1):0.80沸点(℃):56.5相对蒸气密度(空气=1):2.00分子式:C3H6O分子量:58.08饱和蒸气压(kPa):53.32(39.5℃)燃烧热(kJ/mol):1788.7 临界温度(℃):235.5临界压力(MPa):4.72辛醇/水分配系数的对数值:-0.24闪点(℃):-20爆炸上限%(V/V):13.0引燃温度(℃):465爆炸下限%(V/V):2.5溶解性:与水混溶,可混溶于乙醇、乙醚、氯仿、油类、烃类等多数有机溶剂。
正己烷物化性质【熔点(℃)】-95.3【沸点(℃)】68.74【闪点(℃)】-23【密度(D.)】:0.692 g/mL at 20 ℃[2]【爆炸下限%(VN)】1.2%【爆炸上限%(VN)】7.4%【性状】有微弱的特殊气味的无色挥发性液体。
【溶解性】不溶于水,可与乙醚、氯仿、乙醇混溶,溶于丙酮,与甲醇不互溶甲醇理化性质编辑物理性质物态液体颜色透明,无色气味纯品清淡,类似乙醇;粗品刺激难闻熔点-98 °C(lit.)沸点64.5~64.7 °C(lit.)密度0.791 g/mL at 25 °C 闪点52 °F(约11°C)蒸气密度 1.11 (大气压=1)log P(辛醇/水分配系数)-0.69[4]蒸气压127 mm Hg(25°C)[5] 410 mm Hg(50°C)折射率n20/D 1.329(lit.)爆炸上限%(V/V):44.0 爆炸下限%(V/V): 5.5沾染量<10(APHA)水溶解性易溶储存条件室温水物理水通常是无色、无味的液体。
沸点:100℃(气压为一个标准大气压时)。
凝固点:0℃三相点:0.01℃最大相对密度时的温度:3.98℃比热容:4.186kJ/(kg·℃)0.1MPa 15℃蒸发潜热:2257.2kJ/(kg)0.1MPa 100℃title密度:1000 kg/m3(4℃时)。
丙酮的熔沸点

丙酮的熔沸点丙酮,化学名为丙酮,是一种常见的有机溶剂。
它的熔沸点是关于丙酮性质的重要物理性质之一,对于了解丙酮的性质和应用具有重要意义。
丙酮的熔沸点在不同的文献和参考资料中可能会有些许差异,但一般来说,丙酮的熔点约为-94°C,沸点约为56°C。
这个范围是在标准环境条件下(海平面、常温常压)得到的数值,因此在不同的环境下,丙酮的熔沸点也可能会有所不同。
丙酮的熔沸点与其分子结构和分子间相互作用有密切关系。
丙酮的分子式为C3H6O,其分子中含有一个羰基(C=O)基团。
这个羰基让丙酮具有了一定的极性,因此在分子间存在一定的氢键和偶极-偶极作用力。
这些相互作用力会影响丙酮的凝固和汽化过程,从而影响了其熔沸点。
在低温下,丙酮以分子固态存在,通过分子间力保持着固态晶格的结构。
当温度升高,丙酮分子间的作用力逐渐减弱,分子开始获得足够的热能,从而克服相互作用力,脱离固态结构,转变为液态。
这个转变点就是丙酮的熔点。
丙酮的熔沸点还受到外界环境的影响。
比如在高海拔山区,由于大气压力较低,会导致丙酮的沸点降低;而在高压环境下,丙酮的沸点会升高。
这是因为压力改变了分子之间的平衡态,从而影响了丙酮分子克服相互作用力所需的能量。
熔沸点的数据对于丙酮的应用和储存也具有重要意义。
例如,通过了解丙酮的沸点,我们可以根据需要调整工作温度来控制丙酮的汽化速率,从而满足实验或工业生产的要求。
另外,知道丙酮的熔点也可以帮助我们在储存和运输过程中避免或减少丙酮的损失和泄漏。
总结起来,丙酮作为一种重要的有机溶剂,其熔沸点是了解其性质和应用的关键物理性质之一。
了解丙酮的熔沸点可帮助我们更好地应用和操作丙酮,并确保其安全和高效使用。
乙醇和水中的zeta电位

乙醇和水中的zeta电位
【原创实用版】
目录
1.乙醇和水的性质
2.Zeta 电位的概念
3.乙醇和水中 Zeta 电位的区别
4.影响 Zeta 电位的因素
5.Zeta 电位在实际应用中的意义
正文
乙醇和水是两种常见的溶剂,它们在化学和生物学领域中有着广泛的应用。
在这两种溶剂中,Zeta 电位是一个重要的物理性质,它可以反映
出溶剂的电离程度和空间结构。
Zeta 电位是指在电场中,溶剂中带电粒子所受到的电势差。
它与溶
剂的酸碱性、离子强度、温度等因素密切相关。
在不同的溶剂中,Zeta 电位的数值和符号可能不同,这取决于溶剂的化学性质和溶液中的离子种类。
乙醇和水中的 Zeta 电位有很大的区别。
乙醇是一个非极性溶剂,它对离子的溶解度较小,因此乙醇中的 Zeta 电位通常较小。
水是一个极性溶剂,它可以溶解大量的离子,因此水中的 Zeta 电位通常较大。
影响 Zeta 电位的因素有很多,包括溶剂的极性、溶剂的酸碱性、溶液中的离子种类和浓度、温度等。
在实际应用中,Zeta 电位可以用来预
测溶液的稳定性和胶体颗粒的聚沉行为。
总之,乙醇和水中的 Zeta 电位有很大的区别,这主要是由于它们自身的性质和溶液中的离子种类不同所导致的。
第1页共1页。
