第十二章习题d区元素和f区元
无机化学ds区、d区和f区过度元素

上页 下页 目录 返回
● 酸碱性 过渡元素氧化物的水合物的酸碱性变化规律和主族相似 ,对同一元素而言,一般是低价显碱性,高价显酸性。 Mn(OH)2 弱碱;HMnO4 强酸(Φ=Z/r) ● 参与工业催化过程和酶催化过程的能力强 d 区元素较高的催化活性椐认为与电子容易失去,容易得 到,或容易由一种能级迁移至另一能级的事实有关;例如, V2O5催化 SO2 氧化的反应,可能涉及到 V(+5) 与V(+4) 氧 化态之间的转换: 1/2 O2 + 2 V(Ⅳ) = O 2- + 2 V(Ⅴ) +) SO2 + 2 V(Ⅴ) + O 2- = 2 V(Ⅳ) + SO3 1/2 O2 + SO2 = SO3
上页 下页 目录 返回
f 区元素的价层电子构型为(n-2)f0~14(n-1)d0~2ns2, 其特 征是随着核电荷的增加,电子依次填入外数第三层 (n-2)f 轨道,因而又统称内过渡元素。 f 区元素包括周期系中的镧系元素(原子序数57~71共 15种元素)和锕系元素(原子序数89~103共15种元素)。 镧系元素中只有钷是人工合成的,具有放射性。 锕系元素均有放射性,铀后元素为人工合成元素,称超 铀元素。
上页 下页 目录 返回
铬化合物毒性浅析 绝大多数三价铬化合物不溶于水,无毒、无害,但水 溶性无机三价铬盐极易在酸性环境下水解,形成的游离酸 对人体有剌激作用。 六价铬毒性主要是由于强氧化性对有机体的腐蚀与破坏, 可以通过吸入、接触、口服造成人体中毒。吸入六价铬将 引起呼吸道感染,粘膜溃疡,甚至鼻穿孔;皮肤接触六价 铬可能引发皮炎,伤口若接触六价铬将出现铬疮;口服大 剂量六价铬化合物将引起消化系统腐烂,出现肾损伤。流 行病学研究证实,长期暴露在高浓度六价铬的气雾中的工 人,呼吸系统癌症(主要是肺癌)发病率高于平均值,其 潜伏期超过15年。
元素周期表的基本结构和特点

元素周期表的基本结构和特点一、元素周期表的起源和发展•1869年,门捷列夫发现了元素周期律,并编制出第一个元素周期表。
•随着化学元素的不断发现和核反应技术的进步,周期表逐渐完善和扩展。
二、元素周期表的基本结构•横行称为周期,竖列称为族。
•周期表共有7个周期,从第1周期到第7周期。
•周期表共有18个族,包括7个主族、7个副族、1个0族和1个第Ⅷ族。
三、周期表的排列规律•周期表中,元素的原子序数依次增加。
•周期表中,同一周期的元素电子层数相同,同一族的元素最外层电子数相同。
四、元素周期表的特点•周期表反映了元素的原子结构与元素性质之间的关系。
•周期表中,周期与周期的交界处往往是一些特殊元素的所在,如超铀元素。
•周期表中,族与族之间的过渡元素往往具有相似的化学性质。
五、元素周期表的应用•周期表是化学领域的重要工具,可以查找到元素的物理和化学性质。
•周期表有助于预测和解释新元素的发现及其可能的性质。
•周期表为化学教育和研究提供了系统的分类和归纳方式。
六、元素的命名和符号•元素以化学符号表示,符号通常由一个或两个字母组成。
•元素符号的第一个字母大写,第二个字母小写。
•元素名称通常以英文表示,也有一些元素的名称来源于其他语言。
七、周期表的拓展•周期表还包括了一些具有特定性质的元素,如过渡元素、镧系元素和锕系元素。
•周期表的研究还涉及到同位素、元素周期律的微观解释等方面。
以上是关于元素周期表的基本结构和特点的知识点介绍,希望对你有所帮助。
习题及方法:1.习题:元素周期表中有多少个周期?解题方法:回顾元素周期表的基本结构,周期表共有7个周期。
答案:7个周期。
2.习题:元素周期表中有多少个族?解题方法:根据元素周期表的基本结构,周期表共有18个族。
答案:18个族。
3.习题:请列举出周期表中的7个主族。
解题方法:根据元素周期表的基本结构,主族元素位于周期表的左侧。
答案:第1主族(碱金属族)、第2主族(碱土金属族)、第3主族(硼族)、第4主族(碳族)、第5主族(氮族)、第6主族(氧族)、第7主族(卤素族)。
高中《无机化学》第十六至十八章测试题及答案

高中《无机化学》第十六至十八章测试题及答案(d区元素、f区元素)(总9页)-本页仅作为预览文档封面,使用时请删除本页-高中《无机化学》第十六至十八章测试题及答案(d区元素、f区元素)第十六章 d区元素(一)一、填空题1、在所有过渡元素中,熔点最高的金属是 W ,熔点最低的是 Hg ,硬度最大的是 Cr ,密度最大的是 Os ,导电性最好的是 Ag ,耐海水腐蚀的是Ti 。
2、分别写出下列离子的颜色:[Fe(H2O)6]2+淡绿色,FeO42-紫色,[FeCl4]-黄色,[Fe(H2O)6]3+淡紫色,[Ti(H2O)6]3+紫色,VO43-淡黄色,[Co(H2O)6]2+粉红色,[Mn(H2O)6]2+粉红色,[Ni(H2O)6]2+绿色。
3、CrCl3溶液与氨水反应生成灰绿色的 Cr(OH)3沉淀该产物与NaOH溶液反应生成亮绿色的 Cr(OH)4-。
4、锰在自然界主要以软锰矿的形式存在,在强氧化剂(如KClO3)作用下碱熔时只能得到 +6 价锰的化合物,而得不到高锰酸盐,这是因为后者在碱中和受热均分解。
5、K2Cr2O7(s)与浓H2SO4反应生成的氧化物为 CrO3,它为橙红色,遇酒精立即着火,生成铬的一种绿色氧化物,其化学式为 Cr2O3。
KMnO4(s)与浓H2SO4作用生成的氧化物为 Mn2O7;MnO2与浓H2SO4反应生成的气体是O2。
6、高锰酸钾是强氧化剂,它在酸性溶液中与H2O2反应的主要产物是 O2和 Mn2+,它在中性或弱碱性溶液中与Na2SO3反应的主要产物为 SO42-和MnO2。
7、在强碱性条件下,KMnO4溶液与MnO2反应生成绿色的 K2MnO4;在该产物中加入硫酸后生成紫色的 KMnO4和褐色的 MnO2。
8、三氯化铁蒸气中含有的聚合分子化学式为 Fe2Cl6,其结构与金属 Al 的氯化物相似。
FeCl3能溶于有机溶剂。
9、既可用于鉴定Fe3+,又可用于鉴定Co2+的试剂是 KCNS ,当Fe3+存在时,能干扰Co2+的鉴定,可加入 NaF 因生成 FeF63-而将Fe3+掩蔽起来,消除对Co2+鉴定的干扰。
第12-16章 p区元素习题

第12-16章P区元素习题目录一判断题;二选择题;三填空题;四完成方程式;五计算并回答问题一判断题 (返回目录)1 硼在自然界主要以含氧化合物的形式存在。
()2 在硼与氢形成的一系列共价型氢化物中,最简单的是BH3。
()3 硼酸是三元酸。
()4 硼是非金属元素,但它的电负性比氢小。
()5 由于B-O键键能大,所以硼的含氧化合物很稳定。
()6 硼砂的化学式为Na2B2O7。
()7 B2H6为平面形分子。
()8 硼是缺电子原子,在乙硼烷中含有配位键。
()9 三卤化硼熔点的高低次序为BF3<BCl3<BBr3<BI3。
()10 三卤化硼沸点的高低次序为BF3>BCl3>BBr3>BI3。
()11 地壳中丰度最大的金属元素是铝。
()12 Al2O3是两性氧化物,因而各种晶型的Al2O3既可溶于酸,又可溶于碱。
()13 只有在强酸性溶液中才有Al(H2O)63+存在。
()14 在气相中三氯化铝以双聚分子Al2Cl6的形式存在。
()15 AlX3都是共价型化合物。
()16 KAl(SO4)2·12H2O与KCr(SO4)2·12H2O属于同分异构体。
()17 在氯化氢气流中加热金属铝可制得无水AlCl3。
()19 因AlCl3分子中Al为缺电子原子,所以AlCl3中有多中心键。
()20 碳酸盐的溶解度均比酸式碳酸盐的溶解度小。
()21 Na2CO3比NaHCO3的溶解度大,同理,CaCO3比Ca(HCO3)2的溶解度也大。
()22 硅在地壳中的含量仅次于氧。
()23 分子筛是人工合成的硅铝酸盐,具有吸附和催化作用。
()24 活性炭具有吸附作用,它是颗粒状的石墨。
()25 金刚石比石墨更稳定,即使在纯氧气中,金刚石也不能燃烧。
()26 一般情况下,CO2不能助燃,但是镁在二氧化碳气体中能燃烧。
()27 高纯度的硅和锗是良好的半导体。
()28 金刚石与石墨是同素异形体,由金刚石转变为石墨的△r H>0。
精品:2015届高考化学大一轮课件:12-37原子结构与性质

(2)电离能:气态电中性基态原子失去一个电子转化为气 态基态正离子所需要的最低能量叫做第一电离能(用I1表示), 一价气态基态正离子再失去一个电子所需消耗的最低能量叫 做第二电离能(用I2表示),依此类推,可得到I3、I4„„同一 种元素的逐级电离能的大小关系为I1<I2<I3<I4<„„即一 个原子的逐级电离能是逐渐增大的。这是因为随着电子的逐 个失去,阳离子所带的正电荷数越来越大,再要失去一个电 子需克服的电性引力也越来越大,消耗的能量也越来越多。
特别提醒
确定某个原子轨道需能层、能级、伸展方向
三个方面,而确定某个电子运动状态需能层、能级、伸展方 向、自旋状态四个方面。
助学微博
三个要点 原子结构“三、二、一”要点 三个原理:核外电子排布三个原理——能量最低原理、 泡利原理、洪特规则 两个图式:核外电子排布两个表示方法——电子排布 式、电子排布图 一个顺序:核外电子排布顺序——构造原理
3.基态原子核外电子排布式书写应遵循的规律 4 基态原子核外电子排布式的书写要考虑□
泡利不相容原理 洪特规则 能量最低原理 5 ___________________ 6 __________ ______________、□ 、□
等多方面因素。
“能量相同的原子轨道在全满(如p6,d10)、半满(如p3, d5)和全空(p0,d0)状态时,体系的能量最低”,这一点违反 了洪特规则,可看成是洪特规则的特例。如:24Cr的电子排 布式:1s22s22p63s23p63d54s1(3d5、4s1均为半充满状态);29Cu 的电子排布式:1s22s22p63s23p63d104s1(3d10为全充满状态, 4s1为半充满状态)。
(2)核外电子排布与族的划分:族的划分与原子的价电子 数和价电子排布有关。
d,f区元素

12.1.1 d区元素的特殊性
d区元素显示出许多区别于主族元素的性质:
• 熔沸点高、硬度密度大的金属大都集中在这一区 • 同一周期从左到右,元素化学性质的变化远不如s区p区
显著。
• 不少元素形成有颜色的化合物 • 许多元素形成多种氧化态从而导致丰富的氧化还原行为 • 形成配合物的能力比较强 ,参与工业催化过程和酶催
化过程的能力强
12.2 钒
• 钒的价电子层结构为3d34s2,5个电子都有成键作用,所以 • 在酸性介质中,钒的元素电势图为
A / V
VO2+ 主要氧化态为+5,但也存在+4,+3,+2。
-0.25 -1.2 1.0 VO2+ 0.36 V3+ V2+ V -0.25
所以V2+、V3+具有还原性,VO2+是稳定的,而VO2+具有氧化 性。 不同的氧化态的钒具有不同的颜色。例如: VO2+(黄色)可 被Fe2+、H2C2O4等还原为VO2+(蓝色)
[Cr(H2O)6]Cl3 紫色
[Cr(H2O)5Cl]Cl2· H2O 浅绿 [Cr(H2O)4Cl2]Cl· 2H2O 深绿
2. Cr(VI)的化合物
Cr(VI)的化合物通常是由自然界存在的铬铁矿Fe(CrO2)2,
借助于碱熔法制得的,即把铬铁矿和Na2CO3混合,并在空 气中煅烧。用水浸取煅烧后的熔体,Na2CrO4进入水中,浓 缩,得黄色晶体Na2CrO4;酸化得红色晶体。 4Fe(CrO2)2 + 8Na2CO3 + 7O2 8Na2CrO4 + 2Fe2O3 + 8CO2
电子分别填充在3d 亚层4d 亚层和5d 亚层上.
ds区,d区和f区元素

子构型具有接受配位体孤对电子的条件,因此它
们容易形成配合物,一般容易形成氟配合物、氰 配合物和氨配合物。 此外,过渡元素氧化物水合物的酸碱变化规律 和主族元素相似。对同种元素而言,低价的显碱
性,高价的显酸性。注意p304列出的ⅢB-ⅦB族过
渡元素最高价态氧化物水合物的酸碱性。
8.2 铜族和锌族元素的化合物 8.2.1 通性
3. 锌配合物 Zn2+和氨水、KCN等能形成无色的四配位离子: [Zn(NH3)4]2+、[Zn(CN)4]2-、[Zn(CN)4]2-用于电镀中 4. 汞配合物 Hg(I)形成配合物倾向较小。 Hg(II)易和CN-、SCN-、Cl-、Br-、I-离子均生成 [ML4]2-配离子。
Hg2++2I-→HgI2↓(红色)+2I-→[HgI4]2[HgI4]2-与碱混合后叫奈氏试剂,用于鉴定NH4+、
3. 形成配合物(Zn2+,Al3+的分离)
Zn 2 Al3
2 NH 3O H
Zn(OH ) 2 Al(OH ) 3
2 NH 3O H
[ Zn( NH 3 ) 4 ] 2 (白色) Al(OH )(白色) 3
8.2.3 重要的盐类 1. 几种常用的盐 硫酸铜、硝酸银、氯化汞、氯化亚汞(p306-308自 己看书,了解基本性质和用途) 2. Cu2+和Cu+的相互转化 从Cu(I)结构(3d10)看,Cu(I)是稳定的,如自然 界中有Cu2O和Cu2S的矿物存在。但在水溶液中Cu+ 易歧化,这是由于Cu2+的电荷比Cu+多,半径又小, 所以Cu2+的水合焓(-2100kJ· -1)比Cu+的(-593 mol kJ· -1)代数值小得多,∴水溶液中Cu2+比Cu+稳)4)]2+、[CuCl4]2-、[Cu(NH3)4]2+等,
无机课后习题答案12-17、20

3Cu+8HNO3(稀)==3Cu(NO3)2+2NO+4H2O (4)实验室制备 NO2 的反应为: Cu+4HNO3==Cu(NO3)2+2NO2+2H2O
12.3 解:N2 分子中氮氮三键键能很大,不易参加反应;而 NH3 分子中的 N—H 键则键能较小,易 断裂参加反应,故常作为制备含氮化合物的原料。
市售硝酸的百分比浓度为:68%;密度为:1.4g/cm-3;;体积摩尔浓度为:15.1mol/cm-3。市售 磷酸的百分比浓度为:85%密度为 1.6g/cm-3; 体积摩尔浓度为:13.9mol/cm-3。 12.25 解:向 SbCl5 溶液中通入 H2S 时,伴随 Sb2S5 的生成,溶液的酸度提高,Sb5+氧化能力提高而 与 H2S 发生氧化还原反应,有 Sb2S3 和 S 沉淀生成。 2Sb5++5H2S==Sb2S5+10H+ 2Sb5++5H2S==Sb2S3+2S+10H+ 若制较纯的 Sb2S5,应在碱性条件下先得到 SbS43-,再小心加入稀酸即可。 2Sb5++5S2-==Sb2S5 Sb2S5+3S2-==2SbS432SbS43-+6H+==Sb2S5+3H2S 12.26 解:Sb2S3 是两性氧化物,故可以和碱性氧化物反应。反应方程式为: 3Na2S+Sb2S3==2Na3SbS5 而 Bi2S3 没有酸性,不溶于碱金属硫化物中。 Sb2S3 具有还原性,它们可以和具有氧化性的多硫化物反应生成硫代锑酸盐,方程式为: Sb2S3+(NH4)2S2==(NH4)2SbS4 由于 Bi2S3 中 Bi(III)的还原性极若,故不和多硫化物反应。 12.27 解:并不矛盾。碱性条件下:E(AsO43-/AsO2-)=-0.68V,E(I2/I-)=0.5355V,故碘单质可以
医学遗传学习题附答案第12章免疫遗传学

医学遗传学习题附答案第12章免疫遗传学第⼗⼆章免疫遗传学(⼀)选择题(A型选择题)1决定个体为分泌型ABC抗原者的基因型是__________ 。
A. i/i B . I B/I B C . Se/se D |. se/se E . I A/I B 2?孟买型个体的产⽣是因为基因为⽆效基因。
A. I A B .I B C . i D . Se E .H3 . Rh⾎型的特点是_______ 。
A.具有天然抗体 B ■⽆天然抗体 C .具有8种抗体D.具有3种抗体E .由3个基因编码。
4 . Rh溶⾎病很少发⽣于第⼀胎的原因是________ 。
A. Rh阳性的胎⼉⾎细胞不能进⼊母体C. 母体具有⾜量的抗体,但不能进⼊胎⼉内D. 胎⼉组织能够吸收母体的抗体E. 以上都不是5 . HLA-A HLA-B和HLA-C编码⼀类抗原的重链,⽽轻链则由________ 编码A. HLA-E B . HLA-F C . HLA-GD. B 2微球蛋⽩基因 E . HLA-H类基因6 . HLA-L、HLA-H HLA-J和HLA-X这些基因均因突变⽽⽆表达产物,它们被称为。
A.假基因 B .⾮经典基因 C . MIC基因D.补体基因 E .肿瘤坏死因⼦基因7.在同⼀染⾊体上HLA各座位等位基因紧密连锁, 完整传递,这种组成称为A.单倍体 B .单倍型.单体型D.单⼀型 E .单位点8.同胞之间HLA完全相同的可能性是_________9 .⽗⼦之间HLA 完全相同的可能性是10 .与⽆丙种球蛋⽩⾎症疾病相关的基因是D.缺乏丫球蛋⽩ E .细胞免疫缺陷14 . HLA 复合体所不具有特点是E.是与疾病关联最为密切的⼀个区域15 . HLA- I 类基因区中的经典基因包含D. 5组基因 E . 617. I A 基因的编码产物为是A. D-半乳糖转移酶B. L-岩藻糖转移酶C. 胸苷激酶D.乳糖转移酶E. | N-⼄酰半乳糖胺转移酶18. Rh 阳性个体既有RHD 基因,也有RHCE S 因,⽽Rh 阴性个体仅有 _________ 。
第四版无机化学习题及答案

第一章原子结构和原子周期系1-1根据原子序数给出下列元素的基态原子的核外电子组态:(a)K (b)Al (c)Cl (d)Ti(Z=22)(e)Zn(Z=30)(f)As(Z=33)答:(a)[Ar]4s1(b)[Ne]3s23p1(c)[Ne]3s23p5(d)[Ar]3d54s2(e)[Ar] 3d104s1(f)[Ar]4s24p3 1-2给出下列原子或离子的价电子层电子组态,并用方框图表示轨道,填入轨道的电子用箭头表示。
(a)Be (b)N (c)F (d)Cl-(e)Ne+(f)Fe3+(g)As3+1-3 Li+、Na+、K+、Rb+、Cs+的基态的最外层电子组态与次外层电子组态分别如何1-4以下+3价离子那些具有8电子外壳Al3+、Ga3+、Bi3+、Mn3+、Sc3+答:Al3+和Sc3+具有8电子外壳。
1-5已知电中性的基态原子的价电子层电子组态分别为:(a)3s23p5(b)3d64s2(c)5s2(d)4f96s2(e)5d106s1试根据这个信息确定它们在周期表中属于那个区、哪个族、哪个周期。
答:(a)p区,ⅦA族,第三周期(b)d区,Ⅷ族,第四周期(c)s区,ⅡA族,第五周期(d)f区,ⅢB族,第六周期(e)ds区,ⅠB族,第六周期1-6根据Ti、Ge、Ag、Rb、Ne在周期表中的位置,推出它们的基态原子的电子组态。
答:Ti位于第四周期ⅣB族,它的基态原子的电子组态为[Ar]3d24s2;Ge位于第四周期ⅣA族,它的基态原子的电子组态为[Ar]3d104s24p2;Ag位于第五周期ⅠB族,它的基态原子的电子组态为[Kr] 4d105s1;Rb位于第五周期ⅠA族,它的基态原子的电子组态为[Kr] 5s1;Ne位于第二周期0族,它的基态原子的电子组态为[He] 2s22p6。
1-7某元素的基态价层电子构型为5d36s2,给出比该元素的原子序数小4的元素的基态原子电子组态。
答:该元素的基态原子电子组态为[Xe] 4f126s2。
d区元素和f区元素

第12章d区元素和f区元素【12-1】试用d区元素价电子层结构的特点来说明d区元素的特性。
解:d 区元素最后一个电子填充到d 轨道上,其价层电子组态为:(n-1)d1-8ns1-2,位于周期表的中部,包括ⅢB -ⅦB和Ⅷ族元素,它们都是过渡元素,每个元素都有多种氧化值。
同周期过渡元素的原子半径随着原子序数的增加而缓慢地依次减小,到了第Ⅷ族元素后又缓慢增大。
同族过渡元素的原子半径,除了ⅢB外,自上而下随着原子序数的增大而增大。
各过渡系元素电离能随原子序数的增大,总的变化趋势是逐渐增大的。
同副族过渡元素的电离能递变不很规则。
熔点、沸点高, 密度大, 导电性、导热性、延展性好。
在化学性质方面,第一过渡系元素的单质比第二、三过渡系元素的单质活泼。
化学性质变化总趋势是同一过渡系单质的活泼性从左到右降低。
或:d 区元素价电子层结构是(n-1)d1-8ns1-2。
它们ns轨道上的电子数几乎保持不变,主要差别在于(n-1)d 轨道上的电子数不同。
又因(n-1)d轨道和ns轨道的能量相近,d电子可以全部或部分参与成键,由此构成了d区元素的一些特性:全部是金属,原子半径小,密度大,熔、沸点高,有良好的导热、导电性能,化学性质相近。
大多具有可变的氧化态。
由于d轨道有未成对电子,水合离子一般具有颜色。
由于所带电荷高,离子半径小,且往往具有未充满的d电子轨道,所以容易形成配合物。
【12-2】完成下列反应式:(1)TiO2+H2SO4(浓)→(2)TiO2++Zn+H+→(3)TiO2+C+Cl2→(4)V2O5+NaOH→(5)V2O5+H2SO4→(6)V2O5+HCl→(7)VO2++H2C2O4+H+→解:(1)TiO2 + H2SO4 (浓) = TiOSO4 + H2O(2)2TiO2+ + Zn + 4 H+ = 2 Ti3+ + Zn2+ +2 H2O(3)TiO2 + 2 C + 2 Cl2 (加热) = TiCl4 + 2 CO(4)V2O5 + 6 NaOH = 2 Na3VO4 + 3 H2O(5)V2O5 + H2SO4 = (VO2)2SO4 + H2O(6)V2O5 + 6 HCl = 2 VOCl2 + Cl2 + 3 H2O(7)2VO+ + H2C2O4 + 2 H+ = 2VO2+ + 2CO2 +2H2O【12-3】在酸性溶液中钒的电势图为已知φθ(Zn2+/Zn)=-0.76V, φθ(Sn2+/Sn)=-0.14V, φθ(Fe3+/Fe2+)=0.77V。
无机化学习题----d区元素

10 分 (4602) 根据下列实验写出有关的反应式: (1) 将装有TiCl4 的瓶塞打开立即冒出白烟; (2) 向TiCl4溶液中加入浓HCl和金属锌时生成紫色溶液; (3) 向(2)的紫色溶液中慢慢加入 NaOH 至溶液呈碱性,出现紫色沉淀; (4) 先用HNO3处理沉淀,使其溶解,然后用稀碱溶液处理,生成白色沉淀; (5) 将白色沉淀过滤并灼烧,再与等物质的量的 MgO 共熔。
5 分 (4638) 某绿色固体A 可溶于水,水溶液中通入CO2即得棕黑色固体B和紫红色溶液C。B与浓HCl 溶液共热时得黄绿色气体D和近乎无色溶液E。将此溶液和溶液C混合即得沉淀B。将气体D 通入 A 的溶液,可得 C。试判断 A、B、C、D、E 各为何物?
10 分 (4684) 现有一种钛的化合物A ,它是无色液体,在空气中迅即冒白“烟”,其水溶液和金属锌 反应,生成紫色溶液B,加入NaOH至溶液呈现碱性后,产生紫色沉淀C,过滤后,沉淀C用 稀HNO3处理,得无色溶液D。将D逐滴加入沸腾的热水中得白色沉淀E,将E过滤灼烧后, 再与BaCO3共熔,得一种压电性晶体F。试写出各步化学反应式并鉴别A 、B、C、D、E、F 各为何种物质?
10 分 (7629) 某金属M溶于稀盐酸生成MCl2,其磁矩测定为 5.0 B.M.,在隔绝空气无氧下操作,加入 NaOH溶液生成白色沉淀A。A 接触空气,白色沉淀迅速转变为绿色,之后又转变为棕色沉 淀B;灼烧B得到红棕色粉末C;C经不彻底还原,得黑色的磁性物质D;B溶于稀盐酸生成 溶液E,E可使KI-淀粉溶液氧化生成碘,但如果在KI-淀粉溶液加入前加入NaF则无I2生成; 若向B的浓NaOH悬浊液中通入氯气,可得紫红色溶液F,向溶液F中加入BaCl2可得红棕色固 体G, G是一种很强的氧化剂。请问A —G各是何物? 写出有关反应式。
元素周期律习题

原子结构和元素周期律练习题一、选择题1、已知某元素+3价离子的电子排布式为1s 22s 22p 63s 23p 63d 5,该元素在周期表中属于(C )。
(A )VB 族 (B )Ⅲ族 (C )ⅧB 族 (D )VA 族2、下列哪种元素具有最强的电子亲和能( C )。
(A )P (B )S (C )Cl (D )He (E )Ne3、在下列原子中,第一电子亲和能最大的是( D )。
(A )N (B )O (C )P (D )S4、在下列原子中,第一电离能最小的是( C )。
(A )B (B )C (C )Al (D )Si5、下列四种电子构型的元素中,其+2离子状态在水溶液中呈无色的是( D )。
(A )2、8、18、1 (B )2、8、14、2(B )2、8、16、2 (D )2、8、18、26、已知多电子原子中,下列各电子具有如下量子数,其中能量最高的电子应是( D )。
(A )(2,1,1,-21) (B )(2,1,0,-21) (C )(3,1,1,-21) (D )(3,2,-2,-21) 7、下列用来表示核外某电子运动状态的各组量子数(n ,l 、m 、m s )中,合理的是( A )。
(A )(2,1,-1,-21) (B )(0,0,0,21) (C )(3,1,2,+21) (D )(2,1,0,0)(E )(1,2,0,+21) 8、氧原子一个2p 电子可以被描述为下列六组量子数之一,试指出氧原子四个电子组合中正确的有( AC )。
①(2,1,0,+21)②(2,1,0,-21)③(2,1,1,+21) ④(2,1,1,-21)⑤(2,1,-1,+21)⑥(2,1,-1,-21) (A )①②③⑤ (B )①②⑤⑥(C )②④⑤⑥ (D )③④⑤⑥9、在下列所示的电子排布中,哪些是激发态的原子(BC ),哪些是不存在的( E )。
(A )1s 22s 22p 6 (B )1s 22s 23s 1 (C )1s 22s 14d 1(D )1s 22s 22p 63s 1 (E )1s 22s 22p 52d 13s 110、甲、乙两元素,甲原子的M 层和N 层的电子数分别比乙原子的M 层和N 层的电子数少7个和4个。
f区元素
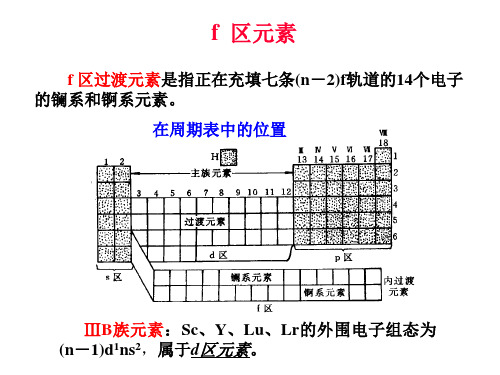
f 区过渡元素是指正在充填七条(n-2)f轨道的14个电子 的镧系和锕系元素。 f 区元素在周期表中的位置如图所示:
ⅢB族元素:Sc、Y、Lu、Lr的外围电子组态为 (n-1)d1ns2,属于d区元素。
镧系元素和锕系元素
习惯上所称的镧系元素是指从 57 La-71Lu的15个元素, 以Ln表示。本来镧系元素并不包括Lu(镥), 将它归在一起 是因Lu与其前面的从 57La到 70Yb(镱)的14个填充4f轨道电 子的元素的性质非常相似。 同样,Lr(铑)与其前面的89Ac到102No(锘)的14个填 充5f轨道电子的元素性质也非常相似,因而在习惯上也把从 89Ac到103Lr的15个元素统称为锕系元素,记作An,按理锕系 元素并不包括Lr。
而呈现+2氧化态。显然镧系离子在氧化态变化的 周期性规律正是镧系元素电子层排布呈现周期性规 律的反映。
镧系元素的光学性质
镧系离子的颜色来源于: ① 荷移跃迁 电荷从配体的分子轨道向金属离子空轨道跃迁 。其光谱的谱带具有较大的强度和较短的波长,且受配体及金 属离子的氧化还原性所影响。 ② f-d(u→g)跃迁 光谱选律所允许的跃迁。因而谱线强度 大,一般出现在紫外区,其中+2价离子也可能出现在可见区。 ③ f-f(u→u)跃迁 光谱选律所禁阻的跃迁。然而, 由于中心 离子与配体的电子振动偶合、晶格振动和旋-轨偶合使禁阻产 生松动,从而使f-f跃迁得以实现。 可以发现: 除La3+和Lu3+的4f亚层为全空或全满外,其余+3 价离子的4f电子都可以在7条4f轨道之间任意配布,从而产生多 种多样的电子能级,这种能级不但比主族元素多,而且也比d区 过渡元素多,因此,+3价镧系元素离子可以吸收从紫外、可见 到红外光区的各种波长的辐射。据报导,具有未充满f电子轨道 的原子或离子的光谱约有3万条可以观察到的谱线。
高中化学(新人教版)选择性必修二课后习题:原子结构与元素周期表(课后习题)【含答案及解析】

原子结构与元素的性质原子结构与元素周期表课后篇素养形成必备知识基础练1.硒(34Se)是人体必需的微量元素,适当摄入能有效提高人体免疫机能并能预防癌症和心脑血管疾病。
下列有关硒元素的说法不正确的是()A.Se元素处于元素周期表的第15列B.Se原子的价层电子排布式为4s24p4C.Se元素处于元素周期表中的p区D.基态Se原子的核外电子排布中共有8个能级元素原子核外有34个电子,处于元素周期表中第16列,与O元素处于同一主族。
Se元素的基态原子的电子排布式为1s22s22p63s23p63d104s24p4,共有8个能级,其价电子排布式为4s24p4,处于元素周期表的p区。
2.下列说法正确的是()A.所有金属元素都分布在d区和ds区B.最外层电子数为2的元素都分布在s区C.元素周期表中第ⅢB族到第ⅡB族10个纵列的元素都是金属元素D.s区均为金属元素区除H外均为金属元素,故A、D两项错误;He、Zn等虽然最外层电子数为2,却不是s区元素,B项错误;元素周期表中第ⅢB族~第ⅡB族为过渡元素,全部为金属元素,C项正确。
3.电子排布式为[Ar]3d54s2的元素是()A.稀有气体元素B.过渡元素C.主族元素D.卤族元素p能级上填充有电子且未满时,一定为主族元素;最外能层p能级上未填充电子,而在次外层d(或次次外层f)能级上填充有电子的元素,一定是过渡元素。
故电子排布式为[Ar]3d54s2的元素为过渡元素。
4.下列说法正确的是()A.最外层电子排布为n s2的基态原子对应的元素一定位于第ⅡA族B.最外层电子排布为n s1的基态原子对应的元素一定属于金属元素C.p区元素的原子p能级中一定都有电子D.基态原子价层电子排布为n s n n p n的元素一定是非金属元素n s2的基态原子可能是氦元素,也可能是过渡元素,不一定是第ⅡA族元素,A 项错;最外层电子排布为n s1的基态原子不一定是金属元素,如H元素不是金属元素,除氢元素外,其他最外层电子排布为n s1的基态原子对应的元素都是金属元素,B项错;p区元素中的He原子最外层电子排布为1s2,故C项错误;最外层电子排布符合n s n n p n的元素只有n=2这一种情况,n=2时,该元素的价层电子排布式为2s22p2,是碳元素,属于非金属元素,D项正确。
武汉大学版无机化学课后习题答案(第三版)第17章d区元素

D区元素〔1〕1.钛的主要矿物是什么?简述从钛铁矿制取钛白得反响原理。
解:钛的主要矿物有钛铁矿FeTiO2反响原理:FeTiO3 + 2H2SO4 = TiOSO4 + FeSO4 + 2H2OTiOSO4 + 2H2O =TiO2•H2O↓ + H2SO4TiO2•H2O = TiO2 + H2O2.解释TiCl3和[Ti(O2)OH(H2O)4]+ 有色得原因。
解:TiCl3显色是因为产生了电核跃迁,[Ti(O2)OH(H2O)4]+有色是因为O22-离子变形性较强,d—d跃迁所引起。
3.完成并配平以下反响方程式。
(1)Ti + HF →(2)TiO2 + H2SO4→(3)TiCl4 + H2O →(4)FeTiO3 + H2SO4→(5)TiO2 + BaCO3→(6)TiO2 + C + Cl2→解:(1) Ti + 5HF = H2TiF6 + 2H2↑(2)TiO2 + H2SO4 = TiOSO4 + H2O(3)TiCl4 + 2H2O = TiO2 + 4HCl(4)FeTiO3 + 2H2SO4 = TiOSO4 + FeSO4 + 2H2O(5)TiO2+ BaCO3 = BaTiO3 + CO2↑(6)TiO2 + 2C + 2Cl2 = TiCl4+ 2CO↑4.完成以下反响(1)TiI4在真空中强热;(2)FeTiO3和碳得混合物在氯气中加热;(3)向含有TiCl-2得水溶液参加过量得氨;6(4) 向VCl 3的水溶液参加过量的氨;(5) 将VCl 2的固体加到HgCl 2水溶液中。
解:(1) TiI 4 = Ti + 2I 2(2) 2FeTiO 3 + 6C + 5Cl 2 = 2FeCl 3 + 2TiCl 4 + 6CO(3) TiCl 62- + NH 3 = [Ti(NH 3)6]4+ + 6Cl -(4) VCl 3 + Na 2SO 3 =(5) VCl 2 + HgCl 2=5. 根据以下实验写出有关的反响方程式:将一瓶TiCl 4翻开瓶塞时立即冒白烟。
第20、21章d区元素习题

第20、21章d区元素习题目录一判断题;二选择题;三填空题;四完成反应方程式;五计算和回答问题一判断题返回目录1 所谓内过渡元素指的是d区元素。
()2 第一过渡系元素是指第四周期的过渡元素。
()3 第二过渡系元素是指第五周期的过渡元素。
()4 第三过渡系元素是指第六周期的过渡元素。
()5 第Ⅷ族过渡元素属于内过渡元素。
()6 Zr与Hf性质相似是由惰性电子对效应造成的。
()7 钼是我国的丰产元素之一。
()8 钨是我国的丰产元素,储量为世界首位。
()9 Fe3+和Cr3+的硫酸盐都可形成矾。
()10 d区元素全都是重金属。
()11 一般说来,同一族过渡元素的原子半径随原子序数的增加而增大。
()12 同一周期副族元素的原子半径随着原子序数的增加而依次减小。
()13 过渡元素都是金属元素,也称作过渡金属。
()14 在过渡元素中化学性质最活泼的是钪副族。
()15 多数过渡元素都可以形成多种氧化值的化合物。
()16 第一过渡系元素的第一电离能随原子序数的增大而依次减小。
()17 MnO4-具有颜色是由于发生电荷迁移而造成的。
()18 CrO42-具有颜色是由于产生d-d跃迁而造成的。
()19 中心离子电子构型为d1~d9的配离子大多具有颜色。
()20 中心离子电子构型为d0或d10的配离子大多是无色的。
()21 过渡元素的许多水合离子和配合物呈现颜色,其原因多是发生d-d跃迁而造成的。
()22 在所有金属羰合物中,金属元素的氧化值都是零。
()23 金属羰基配合物受热易分解为金属和一氧化碳。
()24 ds区元素原子的次外层都有10个d电子。
()25 在d区元素中以ⅢB族元素最活泼。
()26 许多过渡元素的化合物因具有未成对电子而呈现顺磁性。
()27 许多过渡金属及其化合物具有催化性能。
()28 第一过渡系元素比相应的第二、三过渡系元素活泼。
()29 第一过渡系元素中,从Sc到Mn,元素的最高氧化值等于其族序数。
原子结构

二、基态电子运动状态数的表示
电子运动状态数的取值
n L 1 0 0 2 1 m 0 0 0,+1,-1 轨道 1s 2s 2PX ,2PY ,2PZ 3s 3PX ,3PY ,3PZ 3d的五个轨道 4s 4Px ,4Py ,4Pz 4d的五个轨道 4f的七个轨道 ms ± 1/2 ± 1/2 轨道数 (n2) 1 4 电子数 (2n2) 2 8
原子核外的电子排布又称为电子组 态。基态原子核外电子排布遵守Pauli不相 容原理、能量最低原理和Hund 规则。
(一)Pauli不相容原理:
在一个原子中,不可能存在四个量子数完 全相同的两个电子,即每个原子轨道中最多只 能容纳自旋相反的两个电子,称为Pauli不相容 原理。 根据Pauli不相容原理可以知道,各电子层 最多能容纳的电子数为2n2 ,各亚层最多可容 纳的电子数为 2(2l + 1)个,即 s、p、d、f 各 亚层的电子数分别为 2、 6、10、14 。
HAtO4 At2O7
At
元素最高价氧化物对应水化物的酸碱性
酸性逐渐增强
H
碱 性 逐 渐 增 强 酸 性 逐 渐 增 强
Li
Be
B
C
N
O
F
Na
K Rb Cs
Mg
Ca Sr Ba
Al
Ga In Tl
Si
Ge Sn Pb
P
As Sb Bi
S
Se Te Po
Cl
Br I At
碱性逐渐增强
元素气态氢化物的热稳定性
S、p区的为主族元素(除零族),其族序数为最外层电子数,即最外能层 中s.p能级上电子数之和。
科学史话:
第一张元素周期表
1829年德国化学家德贝菜纳发现当时已知的44种元素中有15种元素可分成5组, 每组的三个元素性质相似,而且中间元素的相对原子质量约为较轻和较重的两个 元素相对原子质量之和的一半。例如,钙、锶、钡性质相似,锶的相对原子质量 大约是钙和钡的相对原子质量之和的一半。氯、溴、碘,锂、钠、钾等组元素的 情况类似,由此提出了“三素组”的概念,为发现元素性质的规律性打下了基 础。„„„„ 1859年,24罗的俄国彼得堡大学年轻讲师门捷列夫来到德国海德堡大学 本生的实验室进修。当年,本生和基尔霍夫发明了光谱仪,用光谱发现了一些新 元素,掀起一股发现新元素热。次年,门捷列夫出席了在化学史土具有里程碑意 义的德国卡尔斯鲁厄化学大会。门捷列夫回忆道: “我的周期律的决定性时刻 在1860年,我„„在会土我聆听了意大利化学家康尼查罗的演讲„„正是当时, 元素的性质随原子量(相对原子质量)递增而呈现周期性变化的基本思想冲击了我 。”此后, 门捷列夫为使他的思想信念转化为科学理论,作出了10年艰苦卓绝 的努力, 系统地研究了元素的性质,按照相对原子质量的大小,将元素排成序 ,终于发现了元素周期律。„„„„
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第十二章d区元素和f区元素
1.试用d区元素家电子层结构的特点来说明d区元素的特性。
2.完成下列反应式:
(1)TiO2+H2SO4(浓)→
(2)TiO2++Zn+H+→
(3)TiO2+C+Cl2→
(4)V2O5+NaOH→
(5)V2O5+H2SO4→
(6)V2O5+HCl→
(7)VO2++H2C2O4+H+→
3.在酸性溶液中钒的电势图为
已知φθ(Zn2+/Zn)=-0.76V, φθ(Sn2+/Sn)=-0.14V, φθ(Fe3+/Fe2+)=0.77V.问实现下列变化,各使用什么还原剂为宜?
(1)VO2+→V2+
(2) VO2+→V3+
(3)VO2+→VO2+
4.完成下列反应式:
(1)(NH4)2Cr2O7→
(2)Cr2O3+NaOH→
(3)Cr3++NH3·H2O→
(4)Cr(OH)4-+Br2+OH-→
(5)Cr2O72-+Pb2++H2O→
(6)MoO42-+NH4++PO43-+H+→
(7)Na2WO4+HCl→
5.BaCrO4和BaSO4的溶度积相近,为什么BaCrO4可溶于强酸,而BaSO4则不溶?
6.以K2Cr2O7为主要原料制备K2CrO4,CrCl3和Cr2O3,用方程式表示各步的反应。
7.试用热力学原理判断,(NH4)2Cr2O7的下列两种分解过程,哪种反应趋势更大?
(1)(NH4)2Cr2O7(s)=Cr2O3(s)+N2(g)+4H2O(g)
(2) (NH4)2Cr2O7(s)=2Cr2O3(s)+NH3(g)+H2O(g)
8.完成下列反应式:
−∆
(1)MnO2+KOH+KClO3−→
(2)MnO4-+H2O2+H+→
(3)MnO4-+NO2-+H2O→
(4)MnO4-+NO2-+OH-→
(5)K2MnO4+HAc→
9.以MnO2为主要原料制备MnCl2,K2MnO4和KMnO4,用方程式来表示各步反应。
10.完成下列反应式:
(1)FeCl3+NaF→
(2)Co(OH)3+H2SO4→
(3)Co2++SCN-
(4)Ni(OH)2+Br2+OH-→
(5)Ni+CO→
11.铁能使Cu2+还原,而铜能使Fe3+还原,这两事实有无矛盾?
12.用反应式说明下列现象:
(1)在Fe2+溶液中加入NaOH溶液,先生成灰绿色沉淀,然后沉淀逐渐变成红棕色。
(2)过滤后,沉淀用酸溶解,加几滴KSCN溶液,立刻变成血红色,再通入SO2气体,则血红色消失。
(3)向红色消失的溶液中滴加KMnO4溶液,其紫红色会褪去。
(4)最后加入黄血盐溶液生成蓝色沉淀。
13.指出下列实验结果,并写出反应式:
(1)用浓盐酸分边处理Fe(OH)3,CoO(OH)及NiO(OH)沉淀。
(2)分边在FeSO4,CoSO4及NiSO4溶液中加入过量氨水,然后放置在无CO2是空气中。
14.已知Cr(CO)6,Ru(CO)5和Pt(CO)4都是反磁性的羰基化合物。
根据价键理论推测他们中心原子的杂化类型和分子的空间构型。
15.找出实现下列变化所需的物质,并写出反应方程式:
(1)Mn2+→MnO4-
(2)Cr3+→CrO42-
(3)Fe3+→[Fe(CN)6]3-
(4)Co2+→[Co(CN)6]3-
16.试用简单的方法分离下列混合离子:
(1)Fe2+和Zn2+(2)Mn2+和Co2+
(3)Fe3+和Cr3+(4)Al3+和Cr3+
17.判断下列四种酸性未知液的定性分析报告是否合理?
(1)K+,NO2-,MnO4-,CrO4-(2)Fe2+,,Mn2+,SO42-,Cl-
(3)Fe3+,Co3+,I-,Cl-(4)Cr2O72-,Ba2+,NO3-,Br-
18.简单回答下列问题:
(1)Mg和Ti原子的外层都是两个电子,为什么Ti有+2,+3,+4价,而Mg只有+2价?(2)为什么TiCl4暴露在空气中会冒烟?
(3)为什么金属铬的密度,硬度,熔点都比金属镁的大?
(4)在水溶液中为什么Ca2+,Zn2+无色,而Fe2+,Mn2+,Ti3+有色?
(5)Ni2+的半径为69pm,Mg2+的半径是66pm,它们的电荷数又相同,为什么形成配合物的能力Ni2+比Mg2+大得多?
19.根据下列反应现象,写出有关的反应式:
(1)在Cr2(SO4)3溶液中滴加NaOH溶液,先析出灰蓝色絮状沉淀,后又溶解,此时加入溴水,溶液颜色由绿变黄。
(2)将H2S通入H2SO4酸化的K2Cr2O7溶液中,溶液的颜色由橙变绿,同时有乳白色沉淀析出。
(3)黄色的BaCrO4沉淀溶解在浓盐酸中,得到一种绿色溶液。
(4)在Co2+溶液中加入KSCN,稍稍加热有气体逸出。
(5)在FeCl3溶液中通入H2S,有乳白色沉淀析出。
20.有一黑色化合物A,不溶于碱液,加热时可溶于浓盐酸而放出气体B。
将A与NaOH 和KClO3共热,它就变成可溶于水的绿色化合物C。
若将C酸化,则得到紫红色溶液D和沉淀A。
用Na2SO3溶液处理D时也可得到沉淀A.若用H2SO4酸化的Na2SO3溶液处理D,则得到几乎无色的溶液E.问A,B,C,D,E各为何物?写出有关反应式。
21.有一浅绿色晶体A,可溶于水。
在无氧操作下,在A溶液中加入NaOH溶液,得到白色沉淀B。
B在空气中慢慢变成棕色沉淀C。
C溶于HCl溶液得黄棕色溶液D.在D溶液中
加几滴KSCN溶液,立即变成血红色溶液E.在E中通入SO2气体或加入NaF溶液均可使血红色褪去。
在A溶液中加入几滴BaCl2溶液,得白色沉淀F,F不溶于HNO3。
问A,B,C,D,E 和F各为何物?写出有关反应式。
22.已知[Fe(bipy)3]3++e- [Fe(bipy)3]2+的φθ=0.96V, [Fe(bipy)3]3+的β3θ=1.8×1014。
求[Fe(bipy)3]2+的β3θ。
bipy=
N N。
