常见物质的标准生成焓,反应熵,Gibbs自由能
常见物质的标准生成焓,反应熵,Gibbs自由能
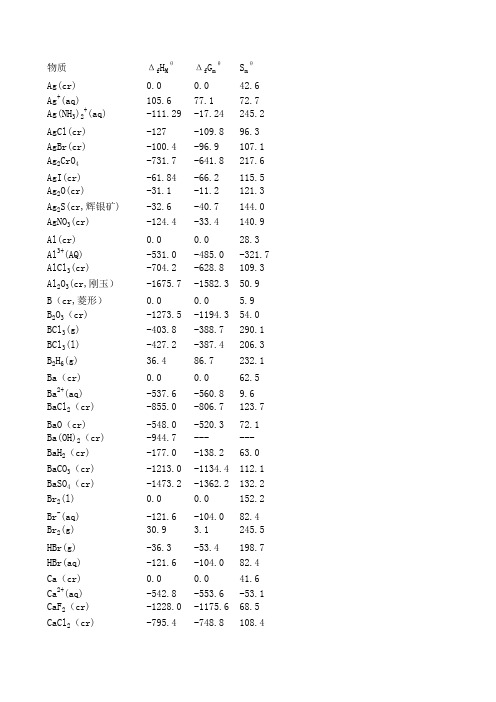
物质Δf H MθΔf G mθS mθAg(cr)0.00.042.6 Ag+(aq)105.677.172.7 Ag(NH3)2+(aq)-111.29-17.24245.2 AgCl(cr)-127-109.896.3 AgBr(cr)-100.4-96.9107.1 Ag2CrO4-731.7-641.8217.6 AgI(cr)-61.84-66.2115.5 Ag2O(cr)-31.1-11.2121.3 Ag2S(cr,辉银矿)-32.6-40.7144.0 AgNO3(cr)-124.4-33.4140.9 Al(cr)0.00.028.3 Al3+(AQ)-531.0-485.0-321.7 AlCl3(cr)-704.2-628.8109.3 Al2O3(cr,刚玉)-1675.7-1582.350.9 B(cr,菱形)0.00.0 5.9B2O3(cr)-1273.5-1194.354.0 BCl3(g)-403.8-388.7290.1 BCl3(l)-427.2-387.4206.3 B2H6(g)36.486.7232.1 Ba(cr)0.00.062.5 Ba2+(aq)-537.6-560.89.6 BaCl2(cr)-855.0-806.7123.7 BaO(cr)-548.0-520.372.1 Ba(OH)2(cr)-944.7------BaH2(cr)-177.0-138.263.0 BaCO3(cr)-1213.0-1134.4112.1 BaSO4(cr)-1473.2-1362.2132.2 Br2(l)0.00.0152.2 Br-(aq)-121.6-104.082.4 Br2(g)30.9 3.1245.5 HBr(g)-36.3-53.4198.7 HBr(aq)-121.6-104.082.4 Ca(cr)0.00.041.6 Ca2+(aq)-542.8-553.6-53.1 CaF2(cr)-1228.0-1175.668.5 CaCl2(cr)-795.4-748.8108.4CaO(cr)-634.9-603.338.1 CaH2(cr)-181.5-142.541.2 Ca(OH)2(cr)-985.2-897.583.4 CaCO3(cr,方解石)-1207.6-1129.191.7 CaSO4(cr,无水石膏)-1434.5-1322.0106.5 C(石墨)0.00.0 5.7C(金刚石) 1.9 2.9 2.34 C(g)716.7671.3158.1 CO(g)-110.5-137.2197.7 CO2(g)-393.5-394.4213.8 CO32-(aq)-667.1-527.8-56.9 HCO3-(aq)-692.0-586.891.2 CO2(aq)-413.26-386.0119.36 H2CO3(aq,非电离)-699.65-623.16187.4 CCl4(l)-128.2-62.6216.2 CH3OH(l)-239.2-166.6126.8 C2H5OH(l)-277.6-174.8161 HCOOH(l)-425.0-361.4129.0 CH3COOH(l)-484.3-389.9159.8 CH3COOH(aq,非电离)-485.76-396.46178.7 CH3COO-(aq)-486.01-369.3186.6 CH3CHO(l)-192.2-127.6160.2 CH4(g)-74.6-50.5186.3 C2H2(g)227.4209.9200.4 C2H4(g)52.468.4219.3 C2H6(g)-84.0-32.0229.2 C3H8(g)-103.8-23.4270.3 C4H6(l,丁二烯-1,3)88.5---199.0 C4H6(g,丁二烯-1,3)165.5201.7293.0 C4H8(l,丁二烯-1)-20.8---227.0 C4H8(g,丁二烯-1) 1.1772.04307.4 n-C4H10(l,正丁烷)-14.3------n-C4H10(g,正丁烷)-124.73-15.71310.0 C6H6(g)82.9129.7269.2 C6H6(l)49.1124.5173.4 Cl2(g)0.00.0223.1 Cl-(aq)-167.2-131.256.5HCl(g)-92.3-95.3186.9 ClO3-(aq)-104.0-8.0162.3Co(cr)0.00.030.0 Co(OH)2-539.7-454.379.0Cr(cr)0.00.023.8 Cr2O3(cr)-1139.7-1058.181.2 Cr2O72-(aq)-1490.3-1301.1261.9 CrO42-(aq)-881.2-727.850.2 Cu(cr)0.00.033.2 Cu+(aq)71.750.040.6 Cu2+(aq)64.865.5-99.6 Cu(NH3)42+(aq)-348.5-111.3273.6 CuCl(cr)-137.2-119.986.2 CuBr(cr)-104.6-100.896.2 CuI(cr)-67.8-69.596.7 Cu2O(cr)-168.6-146.093.1 CuO(cr)-157.3-129.742.6 Cu2S(cr)-79.5-86.2120.9 Cu2S(cr)-53.1-53.766.5 Cu2SO4(cr)-771.4-662.2109.2 Cu2SO4•H2O(cr)-2279.65-1880.04300.4 HF-273.30-275.4173.8 F2(g)0.00.0202.8 F-(aq)-332.6-278.8-13.8 F(g)79.462.3158.8 Fe(cr)0.00.027.3 Fe2+(aq)-89.1-78.9-137.7 Fe3+(aq)-48.5-4.7-315.9 Fe2O3(cr)-824.2-742.287.4 Fe3O4(cr)-1118.4-1015.4146.4 H2(g)0.00.0130.7 H(g)218.0203.3114.7 H+(aq)0.00.00.0H3O+(aq)-285.83-237.1369.91Hg(g)61.431.8175.0 Hg(l)0.00.075.9 HgO(cr)-90.8-58.570.3HgS(cr)-58.2-50.682.4 HgCl2(cr)-224.3-178.6146.0 Hg2Cl2(cr)-265.4-210.7191.6 I2(cr)0.00.0116.1 I2(g)62.419.3260.7 I-(aq)-55.2-51.6111.3 HI(g)26.5 1.7206.6 K(cr)0.00.064.7 K+(aq)-252.4-283.3102.5 KCl(cr)-436.5-408.582.6 KI(cr)-327.9-324.9106.3 KOH(cr)-424.6-378.778.9 KClO3(cr)-397.7-296.3143.1 KClO4(cr)-432.8-303.1151.0 KMnO4(cr)-837.2-737.6171.7 Mg(cr)0.00.032.7 Mg2+(aq)-466.9-454.8-138.1 MgCl2(cr)-641.3-591.889.6 MgCl2•6H2O(cr)-2499.0-2115.0315.1 MgO(cr)-601.6-569.327.0 Mg(OH)2(cr)-924.5-833.563.2 MgCO3(cr)-1095.8-1012.165.7 MgSO4(cr)-1284.9-1170.691.6 Mn(cr)0.00.032.0 Mn2+(aq)-220.8-228.1-73.6 MnO2(cr)-520.0-465.153.1 MnO4-(aq)-541.4-447.2191.2 MnCl2(cr)-481.3-440.5118.2 Na(cr)0.00.051.3 Na+(aq)-240.1-261.959.0 NaCl(cr)-411.2-384.172.1 Na2O(cr)-414.2-375.575.1 NaOH(cr)-425.6-379.564.5 Na2CO3(cr)-1130.7-1044.4135.0 NaI(cr)-287.8-286.198.5 Na2O2(cr)-510.9-447.795.0 HNO3(l)-174.1-80.7155.6NO3-(aq)-207.4-111.3146.4 NH3(g)-45.9-16.4192.8 NH3(aq)-80.29-26.5111.3 NH3•H2O(aq,非电离)-366.12-263.63181.21 NH4+(aq)-132.51-79.31113.4 NH4Cl(cr)-314.4-202.994.6 NH4NO3(cr)-365.6-183.9151.1 (NH4)SO4-1180.9-910.7220.1 N2(g)0.00.0191.6 NO(g)91.387.6210.8 NO2(g)33.251.3240.1 N2O(g)81.6103.7220.0 N2O4(g)11.199.8304.2 N2O4(l)-19.597.5209.2 N2H4(g)95.4159.4238.5 N2H4(l)50.6149.3121.2 NiO(cr)-240.6-211.738.00 O3(g)142.7163.2238.9 O2(g)00205.2 OH-(aq)-230.0-157.24-10.75 H2O(l)-285.83-237.1369.91 H2O(g)-241.8-228.6188.8 H2O2(l)-187.8-120.4109.6 H2O2(aq)-191.17-134.10143.9 P(cr,白)0.00.041.01 P(cr,红)-17.6---22.8 PCl3(g)-287.0-267.8311.8 PCl3(l)-314.7-272.3217.1 PCl5(cr)-443.5------PCl5(g)-374.9-305.0364.6 Pb(cr)0.00.064.8 Pb2+(aq)-1.7-24.410.5 PbO(cr,黄)-217.3-187.968.7 PbO(cr,红)-219.0-188.966.5 PbO2(cr)-277.4-217.368.6 Pb3O4(cr)-718.4-601.2211.3 H2S(g)-20.6-33.4205.8H2S(aq)-38.6-27.87126 HS-(aq)-16.312.0567.5 S2-(aq)33.185.8-14.6 H2SO4(l)-814.0-690.0156.9 HSO4-(aq)-887.3-755.9131.8 SO42-(aq)-909.3-744.5210.1 SO2(g)-296.8-300.1248.2 SO3(g)-395.7-371.1256.8 SO3(l)-441.0-373.8113.8 Si(cr)0.00.018.8 SiO2(cr,α-石英)-910.7-856.341.5 SiF4(g)-1615.0-1572.8282.8 SiCl4(l)-687.0-619.8239.7 SiCl4(g)-657.0-617.0330.7 Sn(cr,白)0.00.051.2 Sn(cr,灰)-2.10.144.1 SnO(cr)-280.7-251.957.2 SnO2(cr)-577.6-515.849.0 SnCl2(cr)-325.1------SnCl4(cr)-511.3-440.1258.6 Ti(cr)0030.72 TiO2(cr)-944.0-888.850.62 TiCl4(g)-763.2-726.3353.2 Zn(cr)0.00.041.6 Zn2+(aq)-153.9-147.1-112.1 ZnO(cr)-350.5-320.543.7 ZnCl2(aq)-488.2409.50.8Zn(cr,闪锌矿)-206.0-201.357.7。
稳定单质的标准摩尔生成焓

稳定单质的标准摩尔生成焓
的讨论文
标准摩尔生成焓是重要的物理概念,在算热力学计算时必不可少。
本文将对标准摩尔生成焓的定义、公式及其在计算中的应用等进行讨论。
标准摩尔生成焓(Standard molar enthalpy of formation)是一种来自化学反应中物质状态发生变化所产生的热量测量单位,它用于描述“某一物质在标准状态下与其它物质组成的
化合物的构成能力,即物质的可溶性”。
它的公式可以用“Hf=ΔHf(products)-ΔHf(reactants)”来表示,其中Hf表示标准摩尔生成焓,ΔHf表示标准状态下物质的可溶性,products表
示产物,reactants表示反应物。
标准摩尔生成焓的计算首先需要确定产物和反应物的数量以及它们的熵值。
然后,根据需要计算每种物质的标准摩尔熵,即每单位的重量或体积所需的标准摩尔熵。
最后,根据所
需的反应,计算出该反应的标准摩尔生成焓,即反应物的可溶性减去产物的可溶性。
标准摩尔生成焓主要应用于计算化学反应物质在特定条件下的构成能力,以及热力学计算,如Berthelot-Clausius方程、GibbsFreeEnergy方程等,其中,Berthelot-Clausius方程是
物质在不同温度下的特性可推导出的热力学理论。
Gibbs自由能方程则是衡量一系列化学
反应的活性的重要指标。
此外,标准摩尔生成焓对了解反应机理也有重要帮助。
总之,标准摩尔生成焓是一个重要的热力学概念,它一般用来衡量物质在标准状态下的构成能力,并可用于热力学计算和反应机理的研究。
它为研究化学反应中物质状态发生变化
而产生的热量提供了重要参考。
标准生成自由能

标准生成自由能自由能是热力学中的重要概念,它代表了系统在恒定温度和压力下能够做的最大功。
在化学和物理领域,自由能的概念被广泛应用,它不仅能够帮助我们理解物质变化的方向和程度,还可以指导实际操作和工程设计。
本文将介绍自由能的标准生成过程,以及相关的计算方法和应用。
首先,我们来了解一下自由能的标准生成过程。
在热力学中,标准生成自由能(ΔG°)是指在标准状态下,物质从其组成元素的标准状态生成的自由能变化。
标准状态是指物质在1个大气压下,摩尔浓度为1 mol/L(对溶液)或分压为1 atm(对气体)的状态。
标准生成自由能的计算公式为ΔG° = ΔH° TΔS°,其中ΔH°表示标准生成焓变,ΔS°表示标准生成熵变,T表示温度(单位为K)。
标准生成焓变ΔH°可以通过热化学反应方程式和反应热实验数据来确定。
而标准生成熵变ΔS°则可以通过熵变表和统计热力学原理来计算。
通过这两个参数的计算,我们可以得到标准生成自由能的数值,从而判断反应的进行方向和程度。
在实际应用中,标准生成自由能的计算对于化学反应的研究和工程设计具有重要意义。
通过对反应物和生成物的标准生成自由能进行比较,我们可以预测反应的进行方向。
当ΔG°为负时,表示反应是自发进行的,反之则需要外界能量输入才能进行。
这为化学工艺的设计和优化提供了重要依据,可以帮助我们选择合适的反应条件和催化剂,提高反应的产率和选择性。
除此之外,标准生成自由能还可以用于电化学反应和生物化学反应的研究。
在电化学中,通过对电极反应的标准生成自由能进行计算,可以确定电池的电动势和电化学反应的进行方向。
在生物化学中,标准生成自由能的计算可以帮助我们理解生物代谢途径和酶催化反应的进行机理。
总之,标准生成自由能是热力学中的重要概念,它不仅可以帮助我们理解物质变化的方向和程度,还可以指导实际操作和工程设计。
反应的焓变、熵变和自由能变化的符号

一、概述在化学和物理学中,我们经常会遇到反应的焓变、熵变和自由能变化的概念。
这些物理量可以帮助我们理解化学反应和物质变化的过程。
在本文中,我们将深入探讨这些概念的符号表示及其意义。
二、焓变的符号表示1. 反应的焓变表示为ΔH,其中Δ表示变化。
2. 当ΔH为正值时,表示反应吸热;当ΔH为负值时,表示反应放热。
3. 焓是系统的热力学函数,表示系统的内能加上压力乘以体积的乘积。
焓变则表示反应前后系统焓的变化。
三、熵变的符号表示1. 反应的熵变表示为ΔS,其中Δ表示变化。
2. 当ΔS为正值时,表示系统的熵增加;当ΔS为负值时,表示系统的熵减少。
3. 熵是系统的无序程度的度量,熵变则表示反应前后系统熵的变化。
四、自由能变化的符号表示1. 反应的自由能变化表示为ΔG,其中Δ表示变化。
2. 当ΔG为负值时,表示反应是自发进行的,即反应是在标准状态下自发进行的;当ΔG为正值时,表示反应是不自发进行的;当ΔG为零时,表示反应处于平衡状态。
3. 自由能是系统可供做非体积功的能量,自由能变化则可以表示反应的驱动力及反应的方向。
五、结论通过以上的讨论,我们可以看出反应的焓变、熵变和自由能变化在化学和物理学中是非常重要的物理量。
它们可以帮助我们理解化学反应和物质变化的过程,指导我们进行实验和工程应用。
在实际应用中,我们可以根据反应的焓变、熵变和自由能变化来预测反应的进行性质,以及调控反应的方向和速率。
希望本文可以为大家对这些概念有一个更加清晰的认识。
六、参考资料1. Atkins P., de Paula J. Atkins' Physical Chemistry. Oxford University Press, 2006.2. Chang R. General Chemistry: The Essential Concepts. McGraw-Hill, 2010.七、深入探讨焓变、熵变和自由能变化的意义在化学和物理学领域中,焓变、熵变和自由能变化是研究化学反应和物质变化过程中的重要物理量。
化学五十八物质的热力学稳定性与自由能变化的计算

化学五十八物质的热力学稳定性与自由能变化的计算热力学是研究物质在化学反应中产生和转化的热和能量变化的科学。
在化学反应中,物质的稳定性和自由能变化是热力学中的重要概念。
本文将介绍化学五十八物质的热力学稳定性以及自由能变化的计算方法。
一、热力学稳定性热力学稳定性是指化学物质在给定条件下是否趋向于保持原来的状态,并且不发生自发的不可逆反应。
热力学稳定性通常通过比较不同物质的标准摩尔生成焓、标准摩尔生成自由能或标准摩尔生成熵来判断。
其中,标准摩尔生成焓(ΔH°f)表示在标准状态下,1摩尔物质生成的焓变化。
标准摩尔生成自由能(ΔG°f)表示在标准状态下,1摩尔物质生成的自由能变化。
标准摩尔生成熵(ΔS°f)表示在标准状态下,1摩尔物质生成的熵变化。
根据热力学的第一定律,化学反应的焓变(ΔH)等于吸收的热量减去放出的热量。
当ΔH < 0时,反应放热,物质稳定;当ΔH > 0时,反应吸热,物质不稳定。
根据热力学的第二定律,自由能变化(ΔG)等于吸收的热量减去产生的熵增。
当ΔG < 0时,反应自发进行,物质稳定;当ΔG > 0时,反应不自发进行,物质不稳定。
二、自由能变化的计算方法根据Gibbs-Helmholtz方程,自由能变化(ΔG)和温度(T)之间存在如下关系:ΔG = ΔH - TΔS其中,ΔH为焓变,ΔS为熵变。
为了计算五十八种化学物质的自由能变化,我们需先给出它们的标准摩尔生成焓(ΔH°f)和标准摩尔生成熵(ΔS°f)的数值。
这些数据可通过参考热力学手册或相关数据库获得。
将所给的ΔH°f和ΔS°f代入Gibbs-Helmholtz方程,我们可以计算出五十八种化学物质在不同温度下的自由能变化。
举例来说,假设我们要计算氧气(O2)的自由能变化。
根据热力学数据,氧气的标准摩尔生成焓为0 kJ/mol,标准摩尔生成熵为205J/(mol·K)。
物质的标准摩尔生成焓(新)

187.9
C6H4(CH3)2(g),间二甲苯
17.238
118.977
357.80
127.57
C6H(CH3)2(l), 间二甲苯
-25.418
107.817
252.17
183.3
C6H4(CH3)2(g), 对二甲苯
17.949
121.266
352.53
126.86
C6H4(CH3)2(l), 对二甲苯
25.48
Ag2CO3(s)
-506.14
-437.09
167.36
Ag2O(s)
-30.56
-10.82
121.71
65.57
Al(s)
0
0
28.315
24.35
Al(g)
313.80
273.2
164.553
Al2O3-α
-1669.8
-2213.16
0.986
79.0
Al2(SO4)3(s)
-3434.98
-25.94
-1.32
206.42
29.12
H2O(g)
-241.825
-228.577
188.823
33.571
H2O(l)
-285.838
-237.142
69.940
75.296
H2O(s)
-291.850
(-234.03)
(39.4)
H2O2(l)
-187.61
-118.04
102.26
82.29
194.93
C6H5CH3(g),甲苯
49.999
122.388
常见物质的标准生成焓,反应熵,Gibbs自由能

物质Δf H MθΔf G mθS mθAg(cr)0.00.042.6 Ag+(aq)105.677.172.7 Ag(NH3)2+(aq)-111.29-17.24245.2 AgCl(cr)-127-109.896.3 AgBr(cr)-100.4-96.9107.1 Ag2CrO4-731.7-641.8217.6 AgI(cr)-61.84-66.2115.5 Ag2O(cr)-31.1-11.2121.3 Ag2S(cr,辉银矿)-32.6-40.7144.0 AgNO3(cr)-124.4-33.4140.9 Al(cr)0.00.028.3 Al3+(AQ)-531.0-485.0-321.7 AlCl3(cr)-704.2-628.8109.3 Al2O3(cr,刚玉)-1675.7-1582.350.9 B(cr,菱形)0.00.0 5.9B2O3(cr)-1273.5-1194.354.0 BCl3(g)-403.8-388.7290.1 BCl3(l)-427.2-387.4206.3 B2H6(g)36.486.7232.1 Ba(cr)0.00.062.5 Ba2+(aq)-537.6-560.89.6 BaCl2(cr)-855.0-806.7123.7 BaO(cr)-548.0-520.372.1 Ba(OH)2(cr)-944.7------BaH2(cr)-177.0-138.263.0 BaCO3(cr)-1213.0-1134.4112.1 BaSO4(cr)-1473.2-1362.2132.2 Br2(l)0.00.0152.2 Br-(aq)-121.6-104.082.4 Br2(g)30.9 3.1245.5 HBr(g)-36.3-53.4198.7 HBr(aq)-121.6-104.082.4 Ca(cr)0.00.041.6 Ca2+(aq)-542.8-553.6-53.1 CaF2(cr)-1228.0-1175.668.5 CaCl2(cr)-795.4-748.8108.4CaO(cr)-634.9-603.338.1 CaH2(cr)-181.5-142.541.2 Ca(OH)2(cr)-985.2-897.583.4 CaCO3(cr,方解石)-1207.6-1129.191.7 CaSO4(cr,无水石膏)-1434.5-1322.0106.5 C(石墨)0.00.0 5.7C(金刚石) 1.9 2.9 2.34 C(g)716.7671.3158.1 CO(g)-110.5-137.2197.7 CO2(g)-393.5-394.4213.8 CO32-(aq)-667.1-527.8-56.9 HCO3-(aq)-692.0-586.891.2 CO2(aq)-413.26-386.0119.36 H2CO3(aq,非电离)-699.65-623.16187.4 CCl4(l)-128.2-62.6216.2 CH3OH(l)-239.2-166.6126.8 C2H5OH(l)-277.6-174.8161 HCOOH(l)-425.0-361.4129.0 CH3COOH(l)-484.3-389.9159.8 CH3COOH(aq,非电离)-485.76-396.46178.7 CH3COO-(aq)-486.01-369.3186.6 CH3CHO(l)-192.2-127.6160.2 CH4(g)-74.6-50.5186.3 C2H2(g)227.4209.9200.4 C2H4(g)52.468.4219.3 C2H6(g)-84.0-32.0229.2 C3H8(g)-103.8-23.4270.3 C4H6(l,丁二烯-1,3)88.5---199.0 C4H6(g,丁二烯-1,3)165.5201.7293.0 C4H8(l,丁二烯-1)-20.8---227.0 C4H8(g,丁二烯-1) 1.1772.04307.4 n-C4H10(l,正丁烷)-14.3------n-C4H10(g,正丁烷)-124.73-15.71310.0 C6H6(g)82.9129.7269.2 C6H6(l)49.1124.5173.4 Cl2(g)0.00.0223.1 Cl-(aq)-167.2-131.256.5HCl(g)-92.3-95.3186.9 ClO3-(aq)-104.0-8.0162.3Co(cr)0.00.030.0 Co(OH)2-539.7-454.379.0Cr(cr)0.00.023.8 Cr2O3(cr)-1139.7-1058.181.2 Cr2O72-(aq)-1490.3-1301.1261.9 CrO42-(aq)-881.2-727.850.2 Cu(cr)0.00.033.2 Cu+(aq)71.750.040.6 Cu2+(aq)64.865.5-99.6 Cu(NH3)42+(aq)-348.5-111.3273.6 CuCl(cr)-137.2-119.986.2 CuBr(cr)-104.6-100.896.2 CuI(cr)-67.8-69.596.7 Cu2O(cr)-168.6-146.093.1 CuO(cr)-157.3-129.742.6 Cu2S(cr)-79.5-86.2120.9 Cu2S(cr)-53.1-53.766.5 Cu2SO4(cr)-771.4-662.2109.2 Cu2SO4•H2O(cr)-2279.65-1880.04300.4 HF-273.30-275.4173.8 F2(g)0.00.0202.8 F-(aq)-332.6-278.8-13.8 F(g)79.462.3158.8 Fe(cr)0.00.027.3 Fe2+(aq)-89.1-78.9-137.7 Fe3+(aq)-48.5-4.7-315.9 Fe2O3(cr)-824.2-742.287.4 Fe3O4(cr)-1118.4-1015.4146.4 H2(g)0.00.0130.7 H(g)218.0203.3114.7 H+(aq)0.00.00.0H3O+(aq)-285.83-237.1369.91Hg(g)61.431.8175.0 Hg(l)0.00.075.9 HgO(cr)-90.8-58.570.3HgS(cr)-58.2-50.682.4 HgCl2(cr)-224.3-178.6146.0 Hg2Cl2(cr)-265.4-210.7191.6 I2(cr)0.00.0116.1 I2(g)62.419.3260.7 I-(aq)-55.2-51.6111.3 HI(g)26.5 1.7206.6 K(cr)0.00.064.7 K+(aq)-252.4-283.3102.5 KCl(cr)-436.5-408.582.6 KI(cr)-327.9-324.9106.3 KOH(cr)-424.6-378.778.9 KClO3(cr)-397.7-296.3143.1 KClO4(cr)-432.8-303.1151.0 KMnO4(cr)-837.2-737.6171.7 Mg(cr)0.00.032.7 Mg2+(aq)-466.9-454.8-138.1 MgCl2(cr)-641.3-591.889.6 MgCl2•6H2O(cr)-2499.0-2115.0315.1 MgO(cr)-601.6-569.327.0 Mg(OH)2(cr)-924.5-833.563.2 MgCO3(cr)-1095.8-1012.165.7 MgSO4(cr)-1284.9-1170.691.6 Mn(cr)0.00.032.0 Mn2+(aq)-220.8-228.1-73.6 MnO2(cr)-520.0-465.153.1 MnO4-(aq)-541.4-447.2191.2 MnCl2(cr)-481.3-440.5118.2 Na(cr)0.00.051.3 Na+(aq)-240.1-261.959.0 NaCl(cr)-411.2-384.172.1 Na2O(cr)-414.2-375.575.1 NaOH(cr)-425.6-379.564.5 Na2CO3(cr)-1130.7-1044.4135.0 NaI(cr)-287.8-286.198.5 Na2O2(cr)-510.9-447.795.0 HNO3(l)-174.1-80.7155.6NO3-(aq)-207.4-111.3146.4 NH3(g)-45.9-16.4192.8 NH3(aq)-80.29-26.5111.3 NH3•H2O(aq,非电离)-366.12-263.63181.21 NH4+(aq)-132.51-79.31113.4 NH4Cl(cr)-314.4-202.994.6 NH4NO3(cr)-365.6-183.9151.1 (NH4)SO4-1180.9-910.7220.1 N2(g)0.00.0191.6 NO(g)91.387.6210.8 NO2(g)33.251.3240.1 N2O(g)81.6103.7220.0 N2O4(g)11.199.8304.2 N2O4(l)-19.597.5209.2 N2H4(g)95.4159.4238.5 N2H4(l)50.6149.3121.2 NiO(cr)-240.6-211.738.00 O3(g)142.7163.2238.9 O2(g)00205.2 OH-(aq)-230.0-157.24-10.75 H2O(l)-285.83-237.1369.91 H2O(g)-241.8-228.6188.8 H2O2(l)-187.8-120.4109.6 H2O2(aq)-191.17-134.10143.9 P(cr,白)0.00.041.01 P(cr,红)-17.6---22.8 PCl3(g)-287.0-267.8311.8 PCl3(l)-314.7-272.3217.1 PCl5(cr)-443.5------PCl5(g)-374.9-305.0364.6 Pb(cr)0.00.064.8 Pb2+(aq)-1.7-24.410.5 PbO(cr,黄)-217.3-187.968.7 PbO(cr,红)-219.0-188.966.5 PbO2(cr)-277.4-217.368.6 Pb3O4(cr)-718.4-601.2211.3 H2S(g)-20.6-33.4205.8H2S(aq)-38.6-27.87126 HS-(aq)-16.312.0567.5 S2-(aq)33.185.8-14.6 H2SO4(l)-814.0-690.0156.9 HSO4-(aq)-887.3-755.9131.8 SO42-(aq)-909.3-744.5210.1 SO2(g)-296.8-300.1248.2 SO3(g)-395.7-371.1256.8 SO3(l)-441.0-373.8113.8 Si(cr)0.00.018.8 SiO2(cr,α-石英)-910.7-856.341.5 SiF4(g)-1615.0-1572.8282.8 SiCl4(l)-687.0-619.8239.7 SiCl4(g)-657.0-617.0330.7 Sn(cr,白)0.00.051.2 Sn(cr,灰)-2.10.144.1 SnO(cr)-280.7-251.957.2 SnO2(cr)-577.6-515.849.0 SnCl2(cr)-325.1------SnCl4(cr)-511.3-440.1258.6 Ti(cr)0030.72 TiO2(cr)-944.0-888.850.62 TiCl4(g)-763.2-726.3353.2 Zn(cr)0.00.041.6 Zn2+(aq)-153.9-147.1-112.1 ZnO(cr)-350.5-320.543.7 ZnCl2(aq)-488.2409.50.8Zn(cr,闪锌矿)-206.0-201.357.7。
标准生成自由能

标准生成自由能
标准生成自由能的定义是指在标准状态下,1摩尔物质生成的自由能变化。
标
准状态通常指的是温度为298K(25摄氏度)和压力为1atm,此时物质的标准生成自由能用ΔG°表示。
标准生成自由能可以通过热力学数据表中的标准生成焓和标
准熵来计算,其计算公式为ΔG°=ΔH°-TΔS°,其中ΔH°为标准生成焓,ΔS°为标准熵,T为温度。
标准生成自由能的单位通常为焦耳/摩尔或千焦/摩尔。
标准生成自由能在化学和工程中有着重要的应用。
首先,它可以帮助我们预测
化学反应的方向。
当ΔG°<0时,表示反应是自发进行的,反之当ΔG°>0时,表示反应不会自发进行。
其次,标准生成自由能还可以帮助我们比较不同化学反应的进行程度,从而选择合适的反应条件。
此外,在工程领域中,标准生成自由能也被广泛应用于设计化工过程和优化能量利用。
总之,标准生成自由能是描述化学反应是否能够进行的重要参数,它的计算方
法简单清晰,应用广泛。
通过对标准生成自由能的理解和应用,我们可以更好地理解和预测化学反应的行为,为化学和工程领域的研究和应用提供重要的理论基础。
熵和自由能

即同一物质S气>S液>S固 S高温>S低温 S混合物>S纯物质
(2)有类似分子结构且分子量又相近的物 质,其标准熵相近 如S θ 298 CO=197.9 J· mol-1 · K -1 S θ 298 N2=191.4 J· mol-1 · K -1 分子结构相似分子量不同,其标准熵随分子量 增大而增大 如卤素的氢化物 HF HCl HBr HI 173.7 186.7 198.5 206.5 J· mol-1 · K -1
化学反应的熵变与温度有关,因为 每一物质的熵都随温度升高而增加。但 大多数情况下产物的熵与反应物的熵增 加的数量相近,所以反应的△rS 随温度 无明显的变化,在近似计算中可忽略其 变化。
吉布斯自由能及其应用
一、吉布斯(Gibbs)自由能 用式(2-13)来判断变化的自发性不方便,
为了方便,我们可引入另一个热力学函数—— 吉布斯自由能,也称自由焓,用符号G表示,其
△G θ T ≈ △H θ 298-T△S θ 298 (2-19) 例2-7 已知
C2H5OH(l) C2H5OH(g) △fH θ m/( kJ· mol-1 )-277.6 -235.3 S θ m /(J · k -1 · mol-1 ) 161 282 求(1)在298K和标准态下, C2H5OH(l)能否自发地变成 C2H5OH(g)? (2)在373K和标准态下, C2H5OH(l)能否自发地变成 C2H5OH (g)? (3)估算乙醇的沸点。
1、熵的概念
撒落在地面上的液氨,会自动蒸发, 氨气充满整个空间;把几粒糖放到一杯 水中,糖块会溶解,整杯水变甜;固体 NH4Cl在一定条件下可自动分解产生 NH3和HCl气体,这些过程都是吸热的, 为什么会自动进行呢?
液氨中,氨分子只能在液氨所占的体积 范围内运动,蒸发成气体后,分子运动范围 增大了,分子在空间分布与在液体中相比, 混乱度增加了(在NaCl晶体中,粒子排列很 规则,正负离子只能在晶粒的平衡位置作振 动,食盐溶解后,正负离子之间的引力大大 减弱了,离子可以在aq中自由运动,原先规 则的排列次序被破坏,混乱度加大了)NH4Cl 固体分解成2种气体,混乱度将变得更大,因 此,体系混乱度的增加也是自发过程的推动 力之一。
附录Ⅵ 物质的标准摩尔生成焓、标准摩尔生成吉

Cl2(g) Cu(s) CuO(s) Cu2O-α F2(g) Fe-α
0 0 -155.2 -166.69 0 0
0 0 -127.1 -146.33 0 0
222.948 33.32 43.51 100.8 203.5 27.15
33.9 24.47 44.4 69.8 31.46 25.23
-2213.16 -3728.53
82.396
0.986 239.3 175.021
79.0 259.4
Br2(g) Br2(l) C(g)
30.71 0
718.384
3.109 0
672.942
245.455 152.3
158.101
35.99 35.6
C(金刚石) C(石墨)
CO(g) CO2(g) Ca(s) CaC2(s) CaCO3(方解
附录Ⅵ 物质的标准摩尔生成焓、标准摩尔生成吉 布斯函数、标准摩尔熵和摩尔热容(100kPa)> (1)单质和无机物
物质
Ag(s) Ag2CO3(s)
ΔfHm(298.15 K)
kJ·mol-1 0
-506.14
ΔfGm(298.15 K)
kJ·mol-1 0
-4ห้องสมุดไป่ตู้7.09
Sm(298.1 5K)
J·K-1mol-1 42.712 167.36
H4 .9 1. 2. 6.
( 49 26 53 86
CH
6
3)
2(
g)
,
对 二 甲 苯 C6 -2 11 24 18 H4 4. 0. 7. 3. ( 42 24 36 7 CH 6 4 3) 2( l) , 对 二 甲 苯
常见物质的标准生成焓,反应熵,Gibbs自由能

常见物质的标准生成焓,反应熵,Gibbs自由能物质Δf H MθΔf G mθS mθAg(cr)0.00.042.6 Ag+(aq)105.677.172.7 Ag(NH3)2+(aq)-111.29-17.24245.2 AgCl(cr)-127-109.896.3 AgBr(cr)-100.4-96.9107.1 Ag2CrO4-731.7-641.8217.6 AgI(cr)-61.84-66.2115.5 Ag2O(cr)-31.1-11.2121.3 Ag2S(cr,辉银矿)-32.6-40.7144.0 AgNO3(cr)-124.4-33.4140.9 Al(cr)0.00.028.3 Al3+(AQ)-531.0-485.0-321.7 AlCl3(cr)-704.2-628.8109.3 Al2O3(cr,刚玉)-1675.7-1582.350.9 B(cr,菱形)0.00.0 5.9B2O3(cr)-1273.5-1194.354.0 BCl3(g)-403.8-388.7290.1 BCl3(l)-427.2-387.4206.3 B2H6(g)36.486.7232.1 Ba (cr)0.00.062.5 Ba2+(aq)-537.6-560.89.6 BaCl2(cr)-855.0-806.7123.7 BaO(cr)-548.0-520.372.1 Ba(OH)2(cr)-944.7------BaH2(cr)-177.0-138.263.0 BaCO3(cr)-1213.0-1134.4112.1 BaSO4(cr)-1473.2-1362.2132.2 Br2(l)0.00.0152.2 Br-(aq)-121.6-104.082.4 Br2(g)30.9 3.1245.5 HBr(g)-36.3-53.4198.7 HBr(aq)-121.6-104.082.4 Ca(cr)0.00.041.6 Ca2+(aq)-542.8-553.6-53.1 CaF2(cr)-1228.0-1175.668.5 CaCl2(cr)-795.4-748.8108.4 CaO(cr)-634.9-603.338.1 CaH2(cr)-181.5-142.541.2 Ca(OH)2(cr)-985.2-897.583.4 CaCO3(cr,方解石)-1207.6-1129.191.7 CaSO4(cr,无水石膏)-1434.5-1322.0106.5 C(石墨)0.00.0 5.7C(金刚石) 1.9 2.9 2.34 C(g)716.7671.3158.1 CO(g)-110.5-137.2197.7 CO2(g)-393.5-394.4213.8 CO32-(aq)-667.1-527.8-56.9 HCO3-(aq)-692.0-586.891.2 CO2(aq)-413.26-386.0119.36 H2CO3(aq,非电离)-699.65-623.16187.4 CCl4(l)-128.2-62.6216.2 CH3OH(l)-239.2-166.6126.8 C2H5OH(l)-277.6-174.8161 HCOOH(l)-425.0-361.4129.0 CH3COOH(l)-484.3-389.9159.8 CH3COOH(aq,非电离)-485.76-396.46178.7 CH3COO-(aq)-486.01-369.3186.6 CH3CHO(l)-192.2-127.6160.2 CH4(g)-74.6-50.5186.3 C2H2(g)227.4209.9200.4 C2H4(g)52.468.4219.3 C2H6(g)-84.0-32.0229.2 C3H8(g)-103.8-23.4270.3 C4H6(l,丁二烯-1,3)88.5---199.0 C4H6(g,丁二烯-1,3)165.5201.7293.0 C4H8(l,丁二烯-1)-20.8---227.0 C4H8(g,丁二烯-1) 1.1772.04307.4 n-C4H10(l,正丁烷)-14.3------n-C4H10(g,正丁烷)-124.73-15.71310.0 C6H6(g)82.9129.7269.2 C6H6(l)49.1124.5173.4 Cl2(g)0.00.0223.1 Cl-(aq)-167.2-131.256.5HCl(g)-92.3-95.3186.9 ClO3-(aq)-104.0-8.0162.3Co(cr)0.00.030.0 Co(OH)2-539.7-454.379.0Cr(cr)0.00.023.8 Cr2O3(cr)-1139.7-1058.181.2 Cr2O72-(aq)-1490.3-1301.1261.9 CrO42-(aq)-881.2-727.850.2 Cu (cr)0.00.033.2 Cu+(aq)71.750.040.6 Cu2+(aq)64.865.5-99.6 Cu(NH3)42+(aq)-348.5-111.3273.6 CuCl(cr)-137.2-119.986.2 CuBr(cr)-104.6-100.896.2 CuI(cr)-67.8-69.596.7 Cu2O(cr)-168.6-146.093.1 CuO(cr)-157.3-129.742.6 Cu2S(cr)-79.5-86.2120.9 Cu2S(cr)-53.1-53.766.5 Cu2SO4(cr)-771.4-662.2109.2 Cu2SO4?H2O(cr)-2279.65-1880.04300.4 HF-273.30-275.4173.8 F2(g)0.00.0202.8 F-(aq)-332.6-278.8-13.8 F(g)79.462.3158.8 Fe(cr)0.00.027.3 Fe2+(aq)-89.1-78.9-137.7 Fe3+(aq)-48.5-4.7-315.9 Fe2O3(cr)-824.2-742.287.4 Fe3O4(cr)-1118.4-1015.4146.4 H2(g)0.00.0130.7 H(g)218.0203.3114.7 H+(aq)0.00.00.0H3O+(aq)-285.83-237.1369.91Hg(g)61.431.8175.0 Hg(l)0.00.075.9 HgO(cr)-90.8-58.570.3 HgS(cr)-58.2-50.682.4 HgCl2(cr)-224.3-178.6146.0 Hg2Cl2(cr)-265.4-210.7191.6 I2(cr)0.00.0116.1 I2(g)62.419.3260.7 I-(aq)-55.2-51.6111.3 HI(g)26.5 1.7206.6 K (cr)0.00.064.7 K+(aq)-252.4-283.3102.5 KCl(cr)-436.5-408.582.6 KI(cr)-327.9-324.9106.3 KOH(cr)-424.6-378.778.9 KClO3(cr)-397.7-296.3143.1 KClO4(cr)-432.8-303.1151.0 KMnO4(cr)-837.2-737.6171.7 Mg(cr)0.00.032.7 Mg2+(aq)-466.9-454.8-138.1 MgCl2(cr)-641.3-591.889.6 MgCl2?6H2O (cr)-2499.0-2115.0315.1 MgO(cr)-601.6-569.327.0 Mg(OH)2(cr)-924.5-833.563.2 MgCO3(cr)-1095.8-1012.165.7 MgSO4(cr)-1284.9-1170.691.6 Mn(cr)0.00.032.0 Mn2+(aq)-220.8-228.1-73.6 MnO2(cr)-520.0-465.153.1 MnO4-(aq)-541.4-447.2191.2 MnCl2(cr)-481.3-440.5118.2 Na(cr)0.00.051.3 Na+(aq)-240.1-261.959.0 NaCl(cr)-411.2-384.172.1 Na2O(cr)-414.2-375.575.1 NaOH(cr)-425.6-379.564.5 Na2CO3(cr)-1130.7-1044.4135.0 NaI(cr)-287.8-286.198.5 Na2O2(cr)-510.9-447.795.0 HNO3(l)-174.1-80.7155.6NO3-(aq)-207.4-111.3146.4 NH3(g)-45.9-16.4192.8 NH3(aq)-80.29-26.5111.3 NH3?H2O(aq,非电离)-366.12-263.63181.21 NH4+(aq)-132.51-79.31113.4 NH4Cl(cr)-314.4-202.994.6 NH4NO3(cr)-365.6-183.9151.1 (NH4)SO4-1180.9-910.7220.1 N2(g)0.00.0191.6 NO(g)91.387.6210.8 NO2(g)33.251.3240.1 N2O(g)81.6103.7220.0 N2O4(g)11.199.8304.2 N2O4(l)-19.597.5209.2 N2H4(g)95.4159.4238.5 N2H4(l)50.6149.3121.2 NiO(cr)-240.6-211.738.00 O3(g)142.7163.2238.9 O2(g)00205.2 OH-(aq)-230.0-157.24-10.75 H2O(l)-285.83-237.1369.91 H2O(g)-241.8-228.6188.8 H2O2(l)-187.8-120.4109.6 H2O2(aq)-191.17-134.10143.9 P(cr,白)0.00.041.01 P(cr,红)-17.6---22.8 PCl3(g)-287.0-267.8311.8 PCl3(l)-314.7-272.3217.1 PCl5(cr)-443.5------PCl5(g)-374.9-305.0364.6 Pb(cr)0.00.064.8 Pb2+(aq)-1.7-24.410.5 PbO(cr,黄)-217.3-187.968.7 PbO(cr,红)-219.0-188.966.5 PbO2(cr)-277.4-217.368.6 Pb3O4(cr)-718.4-601.2211.3 H2S(g)-20.6-33.4205.8H2S(aq)-38.6-27.87126 HS-(aq)-16.312.0567.5 S2-(aq)33.185.8-14.6 H2SO4(l)-814.0-690.0156.9 HSO4-(aq)-887.3-755.9131.8 SO42-(aq)-909.3-744.5210.1 SO2(g)-296.8-300.1248.2 SO3(g)-395.7-371.1256.8 SO3(l)-441.0-373.8113.8 Si (cr)0.00.018.8 SiO2(cr,α-石英)-910.7-856.341.5 SiF4(g)-1615.0-1572.8282.8 SiCl4(l)-687.0-619.8239.7 SiCl4(g)-657.0-617.0330.7 Sn(cr,白)0.00.051.2 Sn(cr,灰)-2.10.144.1 SnO(cr)-280.7-251.957.2 SnO2(cr)-577.6-515.849.0 SnCl2(cr)-325.1------SnCl4(cr)-511.3-440.1258.6 Ti(cr)0030.72 TiO2(cr)-944.0-888.850.62 TiCl4(g)-763.2-726.3353.2 Zn(cr)0.00.041.6 Zn2+(aq)-153.9-147.1-112.1 ZnO(cr)-350.5-320.543.7 ZnCl2(aq)-488.2409.50.8Zn(cr,闪锌矿)-206.0-201.357.7。
氯化钠的吉布斯生成焓

氯化钠的吉布斯生成焓氯化钠是一种常见的无机盐,化学式为NaCl。
它是由钠离子(Na+)和氯离子(Cl-)组成的,常见于生活中的食盐。
在化学反应中,氯化钠的吉布斯生成焓是一个重要的热力学参数,它描述了在标准条件下氯化钠形成的反应的热力学性质。
吉布斯生成焓是指在标准状态下生成一个摩尔物质所释放或吸收的热量。
对于氯化钠,它的吉布斯生成焓可以通过实验测定或计算来获得。
在实验中,可以通过测定氯化钠与相应反应的热量变化来确定其吉布斯生成焓。
而在计算中,可以使用热力学数据表中的标准摩尔生成焓和标准摩尔反应熵来计算吉布斯生成焓。
要计算氯化钠的吉布斯生成焓,首先需要了解氯化钠的标准摩尔生成焓和标准摩尔反应熵。
标准摩尔生成焓指的是在标准状态下,生成一摩尔氯化钠所释放的热量。
而标准摩尔反应熵是指在标准状态下,反应一摩尔氯化钠所产生的混合物的混合度。
标准摩尔生成焓和标准摩尔反应熵可以通过实验测定或计算得到。
在实验中,可以使用燃烧弧法或燃烧热计法来测定氯化钠的标准摩尔生成焓。
而在计算中,则可以使用反应热力学数据和热力学函数来计算标准摩尔生成焓和标准摩尔反应熵。
在计算氯化钠的吉布斯生成焓时,可以使用吉布斯自由能的定义公式:ΔG = ΔH - TΔS,其中ΔG表示吉布斯生成焓,ΔH表示标准摩尔生成焓,T表示反应温度,ΔS表示标准摩尔反应熵。
根据此公式,可以通过已知的标准摩尔生成焓和标准摩尔反应熵,以及反应温度来计算氯化钠的吉布斯生成焓。
需要注意的是,上述公式仅适用于恒温恒压条件下的反应。
对于非恒温条件下的反应,需要考虑反应温度对反应热力学性质的影响。
总之,氯化钠的吉布斯生成焓是一个重要的热力学参数,它描述了在标准条件下氯化钠形成的反应的热力学性质。
可以通过实验测定或计算标准摩尔生成焓和标准摩尔反应熵,然后利用吉布斯自由能的定义公式来计算氯化钠的吉布斯生成焓。
这对于深入理解氯化钠的热力学性质和化学反应机理有着重要的意义。
标准反应生成焓

标准反应生成焓在化学反应中,反应生成焓是指在标准状态下,物质生成的焓变化。
它是描述化学反应能量变化的重要物理量,对于研究化学反应的热力学性质具有重要意义。
本文将对标准反应生成焓进行深入探讨,以便更好地理解和应用这一概念。
首先,我们需要了解标准状态的定义。
在化学中,标准状态通常指气体在标准大气压下的状态,即1 atm 的压强。
对于溶液,标准状态是指溶质的摩尔浓度为1 mol/L。
在固体和液体的情况下,标准状态是指物质的纯度为1 mol/L。
在研究化学反应时,我们通常将反应物和生成物的浓度、压强等参数设定为标准状态,以便进行比较和计算。
接下来,我们来看一下标准生成焓的计算方法。
标准生成焓的计算是通过反应物和生成物之间的焓变化来实现的。
在标准状态下,生成1 mol 的物质所释放或吸收的能量即为标准生成焓。
在一般情况下,我们可以通过实验数据或热力学计算来确定化学反应的焓变化,从而得到标准生成焓的数值。
标准生成焓的计算公式为:ΔH° = ΣnΔHf°(生成物) ΣmΔHf°(反应物)。
其中,ΔH°表示标准生成焓,ΔHf°表示标准生成焓,n和m分别表示生成物和反应物的摩尔数。
通过这个公式,我们可以计算出化学反应在标准状态下的生成焓,从而了解反应的热力学性质。
标准生成焓的正负值代表了反应是放热还是吸热。
当标准生成焓为负值时,表示反应放热,释放能量;当标准生成焓为正值时,表示反应吸热,吸收能量。
这一点对于工业生产和实验室研究具有重要意义,可以帮助我们选择合适的反应条件和控制反应过程。
此外,标准生成焓还可以用来计算化学反应的热力学平衡常数。
根据热力学原理,反应的热力学平衡常数与反应生成焓之间存在一定的关系,通过计算标准生成焓可以帮助我们预测反应的热力学平衡位置和方向。
总之,标准反应生成焓是描述化学反应能量变化的重要物理量,它可以帮助我们理解和预测化学反应的热力学性质,对于工业生产和科学研究具有重要意义。
氢气标准生成焓和标准熵

氢气标准生成焓和标准熵氢气是一种重要的能源载体,其标准生成焓和标准熵的研究对于氢能的利用具有重要的意义。
标准生成焓是指在标准状态下,1mol物质生成的焓变化,通常用ΔH°表示。
而标准熵则是指在标准状态下,1mol物质的熵,通常用S°表示。
本文将对氢气的标准生成焓和标准熵进行详细的介绍和分析。
首先,我们来看氢气的标准生成焓。
氢气的标准生成焓是指在标准状态下,1mol氢气生成的焓变化。
氢气的标准生成焓可以通过燃烧反应或其他化学反应进行测定。
在常温常压下,氢气的标准生成焓为0,这是因为氢气是元素状态,其标准生成焓被定义为0。
而在其他温度和压力下,氢气的标准生成焓可以通过热化学方法进行测定。
通过测定氢气在不同温度和压力下的焓变化,可以得到氢气的标准生成焓的数值。
氢气的标准生成焓的数值可以用来计算氢气在不同条件下的热力学性质,对于氢能的利用具有重要的意义。
接下来,我们来看氢气的标准熵。
氢气的标准熵是指在标准状态下,1mol氢气的熵。
氢气的标准熵可以通过热力学方法进行测定。
在常温常压下,氢气的标准熵为130.68 J/(mol·K),这是因为氢气是一种简单的双原子分子,其分子自由度为5,因此其标准熵的数值可以通过热力学方法进行计算。
氢气的标准熵的数值可以用来计算氢气在不同条件下的热力学性质,对于氢能的利用具有重要的意义。
总结一下,氢气的标准生成焓和标准熵是氢能研究中的重要参数,其数值可以通过实验测定或热力学方法计算得到。
这些参数对于氢能的利用具有重要的意义,可以用来计算氢气在不同条件下的热力学性质,为氢能的应用提供重要的参考。
希望本文对氢气的标准生成焓和标准熵有所帮助,感谢阅读。
以上就是关于氢气标准生成焓和标准熵的介绍,希望对大家有所帮助。
感谢阅读!。
[精品]G和G在使用上的区别
![[精品]G和G在使用上的区别](https://img.taocdn.com/s3/m/7e5a41961a37f111f1855b60.png)
这样一来, Q 对 K 的比值,从而也就是△ G 的大小和符号表 征了体系在除上述两种特殊情况之于一个反应 Zn+Cu2+ Zn2++Cu 在通常使用标准电极电势或标准电动势去进行判断时 Eθ(Zn2+/Zn) < Eθ(Cu2+/Cu) 标准电动势 Eθ >0
如果反应有较大的熵变, 特别是当温度有显著的改变时, △G 的符号就有可能由熵变项决定,如 NH4Cl(s) NH3(g)+HCl(g) 反应进行时产生了气体物质,△n(g)=2,将伴随有明显的熵 增, △Sθ=285 J· K- 1· mol-1,随着温度升高,△Gθ将从大于0 (= 21.2 kJ· mol-1)变为小于0。此时NH4Cl (s)将发生自发分解。 △G=△H-T△S
由此可见,反应的自发性是和体系中各物质的起始分压或起 始浓度有关的,除了指定是上述两种特定状态可用△Gθ去判断方 向以外,其它状态都必须使用△G去判断。 事实上,由等温方程可见△G=△Gθ+RTlnQ,对于一个给定 反应,△Gθ是一个定值,但却可以通过调节Q值来改变△G的大小 和符号。换句话说,起始分压或浓度可以确定△ G的大小和符号, 从而确定反应的自发方向。 CaSO4 Ca2+(aq)+SO42-(aq), Kspθ=[Ca2+][SO42-]/(cθ)2=9.1×10-6 △Gθ=-RTlnKspθ=28.7 kJ· mol-1 > 0 表明在标准状态下 , 即 (Ca2 + ) 和 (SO42 - ) 均为 1mol· L - 1 时, CaSO4的溶解是非自发的;相反,其逆过程亦即1 mol· L-1的Ca2+ 和1 mol· L-1的SO42-遇到一起发生沉淀却是自发的(逆过程的△Gθ =-28.7 kJ· mol-1< 0),这完全符合事实, 这时沉淀过程将一直进 行到固液相达到平衡,亦即离子浓度积减小到等于Ksp时为止。如 果溶液中起始离子浓度积比 Ksp 还要小, 则△G= RTlnQ/Kspθ< 0,必 将引起自发的溶解, 直到建立新的固液平衡,△G=0为止。 再如:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
物质Δf H MθΔf G mθS mθAg(cr)0.00.042.6 Ag+(aq)105.677.172.7 Ag(NH3)2+(aq)-111.29-17.24245.2 AgCl(cr)-127-109.896.3 AgBr(cr)-100.4-96.9107.1 Ag2CrO4-731.7-641.8217.6 AgI(cr)-61.84-66.2115.5 Ag2O(cr)-31.1-11.2121.3 Ag2S(cr,辉银矿)-32.6-40.7144.0 AgNO3(cr)-124.4-33.4140.9 Al(cr)0.00.028.3 Al3+(AQ)-531.0-485.0-321.7 AlCl3(cr)-704.2-628.8109.3 Al2O3(cr,刚玉)-1675.7-1582.350.9 B(cr,菱形)0.00.0 5.9B2O3(cr)-1273.5-1194.354.0 BCl3(g)-403.8-388.7290.1 BCl3(l)-427.2-387.4206.3 B2H6(g)36.486.7232.1 Ba(cr)0.00.062.5 Ba2+(aq)-537.6-560.89.6 BaCl2(cr)-855.0-806.7123.7 BaO(cr)-548.0-520.372.1 Ba(OH)2(cr)-944.7------BaH2(cr)-177.0-138.263.0 BaCO3(cr)-1213.0-1134.4112.1 BaSO4(cr)-1473.2-1362.2132.2 Br2(l)0.00.0152.2 Br-(aq)-121.6-104.082.4 Br2(g)30.9 3.1245.5 HBr(g)-36.3-53.4198.7 HBr(aq)-121.6-104.082.4 Ca(cr)0.00.041.6 Ca2+(aq)-542.8-553.6-53.1 CaF2(cr)-1228.0-1175.668.5 CaCl2(cr)-795.4-748.8108.4CaO(cr)-634.9-603.338.1 CaH2(cr)-181.5-142.541.2 Ca(OH)2(cr)-985.2-897.583.4 CaCO3(cr,方解石)-1207.6-1129.191.7 CaSO4(cr,无水石膏)-1434.5-1322.0106.5 C(石墨)0.00.0 5.7C(金刚石) 1.9 2.9 2.34 C(g)716.7671.3158.1 CO(g)-110.5-137.2197.7 CO2(g)-393.5-394.4213.8 CO32-(aq)-667.1-527.8-56.9 HCO3-(aq)-692.0-586.891.2 CO2(aq)-413.26-386.0119.36 H2CO3(aq,非电离)-699.65-623.16187.4 CCl4(l)-128.2-62.6216.2 CH3OH(l)-239.2-166.6126.8 C2H5OH(l)-277.6-174.8161 HCOOH(l)-425.0-361.4129.0 CH3COOH(l)-484.3-389.9159.8 CH3COOH(aq,非电离)-485.76-396.46178.7 CH3COO-(aq)-486.01-369.3186.6 CH3CHO(l)-192.2-127.6160.2 CH4(g)-74.6-50.5186.3 C2H2(g)227.4209.9200.4 C2H4(g)52.468.4219.3 C2H6(g)-84.0-32.0229.2 C3H8(g)-103.8-23.4270.3 C4H6(l,丁二烯-1,3)88.5---199.0 C4H6(g,丁二烯-1,3)165.5201.7293.0 C4H8(l,丁二烯-1)-20.8---227.0 C4H8(g,丁二烯-1) 1.1772.04307.4 n-C4H10(l,正丁烷)-14.3------n-C4H10(g,正丁烷)-124.73-15.71310.0 C6H6(g)82.9129.7269.2 C6H6(l)49.1124.5173.4 Cl2(g)0.00.0223.1 Cl-(aq)-167.2-131.256.5HCl(g)-92.3-95.3186.9 ClO3-(aq)-104.0-8.0162.3Co(cr)0.00.030.0 Co(OH)2-539.7-454.379.0Cr(cr)0.00.023.8 Cr2O3(cr)-1139.7-1058.181.2 Cr2O72-(aq)-1490.3-1301.1261.9 CrO42-(aq)-881.2-727.850.2 Cu(cr)0.00.033.2 Cu+(aq)71.750.040.6 Cu2+(aq)64.865.5-99.6 Cu(NH3)42+(aq)-348.5-111.3273.6 CuCl(cr)-137.2-119.986.2 CuBr(cr)-104.6-100.896.2 CuI(cr)-67.8-69.596.7 Cu2O(cr)-168.6-146.093.1 CuO(cr)-157.3-129.742.6 Cu2S(cr)-79.5-86.2120.9 Cu2S(cr)-53.1-53.766.5 Cu2SO4(cr)-771.4-662.2109.2 Cu2SO4•H2O(cr)-2279.65-1880.04300.4 HF-273.30-275.4173.8 F2(g)0.00.0202.8 F-(aq)-332.6-278.8-13.8 F(g)79.462.3158.8 Fe(cr)0.00.027.3 Fe2+(aq)-89.1-78.9-137.7 Fe3+(aq)-48.5-4.7-315.9 Fe2O3(cr)-824.2-742.287.4 Fe3O4(cr)-1118.4-1015.4146.4 H2(g)0.00.0130.7 H(g)218.0203.3114.7 H+(aq)0.00.00.0H3O+(aq)-285.83-237.1369.91Hg(g)61.431.8175.0 Hg(l)0.00.075.9 HgO(cr)-90.8-58.570.3HgS(cr)-58.2-50.682.4 HgCl2(cr)-224.3-178.6146.0 Hg2Cl2(cr)-265.4-210.7191.6 I2(cr)0.00.0116.1 I2(g)62.419.3260.7 I-(aq)-55.2-51.6111.3 HI(g)26.5 1.7206.6 K(cr)0.00.064.7 K+(aq)-252.4-283.3102.5 KCl(cr)-436.5-408.582.6 KI(cr)-327.9-324.9106.3 KOH(cr)-424.6-378.778.9 KClO3(cr)-397.7-296.3143.1 KClO4(cr)-432.8-303.1151.0 KMnO4(cr)-837.2-737.6171.7 Mg(cr)0.00.032.7 Mg2+(aq)-466.9-454.8-138.1 MgCl2(cr)-641.3-591.889.6 MgCl2•6H2O(cr)-2499.0-2115.0315.1 MgO(cr)-601.6-569.327.0 Mg(OH)2(cr)-924.5-833.563.2 MgCO3(cr)-1095.8-1012.165.7 MgSO4(cr)-1284.9-1170.691.6 Mn(cr)0.00.032.0 Mn2+(aq)-220.8-228.1-73.6 MnO2(cr)-520.0-465.153.1 MnO4-(aq)-541.4-447.2191.2 MnCl2(cr)-481.3-440.5118.2 Na(cr)0.00.051.3 Na+(aq)-240.1-261.959.0 NaCl(cr)-411.2-384.172.1 Na2O(cr)-414.2-375.575.1 NaOH(cr)-425.6-379.564.5 Na2CO3(cr)-1130.7-1044.4135.0 NaI(cr)-287.8-286.198.5 Na2O2(cr)-510.9-447.795.0 HNO3(l)-174.1-80.7155.6NO3-(aq)-207.4-111.3146.4 NH3(g)-45.9-16.4192.8 NH3(aq)-80.29-26.5111.3 NH3•H2O(aq,非电离)-366.12-263.63181.21 NH4+(aq)-132.51-79.31113.4 NH4Cl(cr)-314.4-202.994.6 NH4NO3(cr)-365.6-183.9151.1 (NH4)SO4-1180.9-910.7220.1 N2(g)0.00.0191.6 NO(g)91.387.6210.8 NO2(g)33.251.3240.1 N2O(g)81.6103.7220.0 N2O4(g)11.199.8304.2 N2O4(l)-19.597.5209.2 N2H4(g)95.4159.4238.5 N2H4(l)50.6149.3121.2 NiO(cr)-240.6-211.738.00 O3(g)142.7163.2238.9 O2(g)00205.2 OH-(aq)-230.0-157.24-10.75 H2O(l)-285.83-237.1369.91 H2O(g)-241.8-228.6188.8 H2O2(l)-187.8-120.4109.6 H2O2(aq)-191.17-134.10143.9 P(cr,白)0.00.041.01 P(cr,红)-17.6---22.8 PCl3(g)-287.0-267.8311.8 PCl3(l)-314.7-272.3217.1 PCl5(cr)-443.5------PCl5(g)-374.9-305.0364.6 Pb(cr)0.00.064.8 Pb2+(aq)-1.7-24.410.5 PbO(cr,黄)-217.3-187.968.7 PbO(cr,红)-219.0-188.966.5 PbO2(cr)-277.4-217.368.6 Pb3O4(cr)-718.4-601.2211.3 H2S(g)-20.6-33.4205.8H2S(aq)-38.6-27.87126 HS-(aq)-16.312.0567.5 S2-(aq)33.185.8-14.6 H2SO4(l)-814.0-690.0156.9 HSO4-(aq)-887.3-755.9131.8 SO42-(aq)-909.3-744.5210.1 SO2(g)-296.8-300.1248.2 SO3(g)-395.7-371.1256.8 SO3(l)-441.0-373.8113.8 Si(cr)0.00.018.8 SiO2(cr,α-石英)-910.7-856.341.5 SiF4(g)-1615.0-1572.8282.8 SiCl4(l)-687.0-619.8239.7 SiCl4(g)-657.0-617.0330.7 Sn(cr,白)0.00.051.2 Sn(cr,灰)-2.10.144.1 SnO(cr)-280.7-251.957.2 SnO2(cr)-577.6-515.849.0 SnCl2(cr)-325.1------SnCl4(cr)-511.3-440.1258.6 Ti(cr)0030.72 TiO2(cr)-944.0-888.850.62 TiCl4(g)-763.2-726.3353.2 Zn(cr)0.00.041.6 Zn2+(aq)-153.9-147.1-112.1 ZnO(cr)-350.5-320.543.7 ZnCl2(aq)-488.2409.50.8Zn(cr,闪锌矿)-206.0-201.357.7。
