胶体化学 (1)
人教版高一化学必修一《胶体》课件

。
后氢氧化铁沉淀又 溶于稀硫酸。 _________________________________
OH Fe3+
ClFe3+ Fe3+ Fe3+
Fe3+ Cl-
OH-
3+ ClFe ClOH3+ Cl Fe Fe3+ Fe3+ [Fe(OH)3]n Fe3+ Cl3+ Fe 3+ Fe OHCl ClFe3+
<1nm
均一、透明 稳定
1nm~100nm
均一、透明
介稳性
>100nm
不均一、不透明
不稳定 不能 不能
能 能
能
不能
胶体与溶液分离方法: 渗析
胶体
1. 概念: 分散质粒子大小介于1nm~100nm之间的 分散系。
2. 分类:
按分散剂 的状态
胶体
气溶胶 液溶胶 固溶胶
云、雾 ห้องสมุดไป่ตู้奶、豆浆 有色玻璃、烟水晶
非金属氧化物、金属硫化物的胶体粒子及土壤胶 体、硅酸胶体的胶体粒子,带负电荷。 某些大分子胶体,如淀粉溶液的胶体粒子, 不带电荷。
胶体
(3)布朗运动
胶体粒子不停地做无规则运动。
胶体粒子吸附同种电 荷,相互排斥
胶体处于介稳体系
布朗运动
胶体
(4)聚沉
a.表现:胶体粒子在一定条件下聚集起来 形成较大颗粒,从分散剂里析出的过程。 b.方法: i.加热或搅拌 ii.加入带相反电荷的胶体 iii.加入电解质
胶体
常见的胶体有: 按分散质粒子大小分(当分散剂为水或 其他液体时): 胶体 胶体 淀粉溶液、蛋白质溶液、豆浆、牛奶、血液、 烟、云、雾、墨水、肥皂水、Fe(OH)3胶体等。
高一化学胶体的知识点归纳

高一化学胶体的知识点归纳在高一化学学习中,胶体是一个重要的知识点。
胶体是指由两种或多种物质组成的混合体系,其中一种物质以微小颗粒的形式悬浮在另一种物质中。
下面将对胶体的定义、性质以及应用进行归纳总结。
一、胶体的定义胶体是介于溶液与悬浮液之间的一种混合体系。
它的特点是悬浮的微粒大于分子,但又小于机械混合物的粒径。
胶体的形成是由于相互作用力的存在导致溶质不能完全溶解于溶剂中,而形成微小颗粒悬浮在溶剂中,形成胶体。
二、胶体的性质1. 可见性:胶体的微粒大小在10-9到10-6m之间,透过显微镜可以观察到。
2. 不稳定性:胶体由于微粒之间存在相互作用力,导致胶体不稳定,容易发生凝聚和沉淀现象。
3. 混浊性:胶体在光线的照射下呈现混浊状态,散射光使得胶体呈现浑浊的外观。
4. 过滤性:胶体可以通过一次普通滤纸进行过滤,不通过超微滤膜。
三、胶体的分类根据胶体的组成和性质,胶体可以分为溶胶、凝胶和胶体溶液三类。
1. 溶胶:溶胶是指胶体中溶质颗粒多分散且呈无定形结构的胶体,如烟雾、煤粉等。
2. 凝胶:凝胶是指胶体中溶质颗粒呈现有规律的立体结构的胶体,如明胶等。
3. 胶体溶液:胶体溶液是指胶体中溶质颗粒保持在溶液中的胶体,如乳液、胶束等。
四、胶体的应用1. 工业上的应用:胶体在工业生产中有广泛的应用,例如纺织、造纸、涂料、医药等行业中常用的乳液和胶束都是胶体的应用。
2. 日常生活中的应用:胶体在日常生活中也有一些重要的应用,如牙膏、洗洁精等产品中的凝胶胶体,以及乳化液体、奶粉等产品都是胶体的应用。
3. 环境保护中的应用:胶体的特性使其在环境保护方面具有重要作用,如胶束能够帮助清洁污染物,减少环境污染。
总结:高一化学中胶体的知识点主要包括胶体的定义、性质、分类以及应用。
胶体是由两种或多种物质组成的混合体系,具有可见性、不稳定性、混浊性以及过滤性等特点。
根据组成和性质的不同,胶体可以分为溶胶、凝胶和胶体溶液三类。
胶体在工业生产、日常生活以及环境保护中都有广泛的应用。
物理化学第十章 胶体化学

3. 沉降与沉降平衡
多相分散系统中的粒子,因受重力作用而下 沉的过程,称为沉降。沉降与扩散为一对矛盾 的两个方面
沉降 扩散 分散相分布
真溶液
粗分散系统 胶体系统 平衡
均相
沉于底部 形成浓度梯度
贝林(Perrin)导出沉降平衡时粒子浓度随高度的分布:
o c2 Mg ln 1 ( h2 h1 ) c1 RT
胶核 可滑动面
胶粒
{[AgI]m nI-(n-x)K+}x- xK+ 胶团结构
K+
K+
I-
K+
(AgI)m
I-
I-
K+
特点:
1) 胶核:首先吸附过量的成核离子,然后吸附反离子; 2) 胶团整体为电中性
I-
§10.5
溶胶的稳定与聚沉
Derjaguin&Landau(1941)
1. 溶胶的经典稳定理论DLVO理论
溶胶粒子间的作用力:
Verwey &Overbeek(1948) van der Waals 吸引力:EA -1/x2
势 能 ER
双电层引起的静电斥力:ER ae-x 总作用势能:E = ER + EA
E
EA 曲线的形状由粒子本
性决定,不受电解质影响;
Emax
0 x 第二最小值 EA 第一最小值
势 能 ER 电解质浓度: c1 < c2 < c3 ,
0EAc3源自c2c1E电解质浓度,ER,E,
溶胶稳定性。在 c3 以后, 引力势能占绝对优势,分散 相粒子一旦相碰,即可聚合。
41
电解质对溶胶的聚沉规律:
(i)反离子的价数起主要作用
高一化学第一章知识点胶体

高一化学第一章知识点胶体胶体是化学中的一个重要概念和研究对象,涉及到许多我们日常生活中都会遇到的现象和应用。
在高一化学的第一章中,我们主要学习与胶体相关的知识点,包括定义、分类、形成条件、性质、应用等方面。
本文将对这些知识点进行详细的介绍和论述,以帮助大家更好地理解和掌握。
一、胶体的定义胶体是指由两种或两种以上的物质组成的混合系统,其中一种物质以微细颗粒分散在另一种物质中。
在胶体中,分散相的颗粒尺寸通常在1纳米到1000纳米之间。
胶体的粒子较小,使得其呈现出特殊的性质和行为,例如散射光线、凝聚与分散、滤过等。
胶体在生活中有着广泛的应用,例如乳液、胶水、泡沫等。
二、胶体的分类根据胶体中溶质和溶剂的性质,胶体可以分为溶胶、凝胶和乳胶三类。
1. 溶胶:溶胶指的是固体微粒均匀分散在液体中的胶体。
在溶胶中,微粒不会沉淀,并可以通过过滤器隔离出来。
溶胶的例子包括不溶性染料颗粒悬浮在水中的溶液。
2. 凝胶:凝胶是指由液体分子组成的三维网状结构,形成的胶体。
凝胶的溶胶性质使其具有半固体状态,可以流动但又具有一定的刚性。
凝胶的例子包括明胶、琼脂等。
3. 乳胶:乳胶是指由液体分散相和另一种液体连续相组成的胶体。
乳胶通常为白色乳状液体,如牛奶、橡胶乳等。
三、胶体的形成条件胶体的形成需要满足一定的条件,主要包括溶解度、浓度、剪切作用和共沉淀等。
1. 溶解度:胶体形成时,存在一定量的物质在溶液中不溶解,从而形成微粒。
这种微粒的溶解度很小,所以会以胶体的形式存在。
2. 浓度:胶体形成还需要一定的溶质浓度。
当溶质的浓度达到一定程度时,会发生聚集现象,从而形成胶体。
3. 剪切作用:外界的剪切力作用也可以促使溶质聚集成胶体。
例如,我们普通生活中搅拌牛奶时,会使乳胶变得更加稳定。
4. 共沉淀:共沉淀是指在溶液中存在两种不相容的物质,在一定条件下一起析出形成胶体。
例如,当铁(Ⅲ)离子和氢氧化钠共沉淀时,会形成铁(Ⅲ)氢氧化物胶体。
四、胶体的性质胶体具有许多独特的性质,与溶液、悬浮液和晶体等有所不同。
胶体化学大汇总 (1)

1.分散体系的分类?根据被分散物质分散的程度可将分散体系分为粗分散体系、胶体分散体系和分子分散体系。
2.什么是胶体?颗粒大小在1~1000nm范围内的分散相粒子称为胶体3.胶体制备一般需具备什么条件?常用的制备方法有哪些,举例说明?条件:a。
固体分散相粒子要足够小,使其有一定的动力学稳定性;b。
分散相在分散介质中的溶解度要足够小,形成分散相的反应物浓度低;c。
为了使分散相粒子具有抗凝结而保持稳定的性质,体系中必须有第三种物质存在方法:分散法——机械粉碎法、超声分散法、电分散法、胶溶法凝聚法——化学凝聚、物理凝聚胶溶法——吸附溶胶、洗涤沉淀胶溶、表面解离溶胶例子:洗涤沉淀胶溶法制备普鲁士蓝溶胶、改换介质法制备硫溶胶。
4.什么是单分散溶胶?单分散溶胶制备的原理?在特定条件下制备的粒子大小、形状、组成均相同的溶胶称为单分散溶胶。
原理:在溶液中产物浓度超过其饱和浓度,并略高于成核浓度时,在短时间内形成全部晶核。
晶核形成后,溶液浓度迅速减小,低于成核浓度(仍高于饱和浓度),不再形成新晶核。
已形成的晶核在此浓度下以相同速度长大,从而得到单分散胶体粒子。
5.什么是胶体晶体?胶体晶体制备中采用模板剂的作用是什么?由一种或多种单分散的胶体粒子组装并规整排列的二维或三维有序结构称为胶体晶体,又称合成蛋白石。
作用:引导,组装胶体粒子6.什么是反渗透?若在渗透平衡后在浓相一侧施加外压p(p>Π),则浓相的溶剂分子将向稀相迁移,故称反渗透。
7.纳米粒子的特性是什么?产生电动现象的根本原因是什么?特性:①表面与界面效应②小尺寸效应③量子尺寸效应④宏观量子隧道效应根本原因:胶体粒子常带有一定符号和数量的电荷。
8.为什么分散相质点在分散介质中表面常会带某种电荷?当分散相与分散介质接触时,因为分散相质点表面解离或者吸附溶液中某些离子从而使表面带有电荷。
9.界面移动电泳和显微电泳各适用何种体系?界面移动电泳主要用于蛋白质系统等生物大分子体系,显微电泳主要用于显微镜下可见胶体粒子的体系。
胶体与表面化学(1)

0 绪 论 ---胶体化学发展简史
现今所用的一些名词,如溶胶(sol)、凝胶(gel)、胶溶 (peptization)、渗析(dialysis)、离浆(syneresis)都是 Graham提出的。尽管在这一时期积累了大量的经验和知识, 但胶体化学真正为人们所重视并获得较大的发展是从1903年 开始的。这时席格蒙迪Zsigmondy(德)发明了超显微镜, 肯定了溶胶的一个根本问题——体系的多相性,从而明确了 胶体化学是界面化学。1907年,德国化学家Ostwald创办了 第一个胶体化学的专门刊物——《胶体化学和工业杂志》, 因而许多人把这一年视为胶体化学正式成为一门独立学科的 一年。接着Freundlich和Zsigmondy先后出版了他们的名著 《毛细管化学》(1909)和《胶体化学》(1902)。
界面化学的统计力学研究是从范德华开 始的。1893年,范德华认识到在界面层中 密度实际上是连续变化的。他应用了局部 自由能密度的概念,结合范德华方程,并 引入半经验修正,从理论上研究了决定于 分子间力的状态方程参数与界面张力间的 关系。
50年代以后,界面现象的统计力学研究 经 过 勃 夫 ( F.Buff ) 、 寇 克 伍 德 (Kirkwood ) 、哈拉西玛 (Harasima ) 等的研究工作,取得了实质性的进展.
Vacuum Technology.
Elsevier (NL) [E]
0 绪 论 ---胶体化学发展简史
胶体化学也是一门古老而又年轻的科学。 有史以前,我们的祖先就会制造陶器;汉朝已能利用纤 维造纸;后汉时又发明了墨;其他像做豆腐、面食以及 药物的制剂等等在我国都有悠久的历史,这些成品及其 制作过程都与胶体化学密切相关。 1809年,俄国化学家Scheele发现了土粒的电泳现象; 1829年英国植物学家Brown观察到花粉的布朗运动。此 后,许多人相继制备了各种溶胶,并研究了它们的性质。
第十二章胶体化学主要公式及其适用条件

第十二章 胶体化学主要公式及其适用条件1. 胶体系统及其特点胶体:分散相粒子在某方向上的线度在1~100 nm 范围的高分散系统称为胶体。
对于由金属及难溶于水的卤化物、硫化物或氢氧化物等在水中形成胶体称憎液溶胶(简称为胶体)。
憎液溶胶的粒子均是由数目众多的分子构成,存在着很大的相界面,因此憎液溶胶具有高分散性、多相性以及热力学不稳定性的特点。
2. 胶体系统的动力学性质(1) 布朗运动胶体粒子由于受到分散介质分子的不平衡撞击而不断地作不规则地运动,称此运动为布朗运动。
其平均位移可x 按下列爱因斯坦-布朗位移公式计算2/1)π3/(ηr L RTt x =式中:t 为时间,r 为粒子半径,η为介质的粘度。
(2) 扩散、沉降及沉降平衡扩散是指当有浓度梯度存在时,物质粒子(包括胶体粒子)因热运动而发生宏观上的定向位移之现象。
沉降是指胶体粒子因重力作用而发生下沉的现象。
沉降平衡:当胶体粒子的沉降速率与其扩散速率相等时,胶体粒子在介质的浓度随高度形成一定分布并且不随时间而变,这一状态称为胶体粒子处于沉降平衡。
其数密度C 与高度h 的关系为}{[])()/(1)/()/ln(12012h h RT Mg C C ---=ρρ式中ρ及ρ0分别为粒子及介质的密度,M 为粒子的摩尔质量,g 为重力加速度。
此式适用于单级分散粒子在重力场中的沉降平衡。
3. 光学性质当将点光源发出的一束可见光照射到胶体系统时,在垂直于入射光的方向上可以观察到一个发亮的光锥,此现象称为丁达尔现象。
丁达尔现象产生的原因是胶体粒子大小,小于可见光的波长,而发生光的散射之结果。
散射光的强度I 可由下面瑞利公式计算:()22222200422209π1cos 22n n V C I I l n n αλ⎛⎫-=+ ⎪+⎝⎭式中:I0及λ表示入射光的强度与波长;n 及n0分别为分散相及分散介质的折射率;α为散射角,为观测方向与入射光之间的夹角;V 为单个分散相粒子的体积;C 为分散相的数密度;l 为观测者与散射中心的距离。
高一化学必修一胶体

第1节元素与物质的分类(第2课时)【学习目标】1.知道胶体是一种重要的分散系,能列举生活中的胶体,了解胶体与其他分散系的区别。
2.能运用胶体的丁达尔现象、电泳、聚沉等特性解释简单的实验现象和实例。
【重难点】知道胶体是一种重要的分散系,了解胶体的性质(如丁达尔现象、聚沉以及电泳)。
【课前预习区】1、称为分散系。
试根据分散系定义说明硫酸铜溶液中分散质是,分散剂是。
2、简述分散系的分类依据及具体类别3、溶液、胶体、浊液三种分散系的本质区别是什么?【学案导学】【问题组一】1、清晨,在茂密的森林里,会看到缕缕阳光穿过树木的枝叶铺洒在地面上,你知道为什么会产生这美丽的景象吗?2、列举你在生活中观察到的与胶体有关的现象。
3、如何简单区分胶体和溶液?【规律总结1】三、一种重要的混合物—胶体1、胶体的本质特征_________________________________________________常见的胶体分散系:① FeCl3溶液、AlCl3溶液或明矾溶液;水玻璃、肥皂水等形成胶体②其他:有色玻璃、土壤胶体、烟、云、雾2、几种分散系的比较[注意]①分散系的根本区别是分散质粒子的直径大小,正是由于这一原因,决定了各分散系的性质的不同。
②胶体按照分散质的不同可分为:粒子胶体:许多粒子的集合体,如Fe(OH)3胶体、碘化银胶体分子胶体:高分子的单个分子的直径已达胶体粒子的范围,如:淀粉、蛋白质等分子。
③若分散质粒子的直径范围发生改变,则分散系的性质也随之改变。
即溶液、胶体、浊液之间是可以相互转化的。
【课堂练习】1、下列关于胶体的说法正确的是()A.胶体外观不均匀B.胶体做不停的、无秩序的运动C.胶体不能通过滤纸D.胶体不稳定,静置后容易产生沉淀2、医学上治疗肾功能衰竭等疾病引起的血液中毒时,最常用的血液净化手段是血液透析。
透析时,病人的血液通过浸在透析液中的透析膜进行循环和透析。
透析原理同胶体的_______类似,透析膜同____________类似,透析膜的孔应____________(填“大于”“等于”“小于”)血液内毒性粒子直径,毒性物质才可能扩散到透析液中而被除去。
化学高一知识点归纳必修一胶体

化学高一知识点归纳必修一胶体胶体是一种特殊的物质状态,介于溶液和悬浮液之间。
它有着许多有趣且重要的性质,对于我们理解和应用化学知识起着非常重要的作用。
在高一化学中,我们学习了关于胶体的基本概念、分类、性质和应用等内容。
下面,我将对这些知识点进行归纳总结。
一、胶体的概念胶体是一种由两种或更多种物质组成的混合物,其中一种物质是微细分散相,另一种物质是连续相。
微细分散相的粒径一般在1纳米到1000纳米之间,呈现出浑浊或乳白色的外观。
二、胶体的分类根据连续相和分散相的性质不同,胶体可以分为溶胶、凝胶和乳胶三种类型。
溶胶的连续相是液体,分散相是固体或液体。
凝胶的连续相是液体,分散相形成了三维网状结构。
乳胶的连续相是液体,分散相是液体。
三、胶体的性质1. 稳定性:胶体具有较好的稳定性,不易分散或凝聚。
2. 色散性:胶体表现出良好的色散性,呈现出乳白色或其他颜色。
3. 光学性质:胶体具有散射和吸收光线的能力,导致光的路径改变和颜色变化。
4. 流动性:胶体可以流动,但粘度较高。
5. 过滤性:胶体不能通过常规过滤器进行分离。
6. 电性质:胶体具有电荷,可以表现出电泳现象。
四、胶体的制备胶体可以通过多种方法制备,如溶胶凝胶法、凝胶法、与化学反应法、共聚合法等。
其中,溶胶凝胶法是最常用的制备胶体的方法。
五、胶体的应用1. 医药领域:胶体在药物输送系统中起到载体的作用,可以提高药物的生物利用率和疗效。
2. 日用品领域:胶体可以用于制作食品、化妆品和清洁产品等。
3. 材料科学领域:胶体可以应用于纳米材料的合成和涂层材料的制备。
4. 环境治理领域:胶体在水处理和废物处理中起到重要作用。
5. 生物技术领域:胶体可以用于生物传感器的制备和生物成像技术的开发等。
综上所述,胶体作为一种特殊的物质状态,具有丰富多样的特性和广泛的应用领域。
对于我们理解化学知识和应用化学原理具有重要意义。
通过学习和掌握胶体的概念、分类、性质和应用等知识点,我们能够更加深入地了解化学世界的奥秘,同时也为未来的科学研究和实践应用打下基础。
胶体的定义高一化学知识点

胶体的定义高一化学知识点胶体的定义是高一化学课程中的一个重要知识点。
胶体是一种特殊的物质状态,介于溶液和悬浮液之间。
在胶体中,微粒的大小介于溶液中的分子和悬浮液中的颗粒之间。
一、胶体的组成胶体由两个基本部分组成:连续相和分散相。
连续相是胶体组成中占据主导地位的物质,常为液体。
分散相是被分散在连续相中的微粒,常常是固体或液体。
二、胶体的分类根据连续相和分散相的不同,胶体可以分为凝胶、溶胶和乳胶三种基本类型。
1. 凝胶凝胶是一种具有三维空间网络结构的胶体。
在凝胶中,连续相是液体,而分散相则形成了一个固体的网状结构。
凝胶的例子包括明胶、硅胶等。
溶胶是一种固体微粒分散在液体中的胶体。
在溶胶中,连续相是液体,而分散相是固体微粒。
常见的溶胶有胶体金溶液、银溶胶等。
3. 乳胶乳胶是液体微粒分散在液体中的胶体。
在乳胶中,连续相和分散相都是液体。
牛奶就是一个常见的乳胶。
三、胶体的特性胶体具有一些独特的物理和化学特性,而这些特性是由于其微粒大小和表面性质造成的。
1. 稳定性胶体具有较高的稳定性,即微粒不易沉淀或聚集。
这是由于胶体微粒的表面带有电荷,使得微粒之间发生排斥导致的。
当两个带有同种电荷的微粒相互靠近时,它们之间的相互斥力会阻止它们的聚集。
由于胶体微粒的尺寸与可见光波长相当,当光通过胶体时,会发生散射。
这种散射使胶体呈现出特殊的光学效应,如乳光现象。
3. 水合性许多胶体微粒表面带有亲水基团,使得它们与水分子之间发生相互作用。
这种水合性使得胶体能够在水中稳定存在,并且能够吸附水分。
四、胶体的应用胶体具有广泛的应用领域。
以下是一些常见的应用:1. 食品工业胶体在食品工业中被广泛应用,如明胶用于制作果冻、冻糕等食品,乳胶用于制作巧克力、奶油等。
2. 药物制剂许多药物制剂中含有胶体。
这是因为胶体能够保护药物分子,延长其在体内的作用时间。
3. 化妆品胶体在化妆品中起着很重要的作用。
乳液、凝胶等化妆品中的胶体可以使得化妆品更易于使用和涂抹,并且对皮肤具有保湿作用。
高一化学必修一知识点化学胶体

高一化学必修一知识点化学胶体1、胶体的定义:分散质粒子直径大小在10-9~10-7m之间的分散系。
2、胶体的分类:①.根据分散界定质微粒组成的状况分类:如:胶体胶粒是由许多汇聚等小分子聚集一起形成的微粒,其直径在1nm~100nm之间,这样的胶体叫粒子胶体。
又如:淀粉属高分子化合物,其单个分子的直径约在1nm~100nm范围之内,这样的胶体叫分子胶体。
②.根据分散剂的状态划分:如:烟、云、雾等的分散剂为气体,这样的胶体叫做气溶胶;AgI溶胶、溶胶、溶胶,其分散剂为水,分散剂胶体为液体的胶体叫做液显色;有色玻璃、烟水晶均以固体为分散剂,这样的胶体叫做固溶胶。
3、胶体的制备A.物理方法①机械法:利用机械磨碎法将固体固体直接磨成胶粒的大小②溶解法:高分子化合物分散在合适的溶剂中形成胶体,如蛋白质溶于水,淀粉溶于水、聚乙烯熔于某氯气等。
B.化学方法①水解促进法:FeCl3+3H2O(沸)=(胶体)+3HCl②复分解反应法:KI+AgNO3=AgI(胶体)+KNO3Na2SiO3+2HCl=H2SiO3(胶体)+2NaCl思考:若上述两种反应物的量两类中均为大量,则可观察到什么现象?如何表达对应的两个反应方程式?提示:KI+AgNO3=AgI↓+KNO3(黄色↓)Na2SiO3+2HCl=H2SiO3↓+2NaCl(白色↓)4、胶体的性质:①丁达尔效应——丁达尔效应是粒子对光散射作用的结果,是一种物理现象。
丁达尔现象产生的其原因,是因为胶体微粒直径大小恰当,当光照射胶粒上时,胶粒将光从各个方面全部反射,胶粒即成前段光源(这一现象叫光的热辐射),故可明显地看到由小光源形成的光亮“通路”。
当光照在比较大或小的颗粒或微粒上则无此现象,只发生反射或将光全部吸收的现象,而以溶液和浊液无丁达尔现象,所以丁达尔效应常用于鉴别胶体和其他分散系。
②布朗运动——在胶体中,由于胶粒在各个方向所受的力不能相互平衡而产生运动无规则的的,称为布朗运动。
胶体化学

胶体的制备
分散法
凝聚法
机械法 电分散法 超声分散法 胶溶法
化学凝聚法 物理凝聚法
采用物理手段
采用化学手段
胶体化学的应用领域
轻工业:造纸、织物、陶瓷、涂料、黏合剂 等。 油田开发:钻井液中颗粒大小的控制、流变 性、稳定性、絮凝作业、粘土分散雨防塌等。 农业:土壤中的离子交换、土壤团粒、农药 的乳化与分散等。 生物学与医学:生物流变学、血液学、电泳、 渗透与膜、各种凝胶、病毒、蛋白质等。
日用品的生产与使用:洗涤剂、化妆品等。
环境科学:气溶胶、烟雾、水净化、 污水处理等。 分析化学:离子交换、胶束增溶、 浊度、吸附指示剂、脱色等。 材料:水泥、纤维、橡胶等。
海洋科学:稀有元素的吸附提取、 污染油膜的处理。
胶体前沿
碟状胶体:软物质的新兴前沿
微纳米碟状胶体的研究发展近况,侧重于合成、自组装和 它们在软凝聚态物质及材料科学中的角色.
胶体未来发展着重方向
添加剂、助剂以及表面活性剂的多品种开发
涂浮剂的分散稳定 胶体与界面现象的深入研究 与产品外观提高相关的产品在胶体领悟的相关研究
谢谢观看
胶体化学
应化144
胶体的发现
胶体这个名词史由英国科学家 Thomas Graham(1861 年 ) 提出来的。
他用的仪器极为简单,将一块羊皮纸缚在一个玻璃筒上, 筒里装着要试验的溶液,并把筒浸在水中。Graham 用此 种装置研究许多物质的扩散速度,发现有些物质,如糖、 无机盐、尿素等扩散快,很容易自羊皮纸渗析出来;另一 下物质,如明胶、氢氧化铝、硅酸等扩散很慢,不能或很 难透过羊皮纸。前一类物质当溶剂蒸发时易于形成晶体析 出,后一类物质则不能结晶,大多成无定形胶状物质。于 是, Graham 把后一类物质称为胶体( Colloid ),其 溶液称之为溶胶。胶体源自希腊文的 κολλα(胶)。
胶体化学

的形状对胶体性质有重要影响。
胶粒的形状
例如:(1)聚苯乙烯胶乳是球形质点
(2) V2O5 溶胶是带状的质点 (3) Fe(OH)3 溶胶是丝状的质点
§14.5 溶胶的稳定和聚沉
溶胶是热力学不稳定系统,但有些溶胶却能在相 当长时间内稳定存在。 1、溶胶的经典稳定理论—DLVO理论 胶体带电是其稳定存在的主要原因 (1)胶团之间既存在引力势能,也存在斥力势能。
例1:AgNO3 + KI→KNO3 + AgI↓ 过量的 KI 作稳定剂 胶团的结构表达式 : [(AgI)m n I – (n-x)K+]x– xK+ 胶核 胶粒(带负电) 胶团的图示式: 胶核 胶粒
胶团
胶团(电中性)
例2:AgNO3 + KI → KNO3 + AgI↓
过量的 AgNO3 作稳定剂
溶胶的电动现象体现在以下四个方面: 电泳:在外电场作用下,胶体粒子在分散介质中定 向移动的现象。
1、溶胶的电动现象 电渗:在多孔膜(或毛细管)两端施加一定电压,
液体将通过多孔膜而定向移动。在外电场作用下,胶
体粒子相对静止,分散介质定向移动的现象。 流动电势:在外力的作用下,迫使液体通过多孔膜 (或毛细管)定向流动,多孔膜两端所产生的电势差 沉降电势:分散相粒子在重力场或离心力场的作用
的最简便的方法。
光散射现象 当光束通过分散系统时,一部分自由地通过,一 部分被吸收、反射或散射。 入射光频率与分子的固有频率相同时,吸收 入射光波长小于分散粒子尺寸时,反射
入射光波长大于分散粒子尺寸时,散射
散射光的强度可利用瑞利公式进行计算
2、瑞利公式 I=
9π2V 2C
2λ4l 2
2 n2 - n 0 2 ( 2 ) (1 + cos2α)I0 2 n + 2n 0
化学:《胶体》课件-鲁科版必修1

均一、稳定
能
不能
胶体的提纯 其原理为胶体微粒不能透过半透膜,而溶液中的分子和离 子能透过半透膜。 利用半透膜把胶体中混有的离子或分子从胶体溶液里分离 的操作,叫做渗析。
淀粉胶体和 Na Cl溶液于半透膜 内
应用: 胶体净化提纯, 使胶体和溶液 分离
蒸镏水
3、胶体的性质 (1)、丁达尔现象(光学性质) 实验:光束分别通过Fe(OH)3胶体和CuSO4溶液,观察现象。
重要胶粒带电的一般规律:
带正电荷胶粒 金属氢氧化物 金属氧化物 带负电荷胶粒 金属硫化物(如Sb2S3) 非金属硫化物(如As2S3) 水泥 泥沙 硅酸胶体 土壤
拓展思考:胶体为什么能够稳定存在?
胶体为什么能稳定存在?
例题:已知土壤胶体中的粒子带负电荷,又有很 大的表面积,因而具有选择吸附能力。 有下列阴 阳离子,NH +、K+、H+、NO -、H PO -、PO 34 3
2
4
4
哪些易被吸附?在土壤里施用含氮量相同的下列
肥料,肥效较差的是 : (NH4)2SO4 、 NH4HCO3 、
NH4NO3 NH4Cl
(3)、胶体的聚沉
使胶体微粒凝聚成更大的颗粒,形成沉淀,
胶体形成沉淀析出的现象叫胶体的聚沉。 Q:如何破坏胶体的稳定状态
?
A.加入可溶性盐
实例: ①豆浆里加盐卤(MgCl2· 6H2O)或石膏 (CaSO4· 2H2O)溶液使之凝聚成豆腐; ②在江河与海的交汇处形成的沙洲。
1.分散系: (1)定义 把一种(或多种)物质分散在另 一种(或多种)物质中所得到的 体系
分散质: 被分散的物质(可以是固、液、气) 分散剂: 起容纳分散质作用的物质(可以是固、液、 气)
化学中胶体知识点总结

化学中胶体知识点总结一、胶体的定义和性质1. 胶体的定义胶体是由两种或多种物质组成的混合物,其中至少有一种物质分散在另一种物质中形成胶体颗粒。
这些颗粒的直径范围在1~1000纳米之间,与溶液中的溶质颗粒直径相当。
2. 胶体的性质(1)悬浮性:胶体颗粒在溶剂中形成悬浮系统,不会很快沉淀下来。
(2)分散性:胶体颗粒的分散程度较高,不容易团聚。
(3)不可过滤性:胶体颗粒的大小与溶质颗粒相近,不容易通过过滤器。
(4)光学性质:胶体颗粒对光有一定的散射和吸收作用,显示出乳白或彩色。
(5)电性质:胶体颗粒可以带电,形成电性胶体。
(6)表面效应:胶体颗粒的表面活性较高,与外界有较强的相互作用。
二、胶体的形成和稳定1. 胶体的形成胶体的形成是由于两种或多种物质之间的相互作用所导致的。
常见的胶体形成方式包括:(1)机械法:通过机械方式混合两种或多种物质而形成的胶体。
(2)凝聚法:由于凝聚或凝聚抑制作用导致的胶体形成。
(3)化学法:由化学反应而形成的胶体,如溶胶凝胶法。
2. 胶体的稳定胶体颗粒在溶液中往往会因为分散力和聚合力的作用而发生团聚,影响胶体的稳定性。
为了稳定胶体颗粒,通常采用以下方法:(1)增加分散剂:通过增加分散剂的使用量来提高胶体颗粒的分散性。
(2)控制电荷:通过改变胶体颗粒的表面电荷来调控其相互作用,从而提高稳定性。
(3)控制溶液条件:通过调节溶液的pH值、温度等条件来影响胶体颗粒的稳定性。
三、胶体的分类1. 根据分散介质的性质,胶体可分为溶胶、凝胶和胶体溶液。
溶胶是指液体中形成的胶体,凝胶是指固体中形成的胶体,胶体溶液是指固体和液体相混合形成的胶体。
2. 根据胶体颗粒的大小,胶体可分为溶胶胶体(颗粒直径小于1纳米)、胶体(颗粒直径1~1000纳米)和胶束(颗粒直径大于1000纳米)。
3. 根据分散相和连续相之间的互作用,胶体可分为溶胶性胶体和胶凝性胶体。
溶胶性胶体是指分散相和连续相间的互作用力比较弱,易于分散;胶凝性胶体是指分散相和连续相间的互作用力比较强,不容易分散。
胶体化学
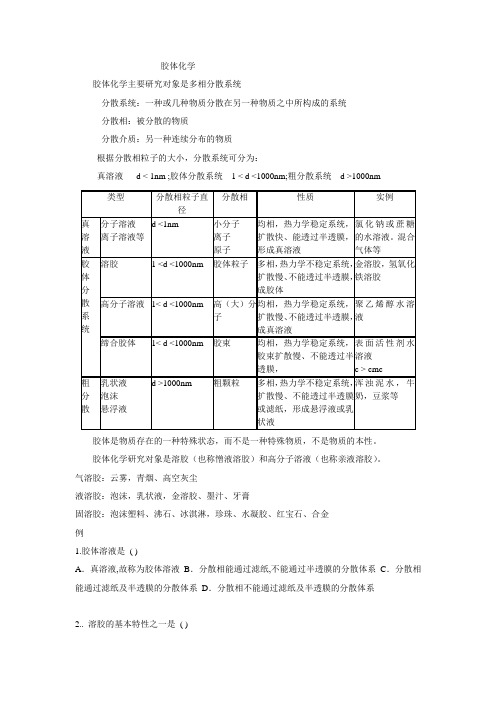
胶体化学胶体化学主要研究对象是多相分散系统分散系统:一种或几种物质分散在另一种物质之中所构成的系统分散相:被分散的物质分散介质:另一种连续分布的物质根据分散相粒子的大小,分散系统可分为:真溶液 d < 1nm ;胶体分散系统 1 < d <1000nm;粗分散系统 d >1000nm胶体是物质存在的一种特殊状态,而不是一种特殊物质,不是物质的本性。
胶体化学研究对象是溶胶(也称憎液溶胶)和高分子溶液(也称亲液溶胶)。
气溶胶:云雾,青烟、高空灰尘液溶胶:泡沫,乳状液,金溶胶、墨汁、牙膏固溶胶:泡沫塑料、沸石、冰淇淋,珍珠、水凝胶、红宝石、合金例1.胶体溶液是( )A.真溶液,故称为胶体溶液B.分散相能通过滤纸,不能通过半透膜的分散体系C.分散相能通过滤纸及半透膜的分散体系D.分散相不能通过滤纸及半透膜的分散体系2.. 溶胶的基本特性之一是( )A.热力学上和动力学上皆属于稳定体系B.热力学上和动力学上皆属不稳定体系C.热力学上不稳定而动力学上稳定体系D.热力学上稳定而动力学上不稳定体系3.. 雾属于分散体系,其分散介质是( )A.液体B.气体C.固体D.气体或固体4. 将高分子溶液作为胶体体系来研究,因为它( )A.是多相体系B.热力学不稳定体系C.对电解质很敏感D.粒子大小在胶体范围内5. 溶胶与大分子溶液的区别主要在于( )A.粒子大小不同B.渗透压不同C.丁达尔效应的强弱不同D.相状态和热力学稳定性不同6. 下列物系中,不属于胶体的是( )A.云雾B.烟C.珍珠D.空气7. 对于胶体与大分子溶液( )A.都属于同类的分散体系B.两者的分散相质点均能通过滤纸,因此都属于均相混和物C.胶体属于介稳体系,大分子溶液属于稳定体系D.粘度都大1.溶胶的制备与净化1).溶胶制备的一般条件:(1)分散相在介质中的溶解度必须极小(2)必须有稳定剂存在2).胶体的制备方法:(1)凝聚法: ①蒸气凝聚法,②过饱和法(2)分散法: ①胶体磨, ②气流粉碎机(又称喷射磨)③电弧法—用于制备贵金属的水溶胶2.溶胶的光学性质1).光散射(1)丁达尔效应:以一束强光射入溶胶后,在入射光的垂直方向可以看到一道明亮的光带,被称为丁达尔效应光本质是电磁波,当光波作用到介质中小于光波波长的粒子上时,粒子中的电子被迫振动(其振动频率与入射光波的频率相同),成为二次波源,向各个方向发射电磁波,这就是散射光波也就是我们看到的散射光。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
膜两侧离子的浓度差:
,此时渗透压为: 。
1
什么是毛细管现象,解释之
2
如何增大固体表面润湿程度
3
解释为何形成过饱和溶液
4
如何测定固体表面张力
5
BET双分子层的吸附直线式,及成立的条件
表面吸附量与表面张力关系
中 为溶溶液粘度液的特性粘度,与溶液粘度 、溶剂粘度 和溶液浓度c的的关系亦表示如上; 、 为与溶剂性质、大分子柔性有关的常数。
p应注意:1、 值的大小与温度有关,测定时需保持定温;2、本方法是相对方法,需要首先用标准方法(渗透压或光散射法)确定出标准试样的分子量;3、
8、何为接触角?并说明影响接触角的主要因素。
五、试用相分离模型推导An-M+n型表面活性剂溶液胶束形成过程的标准自由能变量与临界胶束浓度的理论关系式。
答:根据相分离模型的,每个胶束的形成被认为是新相的形成,设每个胶束分子的形成需要j个表面活性剂分子的参与,则平衡时:
;
平衡常数为 ,式中a为相应的活度。
每1mol表面活性剂分子参与反应的标准自由能变可通过如下方式计算:
胶体化学
一、问答题与简述题
1、何为胶体?何为单分散胶体?制备单分散胶体常采取哪些措施?
答:1)粒度在1—1000nm范围的分散相粒子称为胶体。
2)颗粒大小形状组成完全一样的胶体称为单分散胶体。
3)①使晶核形成期和生长期分开。爆发性成核或种晶法(先制备高度分散的胶体作为晶种,放入过饱和溶液,只发生晶核生长)。②避免颗粒聚结。利用双电层排除作用;利用凝胶结构;使用保护剂,如加入高分子物质,吸附在颗粒上,阻止期直接接触。③尽量选择由扩散控制晶核生长的体系。
②以 对p作直线,求出斜率和截距进而求出常数b和饱和吸附量 ;
③通过气体的分子截面积σ,饱和吸附量 ,进而求出固体的比表面积 。
四、适用DLVO理论解释胶体体系在一定时间内能稳定存在的原因。
答:疏液胶体粒子间既有因粒子带电形成的扩散双电层交联时产生的静电排斥力,又有粒子间van der waals力相互吸引作用,此两作用与粒子间的距离有关。当粒子间的排斥能大于吸引能时,胶体体系稳定;当吸引能大于排斥能时,粒子发生聚集,胶体体系破坏。
2、比表面自由能的热力学定义?物理意义?
答:1)热力学定义:改变单位面积所引起的热力学能变化。其定义式为: ,式中 为比表面自由能, 为Gibbs自由能, 为面积。
2)物理意义:①在()T,P,n,i条件下,可逆改变第i种界面单位面积而其他界面不变时,体系自由能的变化值。②是表面过剩量。
3、何为HLB值?说明表面活性剂亲水亲油强弱与HLB值大小的关系。
,
生成的胶束浓度很低,则有 , ,相平衡时的离子浓度为临界胶束浓度CMC, ,则:
。
六、在膜之一侧胶体RNa浓度为c1,并假设完全解离。(1)若膜之另一侧为纯水,求其渗透压?(2)若膜之另侧放浓度为c2的NaCl溶液,求其渗透压?
解:(1)当膜的两侧分别为RNa和纯水时,如右图所示:左侧的 要向膜右侧扩散,为维持溶液电中性,右侧必然有等量的 进入左侧,则平衡后的离子分布如右下图所示。
6、如何估测胶体溶剂化层的厚度?
答:根据增比粘度与溶剂化层的厚度的关系式:
,
式中 为增比粘度,与溶液粘度 、溶剂粘度 的关系如上; ,为溶剂化前质点的体积分数。r为胶体的半径,通过测定胶体分散系的粘度 ,从而可以估算得到溶剂化层的厚度 。
7、粘度法测定高分子分子量时应注意什么问题?
答:粘度法测定高分子分子量的公式为:
答:1)接触角的定义:当气液固三相在固体表面接触并达到平衡时,气液界面与固液界面之间所成的夹角 被称为接触角。
2)影响因素:①滞后现象②固体表面的粗糙度③吸附作用。
9、浓分散体系存在哪几种流型?并写出各流型的流变方程。
答:1)牛顿流体τ=ηD(水,甘油等)
2)塑性流体τ-τy=η塑D(其中τy屈服力,η塑塑性粘度)
二、请说明单分子膜可能存在的物理状态及其状态方程。
答:①气态膜:理想气态膜 ;
非理想气态膜 和 。
2液态扩张膜:
3转变膜
4液态凝聚膜: ;
5固态膜:
三、试写出Langmuir固—气单分子层吸附直线式,说明成立的条件,并具此理论设计一个测定固体比表面积的实验方案。
答:1)Langmuir单分子层吸附直线式, ,
其中,p平衡时的分压;
:单分子层的饱和吸附量;
b:与吸附量有关的常数。
2)成立的条件:
①任何吸附分子的几率不受临近有无吸收分子的影响——吸收分子之间无相互作用;
②无论分子吸附在表面的哪个位置,所释放出的热量是一样的——表面是均匀的;
③只有撞在空白表面上的分子才可能被吸附——吸附式单分子层的。
3)①测定一定温度下某气体在膜固体上的吸附数据p和V(g/g)
根据Donnan平衡的原理:
,带入各离子浓度,其中 ,得到: ,当 很小时有: 。此时计算渗透压:
膜两侧离子的浓度差:
,此时渗透压为: 。
(2)当膜的两侧分别为RNa和NaCl时,如右图所示:右侧的 要向膜左侧扩散,为维持溶液电中性,右侧必然有等量的 进入左侧,则平衡后的离子分布如右下图所示。
根据Donnan平衡的原理:
粒子总作用能U为排斥能Ui与吸引能Um之和,均为粒子间距离h的函数。从粒子间总作用能U与粒子间距离h关系曲线上看出,当h减小时,出现第一个极小值时,势能谷浅,聚沉的聚集体易分散;继续减小时,出现峰值,在峰值附近,总作用能U大于0,即排斥能大于吸引能,此时胶体体系稳定;当h继续减小时,U开始小于0,体系不再稳定。当图上的峰值即势垒足够大时,可阻止粒子进一步接近,使聚沉不再发生,使体系稳定。所以胶体在一定时间内能稳定存在。
答:1)HLB值为亲水亲油平衡值,是相对值。
2)HLB值越大,亲水性越强。
4、球形肥皂泡附加压力与半径的关系?
答: 其中, 为附加压力,R为半径, 为比表面自由能。
5、何为胶体增溶作用?说明特点。
答:1)表面活性剂提高难溶物在水中的溶解度的现象叫胶体增溶作用。
2)特点:①表面活性剂浓度大于后才有明显增溶作用。②增溶作用是个自发过程,被增溶后物质化学势下降。③增溶与溶解不同:溶解会使体系依数性明显变化,而增溶后体系依数性没有明显变化,因为溶胶数目无变化,只是增大胶束。④增溶后不存在两相,溶液透明。⑤增溶作用是可逆平衡过程。
3)假塑流型流Biblioteka τ=kDn(0<n<1)(k稠度)
4)胀流型流体τ= kDn(n>1)
10、简述高分子对胶体稳定性的影响。
答:1)空间稳定性①体积限制效应(高分子表面有吸附层,有弹性斥力)②渗透压效应(中间吸附层可交错使高分子溶液聚集,溶剂易渗入产生渗透压)
2)絮凝作用,桥聚作用。一般规律:当浓度低或是高分子分子量大时,絮凝作用;浓度高或是高分子分子量小时,稳定作用
