高中化学电荷守恒,物料守恒,质子守恒的写法
化学中三大守恒式资料讲解

化学中三大守恒式如何写化学中三大守恒式(电荷守恒,物料守恒,质子守恒)这三个守恒的最大应用是判断溶液中粒子浓度的大小,或它们之间的关系等式。
知识点诠释:知识点一:电荷守恒,--即溶液永远是电中性的,所以阳离子带的正电荷总量=阴离子带的负电荷总量例,NH4Cl溶液,NH4+ + H+ = Cl- + OH-写这个等式要注意2点:1、要判断准确溶液中存在的所有离子,不能漏掉(除六大强酸,四大强碱外都水解)。
2、注意离子自身带的电荷数目。
如,Na2CO3溶液:Na+ + H+ = 2CO32- + HCO3- + OH-NaHCO3溶液:Na+ + H+ = 2CO32- + HCO3- + OH-NaOH溶液:Na3PO4溶液:知识点二:物料守恒,--即加入的溶质组成中存在的某些元素之间的特定比例关系,由于水溶液中一定存在水的H、O元素,所以物料守恒中的等式一定是非H、O元素的关系。
例,NH4Cl溶液,化学式中N:Cl=1:1,即得到,NH4+ + NH3.H2O = Cl-Na2CO3溶液,Na:C=2:1,即得到,Na+ = 2(CO32- + HCO3- + H2CO3)NaHCO3溶液,写这个等式要注意,把所有含这种元素的粒子都要考虑在内,可以是离子,也可以是分子。
知识点三:质子守恒(两种方法)1、电荷守恒-物料守恒=质子守恒NH4Cl溶液,电荷守恒:NH4+ + H+ = Cl- + OH-物料守恒:NH4+ + NH3.H2O = Cl-质子守恒:H+ = OH- + NH3.H2ONa2CO3溶液,电荷守恒:物料守恒:质子守恒:2、质子守恒就是氢离子守恒,即溶液当中的溶质和溶剂得失氢离子要相等写出下列中的质子守恒NH4Cl溶液:Na2CO3溶液:例题:1、在0.1 mol·L-1NaHCO3溶液中有关粒子浓度关系正确的是A.c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-)B.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)C.c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)D.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)2、关于Na2CO3溶液,下列关系不正确的是A、c(Na+)>2c(CO32-)B、c(Na+)>c(CO32-)>c(H CO3-)>c(OH—)C、c(Na+)>c(CO32-)>c(OH—)>c(H CO3-)>c(H2CO3)D、c(Na+)+c(H+)=c(OH—)+c(H CO3-) +2c(CO32-)3、25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是A、c(NH4+)=c(SO42-)B、c(NH4+)>c(SO42-)C、c(NH4+)<c(SO42-)D、c(OH-)+c(SO42-)=c(H+)+(NH4+)习题:1、(2011江苏高考)下列有关电解质溶液中微粒的物质的量浓度关系正确的是A. 在0.1 mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)B. 在0.1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-) + 2c(H2CO3-)C. 向0.2 mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+)D. 常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol·L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)2、(2011广东高考)对于0.1mol·L-1 Na2SO3溶液,正确的是A. 升高温度,溶液的pH降低B. c(Na+)=2c(SO32―)+ c(HSO3―)+ c(H2SO3)C. c(Na+) + c(H+) = 2c(SO32―)+ 2c(HSO3―) + c(OH―)D. 加入少量NaOH固体,c(SO32―)与c(Na+)均增大3、下列溶液中微粒的物质的量关系正确的是A. 将等物质的量的KHC2O4和H2C2O4溶于水配成溶液:2c(K+)=c(HC2O4-) +c(H2C2O4)B. ① 0.2mol/L NH4Cl溶液、②0.1mol/L (NH4)2Fe(SO4)2溶液、③0.2mol/LNH4HSO4溶液、④0.1 mol/L (NH4)2CO3溶液中,c(NH4+)大小:③>②>①>④C. 0.1 mol/L CH3COONa溶液与0.15 mol/L HCl等体积混合:c(Cl―)>c(H+)>c(Na+)>c(CH3COO―)>c(OH―)D. 0.1 mol/L 的KHA溶液,其pH=10, c(K+)>c(A2―)>c(HA―)>c(OH―)。
高中化学电荷守恒-物料守恒-质子守恒的写法复习课程

如何写化学中三大守恒式(电荷守恒,物料守恒,质子守恒)这三个守恒的最大应用是判断溶液中粒子浓度的大小,或它们之间的关系等式。
电荷守恒--即溶液永远是电中性的,所以阳离子带的正电荷总量=阴离子带的负电荷总量例:NH4Cl溶液:c(NH+ 4)+ c(H+)= c(Cl-)+ c(OH-)写这个等式要注意2点:1、要判断准确溶液中存在的所有离子,不能漏掉。
2、注意离子自身带的电荷数目。
如,Na2CO3溶液:c(Na+)+ c(H+)= 2c(CO2- 3)+ c(HCO- 3)+ c(OH-) NaHCO3溶液:c(Na+)+ c(H+)= 2c(CO2- 3) + c(HCO- 3)+ c(OH-) NaOH溶液:c(Na+) + c(H+)= c(OH-)Na3PO4溶液:c(Na+) + c(H+) = 3c(PO3- 4) + 2c(HPO2- 4) + c(H2PO- 4) + c(OH-)物料守恒--即加入的溶质组成中存在的某些元素之间的特定比例关系,由于水溶液中一定存在水的H、O元素,所以物料守恒中的等式一定是非H、O元素的关系。
例:NH4Cl溶液:化学式中N:Cl=1:1,即得到,c(NH+ 4)+ c(NH3•H2O) = c(Cl-)Na2CO3溶液:Na:C=2:1,即得到,c(Na+) = 2c(CO32- + HCO3- +H2CO3) NaHCO3溶液:Na:C=1:1,即得到,c(Na+) = c(CO32-)+ c(HCO3-)+ c(H2CO3)写这个等式要注意,把所有含这种元素的粒子都要考虑在内,可以是离子,也可以是分子。
质子守恒--即H+守恒,溶液中失去H+总数等于得到H+总数,利用物料守恒和电荷守恒推出。
实际上,有了上面2个守恒就够了,质子守恒不需要背。
例如:NH4Cl溶液:电荷守恒:c(NH4+) + c(H+) = c(Cl-) + c(OH-)物料守恒:c(NH4+) + c(NH3•H2O) = c(Cl-)处理一下,约去无关的Cl-,得到,c(H+) = c(OH-) + c(NH3•H2O),即是质子守恒Na2CO3溶液:电荷守恒:c(Na+) + c(H+) = 2c(CO2- 3) + c(HCO- 3) + c(OH-)物料守恒:c(Na+) = 2c(CO32- + HCO3-+H2CO3)处理一下,约去无关的Na+,得到,c(HCO3-) + 2c(H2CO3) + c(H+) = c(OH-),即是质子守恒同样,可以得到其它的。
电荷守恒、物料守恒、质子守恒知识
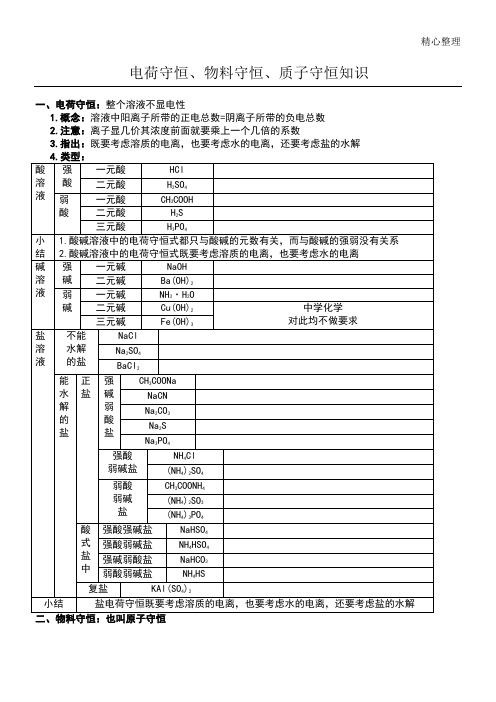
精心整理电荷守恒、物料守恒、质子守恒知识
一、电荷守恒:整个溶液不显电性
1.概念:溶液中阳离子所带的正电总数=阴离子所带的负电总数
2.注意:离子显几价其浓度前面就要乘上一个几倍的系数
3.指出:既要考虑溶质的电离,也要考虑水的电离,还要考虑盐的水解
在电解质溶液中,某些离子能够发生水解或者电离,变成其它离子或分子等,这虽然可使离子的种类增多,但却不能使离子或分子中某种特定元素的原子的数目发生变化,因此应该始终遵循原子守恒。
1.某一种原子(团)的数目守恒:
若已知以下各电解质的浓度均为0.1mol/L
1.概念:。
化学中三大守恒式

如何写化学中三大守恒式(电荷守恒,物料守恒,质子守恒)这三个守恒得最大应用就是判断溶液中粒子浓度得大小,或它们之间得关系等式。
知识点诠释:知识点一:电荷守恒,--即溶液永远就是电中性得,所以阳离子带得正电荷总量=阴离子带得负电荷总量例,NH4Cl溶液,NH4+ + H+ = Cl- + OH-写这个等式要注意2点:1、要判断准确溶液中存在得所有离子,不能漏掉(除六大强酸,四大强碱外都水解)。
2、注意离子自身带得电荷数目。
如,Na2CO3溶液:Na+ + H+ = 2CO32- + HCO3- + OH-NaHCO3溶液:Na+ + H+ = 2CO32- + HCO3- + OH-NaOH溶液:Na3PO4溶液:知识点二:物料守恒,--即加入得溶质组成中存在得某些元素之间得特定比例关系,由于水溶液中一定存在水得H、O元素,所以物料守恒中得等式一定就是非H、O元素得关系。
例,NH4Cl溶液,化学式中N:Cl=1:1,即得到,NH4+ + NH3、H2O = Cl-Na2CO3溶液,Na:C=2:1,即得到,Na+ = 2(CO32- + HCO3- + H2CO3)NaHCO3溶液,写这个等式要注意,把所有含这种元素得粒子都要考虑在内,可以就是离子,也可以就是分子。
知识点三:质子守恒(两种方法)1、电荷守恒-物料守恒=质子守恒NH4Cl溶液,电荷守恒:NH4+ + H+ = Cl- + OH-物料守恒:NH4+ + NH3、H2O = Cl-质子守恒:H+ = OH- + NH3、H2ONa2CO3溶液,电荷守恒:物料守恒:质子守恒:2、质子守恒就就是氢离子守恒,即溶液当中得溶质与溶剂得失氢离子要相等写出下列中得质子守恒NH4Cl溶液:Na2CO3溶液:例题:1、在0、1 mol·L-1NaHCO3溶液中有关粒子浓度关系正确得就是A、c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-)B、c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)C、c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)D、c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)2、关于Na2CO3溶液,下列关系不正确得就是A、c(Na+)>2c(CO32-)B、c(Na+)>c(CO32-)>c(H CO3-)>c(OH—)C、c(Na+)>c(CO32-)>c(OH—)>c(H CO3-)>c(H2CO3)D、c(Na+)+c(H+)=c(OH—)+c(H CO3-) +2c(CO32-)3、25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液得pH=7时,下列关系正确得就是A、c(NH4+)=c(SO42-) B、c(NH4+)>c(SO42-)C、c(NH4+)<c(SO42-) D、c(OH-)+c(SO42-)=c(H+)+(NH4+)习题:1、(2011江苏高考)下列有关电解质溶液中微粒得物质得量浓度关系正确得就是A、在0、1 mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)B、在0、1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-) + 2c(H2CO3-)C、向0、2 mol·L-1NaHCO3溶液中加入等体积0、1 mol·L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+)D、常温下,CH3COONa与CH3COOH混合溶液[pH=7,c(Na+)=0、1 mol·L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)2、(2011广东高考)对于0、1mol·L-1 Na2SO3溶液,正确得就是A、升高温度,溶液得pH降低B、c(Na+)=2c(SO32―)+ c(HSO3―)+ c(H2SO3)C、c(Na+) + c(H+) = 2c(SO32―)+ 2c(HSO3―) + c(OH―)D、加入少量NaOH固体,c(SO32―)与c(Na+)均增大3、下列溶液中微粒得物质得量关系正确得就是A、将等物质得量得KHC2O4与H2C2O4溶于水配成溶液:2c(K+)=c(HC2O4-) +c(H2C2O4)B、① 0、2mol/L NH4Cl溶液、②0、1mol/L (NH4)2Fe(SO4)2溶液、③0、2mol/LNH4HSO4溶液、④0、1 mol/L (NH4)2CO3溶液中,c(NH4+)大小:③>②>①>④C、 0、1 mol/L CH3COONa溶液与0、15 mol/L HCl等体积混合:c(Cl―)>c(H+)>c(Na+)>c(CH3COO―)>c(OH―)D、 0、1 mol/L 得KHA溶液,其pH=10, c(K+)>c(A2―)>c(HA―)>c(OH―)。
高中化学知识点—电荷守恒、 物料守恒、 质子守恒定律解析

高中化学知识点—电荷守恒、物料守恒、质子守恒定律解析电荷守恒即溶液永远是电中性的,所以阳离子带的正电荷总量=阴离子带的负电荷总量。
例:NH4Cl溶液:c(NH+ 4)+c(H+)= c(Cl-)+ c(OH-)写这个等式要注意2点:1、要判断准确溶液中存在的所有离子,不能漏掉。
2、注意离子自身带的电荷数目。
如:Na2CO3溶液:c(Na+)+ c(H+)= 2c(CO32-)+ c(HCO3-)+ c(OH-)NaHCO3溶液:c(Na+)+ c(H+)= 2c(CO32-) + c(HCO3-)+ c(OH-)NaOH溶液:c(Na+) + c(H+) =c(OH-)Na3PO4溶液:c(Na+) + c(H+) = 3c(PO43-) + 2c(HPO42-) + c(H2PO4-) + c(OH-)物料守恒即加入的溶质组成中存在的某些元素之间的特定比例关系,由于水溶液中一定存在水的H、O元素,所以物料守恒中的等式一定是非H、O元素的关系。
例:NH4Cl溶液:化学式中N:Cl=1:1,即得到,c(NH4+)+ c(NH3?H2O) = c(Cl-)Na2CO3溶液:Na:C=2:1,即得到,c(Na+) = 2c(CO32- + HCO3- + H2CO3)NaHCO3溶液:Na:C=1:1,即得到,c(Na+) = c(CO32-)+ c(HCO3-) + c(H2CO3)写这个等式要注意,把所有含这种元素的粒子都要考虑在内,可以是离子,也可以是分子。
质子守恒即H+守恒,溶液中失去H+总数等于得到H+总数,或者水溶液的由水电离出来的H+总量与由水电离出来的OH-总量总是相等的,也可利用物料守恒和电荷守恒推出。
实际上,有了上面2个守恒就够了,质子守恒不需要背。
例如:NH4Cl溶液:电荷守恒:c(NH4+) + c(H+) = c(Cl-) + c(OH-)物料守恒:c(NH4+)+ c(NH3?H2O)= c(Cl-)处理一下,约去无关的Cl-,得到,c(H+) = c(OH-) + c(NH3?H2O),即是质子守恒。
电荷守恒、物料守恒、质子守恒知识讲解

c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
例2 : NaHCO3溶液 方法一:可以由电荷守恒和物料守恒关系联立得到
NaHCO3 溶液中存在下列等式 C(H+)+C(Na+)=C(HCO3-)+2C(CO32-)+C(OH-) {电荷守恒} C(Na+)=C(HCO3-)+ C(CO32-)+C(H2CO3) {物料守恒}
NaOH溶液:
C(Na+)+C(H+)= C(OH-)
二.物料守恒
溶液中某一组分的原始浓度应该等于它在溶液 中各种存在形式的浓度之和。
也就是元素守恒,即变化前后某种元素的原子
个数守恒。物料守恒实际属于原子个数守恒和质量 守恒。即加入的溶质组成中存在的某些元素之间的 特定比例关系,由于水溶液中一定存在水的H、O 元素,所以物料守恒中的等式一定是非H、O元素 的关系。
练习
NaH2PO4溶液
原始物种:H2PO4-,H2O 消耗质子产物:H3PO4 产生质子产物:HPO42-(产生一个质子),
PO43-(产生二个质子),OH-
c(H+)=c(HPO42-)+2c(PO43-)+c(OH-)-c(H3PO4)
快速书写质子守恒的方法:
第一步:确定溶液的酸碱性,溶液显酸性,把 氢离子浓度写在左边,反之则把氢氧根离子浓度写 在左边。
第二步:根据溶液能电离出的离子和溶液中存 在的离子,来补全等式右边。具体方法是,判断溶 液能直接电离出的离子是什么。然后选择能电离产 生氢离子或者水解结合氢离子的离子为基准,用它 和它电离或者水解之后的离子(这里称为对比离子) 做比较,是多氢还是少氢,多N个氢,就减去N倍 的该离子(对比离子)浓度。少N个氢离子,就减 去N倍的该离子(对比离子)。
电荷守恒、物料守恒、质子守恒综述

电荷守恒、物料守恒、质子守恒综述电荷守恒,物料守恒,质子守恒同为溶液中的三大守恒关系。
这三个守恒的最大应用是判断溶液中粒子浓度的大小,或它们之间的关系等式。
电荷守恒:是指溶液中所有阳离子所带的正电荷总数与所有阴离子所带的负电荷总数相等。
即溶液永远是电中性的,所以阳离子带的正电荷总量=阴离子带的负电荷总量1.溶液必须保持电中性,即溶液中所有阳离子所带的电荷数等于所有阴离子所带的的电荷数2.除六大强酸,四大强碱外都水解,多元弱酸部分水解。
产物中有分步水解产物。
3.这个离子所带的电荷数是多少,离子前就写几。
例如:Na2CO3:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO3 2-)因为碳酸根为带两个单位负电荷,所以碳酸根前有一个2。
在下列物质的溶液中CH3COONa:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)Na2CO3:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO3 2-)NaHCO3:c(Na+)+c(H+)=c(HCO3-)+2(CO32-)+c(OH-)Na3PO4:c(Na+)+c(H+)=3c(PO4 3-)+2c(HPO4 2-)+c(H2PO4-)+c(OH-)电荷守恒定律:物理学的基本定律之一。
它指出,对于一个孤立系统,不论发生什么变化,其中所有电荷的代数和永远保持不变。
电荷守恒定律表明,如果某一区域中的电荷增加或减少了,那么必定有等量的电荷进入或离开该区域;如果在一个物理过程中产生或消失了某种符号的电荷,那么必定有等量的异号电荷同时产生或消失。
注意:1.正确分析溶液中存在的阴、阳离子是书写电荷守恒式的关键,需要结合电解质电离及盐类的水解知识,尤其是对多级电离或多级水解,不能有所遗漏。
如Na2CO3溶液中存在如下电离和水解平衡:Na2CO3 2 Na+ +CO32-;CO32-+ H2OHCO3-+OH-;HCO3- +H2O H2CO3 +OH-;H2O H++OH- 。
高中化学三守恒

高中化学三大守恒:电荷守恒、物料守恒、质子守恒一、电荷守恒:溶液永远呈电中性;阳离子带的正电荷总量=阴离子带的负电荷总量..例:NH4Cl溶液:cNH+4+ cH+= cCl-+ cOH-写这个等式要注意2点:1、要判断准确溶液中存在的所有离子;不能漏掉..2、注意离子自身带的电荷数目..如NaOH溶液:cNa+ + cH+= cOH-Na2CO3溶液:cNa++ cH+= 2cCO2-3+ cHCO-3+ cOH-练习:1、请写出CH3COONa溶液中的电荷守恒式:2、请写出H2SO4溶液中的电荷守恒式:3、请写出KHCO3溶液中的电荷守恒式:二、物料守恒--即加入的溶质组成中存在的某些元素之间的特定比例关系;由于水溶液中一定存在水的H、O元素;所以物料守恒中的等式一定是非H、O元素的关系..例:NH4Cl溶液:化学式中N:Cl=1:1;即得到;cNH+4+ cNH3H2O = cCl-Na2CO3溶液:Na:C=2:1;即得到;cNa+ = 2cCO2-3+ HCO-3+ H2CO3NaHCO3溶液:Na:C=1:1;即得到;cNa+ = cCO2-3+ cHCO-3+ cH2CO3写这个等式要注意;所有含这种元素的粒子都要考虑在内;既可以是离子;也可以是分子..三、质子守恒--即H+守恒;溶液中失去H+总数等于得到H+总数;利用物料守恒和电荷守恒推出..实际上;有了上面2个守恒就够了;质子守恒不需要背..例:NH 4Cl 溶液:电荷守恒:cNH + 4 + cH += cCl - + cOH -物料守恒:cNH + 4 + cNH 3 H 2O = cCl -处理一下;约去无关的Cl -;得到;cH + = cOH - + cNH 3 H 2O;即是质子守恒 Na 2CO 3溶液:电荷守恒:cNa + + cH + = 2cCO 2- 3 + cHCO - 3 + cOH -物料守恒:cNa + = 2cCO 2- 3 + HCO - 3 + H 2CO 3处理一下;约去无关的Na +;得到;cHCO - 3+ 2cH 2CO 3 + cH + = cOH -;即是质子守恒.. 另一种思路:Na 2CO 3溶液中;水电离出的cH + = cOH -;但是部分H +被CO 2- 3以1:1结合结合成HCO - 3;还有部分继续被HCO - 3结合成H 2CO 3;相当于被CO 2- 3以1:2结合;而OH -不变;所以得到cOH - = 原来总cH + = cHCO - 3 + 2cH 2CO 3 + 剩余cH + 即cOH - = cH ++cHCO - 3+2cH 2CO 3练习:请写出NH 4Cl 溶液中的物料守恒式: 练习1、在下列反应中;aXO4-+bY ―+cH +=dX 2++eY 2+8H 2O;化学计量数b 、d 分别为 A .5;6 B .10;2 C .6;2 D .10;52、0.5mol/L 的Na 2CO 3溶液中;下列有关离子浓度的叙述中;正确的是A 、cNa +:cCO 32- =2:1B 、cNa +>cCO 32->cHCO 3->cH +>cOH -C 、cNa ++cH +=cCO 32-+cHCO 3-+cOH -D 、cNa+=2cCO32-+cHCO3-+cH2CO33、常温时;将V1mL c1 mol/L 的醋酸滴加到V2mL c2 mol/L 的烧碱溶液中;下列结论正确的是A.若V1=V2;且混合溶液pH<7;则有c1<c2B.若V1=V2;c1=c2;则混合溶液中cNa+=cCH3COO-C.若混合溶液的pH=7;则有c1V1>c2V2D.若混合溶液的pH=7;则混合溶液中cNa+>cCH3COO-4、在25℃时;将pH=11的NaOH溶液与pH=3的CH3COOH溶液等体积混合后;下列关系式中正确的是A、c Na+=c CH3COO-+c CH3COOHB、c Na+>c CH3COO->c OH->c H+C、c H+=c CH3COO-+c OH-D、c CH3COO->c Na+>c H+>c OH-5、常温时;将V1mL c1mol/L的氨水滴加到V2mL c2mol/L的盐酸中;下述结论中正确的是A.若混合溶液的pH=7;则c1V1=c2V2B.若V1=V2;c1=c2;则混合液中cNH4+=cCl-C.若混合液的pH<7;则混合液中c Cl->cNH4+>CH+>COH-D.若V1=V2;且混合液的pH<7;则一定有c1<c26、等体积的下列溶液;阴离子的总浓度最大的是A 0.2mol/L K2SB 0.1mol/L BaOH2C 0.2mol/L NaClD 0.2mol/L NH42SO47、把0.02mol/LCH3COOH溶液和0.01mol/LNaOH溶液等体积混合;则混合溶液中微粒浓度关系错误的是A.cCH3COO->cNa+ B.cHAc>cAc-C.2cH+=cAc--cHAc D.cHAc+ cAc-=0.01mol/L9、一定温度下;Na2CO3溶液中Na+/CO32-=a;加入一定量的水稀释;稀释后溶液中Na+与CO32-之比A 大于aB 小于aC 等于aD 无法确定10、在0.1 mol/LNaHCO3溶液中有关粒子浓度关系正确的是a+>cHCO3->cCO32->cH+>cOH-a++cH+=cHCO3-+cCO32-+cOH-a++cH+=cHCO3-+2cCO32-+cOH-a+=cHCO3-+2cCO32-+cH2CO311、NH42CO3溶液中存在_______种粒子..试完成下列问题:1根据电荷守恒;写出一个用离子浓度表示的等式:;2根据水的电离;写出一个含有c H+和c OH-的等式:;3根据NH42CO3中;C、N原子个数关系;写出一个含有c NH4+和c CO32-的等式: ..。
化学中三大守恒式

如何写化学中三大守恒式(电荷守恒,物料守恒,质子守恒)这三个守恒的最大应用是判断溶液中粒子浓度的大小,或它们之间的关系等式。
知识点诠释:知识点一:电荷守恒,--即溶液永远是电中性的,所以阳离子带的正电荷总量=阴离子带的负电荷总量例,NH4Cl溶液,NH4+ + H+ = Cl- + OH-写这个等式要注意2点:1、要判断准确溶液中存在的所有离子,不能漏掉(除六大强酸,四大强碱外都水解)。
2、注意离子自身带的电荷数目。
如,Na2CO3溶液:Na+ + H+ = 2CO32- + HCO3- + OH-NaHCO3溶液:Na+ + H+ = 2CO32- + HCO3- + OH-NaOH溶液:Na3PO4溶液:知识点二:物料守恒,--即加入的溶质组成中存在的某些元素之间的特定比例关系,由于水溶液中一定存在水的H、O元素,所以物料守恒中的等式一定是非H、O元素的关系。
例,NH4Cl溶液,化学式中N:Cl=1:1,即得到,NH4+ + NH3.H2O = Cl-Na2CO3溶液,Na:C=2:1,即得到,Na+ = 2(CO32- + HCO3- + H2CO3) NaHCO3溶液,写这个等式要注意,把所有含这种元素的粒子都要考虑在内,可以是离子,也可以是分子。
知识点三:质子守恒(两种方法)1、电荷守恒-物料守恒=质子守恒NH4Cl溶液,电荷守恒:NH4+ + H+ = Cl- + OH-物料守恒:NH4+ + NH3.H2O = Cl-质子守恒:H+ = OH- + NH3.H2ONa2CO3溶液,电荷守恒:物料守恒:质子守恒:2、质子守恒就是氢离子守恒,即溶液当中的溶质和溶剂得失氢离子要相等写出下列中的质子守恒NH4Cl溶液:Na2CO3溶液:例题:1、在0.1 mol·L-1NaHCO3溶液中有关粒子浓度关系正确的是A.c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-)B.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)C.c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)D.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)2、关于Na2CO3溶液,下列关系不正确的是A、c(Na+)>2c(CO32-)B、c(Na+)>c(CO32-)>c(H CO3-)>c(OH—)C、c(Na+)>c(CO32-)>c(OH—)>c(H CO3-)>c(H2CO3)D、c(Na+)+c(H+)=c(OH—)+c(H CO3-) +2c(CO32-)3、25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是A、c(NH4+)=c(SO42-)B、c(NH4+)>c(SO42-)C、c(NH4+)<c(SO42-)D、c(OH-)+c(SO42-)=c(H+)+(NH4+)习题:1、(2011江苏高考)下列有关电解质溶液中微粒的物质的量浓度关系正确的是A. 在0.1 mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)B. 在0.1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-) + 2c(H2CO3-)C. 向0.2 mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+)D. 常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol·L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)2、(2011广东高考)对于0.1mol·L-1 Na2SO3溶液,正确的是A. 升高温度,溶液的pH降低B. c(Na+)=2c(SO32―)+ c(HSO3―)+ c(H2SO3)C. c(Na+) + c(H+) =2c(SO32―)+ 2c(HSO3―) + c(OH―)D. 加入少量NaOH固体,c(SO32―)与c(Na+)均增大3、下列溶液中微粒的物质的量关系正确的是A. 将等物质的量的KHC2O4和H2C2O4溶于水配成溶液:2c(K+)=c(HC2O4-) + c(H2C2O4)B. ①0.2mol/L NH4Cl溶液、②0.1mol/L (NH4)2Fe(SO4)2溶液、③0.2mol/L NH4HSO4溶液、④0.1 mol/L (NH4)2CO3溶液中,c(NH4+)大小:③>②>①>④C. 0.1 mol/L CH3COONa溶液与0.15 mol/L HCl等体积混合:c(Cl―)>c(H+)>c(Na+)>c(CH3COO―)>c(OH―)D. 0.1 mol/L 的KHA溶液,其pH=10,c(K+)>c(A2―)>c(HA―)>c(OH―)。
三大守恒

Na2CO3溶液: 溶液: (1) 物料守恒: 物料守恒: c(Na+) = 2[c(CO32-)+c(HCO3-)+c(H2CO3)] (2) 电荷守恒: 电荷守恒: c(Na+)+c(H+) = c(OH-)+c(HCO3-)+2c(CO32-) (3) 质子守恒: 质子守恒: c(OH-) = c(H+)+c(HCO3-)+2c(H2CO3) NaHCO3溶液: 溶液: (1) 物料守恒: 物料守恒: c(Na+) = c(CO32-)+c(HCO3-)+c(H2CO3) (2) 电荷守恒: 电荷守恒: c(Na+)+c(H+) = c(OH-)+c(HCO3-)+2c(CO32-) (3) 质子守恒: 质子守恒: c(H+)+c(H2CO3) = c(OH-)+c(CO32-)
练1、(2010江苏卷) 常温下, (2010江苏卷 常温下, 江苏卷) NaOH溶液 用 0.1000 mol·L NaOH溶液 滴定 20.00mL0.1000 mol·L CH3COOH溶液所得滴定曲 COOH溶液所得滴定曲 线如图。 线如图。下列说法正确的是 A.点①所示溶液中: 所示溶液中: c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+) B.点②所示溶液中: 所示溶液中: c(Na+)=c(CH3COOH)+c(CH3COO-) C.点③所示溶液中: 所示溶液中: c(Na+)>c(OH-)>c(CH3COO-)>c(H+) D.滴定过程中可能出现: 滴定过程中可能出现: c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
高中化学 水溶液中的三大守恒书写技巧

(1)电荷守恒:电解质溶液中阴离子所带电荷总数等于阳离子所带电荷总数,根据电荷守恒可准确、快速地解决电解质溶液中许多复杂的离子浓度问题。
(2)物料守恒:物质发生变化前后,有关元素的存在形式不同,但元素的种类和原子数目在变化前后保持不变,根据物料守恒可准确、快速地解决电解质溶液中复杂离子、分子物质的量浓度或物质的量的关系。
(3)质子守恒:在电离或水解过程中,会发生质子(H+)转移,但质子转移过程中其数量保持不变。
例子在下一页。
化学中三大守恒式资料讲解

化学中三大守恒式如何写化学中三大守恒式(电荷守恒,物料守恒,质子守恒)这三个守恒的最大应用是判断溶液中粒子浓度的大小,或它们之间的关系等式。
知识点诠释:知识点一:电荷守恒,--即溶液永远是电中性的,所以阳离子带的正电荷总量=阴离子带的负电荷总量例,NH4Cl溶液,NH4+ + H+ = Cl- + OH-写这个等式要注意2点:1、要判断准确溶液中存在的所有离子,不能漏掉(除六大强酸,四大强碱外都水解)。
2、注意离子自身带的电荷数目。
如,Na2CO3溶液:Na+ + H+ = 2CO32- + HCO3- + OH-NaHCO3溶液:Na+ + H+ = 2CO32- + HCO3- + OH-NaOH溶液:Na3PO4溶液:知识点二:物料守恒,--即加入的溶质组成中存在的某些元素之间的特定比例关系,由于水溶液中一定存在水的H、O元素,所以物料守恒中的等式一定是非H、O元素的关系。
例,NH4Cl溶液,化学式中N:Cl=1:1,即得到,NH4+ + NH3.H2O = Cl-Na2CO3溶液,Na:C=2:1,即得到,Na+ = 2(CO32- + HCO3- + H2CO3)NaHCO3溶液,写这个等式要注意,把所有含这种元素的粒子都要考虑在内,可以是离子,也可以是分子。
知识点三:质子守恒(两种方法)1、电荷守恒-物料守恒=质子守恒NH4Cl溶液,电荷守恒:NH4+ + H+ = Cl- + OH-物料守恒:NH4+ + NH3.H2O = Cl-质子守恒:H+ = OH- + NH3.H2ONa2CO3溶液,电荷守恒:物料守恒:质子守恒:2、质子守恒就是氢离子守恒,即溶液当中的溶质和溶剂得失氢离子要相等写出下列中的质子守恒NH4Cl溶液:Na2CO3溶液:例题:1、在0.1 mol·L-1NaHCO3溶液中有关粒子浓度关系正确的是A.c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-)B.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)C.c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)D.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)2、关于Na2CO3溶液,下列关系不正确的是A、c(Na+)>2c(CO32-)B、c(Na+)>c(CO32-)>c(H CO3-)>c(OH—)C、c(Na+)>c(CO32-)>c(OH—)>c(H CO3-)>c(H2CO3)D、c(Na+)+c(H+)=c(OH—)+c(H CO3-) +2c(CO32-)3、25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是A、c(NH4+)=c(SO42-)B、c(NH4+)>c(SO42-)C、c(NH4+)<c(SO42-)D、c(OH-)+c(SO42-)=c(H+)+(NH4+)习题:1、(2011江苏高考)下列有关电解质溶液中微粒的物质的量浓度关系正确的是A. 在0.1 mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)B. 在0.1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-) + 2c(H2CO3-)C. 向0.2 mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+)D. 常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol·L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)2、(2011广东高考)对于0.1mol·L-1 Na2SO3溶液,正确的是A. 升高温度,溶液的pH降低B. c(Na+)=2c(SO32―)+ c(HSO3―)+ c(H2SO3)C. c(Na+) + c(H+) = 2c(SO32―)+ 2c(HSO3―) + c(OH―)D. 加入少量NaOH固体,c(SO32―)与c(Na+)均增大3、下列溶液中微粒的物质的量关系正确的是A. 将等物质的量的KHC2O4和H2C2O4溶于水配成溶液:2c(K+)=c(HC2O4-) +c(H2C2O4)B. ① 0.2mol/L NH4Cl溶液、②0.1mol/L (NH4)2Fe(SO4)2溶液、③0.2mol/LNH4HSO4溶液、④0.1 mol/L (NH4)2CO3溶液中,c(NH4+)大小:③>②>①>④C. 0.1 mol/L CH3COONa溶液与0.15 mol/L HCl等体积混合:c(Cl―)>c(H+)>c(Na+)>c(CH3COO―)>c(OH―)D. 0.1 mol/L 的KHA溶液,其pH=10, c(K+)>c(A2―)>c(HA―)>c(OH―)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
如何写化学中三大守恒式(电荷守恒,物料守恒,质子守恒)
这三个守恒的最大应用是判断溶液中粒子浓度的大小,或它们之间的关系等式。
电荷守恒--即溶液永远是电中性的,所以阳离子带的正电荷总量=阴离子带的负电荷总量例:
+-- NH4Cl溶液:c(NH+ )+ c(H)= c(Cl)+ c(OH)4
写这个等式要注意2点:
1、要判断准确溶液中存在的所有离子,不能漏掉。
2、注意离子自身带的电荷数目。
如,
++- - Na2CO3溶液:c(Na)+ c(H)= 2c(CO2)+ c(HCO-)+ c(OH)33
++- - NaHCO3溶液:c(Na)+ c(H)= 2c(CO2) + c(HCO-)+ c(OH)33
NaOH溶液:c(Na) + c(H)= c(OH)
++- -- Na3PO4溶液:c(Na) + c(H) = 3c(PO3) + 2c(HPO2) + c(H2PO-) + c(OH)444
物料守恒--即加入的溶质组成中存在的某些元素之间的特定比例关系,由于水溶液中一定存在水的H、O元素,所以物料守恒中的等式一定是非H、O元素的关系。
例:
- NH4Cl溶液:化学式中N:Cl=1:1,即得到,c(NH+ )+ c(NH3?H2O) = c(Cl)4
+- Na2CO3溶液:Na:C=2:1,即得到,c(Na) = 2c(CO2 + HCO- + H2CO3) 33
+- NaHCO3溶液:Na:C=1:1,即得到,c(Na) = c(CO2)+ c(HCO-) + c(H2CO3) 33
写这个等式要注意,把所有含这种元素的粒子都要考虑在内,可以是离子,也可以是分子。
+++质子守恒--即H守恒,溶液中失去H总数等于得到H总数,利用物料守恒和电荷守恒推出。
