第十章 酶催化反应动力学
酶催化反应的动力学模拟与实验研究

酶催化反应的动力学模拟与实验研究酶催化反应是生物常见的化学反应之一,其在人类生命和健康中具有重要的作用。
酶催化反应的动力学模拟与实验研究,是一个非常有意义的课题。
本文将从酶催化反应的基本原理、动力学模拟方法、实验研究等方面进行探讨。
一、酶催化反应的基本原理酶是一种特殊的蛋白质分子,可以加速化学反应的进行而不改变反应自身的本质。
在酶催化反应中,酶与反应物发生作用,形成酶-底物复合物,接着发生化学反应,生成产物。
该反应过程遵循酶动力学原理,即反应速率与反应物浓度、酶浓度等因素有关。
二、酶催化反应的动力学模拟方法酶催化反应的动力学模拟常用的方法有两种:基于玻尔兹曼方程的分子动力学模拟和基于传统动力学方法的酶cinética模拟。
基于玻尔兹曼方程的分子动力学模拟是一种从分子层面模拟酶催化反应过程的方法。
该方法主要针对酶-底物复合物的形成、分子振动、化学反应等方面进行模拟研究。
通过该方法,可以精确描述反应过程中分子的能量、位移、速度等信息,揭示反应从活性位置到产物生成的全过程。
基于传统动力学方法的酶kinética模拟是一种通过数学模型描述酶催化反应过程的方法。
该模型基于酶动力学原理,考虑反应物浓度、酶浓度、反应速率等多个因素,建立了酶催化反应的动力学模型。
该方法主要研究反应过程中的热力学特性,如反应速率的变化、转移态的分析等。
三、酶催化反应的实验研究酶催化反应的实验研究是将酶在一定反应条件下挑战不同反应物,探索反应过程中的动力学特性、产物性质等信息。
实验研究中,对于反应物浓度、pH值、温度等条件进行控制,再加入一定量的酶,观察反应过程中产生的产物种类和数量,并通过实验数据拟合等手段,解析酶催化反应的动力学性质。
四、酶催化反应的应用酶催化反应在生产和科研中具有广泛应用。
例如,在医疗领域中,酶催化反应可以用于新型药物的合成和分离纯化等方面;在食品工业中,酶催化反应可以用于酿造和加工过程中的催化处理和防腐鲜等领域;在环境领域中,酶催化反应可用于废水的处理和固体废物降解等方面。
第10章 酶促反应动力学

用这些数据求丝氨酸脱水酶的表观米氏常数。 解:1、v对[S]作图法:
v
丙 酮 0.3 酸
Vm
0.2 Vm 2 0.1
Vmax=0.36 1/2Vmax=0.18 Km=3.210-7
M/20min
0
1
2
3
4
5
6
7
8 10-6 [S]
解2、1/v 对1/[S]作图法:
[S]
0.20 0.40 0.85 1.25 1.70 2.00 8.00
说:当酶催化反应时,酶首先与底物结合,生成酶-底物复合物,
然后生成产物,并释放出酶。
V
Vmax
[S] 当底物浓度较低时 反应速度与底物浓度成正比;反 应为一级反应。
V
Vmax
[S]
随着底物浓度的增高 反应速度不再成正比例加速;反应 为混合级反应。
V
Vmax
[S]
当底物浓度高达一定程度 反应速度不再增加,达最大速度; 反应为零级反应
[S] 1000km 100km 10km 4km 3km v 0.999V 0.99V 0.91V 0.8V 0.75V
1km
0.10km
0.5V
0.091V
(5)判断反应方向或趋势:催化正逆反应的酶,其正逆 两向的反应的Km不同。如果正逆反应的底物浓度相当,则
反应趋向于Km小方向进行。
4、Vmax
磺胺药物的抑菌作用
增效联磺(抗菌增效剂-甲氧苄氨嘧啶(TMP))能特异地抑制细 菌的二氢叶酸还原为四氢叶酸,故能增强磺胺药的作用。
(四)一些重要的抑制剂
• 1、不可逆抑制剂
①有机磷化合物:与酶活性直接有关的丝氨酸羟基共价结合,从而抑制
酶催化反应的动力学和热力学模型

酶催化反应的动力学和热力学模型酶催化反应是生命体系中关键的一环,它在细胞代谢、信号传导、免疫反应等生命活动中发挥着至关重要的作用。
酶催化反应的动力学和热力学模型则是研究这些反应本质和控制机制的关键工具。
本文将介绍酶催化反应的动力学和热力学背景,探讨几种常见的酶催化反应模型,并简述大分子反应的特点及控制机制。
一、酶催化反应的动力学和热力学背景酶催化反应是指在生物体内,酶作为催化剂促进化学反应的进行。
酶能够显著降低反应所需的能垒,从而提高反应速率。
这是因为酶与底物之间形成的酶底物复合物能够在化学反应中提供一个更加稳定的、能量较低的过渡态,从而降低反应所需的能量和活化能。
在酶催化反应中,反应速率是非常重要的一个参数。
反应速率和底物浓度、酶浓度、反应温度等因素相关,因此需要建立反应速率的动力学模型。
此外,酶催化反应的热力学特性也是研究的关键点之一,热力学模型的建立可以帮助我们理解反应的驱动力和热力学限制。
二、几种常见的酶催化反应模型1. 米高斯-明茨动力学模型米高斯-明茨动力学模型是最早提出的酶动力学模型之一。
这个模型假设底物结合酶的速率比化学反应速率快很多,因此酶底物复合物的形成是反应速率的控制步骤。
当底物浓度很低时,酶活性不会受到抑制。
但是随着底物浓度的增加,酶活性会逐渐达到饱和,反应速率也会趋于常数。
2. 酶抑制模型酶抑制模型是一种描述酶和抑制剂之间互作关系的动力学模型。
抑制剂可以直接地或者通过结合酶活性部位抑制酶的活性。
在酶活性被抑制的情况下,反应速率呈现非线性关系,其动力学方程可以写成一个双曲线形式。
3. 酶电化学模型酶电化学模型结合了动力学和电化学的理论,描述酶催化反应的电化学过程和催化剂对电极反应动力学的影响。
这种模型在电化学和生物传感领域有着广泛的应用。
三、大分子反应的特点及控制机制除了小分子酶催化反应,大分子反应也是生物体系中一种重要的反应类型。
大分子反应包括蛋白质合成和降解、DNA复制和修复等过程。
酶催化反应动力学

• 在一定条件下每种酶都
有其催化反应的最适温
度。
图 温度对酶促反应速度的影响
• 最适温度不是酶的特征物理常数,相反它常常受 到其他各种条件如底物种类、作用时间、pH和离 子强度等因素影响。如最适温度随酶促反应进行 时间的长短而改变,这是因为温度使酶蛋白发生 变性效应是随时间而逐步累加的。
• 一般而言,酶促反应进行时间长时酶的最适温度 低,酶促反应进行时间短则最适温度高,所以只 有在规定的酶促反应时间内才可确定酶的最适温 度。
在不同pH条件下进行某种酶促化学反应, 然后将所测得的酶促反应速度相对于pH 来作图,即可得到钟罩形曲线。
图 pH对酶活力的影响
• 各种酶在一定条件下都有其特定的最适pH, 因此最适pH是酶的特性之一。
• 但是酶的最适pH并不是一个常数,它受诸 如底物种类和浓度、缓冲液种类和浓度等 众多因素的影响,因此只有在一定条件下 最适pH才有意义。
• 如抑制剂调节、共价修饰调节、反馈调节、酶原 激活及激素控制等。
• 某些酶催化活力与辅酶、辅基及金属离子有关。
2. 酶促反应动力学
研究各种因素对酶促反应速度的影响, 对阐明酶作用的机理和建立酶的定量方法都 是重要的。
影响因素包括有 酶浓度、底物浓度、pH、温度、 抑制剂、激活剂等。
研究某一因素对酶反应速度的影响时,必须使 酶反应体系中的其他因素维持不变,而单独变动 所要研究的因素。
• 酶所表现的最适温度是上述两种影响综合作用的 结果。
在较低的温度范围内, 酶催化反应速率会随着 温度的升高而加快,超 过某一温度,即酶被加 热到生理允许温度以上 时,酶的反应速率反而 随着温度的升高而下降。
这是由于温度升高,虽然可加速酶的催化反应速率, 同时也加快了酶的热失活速率。
酶工程第10章固定化酶催化的动力学特征)

一些酶在溶液中和固定化后的米氏常数值
酶
底物
固定化试剂
肌酸激酶 乳酸脱氢酶 α-糜蛋白酶 无花果蛋白酶 胰蛋白酶
ATP NADH N-乙酰酪氨酸乙酯 N-苯酰精氨酸乙酯 苯酰精氨酰胺
无(溶液酶) 对氨苯基纤维素
当 Da <<1时,酶催化的最大反应速度要大大 慢于底物的传质速率,此时该反应过程由反应动 力学控制;当 Da>>1时,底物的传质速率大大慢 于酶催化的最大反应速度,此时该反应过程由传 质扩散控制。
外扩散限制效应
(2)作图法求[S]i值和Vi值
根据 Vm[S]i
Km [S]i
kLa ([S]0
[S ]0
[S]0 [S]0
外扩散限制效应
引入 [S] [S]i , K K m ,并定义 Da Vm ,
[S ]0
[S ]0
k L a [S ]0
[S ]i
Vm [S]0 1 [S]i
kLa [S]0 K m [S]i
[S ]0
[S]0 [S]0
Da [S] 1 [S] K [S]
Viห้องสมุดไป่ตู้
Vm [S ]0 Km [S]0
V0
在这种情况下,酶反应速度不受传质速率的 影响,为该酶的本征反应速度,或称在此条件下 可能达到的最大反应速度,用V0表示。
外扩散限制效应
当外扩散传质速率很慢,而酶表面上的反应 速度很快,此时传质速率成为限制步骤。固定化 酶外表面上的底物浓度趋于零,有
Vi k L a[S ]0 Vd max
kLa ([S]0
[S]i )
酶催化反应动力学概况课件

目 录
• 酶催化反应动力学概述 • 酶催化反应的速率方程 • 酶促反应的速率常数与酶活性 • 酶促反应的抑制剂与激活剂 • 酶催化反应的动力学应用
01
酶催化反应动力学概述
酶的定义与特性
总结词
酶是一种生物催化剂,具有高度专一性和高效性的特性,能够加速生物体内的 化学反应。
03
利用酶的催化作用可以构建生物传感器,用于检测生物分子或
小分子物质,用于医学诊断和环境监测。
酶催化反应在农业领域的应用
有机肥料生产
利用酶催化反应可以将农业废弃物转化为有机肥料,提高土壤肥 力。
生物农药
通过酶的催化作用可以合成具有杀虫、杀菌或除草功能的生物农药 ,减少化学农药的使用。
转基因作物
通过基因工程技术将酶编码基因导入作物中,以提高作物的抗逆性 、产量和品质。
蛋白质工程
通过酶催化反应对蛋白质进行定向进化或改造,以优化蛋白质的性 能,应用于生物医学、工业和农业等领域。
酶催化反应在医药领域的应用
药物研发
01
酶催化反应可用于合成新药或优化现有药物的合成路线,降低
药物的生产成本。
疾病诊断
02
某些酶的活性与某些疾病相关,通过检测酶的活性可以用于疾
病的诊断。
生物传感器
金属离子
如Mg^2+、Zn^2+等, 能够通过提供催化活性所 需的电子或稳定酶的结构 来促进酶促反应。
蛋白质
如蛋白激酶等,能够通过 磷酸化等方式激活酶的活 性。
抑制剂与激活剂的应用
药物研发
通过抑制或激活特定的酶来治疗疾病。
生物工程
在发酵工程、酶工程等领域中,利用抑制剂与激 活剂来调控酶促反应过程。
酶催化反应动力学分析

酶催化反应动力学分析酶是生物体内最常见的催化剂,能够加速化学反应的速率,使化学反应在生命体内发生。
酶结构复杂,需要在特定的温度、pH值和离子浓度等条件下才能发挥最佳催化作用。
酶催化反应动力学分析是研究酶催化反应特性和机理的重要手段。
本文将对酶催化反应动力学分析进行探讨。
一、酶催化反应动力学酶催化反应动力学是研究酶催化反应速率的学科,主要关注酶催化反应的速率常数。
速率常数即反应速度与物质浓度之间的关系。
酶催化反应基本上遵循米氏动力学(Michaelis-Menten,简称M-M)方程。
M-M方程是描述酶催化反应速率的一种数学表达式。
其中,Vmax表示酶反应速率的最大值,Km表示酶与底物结合能力的常数。
酶对底物的亲和力越强,则Km值越小,酶在底物浓度足够大的条件下,其反应速率趋向于最大值Vmax。
当底物浓度为Km时,反应速率的一半为Vmax/2。
公式:V=Vmax*[S]/(Km+[S])其中,V表示反应速率,[S]表示底物浓度。
二、酶催化反应动力学分析过程1.测定酶反应速率酶催化反应速率可以通过测定产生的产物量或消耗的底物量来反应。
通常需要对底物和产物的浓度进行测定分析。
比如,在酶催化下,葡萄糖可以被转化为葡萄糖酸,可以通过测定葡萄糖和葡萄糖酸的浓度来反应酶的催化速率。
2.绘制酶反应速率曲线在实验中,通常会对不同底物浓度下的反应速率进行测定,并将反应速率与底物浓度绘制成曲线。
根据M-M方程,当底物浓度充分大时,反应速率趋向于最大值Vmax。
曲线的最大值即为酶反应速率的最大值Vmax,曲线的一半处即为酶的底物浓度Km。
3.计算酶催化常数通过实验测定的结果,可以计算出酶的催化常数。
其中,Km越小,表示酶与底物结合的亲和力越强,反应速率越快;Vmax则表示酶催化反应的最大速率,与酶的浓度和酶的催化效率有关。
三、酶催化反应动力学分析在生物学中的应用酶催化反应动力学分析是生物学领域中的重要研究方法之一。
酶催化反应机理的研究可以帮助我们理解生物反应的基本特性,例如代谢反应和细胞信号转导等。
酶工程 第十章 酶的催化特性与反应动力学 2013-2

½Vmax 分数级反应 一级反应 [S]<<K
零级反应 [S]>>K
K
[S]
当v = ½Vmax时,K=[S],即米氏常数,记做Km
35/138
3. 稳态学说
中间复合物假说
假定[ES]处于稳态中,即形成速率等于分解速率: k1[E][S]=k-1[ES]+k2[ES] k1[E][S] [ES]= k-1+k2 酶以ES形式存在的比例: [S] k-1+k2 +[S] k1
41/138
(4)直接线性作图法:
Vmax
Vmax (Vmax, Km)
v1
v2 [S]2 -[S]1 -[S]3
Km
42/138
(5)常用动力学数据处理方法的比较 Lineweaver-Burk法最常用,优点是v和[S]在不同轴上 ,但误差分布不均衡 直接线性作图法优点是v 和[S]直接表现在图线上,具有 统计合理性,可采用Vmax和Km的中位数。采用非线性回 归进行拟合,可得到最优Vmax和Km的值。
15/138
4. 酶专一性的确定
(1)选择底物,测定最适温度、pH等条件 (2)确定米氏常数Km和最大反应速度Vmax (3)选用结构类似物确定专一性 (4)相对专一性的酶确定几个底物的Km、Vmax (5)确定是否有立体异构专一性
16/138
(二)酶催化作用的效率高
转换数(每个酶分子每分钟催化底物转化的分子数)一般 103 min-1,β-半乳糖苷酶的转换数为12.5×103min-1, 碳酸酐酶的转换数达到3.6×107min-1 。 酶的催化作用可使反应速度提高107~1013倍 例如:H2O2的分解反应
H2O2 → H2O +
酶催化反应动力学(共49张PPT)

❖ 中间络合物学说最早是由 Henri和Wurtz两位科学家 提出的。
❖ 在1903年,Henri在用蔗 糖酶水解蔗糖实验研究化 学反响中底物浓度与反响 速度的关系时发现,当酶 浓度不变时,可以测出一 系列不同底物浓度下的化 学反响速度,以该反响速 度对底物浓度作图,可得 到如图3-2所示的曲线。
酶底物中间络合物学说
本质上来说就是酶的修饰抑制
竞争性抑制剂。 ⑴ Vm值降低,Km值不变;
3酶活力测定时需注意:
测定酶活力常用的方法:
❖ 有某些重金属离子如Ag 、Cu 、Hg 、Pb 等 K+、Na+、Ca2+、Mg2+、Zn2+及Fe2+
图3-1 酶促反响的速度曲线 测定酶活力常用的方法:
+
2+
2+
2+
对酶的抑制作用也属于这一类。 3激活剂对酶促反响速度的影响
1 竞争性抑制 2 非竞争性抑制 3 反竞争性抑制
①竞争性抑制(competitive inhibition) :
❖ 是最常见的一种可逆抑制作用。
❖ 大多数竞争性抑制剂与底物的结构相似,能与底
物竞争酶的活性中心,从而阻碍酶底物复合物的形 成,使酶的活性降低。这种抑制作用称为竞争性抑 制作用。 ❖ 其抑制程度取决于底物和抑制剂的相对浓度,可以 通过增加底物浓度的方法来解除这种抑制作用。
竞争性抑制反响模式
❖ 在竞争性抑制中,底物(S)或抑制剂(I)与酶(E)的结合
都是可逆的,因此存在着如下的化学平衡式:
[S]>>[I]:高浓度的底物可解除抑制
图3-5 竞争性抑制曲线
特点:
⑴ Vm值不变,(表观)Km值增大; ⑵ Km随抑制剂浓度[I]的增加而增加; ⑶双倒数作图所得直线相交于纵轴; ⑷抑制作用可以被高浓度的底物减低以致消除。
10章酶反应动力学-教学用

将实验测定的米-曼氏曲线的坐 标作平移,并用新坐标系 (x,y) 表示旧坐标系(v0,[S]),米-曼 氏方程可以转变为 xy = -Km 其 曲线为以坐标轴(x,y)为渐近线 的直角或等轴或等边双曲线
Vmax 2
从米-曼氏方程或其曲线可以看出三种情况:
当[ S ] [ K m ],v0 Vmax[ S ] Km
基于快速平衡模型或平衡稳态模型的米氏方程: 早年的米式方程 最初,Michaelis 和 Menten 根据“快速平衡假说”推出米式方程。 快速平衡假说:一些假设
k1 E S ES k-1
反应可逆,且很快达到平衡 限速步骤,K2 << K-1 P的生成不足以破坏快速平衡
k2 ES PE
5为初始底物浓度s的函数所做的底物饱和曲线也称米曼氏作图或米曼氏曲线将实验测定的米曼氏曲线的坐标作平移并用新坐标系xy表示旧坐标系v0s米曼氏方程可以转变为xykm其曲线为以坐标轴xy为渐近线的直角或等轴或等边双曲线从米曼氏方程或其曲线可以看出三种情况
第 10 章
教学内容
酶促反应动力学
酶促反应动力学: 研究酶促反应的速度及其影响因素的科学。为酶的机理研究提供实验 证据,指导酶在生产中的应用。
2. Kcat 的意义: 催化常数或转换数
3. Kact/KM 的意义: 催化效率指数或专一性常数
1. KM的意义: 真实解离常数和表观解离常数
① 米氏常数KM是 v0=1/2 Vmax时的底物浓度。遵循米-曼氏动力 学的酶,也称为米-曼型酶, 是指呈现v0对[S]的双曲线关系的酶。 ② KM的真实意义决定于酶促反应机制的特定方面, 如反应步骤 数目和各步的速率常数。对于简单的二步反应: KM=(K-1+K2)/K1 当K2是限速步骤的速率常数时,即k2<<k-1 ,KM即Ks。 此时, KM 的意义是真实解离常数,代表ES复合体中酶对 底物的亲和力大小, 但是这种意义对大多数酶是不适用的。 当 k2、k-1 相当时,KM是三个速率常数的函数。
酶催化反应动力学解析

酶催化反应动力学解析背景介绍:酶是一种生物催化剂,能够加速化学反应速率。
它们在许多生物体内起着至关重要的作用,包括代谢过程、信号转导、分子识别和DNA复制等。
了解酶催化反应动力学是理解生物学中许多关键过程的关键。
酶动力学:酶催化反应的动力学是关于酶催化反应速率与底物浓度、温度和pH等环境因素之间关系的研究。
通过实验测量酶活性并分析数据可以获得这些关系,这对我们理解和控制酶催化反应至关重要。
酶催化反应速率的表达式:酶催化反应速率可以用麦克斯韦-玛格努斯方程(Michaelis-Menten equation)来表达:v = Vmax * [S] / (Km + [S])其中,v是酶催化反应速率,[S]是底物浓度,Vmax是在无限大底物浓度下酶反应速率的最大值,Km是米氏常数,代表底物浓度为一半时的酶催化反应速率。
米氏常数Km的意义:酶的米氏常数Km反映了底物与酶之间相互作用的亲和力。
Km越小,酶的亲和力越大;Km越大,底物与酶的结合较弱。
Km值对于酶活性的影响非常重要,它决定了在给定底物浓度下酶催化反应速率的快慢。
酶催化反应速率与底物浓度的关系:麦克斯韦-玛格努斯方程中的[S] / (Km + [S]) 这一项表示底物浓度对酶催化速率的贡献。
当底物浓度远小于Km值时,可以简化为[S] / Km,速率与底物浓度成正比,速率随着底物浓度的增加而增加;当底物浓度远大于Km值时,可以简化为1,速率不再受底物浓度的影响。
酶反应速率对底物浓度的响应图像通常符合麦克斯韦-玛格努斯方程预测的双曲线形状。
图像的初始阶段速率随底物浓度线性增加,当底物浓度达到一定程度后,速率趋于平缓。
催化常数kcat:酶的催化常数kcat是与酶催化效率相关的参数。
它表示在单位时间内酶分子催化底物数量的能力。
kcat的大小与酶催化底物的速率相关,kcat越大,酶的催化效率越高。
抑制剂对酶催化动力学的影响:抑制剂是一种可以降低酶催化反应速率的物质。
第十章酶动力学

(二)可逆抑制作用: • 抑制剂以非共价键与酶分子可逆性 结合造成酶活性的抑制,且可采用 透析等简单方法去除抑制剂而使酶 活性完全恢复的抑制作用就是可逆 抑制作用。 • 可逆抑制作用包括竞争性、反竞争 性、和非竞争性抑制几种类型。
抑制程度是由酶与抑制剂之间的亲和力大 小、抑制剂的浓度以及底物的浓度决定。
四、pH对反应速度的影响
观察pH对酶促反应速度的影响,
通常为一“钟形”曲线,即pH过高 或过低均可导致酶催化活性的下降。 酶催化活性最高时溶液的pH值就 称为酶的最适pH。
pH对酶促反应速度的影响
木瓜蛋白酶
乙酰 胆碱 酯酶
人体内大多数酶的最适pH在6.5~ 8.0之间。 酶的最适pH不是酶的特征性常数。
与 图 形 特 征
反 竞 争 性 抑 制 的 速 度 方 程
反竞争性抑制的双倒数图形特征
• • • • •
反竞争性抑制的特点: ⑴ 反竞争性抑制剂的化学结构不一定与底物的 ⑵ 抑制剂与底物可同时与酶的不同部位结合; ⑶ 必须有底物存在,抑制剂才能对酶产生抑制 ⑷ 动力学参数:Km减小,Vm降低。
1. 反应体系中不加I。 2.反应体系中加入 一定量的不可逆抑 制剂。
v
1
2
3
3.反应体系中加入一定 量的可逆抑制剂。
4、可逆抑制强度与时间 无关,而不可逆抑制强 度与时间有关
[E]
v
[I ]→
v
[I ]
[E]
不可逆抑制剂的 作用 可逆抑制剂的作用
[E]
• 1.竞争性抑制(competitive inhibition): • 抑制剂与底物竞争与酶的同一活性中心结 合,从而干扰了酶与底物的结合,使酶的 催化活性降低,称为竞争性抑制作用。
第10章_酶动力学
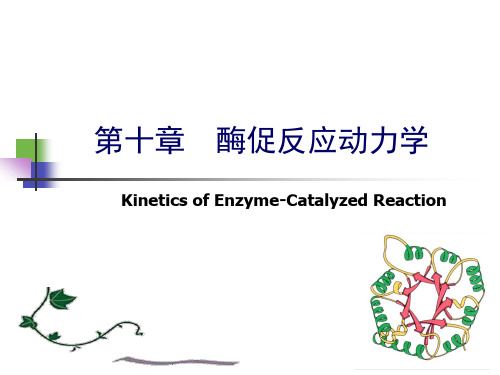
2.5 12.0 32.0
22
②可以判断酶的专一性和天然底物
已知,Km=(K2+K3)/K1 当:k3<<k2 (k3为限速步骤的速率常数) Km≈K2/K1 即,Km相当于ES分解为E+S的解离常数(Ks), Km代表酶对底物的亲和力。
Km值大表示亲和程度小,酶的催化活性低; Km值小表示亲和程度大,酶的催化活性高。
酶的转换数(k3)
定义 :当酶被底物充分饱和时,单位时间内 每个酶分子催化底物转变为产物的分 子数。 意义 :可用来比较每单位酶的催化能力。
30
3、 Km与V的求取
31
Km值与Vmax值可以通过作图法求取
(1)双倒数作图法(double reciprocal plot), 又称为 林-贝氏(Lineweaver- Burk)作图法 Vmax[S] Km+[S] 两边同取倒数 Km 1/V= 1/[S] + 1/Vmax Vmax (林-贝氏方程)
51
(1) 非专一性不可逆抑制剂
①重金属离子 Ag+ 、 Cu2+ 、 Hg2+ 、 Pb2+ 、 Fe3+ 高浓度时可使酶蛋白变性失活; 低浓度时对酶活性产生抑制。
——通过加入EDTA解除
52
②烷化剂(多为卤素化合物)
E+S
两个假设:
•
k1
k2
ES
k3
E+P
E与S形成ES复合物的反应是快速平衡反应,而 ES分解为E及P的反应为慢反应,反应速率取决 于慢反应即 V = k3[ES]。 (1)
•
S的总浓度远远大于E的总浓度,因此在反应的 初始阶段,S的浓度可认为不变即[S] =[St]。
10 酶促反应动力学-王镜岩生物化学(全)

½ Vmax
Vmax
[S]
Km
(2) 双倒数作图法 •将米氏方程式两侧取双倒数,以1/v-1/[s]作图,得出一直线.
1 V = Km Km+[S] Vmax[S] 1 V
竞 争 性 非 竞 争 性 抑 制 作 用 机 理 示 意 图
底物与酶专一性结合
竞争性抑制作用
非竞争性抑制作用
2、可逆抑制作用的动力学(重点)
(1)竞争性抑制的动力学特征
Vmax不变,Km增大Fra bibliotek竞争性抑制(competitive inhibition)
抑制剂化学结构与底物相似,因而与底物竞争 性地与酶活性中心结合
2. 激活剂对酶作用的特点
• (1)激活剂对酶的作用具有一定的选择 性 ;即一种激活剂对某种酶起激活作用, 而对另一种酶可能起抑制作用 • (2)有时金属离子之间也可相互替代 • (3)激活离子对于同一种酶,可因浓度 不同而起不同的作用,低浓度激活,高 浓度抑制
六、抑制剂对酶促反应速度 的影响(重点)
酶的活力单位
国际单位(IU):在标准条件下,
一分钟内催化1umol底物转化的酶 量为一个酶活力单位 Kat单位:在一定条件下,每 秒钟转化1mol底物所需的酶量
酶的比活力 酶的转换数
(Kcat)
每毫克蛋白所含酶的活力单位数
(常常作为酶制剂纯度的指标)
每秒钟、每个酶分子转换底物的 umol数
影响酶反应速度的因素
竞争性抑制
可逆抑制作用
非竞争性抑制
反竞争性抑制
酶催化反应机理和动力学

酶催化反应机理和动力学酶催化反应是生命体系中的重要过程,它们帮助维持了生物体所有复杂的代谢路径。
许多细胞机体必须通过酶催化来加速反应,使它们在体内发挥作用。
因此,了解酶催化反应的机理和动力学对于理解生物体系的基本原理和解决一些关键问题至关重要。
本文将从机理和动力学两个方面来讲述酶催化反应。
一、酶催化反应的机理酶是蛋白质的一种,能够提供活性位点来催化各种反应。
生物体系中酶的活性位点位置是非常特殊的,它们结合了反应物并促进反应。
酶是选择性的,只会催化特定的反应,这是由于酶结合位点的特殊性。
当分子接近酶的结合位点时,酶分子会形成一个复合物,这是反应的第一步。
与此同时,酶分子的活性位点就开始对反应物进行催化,这是由于它们存在与反应物化学键相互作用的基团。
当反应物结合到活性位点时,它们形成反应中间体,这是一个高能状态的中间体,使得反应能够发生。
如下所示:反应底物 + 酶 - > 过渡态中间体 - > 反应产物 + 酶除了活性位点的存在外,酶的结构上还有一些重要的特点,这些特点可以使酶以特定的方向选择性地催化反应。
例如,在某些酶中,即使存在两种互为镜像的底物,并且它们具有相同的化学性质,酶也只能选择其中的一种进行催化反应。
这常常是由于酶的立体化学结构和修饰功能造成的。
二、酶催化反应的动力学酶动力学涉及到酶反应速率和底物浓度之间的关系。
根据麦克斯韦玻尔兹曼分布定理,分子在系统中的浓度随着温度的升高而增大,从而提高了反应速率。
然而,上述分布定理仅仅适用于基础化学反应,无法解释酶催化反应。
在酶催化反应的过程中,酶并不会影响反应的热力学状态,而只会影响活化能。
这是由于酶的催化作用使得反应可以在更短的时间内完成,反应的全过程变得更加容易。
因此,酶催化反应的动力学表现为反应速率随酶浓度的增加而增加,同时也与反应底物的浓度有关。
一般来说,酶底物复合物的结合速率比较快,而反应产物的脱离速率较低。
因此,在浓度限制下,反应速率取决于底物浓度。
《酶促反应动力学》课件

底物浓度对反应速率的影响
总结词
随着底物浓度的增加,反应速率通常会加快,但当底 物浓度达到一定值后,反应速率将不再增加。
详细描述
底物是酶催化反应的对象,底物的浓度也会影响反应速 率。通常情况下,随着底物浓度的增加,反应速率会加 快。然而,当底物浓度达到一定值后,反应速率将趋于 稳定,不再增加。这是因为酶的活性位点有限,只能与 一定量的底物结合。
详细描述
酶促反应的活化能是酶促反应所需的最小能量,只有当底物获得足够的能量时,才能够 被酶催化发生反应。活化能的大小反映了酶促反应发生的难易程度,活化能越高,反应 越难以进行。通过实验测定活化能的大小,可以帮助我们了解酶促反应的动力学特征和
机制。
03
米氏方程与双倒数图
米氏方程的推导
总结词
米氏方程是描述酶促反应速度与底物浓 度关系的数学模型,通过实验数据和推 导,可以得出该方程的具体形式。
酶促反应动力学在药物代谢领域的应用,如研究药物在体内的代 谢过程和代谢产物的生成,有助于了解药物的作用机制和药效。
药物合成
在药物合成过程中,酶促反应动力学可用于优化药物合成 的反应条件和提高产物的纯度,降低副反应和废物产生。
在Hale Waihona Puke 境科学中的应用污染物降解酶促反应动力学可用于污染物降解领域,如有机污染物的 生物降解和重金属离子的转化,通过研究酶促反应动力学 参数,实现污染物的有效降解和转化。
温度对反应速率的影响
总结词
温度的升高通常会加快反应速率,但过高的温度可能导致酶失活。
详细描述
温度可以影响酶促反应的速率。一般来说,温度越高,分子间的运动越快,从而促进酶与底物的结合和反应的进 行。然而,过高的温度可能导致酶失活,从而降低反应速率。因此,选择合适的温度对于维持酶的活性和促进反 应的进行非常重要。
第十章 酶催化反应动力学 ppt课件

[ E ][ S ] [ ES ]
KM
反应体系的总酶量为:Et [E]S[E]
[E]SEt [E]Et KM [S [E ] ]S
经整理得: ES
Et S KM S
(1)
由于酶促反应速度由[ES]决定,即 vk2ES
将(2)代入(1)得:
v k2
Et S KM S
,所以 ES v
❖ 竞争性抑制 ❖ 非竞争性抑制 ❖ 反竞争性抑制 ❖ 混合性抑制
1.竞争性抑制(competitive inhibition)
(1)含义和反应式
抑制剂I和底物S结构相似,抑制剂I和底物S对游离酶E的结合有 竞争作用,互相排斥,已结合底物的ES复合体,不能再结合I。
(2)特点:
① 抑制剂I与底物S在化学结构上相似,能与底物S 竞争酶E分子活性中心的结合基团.
很强的专一性
绝对专一性 :一种酶只能催化一种化合物进行一种反应
相对专一性:一种酶能够催化一类具有相同化学键或基团的 物质进行某种类型的反应
反应专一性:一种酶只能催化某化合物在热力学上可能进行 的许多反应中的一种反应
底物专一性 :一种酶只能催化一种底物 立体专一性:一种酶只能作用于所有立体异构体中的一种
具有温和的反应条件
一般在生理温度25~37℃的范围,仅有少数酶 反应可在较高温度下进行。
在接近中性的pH值条件下进行
易变性与失活
蛋白酶的化学本质是蛋白质,因而具有蛋白质 的所有性质。
常因变性而使活力下降,甚至完全失活。 酶的变性多数为不可逆。
激活剂和抑制剂
激活剂:能提高酶活性的物质
1)无机离子:酶的辅因子;桥梁作用 2)中等大小的有机分子:还原剂;EDTA 3)蛋白质性质的大分子:激活酶原
酶催化反应动力学探究

酶催化反应动力学探究酶是生命体内的一类特殊蛋白质,具有高效、高特异性和高度选择性等特点。
它们在维持生命体的代谢和生物合成过程中发挥着至关重要的作用。
酶催化反应动力学研究的目的在于揭示酶在化学反应过程中的催化机制,为深入理解生命体代谢反应提供理论支持。
动力学的基本原理动力学是研究物质运动和变化的一门学科,它涉及到微观和宏观两个领域。
在化学反应中,动力学用于研究物质之间的相互作用,包括反应速率、反应机理和反应的平衡状态等。
其中,反应速率是反应动力学研究中最基本的性质,它是指在单位时间内反应物消耗的量或产物生成的量。
反应速率的表达式为:$v=k[A]^m[B]^n$式中,$v$表示反应速率,$k$为速率常数,$m$和$n$为反应物各自的反应级数,$[A]$和$[B]$分别表示反应物A和B的浓度。
酶催化反应的动力学反应速率的大小取决于反应物浓度、温度、压力等因素。
在生物体内,酶催化反应不同于无催化反应,它们的速率与反应物浓度之间的关系并不符合简单的反应速率公式,而呈现出酶浓度、底物浓度和酶底物复合物浓度之间的复杂关系。
这种复杂性是由于酶分子的独特结构和其与反应物间的相互作用导致的。
酶催化反应的动力学主要涉及到酶的催化机制、底物浓度、反应物结构和反应温度等方面。
酶的催化机制涉及到酶分子和底物之间的亲和力、酶分子的构象变化和活性位点的位置等的影响下,底物在酶分子活性位点上发生了一系列的催化反应,最终产生了产物。
底物浓度对酶反应的速率具有直接影响。
当底物浓度低于一定程度时,产物生成的速率可以与底物浓度无关;而当底物浓度达到一定程度时,反应速率将随底物浓度的增加而增加。
但当底物浓度过高时,反应速率将趋于饱和,即不再对底物浓度敏感。
反应物结构的特殊性也会影响反应速率。
某些底物分子的空间结构不利于试剂与复合物的形成,从而导致反应速率的降低。
而有些官能团的存在则能够优化反应物的结构,促进复合物的形成,从而增加反应速率。
酶催化反应动力学

酶催化反应动力学酶是生物体内一类非常重要的催化剂,可以加速化学反应的速率,而不影响反应的化学平衡。
酶催化反应动力学,即研究酶催化反应速率的变化规律以及影响反应速率的因素。
本文将重点介绍酶催化反应动力学的基本概念、实验方法和相关影响因素。
一、酶催化反应速率酶催化反应速率是反应物转化为产物的速度。
在酶催化下,反应速率明显增加,可以达到每秒数百倍甚至上千倍。
反应速率由酶的浓度、底物浓度、反应温度和pH值等因素决定。
酶催化反应速率通常遵循麦克斯韦-玛尔计算公式,即速率v等于最大反应速率vmax与反应物浓度[S]的比例关系:v = vmax[S] / (Km + [S])。
其中Km称为米氏常数,表示反应物浓度为一半时的速率。
当[S]远大于Km时,速率v ≈ vmax,此时反应速率近似与反应物浓度成正比;当[S]远小于Km时,速率v ≈vmax[S]/Km,此时反应速率与反应物浓度成线性关系。
二、酶催化反应的实验方法进行酶催化反应动力学研究,需要了解反应速率及其影响因素。
实验方法主要包括测定酶催化反应速率的变化和测定酶的两个重要参数:最大反应速率vmax和米氏常数Km。
1. 测定酶催化反应速率的变化测定酶催化反应速率的变化,可以通过观察底物消失或产物增加的速度来确定。
常用的方法包括光度法、荧光法、比色法等。
这些方法都是通过测量反应物和产物的光学性质的变化,建立光学性质与反应速率之间的关系,来间接确定反应速率。
2. 测定最大反应速率vmax测定最大反应速率vmax是了解酶催化能力的重要指标。
最常用的方法是通过实验测量不同底物浓度下的反应速率,并将速率与底物浓度作图。
根据麦克斯韦-玛尔计算公式,绘制速率-底物浓度曲线,可以确定最大反应速率vmax。
3. 测定米氏常数Km米氏常数Km是衡量底物与酶结合力的指标。
测定Km的常用方法是选择一种底物,通过实验测量不同底物浓度下的反应速率,并将速率与底物浓度作图。
绘制速率-底物浓度曲线,可以确定Km。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
ES
k1 k-1
ES
k2
k-2
EP
1、与底物浓度 [S]相比,酶的浓度 [E] 是很小的, 因而可忽略由于生成中间复合物[ES]而消耗的底物。
2、不考虑这个逆反应的存在 3、认为基元反应的反应速率最慢,为该反应速率 的控制步骤。 4、在一定时间内虽然[S]和[P]在不断变化,ES复 合体也在不断地生成和分解,但ES的生成速率 与分解速率接近相等,[ES]基本保持不变
非竞争性抑制 1 = (1+ 〔I〕 ) × Vi Ki ( Vmax 1
Km 1 + ) Vmax〔S〕
Vmax〔S Vi= 〔I 〕 ( Km+〔S ) ( 1+ ) Ki 〕 〕
3. 反竞争性抑制
(1)含义和反应式
反竞争性抑制剂必须在酶结合了底物之后才能与酶与 底物的中间产物结合,该抑制剂与单独的酶不结合。
快速平衡学说:米氏方程
S
ES k1 [ E ][S ] KM 反应快速建立平衡: k1 [ ES ]
Et ES
反应体系的总酶量为:Et
t
SE
k 1
k1
ES
P E
k2
[ ES ]
[ E ][S ] KM
[ ES] [ E]
具有温和的反应条件
一般在生理温度25~37℃的范围,仅有少数酶 反应可在较高温度下进行。
在接近中性的pH值条件下进行
易变性与失活
蛋白酶的化学本质是蛋白质,因而具有蛋白质 的所有性质。
常因变性而使活力下降,甚至完全失活。
酶的变性多数为不可逆。
激活剂和抑制剂
激活剂:能提高酶活性的物质
1)无机离子:酶的辅因子;桥梁作用 2)中等大小的有机分子:还原剂;EDTA 3)蛋白质性质的大分子:激活酶原
v Vm
Vm k2 Et
(4)
米氏常数的意义
(1)物理意义:Km值等于酶反应速度为最大速度一半时的底物 浓度。 (2)Km 值愈大,酶与底物的亲和力愈小;Km值愈小,酶与底 物亲和力愈大。酶与底物亲和力大,表示不需要很高的底物 浓度,便可容易地达到最大反应速度。 (3)Km 值是酶的特征性常数,只与酶的性质,酶所催化的底 物和酶促反应条件(如温度、pH、有无抑制剂等)有关,与酶 的浓度无关。酶的种类不同,Km值不同,同一种酶与不同底 物作用时,Km 值也不同。
第七章 酶的催化特性和反应动力学
7.1 酶的催化特性
能降低反应的活化能,加快生化反应的 速率 不改变反应的方向和平衡关系,即不能 改变反应的平衡常数,而只能加快反应 达到平衡的速率
7.1 酶的催化特性
(1)较高的催化效率 (2)很强的专一性 (3)具有温和的反应条件 (4)易变性与失活
很强的专一性
根据产生抑制的机理不同,可逆抑制分为:
竞争性抑制 非竞争性抑制 反竞争性抑制 混合性抑制
1.竞争性抑制(competitive inhibition)
(1)含义和反应式
抑制剂I和底物S结构相似,抑制剂I和底物S对游离酶E的结合有 竞争作用,互相排斥,已结合底物的ES复合体,不能再结合I。
(2)特点:
① 抑制剂I与底物S在化学结构上相似,能与底物 S竞争酶E分子活性中心的结合基团.
例如,丙二酸、苹果酸及草酰乙酸皆和琥珀酸的结构 相似,是琥珀酸脱氢酶的竞争性抑制剂。
②抑制程度取决于抑制剂与底物的浓度比、 〔ES〕和〔EI〕的相对稳定性; ③加大底物浓度,可使抑制作用减弱甚至消除。
(3)竞争性抑制剂的动力学方程 ki k1 k3 E+S ES E+P E+I k2
Et S K m S
由于酶促反应速度由[ES]决定,即 将(2)代入(1)得:
v k2 ES
,所以
ES
Et S v k2 K m S
所以
v
k2 Et S (3) Km S
v k2
(2)
当[Et]=[ES]时,
Vmax S v 将(4)代入(3),则: K m S
由米氏方程得:Km=
EI
①
〔E〕〔S〕
〔ES〕
〔E〕〔I〕 Ki= 〔EI〕
②
〔E〕=〔E〕t-〔ES〕-〔EI〕 ③
解方程①②③得: 〔E〕t
〔 I〕 (1 + )+1 Ki 〔 S〕 又因vi=k3〔ES〕,代入上式得:
Vi=
Km
〔ES〕=
Vmax〔S〕
Km (1 +
〔 I〕 )+〔S〕 Ki
绝对专一性 :一种酶只能催化一种化合物进行一种反应
相对专一性:一种酶能够催化一类具有相同化学键或基团的 物质进行某种类型的反应
反应专一性:一种酶只能催化某化合物在热力学上可能进行 的许多反应中的一种反应
底物专一性 :一种酶只能催化一种底物
立体专一性:一种酶只能作用于所有立体异构体中的一种
抑制剂:降低酶的催化活性甚至完全失活的 物质(区别于变性剂)
7.2.1 Michaelis-Menten 方程:快速平衡学说
ES
k1 k-1
ES
k2 k-2
EP
①与底物浓度 [S] 相比,酶的浓度 [E] 是很小的, 因而可忽略由于生成中间复合物[ES]而消耗的底物。 ②不考虑这个逆反应的存在(只适应于反应初期) ③认为基元反应的反应速率最慢,为该反应速率的 控制步骤, k-1>>k2,也就是说ES分解生成P的速率不足 以破坏E和ES之间的快速平衡
1
2.非竞争性抑制(non-competitive inhibition)
(1)含义和反应式 抑制剂I和底物S与酶E的结合完全互不相关,既不排 斥,也不促进结合,抑制剂I可以和酶E结合生成EI, 也可以和ES复合物结合生成ESI。底物S和酶E结合成ES 后,仍可与I结合生成ESI,但一旦形成ESI复合物,再 不能释放形成产物P。
k2 Et S (3) K M S
v k2
(2)
当[Et]=[ES]时,
Vmax S v 将(4)代入(3),则: K m S
v Vm
Vm k2 Et
(4)
7.2.1 Briggs-Haldane 方程:拟稳态学说
1925年Briggs G. E.和Haldane J. B. S.对该模型提出了修正
竞争性抑制剂双倒数曲线,如下图所示:
1 Km 1 〔 I 〕 + = (1+ ) Ki 〔S Vmax vi Vmax 〕
有竞争性抑制剂存在的 曲线与无抑制剂的曲线相 交于纵坐标1/Vmax处,但 横坐标的截距,因竞争性 抑制存在变小,说明该抑 制作用,并不影响酶促反 应的最大速度Vmax,而使 Km值变大。
(2)特点:
① I和S在结构上一般无相似之处,I常与酶分子上结合 基团以外的化学基团结合,这种结合并不影响底物和酶 的结合,增加底物浓度并不能减少I对酶的抑制。
② 非竞争性抑制剂的双倒数曲线:有非竞争性抑制剂 存在的曲线与无抑制剂的曲线相交于横坐标 -1/Km处, 但纵坐标的截距,因竞争性抑制存在变大,说明该抑 制作用,并不影响酶促反应的Km值,而使Vmax值变小, 如下图所示:
复杂的酶促反应——双底物反应
复杂的酶促动力学:乒乓反应(无三元复合物, 酶的过度态
乒乓反应:氨基酸的氨基转移反应
序列反应和乒乓反应的区别
本章重点
酶催化的基本特征 影响酶催化活性的因素 米氏方程的推导 米氏常数的意义 酶反应抑制动力学,几种抑制的反应式 和特点
7.3 有抑制的Βιβλιοθήκη 催化反应动力学在酶催化反应中,由于某些外源化合物的存在而 使反应速率下降,这种物质称为抑制剂。
可逆抑制
可用诸如透析等物理方法把抑制剂去掉而恢复酶的 活性,酶与抑制剂的结合存在着解离平衡的关系。
不可逆抑制
抑制剂与酶的基因成共价结合,不能用物理方法去 掉抑制剂。此类抑制可使酶永久性地失活。例如重 金属离子Hg2+”、Pb2+”等对木瓜蛋白酶、菠萝蛋白 酶的抑制都是不可逆抑制。
k1 Et ESS k1ES k2 ES
k1 k2 Km k1
Et S ESS k1 k2 ES k1 则: Km ES ESS Et S
(1)
v1 v2
经整理得:
ES
M t
[ES] E [E] E K
ES
[ ES] [S ]
(1)
经整理得:
Et S K M S
由于酶促反应速度由[ES]决定,即 将(2)代入(1)得:
v k2 ES
,所以
ES
Et S v k 2 K M S
所以
v
酶
(2)特点:
反竞争性抑制剂存在下,Km、Vmax都变小。 1 = Km 1 + 〔 I〕 (1+ ) Vmax Ki 1 Vi=
Vmax〔S〕
Vi
Vmax 〔S〕
〔 I〕 K m+ (1+ Ki 〔 )S〕
复杂的酶促反应——双底物反应
A+B
P+Q
序列反应:在任何产物释放前两种底物 必须先结合到酶上 乒乓反应:在所有底物完全结合之前即 有产物释放
稳态学说:Brigges-Haldane方程
S
ES [ES]生成速度: v1 k1 Et ESS
Et ES
SE
k1 k 1
ES
