天然抗癌药紫杉醇及其半合成类似物的研究进展_何晓明
紫杉醇研究进展

紫杉醇的研究进展1.概述紫杉醇是从紫杉(Taxus brevifolia)树皮中所提得,是红豆杉属植物中的一种复杂的次生代谢产物。
1971年由 Wani 等首先从短叶红豆杉中提取分离出来。
于1992年12月紫杉醇被FDA批准上市,目前紫杉醇已成为世界公认的强活性广谱抗癌药物。
然而由于这种天然化合物资源极其有限,严重的限制了其研究和应用的进度。
同时尖锐的供需矛盾也在医学、化学和植物组织培养领域中引起了一场非同寻常的广泛研究,以增加这种化合物的来源和寻找高效、低毒、来源丰富的紫杉醇类似物。
已成为目前全球销售量排名第一的抗肿瘤药物。
它的作用方式和药理及临床特性均具有独特之处,被称癌症化疗上的新突破。
紫杉醇,英文名称 Paclitaxel,别名,,特素,化学名称5β,20-环氧-1,2α,4,7β,10β,13α-六羟基紫杉烷-11-烯-9-酮-4,10-二乙酸酯-2-苯甲酸酯-13[(2’R,3’S)-N-苯甲酰-3-苯基异丝氨酸酯],分子量 853.92,分子式C47H51NO14。
熔点为213~216℃。
紫杉醇具有高度亲脂性,不溶于水,血浆蛋白结合率 89%~98%,终末半衰期平均值为 5.3~l7.4h, 主要经肝脏代谢,肾脏清除仅 5%。
[1] 结构式如下:2紫杉醇的药用植物资源及药源植物中有效含量研究红豆杉为红豆杉科植物,也称紫杉,全世界约有11种,主要分布于北半球,我国有4种1变种,主要分布于甘肃、陕西、安徽、湖北、湖南、广西、贵州、四川、云南等省区[2-3]。
研究表明[4],植物中紫杉醇含量在万分之二以下,极其低微。
短叶红豆杉树皮中紫杉醇含量最高,其次为中间红豆杉树皮;东亚产四种红豆杉中,云南红豆杉枝叶中紫杉醇含量最高东北红豆杉和美丽红豆杉次之,短叶醇含量则以短叶红豆杉叶最高,东北红豆杉及云南红豆杉次之。
植物中紫杉醇的含量极低,从植物中提取不能满足临床需求,因此大力种植红豆杉、植物细胞培养、化学合成等是解决紫杉醇来源的重要方法。
紫杉醇及其类似物的研究进展

紫杉醇及其类似物的研究进展摘要:紫杉醇(Taxol)是近40年从红豆杉属植物中发现的最著名的天然抗肿瘤药物,在过去30年多年间紫杉醇因其独特的结构、新颖的作用机制和显著的抗癌活性成为化学家、药理学家和生物学家的研究热点。
本文对紫杉醇及其类似物的基本结构、作用机理、开发利用以及合成方法方面进行了总结。
关键词:紫杉醇作用制剂合成正文:紫杉醇是一种从红豆杉属植物中提取的四环二萜化合物(结构式如图1所示)。
美国化学家瓦尼(M.C. Wani)和沃尔(Monre E. Wall)于1963 年首次从一种生长在美国西部的名为太平洋杉(Pacific Yew)的树皮和木材中分离到了紫杉醇的粗提物。
直至1979年分子药理学家Dr. Horw itz阐明了紫杉醇的独特作用机制:紫杉醇能与微管蛋白结合,并促进其聚合,抑制癌细胞的有丝分裂,有效阻止癌细胞的增殖。
图-1紫杉醇的抗肿瘤作用机制1 阻滞肿瘤细胞有丝分裂微管是真核细胞的一种组成成分,它由两条类似的多肽为单位构成的微管蛋白二聚体形成。
微管具有构成细胞网状支架,维持细胞形态,参与细胞运动,参加细胞器的位移及胞内物质运输等功能,尤为重要的是染色体的分裂和位移,均需在微管的帮助下进行。
正常情况下,微管蛋白和组成微管的微管蛋白二聚体存在动态平衡。
紫杉醇可使二者之间失去动态平衡,导致细胞在有丝分裂时不能形成纺锤体和纺锤丝,抑制了细胞分裂和增殖,使癌细胞停止在G2期和M期,直至死亡,进而起到抗癌作用。
2 诱导细胞凋亡Fas /Fasl信号传导系统是细胞凋亡信号传导的重要途径之一。
用Fasl抗体可以抑制紫杉醇诱导的凋亡, 表明紫杉醇诱导细胞凋亡与Fas/Fasl相关。
实验中发现, 紫杉醇作用于人肉瘤细胞Saos-2后Fas的表达持续升高, Fasl的表达也增高了3倍。
Bcl-2家族中一些成员促进凋亡,如Bax基因;另一些则阻碍凋亡,如Bcl-2基因。
有研究表明紫杉醇诱导MCF-7细胞凋亡,使Bcl-2降低、Bax增加,同时Bcl-2/Bax的比率亦随时间延长及剂量的增加而逐渐下降,呈现出明显的时间及剂量依赖性。
【doc】紫杉醇手性侧链合成与紫杉醇半合成

紫杉醇手性侧链合成与紫杉醇半合成第13卷第18期2005年9月21日精细与专用化学品FineandSpecialtyChemicalsV o1.13,No.18l?专论与综述紫材醇手牲坝殂链合成与紫材醇半合成阎家麒(江苏佩沃特生物基因工程有限公司,江苏常熟215500)摘要:介绍抗癌药物紫杉醇的几种合成方法,重点阐述紫杉醇手性侧链合成以及应用紫杉醇手性侧链的重要性.同时论述了国内外紫杉醇半合成的研究进展,重点讨论了江苏佩沃特公司研发的对映异构纯的口一内酰胺侧链中间体及其高效的对接路线.关键词:紫杉醇;半合成法;手性侧链;抗癌药物ChiralSynthesisoftheTaxolSideChainandSemisynthesisofTaxolNJia—qi(JiangsuPivertBio—geneticEngineeringCo.,Ltd.,Changshu215500,China) Abstract:Themethodsforsynthesizinganticarcinogentaxolareintroduced.Thesynthesisof chiralsidechainoftaxol andthesignificanceofapplicationofchiralsidechainaredescribedindetail.Meanwhile,ther esearchprogressonsemi—synthesisoftaxolathomeandabroadarenarrated,theenantiotropicpure口一lactamsidechainintermediatedevelopedJiang—SUPivertCo.,Ltd.Andhighlyeffectivemethodforcouplingisdiscussedemphatically. Keywords:taxol;semisyntheticmethod;chiralsidechain;anticarcinogen紫杉醇是一种来源于红豆杉属植物的二萜类化合物,由A,B,c,D四元环和一个苯基异丝氨酸侧链构成,见图1.1963年,美国科学家Wall和Wani从太平洋红豆杉的树皮中得到这种化合物…,发现其对离体培养的肿瘤细胞,包括L1210和P288白血病,Walker256肉瘤及B16黑色素瘤细胞都具有很强的抑制作用.图1紫杉醇化学结构紫杉醇是人类迄今发现的最有效的抗癌药物,1992年,美国食品药品管理局(FDA)批准紫杉醇上市和临床应用.作为广谱抗癌药物,紫杉醇对卵巢癌,乳腺癌,肺癌,食管癌等具有很好的疗效,现已在60多个国家获准临床应用.l专利之争紫杉醇于1992年由美国施贵宝公司(BMS)上市,在此后的8年内,BMS都是紫杉醇专利药持有者.但是在2000年后,BMS经过与Ivax公司一次旷日持久的斗争后失去了该药在美国的专利保护,Ivax公司的口服紫杉醇产品Onxol获准上市,使美国向非专利紫杉醇敞开了大门,至今已有多种非专利紫杉醇药物上市.紫杉醇的专利权和排它权均于收稿日期:2005-07—28作者简介:阎家麒,男,教授,中国药学会高级会员,主要研究领域为生物制药和天然产物的有机合成,在紫杉醇半合成和埃坡霉素全合成研究上取得较好成绩,发表学术论文50余篇,获发明专利11项.2-精细与专用化学品第13卷第18期1997年12月29El到期,其中包含NP和NCE(新药物和新化学实体).2合成方法2.1植物提取在我国提取紫杉醇所用植物材料主要是云南红豆杉.红豆杉属植物是冰川时期的孑遗物种,属于珍稀物种,在我国被列入国家一级保护植物.红豆杉树皮中紫杉醇含量极低,约0.009%左右,实际生产Ikg紫杉醇,需要大约20t红豆杉树皮,即需毁掉3000多株百年以上的红豆杉.然而,在经济利益的驱动下,我国红豆杉被非法采伐了80%以上,红豆杉物种在我国濒于灭绝.为了保护我国的红豆杉资源,政府加大了对红豆杉的保护力度,严惩了数十家用红豆杉提取紫杉醇的生产厂家以及经营企业,有效地遏止了对红豆杉的毁灭性破坏.2.2细胞培养法癌症是仅次于心血管疾病,危及人类生命的第二大病种,每年癌症的发病率是700万人.寻求紫杉醇新的药物来源是全世界科学家们孜孜以求的目标.近20年来,相继有多学科,多角度地探索性研究报道,有紫杉醇细胞培养,真菌发酵,全合成与半合成等等.其中,细胞培养生产紫杉醇不失为一种较理想的方法,但是其最高产率仅为22mg/L.细胞培养面临的主要难题有:①紫杉醇低水平表达;②由于植物细胞易于变异,长时间培养后,紫杉醇含量降低;③细胞对放大培养中的剪切耐受力低;④产量不稳定.只有这些问题解决之后,才能实现工业化生产.另一方面,细胞培养产出的细胞材料尚需下游工艺分离纯化,其工艺过程与植物提取紫杉醇方法完全相同.这样,两项成本的叠加,将使终产品紫杉醇在价格上失去市场竞争能力.至于真菌发酵法目前也只有在实验室进行,没有实用价值.紫杉醇全合成无疑是天然产物有机合成史上的丰碑,但是因步骤冗长烦琐,产率过低,不可能实现工业化生产.2.3半合成法1988年,法国Denis等首次报道了以10.去乙酰巴卡亭111(10一deacetylbaccatinIi/,10.DAB)为原料半合成紫杉醇.其后,美国Hohon教授和法国的Potier教授等也以巴卡亭Ⅲ为原料半合成了紫杉醇.10?去乙酰巴卡亭Ⅲ是从欧洲红豆杉的枝叶中分离出来的,其含量可达0.1%,由于枝叶再生能力强,因此紫杉醇半合成可有较丰富的原料.1992年在NCI主持召开的第二次红豆杉与紫杉醇研讨会上,Hohon等报道了紫杉醇的半合成路线,即利用紫杉醇侧链Ⅳ.苯甲酰.(2R,3S).3一苯基异丝氨酸经酯化后与巴卡亭Ⅲ相连接的方法.1994年美国施贵宝公司(BMS)采用Hohon教授半合成方法的专利生产半合成紫杉醇.1997年,半合成紫杉醇通过美国FDA批准上市.Hohon教授的半合成方法是弗罗里达州立大学科学家小组的专利技术,目前被称为"FSU'S紫杉醇半合成方法".比较之下,半合成紫杉醇则是最具商业应用价值的技术.本课题组曾在我国最早报道了紫杉醇提取纯化,纯度测定以及新型控释缓释制剂等系列研究..我国红豆杉资源贫乏的现实促使科研工作者改变了研究方向,提出"战胜癌症不再以毁灭红豆杉为代价"的科研宗旨.临床需要的紫杉醇必须满足,又要从根本上有效地保护红豆杉不被灭绝.因此,研究工作的重点必须由植物提取转移到化学合成方法上来.经过10年的精心探索,刻苦钻研,无数次地试验,紫杉醇半合成终于取得了成功.3半合成关键技术评价紫杉醇的化学合成可谓是20世纪最后10年中对有机合成的重大挑战.在迎接这场挑战中,各国科学家都将其作为热点课题,做出了杰出成绩.仅半合成紫杉醇的路线就有20多条,各种结构的侧链30余种.在药物研究的历史上,研究时间之长,文献量之大,当属紫杉醇.在浩如烟海的文献中,有些是有借鉴价值的,但也不乏空洞不实文章,这些对我国紫杉醇的研究影响颇大.3.1紫杉醇手性侧链合成侧链是合成紫杉醇的关键中间体.美国紫杉醇半合成着名科学家Hohon认为使用外消旋体侧链与7.TES.baccatinⅢ对接时其立体选择性的范围可以从3:1到100:1,不需要用手性侧链,即不需要将外消旋体侧链拆分成手性侧链,因为拆分成本过高.但是,在产业化半合成紫杉醇中发现,如要合成1kg紫杉醇,依据Hohon在其文献中强调的按5~7比例投料,则需要消耗1.5kg10.DAB和4.08~5.72kg外消旋体侧链.按每千克侧链8万元计,侧链费用32万~40万元,占总合成成本的一半还多.在Hohon本人的文献中有这样一个反应,路线如图2所示.2005年9月21日阎家麒:紫杉醇手性侧链合成与紫杉醇半合成?3? …...…:::=盏嚣鉴强秘图2外消旋体侧链合成紫杉醇反应路线对接后产物为8:2的非对映异构体的混合物,两者合计产率为80%一90%,其中被外消旋体侧链"带走"7-TES.baccatinllI而生成的(要弃掉的)异构体就占了20%,故在理论上总产率只有80%~90%的80%,即64%~72%.因此,使用外消旋体侧链是不经济的.更重要的是,Hohon所提出的"可以不必拆分成手性侧链,使用外消旋体侧链就可以低成本地合成紫杉醇"的理论,实践证明是不可行的.使用外消旋体侧链生成的是一对非对映异构体紫杉醇,这2个异构体化合物很难分离,必须采用手性色谱方法,况且采用哪种手性色谱分离技术尚在探讨中.所以,Hohond的提法实际上是一种误导,其目的无非在于保持美国在紫杉醇半合成上的垄断地位.尽管Holton在许多文献中极力鼓吹使用外消旋体侧链合成紫杉醇,但是,在美国以施贵宝为代表的半合成紫杉醇生产企业,却一直在使用手性侧链,从不使用外消旋体侧链.如果使用手性侧链,对接产物就只有2',3'.s非对映异构体一种.根据美国大规模生产的工艺,使用光学纯手性侧链仅为1.6~1.8,产率≥84%.7-TES—baccatinnl的分子量为700,最大也最常用的侧链(3R,4S)一1.benzoyl一3一(triethylsilyloxy)-4.phe. nylazetidin一2一one分子量为381.42.由此可以计算出,合成1kg紫杉醇,产率即使按80%计算,则需要7一TES—baccatin11I1250g(由10一DAB1200g合成), 手性侧链1089.77g,即合成1kg紫杉醇需用1.2kg10一DAB和大约1kg手性侧链.这不但提高了产率, 又节省了侧链费用,降低了合成成本,更重要的是使用手性侧链与7-TES—baccatinnl对接成功率高.美国施贵宝公司采用Hohon及其FloridaState University研究小组的最新紫杉醇半合成方法,所使用的侧链就是手性光学纯的(3,4S)一3.(1.甲氧基.1.甲基乙氧基)-4.苯基.2.氮杂环丁酮,见图3. BzOTE$CIHo…Ph/~n....AcOqt,00TES'--k--./oco卜嘲0..AcO0OH图3施贵宝公司使用手性侧链半合成紫杉醇路线最初,美国研发紫杉醇侧链时,有3种主要类型:"直线型",即苯基异丝氨酸型;恶唑烷五环型和口一内酰胺四环型(图4).截至2004年,国外半合成紫杉醇主要使用手性』B.内酰胺侧链,如图5的(3R, 4S)的手性化合物,Hohon在其许多文献中所倡导的"可以使用外消旋体侧链,不必拆分成手性侧链" 的观点,在美国的大规模生产中(如施贵宝公司)也没有被采用,实施.但是,这一论点却对我国的紫杉醇半合成研发工作影响很大.在实际生产中,外消旋体侧链消耗量很大,成本居高不下.0ncoHMeNO/×苯基异丝氨酸甲酯型恶唑烷型-内酰胺型(直线型)(五环型)(四环型)图4紫杉醇的3种侧链在外消旋体侧链拆分中,美国是采用一种来源于洋葱假单胞菌的脂肪酶(如lipasePS.30),可以高对映选择性水解消旋体中的顺.3.乙酰氧基4.苯基一2一杂环丁酮分子中的(3S)乙酰基,未水解的(3R)乙S¨^●●●●●●●,4?精细与专用化学品第13卷第18期酸酯可作为侧链合成的前体¨….这种拆分方法成本很高,PS.30价格昂贵且不容易得到.用动物肝脏酯酶拆分成本相对低廉,对此进行探索,效果比较理想….直接合成手性侧链是大规模生产最低成本的策略.氨基酸属于手性化合物,采用一种氨基酸作为手性模板,直接合成手性/3一内酰胺侧链(图5).3.2紫杉醇半合成3.2.1国外的合成路线半合成紫杉醇是以10一去乙酰巴卡亭Ⅲ作为母核,首先用硅烷基团保护7位羟基,再乙酰化10位羟基.然后7-TES.baccatinⅢ与侧链前体缩合,然后水解除去7位和2位上的保护基团成为紫杉醇(图6).在紫杉醇半合成的4步反应中,最重要而且难以成功的关键技术是7-TES—baccatinⅢ与侧链对接,即酯化C.13或巴卡亭Ⅲ酰化反应.在对接反应的方法上,美国所发表的大多数文献是不真实的,比如Hohon的方法¨(图7).Ph.BzO'侧链阿体OOOOOOO./,OSiE\N—//...LJ...In;Ftr3~~图5外消旋体与手性紫杉醇和多烯紫杉醇侧链OAcSOj%HaO图6紫杉醇半合成路线BzNHO.EEO.PhOEE1NBz《5eq)皲96%图7Hohon的对接路线TEs里:!兰.91%Ta)(o1?______.?_-.--.?.………0.C.4days.2005年9月21日阎家颇:紫杉醇手性侧链合成与紫杉醇半合成?5? 这个反应实际无法进行,因为吡啶的加入量根本不能将7-TES—baccatinm和侧链溶解,更谈不上有那么高的产率.还是Holton的文献,他主张的醇锂盐方法,即用锂置换C.13位的氢,形成醇锂盐再与-内酰胺反应生成.氨基酯,然后转化成紫杉醇(图8).用正丁基锂对接侧链方法可取,但是Holton提出的反应条件是一78℃.在一78℃,正丁基锂是不能反应的,对接的转化率为≤5%,收率为0.国内有采用正丁基锂方法对接侧链的,使正丁基锂反应条件改变为一40℃左右,效果也算理想.Ojima等详尽地阐述了-内酰胺型侧链与7-TES.baccatinⅢ对接反应中碱的选用,比较了各种碱,反应条件及产率(表1).髓PhCONHO….广lIlO…?U图8Hohon醇锂盐法对接路线表1口-内酰胺型侧链与7-TES?baccatinm的对接方法比较堡:坚.紫杉酵由表1可知,最佳的反应条件应该是:NaHMDS(1.2equiv),溶剂THF,温度一30℃,时间30min,转化9l%,离析收率88%,转化收率97%.同时指出,使用Nail方法简便,90%的转化率也不低,但是转化率一旦超过90%,有时会突然发生产物分解.在实验中发现,NaHMDS作为碱活化13.OH与侧链酯化,并非Ojima认为的"最佳"反应,在这个对接反应中不是产生分解产物,而是在一30℃下基本上不反应.天津大学的专着里也论及到使用NaH.MDS产生一种去除不掉保护基的白色分解产物.在实际生产中,使用NaH方法较好.Ojima等认为按标准的方法(即Holton方法),在侧链加入之前,7-TES-baccatinⅢ用正丁基锂处理会发生严重的分解.对接反应是紫杉醇半合成成功与否的关键,也正因为如此,大量的不真实文献让人们扑朔迷离. 为此,我们不能轻信国外权威们的文献,要自己反复探索,去伪存真,因为研究的过程实际上就是明辨是非的过程.半合成紫杉醇是未来紫杉醇来源的惟一途径.合成步骤简化,产率,纯度高,原料完全国产化,生产成本低廉,是半合成紫杉醇在未来的国际市场竞争的优势所在.就技术经济而言,美国半合成1kg紫杉醇的生产成本至少26万美元,而我们目前半合成1kg紫杉醇则仅需不到40万元人民币.3.2.2国内的合成路线江苏佩沃特公司的半合成紫杉醇样品经中国科学院上海药物研究所H和"C.NMR,MS,IR和uV4 项光谱鉴定证实,化学合成的紫杉醇与天然产物结构完全一致.该所HPLC测定的产品纯度达到99.6%,远远高于美国FDA制定的紫杉醇原料药纯度(≥98.50%)标准.1997年,意大利科学家在紫杉醇半合成上取得了更大的突破.他们在法国Rhone.PoulencRorer公司半合成多烯紫杉醇和美国Bdsto1.MyereSquibb (施贵宝)公司半合成紫杉醇技术的基础上,研发了6?精细与专用化学品第13卷第18期新的合成工艺.其技术指标是,每合成1kg紫杉醇只需1.2kgl0.DAB和大约2kg的手性侧链,而且手性侧链的合成路线缩短,只需5步反应.其侧链结构如图9所示.本公司及时就这一侧链进行研究, 并成功合成了这一新型侧链.OPhSPh图9侧链pheny!(4S.5R)-2.4-dipheny!-4.5-dihydrooxazole-5-thiocarboxylate用该侧链合成紫杉醇收率高于美国和法国的方法,合成(对接)路线如图1O所示.rHF,15mj.L0℃004mo卜LHC¨nMeOH:H20,'p:1.5:1NaI-ICO3,H20,pH75,1OH..图lO佩沃特公司紫杉醇合成路线与20世纪90年代初Hohon的施贵宝公司半合成紫杉醇以及法国半合成多烯紫杉醇的工艺比较,1997年意大利报道的新工艺更适合大规模生产,无疑是一个较好,较实用的半合成紫杉醇方法.目前,比较可信的有关使用手性侧链半合成紫杉醇的技术大致有4种,重要中间体消耗(经济技术指标)各异,见表2.表2使用手性侧链半合成紫杉醇1kg所需重要中间体(经济技术指标)的比较kg(1)侧链为(3R,4S).1一benzoyl-3-(1-methoxy-1-methylethoxy)4? phenylazeIjdjn-2-one(2)侧链为Phenyl(4S,5R)-2,4-dipheny1..4,5-dihydrooxazole.5- thiocarboxylate4结语"泰素"是美国施贵宝公司全球销量最大的紫杉醇注射剂,年销售额15亿美元以上.自1997年美国FDA正式批准该公司半合成紫杉醇作为泰素的原料药开始,1999年起,施贵宝公司全部采用半合成紫杉醇生产制剂,废止天然红豆杉提取的紫杉醇.也就从1997年起,放开了曼地亚红豆杉植物物种对中国的出口.诸多文献公认,植物提取纯化紫杉醇是一件烦琐,艰辛,费力的工作,而且,对环境的污染很严重.于是,一些发达国家(甚至发展中国家的印度)都把这种植曼地亚红豆杉提取纯化紫杉醇的"烦琐","艰辛","费力"的工作交给中国人去做,他们压价回收产品.事实上,他们利用了我国的廉价劳动力,并把环境问题留给我们.近年来,植物提取紫杉醇在国际市场所占份额越来越少,取而代之的是半合成紫杉醇.现在,在国际市场上占有90%以上,具有垄断地位的美国施贵宝公司的"泰素",也在包装上赫然明确地用中,英文注明"人工半合成紫杉醇".紫杉醇半合成产业化将为临床提供充足的紫杉醇原料药和制剂,大大降低临床治疗费用,使得收入偏低的癌症病人能够用得起药,并且更少依靠国外进口紫杉醇,最终让我国的紫杉醇原料药与制剂进入世界药物的主流市场,造福广大肿瘤患者.口(参考文献见第11页)2005年9月21日李斌,等:2-巯基苯并噻唑>NH'+CS:+s\s/图22一巯基苯并噻唑的反应方程式苯胺法生产2-巯基苯并噻唑的特点是原料来源稳定,操作难度小,对反应器材质要求低;其缺点是由于该法生产的粗产品中2-巯基苯并噻唑含量较低(85%),焦油量大,收率较低.3生产在我国有上海汉飞生化科技有限公司,上海威方精细化工有限公司和上海实验试剂有限公司等企业进行2.巯基苯并噻唑的生产.日本主要有4家生产厂商:住友化学,大内新兴,川口化学和三新化学. 其他国外生产企业还有富莱克斯(Flexsys)和拜耳公司等.4需求噻唑类橡胶硫化促进剂的硫化速度并不是很快,但硫化状态比较平缓,硫化物性良好,因此是一类通用助剂.2-巯基苯并噻唑为通用型橡胶促进剂,对天然胶和一般硫磺硫化的合成胶具有快速促进作用,其硫化I临界温度低.作为酸性硫化促进剂, 可以使橡胶制品具有很高的拉伸强度和硬度,通过选择不同的组合成分,还能使其满足不同要求的性能,可用作增塑剂,增加天然胶的塑性.不过制品本身带有苦味,不适于制造与食品接触的橡胶制品,主要用于制造轮胎,内胎,胶带,胶鞋和工业品等.可以添加的对象橡胶有:天然橡胶(NR),异戊二烯橡胶(IR),丁苯橡胶(SBR),丁二烯橡胶(BR),丁腈橡胶(NBR),三元乙丙橡胶(EPDM),丁基橡胶(IIR)等.在橡胶中的用量(phr)为0.5~2.在作为橡胶助剂使用的需求方面,往往要受到汽车和房地产业波动的影响.日本国内的市场需求大约为200t/a.5价格在我国,上海实验试剂有限公司规格为分析纯,25g包装的牌价为29.25元.在日本,价格为600~800日元/kg,包装为20kg纸袋.口参考文献[1]奚国辉,王晓华.2一巯基苯并噻唑合成反应工艺研究[J].石化技术与应用,2003,21(4):259—262[2]范文革.硫化促进剂M合成新工艺研究[J].西北民族学院(自然科学版).2001.22(3):1317(上接第6页)参考文献[1]WaniMC,TaylorHL,WallME,eta1.PlantantitumoragentsVI. Theisolationandstructureoftaxol,anovelantileukemicandantitu—moragentfromtaxusbrecifolia[J].JAmChemSo.1971.93: 2325—2327[2]RowinskyEK,OnettoN,CanettaRM,eta1.Taxol:thefirstofthe taxanes,animportantnewclassofantitumoragents[J].SeminOn—col,1992,19:646—655[3]阎家麒,范金城,王九一.紫杉醇提取纯化工艺[J].中国医药工业杂志,1996,27(12):531—535[4]王九一,阎家麒.紫杉醇半合成[J].中国药物化学杂志,1999.9(1):56—58[5]阎家麒,童岩,王九一.紫杉醇脂质体的制备及其抑瘤作用的研究[J].药物生物技术,1996,3(3):154—157[6]阎家麒,王悦,王九一.紫杉醇隐形脂质体的制备及其在小鼠体内的组织分布[J].药学,2000,35(9):706709[7]阎家麒,王惠杰,童岩,等.紫杉醇微乳的研究[J].中国药学杂志,2000,35(3):173—176[8]RobertAHohon.MethodforpreparationoftaxolusingaB-lactam[A].AbstractsofPapers.203rdNationalMeetingoftheAmerican ChemicalSociety[C】.SanFranciscoCA,AmericanChemicalSoci. ety:WashingtonDC,1992[9]SusanRM.MaximizingReturns[J].C&ENews,2003,Sept15: l7—2O[1O]PatelRN.Semisynthesisoftaxol[A].StereoselectiveBiocatalysis [M].2000,MarcelDekker,Inc:270MadisonAvenue.NewY ork,NY10016,108—112[11]阎家麒.牛肝酯酶催化紫杉醇侧链手性合成的研究[J].药物生物技术,2005,12(2):90—92[12]RobertAHohon.Methodforpreparationoftaxol[P].EP400971, l990.125[13]RobertAHohon.Methodforpreparationoftaxolusingtetalactam [P].US5175315.1992.12-29[14]元英进,葛志强,冯霞.抗癌新药紫杉醇和多烯紫杉醇[M].北京:化学工业出版社,2002.61。
对紫杉醇及其类似物的研究

生物活性测试
4、检测三种类似物的抗肿瘤活性
分别取等量的某型肿瘤组织若干份在 相同的适宜环境下分开进行体外培养, 待条件成熟后,分别加入等量的以上三 种类似物及紫杉醇,一定时间后,查看 肿瘤组织生长情况来查看三种类似物的 抗肿瘤活性。
三、羟基变成氟原子的等电子体的转换
紫杉醇在二乙胺基三氟化硫(DAST) 的试剂的存在下发生亲核取代得到目标产 物。
产物分析方法
核磁氢谱 红外光谱分析。 反相高效液相色谱法(紫杉醇及其类似物的含量 进行测定)
HPLC内标法
固相萃取-高效液相联用(SPE-HPLC) 液相色谱-质谱联用(LC/MS)
C2’位羟基是非常重要的结构单元 , 酯化或酰化后会使体外活性降低,但 在体内活性变化不大。要想使紫杉醇 C2’位衍生化成为前药,除了水溶性和 活性增加以外, 还必须具备较高的稳定 性。
生物活性测试
3、C3’位苯基对生物活性的影响
C3’苯基为重要的生物活性必需单 元。 如果用疏水性取代基或者芳香性取 代基取代 C3’苯基对紫杉醇活性影响不 大。
生物活性测试
1、C 2位苯甲酰基对生物活性的影响
对于已经合成的 C2 位去苯甲酰基紫杉 醇类似物,发现其活性比紫杉醇更低,由 此证明 C2 位苯甲酰基对生物活性是至关重 要的。它的重要性在于: 把紫杉醇生物活性 和侧链、 C2 位、 C4 位之间的疏水缝隙联 系在一起。
生物活性测试
2、C2’ 位羟基对生物活性的影响及其 前药的研究
类似物的设计及合成路线
紫杉醇
类似物1
类似物2
类似物3
一、羟基变成烷基的等电子体的转换
紫杉醇先与对甲基苯磺酰氯室温反应生成对 甲基苯磺酸酯衍生物,衍生物再和甲烷格氏试剂 反应烷基化,生成目标产物。
紫杉醇

• 紫杉醇的应用受到限制
• (1)药源紧张。 • (2)水溶性低,口服生物利用度差。 • (3)助溶剂聚氧乙烯蓖麻油会引起不良 反应。 • (4)紫杉醇本身引起的毒性反应,如神 经毒性。
• 紫杉醇新剂型开发 • 前体药物:与其他化合物交联形成无活性 的衍生物 ,在体内经酶解或水解后解离出 活性药物。 • 糊剂 :选择生物相容性聚合物 ,制成外用 糊剂 ,亦可实现紫杉醇局部用药,具有持 续释放和缓慢的抗血管活性作用。 • 脂质体:利用脂质体包裹技术,提高了紫 杉醇水溶性,在耐药性方面比Cremophor 为溶媒有了较大的进步。
紫杉醇及其类似物的研 究进展
紫杉醇(Taxol)
• 紫杉醇(Taxol)从短叶红豆杉树皮中分离得 到的一种四环二萜化合物。 • 美国化学家瓦尼(M.C. Wani)和沃尔 (Monre E. Wall)于1963 年首次从一种生 长在美国西部的名为太平洋杉(Pacific Pacific B C Yew)的树皮和木材中分离到了紫杉醇的粗 A D 提物。
C13位支链、C2位苯甲酰基和C4位乙酰基以 及D环对其生物活性是必需的,而对C1位、 C7位、C9位和C10位等的结构进行修饰往往能 改善其生物活性和水溶性。 将C2-OBz立体构型翻转得到2-epi-Taxol, HCT116细胞毒性和微管蛋白聚合试验测定 显示:该修饰物既无细胞毒性,也无促微 管蛋白聚合的活性修饰。 C7位被OCH2SCH3可以提高活性。
紫杉醇的抗肿瘤作用机制
①紫杉醇可使微管蛋白( α微管蛋白和β微管 蛋白)和组成微管的微管蛋白二聚体失去动 态平衡,诱导与促进微管蛋白聚合、微管装 配,防止解聚,使微管稳定,从而阻止癌细 胞的生长。
微管是真核细胞的一种组成成分, 它由两条 类似的多肽为单位构成的微管蛋白二聚体形 成。微管具有构成细胞网状支架, 维持细胞 形态,参与细胞运动,参加细胞器的位移及 胞内物质运输等功能, 尤为重要的是染色体 的分裂和位移,均需在微管的帮助下进行。
天然抗癌药紫杉醇及其半合成类似物的研究进展_何晓明

口服降糖药与血糖监测④服用口服降糖药期间低血糖的预防 和治疗 2. 4 糖尿病的病情监测 监测自觉症状的变化; 监测体重, 血压的改变; 化验指标的监测: 血糖,糖化血红蛋白,尿糖,酮 体,血脂,尿蛋白及肾功能等; 监测胰岛功能的变化; 监测并发 症的早期发现或进展; 监测药物治疗的效果; 认真填写每天观 察记录表,尤其病情严重的患者更应注意。 2. 5 糖尿病教育 通过定期举行健康知识讲座,使患者和家 属掌握了糖尿病预防和自我护理知识,密切了患者与专科护 士的关系,取得 了 相 互 间 的 信 任,使 健 康 指 导 及 管 理 顺 利 开 展。提高了糖尿病患者健康管理的有效性和及时性。
【Key words】 Paclitaxel; Semi-synthesis; Structural modify
1 概述 紫杉醇( Paclitaxel,商品名 Taxol) 是近年来最令人瞩目的
抗癌药之一。1966 年,美国化学家 M. Wall 和 M. Wani 首先 从太平洋紫杉( Taxus brevifolia) 的树皮中分离得到了这种天 然紫杉烷类二萜化合物。1992 年 12 月 29 日,美国 FDA 正式 批准紫杉醇 做 为 治 疗 晚 期 卵 巢 癌 的 新 型 抗 癌 药 上 市。1996 年,紫杉醇的半合成类似物脱乙酰紫杉醇( 紫杉特尔,docetaxel,商品名 Taxotere) 也获得了美国 FDA 做为治疗晚期乳腺癌 和卵巢癌的抗癌药的批准。体外抗肿瘤活性实验表明,其抗 肿瘤活性强于紫杉醇。
[4] Ringel I,Horwitz S. Studies with RP56976 ( Taxotere) : a semisynthetic analog of taxol. J Natl Cancer Ins,1991,83( 4) : 288-291.
天然抗癌药物紫杉醇的研究进展

2 0 1 4年 1 0月 d o i : 1 0 . 3 9 6 9 / j . i s s n . 1 0 0 6—9 6 9 0 . 2 0 1 4 . 0 5 . 0 1 2
中 国 野 生 植 物 资 源
C h i n e s e Wi l d Pl a n t Re s o u r c e s
a r e l o t s o f s t u d i e s a b o u t t a x o 1 . Th e a r t i c l e s u mma r i z e d t h e r e s e a r c h p r o g r e s s o f t a x o l i n s u c h a s p e c t s a s c h e mi c a l s y n t h e s i s a n d b i o s y n t h e s i s, a n d i t s d e v e l o p me n t t r e n d s we r e a l s o p r o s p e c t e d.
紫 杉醇 为 白色结 晶性粉末 , 不 溶于水 , 易 溶于 氯
卵巢 癌 、 乳 腺癌 、 肺癌 以及 K a p o s i ’ S肉瘤 的治 疗 , 同 时也 在研 究与其 他 抗 癌药 物 联 用 的治疗 方 法 , 是 获
得F D A批 准 的第 一个 来 自天然植 物 的化 学药 物 。
Ke y wo r d s t a x o l ;s o u r c e;b i o s y n t h e s i s
l 紫 杉 醇 介 绍
紫杉 醇 ( P a c l i t a x e l , 商品名 T a x o 1 )被 用 于 治 疗
抗癌药物紫杉醇的最新研究进展讲课稿

环糊精包合
提高药物的稳定性、生物相容性
大分子结合物给药系统
利用单抗、白蛋白、球蛋白等能在肿瘤部位聚集的大分子与紫 杉醇结合(7-succinylpaclitaxel-HAS结合物)
提高靶向性、水溶性
聚合物(微囊、微球等)
用生物可降解聚合物包载紫杉醇 生物适应性好可生物降解
药源问题解决办法(三)
生物方法 组织和细胞培养
微生物发酵
优点:1、摆脱自然因素,可长期稳定 生长
2、适应市场、方便调节 3、成分简单,有利于分离纯化 4、成本低、生长周期短 5、为半合成提供原料 6、有望工业化生产
生物合成
缺点:1、产量低、不稳定 2、工业化放大研究
研究阶段
红豆杉生物合成途径基本明确
药源问题解决办法(一)
人工栽培
采用种子繁殖、扦插等无性繁殖方 法快速、大面积人工繁育红豆杉幼 苗
寻找红豆衫的替代物
从红豆杉非树皮部位提取 产紫杉醇的非红豆杉植物
优点:生长周期缩短 简便、直接
缺点:1、紫杉醇含量低 生长缓慢
2、提取工艺复杂
药源问题解决办法(二)
化学合成
全合成
缺点:1、合成过程烦琐复杂,几十步 2、费用高,化学试剂昂贵 3、总收率太低(2%)
但极难还原;
紫杉醇简介
紫杉醇研发过程
年代
1958 1967
进
展
NCI开始大规模植物药研发筛选 发现紫杉醇抗癌活性
•NCI称其为过去 15年中开发的最 好的抗癌药物
1968
从红豆杉中分离出紫杉醇
•20世纪90年代抗
1971
完成结构鉴定
肿瘤药的三大成
1979
发表作用机制
天然药物紫杉醇的研究进展

生物制药与研究2018·01168Chenmical Intermediate当代化工研究天然药物紫杉醇的研究进展*王俊松(大连市第十一中学 辽宁 116031)摘要:紫杉醇作为天然植物化学抗癌药物,被称为“晚期癌症的最后一道防线”。
目前紫杉醇的研究合成工作已经取得较大进展,生物合成、真菌发酵、植物组织细胞培养等现代生物技术手段逐渐进入大众的视野。
它复杂的化学结构,显著的生物活性,独特的作用机理,匮乏的自然资源等受到了各个研究行业的普遍关注。
关键词:紫杉醇;天然药物;抗癌中图分类号:R 文献标识码:AResearch Progress of Natural Medicine PaclitaxelWang Junsong(No.11 Middle School of Dalian City, Liaoning, 116031)Abstract :As a natural phytochemical anticancer drug, paclitaxel is called as "the last line of defense for advanced cancer". At present,paclitaxel research and synthesis work has made great progress. Biosynthesis, fungal fermentation, plant tissue cell culture and other modern biological technology have gradually entered the public field of vision. Its complex chemical structure, remarkable biological activity, unique mechanism of action, scarce natural resources have been widely concerned by various research industries.Key words :paclitaxel ;natural medicine ;anticancer1.紫杉醇的结构特点紫杉醇(taxol),又称作红豆杉醇,泰素,紫素,特素,是从红豆杉的树皮、树根和枝叶中提取出的一种化合物,是第一个获得FDA批准的第一个天然植物化学药物,被认为是已发现的功效最显著的天然抗癌药物。
紫杉醇类抗肿瘤药物的讲解

紫杉醇可以与微管蛋白二聚体以接近1∶1 的比例结合,破 坏微管聚合解聚的动态平衡,使细胞不能正常形成纺锤体 和纺锤丝,从而抑制其正常分裂增殖,并将细胞周期阻断 于G2 /M 期,直至死亡,进而起到抗癌作用。
抗肿瘤药物(二)之
紫杉醇类抗肿瘤药物
红豆杉又称紫杉,为红豆杉科红豆杉属(Taxus)植物,该 属植物全世界约11种,我国有4种1变种,其种子和枝叶在 民间用作利尿和通经药,但未见收载于常用传统中药文献。
1994年红豆杉被我国定为一级珍稀濒危保护植物,同时被 全世界42个有红豆杉的国家称为“国宝”,联合国也明令 禁止采伐,是名符其实的“植物大熊猫”。
紫杉醇注射液
成分:紫杉醇;辅料:聚氧乙烯蓖麻油
性状:无色至淡黄色的澄明黏稠液体
规格:60mg/10ml
适应症:卵巢癌、乳腺癌、非小细胞肺癌;头颈癌、食管 癌、精原细胞癌。
用法用量:单用135-200mg/m2,联合应用135-175mg/m2, 用生理盐水、5%葡萄糖、5%葡萄糖生理盐水稀释成0.31.2mg/ml溶液,静滴3h
不良反应
过敏反应。
主要毒性包括骨髓抑制( 以粒细胞减少症为主) 、神经毒性 和肌肉毒性。
紫杉醇的毒性呈剂量依赖性,紫杉醇与其他药物配伍用时, 给药顺序对中性粒细胞减少的严重程度有影响。
当顺帕治疗后再紫杉醇静脉输注, 或静脉输注紫杉醇先于 阿霉素或环磷酰胺治疗, 这些给药方案与相反的方案相比 较, 中性粒细胞减少比较严重。
4.胃癌:60mg/m2输注1小时,随后给予顺铂60mg/m2输注13小时(均仅 在用药第1天),顺铂输注结束时开始输注5氟尿嘧啶600mg/m2持续24h静滴,连续5天(21天为一周 期)。
抗癌药物紫杉醇的研究进展

优点:1、摆脱自然因素,可长期稳定 生长 2、适应市场、方便调节 3、成分简单,有利于分离纯化 4、成本低、生长周期短 5、为半合成提供原料 6、有望工业化生产 缺点:1、产量低、不稳定 2、工业化放大研究
红豆杉生物合成途径基本明确 10种相关酶基因被克隆表达 利用基因工程手段改造红豆杉提高紫杉醇产量
晋升网简介
晋升网( 晋升网()致力于成为医务工作者晋升职称心灵导师;是目前国内收录医 )致力于成为医务工作者晋升职称心灵导师; 学期刊、医学杂志最多最权威的医学学术平台;提供免费医学期刊在线阅读; 学期刊、医学杂志最多最权威的医学学术平台;提供免费医学期刊在线阅读;网罗和甄 选海量优秀医学论文检索,独立研发医学在线资源分享库和医学在线模拟考试库; 选海量优秀医学论文检索,独立研发医学在线资源分享库和医学在线模拟考试库;整合 刊类、标题、关键词检索及全文检索,并独家研发刊社管理和刊社加盟系统、在线投稿、 刊类、标题、关键词检索及全文检索,并独家研发刊社管理和刊社加盟系统、在线投稿、 在线查稿、在线阅读、远程审稿、在线下载等系统;聚刊社力量,建服务平台, 在线查稿、在线阅读、远程审稿、在线下载等系统;聚刊社力量,建服务平台,让晋升 网通过“专业”走入每一个医务人员的身边是我们不懈的追求目标; 网通过“专业”走入每一个医务人员的身边是我们不懈的追求目标; 晋升网()标准 标准 晋升网 最便捷的晋升通道 最高效的学习方法 最丰富的医学文献 最权威的医学期刊 最专业的医学服务
紫杉醇开发的关键问题
上游产业——药源问题 下游制剂产业
药效(活性、水溶性) 安全性 生物相容性
药源问题
红豆杉
主要原料植物 国家一级保护野生植物,全球十大濒危物种 之一
紫杉醇的应用及其研究的进展

紫杉醇的应用及其研究的进展摘要:紫杉醇是当前乃至未来十几年间理想的抗癌药物,它的研究一直受到很多人关注。
紫杉醇分子是一个极其复杂的四环二萜类化合物,可使微管蛋白和组成微管的微管蛋白二聚体失去动态平衡,达到阻止癌细胞生长的效果。
紫杉醇的生产有化学半合成、红豆杉细胞悬浮培养、直接从红豆杉科植物中分离提取及微生物发酵。
紫杉醇对卵巢癌、乳腺癌、食管癌、肺癌等多种晚期癌症有不错的疗效,对它的研究有着深远的意义。
关键字:紫杉醇药理机制获取途径医疗应用一.紫杉醇的简介紫杉醇是美国北卡罗莱纳州三角研究所的Wall博士和Wani博士于1967年发现的。
之后,他们又从太平洋红豆杉中分离出了这种化合物并发现它具有广泛的抗恶性肿瘤作用[1]。
1970年这两位科学家通过x射线衍射分析测定了紫杉醇的结构,并在1971年发表了这一研究成果。
紫杉醇分子是一个极其复杂的四环二萜类化合物:1个紫杉烷环加1个4元素组成的氧烷环,在C-2和C-13上还分别有一个苯氧基和酯基侧链[2]。
紫杉醇是一种新型抗癌药物,它的作用模式是经过促进微管聚合,并稳定微管并抑制其解聚,目前已经被广泛用于治疗卵巢癌、肺癌和乳腺癌。
紫杉醇早在2O世纪6O年代就被证实是一种具有丰富功能的药物,只要分离于红豆杉。
但是红豆杉生长非常缓慢且紫杉醇含量极低,从树皮中分离紫杉醇相当困难。
我国为了生产紫杉醇,导致红豆杉野生资源遭到严重破坏.紫杉醇含量很低,目前公认含量最高的短叶红豆杉干树皮中也仅有0.060%—069%[3],而且红豆杉生长不仅缓慢,还需要苛刻的自然环境。
目前国际市场上的紫杉醇仍依靠从红豆杉树皮提取及半合成,迄今为止尚未见有第三种形式形成大规模工业化生产的报道。
紫杉醇的工业生产受到了原料和技术两方面的制约,短期内难以突破。
为了解决红豆杉资源短缺与紫杉醇需求量的日益增加的矛盾,人们对生产紫杉醇进行了多方面的研究,包括化学合成、红豆杉细胞培养及微生物发酵。
紫杉醇的提取或生产日益成为许多国家研究的热点,人们希望能找到一条既能满足对紫杉醇需求又不危及红豆杉生存的途径。
紫杉醇制剂研究进展

紫杉醇制剂研究进展唐富山1,焦海胜2,原凌燕1,朱峰梅3,李红卫2(11金川集团公司医院,甘肃金昌 737100;21兰州大学第二医院药剂科,甘肃兰州 730030;31甘肃省医疗器械质量监督检验站,甘肃兰州 730030) 紫杉醇(Paclitaxel,Taxol,TA X)是由Wani和Wall等最早从太平洋红豆杉(Taxus bravifolia Nutt)的树皮中提取得到的一种四环二萜类化合物[1]。
TAX具有稳定微管并促进其聚合和组装的独特作用。
临床用其注射液治疗转移性卵巢癌和乳腺癌效果较好,特别是对顺铂耐药或未控制的卵巢癌亦有效,对食道癌和肺癌也有一定疗效。
被誉为20世纪后叶抗肿瘤药物研究的最大发现[2]。
但由于:(1)TAX药源紧张[3];(2)TAX的水溶性低,口服生物利用度差;(3)现有TA X注射液的不良反应:易引起过敏反应,中性粒细胞减少,骨髓抑制及室性心律不齐等,人们广泛开展了TA X制剂的研究。
本文主要从提高水溶性、增加靶向性等角度概述TA X制剂研究的进展。
1 水溶性制剂由于TAX本身几乎不溶于水(溶解度只有0125μg・mL-1),在体内利用率低,故现行临床使用的紫杉醇注射液(Taxol R)中的TAX是靠聚氧乙烯蓖麻油(Cremop hor EL)与脱水乙醇以1∶1的混合液来稳定和溶解,浓度为6mg・mL-1,使用前用生理盐水或5%葡萄糖稀释到最终给药体积。
这种药物载体会引发一些副作用,其中包括严重的过敏反应,故在给药前病人需预先进行抗敏处理[4]。
提高TAX在水中的溶解度、减少制剂中Cremo2 p hor EL的用量是目前TA X制剂所要解决的重大问题。
人们首先考虑到在TA X的2′2和72位连接上一些水溶性集团制成TAX的前药,以提高TAX 的水溶性[5,6]。
TA X的前药在生理条件下水解释放出TA X。
但水溶性前药一般不稳定,在一定程度上还会影响TA X的药效,因而还没有正式商品化。
抗癌药物-紫杉醇合成和应用研究进展

・ 1 2 9 ・
抗癌药物 一紫杉醇 合成 和应用研究进 展
于 海 涛 ( 哈 药集 团技 术 中心 , 黑龙 江 哈 尔: 紫杉醇是从红豆杉 中所提得 , 是 红豆杉属植物 中的一种 复杂的次生代谢 产物 ,也是 目前所 了解的惟一一种 可以促进微 管聚 合 和稳 定 已聚合微管的药物 , 已成为 目前全球 销售量排 名第一的抗肿瘤药物。对紫杉醇合成和应 用研 究进展进 行 了比较详尽 的综述 , 分 以下几个部 分 : 紫杉醇的发现历 史、 紫杉 醇的合成 、 紫杉 醇的应 用。
关键词 : 紫杉 醇 ; 合 成; 应 用 研 究
紫杉醇 是一种从红 豆杉的枝 、 皮、 叶提取 出来 的一种 有效 的植 的合 成 , 首先 , d一苯丙 氨酸( d— p h e n y l a l a n i n e )在 苯丙 氨酸氨 基变 p h e n y l a l a n i n e a mi n o mu t a s e , P A M)的作用下异构化 为 B苯丙 物抗癌药 , 目前是世界 上唯一从枝 、 皮、 叶、 果 内提取出来物质 。 通 过 位酶 ( Ⅱ一 Ⅲ临床研 究 ,它对肿瘤 细胞 的生长有很强的抑制作用 ,如乳腺 氨酸 ( p— p h e n y l a l a n i n e ) ,再 与 乙酰辅酶 A结合生 成 B— p h e n y — 癌、 肺癌 和卵巢癌等 。 紫 杉醇对乳腺癌 细胞进行杀伤 , 通 过抑制肿瘤 l a l a n y l C o A; 紫杉醇 的形成 , 苯基 异丝氨酸侧链 与紫杉烷母核 的 C 。 , 细胞的迁移 , 诱导 细胞抗凋亡分 子失 活 , 抑制癌基 因的表达 , 激活免 位通过酰化反应 , 在苯基异丝氨酸侧链 C : 。 位和 C ’ 位分别被羟化和 疫细胞对肿瘤细胞 的杀伤 , 调控 微管动力学稳定等 。紫杉醇被普遍 苯 甲酰化 , 最终合成紫杉醇 。 3紫杉醇的应用 认为是人类近年来最有效的抗癌药物之一。 四大植物 中提取 的抗肿瘤药物 紫杉 醇 、 长 春花 碱 、 喜 树碱 、 秋 水 1紫杉醇 的发现研究 紫杉醇 , 英文名称 P a c l i t a x e l , 别 名红豆杉 醇 , 泰素 , 紫素 , 特素, 仙素 , 紫杉醇催化微管蛋 白迅速合成微管并结合 到微管 上起 稳定 和 化学名 称 5 I S, 2 0 一环 氧 一 1 , 2 O t , 4 , 7 B, 1 0 B, 1 3 O t 一六 羟基紫 杉烷 防止微管解聚的作用 , 与其它三个纺锤体毒物 如阻止微 管聚集的作 1 1 一烯 一 9 一酮 I 4 , 1 0 一二 乙酸酯 一 2 一苯 甲酸酯 一 1 3 [ ( 2 ’ R, 3 ’ S ) 一 N 一 用正好相反。 苯 甲酰 一 3 一苯基异丝氨酸酯1 ,分子量 8 5 3 . 9 2 ,分子式 C H N O H 。 紫杉醇 的活性就表 现在两个 方面 : 第一 , 对于迅 速分裂 的肿瘤 1 9 6 3年 美 国化 学家 瓦尼 ( M. C . Wa n i ) 和沃 尔 ( M o n r e E .Wa l 1 ) 第 一 细胞 , 紫杉醇“ 冻结 ” 有丝分裂纺锤体 。 从而使肿瘤细胞停止在 G 2 期 次从 一种叫做太平洋杉的树皮和木材 中提取到 了紫杉醇 的粗提 物 , 和 M期 , 直至死亡I ; 第二 , 紫杉醇也作用于 巨噬细胞上的肿瘤坏死 在随后 的的筛选实验 中 , Wa n i 和 wa J 1 研究 发现紫杉醇 的粗 提物对 因子( T N F ) 受体 , 促使释放 白细胞介 素( I L ) 一 1 、 ( T N F ) 一 2 、 ( I L ) 一 6 、 干扰 素 肿 瘤细胞有很强的活性 , 于是开始分 离紫杉醇的粗提物 。通过不断 ( I F N ) 一 1 , ( I F N ) 一 1因子对肿瘤 细胞起杀 伤或抑制肿 瘤细胞迁 移作用 的研究 以及技术 的发展 , 终于在 1 9 7 1 年, 在杜克( D u k e ) 大学的化学 紫杉醇对于肿瘤细胞或株系是否有作用取决于细胞是否具有敏 教授姆 克法尔 ( A n d r e T .Mc P h a i l ) 的配合下 , 用X 一射线分析 确定 了 感性 ,与 细胞膜上是 否存在磷 酸化 的 1 3 5 一 K D糖蛋 白有密 切的联 敏感 细胞一般都有关 , 而非敏 感细胞 , 1 3 5 一 K D膜蛋 白起 一种将 该 活性成份 的化学结构 为一 种三环二萜化 合物 ,并 命名为紫杉 醇 系 , 紫杉醇泵 出胞外 的作用目 。研 究表 明紫杉 醇治疗卵巢 癌 , 有 效率为 ( t a x o 1 ) 。 2 紫杉醇的合成 3 6 %, 治疗后 可以从事 工作 , 治疗乳腺癌 , 有效率为 6 5 %, 治疗 肝癌 , 2 . 1 紫杉醇的天然提取 有效 率为 4 2 %,有人认 为紫杉醇 的第 一适 应症 是转移性卵巢 癌, 而 目前 市场上销售 的紫杉醇类 药品大部 分是从天 然或者栽培 红 第二适应症是难治性的转移性乳腺癌。 另外临床医学界陆续发现结 豆 杉的树皮或枝 叶 中直接提 取得到 , 主要采取 的提 取方法有 : 有 机 肠癌 、 直肠癌 、 膀胱癌和乳癌都可以应用 紫杉醇 。 人类 于 1 9 6 7年发现紫杉醇 , 对于他 的研究就 一刻没停止过 , 涉 溶剂 提取法 、 组织膜渗 透法 、 液相提取法 、 超 临界 流体提取法 , 采 取 柱层析法 、 薄层 色谱法 、 沉淀法 、 树脂 吸附分离法进行精制 。 及到化学 、 生物、 食品及药品等。 一直 到今天 它的研究热潮没有丝毫 2 . 2紫杉醇的细胞培养 减退 , 每年都会涌现 出很多新颖 的高水平 的研究成果 。其 中很多研 根据细 胞全能化 的观点 ,通过 细胞培养方 式可大量 生产紫杉 究成果都 显示 出很高 的学术 造诣 , 各种 串联反应 的应 用 、 转化合 成 醇 。红豆杉愈伤组织诱导与培养技术 已经成熟 , 诱导愈伤组织 的基 和不对称催化等 , 同时结构修饰和活性研究在 紫杉 醇的研究 中也不 本培养基 , 激素种类 和浓 度 , 外植体类型 , 培养条件等 因素和培养程 断 出新 , 开发 的新 型紫杉醇类似物 日益增多 , 我们有理 由相信紫 杉 序都已经确定 , 目前 细胞培养是解决 紫杉醇来源的一条非常有效 的 醇在未来的药物治疗 、 化学研究和生物制药领域必将继续 占据着举 途 径。同时细胞培养具有方式速度快 、 培养条件易于优化 、 培养过程 足轻重的地位。 易于人工控 制 、 不受时 间地 域等 因素 的限制 的特点 , 被 国内外 厂商 参 考 文 献 普 遍采用 , 并且利用此法 生产 的紫杉醇原料药产量 已达 1 0公斤级。 [ 1 】 刘 可夫 . 合 成 生物 学在 紫 杉醇 合成 中的应 用『 J ] . 生命 科 学仪 器, 2 . 3紫杉醇 的微生物合成 2 0 1 3 , 1 1  ̄) : 2 6 - 2 9 . 从红豆杉韧皮部分离 得到一种寄生真菌 , 在 特定 的培养基中产 [ 2 】唐培 ,王锋鹏 .近年 来紫杉 醇的合成研 究进 展 叽 有机 化 学, 生紫杉醇及其相关络 合物 , 由于真菌生长速度快 、 来源广 的特点 , 可 2 0 1 3 , 3 3 ( 3 ) : 4 5 8 — 4 6 8 . 以通过发酵 大规模生产 。 通过改变培养条件和应用重组 D N A技术 , 【 3 】 黄 淑娟 . 抗肿 瘤 药紫杉醇 的临床应 用及不 良反应 分析 [ J 】 . 当代 医 可望提 高紫 杉醇 的产量 。红豆杉的根也含有大量紫杉醇 , 可以采用 学, 2 0 1 6 。 2 2 ( 3 2 ) : 1 4 6 — 1 4 7 . 根农杆菌侵染红 豆杉植物外植体诱 导生根 , 通过此 培养系统生产紫 【 4 ] 梁华丽. 紫杉醇纳米颗粒制备和应 用『 J ] . 亚太传统 医药, 2 0 1 6 , 1 2 ( 7 ) : — 5 3 . 杉醇 , 可 以大量生产紫 杉醇 , 具 有需外援激 素 、 发根 生产迅速 、 遗传 52 性 状 稳 定 的特 点 。 [ 5 ] 匡雪君, 王彩 霞, 邹 丽秋 等. 紫杉醇 生物合 成途径及 合成 生物学研 2 . 4紫杉醇的人工合成 究进展 『 J 1 . 中国中药杂志, 2 0 1 6 , 4 1 ( 2 2 ) : 4 1 4 4 — 4 1 4 9 . 紫杉醇分子结构 比较复杂 , 由三环 c 6 _c 一c 架 和桥 头双键 以 【 6 】 鲁 治 文, 钱 章君 . 紫杉 醇脂质 体 临床应 用进 展 f J 1 . 亚 太传统 医药, 及众多的含氧取代基构成 。它 的合成一般分 为 3个阶段 : 紫杉烷 环 2 0 1 2 , 8 ( 1 2 ) : 2 2 9 — 2 3 2 . 母核结 构的合成 , 此过程 首先进行三环二 萜骨架 的形 成 , 然后在骨 架上进行 官能 团反应 , 最终 合成生成 巴卡亭 Ⅲ; 苯基异丝 氨酸侧链
紫杉醇生物合成
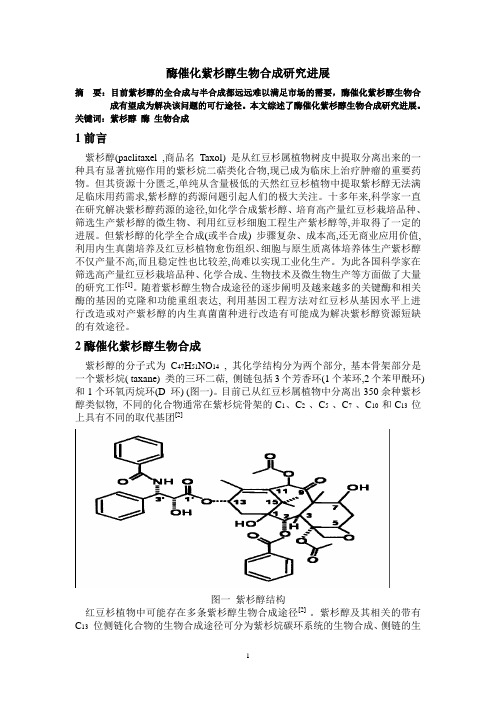
酶催化紫杉醇生物合成研究进展摘要:目前紫杉醇的全合成与半合成都远远难以满足市场的需要,酶催化紫杉醇生物合成有望成为解决该问题的可行途径。
本文综述了酶催化紫杉醇生物合成研究进展。
关键词:紫杉醇酶生物合成1前言紫杉醇(paclitaxel ,商品名Taxol) 是从红豆杉属植物树皮中提取分离出来的一种具有显著抗癌作用的紫杉烷二萜类化合物,现已成为临床上治疗肿瘤的重要药物。
但其资源十分匮乏,单纯从含量极低的天然红豆杉植物中提取紫杉醇无法满足临床用药需求,紫杉醇的药源问题引起人们的极大关注。
十多年来,科学家一直在研究解决紫杉醇药源的途径,如化学合成紫杉醇、培育高产量红豆杉栽培品种、筛选生产紫杉醇的微生物、利用红豆杉细胞工程生产紫杉醇等,并取得了一定的进展。
但紫杉醇的化学全合成(或半合成) 步骤复杂、成本高,还无商业应用价值,利用内生真菌培养及红豆杉植物愈伤组织、细胞与原生质离体培养体生产紫杉醇不仅产量不高,而且稳定性也比较差,尚难以实现工业化生产。
为此各国科学家在筛选高产量红豆杉栽培品种、化学合成、生物技术及微生物生产等方面做了大量的研究工作[1]。
随着紫杉醇生物合成途径的逐步阐明及越来越多的关键酶和相关酶的基因的克隆和功能重组表达, 利用基因工程方法对红豆杉从基因水平上进行改造或对产紫杉醇的内生真菌菌种进行改造有可能成为解决紫杉醇资源短缺的有效途径。
2酶催化紫杉醇生物合成紫杉醇的分子式为C47H51NO14, 其化学结构分为两个部分, 基本骨架部分是一个紫杉烷( taxane) 类的三环二萜, 侧链包括3个芳香环(1个苯环,2个苯甲酰环) 和1个环氧丙烷环(D 环) (图一)。
目前已从红豆杉属植物中分离出350余种紫杉醇类似物, 不同的化合物通常在紫杉烷骨架的C1、C2 、C5 、C7 、C10 和C13 位上具有不同的取代基团[2]图一紫杉醇结构红豆杉植物中可能存在多条紫杉醇生物合成途径[2] 。
紫杉醇及其相关的带有C13位侧链化合物的生物合成途径可分为紫杉烷碳环系统的生物合成、侧链的生物合成、紫杉烷系统和侧链的酯化反应, 形成完整的紫杉醇分子三个主要阶段。
抗癌药物——紫杉醇合成和应用研究进展

抗癌药物——紫杉醇合成和应用研究进展
应站明;李媛;李振宇
【期刊名称】《萍乡高等专科学校学报》
【年(卷),期】2006(000)006
【摘要】紫杉醇是目前最新的具有很好疗效的抗癌药物,本文对紫杉醇发现以来的最新研究进展进行了比较详尽的综述.包括以下几个部分:1.紫杉醇的发现和历史;2.紫杉醇的药效;3.紫杉醇的来源;4.紫杉醇的生物合成途径及其相关酶基因的研究.【总页数】3页(P69-71)
【作者】应站明;李媛;李振宇
【作者单位】萍乡高等专科学校,江西,萍乡,337042;中山大学生命科学学院,广东,广州,510275;中山大学生命科学学院,广东,广州,510275
【正文语种】中文
【中图分类】R979.1
【相关文献】
1.抗癌药物紫杉醇的全合成--Holton合成紫杉醇路线的剖析 [J], 陈巧鸿;王锋鹏
2.抗癌药物-紫杉醇合成和应用研究进展 [J], 于海涛
3.抗癌药物紫杉醇的合成方法进展 [J], 王夏实
4.抗癌药物紫杉醇的合成方法进展 [J], 王夏实;
5.肝素-紫杉醇抗癌药物系统的合成及其对癌细胞生长抑制的研究 [J], 谭平
因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1 概述 紫杉醇( Paclitaxel,商品名 ) 是近年来最令人瞩目的
抗癌药之一。1966 年,美国化学家 M. Wall 和 M. Wani 首先 从太平洋紫杉( Taxus brevifolia) 的树皮中分离得到了这种天 然紫杉烷类二萜化合物。1992 年 12 月 29 日,美国 FDA 正式 批准紫杉醇 做 为 治 疗 晚 期 卵 巢 癌 的 新 型 抗 癌 药 上 市。1996 年,紫杉醇的半合成类似物脱乙酰紫杉醇( 紫杉特尔,docetaxel,商品名 Taxotere) 也获得了美国 FDA 做为治疗晚期乳腺癌 和卵巢癌的抗癌药的批准。体外抗肿瘤活性实验表明,其抗 肿瘤活性强于紫杉醇。
具体内容: ①患者状态的评估②用药指导,包括口服降糖 药的分类; 服用方法及注意事项; 口服降糖药的联合应用。③
口服降糖药与血糖监测④服用口服降糖药期间低血糖的预防 和治疗 2. 4 糖尿病的病情监测 监测自觉症状的变化; 监测体重, 血压的改变; 化验指标的监测: 血糖,糖化血红蛋白,尿糖,酮 体,血脂,尿蛋白及肾功能等; 监测胰岛功能的变化; 监测并发 症的早期发现或进展; 监测药物治疗的效果; 认真填写每天观 察记录表,尤其病情严重的患者更应注意。 2. 5 糖尿病教育 通过定期举行健康知识讲座,使患者和家 属掌握了糖尿病预防和自我护理知识,密切了患者与专科护 士的关系,取得 了 相 互 间 的 信 任,使 健 康 指 导 及 管 理 顺 利 开 展。提高了糖尿病患者健康管理的有效性和及时性。
·237·
0. 07% ,超过了同期国际上报道的 0. 032% 的水平[2]。 3 半合成的紫杉醇类似物
紫杉醇的构效关系已经被众多学者所研究和总结。具有 游离羟基的 C13 位侧链,C2 和 C4 位的酯基,C4 、C5 位四元含氧 环及紫杉烷的刚性环结构对抗癌活性都起着很重要的作用。
1988 年,Potier 等从欧洲紫杉( Taxus baccata) 中分离得到 10-去乙酰巴卡亭( Baccatin) Ⅲ( DAB) ,DAB 已被成功地用来 半合成紫杉醇,并已工业化生产[3]。半合成紫杉醇被认为是 除人工种植外,扩大紫杉醇来源的最有效途径。
糖尿病患者运动治疗的教育: ①合理运动的益处②适宜 运动和不适宜运动的人群③运动方式的选择和强度④运动三 步曲⑤运动治疗与血糖监测 2. 3 药物治疗的管理 药物治疗是糖尿病五大综合疗法中 的重要组成部分,口服降糖药物可直接起到降血糖的作用,口 服的方法相对简单,比较容易被糖尿病患者接受。但是要保 证患者能够正确的服用口服降糖药物,使血糖得到良好控制, 仍有很多需要注意的地方,需要专科护士对口服降糖药物治 疗的患者进行合理的护理和教育。
[8] Polizzi D,Pratei G,Tortoreto M,et al. A novel taxane with improved tolerability and therapeutic activity in a panel of human tumor xenografts. Cancer Res,1999,59( 5) : 1036-1040.
·236·
中国实用医药 2011 年 8 月第 6 卷第 24 期 China Prac Med,Aug 2011,Vol. 6,No. 24
2. 2 运动管理 众所周知“生命在于运动”任何人都需要运 动。而对于糖尿病患者来讲,运动尤其重要。要指导糖尿病 患者进行科学,合理,健康的运动,就需要糖尿病教育工作者 掌握更多的糖尿病运动方面的知识,并亲身投入到健身运动 当中去,从中了解和感受运动带来的好处,这样才能在给患者 进行指导的时候更有说服力和针对性,才能让患者了解和掌 握科学合理并有效的运动方法
4 结语 天然来源是紫杉醇最主要的来源途径。随着科学工作者
对紫杉醇的深 入 研 究,紫 杉 醇 的 多 种 来 源 途 径 被 开 辟 出 来。 通过对其进行结构修饰所得到的紫杉醇类化合物及其类似 物,显示出与紫杉醇相当甚至更强的抗癌活性,并且抗多药耐 药性、水溶性、抗癌谱、毒副作用等诸方面性质均优于紫杉醇。 可以预见,通过计算机辅助药物设计和其他新颖的药物设计 方法,在明确配基与受体三维结构和相互作用的基础上,将会 设计并合成出更好的药理活性、副作用更小、更为安全、有效、 方便的紫杉醇衍生物及其类似物。
参考文献
[1] 卫生部. 科技部. 国家统计局. 中国居民营养与健康现状,2004, 10: 12.
[2] 陈君石,等. 个人健康管理在健康保险中的应用———进展与趋 势. 健康管理与健康保险高层论坛论文集,2003.
天然抗癌药紫杉醇及其半合成类似物的研究进展
·综述·
何晓明
【摘要】 天然来源是紫杉醇最主要的来源途径。随着科学工作者对紫杉醇的深入研究,紫杉醇的 多种来源途径被开辟出来。通过半合成并对其进行结构修饰所得到的紫杉醇类化合物及其类似物,显 示出与紫杉醇相当甚至更强的抗癌活性,并且其抗多药耐药性、水溶性、抗癌谱、毒副作用等诸方面性质 均优于紫杉醇。
参考文献
[1] Holton R,Somoza C,Kim H,et al. First Total Synthesis of Taxol. 1. Functionalization of the B Ring. J Am Chem Soc,1994, 116: 1597-1600.
[2] 李云 . 红豆杉体外培养生产紫杉醇研究 . 北京林业大学学报, 2003,25( 1) : 86-92.
紫杉醇的 C4 甲基碳酸酯衍生物,其水溶性比紫杉醇强 40 多倍,口服给药后血药浓度约为紫杉醇的 50 多倍。在此基础 上进行进一步的修饰,发现了新的紫杉醇类似物化合物,已处 于临床试验阶段[6]。
1992 年,14β-羟基-10-去乙酰巴卡亭 ( Baccatin) Ⅲ ( 14βhydroxyl-DAB) 从喜马拉雅山紫杉( Taxus wallicbiana Zucc. ) 中 分离得到,与紫杉醇及多烯紫杉醇的前体化合物 10-去乙酰巴 卡亭Ⅲ相比较,C14 位多一个羟基。在此基础上,Ojima 研究组 合成了 C3 ' 和 C10 位修饰的 C1 、C14 位碳酸酯基-14β-羟基-10去乙酰巴卡亭( Baccatin) Ⅲ衍生物,如已进入临床试验阶段 的奥兰索,其对多药耐药细胞株的细胞毒性比紫杉醇强 440 多倍[7],口服时具有非常好的生物利用度 ( 48% ~ 50% ) ,可 以减少神经和其他毒性,还可以 做 为 P 糖 蛋 白 ( P-glycoprotein,P-gp) 的逆转剂[8]。
迄今为止,紫杉醇最主要的来源途径是从红豆杉属植物 的茎皮中分离提取得到。在这些树木中,紫杉醇的含量很低。 有人计算曾做过估算,治疗一个卵巢癌患者,需要 6 棵树龄 60 ~ 100 年的红豆杉树。为了解决紫杉醇天然来源困难的情 况,各国科学家进行了多种尝试。
1994 年,美国佛罗里达州立大学 R. Holton 教授的研究组 采用线性途 径,实 现 了 紫 杉 醇 的 全 合 成[1]。 但 是,紫 杉 醇 的 全合成步骤太多,总收率极低,因此没有进行大规模工业生产 的意义。
【关键词】 紫杉醇; 半合成; 结构修饰
【Abstract】 The main source of paclitaxel was nature. A lot of sources were discovered by scientist's research. The paclitaxel derivatives which were semi-synthesized and structural modified,had more anti-cancer activities,anti-multi-drug resistance,water solubility,anti-cancer species,and less poison-side effects than paclitaxel.
[6] Rose W,Long B,Fairchild C,et al. Preclinical pharmacology of BMS-275183: an orally active taxane. Clin Cancer Res,2001,7 ( 7) : 2016-2021.
[7] Distefano M,Scambia G,Ferlini C,et al. Anti-proliferative activity of a new class of taxanes ( 14 beta-hydroxy-10-deacetylbaccatin Ⅲ derivatives) on multidrug-resistance-positive human cancer cells. Int J Cancer,1997,72( 5) : 844-850.
1991 年,Gibson 等申请了用组织细胞培养方法生产紫杉 醇及其类似物的美国专利。中国华中理工大学王君健教授领 导的 研 究 组 于 1993 年 获 得 了 细 胞 培 养 的 紫 杉 醇,含 量 达
中国实用医药 2011 年 8 月第 6 卷第 24 期 China Prac Med,Aug 2011,Vol. 6,No. 24
[3] Ojima I,Habus I,Zhao M,et al. New and efficient approached to the semisynthesis of taxol and its C13 side chain analogs by means of β-lactam synthon method. Tetrahedron, 1992, 48 ( 34 ) : 6985-7012.
[4] Ringel I,Horwitz S. Studies with RP56976 ( Taxotere) : a semisynthetic analog of taxol. J Natl Cancer Ins,1991,83( 4) : 288-291.
