连续搅拌釜式反应器讲述
理想混合连续搅拌釜式反应器(CSTR)

理想混合状态
物料在反应器内达到完全混合,不存在浓度和温度 的梯度分布。
反应器内各点的物料性质(如浓度、温度等)完全 相同,且随时间保持不变。
在理想混合状态下,反应器的性能达到最优,反应 效率和产物质量得到保证。
03
CSTR反应器的数学模型
物料平衡方程
进入反应器的物料流量与离开 反应器的物料流量相等,即输 入等于输出。
用于连续加入反应物和排出产物,实现连续化生产 。
工作流程
01
02
03
04
物料进入
反应物通过进料口连续加入反 应器内。
充分混合
在搅拌装置的作用下,物料在 反应器内充分混合,达到浓度 和温度的均匀分布。
反应进行
在适宜的反应条件下,物料在 反应器内进行化学反应。
产物排出
反应完成后,产物通过出料口 连续排出反应器。
100%
平均停留时间
表示物料在反应器内的平均停留 时间,影响反应器的生产能力和 产品质量。
80%
停留时间分布曲线
通过实验测定,可直观反映反应 器内物料的停留时间分布情况。
转化率与选择性
转化率
表示原料在反应器内转化为产 品的程度,是衡量反应器性能 的重要指标。
选择性
表示在给定转化率下,生成目 标产物的能力,反映反应器的 选择性能。
THANK YOU
感谢聆听
缺点与挑战
能耗较高
连续搅拌过程需要消耗大量能量,导致CSTR反应器的能耗相对较 高。
设备复杂度高
CSTR反应器结构复杂,涉及搅拌、传热、传质等多个过程,设备 设计、制造和维护难度较大。
放大效应
在将实验室规模的CSTR反应器放大至工业生产规模时,可能会遇到 放大效应问题,影响反应器的性能和产物质量。
釜式反应器操作与控制—理想连续操作釜式反应器

理想连续操作釜式反应器的计算
理想连续操作釜式反应器的计算
理想连续操作釜式反应器的计算
通过[例2-1]和[例2-2]的反应结果可以看出:完成相 同的生产任务,连续操作釜式反应器的生产时间比间歇操 作釜式反应器的生产时间要长。主要原因是连续操作釜式 反应器内的化学反应是在出口处的低浓度下进行的。
反应时间不是判别反应器生产效率高低的唯一标准,还需综合考虑
同的搅拌和加料情况,以适应工艺上的不同要求。
理想连续操作釜式反应器
管式反应器
理想连续操作釜式反应器
投资大 职工工作量大
维护成本高 操作难度高
串联釜数一般不超过4
《化学反应器操作与控制》
多釜串联的计算
多釜串联的计算
多釜串联
理想连续操作釜式反应器
n-CSTR的基础设计式
理想连续操作釜式反应器
《化学反应器操作与控制》
理想连续操作釜式反应器的特点
理想连续操作釜式反应器的特点
理想连续操作釜式反应器操作现场
理想连续操作釜式反应器的特点
流体流动符合全混流理想流动模型 连续进料和出料; 过程参数与空间位置、时间无关; 容易自动控制,节省人力。
理想连续操作釜式反应器的特点
反应物浓度、转化率、反应速率处处相等
QkJc/与hT的函数关系式在Q-T坐标图 上为一直线。
▪2. 放热速率Qr和移热速率Qc
结论: 热稳定状态点一定是定态
点,而定态点不一定都具有热 稳定性。
▪ 3.热稳定条件
定常条件:Qr=QC
▪ 稳定条件
dQr dQc dT dT
注意::CSTR中进行吸热反应时 ,
没有热稳定性问题。
▪ 3.热稳定条件
《化学反应器操作与控制》
连续釜式反应器

打漩现象
搅拌器两方面性能: 产生强大的液体循环流量; 产生强烈的剪切作用。 基本原则: 在消耗同等功率的条件下,低转速、大直径 的叶轮,可增大液体循环流量,同时减少液体受到的剪切 作用,有利于宏观混合。 反之,高转速、小直径的叶轮,结果与此恰 恰相反。
常用搅拌器的型式、结构和特点 化学工业中常用的搅拌装置是机械搅拌装置,包 括 搅拌器:包括旋转的轴和装在轴上的叶轮; 辅助部件和附件:包括密封装置、减速箱、搅拌电 机、支架、挡板和导流筒等。 搅拌器是实现搅拌操作的主要部件,其主要的组 成部分是叶轮,它随旋转轴运动将机械能施加给液体, 并促使液体运动。
通常可以采取τ1=τ2,这时整个反应系统最优。 即要
这时
釜式反应器的故障处理及维护要点
序 1 故障现象 壳体损坏 ( 腐蚀、 裂纹、透 孔) 超温超压 故障原因 1.受介质腐蚀(点蚀、晶间腐蚀) 2.热应力影响产生裂纹或碱脆 3.损变薄或均匀腐蚀 1.仪表失灵,控制不严格 2.误操作;原料配比不当;产生剧热反应 3.因传热或搅拌性能不佳,发生副反应 4.进气阀失灵,进气压力过大、压力高 处理方法 1.用耐蚀材料衬里的壳体需呕新修衬或局部补焊 2.焊接后要消除应力,产生裂纹要进行修补 3.超过设计最低的允许厚度需更换本体 1.检查、修复自控系统,严格执行操作规程 2.根据操作法,紧急放压,按规定定量。定时投料, 严防误操作 3.增加传热面积或清除结垢,改善传热效果;修复 搅拌器,提高搅拌效率 4.关总气阀,切断气源修理阀门 1.更换或修补搅拌轴,并在机床上加工,保证表面 粗糙度 2.调整油环位置,清洗油路 3.压紧填料,或更换填料 4.修补或更换 5.更换摩擦副或重新研磨 6.调整比压要合适,加强冷却系统,及时带走热量 7.密封圈选材、安装要合理,要有足够的压紧力 8.停车,重新找正,保证垂直度误差小于0.5mm 9.严格控制工艺指标,颗粒及结晶物不能进入摩擦 副 10.调整、检修使轴的窜量达到标准 11.改进安装工艺,或过盈量要适当,或粘接剂要好 用,粘接牢固
连续搅拌釜式反应器(CSTR)控制系统设计 连续

连续连续搅拌釜式反应器搅拌釜式反应器搅拌釜式反应器((CSTR )控制系统设计1. 前言连续搅拌釜式反应器(continuous stirred tank reactor ,简称为CSTR )是聚合化学反应中广泛使用的一种反应器,该对象是过程工业中典型的、高度非线性的化学反应系统。
在早期反应釜的自动控制中,将单元组合仪表组成位置式控制装置,但是化学反应过程一般都有很强的非线性和时滞性,采用这种简单控制很难达到理想的控制精度。
随着计算机技术和PLC 控制器的发展,越来越多的化学反应采用计算机控制系统,控制方法主要为数字PID 控制。
但PID 控制是一种基于对象有精确数学模型的线性过程,而CSTR 模型最主要的一个特征就是非线性,因此PID 控制在这一过程中的应用受到限制。
随着现代控制理论和智能控制的发展,更加先进有效的控制方法应用于CSTR 的控制,如广义预测控制,神经模糊逆模PID 复合控制,自抗扰控制,非线性最优控制,基于逆系统方法控制,基于补偿算子的模糊神经网络控制,CSTR 的非线性H ∞控制等。
但任何一种复杂的化工反应过程都不能用一种简单的控制方式达到理想的控制效果。
目前先进的反应釜智能控制技术就是将智能控制理论和传统的控制方法相结合,如钟国情、何应坚等于1998年对基于专家系统的CSTR 控制系统进行了研究[1],宫会丽、杨树勋等于2003年发表了关于PID 参数自适应控制的新方法[2],冯斌、须文波等于1999年阐述了利用遗传算法的寻优PID 参数的模型参考自适应控制方法等[3]。
但由于这些控制方法的算法比较复杂,在算法的工程实现、现场调试及通用型方面存在着局限性,因此研究一种相对简单实用的CSTR 控制方法,更易为工程技术人员所接受。
本文在对CSTR 过程及其数学模型进行详细分析的基础上,针对过程的滞后性,采用Smith 预估算法与PID 控制相结合的方法实现CSTR 过程的控制,该方法具有实用性强及控制方法简单等特点,基于西门子PCS7系统完成了CSTR 过程控制系统设计。
第五章釜式连续反应器

n为搅拌器转数;d为搅拌器叶轮直径;NQR为无因次准 数。在有挡板的条件下,对于推进式叶轮NQR=0.5;
对 于 涡 轮 式 叶 轮 ( 六 叶 , 宽 径 比 为 1:5) ,
NQR=0.93D/d(用于Re104,D为反应器内径; d为搅
拌器桨径)。
连续釜式反应器在结构上通常与间歇釜式反应 器相同。其常见的进出料方式如下
①已知反应釜串联的个数n以及反应体积VR(也就 是停留时间τ),求终点转化率xAf ②已知终点转化率xAf,求串联的个数n(已知反应 体积,即停留时间τ) ③已知终点转化率xAf,求反应体积VR(已知串联 的个数n)
第五章 连续釜式反应器
5.1 连续釜式反应器的特点及应用 5.2 连续釜式反应器的设计 5.3连续釜式反应器的并联与串联 5.4釜式反应器的热量衡算与定态操作 5.5返混对复杂反应产品分配的影响
连续釜式反应器的特点
• 定义:连续釜式反应器是一种以釜式反应器实现连续生产的 操作方式。
• 与间歇釜式相比,具有生产效率高,劳动强度低,操作费用 小,产品质量稳定,易实现自控等优点。
FV0CA0=FVfCAf+ rAVR
液相反应时,可视为恒容,FV0=FVf;而且稳态 操作时,xA=xAf,CA=CAf,于是
VR
FV 0 (CA0 rA
-CA)
由于
xA
CA0 - CA CA0
所以
VR
=
FV 0CA0 xA rA
这就是等温恒容液相连续釜式反应器的设计方程。
在给定操作条件以及反应的动力学方程后,可由 简单的代数计算求得反应体积。
CA2 1+ k3 3
CAn-1 1 kn n
连续搅拌釜式反应器

3. 质量检测
本实验中采用电导方法测量反应物A的浓度变化。 对于乙酸乙酯皂化反应,参与导电的离子 有Na+、OH-和CH3COO-。Na+在反应前后浓 度不变,OH-的迁移率远大于CH3COO-的迁移率。随 着反应的进行,OH-不断减少,物 系的电导值随之不断下降。因此,物系的电导值的变化与CH3COOH的浓度变化成正 比,而由电导电极测得的电导率L与其检测仪输出的电压信号U也呈线性关系,则如 下关系式成立:
续搅拌釜式反应器液相反应的速 率常数测定 一、实验目的
本实验采用连续流动搅拌釜式反应器进 行液相反应动力学研究。实验用连续输入 的方法,在定常流动下,测定乙酸乙酯皂 化反应的反应速率和反应速率常数。
二、实验原理
1. 2.
3.
反应速率 反应速率常数 质量检测
1. 反应速率 连续流动搅拌釜式反应器的摩尔衡算基本方程:
FAO-FA-∫0V(-rA)dV=dnA/dt
对于定常流动下的全混流反应器,上式可简化为:
FAO-FA-(-rA)V=0→ (-rA)= FAO-FA /V
对于恒容过程而言,流入反应器的体积流率Vs,0等于流出反应器的体积流率Vs。 若反应物A的起始浓度为CA,0,反应器出口亦即反应器内的反应物A的浓度为 CA,则上式可改写为:(-rA)= (CA,0-CA)/(V/Vs,0)=(CA,0-CA)/τ
2. 标定浓度曲线的实验步骤
3.测定反应速率和反应速率常数的实验步骤
(1)停止加热和搅拌后,将反应器内的纯水放尽。启 动并调定计量泵,同时以等流率向器 内加入料液A和 B。待液面稳定后,启动搅拌器和加热器并控制转速和 温度恒定。当搅拌转速 在600r· min-1时,总体积流率 在2.7~16L· h-1(相当于计量泵显示10~60 r·min-1)范围 内,均可接近全混流。 (2)当操作状态达到稳定之后,按数据采集键,采集 与浓度CA相应的电压信号U。待屏幕 上 显示的曲线平直 之后,按终止采集键,取其平直段的平均值,即为与釜 内最终浓度CA相应 的U值。 (3)改变流量重复上述实验步骤,测得一组在一定温 度下,不同流量时的U值数据。
化学反应工程连续流动釜式反应器

补充知识点:空时与空速的概念:
空时:
Vr V0
反应体积 进料体积流量
(因次:时间)
表明 Vo , 处理能力
空速:
1 V0 FA0
Vr cA0Vr
因次 :时间-1
空速的意义:单位时间单位反应体积所处理的物料量。 空速越大,反应器的原料处理能力越大。
第九页,编辑于星期六:十八点 一分。
第十八页,编辑于星期六:十八点 一分。
2. 一级不可逆等容单一反应 对于一级不可逆反应,可以直接建立级数m和最终转
化率之间的关系,不必逐级计算。
第i级
VRi
V0 (CAi1 CAi ) rAi
式中 rAi kCAi
上式可化为
k i
(CAi1 CAi ) CAi
CAi 1
CAi1 1 k i
第十五页,编辑于星期六:十八点 一分。
在三釜串联操作时,前两釜都是在高于CAf的浓度下 进行,仅第三釜在CAf进行,反应速度比两釜串联时
又有所提高。可见,串联的釜数越多,反应物浓度提 高越多,反应速度越快,需要的反应时间或反应器体 积就越小。 将几个全混釜串联起来操作就构成了多釜串联反应器。
第十六页,编辑于星期六:十八点 一分。
设有4级串联全混流反应器,其浓度推动力如图所示。
ΔCA多=(CA1-CA*)1+(CA2-CA*)2+(CA3-CA*)3+(CA4-CA*)4 显然ΔCA平>ΔCA多>ΔCA全 当级数为∞,则ΔCA平=ΔCA多
CA0
CA0
CA1
CA2
CA1
CA3
CA4
CA2
CA3
CA4
CA*
第十三页,编辑于星期六:十八点 一分。
CSTR 反应器

CSTR 反应器:质量平衡表达式CSTR 反应器(连续搅拌釜反应器)是化学或生物化学工业中非常普遍的一类反应器。
反应器有一个入口和一个出口,并被完美地搅拌。
本页重点介绍将一般质量平衡方程应用于CSTR 反应器。
1、CSTR反应器连续搅拌釜反应器配备有反应物入口和反应器内容物出口,它们在反应器操作期间连续进行。
反应器装有搅拌器,假定它可以有效地搅拌反应介质。
一般的质量平衡方程可以用以下方式表示:入口= 出口+ 消耗+ 累积表达式的每个组成部分的单位是材料流量:例如mol/s。
在下面的应用中,我们考虑考虑的CSTR 反应器的情况是:•完美搅拌:反应器反应介质中任何一点的浓度相同•等温线2. CSTR反应器完全搅拌并处于稳定状态:物料平衡让我们假设反应物 A 和 B 被引入反应器。
反应A +B =C +D生成 C 和D。
入口处只有 A 和B,但在出口流中我们可以发现 A 和 B 未反应,而 C 和D。
与在反应发生时浓度始终变化的间歇式和半间歇式反应器相反,CSTR 反应器具有在稳态下运行的特性,这意味着在入口和出口之间找到平衡,可以防止积累(正或负)在反应器中。
稳态意味着:dnA/dt = dnB/dt = dnC/dt = dnD / dt = 0除了反应器处于稳定状态外,反应体积不会随时间变化,这意味着我们可以直接使用材料平衡方程中的体积V。
将反应器完全搅拌的事实也有助于表达反应物和产物的消耗/产生,因为它可以表示为反应速度与体积(r'V) 和浓度的乘积。
完全搅拌意味着:[A]reactor = [A]out[B]reactor = [B]out[C]reactor = [C]out[D]reactor = [D]out每个组分的质量平衡将如下(r'是消耗速度,r是形成速度):反应性AQ输入*[A]输入= Q输出*[A]输出 + r' A .V + 0反应BQ in *[B] in = Q out *[B] out + r' B .V + 0产品C0 = Q输出*[C]输出+ r C .V + 0产品D0 = Q输出*[D]输出+ r D .V + 03. CSTR反应器搅拌完美且处于稳定状态:反应速度反应速度系统可以由上述方程表示如下:r' A = (Q in .[A] in - Q out *[A] out )/Vr' B = (Q in .[B] in - Q out *[B] out )/Vr C =Q输出*[C]输出/Vr D = Q输出*[D]输出/V这些是稳态CSTR 的特征方程。
连续搅拌釜式反应器(CSTR)控制系统设计 连续

连续连续搅拌釜式反应器搅拌釜式反应器搅拌釜式反应器((CSTR )控制系统设计1. 前言连续搅拌釜式反应器(continuous stirred tank reactor ,简称为CSTR )是聚合化学反应中广泛使用的一种反应器,该对象是过程工业中典型的、高度非线性的化学反应系统。
在早期反应釜的自动控制中,将单元组合仪表组成位置式控制装置,但是化学反应过程一般都有很强的非线性和时滞性,采用这种简单控制很难达到理想的控制精度。
随着计算机技术和PLC 控制器的发展,越来越多的化学反应采用计算机控制系统,控制方法主要为数字PID 控制。
但PID 控制是一种基于对象有精确数学模型的线性过程,而CSTR 模型最主要的一个特征就是非线性,因此PID 控制在这一过程中的应用受到限制。
随着现代控制理论和智能控制的发展,更加先进有效的控制方法应用于CSTR 的控制,如广义预测控制,神经模糊逆模PID 复合控制,自抗扰控制,非线性最优控制,基于逆系统方法控制,基于补偿算子的模糊神经网络控制,CSTR 的非线性H ∞控制等。
但任何一种复杂的化工反应过程都不能用一种简单的控制方式达到理想的控制效果。
目前先进的反应釜智能控制技术就是将智能控制理论和传统的控制方法相结合,如钟国情、何应坚等于1998年对基于专家系统的CSTR 控制系统进行了研究[1],宫会丽、杨树勋等于2003年发表了关于PID 参数自适应控制的新方法[2],冯斌、须文波等于1999年阐述了利用遗传算法的寻优PID 参数的模型参考自适应控制方法等[3]。
但由于这些控制方法的算法比较复杂,在算法的工程实现、现场调试及通用型方面存在着局限性,因此研究一种相对简单实用的CSTR 控制方法,更易为工程技术人员所接受。
本文在对CSTR 过程及其数学模型进行详细分析的基础上,针对过程的滞后性,采用Smith 预估算法与PID 控制相结合的方法实现CSTR 过程的控制,该方法具有实用性强及控制方法简单等特点,基于西门子PCS7系统完成了CSTR 过程控制系统设计。
03 第三章 釜式反应器1

(3-6)
nA0 dX A Vr R A
(3-7)
(3-7)适用于多相,均相及等温,非等温的间歇 反应过程
义:
nA0 c A0 Vr
X Af 0
∴
t c A0
1 dX A R A
(3-8)
若进行a级单一不可逆反应
R A rA k c A
LOGO
化学反应工程
第三章 釜式反应器
1
LOGO
第三章—釜式反应器
连续搅拌釜式反应器
重点掌握: 等温间歇釜式反应器的计算(单一反应、平行与连串反应)。 连续釜式反应器的计算 。 空时和空速的概念及其在反应器设计计算中的应用。 连续釜式反应器的串联和并联。 釜式反应器中平行与连串反应选择性的分析,连接和加料方式 的选择。 连续釜式反应器的质量、热量衡算式的建立与应用。 深入理解: 变温间歇釜式反应器的计算。 广泛了解: 串联釜式反应器最佳体积的求取方法。 连续釜式反应器的多定态分析与计算。 产生多定态点的原因,着火点与熄火点的概念。
j 1
M
(3-2)
ij
关键组分i 在第j个独立均 相反应中的化学计量数
反应物: 产物:
Ri 0
Ri 0
I. 定态操作,累积速率dni/dt,则式(3-1)化为
连续釜式反应器的物料衡算式
Q0 ci 0 Qci Vr i j rj
j 1
M
i 1, 2,, K
(3.4)
dFR 令: dt 0
(3-15)
根据函数求极值方法,目标函数对t求导, (3-16)
dcR cR 得: dt t t0
(3-17)
(3-17)即为FR最大时必须满足的条件,此 时的t即为最优反应时间tm。
釜式反应器

11.2 化工CSTR系统动态特点分析釜式反应器是一种低高径比的圆筒形反应器,用于实现液相单相反应过程和液液、气液、液固、气液固等多相反应过程。
器内常设有搅拌(机械搅拌、气流搅拌等)装置。
在高径比较大时,可用多层搅拌桨叶。
在反应过程中物料需加热或冷却时,可在反应器壁处设置夹套,或在器内设置换热面,也可通过外循环进行换热。
釜式反应器按操作方式可分为:间歇釜式反应器(或称间歇釜)、连续釜式反应器(或称连续釜)、半连续釜式反应器。
本项目所研究的预报对象是连续釜式反应器。
连续搅拌釜式反应器(Continuous Stirred Tank Reactor,CSTR),操作方式为连续进料、连续反应、连续出料,为带有搅拌桨叶的槽式反应设备。
在稳态操作时,反应器同一部位的操作参数不随时间而变,有利于产品质量控制和过程自动控制。
与间歇反应器操作方式不同,没有装料、卸料、升温等不发生化学反应的辅助时间,因而生产能力较大,辅助劳动少。
适用于反应速度慢的液相反应,使用时可用单个反应槽(釜),也可把几个反应槽(釜)串联成一组。
CSTR是聚合化学反应中广泛使用的一种反应器,是过程工业中典型的、高度非线性的化学反应系统。
在化工生产的核心设备中占有相当重要的地位,在染料、医药试剂、食品及合成材料工业中,CSTR 得到了广泛的应用。
在CSTR中,反应原料以稳定的流速进入反应器,反应器的反应物料以同样稳定流速流出反应器。
由于强烈搅拌的作用,刚进入反应器的新鲜物料与已存留在反应器的物料在瞬间达到完全混合,使釜内物料的浓度和温度处处相等。
同样,在反应器出口处即将流出反应器的物料浓度也应该与釜内物料浓度一致,因此流出反应器的物料浓度与反应器内的的物料浓度相等。
连续搅拌釜式反应器中的反应速率即由釜内物料的温度和浓度决定。
CSTR系统模型如下图所示:图11-2 CSTR系统工作原理图由于CSTR系统大多进行的是高温、高压反应,原料、中间体和产品大多具有易燃、易爆等特性,稍有疏忽就很容易出现故障,发生事故。
反应器-8连续操作釜式反应器
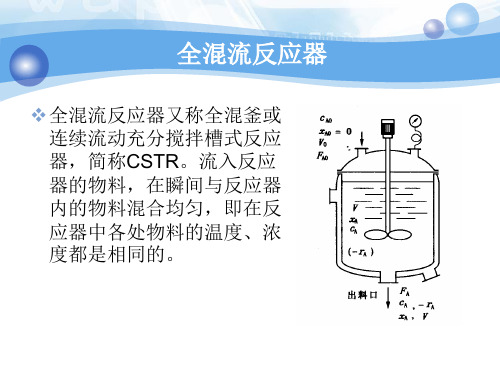
dxA
理想流动反应器的组合
❖ (1)平推流反应器的并联操作
❖ VR=VRl+VR2 ❖因为是并联操作,总物料体积流量等于各反应
器体积流量之和:
❖ V0=V01+V02 ❖ 由平推流反应器的设计方程
VR V0
cA0
xA 0
dxA rA
❖尽可能减少返混是保持高转化率的前提条件, 而只有当并联各支路之间的转化率相同时没有 返混。如果各支路之间的转化率不同,就会出 现不同转化率的物流相互混合,即不同停留时 间的物流的混合,就是返混。因此,
❖对于平推流反应器,在恒温下进行,其设计式
为:
n
❖对于全混流反应P 器kc,1An01在恒0x温A 1下1进AxA行xA , d其xA设计式
为:
❖ ❖
二式相除,当初m始 条kxc件AAn01和1反1应Ax温AxA度n相同时:
n
m
p
VR m VR p
xA
1
1
A xA xA
n
xA 0
1
1
A xA xA
FA0
VRi FA0
xAi
dxA
dx xAn
A
r xAi1
A
0 rA
❖(2)全混流反应器的串联操作 N个全混流反应 器串联操作在工业生产上经常遇到。其中各釜 均能满足全混流假设,且认为釜与釜之间符合 平推流假定,没有返混,也不发生反应。
❖ 对任意第i釜中关键组分A作物料衡算。
❖ 对恒容、定常态流动系统,V0不变,
推流反应器所需反应体积略大些,这是由于间
歇过程需辅助工作时间所造成的。而全混釜反
应器比平推流反应器、间歇反应器所需反应体
积大得多,这是由于全混釜的返混造成反应速
cstr聚乙烯工艺

cstr聚乙烯工艺
CSTR(Continuous Stirred Tank Reactor)是连续搅拌釜式反应器的简称,这种反应器在化工领域被广泛用于各种化学反应过程,包括聚乙烯的生产。
在聚乙烯工业中,CSTR工艺通常与淤浆法结合使用,尤其是在生产高密度聚乙烯(HDPE)时。
淤浆法是一种早期的聚乙烯生产工艺,其特点是将催化剂悬浮在液态烃溶剂(如己烷)中形成淤浆,然后将淤浆引入到CSTR反应器中进行聚合反应。
在反应器内,乙烯单体在催化剂的作用下形成聚乙烯颗粒。
由于反应器内物料处于连续流动和混合状态,因此可以实现连续生产,并且相对容易控制反应条件。
CSTR工艺的优点在于能够提供较好的温度和浓度控制,因为搅拌使得反应物在反应器内的分布较为均匀。
此外,由于反应器内部是一个开放系统,可以通过改变进料速度来调整反应速率,从而满足不同的产品需求。
然而,CSTR工艺也有一些局限性,比如可能会出现局部过热或过冷的情况,导致产品质量不均。
此外,由于需要使用大量的溶剂,所以存在较高的能耗和环保问题。
随着时间的推移,气相法聚乙烯生产工艺因其操作压力低、流程简单、不需要溶剂等优点逐渐取代了淤浆法/CSTR工艺成为主流。
尽管如此,CSTR工艺依然在某些特殊应用场合或者特定类型的聚乙烯产品生产中占有一席之地。
釜式反应器结构及原理
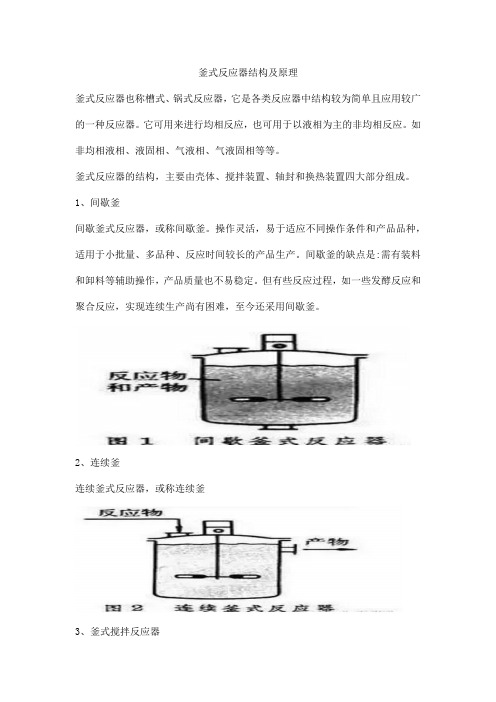
釜式反应器结构及原理
釜式反应器也称槽式、锅式反应器,它是各类反应器中结构较为简单且应用较广的一种反应器。
它可用来进行均相反应,也可用于以液相为主的非均相反应。
如非均相液相、液固相、气液相、气液固相等等。
釜式反应器的结构,主要由壳体、搅拌装置、轴封和换热装置四大部分组成。
1、间歇釜
间歇釜式反应器,或称间歇釜。
操作灵活,易于适应不同操作条件和产品品种,适用于小批量、多品种、反应时间较长的产品生产。
间歇釜的缺点是:需有装料和卸料等辅助操作,产品质量也不易稳定。
但有些反应过程,如一些发酵反应和聚合反应,实现连续生产尚有困难,至今还采用间歇釜。
2、连续釜
连续釜式反应器,或称连续釜
3、釜式搅拌反应器
釜式搅拌反应器有立式容器中心搅拌、偏心搅拌、倾斜搅拌,卧式容器搅拌等类型。
其中以立式容器中心搅拌反应器是最典型的一种。
性能特点:
釜式反应器具有适用的温度和压力范围宽、适应性强、操作弹性大、连续操作时温度浓度容易控制、产品质量均一等特点。
但用在较高转化率工艺要求时,需要较大容积。
通常在操作条件比较缓和的情况下操作,如常压、温度较低且低于物料沸点时,应用此类反应器最为普遍。
4、多级串联反应釜。
连续操作釜式反应器课件

02 03
技术创新
为适应新能源材料制备的需求,连续操作釜式反应器在结 构、材质和控制系统等方面进行了多项创新。例如,采用 新型陶瓷材料增强设备的耐腐蚀性,设计特殊结构的电极 以提高电化学反应效率等。
应用前景
随着新能源产业的快速发展,连续操作釜式反应器在新能 源材料制备领域的应用前景日益广阔。例如,可用于锂离 子电池正极材料的合成、燃料电池催化剂的制备以及太阳 能电池材料的生产等。
根据反应物料性质和反应阶段 ,调整搅拌速度,保证物料在
反应器内充分混合。
连续操作釜式反应器的性能优化
01
02
03
04
反应条件优化
通过实验和模拟手段,寻 找最佳的反应温度、压力 、物料配比等条件,提高 反应转化率和选择性。
设备结构优化
优化反应器内部结构,如 改进搅拌桨叶型、增加传 热面积等,提高传质传热 效率。
连续操作釜式反应 器课件
目录
• 连续操作釜式反应器概述 • 连续操作釜式反应器的工艺设计 • 连续操作釜式反应器的操作与优化 • 连续操作釜式反应器的故障诊断与预防 • 连续操作釜式反应器的安全与环境保护 • 连续操作釜式反应器实例分析
01
连续操作釜式反应器概述
连续操作釜式反应器定义和原理
定义
化学品使用
在连续操作釜式反应器的运行过程中,应严格按照化学品使用说明 添加化学品,避免因使用不当引发的危险。
废弃物处理与环境保护
01
废弃物分类
对连续操作釜式反应器产生的废弃物进行分类,区分可回收物、有害废
弃物等,为后续处理提供依据。
02
废弃物处理
有害废弃物应交由专业机构进行处置,确保废弃物得到妥善处理,防止
设置必要的安全附件,如压力表、安全阀、紧急切断阀等,确 保设备的安全运行。
搅拌式反应器

搅拌釜式反应器的双区模型化学反应器是化工生产的核心设备,也是化学反应工程研究的核心,它的操作情况对整个生产过程起着决定性的作用。
在连续操作的反应器内,物料的流动与混合状况和因此而产生的反应时间、反应物浓度以及温度等反应参数的分布状况反映了工业反应器的最根本特征。
实际反应器内流体的流动状况存在着非理想流动,改变了物料的流动情况,进而改变了物料的浓度分布,最终则是影响结果。
为了准确地掌握反应器的性能,必须充分考虑实际反应器内的非理想流动对反应器的影响,根据实际情况与理想流型偏离的程度,建立一个较接近实际的流动模型。
造成反应器内流体流动情况变化的主要原因是返混。
由于返混改变物料的流动情况,从而改变反应器内物料浓度的分布,并使物料在反应器内部形成停留时间分布(RTD), RTD是流体流动情况的宏观体现,通过流体的RTD曲线能定量地估算每个流体相的混合物性和混合程度,以及每个流体相在反应器内的滞流量.当反应器没有外来传质和传热影响,它的特性就取决于特征动力学性质和RTD 曲线的性质。
在反应过程中。
反应的特征动力学性质不会改变。
所以,使用RTD 可以合理而又精确地描述反应器流体流动情况及混合特性,从而预测反应器的性能。
所以RTD模型即可反映物料的流动模型。
如何分析非理想流动和流型对反应器的影响,建立实际反应器内流体的流动模型,前人已经进行了大量的工作。
在许多的文献中,关于非理想因素对反应器性能的影响报道很多。
下面来讨论下反应器内可能存在的非理想因素的影响。
非理想流动和流型对化学反应产率和选择性的影响。
这两方面的影响因素进行综合考虑,用双区模型来描述实际反应器内流体的流动模型。
1、流动模型釜式反应器内的非理想流动主要有死区和短路。
死区主要存在于反应器的两个顶盖、畸形拐角、挡板与设备的交界处以及压力计的尾部等。
由于死区区域的流体几乎停滞不动,所以死区的存在减少了反应的有效体积;而短路则是当反应器的高径比较小时容易产生。
连续搅拌釜式反应器详解

3.参考下列表格记录测定反应速率和反应速率常数的实验数据
实 验 序 号 1 2 3 4 5
反应温度T/℃
反应体积V/L 总体积流率Vs,0/L· min-1 反应物A的 出口浓 度 U/mV
(U-Uf)/mV
CA/mol· L-1
4.参考下列表格整理实验数据
实 验 组 号
反应温度T/K 空间时间/min 反应速率(-rA)/ mol· L-1· min-1 反应速率常数k/L· mol-1· min-1 (1) (2) (3) (4)
式中:τ=V/Vs,0,即为空间时间。对于恒容过程,进出口又无 返混时,则空间
时间也就是平均停留时间。因此,当V和Vs,0一定时,只要实验测得CA,0和CA, 即可直接测得在一定温度下的反应速率(-rA)。
2. 反应速率常数
CH3COOC2H5(A)+NaOH(B)→CH3COONa(C)+C2H5OH(D) 因为该反应为双分子反应,则反应速率方程为: (-rA)=kCACB 本实验中,反应物A和B采用相同的浓度和相同的流率,则上式可简为: (-rA)=kCA2 将上式线性化后,可得:lg(-rA)=2lgCA+lgk 当反应温度T和反应器有效容积V一定时,可利用改变流率的方法,测得 不同CA下的反 应速率(-rA)。由lg(-rA)对lgCA进行标绘,可得到一条 直线。由直线的截距lgk 求取k值。或用最小二乘法进行线性回归求得k 值。
2.
3.测定反应速率和反应速率常数的实验步骤
(1)停止加热和搅拌后,将反应器内的纯水放尽。启 动并调定计量泵,同时以等流率向器 内加入料液A和 B。待液面稳定后,启动搅拌器和加热器并控制转速和 温度恒定。当搅拌转速 在600r· min-1 时,总体积流率 在2.7~16L· h-1(相当于计量泵显示10~60 r·min-1)范围 (2)当操作状态达到稳定之后,按数据采集键,采集 与浓度CA相应的电压信号U。待屏幕 上 显示的曲线平直 之后,按终止采集键,取其平直段的平均值,即为与釜 内最终浓度CA相应 的U (3)改变流量重复上述实验步骤,测得一组在一定温 度下,不同流量时的U值数据。
理想反应器(连续釜)

3.7
反应器计算与操作的优化
优化的核心是化学因素和工程因素的最优结合。 化学因素包括反应类型及动力学特性
随串联釜数增多,操作的复杂程度增大, 附属设备费用增大。故串联釜数一般不大于 4。
3.4.2 多个串联连续操作釜式反应器 (N-CSTR)
二、nCSTR的基础设计式
CA0
CA1
CA2
V0
CA1 VR1
V0
CA
2
V0
CAi-1 VRi1
CAi-1
CAi
V0
CAi
CAm
V0
CAm V0
VR2
VRi
3.4
理想混合连续搅拌釜式反应器(CSTR)
CA
time
反应器内,物 料的浓度和温度处 处相等,且等于反 应器流出物料的浓 度和温度。
CA,in
CA, out
0
tresidence time
t
CA CA,O
position
CA, out
t
x
0
3.4
理想混合连续搅拌釜式反应器(CSTR)
优点:容易自动控制,操作简单,节 省人力。稳定性好,操作安全。 缺点:在低浓度下进行反应。
VRm
3.4.2 多个串联连续操作釜式反应器 (N-CSTR)
V0CAi 1 V0CAi (rAi )VRi
V0 (C Ai 1 C Ai ) VRi (rAi )
CAi-1
CAi CAi
V0C A0 ( xAi xAi 1 ) VRi (rAi )
VRi
VRi C Ai-1 - C Ai x Ai - x Ai-1 τ≡ = = C A0 i V0 (-rAi ) (-rAi )
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4. 实验结束工作
(1)先关闭加热和恒温系统,后关闭计量泵。 (2)关闭计算机,再将搅拌转速缓慢地调至零, 最后关掉电路总开关。 (3)打开底阀,将釜内的液体排尽,并用蒸馏水 将反应器和电导池冲洗干净。将电导电极 浸泡在 蒸馏水中,备用。
5. 实验注意事项
(1)实验中所用的溶液都必须新鲜配置,确保溶 液浓度准确。同时,配制溶液用水必须是 电导 率≤10-6S· cm-1的纯水。NaOH和CH3COO C2H5料
(2)在浓度标定实验中,每次向电导池装新的试 验液时,必须将电导池按要求冲洗干净。 (3)对于液相反应动力学实验,必须要保证浓度、 温度和流率保持恒定和测量准确。因此 ,要有 足够的稳定时间。
五、实验结果
1. 反应釜的体积:V= L mol· L-1 mol· L-1 NaOH料液浓度:C′B,0=
3. 质量检测
本实验中采用电导方法测量反应物A的浓度变化。 对于乙酸乙酯皂化反应,参与导电的离子 有Na+、OH-和CH3COO-。Na+在反应前后浓 度不变,OH-的迁移率远大于CH3COO-的迁移率。随 着反应的进行,OH-不断减少,物 系的电导值随之不断下降。因此,物系的电导值的变化与CH3COOH的浓度变化成正 比,而由电导电极测得的电导率L与其检测仪输出的电压信号U也呈线性关系,则如 下关系式成立:
式中:τ=V/Vs,0,即为空间时间。对于恒容过程,进出口又无 返混时,则空间
时间也就是平均停留时间。因此,当V和Vs,0一定时,只要实验测得CA,0和CA, 即可直接测得在一定温度下的反应速率(-rA)。
2. 反应速率常数
Cቤተ መጻሕፍቲ ባይዱ3COOC2H5(A)+NaOH(B)→CH3COONa(C)+C2H5OH(D) 因为该反应为双分子反应,则反应速率方程为: (-rA)=kCACB 本实验中,反应物A和B采用相同的浓度和相同的流率,则上式可简为: (-rA)=kCA2 将上式线性化后,可得:lg(-rA)=2lgCA+lgk 当反应温度T和反应器有效容积V一定时,可利用改变流率的方法,测得 不同CA下的反 应速率(-rA)。由lg(-rA)对lgCA进行标绘,可得到一条 直线。由直线的截距lgk 求取k值。或用最小二乘法进行线性回归求得k 值。
(3)启动并调整好控温仪、测速仪和计算机等电 子仪器,并调好软件的数据采集程序。
(1)向反应器中加入纯水;启动搅拌器并将转速调至600r· min-1; 启动加热和 恒温装 置,并设定所需反应温度值;待温度恒定后, 将装有0.01mol· L-1的NaOH的试液和铂 黑电极 的试管(电导池)插 入反应器,启动数据采集软件,测定该温度下,与溶液浓度相应的 电压 信号。待电压值稳定后,取曲线平直段的平均值,即为U0值。 (2)用上述类同的方法,将装有0.01 mol· L-1NaAc的电导池插入 反应器,测得与0. 01 mol· L-1 NaAc浓度相应的电压值Uf。安装电 导池时要注意,试管(电导池)内的电极距离管底10mm,液面高 出电极10mm。试管液 面低于反应器液面10mm以下为宜。为了使 试管内溶液的温度迅速均匀恒定,先可略为搅动一 下。每次向电导 池装试液时,都先要用电导水冲洗试管和电极三次,接着用被测液 再冲洗三 次。若要求在不同温度下进行实验,则可在设定温度下重 复上述实验步骤。一般可在25℃和35℃ 两种温度下进行实验。
CA=K(U-Uf)
式中:U——由电导电极测得在不同转化率下与釜内溶液组成相应的电压信号值; Uf——CH3COOC2H5全部转化为CH3COONa K—— 本实验采用等摩尔进料,乙酸乙酯水溶液和氢氧化钠水溶液浓度相同,且两者进 料的体积流率相同。若两者浓度均为0.02 mol·L-1 应为0 .01mol·L-1 ,则反应过程的起始浓度CA,0, 的氢氧化钠水 。 因此,应预先精确配置浓度为0.01 mol·L-1
续搅拌釜式反应器液相反应的速 率常数测定 一、实验目的
本实验采用连续流动搅拌釜式反应器进 行液相反应动力学研究。实验用连续输入 的方法,在定常流动下,测定乙酸乙酯皂 化反应的反应速率和反应速率常数。
二、实验原理
1. 2.
3.
反应速率 反应速率常数 质量检测
1. 反应速率 连续流动搅拌釜式反应器的摩尔衡算基本方程:
2.
3.测定反应速率和反应速率常数的实验步骤
(1)停止加热和搅拌后,将反应器内的纯水放尽。启 动并调定计量泵,同时以等流率向器 内加入料液A和 B。待液面稳定后,启动搅拌器和加热器并控制转速和 温度恒定。当搅拌转速 在600r· min-1 时,总体积流率 在2.7~16L· h-1(相当于计量泵显示10~60 r·min-1)范围 (2)当操作状态达到稳定之后,按数据采集键,采集 与浓度CA相应的电压信号U。待屏幕 上 显示的曲线平直 之后,按终止采集键,取其平直段的平均值,即为与釜 内最终浓度CA相应 的U (3)改变流量重复上述实验步骤,测得一组在一定温 度下,不同流量时的U值数据。
溶液和浓度为0.01mol·L-1 的CH3COONa水溶液。在预定的反应温度下,分别进行电
导测定,测得电压信号分别为U0和Uf ,由此可确定上式中的比例常数K值。
四、实验步骤
1. 实验前的准备 2. 3.测定反应速率和反应速率常数的实验步骤 4. 实验结束工作
1. (1)新鲜配置0.02 mol· L-1的NaOH和CH3COO C2H5水溶液,分别存放于料液 贮槽,并严加密封。 (2)新鲜配制0.01mol· L-1的NaOH和NaAc水溶
FAO-FA-∫0V(-rA)dV=dnA/dt
对于定常流动下的全混流反应器,上式可简化为:
FAO-FA-(-rA)V=0→ (-rA)= FAO-FA /V 对于恒容过程而言,流入反应器的体积流率Vs,0等于流出反应器的体积流率Vs。 若反应物A的起始浓度为CA,0,反应器出口亦即反应器内的反应物A的浓度为 CA,则上式可改写为:(-rA)= (CA,0-CA)/(V/Vs,0)=(CA,0-CA)/τ
