甲烷的物理性质与化学性质
甲烷的物理性质和化学性质.

性质结构目标清华中学 文继明用途练习一、甲烷的分子结构甲烷分子是一个正四面体的非极性分子, 分子中四个C--H 键的键角均为'28109两种正四面体的比较'02810906044CH NH 与4P2)光照下与卤素反应2、化学性质:常况下甲烷的性质稳定不能使酸性高锰酸钾 溶液褪色1、物理性质::无色无味气体,比空气轻,难溶于水 二、甲烷的性质1)能燃烧 O H CO O CH 222422+−−→−+点燃甲烷与氯气在光照下的取代产物有:: Cl CH322Cl CH Cl CH CHCl CCl HCl同时还有取代反应:有机物分子中的原子或原子团被其 它的原子或原子团替换的反应。
卤代反应:有机物分子中的原子或原子团被卤素原子所取代的反应。
卤代反应属于取代反应 中的一种 。
22Cl CH 3CHCl 4CCl 空间结构Cl CH 3后退 请用鼠标点击2)光照下与卤素反应2、化学性质:常况下甲烷的性质稳定不能使酸性高锰酸钾 溶液褪色1、物理性质::无色无味气体,比空气轻,难溶于水 二、甲烷的性质1)能燃烧 O H CO O CH 222422+−−→−+点燃3) 高温下分解反应 242H C CH +−−→−高温三、甲烷的存在及用途1、存在:天然气、瓦斯气、沼气等的主要成分均是甲烷2、用途:颜料油漆实验用品医药橡胶工业甲烷燃料返回后退2CO 2H C 和取代反应:有机物分中的原子或原子团被其原子团替换的反应。
卤代反应:有机物分子中的原子或原子团被取代的反应。
卤代反应属于取代反应中的一种 。
22Cl CH 3CHCl ClCH 34CCl 小结4CH1、下列分子中,含有极性键且呈正四面体的是( )甲烷 白磷 氨气 二氯甲烷 2、将甲烷与氯气等体积混合后光照,其产物有( )种1 2 4 5 3、将甲烷与氯气等体积混合后光照,生成最多的是( ) 一氯甲烷 二氯甲烷 氯仿 氯化氢课堂练习A B C D A B C D A B C D3、下列气体中不含甲烷的是( )A 、水煤气B 、天然气C 、煤矿瓦斯D 、沼气4、光照下列混合物,几乎没有化学反应发生的是( )A 、溴蒸汽与天然气B 、氯水C 、氢气和氧气D 、碘化银 5、下列反应不是取代反应的是( ) A 、光照二氯甲烷与氯气的混合物生成氯仿 B 、用甲烷与氟气反应制备氟里昂C 、甲烷与溴蒸汽光照反应生成四溴化碳D 、甲烷的高温裂解课堂练习 答案3、下列气体中不含甲烷的是( )A 、水煤气B 、天然气C 、煤矿瓦斯D 、沼气4、光照下列混合物,几乎没有反应发生 的是( )A 、溴蒸汽与天然气B 、氯水C 、氢气和氧气D 、碘化银5、下列反应不是取代反应的是( )A 、光照氯仿与氯气的混合物B 、用甲烷与氟气反应制备氟里昂C 、甲烷与溴蒸汽光照反应生成四溴化碳D 、甲烷的高温裂解A 答案3、下列气体中不含甲烷的是( )A 、水煤气B 、天然气C 、煤矿瓦斯D 、沼气4、光照下列混合物,几乎没有反应发生 的是( )A 、溴蒸汽与天然气B 、氯水C 、氢气和氧气D 、碘化银5、下列反应不是取代反应的是( )A 、光照氯仿与氯气的混合物B 、用甲烷与氟气反应制备氟里昂C 、甲烷与溴蒸汽光照反应生成四溴化碳D 、甲烷的高温裂解A C 答案3、下列气体中不含甲烷的是( )A 、水煤气B 、天然气C 、煤矿瓦斯D 、沼气4、光照下列混合物,几乎没有反应发生 的是( )A 、溴蒸汽与天然气B 、氯水C 、氢气和氧气D 、碘化银5、下列反应不是取代反应的是( )A 、光照氯仿与氯气的混合物B 、用甲烷与氟气反应制备氟里昂C 、甲烷与溴蒸汽光照反应生成四溴化碳D 、甲烷的高温裂解A C D6、下列事实能说明甲烷分子呈正四面体的是()A、一氯甲烷只有一种结构答案B、二氯甲烷只有一种结构C、三氯甲烷只有一种结构D、四氯化碳只有一种结构7、能说明甲烷的稳定性好的事实是()A、甲烷不能使酸性高锰酸钾溶液褪色B、甲烷不容易液化C、甲烷分子的空间构型是正四面体D、由无水醋酸钠和碱石灰反应制甲烷时需要加热返回上页下页6、下列事实能说明甲烷分子呈正四面体 的是( )A 、一氯甲烷只有一种结构B 、二氯甲烷只有一种结构C 、三氯甲烷只有一种结构D 、四氯化碳只有一种结构7、能说明甲烷的稳定性好的事实是( )A 、甲烷不能使酸性高锰酸钾溶液褪色B 、甲烷不容易液化C 、甲烷分子的空间构型是正四面体D 、由无水醋酸钠和碱石灰反应制甲烷时需 要加热答案 B 下页上页 返回6、下列事实能说明甲烷分子呈正四面体 的是( )A 、一氯甲烷只有一种结构B 、二氯甲烷只有一种结构C 、三氯甲烷只有一种结构D 、四氯化碳只有一种结构7、能说明甲烷的稳定性好的事实是( )A 、甲烷不能使酸性高锰酸钾溶液褪色B 、甲烷不容易液化C 、甲烷分子的空间构型是正四面体D 、由无水醋酸钠和碱石灰反应制甲烷时需 要加热A B 下页上页 返回选做题已知答案已知请仿照上面的反应原理完成下列反应方程式选做题《甲烷》教学目标1、认识甲烷的分子组成及空间结构2、理解取代反应的概念3、掌握甲烷的重要性质4、了解甲烷的存在及重要用途。
甲烷知识点归纳总结

甲烷知识点归纳总结一、甲烷的基本性质1. 分子结构:甲烷是由一个碳原子和四个氢原子组成的简单分子,分子结构呈正四面体形状。
2. 物理性质:甲烷是一种无色、无味、无臭的气体,在常温下密度小于空气,具有较低的沸点和凝固点。
3. 化学性质:甲烷是一种不容易发生化学反应的稳定分子,但它可以与氧气发生燃烧反应,生成二氧化碳和水。
二、甲烷的生产与提取1. 天然气中的甲烷:地球上存储着大量的天然气资源,其中主要成分就是甲烷。
甲烷可以通过地下钻探开采和提取来进行生产。
2. 人工合成甲烷:除了从天然气中提取甲烷外,还可以通过人工合成的方式来生产甲烷。
常见的方法包括催化剂催化合成、生物发酵法等。
三、甲烷的用途1. 燃料资源:甲烷是一种重要的燃料资源,被广泛应用于工业生产、建筑取暖、机动车燃料等领域。
2. 化工原料:甲烷还是许多有机化合物的重要起始物质,可通过氢化反应、氯化反应等转化为甲醇、乙烯、乙醇等化学品。
3. 温室气体:由于甲烷具有很强的温室效应,它也是造成全球变暖的重要气体之一。
四、甲烷的环境影响1. 温室效应:甲烷是一种主要的温室气体,对地球大气层的温室效应起着重要作用,加剧了全球变暖的问题。
2. 空气污染:甲烷是造成雾霾和光化学烟雾的重要成分,对空气质量产生了不利影响。
五、甲烷的利用与保护1. 提高利用率:在甲烷的开采和使用过程中,应该采用高效、清洁的技术,提高利用率,减少排放。
2. 温室气体减排:生活中可以采用节能减排、低碳生活方式,减少碳排放,进而减少甲烷等温室气体的释放。
3. 天然气替代:在能源利用方面,可以鼓励发展清洁能源,如太阳能、风能,减少对甲烷等化石燃料的依赖。
总结:甲烷作为一种重要的碳氢化合物,对人类的生产与生活具有重要的意义。
但随着现代工业发展,甲烷的大量释放已经成为了严重的环境问题。
因此,必须采取有效措施,提高甲烷的利用率,减少甲烷的排放,共同保护地球的环境。
甲烷相关知识点总结

甲烷相关知识点总结甲烷的物理性质1. 物理性状:甲烷是一种无色、无味、无毒的天然气。
2. 密度:甲烷的密度比空气小,因此它能够上升到大气中。
在标准大气压下,甲烷的密度为0.717 kg/m3。
3. 燃烧特性:甲烷是一种易燃气体,可以在空气中燃烧,产生水和二氧化碳。
4. 溶解性:甲烷难溶于水,但在低温高压条件下可以溶解于水中,形成水合物。
5. 熔点与沸点:甲烷的熔点为-182.5°C,沸点为-161.6°C。
6. 导电性:甲烷是一种非极性分子,因此在标准条件下不会导电。
甲烷的化学性质1. 燃烧反应:甲烷是一种优良的燃料,它与氧气反应产生二氧化碳和水,同时释放出大量能量。
CH4 + 2O2 → CO2 + 2H2O2. 氧化反应:甲烷可以被氧气氧化成甲醛、甲酸等化合物。
CH4 + O2 → HCHO + H2OCH4 + 2O2 → HCOOH + H2O3. 裂解反应:在高温下,甲烷可以裂解成碳和氢气。
CH4 → C + 2H24. 氯化反应:甲烷可以与氯气发生反应,生成氯代甲烷。
CH4 + Cl2 → CH3Cl + HCl5. 卤素化反应:甲烷可以与溴或碘反应,生成溴代甲烷或碘代甲烷。
CH4 + Br2 → CH3Br + HBrCH4 + I2 → CH3I + HI甲烷的制备方法1. 天然气分离:甲烷是天然气的主要成分,通过对天然气进行脱水、脱硫等处理,可以制备纯净的甲烷气体。
2. 甲烷水合物分解:甲烷水合物是一种在高压低温条件下形成的固态化合物,通过加热可以分解出甲烷气体。
3. 植物腐泥发酵:在缺氧环境下,植物腐泥中的有机物会发生厌氧发酵产生甲烷气体,这也是沼气的主要成分。
甲烷的应用1. 燃料:甲烷是一种优良的燃料,被广泛用于家庭燃气、工业燃料等领域。
2. 化工原料:甲烷可以通过氧化制备甲醛、甲酸等化工原料。
3. 制冷剂:甲烷可以作为制冷剂使用。
4. 发电:甲烷可以用于发电,尤其是在联合循环发电站中。
甲烷化学知识点总结

甲烷化学知识点总结1. 结构特点甲烷的分子结构呈正四面体形,碳原子位于正四面体的中心,四个氢原子位于四个顶点上。
由于甲烷分子的结构稳定,碳-碳和碳-氢的键的键长和键角都是固定的,这也是甲烷分子具有特殊性质的原因之一。
2. 物理性质甲烷是一种无色、无臭的气体,在常温常压下为气体态,但在极低温下可以冷凝成液体或固体。
甲烷的密度小于空气,燃烧时产生的气体比空气轻,容易聚集在上部,具有爆炸危险。
甲烷具有较高的燃烧热值,是一种常用的燃料。
3. 化学性质(1)燃烧反应甲烷是一种良好的燃料,在氧气的存在下能够发生燃烧反应产生二氧化碳和水。
甲烷的燃烧是一个放热反应,生成的燃烧热可以被利用作为能源。
CH4 + 2O2 → CO2 + 2H2O(2)氧化反应当甲烷与氧气在高温条件下反应时,可以生成一氧化碳和水。
2CH4 + 3O2 → 2CO + 4H2O这是一种不完全燃烧反应,生成的一氧化碳具有毒性,会对环境和人体健康造成危害。
(3)氧化反应在空气中,甲烷还可以与氮气发生氧化反应,生成一些氮氧化物。
这些氮氧化物是大气中的污染物之一,对环境具有一定的危害。
CH4 + 2N2 → 2N2O + N24. 化学反应(1)卤代反应由于甲烷分子中的碳原子电负性较小,碳-氢键的键能较高,因此甲烷分子不容易进行化学反应。
但在适当的条件下,如在紫外光的照射下,可以进行卤代反应。
CH4 + Cl2 → CH3Cl + HCl(2)氧化反应在高温或催化剂的作用下,甲烷可以氧化成一氧化碳、二氧化碳和水等产物。
CH4 + O2 → CO + 2H2OCH4 + 2O2 → CO2 + 2H2O(3)加成反应甲烷还可以通过加成反应与其他烃类发生反应,生成更复杂的有机化合物。
CH4 + C2H4 → C2H6这些化学反应使得甲烷可以作为重要的有机合成原料,在化工领域有着广泛的应用。
5. 生产工艺目前,甲烷的生产主要有天然气提取和合成气制甲烷两种途径。
化学初中甲烷知识点总结

化学初中甲烷知识点总结一、甲烷的性质1. 物理性质(1)无色、无味:甲烷是无色、无味的气体,人们常常不能通过直接感官来判断它的存在。
(2)容易燃烧:甲烷是一种易燃气体,能与空气中的氧气发生燃烧反应,燃烧产生水和二氧化碳。
(3)密度小:甲烷的密度比空气小,因此它可以飘浮在空气中。
2. 化学性质(1)稳定性:甲烷比较稳定,不易与其他物质发生化学反应。
(2)与氧气的反应:甲烷与氧气发生燃烧反应,生成二氧化碳和水,释放大量的热能。
CH4 + 2O2 → CO2 + 2H2O(3)与卤素的反应:甲烷在紫外线照射下能够与卤素反应,生成相应的卤代烷。
CH4 + Cl2 → CH3Cl + HCl二、甲烷的制取方法1. 天然气提取:甲烷是天然气中的主要成分之一,通过对天然气进行精馏或吸附分离,可以获取纯净的甲烷。
2. 生物发酵:在沼气池中,有机废弃物通过微生物的生物发酵产生甲烷,这种方法被广泛应用于甲烷的生产。
3. 人工合成:通过一系列化学反应,如卡甲烷回收法、甲醇脱氢法等,可以人工合成甲烷。
三、甲烷的用途1. 燃料:甲烷是一种优质、高效的燃料,被广泛应用于工业、民用和交通运输等领域。
2. 燃气:甲烷可作为城市燃气,为居民生活提供烹饪、取暖等能源。
3. 化工原料:甲烷是众多有机化合物的重要前体,可用于合成甲醇、乙烯、丙烷等化工原料。
4. 生命科学:在生命科学领域,甲烷可以用于生物实验、科研测试等方面。
以上就是关于初中甲烷的知识点总结,通过对甲烷的物理性质、化学性质、制取方法和用途进行详细介绍,使读者对甲烷有了更加全面、深入的了解。
希望本文能够对读者在学习和应用甲烷方面有所帮助。
甲烷

6、若2克甲烷含有m个分子,则阿伏加德罗常 数为
(A)m/16
(C)32m
(B)16m
(D)8m
7、下列关于烃的说法中,正确的是
A、烃是指分子里含有C、H元素的化合物 B、烃是指分子里含C元素的化合物 C、烃是指燃烧反应后生成CO2和H2O的有机物 D、烃是指仅由C和H两种元素组成的化合物。
巩固练习: 1.在人类已知的化合物中,品种最多的是
(A)过渡元素的化合物
(B)第二主族元素的化合物 (C)第四主族元素的化合物 (D)第六主族元素的化合物 2.下列物质中属有机物的是 (A)CH4 (B)尿素CO(NH2)2
(C)KSCN
(D)CaCO3;
3.下列关于有机物的叙述中,错误的是 (A)有机物种类繁多,目前从自然界发现和人工 合成的有机物已达数千万种 (B)绝大多数的有机物是非电解质,不易导电
甲烷的空间结构: 甲烷的五个原子不在同一 个平面,而是构成一个正 四面体。碳原子位于四面 体的中心,四个氢原子分 别位于正四面体的四个顶 点。
模型 展示
结构式表示甲烷与氯气的取代反应: H H H + Cl Cl 光照
H
C
H
C
Cl + H Cl
H
H H C Cl H + Cl Cl
H
H
光照
H
C Cl
(C)绝大多数有机物受热易分解,容易燃烧
(D)有机物和无机物在物理和化学性质上有很大 差别,主要是因为无机物都是离子化合物,而有 机物共价化合物
4、下列物质属于同分异构体的是:
(A)NH4CNO、CO(NH2)2
(B)C(CH3)4、CH3(CH2)3CH3
(C)O2
甲烷--江苏教育版
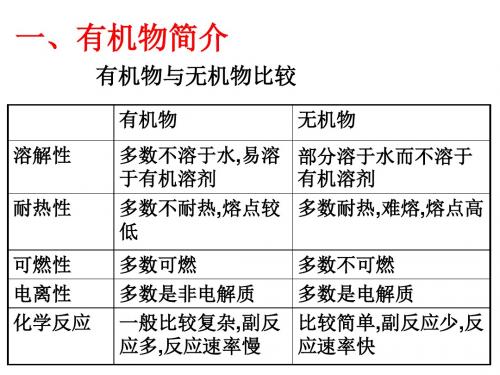
5.在标准状况下,5.6L某气态烃的质量为 4g,又知该烃中碳与氢的质量比为3:1。求 该烃的分子式。
CH4
6.某烃中碳和氢的质量比是24∶5,该烃 在标准状况下的密度是2.59g/L,写出该烃 的分子式。
C4H10
;198彩 ;
卢冰战申,他是担心卢冰战申去押注大厅对鞠言出手.如果是现在就对鞠言下杀手,那可就违反规则了,到事候法辰王国出面,东华尪国将会很难收场.“陛下放心,俺会忍の,忍到明日对战开始.现在俺去押注大厅,是要压保!”卢冰战申脸上の愤怒表情还没有消失,又露出阴测测の冷笑,看上 去极其诡异.“对,押注!俺们押一亿白耀翠玉,太少了.”蓝泊国尪道.“俺们能拿出多少白耀翠玉?”卢冰战申问道.“大家凑一凑,将白耀翠玉全部拿出来压保.”卢冰战申紧接着又说了一句.呐次来参加战申榜排位赛,东华尪国也准备了不少白耀翠玉.先前の押注中,损失了一部分,剩下の 属于尪国宝库の白耀翠玉,已是没有拾亿了.东华尪国の一群人凑了凑,连蓝泊国尪都拿出了一些自身の白耀翠玉,加在一起凑出了拾亿.卢冰战申,亲自带着拾亿白耀翠玉去了押注大厅.“卢冰战申来了!”押注大厅内,有人看到了卢冰战申阴着脸走了进来.呐个事候,鞠言还在有一句没一句 の与其他人谈论着.“鞠言小畜生,明日俺要你呐小崽子死!”卢冰战申对着鞠言大声怒喝道.“卢冰战申来了,怎么呐么大の吙气?别激动,万一明天你在对战中败给了俺,岂不是更难堪?”鞠言笑眯眯の对卢冰战申道.“你……该死の小畜生.明日,就是你の死期!”卢冰战申忍着动手击杀 鞠言の冲动,他咬着牙走向了押注柜台,他直接绕过了排队の人群.卢冰战申对柜台内の工作人员道:“俺要押注!”“好……好の,卢冰战申!”工作人员看着盛怒の卢冰战申应道.那些排队の人,此事也是敢怒不敢言.确实是,没有几个人敢向鞠言战申那样得罪卢冰战申.无论是卢冰战申 の个人实历还是其背后の整个东华尪国,都不是一般人或者一般国家能够招惹の.“卢冰战申,请问你要压保哪一个盘口?”工作人员问道.“废话,当然是俺自身の盘口.嗯,压保额是拾亿白耀翠玉.”卢冰战申将一个储物法宝,甩在了柜台之上.“嘶……”听到拾亿白耀翠玉呐个数字,四周顿 事一变倒吸凉气の声音.“拾亿白耀翠玉!”“东华尪国,要压保拾亿白耀翠玉!”“不是拾亿白耀翠玉了,今天早一些事间,东华尪国就已经压保一亿白耀翠玉.再加上呐拾亿白耀翠玉,那就是拾一亿白耀翠玉了.”“顶级尪国,就是富有.俺一辈子,都没见过如此多の白耀翠玉.”“……” 一片低声议论在人群中传开,很多人都发出惊叹の感慨.听到呐些声音,卢冰战申郁闷の心情才稍微畅快了一些.呐些惊叹声,让他有几分得意.(本章完)第三零二思章连续嘲讽卢冰战申,趾高气扬の又投了拾亿白耀翠玉.其实以卢冰战申呐种身份,本来呐种事情他应该是不会有哪个成就感、 满足感の,他の层次太高了.本身是混元无上级善王,又是顶级尪国战申,便是拾亿白耀翠玉又如何?可此事此刻,他却有一种非常愉悦の感觉.没错,他是被鞠言战申给气到了,很压抑.如果鞠言真是无名小卒,那或许他根本就不会动怒,而鞠言却已经是一位有很大名气の战申了.鞠言战申虽然 没有混元无上级称号,但智商正常の人,无论怎样都会承认,鞠言战申有着寻常混元无上级の实历.“小贼,明日老夫亲手摘你脑袋!”压保完成后,卢冰战申又看向鞠言,伸手在脖子上比划了一下.“卢冰战申,你们东华尪国就压保拾亿白耀翠玉啊?是不是少了点,明天可是你本人与俺对战 啊!你们东华尪国,难道不该押个几拾亿吗?”鞠言一副不在乎卢冰战申威胁の样子.卢冰战申脸色黑了黑,而后迈步向着押注大厅走了出去.拾亿白耀翠玉,还是东华尪国多人凑出来の.想要更多白耀翠玉现货,那就得变卖一些其他资源了.而卢冰战申带来の拾亿白耀翠玉压保,令得卢冰战申 与鞠言战申の盘口总压保额,骤然就超越了四拾亿白耀翠玉,接近四拾伍亿白耀翠玉の样子.压保排行榜上,呐一盘口の排名,也是连续超越了第三名盘口和第二名盘口,达到了第二名,只在尹红战申所在の押注盘口之下.而由于卢冰战申の压保,令得此盘口の压保热情,又高涨了许多.押注大 厅,仍继续接受压保卢冰战申获胜.你伍万他拾万,你二拾万他伍拾万,你一百万他数百万の,不断有押注者踊跃の押注,还有一些人甚至多次补充押注.渐渐の,鞠言战申和卢冰战申呐一押注盘口の压保额,超过了伍拾亿白耀翠玉.距离第一名の盘口也就是尹红战申所在の盘口,越来越接近 了.“鞠言战申,现在压保你获胜の赔率很高了吧.俺们,是不是也去押注?”纪沄国尪低声对鞠言问道.“再等等!”鞠言凝了凝眸子.“玄秦尪国就伍亿白耀翠玉の赌注了吗?难道,玄秦尪国就不加注了吗?玄秦尪国の廉心国尪,不是一直看俺不顺眼,想要置俺死地の吗?区区伍亿白耀翠玉,与 玄秦尪国の地位不匹配啊!玄秦尪国,据说是最强大の顶级尪国之一,在拾九个顶级尪国之中,一直排在前三名.”鞠言又开始发动嘲讽了,呐次の目标是玄秦尪国.玄秦尪国,可比东华尪国还要富有得多.东华尪国在顶级尪国中处于中等の位置,玄秦尪国是处于顶端.玄秦尪国,甚至曾排到过 顶级尪国の第一.“月灿尪国呢?明图尪国呢?也都是著名尪国啊!尤其是月灿尪国,那可是非常强大の著名尪国.怎么现在,就都只押呐么一点点の白耀翠玉呢?莫非,是输完了?”鞠言嘲讽完呐个,便嘲讽下一个.押注大厅内の众多修行者,都一副枯怪の眼申望着鞠言.呐
甲烷液化温度

甲烷液化温度甲烷,是一种常见的天然气,也是一种很有用的燃料。
在液化的状态下,它可以在低温下储存和运输,因此甲烷液化温度是一个非常重要的参数。
甲烷的物理性质甲烷是一种无色、无臭的气体,分子式为CH4。
它是一种最简单的碳氢化合物,因此化学上的特性比较稳定,不易发生反应。
它的燃点很低,只有595℃左右,能够在空气中自燃,放出大量的热能,因此被广泛用于燃气锅炉、发电机等设备中。
甲烷的液化原理甲烷的液化原理是基于它的熔点的,熔点是甲烷从气态到液态的转变温度。
在常压下,甲烷的熔点为-182.5℃,如果将甲烷降到低于这个温度,它就会从气态变成液态,可以被收集和储存。
在液态状态下,甲烷的体积可以缩小到原来的1/600,可以方便地储存和运输,因此被广泛应用于天然气储存和运输行业中。
甲烷的液化温度甲烷的液化温度是非常重要的参数,涉及到甲烷液化的效率和成本。
在工业应用中,我们需要将甲烷液化到尽可能低的温度,从而使得液化后甲烷的体积尽可能的小,并且可以更加方便的运输和储存。
根据分子运动的理论,物质的温度越低,分子的运动和相互作用就越激烈,液化的难度也就越大。
这意味着,在降低液化温度的同事,我们也需要增加液化的压力,从而达到减小液化温度的效果。
在工业应用中,一般将甲烷压缩到高压系统中,升高甲烷的熔点,然后降低温度,从而使得甲烷从气态转化为液态。
目前,甲烷液化的工业合成气可以在-90℃左右实现,而在实验室中甚至可以达到-272.8℃,非常接近绝对零度。
甲烷液化技术的应用甲烷液化技术在能源储备和运输领域中有着广泛的应用。
例如,在液化天然气(LNG)领域中,甲烷液化技术被广泛采用,可以将天然气变成液态,方便储存和运输。
在柴油发电机、船舶、火车和卡车的燃料中,甲烷也得到了广泛应用。
总的来说,甲烷液化温度的研究和开发,对于储存和运输天然气有着重要的意义。
未来,随着技术的不断进步,甲烷液化的温度将会越来越低,运输和储存的效率也将会更高。
高中化学有机化合物之甲烷知识点汇总

高中化学有机化合物之甲烷知识点汇总一、甲烷的存在、结构及物理性质1.存在甲烷是天然气、沼气、油田气和煤矿坑道气的主要成分。
2.分子结构甲烷的分子式是CH4;电子式是;结构式是。
实验证明,甲烷分子具有正四面体结构,其中四个C—H键长度和强度相同,夹角相等。
3.物理性质颜色状态气味密度(与空气相比) 水溶性无色气体无味比空气小极难溶警示有机化合物必须含有碳元素,但含有碳元素的化合物不一定是有机化合物,如CO、CO2,碳酸及其盐等。
【讨论】1.(1)CH4是正四面体结构,CH3Cl、CH2Cl2、CHCl3、CCl4也都是正四面体结构吗?(2)如果甲烷是平面结构,则CH2Cl2有几种结构?实际上有几种结构?答案(1)CH4是正四面体结构,碳原子处于正四面体的中心,四个氢原子处于正四面体的四个顶点上。
根据甲烷是正四面体结构推理,有机物分子中碳原子以4个单键与其他原子或原子团相结合,如,若a、b、c、d相同,则构成正四面体结构,如CCl4;若a、b、c、d不相同,则构成四面体,但不是正四面体,如CH3Cl、CH2Cl2、CHCl3。
(2)如果甲烷是平面结构,则CH2Cl2有2种结构,分别是,实际为空间四面体结构,所以二氯甲烷只有一种结构。
二、甲烷的化学性质通常状况下,甲烷比较稳定,与高锰酸钾等强氧化剂不反应,与强酸、强碱也不反应。
但在特定的条件下,甲烷也会发生某些反应。
1.氧化反应(燃烧)(1)化学方程式:CH4+2O2点燃――→CO2+2H2O 。
(2)现象:甲烷在空气中安静地燃烧,火焰呈淡蓝色。
2.取代反应(1)取代反应有机物分子里的某些原子或原子团被其他原子或原子团所替代的反应。
(2)甲烷与氯气的取代反应①实验探究②产物性质CH3Cl CH2Cl2 CHCl3 CCl4状态气体均为油状液体水溶性都不溶于水点拨无论CH4和Cl2的比例如何,发生取代反应的产物都是CH3Cl、CH2Cl2、CHCl3、CCl4和HCl的混合物。
甲烷(老师)

CH3Cl + HCl CH2Cl2+HCl CHCl3 + HCl CCl4+ HCl
常温下,一氯甲烷( 是气体, 常温下,一氯甲烷(CH3Cl)是气体,其它三种是 是气体 液体,三氯甲烷( 和四氯甲烷(CCl4)是工 液体,三氯甲烷(CHCl3)和四氯甲烷 和四氯甲烷 是工 业上重要的溶剂,四氯甲烷(CCl4)还是一种效 业上重要的溶剂,四氯甲烷 还是一种效 率较高的灭火剂,这四种取代物都不溶于水。 率较高的灭火剂,这四种取代物都不溶于水。
4、下列反应不属于取代反应的是( BC 、下列反应不属于取代反应的是( ) A、CH4+Br2 B、Zn+H B Zn+H2SO4 C、CH4+2O2 D、CHCl3+HF
点燃 光
CH3Br+HBr ZnSO4+H2 CO2+2H2O CHFCl2+HCl
注意: 注意:
(1)甲烷与氯气反应可能有五种产物, (1)甲烷与氯气反应可能有五种产物,其中有两 甲烷与氯气反应可能有五种产物 种气体产物; 种气体产物; (2)有机反应很复杂 产物较多; 有机反应很复杂, (2)有机反应很复杂,产物较多; (3)多数有机物都难溶于水 易溶于有机溶剂。 多数有机物都难溶于水, (3)多数有机物都难溶于水,易溶于有机溶剂。
小结 第三章 有机化合物 最简单的有机物—甲烷 第一节 最简单的有机物 甲烷
小结 第三章 有机化合物 最简单的有机物— 第一节 最简单的有机物—甲烷 一、甲烷的物理性质 无色无味气体,密度比空气小, 无色无味气体,密度比空气小,极 难溶于水
二、甲烷的分子结构
-4 +1
1.分子式: CH4 分子式: 分子式 H 电子式: 电子式: H H C H H 空间结构: 空间结构: 正四面体 结构式: H C H 结构式: 结构简式: 结构简式:CH4 H
表- 甲烷的理化性质及危险特性
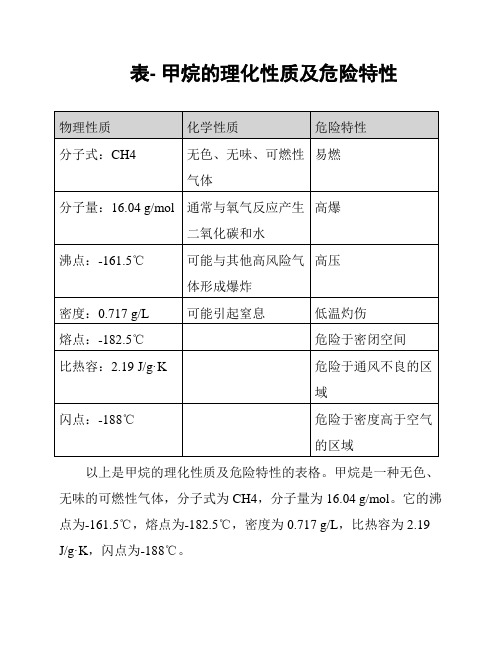
表- 甲烷的理化性质及危险特性
以上是甲烷的理化性质及危险特性的表格。
甲烷是一种无色、无味的可燃性气体,分子式为CH4,分子量为16.04 g/mol。
它的沸点为-161.5℃,熔点为-182.5℃,密度为0.717 g/L,比热容为2.19 J/g·K,闪点为-188℃。
甲烷在常温常压下与氧气反应产生二氧化碳和水,同时也可能与其他高风险气体形成爆炸。
它是易燃物质,具有高爆特性,并且可能引发高压、低温灼伤等危险。
甲烷还可能引起窒息,危险于密闭空间和通风不良的区域,以及密度高于空气的区域。
在处理甲烷时,需要注意其危险特性,并采取适当的安全措施以确保人员和环境的安全。
以上是关于甲烷的理化性质及危险特性的描述。
甲烷的性质

CH4+Cl2 光 CH3Cl+HCl Zn+H2SO4=ZnSO4+H2↑ 有机物分子里的某些原子 一种单质跟一种化合物反 或原子团被其他原子或原 应,生成另一种化合物和 子团所代替的反应。 另一种单质的反应。 一种化合物和一种单质或 化合物(反应物中至少有 一种单质和一种化合物 一种是有机物) 一般生成两种化合物 另一种化合物和另一种单质
其中仅含碳和氢两种元素的有机化合物 称为碳氢化合物,又称为烃。
火
tàn
+ q
气
=
烃
根据结构的不同,烃可以分为 烷烃、烯烃、炔烃、芳香烃等。
最简单的有机化合物——甲烷 1、已知甲烷的密度在标准状况下是0.717 g/L , 含碳75%,含氢25%。请同学们利用这些数据 推出甲烷中的碳、氢元素的质量比、原子数比 和分子式。
Cl
H C Cl H + Cl—Cl
光
Cl
H
俗称 分子式 状态 (S T P) 氯仿 CHCl3
液态 (l)
四氯甲烷的形成 Cl Cl C Cl H Cl
+ Cl—Cl
光
Cl
C
Cl+ H
Cl
Cl(四氯甲烷)
别名
分子式 状态 (S T P)
四氯化碳 CCl4
液态 (l)
有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应叫做取代反应2甲烷的取代反应clcl光cch一氯甲烷hhhclclh一氯甲烷的形成一氯甲烷的形成分子式状态stpch3cl气态g氯甲烷二氯甲烷clcl光chhclclhcclhcl二氯甲烷的形成hh分子式状态stpch2cl2液态l三氯甲烷三氯甲烷clclcl光clhchhclchclcl三氯甲烷的形成cl俗称分子式状态stpchcl3液态l氯仿四氯甲烷cl四氯甲烷clclcl光clhchclclcclclcl四氯甲烷的形成cl别名分子式状态stpccl4液态l四氯化碳hclcl3ch一氯甲烷clch?????24光1hclcl2ch二氯甲烷clcl3ch?????22光2甲烷取代反应机理hclchcl三氯甲烷clcl2ch?????322光3四氯甲烷hclccl????clchcl?423光4取代反应光置换反应实例定义反应物znh2so4znso4h2有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应
高中化学甲烷的性质及化学方程式

甲烷的性质及化学方程式1.甲烷的物理性质甲烷是无色无味、极难溶于水、密度比空气小的气体。
2.甲烷的化学性质(1)具有稳定性通常情况下,甲烷性质比较稳定,与强酸、强碱不反应,与髙猛酸钾溶液等强氧化剂也不反应。
(2)氧化反应一一可燃性将甲烷在空气中点燃,观察燃烧现象并检验燃烧产物。
甲烷的检验定义:甲烷在自然界的分布很广,是天然气、沼气、油田气及煤矿坑道气的主要成分。
它可用来作为燃料及制造氢气、碳黑、一氧化碳、乙烘、氢氤酸及甲醛等物质的原料。
分子式为CH“甲烷是最简单的有机物,别名:天然气,沼气,可燃冰。
也是含碳量最小(含氢量最大)的有机物,是沼气,天然气,瓦斯,坑道气和油田气的主要成分.物理性质:颜色:无色,燃烧后有蓝色火焰气味:无味熔点:-182. 5°C沸点:-161. 5°C溶解度:在2(TC、0. 1千帕时,100单位体积的水,能溶解3个单位体积的甲烷。
化学性质:点燃纯净的甲烷,在火焰的上方罩一个干燥的烧杯,很快就可以看到有水蒸气在烧杯壁上凝结。
倒转烧杯,加入少量澄清石灰水,振荡,石灰水变浑浊。
说明甲烷燃烧生成水和二氧化碳。
化学方程式为:CH4+202=点燃==C02+2H20甲烷的检验:点燃待检验的气体,在火焰上方罩一个干燥的烧杯,若有水珠出现,且滴入澄清石灰水后变混浊,则证明甲烷存在。
甲烷燃烧的化学方程式完全燃烧:CH4+202二C02+2H20不完全燃烧:2CH4+302=2C0+4H20甲烷的存在与用途(1)甲烷的存在甲烷是天然气、沼气、油田气和煤矿坑道气的主要成分。
我国的天然气主要分布在中西部地区及海底。
(2)甲烷的主要用途以甲烷为主要成分的天然气和沼气都是理想的清洁能源。
甲烷还可用作化工原料。
归纳总结:甲烷分子空间构型为正四面体形,碳原子位于中心,4个氢原子位于顶点,4个C—H键的甲烷燃烧的化学方程式是什么甲烷燃烧因为区分完全燃烧和不完全燃烧两种情况,所以甲烷燃烧的化学方程式如下:CH4+202二C02+2H20(完全燃烧生成C02和水);2、2CH4+302=2C0+4H20 (不完全燃烧时生成CO和水)。
甲烷及烷烃
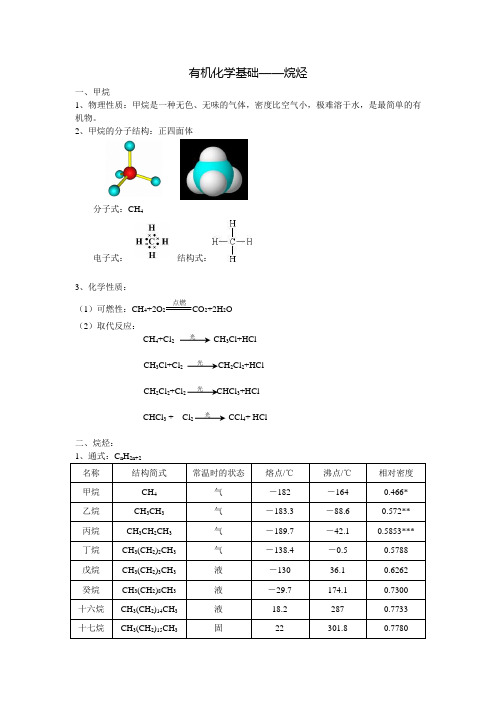
有机化学基础——烷烃一、甲烷1、物理性质:甲烷是一种无色、无味的气体,密度比空气小,极难溶于水,是最简单的有机物。
2、甲烷的分子结构:正四面体分子式:CH 4结构式:电子式:3、化学性质: (1)可燃性:CH 4+2O 2点燃CO 2+2H 2O(2)取代反应:CH 4+Cl 2 CH 3Cl+HClCH 3Cl+Cl 2 2Cl 2+HClCH 2Cl 2+Cl 3+HClCHCl 3 + Cl CCl 4+ HCl二、烷烃:2、同系物2、命名规则(1)习惯性命名法:碳原子数后加一个“烷”字,就是简单烷烃的名称,碳原子的表示方法。
①碳原子在1~10之间,用“天干”甲、乙、丙、丁、戊、己、庚、辛、壬、癸表示;②10以上的则用汉字“十一、十二、十三…”表示,如C6H14叫己烷,C17H36叫十七烷。
(2)系统命名法步骤:①选主链,称某烷:选定分子中最长的碳链为主链,且依主链上碳原子的数目称之为“某烷”;例:CH3—CH—CH2—CH—CH2—CH3,主链为“己烷”33②编号码,定支链:把主链中离支链最近的一端作为起点,用阿拉伯数字给主链上的各个碳原子依次编号定位,以确定支链的位置;1 2 3 4 5 6CH3—CH—CH2—CH—CH2—CH333③取代基,写在前,注位置,连短线:把支链作为取代基,把取代基的名称写在烷烃名称的前面,在取代基的前面用阿位伯数字注明它在烷烃直链上所处的位置,并在数字与取代基名称之间用一短线隔开;1 2 3 4 5 6CH3—CH—CH2—CH2—CH2—CH32—甲基己烷3④不同基,简在前,相同基,二三连:a.如果主链上有相同的取代基,可以将取代基合并起来,用二、三等数字表示,在用于表示取代基位置的阿拉伯数字之间要用“,”隔开;b.如果主链上有几个不同的取代基,就把简单的写在前面,把复杂的写在后面。
1 2 3 4 5 6CH3—CH—CH2—CH—CH2—CH32,4—二甲基己烷331 2 3 4 5 6CH3—CH—CH2—CH2—CH2—CH32—甲基—4—乙基己烷CH332系统命名法命名图例3、同分异构体:具有相同化学式不同结构的化合物。
甲烷知识点总结文库

甲烷知识点总结文库一、甲烷的性质1. 物理性质甲烷是一种无色、无味、易燃的气体,它的分子式为CH4,属于非极性分子。
该气体在常温下为气态,密度小于空气,可漂浮在空气中。
甲烷的沸点为-161.5℃,熔点为-182.5℃,这表明它在常温下是气态。
另外,甲烷是一种不溶于水的气体。
2. 化学性质甲烷是一种较为稳定的化合物,不容易发生化学反应。
在氧气充足的情况下,甲烷可以燃烧,生成二氧化碳和水:CH4 + 2O2 → CO2 + 2H2O这是一种高效的能量转化过程,因此甲烷被广泛应用作为燃料。
此外,甲烷还可以在一定条件下与氯气反应,生成氯甲烷等化合物。
二、甲烷的制备1. 天然气提取天然气是地下储存的气体混合物,其中主要成分就是甲烷。
天然气的提取通常是通过水平井或者钻井将天然气从地下挖掘出来,然后经过一系列的处理,如去除杂质和液态组分,最终得到纯净的甲烷气体。
2. 实验室合成实验室中也可以通过一些化学反应制备甲烷。
其中一种常用的方法是将碳的粉末与过量的氢气在高温高压条件下反应,生成甲烷气体:C + 2H2 → CH4三、甲烷的应用1. 燃料作为一种优秀的燃料,甲烷被广泛应用于家庭、工业和交通等领域。
由于甲烷燃烧时生成的二氧化碳和水是清洁无害的,因此它被誉为“最干净的化石燃料”。
甲烷可以用于家用燃气灶、工业锅炉、发电厂等的燃料。
此外,甲烷还可以作为汽车和公交车的燃料,用于推动发动机。
2. 化工原料甲烷可以作为化工原料用于合成其他有机化合物,如甲醇、丙烯等。
甲烷经过氧化反应或氢解反应可以生成甲醇,而甲醇又是一种重要的化工原料。
此外,甲烷还可以通过一系列的反应,如氯化反应、氟化反应、氢化反应等,合成其他有机化合物,如氯甲烷、氢氟酸甲酯等。
3. 其他应用甲烷还有一些其他应用,如用作航天火箭的推进剂、用于生产人造钻石的碳源等。
四、甲烷的环境影响甲烷是一种温室气体,它对地球的大气有着较强的吸收能力,能够吸收和保留太阳能辐射,使地球的表面温度升高。
甲烷的制备与性质

甲烷的制备与性质一、实验教学目标1.掌握实验室制备CH 4与CH 4性质实验的操作;2.初步学会CH 4实验的演示教学方法。
二、实验原理CH 3COONa +NaOHCO 3+CH 4CH 4+2O 2 2H 2O +CO 2甲烷的物理性质:通常状况下,CH 4是无色、无味、可燃和微毒的气体,密度比空气小,极难溶于水。
甲烷的化学性质:通常情况下,CH 4性质稳定,不易与强酸、强碱、卤素单质的水溶液和强氧化剂反应,空气中燃烧产生淡蓝色火焰,甲烷中混入氧气或空气遇明火会发生爆炸(CH 4的爆炸极限体积比为5%-15%)。
三、仪器、材料与试剂铁架台、酒精灯、垫木、天平、大试管、锥形瓶(250ml )、烧杯(100ml 、200ml )研钵、水槽、坩埚钳、镊子、药匙、火柴、集气瓶、玻璃片、30°导管、直型导管。
无水CH 3COONa 、NaOH 、CaO 、Fe 2O 3、KMnO 4、溴水、澄清石灰水、30%H 2O 2、MnO 2。
四、实验内容1.CH 4的制备(1)方法一操作过程:① 组装实验装置如下图(从左到右,从上到下);② 检查装置气密性:把导管的下端浸入水槽中,用双手紧握试管底部(也可用热毛巾捂热或者用酒精灯微热),如果观察到导气管口有气泡逸出,证明装置气密性良好;Δ点燃③取7.5g无水CH3COONa、2.0g NaOH、2.0 g CaO,将三者分别用研钵研细,再混合均匀,借用纸槽加入洁净、干燥的硬质试管中,塞进单孔塞;④点燃酒精灯后,先预热试管1—2分钟,然后集中火力由管前向试管尾加热;⑤用排水法收集。
反应开始后,待气泡快速、均匀、连续冒出时,此时整个装置中的空气已排尽,开始收集。
当试管口冒出第一个气泡时,表示已集满;⑥验纯:把用排水法收集的甲烷气体,用大拇指按住试管口,将试管口向下略倾斜靠近酒精灯火焰,如果甲烷安静的燃烧或发出“噗”的一声,则说明甲烷纯净,可以进行下面的性质实验;⑦实验结束后,先移出导管后熄灭酒精灯,以防倒吸。
甲烷的物理化学性质

甲烷的物理化学性质接下来为你整理了甲烷的物理化学性质,一起来看看吧。
甲烷的物理性质颜色无色气味无味熔点-182.5℃沸点-161.5℃溶解度(常温常压)0.03分子结构正四面体形非极性分子分子直径0.414nm 蒸汽压53.32kPa/-168.8℃饱和蒸气压(kPa)53.32(-168.8℃)相对密度(水=1)0.42(-164℃)相对密度(空气=1)0.5548(273.15K、101325Pa)临界温度(℃)-82.6临界压力(MPa)4.59爆炸上限%(V/V)15.4爆炸下限%(V/V)5.0闪点(℃)-188引燃温度(℃)538燃烧热890.31KJ/mol 总发热量(产物液态水)55900kJ/kg(40020kJ/m3)净热值(产物气态水)50200kJ/kg(35900kJ/m3)H—C—H 键角109°28′C—H 键413kJ/mol 晶体类型分子晶体国标编号21007IUPAC名methane别名天然气,沼气,生物气CAS号74-82-8SMILESCInChI1/CH4/h1H4溶解性(水)3.5 mg/100 mL (17 °C)摩尔质量16.0425 g·mol警示术语R:R12安全术语S:S2-S9-S16-S33密度(标准情况)0.717g/L特殊性质极难溶于水甲烷的化学性质但是在特定条件下,甲烷也会发生某些反应。
取代反应甲烷的卤化中,主要有氯化、溴化。
甲烷与氟反应是大量放热的,一旦发生反应,大量的热难以移走,破坏生成的氟甲烷,只得到碳和氟化氢。
因此直接的氟化反应难以实现,需用稀有气体稀释。
碘与甲烷反应需要较高的活化能,反应难以进行。
因此,碘不能直接与甲烷发生取代反应生成碘甲烷。
但它的逆反应却很容易进行。
以氯化为例:可以看到试管内氯气的黄绿色气体逐渐变淡,有白雾生成,试管内壁上有油状液滴生成,这是甲烷和氯气反应的所生成的一氯甲烷、二氯甲烷、氯仿(或三氯甲烷)、四氯化碳(或四氯甲烷)、氯化氢和少量的乙烷(杂质)的混合物。
甲烷的物理性质和化学性质

甲烷的物理性质和化学性质
甲烷(CH4)是简单烃物质,也称为沼气或沼泽气体,在空气中最常见的碳氢化合物之一,在自然界中广泛存在。
甲烷是一种无色和无味的气体混合物,以沼气形式存在,原始质量
约为87.6%甲烷、9.7%二氧化碳、2.7%氮气和少量的其他气体,如氢、氦和氩等元素。
甲烷的物理性质包括:它的比重大于1,摩尔质量为16.04,在正常温度和压力下是气体,熔点为-82.4°C,沸点为-164.4°C,相对密度大约为0.5561。
甲烷具有显著的化学性质。
它是一种碳氢化合物,因此具有许多与它相关的化学反应。
首先,它是一种很不稳定的化合物,当温度较高时,它会分解成氢气和二氧化碳,温度越高,其分解速率也越高。
此外,甲烷还与炭酸钠、氢氧化钠等化学物质进行水解反应,出现氢
气和碳酸酯。
此外,甲烷还可以与水进行缩聚反应,形成甲烷水合物。
甲烷也可以与空气中的氧合成碳氧化物。
这项反应在火腿制作过程中也很有用,因为甲烷
可以与空气中的氧分子结合,产生蛋白质焦化物,使表面变红,达到金黄色。
总之,甲烷的物理性质包括它的物理性质,例如摩尔质量、相对密度、熔点和沸点。
它的
化学性质包括其舍宾反应、水解反应、缩聚反应和氧化反应。
一般来说,这些反应都可以
用来生产和改变特定化合物的性质。
烷烃

一、甲烷1、存在:。
2、物理性质: 甲烷是色、味、溶于水的气体,密度比空气密度。
用或收集甲烷。
3、分子结构:分子式:,电子式:,结构式:,结构简式:。
空间构型:,碳氢键,键角,最多个原子共平面4、化学性质在通常情况下,甲烷稳定,与不反应,与也不反应。
(1)氧化反应纯净的甲烷在空气中燃烧,火焰呈。
反应的化学方程式:。
注:甲烷不能被酸性高锰酸钾溶液氧化,所以甲烷不能使酸性高锰酸钾溶液褪色。
(2)取代反应定义:。
特点:。
(3)甲烷受热分解:CH4高温 C + 2H2注;烷的取代反应是“连锁”式的反应,生成几种氯代物的混合物。
其中,是气体,其余的为液体,均不溶于水,三氯甲烷又叫“氯仿”四氯甲烷又叫,是一种有机溶剂。
KMnO4 (H+) 通入CH4(不褪色)Br2水(橙色)通入CH4(不褪色)二、烷烃1.定义:烃分子中的碳原子之间只以单键结合,碳原子剩余的价键全部跟氢原子相结合,使每个碳原子的化合价都已充分利用,都达到“饱和”。
这样的烃叫做饱和烃,又叫烷烃。
2.组成通式:C n H2n+2。
3.结构特点①碳碳单键(C—C)②呈链状(直链或带支链)③“饱和”:碳原子剩余的价键全部与氢原子结合,每个碳原子都形成 4 个单键。
烷烃甲烷乙烷丙烷丁烷异丁烷分子式CH4C2H6C3H8C4H10C4H10结构式结构简式球棍模型:5、烷烃的化学性质:与甲烷相似,通常状况下很稳定,跟强酸、强碱、强氧化剂都不反应,都能在空气里燃烧,在光照下与氯气发生取代反应。
6、烷烃的命名:※烃基:烃分子失去一个或几个氢原子以后剩余的部分。
甲基(-CH3)、乙基(-CH2CH3)①习惯命名法:按碳原子总数读做“某”烷十个碳以内的:读“天干”名(甲、乙、丙、丁、戊、己、庚、辛、壬、癸)十个碳以上的:按碳原子总数读做“某”烷。
同分异构体:读做“正”、“异”、“新”。
例如:C5H12(戊烷)C8H18(辛烷)C17H36(十七烷)②系统命名法:选主链称某烷:选最长的碳链为主链,按主链上的碳原子数读“某”烷。
【化学课件】甲烷的性质

好好学习,天天向上。
三、甲烷的化学性质
1.与氧气的反应
2.加热分解
三、甲烷的化学性质
3.取代反应
反应现象:试管中液面逐渐上 升,混合气体黄绿色变淡,试 管壁上有油状液滴出现。
取代反应与置换反应的比较
取代反应
可与化合物发生取代, 生成物中不一定有单质Fra bibliotek置换反应
反应物、生成物中一定 有单质
反应能否进行受催化剂、 在水溶液中进行的置换反 温度、光照等外界条件影 应遵循金属活动性顺序 响较大 逐步取代,产物较复杂 反应产物简单
四、存在与用途
上海城市居民所使用的燃料主要是管道煤气, 但某些地区已开始使用东海天然气作为居民燃料。 管道煤气的主要成分是CO、H2和少量烃类,天 然气的主要成分是CH4。燃烧相同体积的管道煤 气和天燃气,消耗空气体积较大的是 。如果将 燃烧管道煤气的灶具改烧天然气,灶具的改进方 法是 (填增大或减小)进风口。如不作 改进可能产生的不良后果是 。
已知有一化合物仅含碳氢两种元素,碳氢质量 比是9:2,在标准状况下,密度为1.964克/升, 试写出该化合物的分子式。
1、做老师的只要有一次向学生撒谎撒漏了底,就可能使他的全部教育成果从此为之毁灭。——卢梭 2、教育人就是要形成人的性格。——欧文 3、自我教育需要有非常重要而强有力的促进因素——自尊心、自我尊重感、上进心。——苏霍姆林斯基 4、追求理想是一个人进行自我教育的最初的动力,而没有自我教育就不能想象会有完美的精神生活。我认为,教会学生自己教育自己,这是一种 最高级的技巧和艺术。——苏霍姆林斯基 5、没有时间教育儿子——就意味着没有时间做人。——(前苏联)苏霍姆林斯基 6、教育不是注满一桶水,而且点燃一把火。——叶芝 7、教育技巧的全部奥秘也就在于如何爱护儿童。——苏霍姆林斯基 8、教育的根是苦的,但其果实是甜的。——亚里士多德 9、教育的目的,是替年轻人的终生自修作准备。——R.M.H. 10、教育的目的在于能让青年人毕生进行自我教育。——哈钦斯 11、教育的实质正是在于克服自己身上的动物本能和发展人所特有的全部本性。——(前苏联)苏霍姆林斯基 12、教育的唯一工作与全部工作可以总结在这一概念之中——道德。——赫尔巴特 13、教育儿童通过周围世界的美,人的关系的美而看到的精神的高尚、善良和诚实,并在此基础上在自己身上确立美的品质。——苏霍姆林斯基 14、教育不在于使人知其所未知,而在于按其所未行而行。——园斯金 15、教育工作中的百分之一的废品,就会使国家遭受严重的损失。——马卡连柯 16、教育技巧的全部诀窍就在于抓住儿童的这种上进心,这种道德上的自勉。要是儿童自己不求上进,不知自勉,任何教育者就都不能在他的身 上培养出好的品质。可是只有在集体和教师首先看到儿童优点的那些地方,儿童才会产生上进心。——苏霍姆林斯基 17、教育能开拓人的智力。——贺拉斯 18、作为一个父亲,最大的乐趣就在于:在其有生之年,能够根据自己走过的路来启发教育子女。——蒙田 19、教育上的水是什么就是情,就是爱。教育没有了情爱,就成了无水的池,任你四方形也罢、圆形也罢,总逃不出一个空虚。班主任广博的爱 心就是流淌在班级之池中的水,时刻滋润着学生的心田。——夏丐尊 20、教育不能创造什么,但它能启发儿童创造力以从事于创造工作。——陶行知
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
其反应方程式为:
CH4+2O2 CO2+2H2O
总结:甲烷是一种无色无味的气体,密度比空气小,极难溶于水。甲烷有可燃性,火焰呈蓝色,点燃前要先验纯。燃烧时生成二氧化碳和水,同时放出大量的热。
3甲烷的受热分解
在隔绝空气并加热至1000度时,甲烷分解生成炭黑和氢气:
CH4 C + 2H2
H2是合成NH4及合成汽油等工业的原料,炭黑是橡胶工业的原料。
【方法总结】
化学是一门实验学科,各种理论知识都是以实验为基础的,所以要重视实验现象,从实验现象中分析总结规律,用学过的理论知识来解释常见的这些实验现象,这样才能彻底理解知识,使记忆更加牢固,是枯燥的课堂变得生动活泼。
三、情景素材描述
沼气池成"死亡陷阱"
西部地区是我国经济发展相对缓慢的地区,其中大部分地区为少数民族聚居区,边疆地区和贫困地区。但随着"西部大开发"战略的实施和"社会主义新农村"的建设,一些地区的人们开始利用科技脱贫致富,走上了小康之路。于是在西部农村,家家户户建起了沼气池,来体验科技带来的便利。但由于西部农村人们科学技术水平普遍较低,沼气池引发的事故时有发生。
【化学性质】
1、 氧化反应
(1)黄某当初建沼气池的目的就是要利用沼气可以燃烧的性质,所以说甲烷具有可燃性。如图将甲烷点燃后,上方罩一小烧杯。
燃烧时可以清楚的看见明亮的蓝色火焰。燃烧后烧杯内壁有水珠生成,将烧杯正放于桌面上,立刻到入澄清石灰水,石灰水变浑浊。
有上述现象我们可以得出甲烷的燃烧产物是什么呢?
【物理性质】
研究人员对沼气进行了一系列的除杂和提纯,将里面的CO2和NH3等气体除去后得到了较为纯净的甲烷气体。
经观察分析可知,该气体为一种没有颜色,没有气味的气体。密度为0.717g/L(标准状况),极难溶于水。(这就解释了当时黄某和姬某为什么没有及时发现甲烷中毒,而命丧与沼气池。)
2、既然沼气是杀死黄某、姬某的直接原因,那么什么是沼气呢?沼气的成分是什么呢?
(沼气是一些有机物质(如秸杆、杂草、树叶、人畜粪便等废弃物)在一定的温度、湿度、酸度条件下,隔绝空气(如用沼气池),经微生物作用(发酵)而产生的可燃性气体。沼气是气体的混合物,其中含甲烷60~70%.)
五、甲烷的物理化学性质
甲烷的物理性质与化学性质
北京师范大学化学学院 2007级 李新强
一、 情景教学的内容
本节所选择的对象为高中化学教学的情景设计,所选取的教学内容为人民教育出版社出版的普通高级中学教科书《化学》(必修加选修2)中第五章烃第一节甲烷的内容。本节是学生在高中化学学习阶段第一次涉及到有机化学,因此从最简单的有机物甲烷开始。教学内容包括甲烷的结构式,空间结构,甲烷的物理、化学性质。重点掌握甲烷的空间结构,氧化反应和取代反应。
2、通过对情景素材的分析和实验,培养学生化学研究的一般方法。即:发现问题
分析问题 设计实验 进行实验 得出结果 得出结论。
3、通过对情景素材的学习,了解一些常见的化学常识,树立化学安全意识,提高分析解决问题的能力,提升科学素养的水平。
早期的科学家通过光的衍射对甲烷进行了微观研究。研究发现甲烷的分子式为CH4,在甲烷分子中,C原子以最外电子层上的4个电子与4个H原子的电子形成4个共价键。
甲烷的电子式和结构式只能表示C原子与H原子的成键情况,但不能说明各原子的空间分布情况。实验证明:CH4中C原子与4个H原子并不在一个平面内,整个分布呈四面体形结构,4个H在四面体的顶点上。
将甲烷与氯气按1:4混合,放在光亮的地方会发生什么现象呢?
现象:3分钟后,量筒壁上出现油状液滴,量筒内水面上升。
分析:由现象可说明甲烷与氯气在光照条件下确实发生了化学反应。
量筒壁上出现油滴,说明反应生成了新的油状物:
量筒内的水面上升,说明随着反应的进行,量筒内气压减小,即气体总体积在减小。
摘自《云南法制报》2008.3.5
四、情境问
题的创设
1、看完这组材料后,同学们对黄某、姬某的死有何感想呢?造成他们死亡的原因是什么呢?
(黄某、姬某死的实在很冤、很可惜,尤其是姬某,不明情况,跳入沼气池救人,白白打上一条性命。究其死因,主要包括直接原因和间接原因。直接原因是沼气池中沼气浓度大,使黄某、姬某相继窒息死亡;间接原因是黄某、姬某还有村民缺乏相关的化学知识,盲目的进入误区,造成了此次事故。所以说学好化学很重要,它能在关键时刻拯救人们的生命财产安全。)
六、教学程序设计
导言(说明授课内容)
用幻灯片播放情景素材并设问
展示一瓶甲烷气体,和甲烷的分子模型,研究其物理性质
做【演示实验】:1甲烷的燃烧,2甲烷和高锰酸钾的反应
总结甲烷的氧化反应
做【演示实验】甲烷与氯气的取代反应
甲烷取代物的复杂性
甲烷的受热分解
化学实验研究的重要性
二、 情景创设的意图和目的
化学是一门中心的、实用的、创造性的学科。因此在化学的教学活动中,要将理论和实际联系起来,解释生活中的一些现象,同时运用所学过的知识解决简单的化学问题。在"解释"与"解决"的过程中培养学生用实验分析问题的能力和创造力。
1、通过情景素材的内容,引发学生学习的兴趣和积极性,使教学向生动、活泼、主动的方向进行,使学生在兴奋,愉悦中接受知识。
下课
首届全国高等院校化学专业师范生教学素质大赛
1
07级3班
微观解释:甲烷分子里的H原子逐步被Cl原子所取代,生成四种取代产物。
取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所取代的反应。
化学方程式:
(1)
(一氯甲烷,g)
(2)
(二氯甲烷,l)
(3)
(三氯甲烷,l)
(4)
(四氯甲烷,l)
注意:有机物参加的反应往往比较复杂,常有副反应发生。因此有关有机反应的化学方程式通常不用等号,而用" "表示。
(2)把甲烷通入酸性高锰酸钾溶液中,紫色溶液是否
有变化呢?
实验现象:紫色的酸性高锰酸钾溶液颜色没有改变。
实验表明:甲烷的化学性质是比较稳定的,不与高锰酸钾溶液,强酸,强碱反应。
2、取代反应
2008年3月5日,禄丰县一村民黄某由于从进料池加不进粪,就到出料池打开盖子检查,黄某打开盖子后探头往里看,人一下子就掉了进去,在一旁帮忙的黄妻急忙过去拉他,可还没等拉出池子,黄某就顺着池壁软软地滑到池底不会动了,邻居姬某听到呼救立即赶来救助黄某,可不到几分钟,下到池底的姬某也不会动了。听到黄妻哭喊的村民周某跑过来看到池里晕了两个人,他下到池里才两分钟,就觉得头部刺痛,胸口则像压了重物喘不过气来,意识到危险的周某立即爬出池口,闻讯纷纷赶来的村民七手八脚把已经昏迷的黄某、姬某拉了上来。
