试验流程图模板
医疗器械临床试验工作流程图

医疗器械临床试验工作流程图
申办者准备材料选择研究者及临床试验机构共同制订临床试验方案
伦理委员会审议 SFDA 审批试验方案
临床试验需审批的
医疗器械目录
试验过程中是否
发生严重不良事件出具《临床试验报告》伦理委员会再审议临床试验完成不同意
同意是
临床试验准备阶段
严重不良事件报告临床试验进行阶段
临床试验完成或终止阶段
签订有关协议或合同
临床试验机构整理保存文件
同意不同意否申办者提供样品,选监查
员,研究者及临床试验机构
知情同意观察、记录、分析否
是开始试验申办者
修改知情同意内容
申办者监督管理部门
根据事件危害程度
作出相应处理
申办者要求监督管理部门责令
继续
临床试验终止不得进行临床试验
不同意作必要
修改。
电气试验流程图
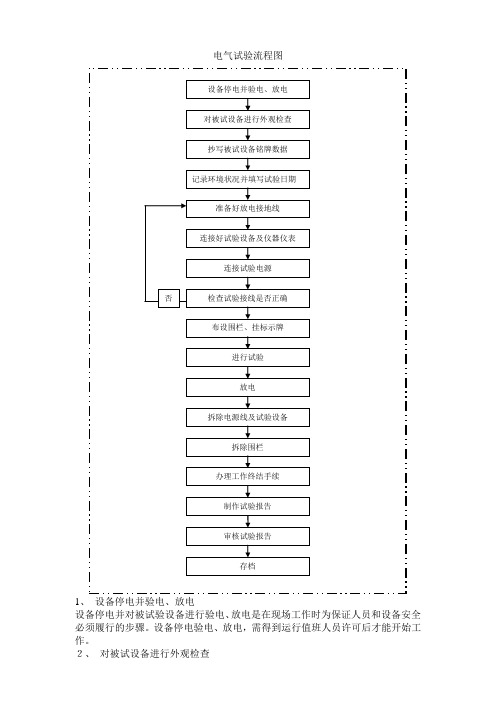
电气试验流程图1、设备停电并验电、放电设备停电并对被试验设备进行验电、放电是在现场工作时为保证人员和设备安全必须履行的步骤。
设备停电验电、放电,需得到运行值班人员许可后才能开始工作。
2、对被试设备进行外观检查外观检查内容包括:瓷件有无破损、充油设备是否缺油、与被试设备连接线是否全部拆除、设备本身有无异常现象等。
3、抄写被试设备铭牌数据凡试验每一台设备,必须将设备铭牌数据完整地抄录下来,这是试验的需要,也是填写试验报告、建立试验台账的需要。
4、记录环境状况并填写试验日期环境状况包括天气状况、环境温度、设备温度及大气气压等,以便将试验数据换算到标准条件下进行比较,同时还要填写试验日期。
5、准备好放电接地线准备好对设备进行放电的接地线,接地线应牢固可靠,保证一定的截面积,一端与接地体相连,另一端与干燥的接地棒相连。
6、连接好试验设备及仪器仪表根据试验项目,按照经批准的试验方案,连接好试验设备及仪器仪表,合理整齐地布置现场。
试验器具应处于试验人员视线之内,并在允许范围内尽量靠近被试品。
7、连接试验电源根据试验项目,确定试验电源。
将电源线与刀开关连接好,并将刀开关打开。
8、检查试验接线是否正确试验接线应由试验工作负责人进行检查。
检查内容有:接线是否正确,试验导线连接处是否牢靠,试验设备及仪器是否在起始位置,仪表是否已调到零位等。
9、布设围栏、挂标示牌在被试设备及试验设备周围应装设封闭遮栏或围栏,悬挂“止步、高压危险”标示牌,标示牌字应朝外,要有专人看守,以防其他人员进入试验区。
如被试品两端不在同一地点,另一端也应派人看守。
10、进行试验试验操作时,应由一人操作,一人监护并作记录,填写好试验项目及测量的数据。
操作者的活动范围应满足与带电部位的最小安全净距。
试验时,应随时注意试验数据,做好降压、限流或断电准备,发现异常现象应立即断电。
电源确已断开后,进行接地放电、检查设备、分析异常,然后再确定是否继续进行试验。
检验与试验管理程序(含流程图)
ABC科技有限公司
文件制修订记录
文件编号II-QP-13 页数2/8 生效版本02
1.目的:
规范检验流程及标准,使公司的生产、服务提供过程品质得到有效的控制,从而不流入不良品、不制造不良品,不流出不良品。
2.范围:
适用于本公司进料(包括客供料)、制程、成品检验工作和可靠性试验作业。
3.参考文件:
3.1产品防护与出货管理程序
3.2不合格品控制程序
3.3采购与供应商管理程序
4.定义:
4.1可靠性试验:对实现产品功能的保障能力的测试。
4.2首件:每个新订单生产前或生产过程中生产条件发生变化后(5M1E等)所生产的第一或前几件产品。
4.3首检:对首件产品进行检查及确认的过程。
5.责任:
5.1品管:负责来料、制程及成品的检验及标识、试验仪器操作及可靠性实验执行。
5.2生产:负责生产成品的送检,制程不合格情况的改善,将生产成品入库。
5.3仓库&采购:负责来料的送检,不合格品的处理,出货成品的送检;检测单位选定及管理。
5.4工程部:负责检验标准技术文档的提供。
6抽样方案:
文件编号II-QP-13 页数3/8 生效版本02
6.1特殊部件进行全检(例如摄像头等),电子料和线材按0.4抽样,壳料和包材按1.5抽样(若质量问题多则加严抽样)
7.相关记录:
7.1进料检验报告
7.2进料品质异常单
7.3制程巡检报表
7.4首件检验记录
7.5成品检验报告
7.6可靠性实验报告。
试验流程图——精选推荐

土的含水量试验(烘干法)流程图(JTJ051-93 P31)压实度试验(环刀法、灌砂法)流程图(JTJ051-93 P40、50)土的界限含水量(液塑限联合测定法)试验流程图(JTJ051-93 P80)击实试验流程图(JTJ051-93 P128)无机结合料稳定土无侧限抗压强度试验流程图(JTJ057-94 P19)集料试验流程图(JTJ058-2000)集料吸水率试验流程图(JTJ058-2000 P27、108)水泥或石灰稳定土中水泥或石灰剂量测定流程图(JTJ057-94 P38)水泥砼抗折试验流程图(JTJ053-94 P64)水泥砼抗压试验流程图(JTJ053-94 P58)砂浆抗压试验流程图(JGJ70-90)集料与沥青粘附性试验流程图(JTJ052-2000 P97)沥青针入度试验流程图(JTJ052-2000 P32)沥青延度试验流程图(JTJ052-2000 P43)个沥青软化点试验流程图(JTJ052-2000 P48)马歇尔稳定度试验流程图(JTJ052-2000 P290)沥青密度试验流程图(JTJ052-2000 P25)沥青含量试验流程图(离心分离法)(JTJ052-2000 P359)宕渣综合毛体积密度试验流程图弯沉试验(贝克曼梁法)流程图(JTJ059-95 P58)路面构造深度试验(手工铺砂法)流程图(JTJ059-95 P90)平整度试验(3m直尺法)流程图(JTJ059-95 P33)水泥混凝土回弹试验流程图(JTJ059-95 P73)集料的坚固性试验(JTJ058-2000 P46、133)粗集料软弱颗粒试验流程图(JTJ058-2000 P65)细集料轻物质试验流程图(JTJ058-2000 P130)细集料云母含量试验流程图(JTJ058-2000 P129)粗、细集料有机物含量试验流程图(JTJ058-2000 P45、127)试验检测流程图浙江中威交通建设有限公司二○○三年四月二十八日质量保证体系框图质量保证体系框图。
公路工程试验检测工作程序流程图

有异议 结作程序图
试验检测工作程序图
不合格
仪器设备 性能保证
环境保证
专人验收、检 定、校验、管 理、记录
环境控制、 记录
技术负责人
检查、验收 合格
进入 检测 状态
检测质量事故处理
重新开始 所有检测
提出处 理意见
质量负责人负责组织调查、 分析原 因
处理记录、意见存档、上报
质量申诉处理
重新开始 所有检测
怀疑原结果
提出处 理意见
质量负责人负责组织 调 查、分 析 原 因
处理意见 记录存档
抽
样品验收、
样
登记、管理
不合格 合格
安排检 选定技术标准、 测人员 规程、方法
检查仪器设备状态、检测环 境、被测件情况、并做记录
检 事故
测 成功
数据处理、填写、复核 检 测 报告
技术负责人审核、签发 检测 报 告
检 测 报 告 归 档、 发送抽检单位
最终检验流程图最终试验流程图

最终检验流程图最终试验流程图
N
Y
N Y N
Y
对工程质量资料核查、对工程质量
进行质量等级评定 工程是否合格? 填写实验委托单送试样 检查核对试样尺寸、数量、外观、编号、委托单内容 计算、评定
填写实验报告 复合、签章 签发报告
交甲方有关部门验收办理竣工验
申请竣工核验 是否合核验、合发合格证书 交付使用 优良工程评定 实验是否合格? 交付放行 执行
“不合格控制程序” 执行 “不合格控制程序” 执行 “不合格控制程序” 对必试项目和要求项目进行实验,填写实验记录。
皮内试验操作流程图

皮内注射操作流程图素质要求核对医嘱病情、治疗情况及有无药物过敏史评估意识状态、心理状态及合作程度注射部位的皮肤情况洗手,戴口罩操作前准备备齐用物患者床号、姓名核对注射单与医嘱药名、剂量、浓度、用法药名、剂量核对标签注射盘:铺无菌盘浓度、有效期抽取或配置皮试溶液药物准备放于无菌盘内瓶身、安瓿有无破损检查核对,解释药液有无变质患者准备安置舒适体位选定注射部位(前臂掌侧下1∕3)75%乙醇消毒皮肤,螺旋式由内向外,直径>5cm核对并抽取药液,排尽空气注射绷紧皮肤,针头与皮肤成5°进针固定针栓(用左手拇指)注药0.1ml形成皮丘协助患者躺卧舒适拔针勿按压计时20min后观察反应告知患者相关药疗的作用,做药物过敏试验后,健康教育告知患者不可用手拭去药液,不可按压皮丘,20min内不可离开病房,不可剧烈活动,如有不适及时联系。
对接受局麻、预防接种者,讲解治疗后如何观察,如有不适,应及时处理清理用物,归还原处皮试结果阴性或阳性的判断方法及记录方法,判断结果告知患者试验结果记录一、青霉素、头孢阳性标记病历:阳性标记单(红色)、体温单、临时医嘱单、住院病案首页办公室:病员一览表、黑板、电脑记录单:护理记录单、入院护理单(带入者)、注射单、服药单、交班本患者处:床尾并告知患者及家属、门诊病历卡、手腕带其他药物阳性标记1、体温单2、临时医嘱单3、住院病案首页4、护理记录单5、入院护理单(带入者)6、门诊病历卡7、手腕带二、目的1)预防接种2)各种药物过敏试验,观察局部反应3)局部麻醉药的先驱步骤三、注意事项1)严格执行查对制度及无菌操作原则2)药液现用现配,剂量准确,用1ml注射器3)注射前询问过敏史,过敏者不注射4)选择前臂掌侧下端内侧为注射部位,用75%酒精消毒待干,绷皮5°进针,左手拇指固定针栓,右手推注药液0.1ml 成皮丘5)进针前核对药液,排尽空气6)记录注射时间,告知患者勿用手拭去药液按揉皮丘,20min内不可离开,不可剧烈运动,有不适及时联系。
试验检测流程图
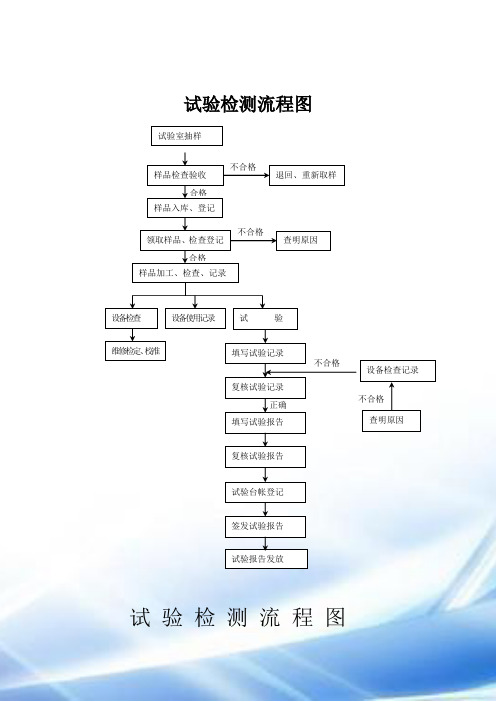
试验检测流程图试 验 检 测 流 程 图试验室抽样 样品检查验收退回、重新取样样品入库、登记 领取样品、检查登记样品加工、检查、记录 不合格 合格合格查明原因不合格 设备检查记录试验报告发放试 验填写试验记录复核试验记录不合格查明原因 不合格 填写试验报告 复核试验报告试验台帐登记签发试验报告正确设备检查 维修检定、校准 设备使用记录烘干箱操作规程一、作业前的准备1、接上电源后,即可开启工作加热开关。
试验室抽样样品检查验收退回、重新取样样品入库、登记 领取样品、检查登记样品加工、检查、记录 设备检查记录 试 验填写试验记录维修检定、校准 复核试验记录不合格 合格合格查明原因不合格 设备检查记录不合格查明原因 不合格 填写试验报告 复核试验报告试验台帐登记签发试验报告试验报告发放正确二、作业中的要求2、再将控制器旋钮由0℃位置按顺时针方向旋至达到的设置的温度,此时箱内开始升温,指示灯亮作指示。
3、当温度升到所需工作温度时此时可再把旋钮作微调至指示灯熄灭处为其恒温(很可能在恒温时,温度仍继续上升,此乃余热影响,此现象约半小时左右即会处于稳定)。
当箱内温度稳定时(即所谓“恒温状态”,如温度计上读数超出或低于所需温度,则可控温器再稍微调整,以达到正确程序为止)。
4、恒温时,可关闭一组加热器工作,以免功率过大,影响恒温灵敏度。
5、温度恒温时,可根据试验需要,令其作一定时间的恒温,在此过程,可借箱内控制恒温器自动控温,而不需另加人工管理。
6、欲观察工作室试品情况,可开启箱外门、借箱内一玻璃门观察之。
但箱门以不常开启为宜,以免影响恒温,并且当温度升至300℃时,开启箱门可能使玻璃门急骤冷却而破裂。
三、作业后的要求7、停止工作后,关闭电源,待冷却至室温时,清洁箱内卫生。
仪器设备管理制度一、仪器设备的管理,包括设备的购置、审批、验收、使用、维修、养护、保养、检定/校准、标识、降低、封存、报废等。
二、检验仪器设备的购置应由试验单位提出书面购置申请报告,包公司测试中心审批,经公司主管领导批准后,固定资产部分有公司测试中心购置,低值易耗品由使用单位购置。
临床试验进行期间及结束流程图

临床试验进行期间及结束流程图
申办者
召开临床试验启动会
进行项目培训
病人初筛选
进行相关检查
按方案进行临床试验
按规定时间填写原如病历及CRF
中期会
受试者试验结束后,监
查员收回CRF并审核
数据管理部门建立数据
盲态审核
锁定数据库
第一次揭盲出具统计分析报告
第二次揭盲项目总结会
知情同意满足条件
CRF及研究资料由机构资料
档案室验收后归档
机构办公室全程质量稽查
伦理委员会
地方药监局和CFDA
申办者SAE报告
获知24h
退
出
返
回
相
关
科
室
按
常
规
继
续
治
疗
方案修改
不满足条件
不满足条件
伦
理
委
员
会。
实验室流程图
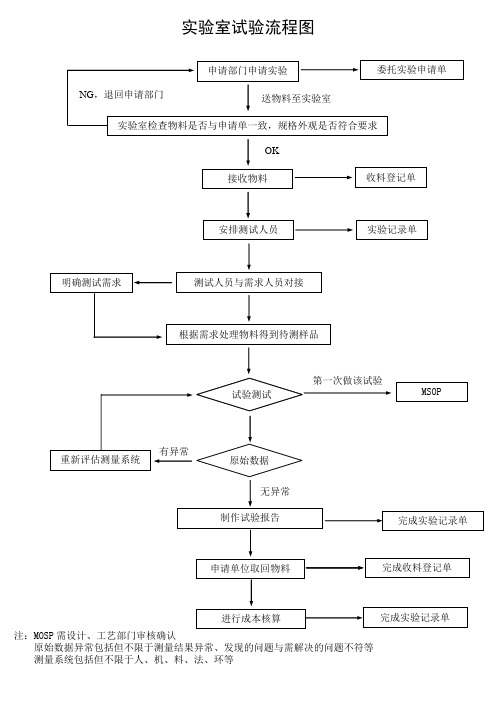
实验室试验流程图
第一次做该试验
试验测试 实验室检查物料是否与申请单一致,规格外观是否符合要求
无异常
有异常
或与 收料登记单
明确测试需求 注:MOSP 需设计、工艺部门审核确认
原始数据异常包括但不限于测量结果异常、发现的问题与需解决的问题不符等 测量系统包括但不限于人、机、料、法、环等 接收物料 安排测试人员 实验记录单
测试人员与需求人员对接
MSOP
试验测试 原始数据
重新评估测量系统 制作试验报告 完成收料登记单
申请单位取回物料 完成实验记录单
根据需求处理物料得到待测样品
申请部门申请实验
委托实验申请单
送物料至实验室 OK
NG ,退回申请部门 进行成本核算
完成实验记录单。
临床试验流程图
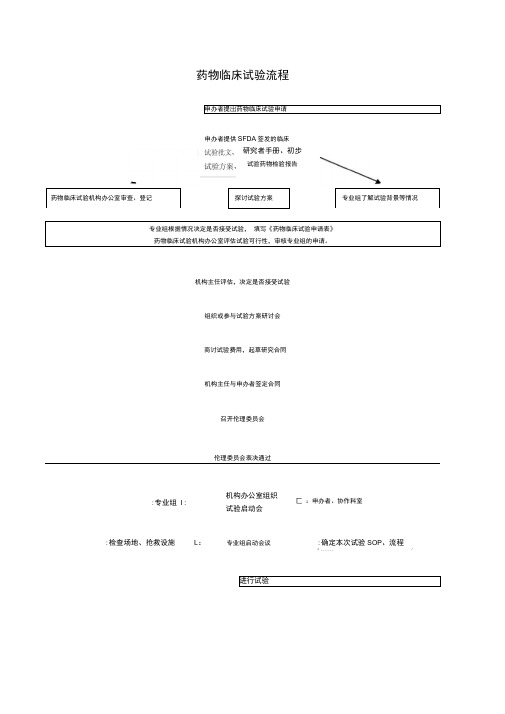
药物临床试验流程 申办者提岀药物临床试验申请
申办者提供SFDA 签发的临床
药物临床试验机构办公室审查、登记
探讨试验方案
专业组了解试验背景等情况
专业组根据情况决定是否接受试验, 填写《药物临床试验申请表》 药物临床试验机构办公室评估试验可行性,审核专业组的申请。
机构主任评估,决定是否接受试验
组织或参与试验方案研讨会
商讨试验费用,起草研究合同
机构主任与申办者签定合同
召开伦理委员会
伦理委员会表决通过
进行试验
:专业组 I :
机构办公室组织 试验启动会 匚 :申办者、协作科室
:检查场地、抢救设施
L : 专业组启动会议 :确定本次试验SOP 、流程 J _ _ _ _ _ _ -1
研究者手册、初步
试验药物检验报告
进行试验
机构办公室向申办者提交 CRF 第一联,退回试验用药物 项目负责人根据统计结果撰写小结 报告,组长单位撰写总结报告
机构办公室审核小结报告,最
后交申办者,小结报告归档
E
组长单位与申办者组织召开临床试验总结会
总结报告归档,与申办者办理相关手续
机构办公室提交财务报告,机构主任
审批,财务科发放劳务费或统一划帐 知情同意过程、签知情同意书 中期试验 协作会 试验数据记录 监查员、机构办公室的监查 <—[文件收集、归档 [ * "1 <3- 1项目负责人监督试验质量 <= 不良事件监查、处理、记录。
