化学选修5《有机化学基础》知识点总结剖析
选修5有机化学知识点总结

选修5有机化学知识点总结work Information Technology Company.2020YEAR高二化学选修5《有机化学基础》知识点整理一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:① 乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
② 苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
*⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、氟代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:① 烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态② 衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2==CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃)一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)*甲乙醚(CH3OC2H5,沸点为10.8℃)*环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
化学选修5有机化学基础知识点总结

化学选修5有机化学基础知识点总结随着社会的发展,化学科学已经成为人类生产和生活中不可或缺的一部分。
而有机化学则是化学科学中的一个重要分支,它研究的是碳元素在化合物中的性质、结构、反应和合成等方面。
化学选修5是高中化学教材中的一本重要教材,其中涵盖了有机化学的基础知识点。
下面就让我们来总结一下化学选修5有机化学基础知识点。
一、化学键的类型化学键是化合物中的原子之间形成的一种化学连接,有机化合物中常见的化学键有共价键、极性共价键、非极性共价键、离子键和金属键等。
共价键是有机化合物中最常见的一种化学键,它是通过原子间的电子共享而形成的。
极性共价键指的是由于原子间电子云密度不均匀而形成的一种电性分布不均的化学键。
非极性共价键则是由于原子间电子云密度相同而形成的一种电性分布均匀的化学键。
离子键是由正负电荷之间的静电作用而形成的化学键,金属键则是由金属原子之间共享电子形成的化学键。
二、有机物的命名有机物的命名是有一定规则的,常用的命名方法包括系统命名法、通用命名法和简称命名法等。
系统命名法是根据有机物分子中碳原子的数目、位置和官能团的类型等进行命名的。
通用命名法则是根据有机物分子中的官能团、基团等进行命名的。
简称命名法则是用缩写或简称来表示有机物的名称,如苯、甲苯等。
三、有机反应的分类有机反应按反应的类型可以分为加成反应、消除反应、取代反应和重排反应等。
加成反应指的是将两个单体化合物通过共价键连接起来形成一个更大的分子的反应。
消除反应则是指从一个分子中去掉两个或更多的原子或基团的反应。
取代反应指的是将一个原子或基团取代为另一个原子或基团的反应。
重排反应则是指在分子中发生原子间的重新排列的反应。
四、有机官能团的特性有机官能团是有机化合物中的一种重要结构单元,其性质影响了有机化合物的许多性质。
常见的有机官能团包括醇、酚、醛、酮、酸、酯、醚、羧酸等。
醇和酚是一类带有羟基的化合物,它们在水中溶解度较高,可以参与氢键的形成。
(完整版)人教版高中化学选修5有机化学基础知识点,推荐文档

有机化学基础第一章认识有机化合物第一节有机化合物的分类第二节有机化合物的结构特点第三节有机化合物的命名第四节研究有机化合物的一般步骤和方法归纳与整理复习题第二章烃和卤代烃第一节脂肪烃第二节芳香烃第三节卤代烃归纳与整理复习题第三章烃的含氧衍生物第一节醇酚第二节醛第三节羧酸酯第四节有机合成归纳与整理复习题第四章生命中的基础有机化学物质第一节油脂第二节糖类第三节蛋白质和核酸归纳与整理复习题第五章进入合成有机高分子化合物的时代第一节合成高分子化合物的基本方法第二节应用广泛的高分子材料第三节功能高分子材料归纳与整理复习题结束语——有机化学与可持续发展高二化学选修 5《有机化学基础》知识点整理2010-2-26一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体。
人教版高中化学选修5有机化学基础知识点

人教版高中化学选修5有机化学基础知识点人教版高中化学选修5有机化学基础知识点一、确定文章类型本文属于说明文,旨在向读者介绍人教版高中化学选修5有机化学基础知识点。
二、关键词1、有机化合物2、有机物分子结构3、官能团4、反应类型三、有机化学基础知识1、有机化合物有机化合物是指含碳元素的化合物,其中主要是碳氢元素,也包含其他元素,如氧、氮、硫等。
有机化合物的特点是其分子结构复杂,且具有特定的官能团。
2、有机物分子结构有机化合物的分子结构主要涉及碳原子的成键和立体化学。
碳原子因其四个价键,可以形成四面体结构。
通过单键、双键和三键,碳原子能够与其他原子形成稳定的键。
此外,有机分子的立体结构对其化学性质和反应活性具有重要影响。
3、官能团官能团是决定有机化合物性质的关键结构单元。
常见的官能团包括羟基、羰基、羧基、卤素原子、氨基等。
这些官能团在反应中起着重要作用,能够与其它官能团发生化学反应,从而改变有机化合物的性质。
4、反应类型有机化学反应主要包括取代、加成、消除、氧化还原、聚合等类型。
这些反应涉及到官能团的转化和新的化合物的生成。
理解反应类型及其机理对于学习有机化学至关重要。
四、总结本文对人教版高中化学选修5有机化学基础知识点进行了简要介绍,包括有机化合物、有机物分子结构、官能团和反应类型。
这些基础知识对于理解有机化学和从事相关领域的研究和工作至关重要。
通过学习和掌握这些知识,我们可以更好地理解有机化合物的性质、合成和转化,从而为未来的化学研究和应用奠定坚实的基础。
有机化学的不断发展也为我们的生活和工业生产带来了诸多便利和改变。
高中化学选修5:有机化学基础知识点大全

有机化学知识点归纳(一)一、有机物的结构与性质1、官能团的定义:决定有机化合物主要化学性质的原子、原子团或化学键。
2、常见的各类有机物的官能团,结构特点及主要化学性质(1)烷烃A) 官能团:无;通式:CnH2n+2;代表物:CH4B) 结构特点:键角为109°28′,空间正四面体分子。
烷烃分子中的每个C原子的四个价键也都如此。
C) 化学性质:(2)烯烃:A) 官能团:;通式:CnH2n(n≥2);代表物:H2C=CH2B) 结构特点:键角为120°。
双键碳原子与其所连接的四个原子共平面。
C) 化学性质:(3)炔烃:A) 官能团:—C≡C—;通式:CnH2n—2(n≥2);代表物:HC≡CHB) 结构特点:碳碳叁键与单键间的键角为180°。
两个叁键碳原子与其所连接的两个原子在同一条直线上。
(4)苯及苯的同系物:A) 通式:CnH2n—6(n≥6);代表物:B)结构特点:苯分子中键角为120°,平面正六边形结构,6个C原子和6个H原子共平面。
C)化学性质:①取代反应(与液溴、HNO3、H2SO4等)(5)醇类:A) 官能团:—OH(醇羟基);代表物:CH3CH2OH、HOCH2CH2OHB) 结构特点:羟基取代链烃分子(或脂环烃分子、苯环侧链上)的氢原子而得到的产物。
结构与相应的烃类似。
C) 化学性质:(与官能团直接相连的碳原子称为α碳原子,与α碳原子相邻的碳原子称为β碳原子,依次类推。
与α碳原子、β碳原子、……相连的氢原子分别称为α氢原子、β氢原子、……)④酯化反应(跟羧酸或含氧无机酸)(6)醛酮B) 结构特点:醛基或羰基碳原子伸出的各键所成键角为120°,该碳原子跟其相连接的各原子在同一平面上。
C) 化学性质:(7)羧酸3、常见糖类、蛋白质和油脂的结构和性质(1)单糖A) 代表物:葡萄糖、果糖(C6H12O6)B) 结构特点:葡萄糖为多羟基醛、果糖为多羟基酮C) 化学性质:①葡萄糖类似醛类,能发生银镜反应、费林反应等;②具有多元醇的化学性质。
选修5-有机化学基础基础知识梳理PPT

目 录
• 有机化学概述 • 烃类化合物 • 烃的衍生物 • 有机合成与反应机理 • 有机化学在生活中的应用 • 实验技能与安全意识培养
01 有机化学概述
有机化学定义与发展
定义
有机化学是研究有机化合物的结 构、性质、合成、反应机理以及 应用的一门科学。
发展历程
从18世纪末开始,随着化学学科 的不断发展,有机化学逐渐从无 机化学中分离出来,成为一门独 立的学科。
生物医用材料
如可生物降解高分子材料,用于手术缝合线、骨 修复材料等。
农业领域中的有机化学应用
01
02
03
04
农药
用于防治农作物病虫害,保障 粮食产量和质量安全。
化肥
提供植物生长所需的氮、磷、 钾等营养元素,促进作物生长
。
植物生长调节剂
通过调节植物内源激素水平, 促进或抑制植物生长和发育。
土壤改良剂
不对称合成法
通过手性辅助剂或手性催化剂,合成具有特定立体构型的手性化合 物。
反应机理类型及特点
取代反应机理
涉及原子或原子团的替换,如 卤代、硝化、磺化等反应。
加成反应机理
发生在不饱和键上,如烯烃、 炔烃的加成反应。
消除反应机理
从一个有机分子中消去两个原 子或原子团的反应,如醇的脱 水、卤代烃的脱卤化氢等。
醛、酮、醌
醛的分类和命名
根据醛基所连碳原子的类型,醛可分 为甲醛、乙醛和其他醛类。命名时, 将醛基作为取代基进行命名。
醛的物理性质
大多数醛是无色透明的液体或固体, 具有刺激性气味。低级醛具有还原性 ,能被弱氧化剂氧化成羧酸。
醛的化学性质
醛的主要化学性质包括氧化反应、还 原反应、缩合反应和歧化反应等。其 中,氧化反应是醛被氧化成羧酸的过 程;还原反应是醛被还原成醇的过程; 缩合反应是两个醛分子在碱性条件下 生成β-羟基醛的过程;歧化反应是醛 在特定条件下同时发生氧化和还原的 过程。
(完整版)高中化学选修五——有机化学基础入门(知识点总结),推荐文档
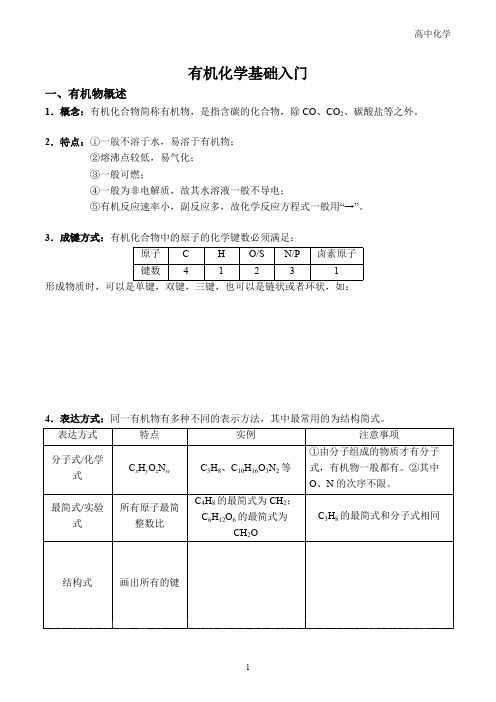
绝大多数情况下,有机化学方程式中除燃烧用分子式外,其它方程式有机物一律写结构简式。
(2)系统命名法:适用于任何有机物的系统的命名方法。
步骤:①选主链。
原则:a、碳链最长;b、一样长时,支链最多。
如:②对主链碳编号。
原则:a、从支链近端开始编号;b、一样时,甲基优先。
如:③命名。
原则:a、先简单基团再复杂基团;b、阿拉伯数字之间用“,”相隔,阿拉伯数字和汉字之间用“-”相连;如:4.等效氢与卤代物种类数(1)等效氢:即相同效果的氢。
因为有机物是空间结构,故其在纸平面上只是投影,凡是在空间中一样的H原子即称为等效氢,它们被卤素取代后的产物相同。
等效氢有两种:①对称;②旋转重合。
如:(2)一卤代物:即用一个卤素原子取代一个氢原子剩下的有机物。
有几种等效氢就有几种一卤代物。
如:(3)二卤代物:即一卤代物的一卤代物。
方法是先用等效氢找出一卤代物,再找它的一卤代物。
如:(4)多卤代物:若烷烃有n个氢,则其m卤代物(m<n)种类数与(n-m)卤代物种类数相同。
如:C3H8的二氯代物和六氯代物种类数都是4种,因为前者是找两个氯的相对位置,后者是找两个氢的相对位置。
5.同分异构体的书写:方法是先写碳骨架,再补充氢原子(利用碳四个键),具体规则为:①主链碳由长到短;②支链碳由中间到两边,注意避免重复;不能改变主链碳数;③两个支链时,先定一个,再定另一个。
如:6.有机物的物理性质(1)溶解性:有机物除了醇、醛、酸外基本均不溶于水,有机物和有机物是互溶的。
(2)密度:有机物密度一般比水小,比水大的常见物质是:CCl4、溴苯、硝基苯等。
(3)熔沸点:同系物随相对分子质量增大,熔沸点升高。
如烷烃随碳数增加,熔沸点增大;烷烃的同分异构体之间,支链越多,熔沸点越低,如正戊烷>异戊烷>新戊烷。
常温下碳数小于等于4的烃为气态,烃的含氧衍生物仅HCHO(甲醛)为气体。
(4)颜色:高中阶段的有机物一般为无色。
7.烷烃的化学性质(1)燃烧:有机物完全燃烧产物均为CO2、H2O等;不完全燃烧会产生黑烟(碳单质)、CO 等。
化学选修5有机化学基础知识点总结

化学选修5有机化学基础知识点总结有机化学是研究有机化合物的结构、性质、合成、反应机理及其在化学生物学和材料科学等方面的应用的一门学科。
下面是有机化学选修5的基础知识点总结。
1.化学键:-共价键:包括σ键和π键,分别是由轨道的轴对称与轨道与螺旋轨道相叠加而形成的。
-极性键:由于原子电负性差异而导致电子密度偏移的键,包括极性共价键和离子键。
2.化学键的构型:-杂化轨道:通过原子轨道的线性组合形成的新轨道,描述分子中的化学键的构型。
- sp 杂化轨道:由 s 轨道和 p 轨道的线性组合形成,形成线性构型。
- sp² 杂化轨道:由 s 轨道和两个 p 轨道的线性组合形成,形成平面三角构型。
- sp³ 杂化轨道:由 s 轨道和三个 p 轨道的线性组合形成,形成四面体构型。
3.分子结构和分子式:-线性结构:分子中原子按一条直线排列。
-支链结构:分子中主链上有侧链延伸。
-环状结构:分子形成环状结构。
4.反应机理:-自由基试剂的反应机理:自由基反应通过自由基的生成、扩散和重组来进行。
-亲电试剂的反应机理:亲电试剂与亲核试剂发生电子转移,生成新的化学键。
-赋电试剂的反应机理:赋电试剂通过配体的脱离或取代发生反应。
5.碳的化学性质:-碳的自由旋转:碳与碳之间的单键可以自由旋转,从而改变分子的构型。
-碳的键强度:碳与碳之间的键强度较弱,易发生断裂和形成新的键。
6.化学键形成与断裂:-电流与溶剂的效应:当溶剂对电流有溶剂化作用时,正电荷离子的形成速率加快。
-酸性溶液中的电离:酸性溶液中的电解质能发生电离,产生正负离子。
7.环状化合物的合成和反应:-还原反应:环状化合物可以通过添加氢或还原试剂来进行还原反应。
-氧化反应:环状化合物可以通过添加氧或氧化剂来进行氧化反应。
-变环反应:环状化合物可以通过改变分子构型来进行变环反应。
8.有机官金属化学:-有机官金属化合物的合成:通过将有机化合物与金属试剂进行反应来合成有机官金属化合物。
高二化学选修5《有机化学基础》知识点整理

高二化学选修5《有机化学基础》知识点整理班级姓名学号一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(....-.29.8....CCl....℃.)....2.F.2.,沸点为..3.Cl..,.沸点为...-.24.2.....CH....℃.).氟里昂(氯乙烯(...HCHO....,沸点为....℃.).甲醛(....-.21..℃.)...2.==CHCl....-.13.9....CH......,沸点为氯乙烷(....℃.).一溴甲烷(CH3Br,沸点为3.6℃)....12.3....CH..2.C.l.,沸点为..3.CH四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)甲乙醚(CH3OC2H5,沸点为10.8℃)环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
(完整版)人教版高中化学选修5有机化学基础知识点,推荐文档

醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
*⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、氟代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2==CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃),沸点为环己烷三硝基甲苯(部分被空气中氧气所氧化变质的苯酚为粉红色;三溴苯酚许多有机物具有特殊的气味,但在中学阶段只需要了解下列有机物的气味:☆甲烷无味☆乙烯稍有甜味(植物生长的调节剂)☆液态烯烃汽油的气味☆乙炔无味☆苯及其同系物芳香气味,有一定的毒性,尽量少吸入。
人教版高中化学选修5有机化学基础知识点

人教版高中化学选修5有机化学基础知识点有机化学基础第一章认识有机化合物第一节有机化合物的分类第二节有机化合物的结构特点第三节有机化合物的命名第四节研究有机化合物的一般步骤和方法归纳与整理复习题第二章烃和卤代烃第一节脂肪烃第二节芳香烃第三节卤代烃归纳与整理复习题第三章烃的含氧衍生物第一节醇酚第二节醛第三节羧酸酯第四节有机合成归纳与整理复习题第四章生命中的基础有机化学物质第一节油脂第二节糖类第三节蛋白质和核酸归纳与整理复习题第五章进入合成有机高分子化合物的时代第一节合成高分子化合物的基本方法第二节应用广泛的高分子材料第三节功能高分子材料归纳与整理复习题结束语——有机化学与可持续发展高二化学选修5《有机化学基础》知识点整理2010-2-26一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
高二化学选修5有机化学基础知识点整理

高二化学选修5有机化学基础知识点整理
有机物的结构与性质
原子:—X官能团原子团(基):—OH、—CHO(醛基)、—COOH(羧基)、C6H5—等化学键:C=C、—C≡C—
2、常见的各类有机物的官能团,结构特点及主要化学性质(1)烷烃
A)官能团:无;通式:CnH2n+2;代表物:CH4
B)结构特点:键角为109°28′,空间正四面体分子。
烷烃分子
中的每个C原子的四个价键也都如此。
C)化学性质:①取代反应(与卤素单质、在光照条件下)
CH4+Cl2光CH3Cl+HCl点燃CH3,Cl+Cl2光CH2Cl2+HCl
1、有机化合物分子的表示法:结构式、投影式;
2、有机化合物中的共价键:碳原子的杂化轨道、σ键和π键;
3、共价键的属性:键长、键角、键能、极性和极化度;
5、烷烃的结构:sp3杂化;同系列;烷基的概念;同分异构现象;伯、仲、叔、季碳原子的概念;烷烃分子的构象:Newmann投影式;
6、烷烃的命名:普通命名法及系统命名法;
7、烷烃的物理性质;
8、烷烃的化学性质:自由基取代反应历程(均裂、链锁反应的概念及能量曲线、过渡态及活化能);
1、烷烃的命名遵循:链长、基多、序数低。
2、烷烃的碳原子都是sp3杂化,四面体结构,连1个C-C的碳原子为伯碳、2个C-C为仲碳,3个C-C的为叔碳,4个C-C的为季碳,与对应碳原子相连的H为伯、仲、叔H。
3、烷烃的光照卤代是游离基机理,叔H最活泼,叔游离基最稳定。
4、三元环由于环张力而容易开环:与H2、HX、X2反应,四元环活泼性次之,五元环基本不开环。
5、环己烷最稳定的构象为椅式构象,大基团在e键上多的构象是优势构象。
选修5有机化学重要知识点总结

选修5有机化学重要知识点总结work Information Technology Company.2020YEAR高二化学选修5《有机化学基础》知识点整理一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:① 乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
② 苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
*⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、氟代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:① 烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态② 衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2==CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃)一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)*甲乙醚(CH3OC2H5,沸点为10.8℃)*环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
选修5《有机化学基础》知识点归纳

选修5《有机化学基础》知识点归纳一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:①乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
②苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
④有的淀粉、蛋白质可溶于水形成胶体..。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂化反应中也有此操作)。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:烃、一氯代烃、氟代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:①烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态②衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)甲醛(HCHO,沸点为-21℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学选修5《有机化学基础》知识点总结一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
(3)具有特殊溶解性的:① 乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。
例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。
② 苯酚:室温下,在水中的溶解度是9.3g(属可溶),易溶于乙醇等有机溶剂,当温度高于65℃时,能与水混溶,冷却后分层,上层为苯酚的水溶液,下层为水的苯酚溶液,振荡后形成乳浊液。
苯酚易溶于碱溶液和纯碱溶液,这是因为生成了易溶性的钠盐。
③乙酸乙酯在饱和碳酸钠溶液中更加难溶,同时饱和碳酸钠溶液还能通过反应吸收挥发出的乙酸,溶解吸收挥发出的乙醇,便于闻到乙酸乙酯的香味。
蛋白质在浓轻金属盐(包括铵盐)溶液中溶解度减小,会析出(即盐析,皂④有的淀粉、蛋白质可溶于水形成胶体..化反应中也有此操作)。
但在稀轻金属盐(包括铵盐)溶液中,蛋白质的溶解度反而增大。
⑤线型和部分支链型高聚物可溶于某些有机溶剂,而体型则难溶于有机溶剂。
⑥氢氧化铜悬浊液可溶于多羟基化合物的溶液中,如甘油、葡萄糖溶液等,形成绛蓝色溶液。
2.有机物的密度(1)小于水的密度,且与水(溶液)分层的有:各类烃、一氯代烃、氟代烃、酯(包括油脂)(2)大于水的密度,且与水(溶液)分层的有:多氯代烃、溴代烃(溴苯等)、碘代烃、硝基苯3.有机物的状态[常温常压(1个大气压、20℃左右)](1)气态:① 烃类:一般N(C)≤4的各类烃注意:新戊烷[C(CH3)4]亦为气态② 衍生物类:一氯甲烷(CH3Cl,沸点为-24.2℃)氟里昂(CCl2F2,沸点为-29.8℃)氯乙烯(CH2==CHCl,沸点为-13.9℃)甲醛(HCHO,沸点为-21℃)氯乙烷(CH3CH2Cl,沸点为12.3℃)一溴甲烷(CH3Br,沸点为3.6℃)四氟乙烯(CF2==CF2,沸点为-76.3℃)甲醚(CH3OCH3,沸点为-23℃)*甲乙醚(CH3OC2H5,沸点为10.8℃)*环氧乙烷(,沸点为13.5℃)(2)液态:一般N(C)在5~16的烃及绝大多数低级衍生物。
如,己烷CH3(CH2)4CH3环己烷甲醇CH3OH 甲酸HCOOH溴乙烷C2H5Br 乙醛CH3CHO 溴苯C6H5Br 硝基苯C6H5NO2★特殊:不饱和程度高的高级脂肪酸甘油酯,如植物油脂等在常温下也为液态(3)固态:一般N(C)在17或17以上的链烃及高级衍生物。
如,石蜡C16以上的烃饱和程度高的高级脂肪酸甘油酯,如动物油脂在常温下为固态★特殊:苯酚(C6H5OH)、苯甲酸(C6H5COOH)、氨基酸等在常温下亦为固态4.有机物的颜色☆绝大多数有机物为无色气体或无色液体或无色晶体,少数有特殊颜色,常见的如下所示:☆三硝基甲苯(俗称梯恩梯TNT)为淡黄色晶体;☆部分被空气中氧气所氧化变质的苯酚为粉红色;☆2,4,6—三溴苯酚为白色、难溶于水的固体(但易溶于苯等有机溶剂);☆苯酚溶液与Fe3+(aq)作用形成紫色[H3Fe(OC6H5)6]溶液;☆多羟基有机物如甘油、葡萄糖等能使新制的氢氧化铜悬浊液溶解生成绛蓝色溶液;☆淀粉溶液(胶)遇碘(I2)变蓝色溶液;☆含有苯环的蛋白质溶胶遇浓硝酸会有白色沉淀产生,加热或较长时间后,沉淀变黄色。
5.有机物的气味许多有机物具有特殊的气味,但在中学阶段只需要了解下列有机物的气味:☆甲烷(无味)☆乙烯稍有甜味(植物生长的调节剂)☆液态烯烃汽油的气味☆乙炔无味☆苯及其同系物芳香气味,有一定的毒性,尽量少吸入。
☆一卤代烷不愉快的气味,有毒,应尽量避免吸入。
☆二氟二氯甲烷(氟里昂)无味气体,不燃烧。
☆ C4以下的一元醇有酒味的流动液体☆C5~C11的一元醇不愉快气味的油状液体☆C12以上的一元醇无嗅无味的蜡状固体☆乙醇特殊香味☆乙二醇甜味(无色黏稠液体)☆丙三醇(甘油)甜味(无色黏稠液体)☆苯酚特殊气味☆乙醛刺激性气味☆乙酸强烈刺激性气味(酸味)☆低级酯芳香气味☆丙酮令人愉快的气味二、重要的反应1.能使溴水(Br2/H2O)褪色的物质(1)有机物①通过加成反应使之褪色:含有、—C≡C—的不饱和化合物②通过取代反应使之褪色:酚类注意:苯酚溶液遇浓溴水时,除褪色现象之外还产生白色沉淀。
③ 通过氧化反应使之褪色:含有—CHO(醛基)的有机物(有水参加反应)注意:纯净的只含有—CHO(醛基)的有机物不能使溴的四氯化碳溶液褪色④通过萃取使之褪色:液态烷烃、环烷烃、苯及其同系物、饱和卤代烃、饱和酯(2)无机物①通过与碱发生歧化反应3Br2 + 6OH- == 5Br- + BrO3- + 3H2O或Br2 + 2OH- == Br- + BrO- + H2O②与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、I-、Fe2+2.能使酸性高锰酸钾溶液KMnO4/H+褪色的物质(1)有机物:含有、—C≡C—、—OH(较慢)、—CHO的物质与苯环相连的侧链碳碳上有氢原子的苯的同系物(与苯不反应)(2)无机物:与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、Br-、I-、Fe2+3.与Na反应的有机物:含有—OH、—COOH的有机物、—COOH的有机物反应加热时,能与卤代烃、酯反应(取代反应)与NaOH反应的有机物:常温下,易与含有酚羟基...与Na2CO3反应的有机物:含有酚.羟基的有机物反应生成酚钠和NaHCO3;含有—COOH的有机物反应生成羧酸钠,并放出CO2气体;含有—SO3H的有机物反应生成磺酸钠并放出CO2气体。
与NaHCO3反应的有机物:含有—COOH、—SO3H的有机物反应生成羧酸钠、磺酸钠并放出等物质的量的CO2气体。
4.既能与强酸,又能与强碱反应的物质(1)2Al + 6H+ == 2 Al3+ + 3H2↑2Al + 2OH- + 2H2O == 2 AlO2- + 3H2↑(2)Al2O3 + 6H+ == 2 Al3+ + 3H2O Al2O3 + 2OH- == 2 AlO2- + H2O(3)Al(OH)3 + 3H+ == Al3+ + 3H2O Al(OH)3 + OH- == AlO2- + 2H2O(4)弱酸的酸式盐,如NaHCO3、NaHS等等NaHCO3 + HCl == NaCl + CO2↑+ H2O NaHCO3 + NaOH == Na2CO3 + H2ONaHS + HCl == NaCl + H2S↑NaHS + NaOH == Na2S + H2O(5)弱酸弱碱盐,如CH3COONH4、(NH4)2S等等2CH3COONH4 + H2SO4 == (NH4)2SO4 + 2CH3COOH CH3COONH4 + NaOH == CH3COONa + NH3↑+ H2O (NH4)2S + H2SO4 == (NH4)2SO4 + H2S↑(NH4)2S +2NaOH == Na2S + 2NH3↑+ 2H2O(6)氨基酸,如甘氨酸等H2NCH2COOH + HCl → HOOCCH2NH3Cl H2NCH2COOH + NaOH → H2NCH2COONa + H2O(7)蛋白质蛋白质分子中的肽链的链端或支链上仍有呈酸性的—COOH和呈碱性的—NH2,故蛋白质仍能与碱和酸反应。
5.银镜反应的有机物(1)发生银镜反应的有机物:含有—CHO的物质:醛、甲酸、甲酸盐、甲酸酯、还原性糖(葡萄糖、麦芽糖等)(2)银氨溶液[Ag(NH3)2OH](多伦试剂)的配制:向一定量2%的AgNO3溶液中逐滴加入2%的稀氨水至刚刚产生的沉淀恰好完全溶解消失。
(3)反应条件:碱性、水浴加热.......若在酸性条件下,则有Ag(NH3)2+ + OH - + 3H+ == Ag+ + 2NH4+ + H2O而被破坏。
(4)实验现象:①反应液由澄清变成灰黑色浑浊;②试管内壁有银白色金属析出(5)有关反应方程式:AgNO3 + NH3·H2O == AgOH↓ + NH4NO3AgOH + 2NH3·H2O == Ag(NH3)2OH + 2H2O 银镜反应的一般通式:RCHO + 2Ag(NH3)2OH 2 Ag↓+ RCOONH4 + 3NH3 + H2O【记忆诀窍】:1—水(盐)、2—银、3—氨甲醛(相当于两个醛基):HCHO + 4Ag(NH3)2OH4Ag↓+ (NH4)2CO3 + 6NH3 + 2H2O乙二醛:OHC-CHO + 4Ag(NH3)2OH4Ag↓+ (NH4)2C2O4 + 6NH3 + 2H2O甲酸:HCOOH + 2 Ag(NH3)2OH 2 Ag↓+ (NH4)2CO3 + 2NH3 + H2O(过量)葡萄糖:CH2OH(CHOH)4CHO +2Ag(NH3)2OH2Ag↓+CH2OH(CHOH)4COONH4+3NH3 + H2O(6)定量关系:—CHO~2Ag(NH)2OH~2 Ag HCHO~4Ag(NH)2OH~4 Ag6.与新制Cu(OH)2悬浊液(斐林试剂)的反应(1)有机物:羧酸(中和)、甲酸(先中和,但NaOH仍过量,后氧化)、醛、还原性糖(葡萄糖、麦芽糖)、甘油等多羟基化合物。
(2)斐林试剂的配制:向一定量10%的NaOH溶液中,滴加几滴2%的CuSO4溶液,得到蓝色絮状悬浊液(即斐林试剂)。
(3)反应条件:碱过量、加热煮沸........(4)实验现象:①若有机物只有官能团醛基(—CHO),则滴入新制的氢氧化铜悬浊液中,常温时无变化,加热煮沸后有(砖)红色沉淀生成;②若有机物为多羟基醛(如葡萄糖),则滴入新制的氢氧化铜悬浊液中,常温时溶解变成绛蓝色溶液,加热煮沸后有(砖)红色沉淀生成;(5)有关反应方程式:2NaOH + CuSO4 == Cu(OH)2↓+ Na2SO4RCHO + 2Cu(OH)2RCOOH + Cu2O↓+ 2H2OHCHO + 4Cu(OH)2CO2 + 2Cu2O↓+ 5H2O OHC-CHO + 4Cu(OH)2HOOC-COOH + 2Cu2O↓+ 4H2OHCOOH + 2Cu(OH)2CO2 + Cu2O↓+ 3H2OCH 2OH(CHOH)4CHO + 2Cu(OH)2CH 2OH(CHOH)4COOH + Cu 2O↓+ 2H 2O(6)定量关系:—COOH ~½ Cu(OH)2~½ Cu 2+(酸使不溶性的碱溶解)—CHO ~2Cu(OH)2~Cu 2OHCHO ~4Cu(OH)2~2Cu 2O7.能发生水解反应的有机物是:卤代烃、酯、糖类(单糖除外)、肽类(包括蛋白质)。
