初中化学中考重难点讲义总结:发光发热现象的变化
【化学】中考科学中考复习化学部分考点归纳与点拨
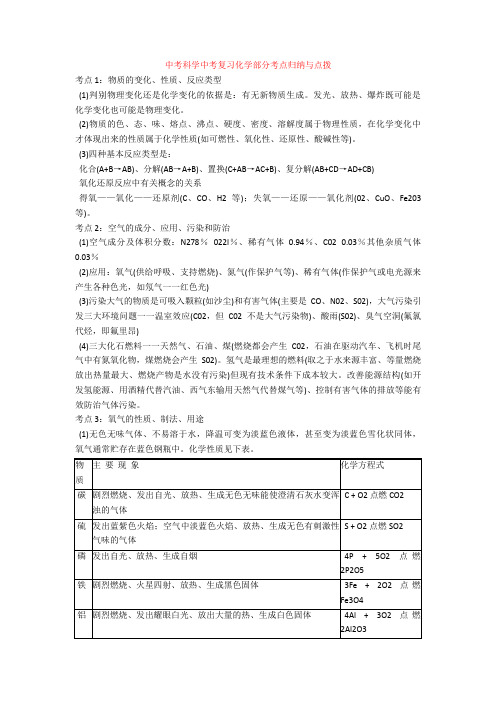
中考科学中考复习化学部分考点归纳与点拨考点1:物质的变化、性质、反应类型(1)判别物理变化还是化学变化的依据是:有无新物质生成。
发光、放热、爆炸既可能是化学变化也可能是物理变化。
(2)物质的色、态、味、熔点、沸点、硬度、密度、溶解度属于物理性质,在化学变化中才体现出来的性质属于化学性质(如可燃性、氧化性、还原性、酸碱性等)。
(3)四种基本反应类型是:化合(A+B→AB)、分解(AB→A+B)、置换(C+AB→AC+B)、复分解(AB+CD→AD+CB)氧化还原反应中有关概念的关系得氧——氧化——还原剂(C、CO、H2等);失氧——还原——氧化剂(02、CuO、Fe203等)。
考点2:空气的成分、应用、污染和防治(1)空气成分及体积分数:N278%022l%、稀有气体0.94%、C02 0.03%其他杂质气体0.03%(2)应用:氧气(供给呼吸、支持燃烧)、氮气(作保护气等)、稀有气体(作保护气或电光源来产生各种色光,如氖气一一红色光)(3)污染大气的物质是可吸入颗粒(如沙尘)和有害气体(主要是CO、N02、S02),大气污染引发三大环境问题一一温室效应(C02,但C02不是大气污染物)、酸雨(S02)、臭气空洞(氟氯代烃,即氟里昂)(4)三大化石燃料一一天然气、石油、煤(燃烧都会产生C02,石油在驱动汽车、飞机时尾气中有氮氧化物,煤燃烧会产生S02)。
氢气是最理想的燃料(取之于水来源丰富、等量燃烧放出热量最大、燃烧产物是水没有污染)但现有技术条件下成本较大。
改善能源结构(如开发氢能源、用酒精代替汽油、西气东输用天然气代替煤气等)、控制有害气体的排放等能有效防治气体污染。
考点3:氧气的性质、制法、用途(1)无色无味气体、不易溶于水,降温可变为淡蓝色液体,甚至变为淡蓝色雪化状同体,氧气通常贮存在蓝色钢瓶中。
化学性质见下表。
2KMnO4 K2MnO4 + MnO2 + O2↑(固固加热型)(组、检、装、夹、点、收、移、熄)2H2O2 H2O+ O2 ↑ (固液不加热型)(Mn02作催化剂“一变两不变”)可用排水法(不易溶于水)或向上捧空气法(密度比空气大,32>29)收集工业上用分离液态空气的方法得到氧气(氧气的沸点比氮气高.物理变化)。
发光发热的物理变化

发光发热的物理变化
发光发热是一种物理变化,指物体在受到能量激发后产生可见光
与热能的过程。
当物体中的分子或原子受到能量激发,其原子能级发
生变化,电子跃迁至较高的能级,并随后返回基态时,释放出能量。
这种能量以光子的形式辐射出来,产生可见光。
同时,物体中分子的
振动与运动加剧,引起温度的升高,产生热能。
这两种能量形式的释
放与转化导致物体发出光亮且发热的现象。
要实现发光发热的物理变化,需要能量输入,以激发物体内部的
分子或原子。
这种能量输入可以是电能、光能、热能等,通过与物体
相互作用转化为物体内部的激发能量。
激发能量使得物体内部的原子
与分子的电子能级发生变化,使得其跃迁至较高的能级。
当电子跃迁
回基态时,能量以光子形式辐射出来,产生可见光。
同时,原子与分
子的运动与振动也会加剧,转化为热能,使物体发热。
物体的发光发热过程受到多种因素的影响,如物体的组成成分、
能量输入的类型与强度等。
不同材料具有不同的发光发热特性,因此
其发光发热的表现也各异。
一些物体在特定条件下会表现出强烈的发
光发热效应,如荧光体、发光二极管等。
这些材料在受到激发能量后,能够产生显著的发光发热效应,应用于照明、显示等领域。
综上所述,发光发热是一种以能量转化为原理的物理变化,利用
外界能量激活物体内部的原子与分子,使其能级发生变化,并释放光
子和热能。
这种现象在实际应用中具有广泛的意义与应用价值。
2024年中考化学考点全透视—物质的变化、性质、用途及化学反应类型(考前必看)

2024年中考化学考点全透视—物质的变化、性质、用途及化学反应类型(考前必看)考点1物理变化和化学变化物理变化化学变化定义没有生成其他物质的变化叫物理变化生成其他物质的变化叫化学变化本质区别是否有新物质生成常见现象物质的状态、形状可能发生变化,可能有发光、放热等现象出现颜色改变、放出气体、生成沉淀等,并吸热、放热、发光等(一定伴随能量改变)微观实质构成物质的分子是否发生变化物理变化分子不改变,化学变化分子发生改变联系发生化学变化时一定同时发生物理变化,而发生物理变化时不一定同时发生化学变化。
举例:蜡烛燃烧时一定伴随蜡烛的熔化。
实例性状改变:破碎、弯曲、拉成丝、压成片等状态改变:熔化、凝固、汽化、液化、升华、凝华、铸造等其他:灯泡通电发光、活性炭吸附色素、金属导电、压强过大导致爆炸(气球、轮胎、高压锅)燃烧变化:物质燃烧、汽油火药等爆炸变质变化:发酵、酿酒、发霉、腐烂等锈蚀变化:金属生锈其他变化:光合呼吸作用、杀菌消毒、物质分解等考点2物理性质和化学性质物理性质化学性质定义物质不需要发生化学变化就可以表现出来的性质物质在化学变化中表现出来的性质区别某种性质是否需要经过化学变化才能表现出来注意物质的性质受外界条件影响,在描述物质性质时注明条件。
(如液体沸点受大气压影响)实例颜色、状态、气味;硬度、密度、燃点、沸点、熔点;溶解性、挥发性、导电性、导热性、吸附性等可燃性、助燃性;氧化性、还原性;稳定性、活泼性;酸性、碱性、毒性等考点3物质性质和用途关系例:木炭具有可燃性,可以发生燃烧变化,生活中用于作燃料。
考点4四种基本化学反应类型的判断类型定义代表式特点化合价变化备注化合反应由两种或两种以上的物质生成另一种物质的反应A+B→C多变一可能变化(就某些反应中某些元素而言)反应物A 、B 既可代表单质,又可代表化合物分解反应由一种物质生成两种或两种以上其他物质的反应A→B+C一变多可能变化(就某些反应中某些元素而言)生成物中的B 、C 既可代表单质,又可代表化合物置换反应由一种单质跟一种化合物反应生成另一种单质和另一种化合物的反应A+BC→B+AC一换一肯定变化(就所有反应中某些元素而言)反应范围:①金属和酸;②金属和盐;③氢气、碳和金属氧化物;④碳和水蒸气等复分解反应由两种化合物互相交换成分,生成另外两种化合物的反应AB+CD→AD+BC相互交换肯定不变(就所有反应中所有元素而言)反应范围:①酸+碱;②酸+盐;③酸+碱性氧化物;④盐+碱;⑤盐+盐(1)关于氧化还原反应及中和反应初中阶段根据在化学反应中得氧或失氧的情况,将化学反应分为氧化反应和还原反应。
初中化学第一单元重难点知识(整理版),附例题!

初中化学第一单元重难点知识重点一:物理变化与化学变化1、化学变化和物理变化常常同时发生。
注意:发生化学变化时一定同时发生物理变化,而发生物理变化时不一定同时发生化学变化。
解析:如蜡烛燃烧时,除了生成了二氧化碳和水,同时蜡烛融化了。
2、如何辨析物理变化和化学变化我们常用颜色改变、放出气体、生成沉淀等,并吸热、放热、发光等现象来帮助辨析是否发生化学反应,但有这些现象不一定发生了化学反应。
比如:氧气由气态变为液态,颜色变为淡蓝色,物理变化。
水的沸腾,放出气体,物理变化。
浑浊的水静止一段时间后,生成沉淀,物理变化。
水的三态变化,要吸热放热,物理变化。
灯泡通电发光,物理变化。
所以物理变化和化学变化的辨析,其本质还是要看是否生成了新物质。
例题:(2020安徽中考)《天工开物》是我国古代科技发展的智慧结晶,书中描述的下列制瓷工序涉及化学变化的是()A. 烧裂矿石B. 粉碎矿石C. 淘洗矿粉D. 取泥制坯【解析】A、烧裂矿石过程中存在燃烧,燃烧一定会产生新的物质,烧裂矿石涉及化学变化,符合题意;B、粉碎知识将大块矿石变为小颗粒矿石,无新物质的生成,为物理变化,不符合题意;C、淘洗知识将矿粉中可以溶解的部分溶解,溶解时物理变化,不符合题意;D、在制坯过程中知识将泥块和矿粉混合,并改变形状,此过程中无化学变化,不符合题意。
故选A。
重点二:物理性质与化学性质1、性质决定用途,用途体现性质。
性质决定变化,变化反映性质。
2、物理变化中表现出来的性质一定是物理性质,但物理性质不一定必须通过物理变化表现出来,如物质的颜色、状态等不需要通过变化就表现出来的性质也处于物理性质。
例题:(2019恩施州中考)下列属于物质化学性质的是()A.颜色、状态B.密度、硬度C.可燃性、酸碱性D.熔点、沸点【答案】选C。
重点三:对蜡烛及其燃烧的探究例题:某同学对蜡烛(主要成分是石蜡)及其燃烧进行如下探究。
请填写下列空格。
(1)取一支蜡烛,用小刀切下一小块把它放入水中,蜡烛浮在水面上。
【化学】中考科学中考复习化学部分考点归纳与点拨
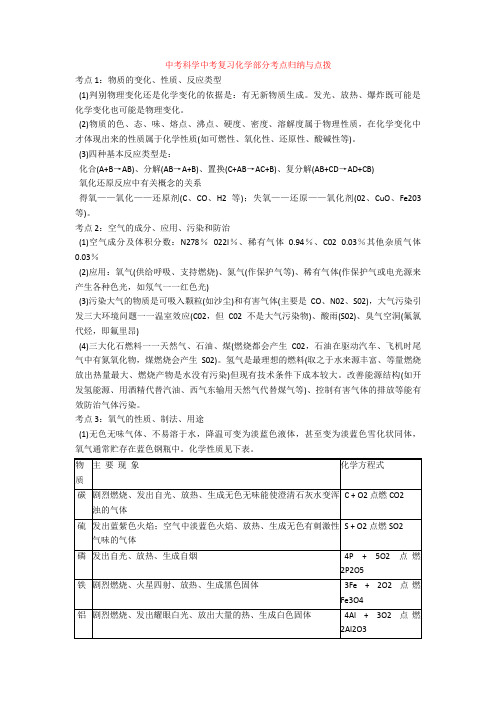
中考科学中考复习化学部分考点归纳与点拨考点1:物质的变化、性质、反应类型(1)判别物理变化还是化学变化的依据是:有无新物质生成。
发光、放热、爆炸既可能是化学变化也可能是物理变化。
(2)物质的色、态、味、熔点、沸点、硬度、密度、溶解度属于物理性质,在化学变化中才体现出来的性质属于化学性质(如可燃性、氧化性、还原性、酸碱性等)。
(3)四种基本反应类型是:化合(A+B→AB)、分解(AB→A+B)、置换(C+AB→AC+B)、复分解(AB+CD→AD+CB)氧化还原反应中有关概念的关系得氧——氧化——还原剂(C、CO、H2等);失氧——还原——氧化剂(02、CuO、Fe203等)。
考点2:空气的成分、应用、污染和防治(1)空气成分及体积分数:N278%022l%、稀有气体0.94%、C02 0.03%其他杂质气体0.03%(2)应用:氧气(供给呼吸、支持燃烧)、氮气(作保护气等)、稀有气体(作保护气或电光源来产生各种色光,如氖气一一红色光)(3)污染大气的物质是可吸入颗粒(如沙尘)和有害气体(主要是CO、N02、S02),大气污染引发三大环境问题一一温室效应(C02,但C02不是大气污染物)、酸雨(S02)、臭气空洞(氟氯代烃,即氟里昂)(4)三大化石燃料一一天然气、石油、煤(燃烧都会产生C02,石油在驱动汽车、飞机时尾气中有氮氧化物,煤燃烧会产生S02)。
氢气是最理想的燃料(取之于水来源丰富、等量燃烧放出热量最大、燃烧产物是水没有污染)但现有技术条件下成本较大。
改善能源结构(如开发氢能源、用酒精代替汽油、西气东输用天然气代替煤气等)、控制有害气体的排放等能有效防治气体污染。
考点3:氧气的性质、制法、用途(1)无色无味气体、不易溶于水,降温可变为淡蓝色液体,甚至变为淡蓝色雪化状同体,氧气通常贮存在蓝色钢瓶中。
化学性质见下表。
2KMnO4 K2MnO4 + MnO2 + O2↑(固固加热型)(组、检、装、夹、点、收、移、熄)2H2O2 H2O+ O2 ↑ (固液不加热型)(Mn02作催化剂“一变两不变”)可用排水法(不易溶于水)或向上捧空气法(密度比空气大,32>29)收集工业上用分离液态空气的方法得到氧气(氧气的沸点比氮气高.物理变化)。
中考化学知识点:燃烧与发光,放热,火焰之间的关系

中考化学知识点:燃烧与发光,放热,火焰之间的关系(学习版)编制人:__________________审核人:__________________审批人:__________________编制学校:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的教育资料,如语文资料、数学资料、英语资料、物理资料、化学资料、地理资料、政治资料、历史资料、艺术资料、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor.I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!In addition, this shop provides various types of educational materials for everyone, such as language materials, mathematics materials, English materials, physical materials, chemical materials, geographic materials, political materials, historical materials, art materials,other materials, etc. Please pay attention to the data format and writing method!中考化学知识点:燃烧与发光,放热,火焰之间的关系新一轮中考复习备考周期正式开始,本店铺为各位初三考生整理了各学科的复习攻略,主要包括中考必考点、中考常考知识点、各科复习方法、考试答题技巧等内容,帮助各位考生梳理知识脉络,理清做题思路,希望各位考生可以在考试中取得优异成绩!下面是《2022中考化学知识点:燃烧与发光,放热,火焰之间的关系》,仅供参考!燃烧与发光,放热,火焰之间的关系:(1)燃烧与发光,放热的关系燃烧一定发光,放热,但发光,放热的变化不一定是化学变化,因而不一定是燃烧,如原子弹,氢弹的爆炸。
2021中考复习人教版九年级化学上册第三单元 课题1 ---2 重难点归纳

课题一物质的变化和性质知识点一:物质的变化分为物理变化和化学变化1.物理变化①定义:没有生成其他物质的变化叫物理变化。
例如:冰融化为水,水蒸发变成水蒸气,胆矾的研碎,汽油挥发,碘升华,蜡烛融化等②特征:没有新物质生成。
③本质:构成物质的粒子本身没有变,主要是指形状改变或三态变化。
④伴随现象:扩散、聚集、膨胀、压缩、挥发、升华、摩擦生热、升温、发光、活性炭吸附等都是物理变化。
2.化学变化①定义:生成了其他物质的变化叫化学变化,又叫化学反应。
②特征:有新物质生成。
③本质:分子或粒子本身被破坏,分裂成原子,原子又重新组合成新物质的分子或粒子。
④伴随现象:颜色改变、放出气体、生成沉淀等3.化学变化与物理变化的区别与联系4.特别提醒①爆炸有可能是物理变化,也可能是化学变化。
如:火药的爆炸属于化学变化,因为生成了新物质。
瓦斯爆炸、轮胎爆炸属于物理变化。
原子弹爆炸既不是物理变化也不是化学变化。
②发光、放热的变化不一定是化学变化。
如:电灯通电发光放热不是化学变化。
③有沉淀生成的变化不一定是化学变化。
如:浑浊的泥浆水放置较长的时间会产生沉淀。
④有变色的变化不一定是化学变化。
如:红墨水加水稀释后颜色变浅。
⑤产生气体的变化不一定是化学变化。
如:干冰升华、碘升华。
知识点二:物质的性质分为物理性质和化学性质1.物理性质①定义:物质不需要发生化学变化就能表现出来的性质。
②性质的确定:由感觉器官直接感知或由仪器测知。
③内容:颜色、状态、气味、熔点、沸点、硬度、密度、溶解性、挥发性、导热性、导电性等。
2.化学性质①定义:物质在化学变化中表现出来的性质。
②性质的确定:通过化学变化来确定。
③内容:可燃性、还原性、氧化性、稳定性、酸性、碱性、毒性、腐蚀性等3.物理性质与化学性质的区别方法是否需要通过化学变化表现出来。
4.性质与用途的关系性质决定用途,用途反应性质例如:因为铜有导电性所以铜可以做导线。
因为导线是用铜做的所以这个用途利用了铜的导电性。
初中化学中考重难点讲义3篇

化学并不神秘,它就来自于生活,却又高于生活。只要你认真观察,生活中到处都充满着化学带给你的惊奇。下面是我给大家带来的初中化学中考重难点讲义,欢迎大家阅读参考,我们一起来看看吧!
初中化学中考重难点讲义总结:发光发热现象的变化
问题:发光发热现象是化学变化的标志之一,如碳、铁和石蜡等物质在氧气中燃烧时就伴随发光发热现象。那么凡是有发光发热现象的变化都一定是化学变化吗?
①蜡烛燃烧时有 和 放出;②蜡烛燃烧时有 和 生成。因此发生的是 变化。
(2)观察白炽灯内钨丝的颜色和状态,然后通电,观察现象,约1 min~2 min后,停止通电,比较通电前后钨丝本身是否发生变化①钨丝是 色的 体;②通电后灯泡发出 光。用手靠近灯泡,有 的感觉。③停止通电后,钨丝颜色和状态变化(填“有”或“没有”)①钨丝通电时也有 和 放出;②通电前后,钨丝本身 发生
答案:
(1)健康问题:②⑤ (2)能源问题:④
(3)粮食问题: ①⑥ (4)环境问题:③⑦⑧⑨
反思:学习化学不但要知道化学对人类的贡献,还要了解化学所造成的污染,同时学会关心与化学相关的社会问题,从而真正意义上认识学习化学的重要价值。请在下面表列举你所了解的与化学有关的问题:
例2 化学是一门重要的自然科学。化学工业的发展给人们的生活质量带来了巨大的变化。试以所学的化学知识谈一下你周围的的变化。
实验:为了找到有说明力的证据,某同学找来蜡烛并与白炽灯做了下列对比实验。请完成下表中有关内容的填写:
蜡烛燃烧和白炽灯内钨丝通电时变化情况的比较
实验内容实验现象
结 论
(1)点燃蜡烛,分别用干冷烧杯和沾有石灰水的烧杯罩在火焰上。观察现象,约1 min~2 min后,再吹灭蜡烛①干冷烧杯内壁出现 ,用手触摸烧杯壁有 感觉;②石灰水变 ;③蜡烛逐渐变 。
【化学】中考科学中考复习化学部分考点归纳与点拨
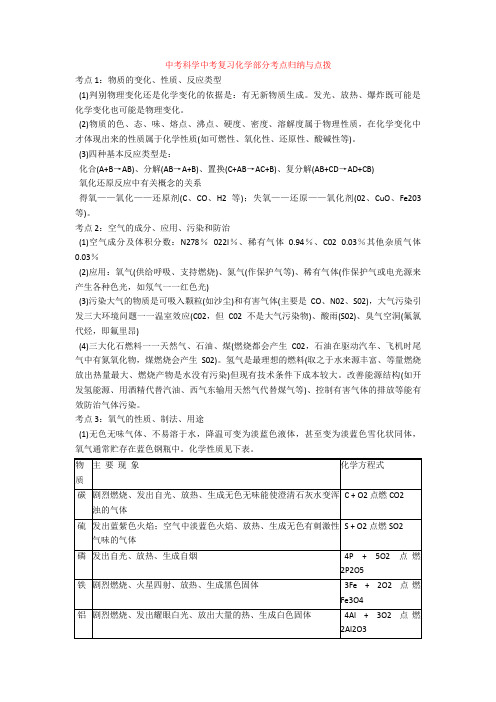
中考科学中考复习化学部分考点归纳与点拨考点1:物质的变化、性质、反应类型(1)判别物理变化还是化学变化的依据是:有无新物质生成。
发光、放热、爆炸既可能是化学变化也可能是物理变化。
(2)物质的色、态、味、熔点、沸点、硬度、密度、溶解度属于物理性质,在化学变化中才体现出来的性质属于化学性质(如可燃性、氧化性、还原性、酸碱性等)。
(3)四种基本反应类型是:化合(A+B→AB)、分解(AB→A+B)、置换(C+AB→AC+B)、复分解(AB+CD→AD+CB)氧化还原反应中有关概念的关系得氧——氧化——还原剂(C、CO、H2等);失氧——还原——氧化剂(02、CuO、Fe203等)。
考点2:空气的成分、应用、污染和防治(1)空气成分及体积分数:N278%022l%、稀有气体0.94%、C02 0.03%其他杂质气体0.03%(2)应用:氧气(供给呼吸、支持燃烧)、氮气(作保护气等)、稀有气体(作保护气或电光源来产生各种色光,如氖气一一红色光)(3)污染大气的物质是可吸入颗粒(如沙尘)和有害气体(主要是CO、N02、S02),大气污染引发三大环境问题一一温室效应(C02,但C02不是大气污染物)、酸雨(S02)、臭气空洞(氟氯代烃,即氟里昂)(4)三大化石燃料一一天然气、石油、煤(燃烧都会产生C02,石油在驱动汽车、飞机时尾气中有氮氧化物,煤燃烧会产生S02)。
氢气是最理想的燃料(取之于水来源丰富、等量燃烧放出热量最大、燃烧产物是水没有污染)但现有技术条件下成本较大。
改善能源结构(如开发氢能源、用酒精代替汽油、西气东输用天然气代替煤气等)、控制有害气体的排放等能有效防治气体污染。
考点3:氧气的性质、制法、用途(1)无色无味气体、不易溶于水,降温可变为淡蓝色液体,甚至变为淡蓝色雪化状同体,氧气通常贮存在蓝色钢瓶中。
化学性质见下表。
2KMnO4 K2MnO4 + MnO2 + O2↑(固固加热型)(组、检、装、夹、点、收、移、熄)2H2O2 H2O+ O2 ↑ (固液不加热型)(Mn02作催化剂“一变两不变”)可用排水法(不易溶于水)或向上捧空气法(密度比空气大,32>29)收集工业上用分离液态空气的方法得到氧气(氧气的沸点比氮气高.物理变化)。
中考-初中化学必过-化学变化-知识点全掌握

中考-初中化学必过-化学变化-知识点全掌握
1. 化学变化的本质特征在于是有新物质生成,放热、发光、变色、放出气体、生成沉淀等可以帮助判断,但有这些现象时并不一定发生了化学变化.
2. 化学反应往往伴随着能量的吸收或释放等的变化,如用木柴燃烧取暖,就是把化学能能转化为热能能和光能能.给蓄电池充电时电能转化成化学能;绿色植物进行光合作用时,太阳能转化成化学能.
3. 分子是保持物质化学性质的最小微粒,在化学变化中分子首先分解成原子,然后原子再重新组合生成新的分子,因此原子在化学变化中不能再分,是最小的微粒;而在其他的变化中原子有可以分为质子和电子.
4. 化学变化是分子分裂成原子,原子重新组合成新分子的过程.故而反应前后原子种类没有改变,原子数目没有增减,原子的质量也没有改变.
5. 化学变化中,必然会发生改变的是分子的种类。
化学变化中物质、分子变,元素、原子不变.
6. 物理变化是没有生成其它物质的变化,只是在形状、状态和大小的改变。
比如:酒精挥发、玻璃破碎、冰雪融化、水结冰、海水蒸发、石蜡熔化、衣服晒干、灯泡发光、玻璃透光等。
7.化学变化是生成其它物质的变化,也叫化学反应。
比如:葡萄酿酒、光合作用、木柴燃烧、金属生锈、食物变质、水果腐烂、生物
发酵等。
【化学】中考科学中考复习化学部分考点归纳与点拨
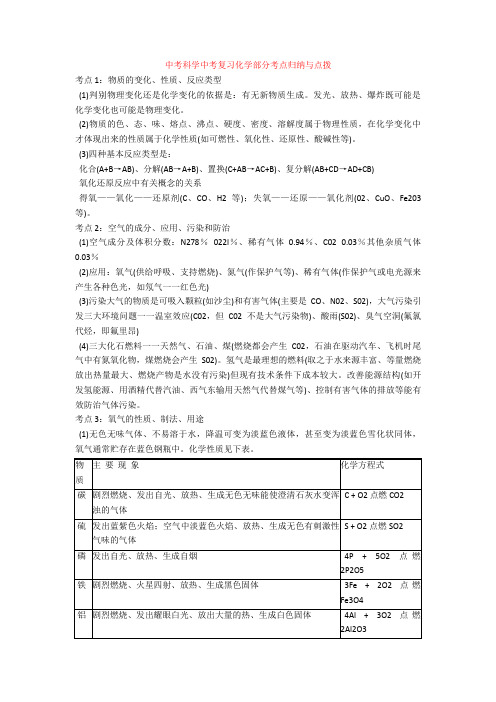
中考科学中考复习化学部分考点归纳与点拨考点1:物质的变化、性质、反应类型(1)判别物理变化还是化学变化的依据是:有无新物质生成。
发光、放热、爆炸既可能是化学变化也可能是物理变化。
(2)物质的色、态、味、熔点、沸点、硬度、密度、溶解度属于物理性质,在化学变化中才体现出来的性质属于化学性质(如可燃性、氧化性、还原性、酸碱性等)。
(3)四种基本反应类型是:化合(A+B→AB)、分解(AB→A+B)、置换(C+AB→AC+B)、复分解(AB+CD→AD+CB)氧化还原反应中有关概念的关系得氧——氧化——还原剂(C、CO、H2等);失氧——还原——氧化剂(02、CuO、Fe203等)。
考点2:空气的成分、应用、污染和防治(1)空气成分及体积分数:N278%022l%、稀有气体0.94%、C02 0.03%其他杂质气体0.03%(2)应用:氧气(供给呼吸、支持燃烧)、氮气(作保护气等)、稀有气体(作保护气或电光源来产生各种色光,如氖气一一红色光)(3)污染大气的物质是可吸入颗粒(如沙尘)和有害气体(主要是CO、N02、S02),大气污染引发三大环境问题一一温室效应(C02,但C02不是大气污染物)、酸雨(S02)、臭气空洞(氟氯代烃,即氟里昂)(4)三大化石燃料一一天然气、石油、煤(燃烧都会产生C02,石油在驱动汽车、飞机时尾气中有氮氧化物,煤燃烧会产生S02)。
氢气是最理想的燃料(取之于水来源丰富、等量燃烧放出热量最大、燃烧产物是水没有污染)但现有技术条件下成本较大。
改善能源结构(如开发氢能源、用酒精代替汽油、西气东输用天然气代替煤气等)、控制有害气体的排放等能有效防治气体污染。
考点3:氧气的性质、制法、用途(1)无色无味气体、不易溶于水,降温可变为淡蓝色液体,甚至变为淡蓝色雪化状同体,氧气通常贮存在蓝色钢瓶中。
化学性质见下表。
2KMnO4 K2MnO4 + MnO2 + O2↑(固固加热型)(组、检、装、夹、点、收、移、熄)2H2O2 H2O+ O2 ↑ (固液不加热型)(Mn02作催化剂“一变两不变”)可用排水法(不易溶于水)或向上捧空气法(密度比空气大,32>29)收集工业上用分离液态空气的方法得到氧气(氧气的沸点比氮气高.物理变化)。
【化学】中考科学中考复习化学部分考点归纳与点拨
中考科学中考复习化学部分考点归纳与点拨考点1:物质的变化、性质、反应类型(1)判别物理变化还是化学变化的依据是:有无新物质生成。
发光、放热、爆炸既可能是化学变化也可能是物理变化。
(2)物质的色、态、味、熔点、沸点、硬度、密度、溶解度属于物理性质,在化学变化中才体现出来的性质属于化学性质(如可燃性、氧化性、还原性、酸碱性等)。
(3)四种基本反应类型是:化合(A+B→AB)、分解(AB→A+B)、置换(C+AB→AC+B)、复分解(AB+CD→AD+CB)氧化还原反应中有关概念的关系得氧——氧化——还原剂(C、CO、H2等);失氧——还原——氧化剂(02、CuO、Fe203等)。
考点2:空气的成分、应用、污染和防治(1)空气成分及体积分数:N278%022l%、稀有气体0.94%、C02 0.03%其他杂质气体0.03%(2)应用:氧气(供给呼吸、支持燃烧)、氮气(作保护气等)、稀有气体(作保护气或电光源来产生各种色光,如氖气一一红色光)(3)污染大气的物质是可吸入颗粒(如沙尘)和有害气体(主要是CO、N02、S02),大气污染引发三大环境问题一一温室效应(C02,但C02不是大气污染物)、酸雨(S02)、臭气空洞(氟氯代烃,即氟里昂)(4)三大化石燃料一一天然气、石油、煤(燃烧都会产生C02,石油在驱动汽车、飞机时尾气中有氮氧化物,煤燃烧会产生S02)。
氢气是最理想的燃料(取之于水来源丰富、等量燃烧放出热量最大、燃烧产物是水没有污染)但现有技术条件下成本较大。
改善能源结构(如开发氢能源、用酒精代替汽油、西气东输用天然气代替煤气等)、控制有害气体的排放等能有效防治气体污染。
考点3:氧气的性质、制法、用途(1)无色无味气体、不易溶于水,降温可变为淡蓝色液体,甚至变为淡蓝色雪化状同体,氧气通常贮存在蓝色钢瓶中。
化学性质见下表。
2KMnO4 K2MnO4 + MnO2 + O2↑(固固加热型)(组、检、装、夹、点、收、移、熄)2H2O2 H2O+ O2 ↑ (固液不加热型)(Mn02作催化剂“一变两不变”)可用排水法(不易溶于水)或向上捧空气法(密度比空气大,32>29)收集工业上用分离液态空气的方法得到氧气(氧气的沸点比氮气高.物理变化)。
2019中考化学知识点:燃烧与发光,放热,火焰之间的关系

2019中考化学知识点:燃烧与发光,放热,火焰之间的关系
各位读友大家好,此文档由网络收集而来,欢迎您下载,谢谢
新一轮复习备考周期正式开始,为各位初三考生整理了各学科的复习攻略,主要包括中考必考点、中考常考知识点、各科复习方法、考试答题技巧等内容,帮助各位考生梳理知识脉络,理清做题思路,希望各位考生可以在考试中取得优异成绩!下面是《化学知识点:燃烧与发光,放热,火焰之间的关系》,仅供参考!
燃烧与发光,放热,火焰之间的关系:
燃烧与发光,放热的关系
燃烧一定发光,放热,但发光,放热的变化不一定是化学变化,因而不一
定是燃烧,如原子弹,氢弹的爆炸。
燃烧与火焰的关系
火焰是气体物质燃烧所特有的现象、液体物质的燃烧主要是其蒸气的燃烧,因而产生火馅。
若固体物质的沸点较高.燃烧时无蒸气逸出,则无火焰,如铁勺燃烧:若固体物质的沸点较低,燃烧时有蒸气逸出,就有火馅,如钠、硫的燃烧。
发光与放热的关系
化学反应瞬间放出热量较多时.就以光的形式出现,反之则不发光,因此,发光一定收热,放热不一定发光。
燃烧反应是既发光又放热的反应,单一的发光或放热反应不一定是燃烧。
各位读友大家好,此文档由网络收集而来,欢迎您下载,谢谢。
【化学】中考科学中考复习化学部分考点归纳与点拨
中考科学中考复习化学部分考点归纳与点拨考点1:物质的变化、性质、反应类型(1)判别物理变化还是化学变化的依据是:有无新物质生成。
发光、放热、爆炸既可能是化学变化也可能是物理变化。
(2)物质的色、态、味、熔点、沸点、硬度、密度、溶解度属于物理性质,在化学变化中才体现出来的性质属于化学性质(如可燃性、氧化性、还原性、酸碱性等)。
(3)四种基本反应类型是:化合(A+B→AB)、分解(AB→A+B)、置换(C+AB→AC+B)、复分解(AB+CD→AD+CB)氧化还原反应中有关概念的关系得氧——氧化——还原剂(C、CO、H2等);失氧——还原——氧化剂(02、CuO、Fe203等)。
考点2:空气的成分、应用、污染和防治(1)空气成分及体积分数:N278%022l%、稀有气体0.94%、C02 0.03%其他杂质气体0.03%(2)应用:氧气(供给呼吸、支持燃烧)、氮气(作保护气等)、稀有气体(作保护气或电光源来产生各种色光,如氖气一一红色光)(3)污染大气的物质是可吸入颗粒(如沙尘)和有害气体(主要是CO、N02、S02),大气污染引发三大环境问题一一温室效应(C02,但C02不是大气污染物)、酸雨(S02)、臭气空洞(氟氯代烃,即氟里昂)(4)三大化石燃料一一天然气、石油、煤(燃烧都会产生C02,石油在驱动汽车、飞机时尾气中有氮氧化物,煤燃烧会产生S02)。
氢气是最理想的燃料(取之于水来源丰富、等量燃烧放出热量最大、燃烧产物是水没有污染)但现有技术条件下成本较大。
改善能源结构(如开发氢能源、用酒精代替汽油、西气东输用天然气代替煤气等)、控制有害气体的排放等能有效防治气体污染。
考点3:氧气的性质、制法、用途(1)无色无味气体、不易溶于水,降温可变为淡蓝色液体,甚至变为淡蓝色雪化状同体,氧气通常贮存在蓝色钢瓶中。
化学性质见下表。
2KMnO4 K2MnO4 + MnO2 + O2↑(固固加热型)(组、检、装、夹、点、收、移、熄)2H2O2 H2O+ O2 ↑ (固液不加热型)(Mn02作催化剂“一变两不变”)可用排水法(不易溶于水)或向上捧空气法(密度比空气大,32>29)收集工业上用分离液态空气的方法得到氧气(氧气的沸点比氮气高.物理变化)。
【化学】中考科学中考复习化学部分考点归纳与点拨

中考科学中考复习化学部分考点归纳与点拨考点1:物质的变化、性质、反应类型(1)判别物理变化还是化学变化的依据是:有无新物质生成。
发光、放热、爆炸既可能是化学变化也可能是物理变化。
(2)物质的色、态、味、熔点、沸点、硬度、密度、溶解度属于物理性质,在化学变化中才体现出来的性质属于化学性质(如可燃性、氧化性、还原性、酸碱性等)。
(3)四种基本反应类型是:化合(A+B→AB)、分解(AB→A+B)、置换(C+AB→AC+B)、复分解(AB+CD→AD+CB)氧化还原反应中有关概念的关系得氧——氧化——还原剂(C、CO、H2等);失氧——还原——氧化剂(02、CuO、Fe203等)。
考点2:空气的成分、应用、污染和防治(1)空气成分及体积分数:N278%022l%、稀有气体0.94%、C02 0.03%其他杂质气体0.03%(2)应用:氧气(供给呼吸、支持燃烧)、氮气(作保护气等)、稀有气体(作保护气或电光源来产生各种色光,如氖气一一红色光)(3)污染大气的物质是可吸入颗粒(如沙尘)和有害气体(主要是CO、N02、S02),大气污染引发三大环境问题一一温室效应(C02,但C02不是大气污染物)、酸雨(S02)、臭气空洞(氟氯代烃,即氟里昂)(4)三大化石燃料一一天然气、石油、煤(燃烧都会产生C02,石油在驱动汽车、飞机时尾气中有氮氧化物,煤燃烧会产生S02)。
氢气是最理想的燃料(取之于水来源丰富、等量燃烧放出热量最大、燃烧产物是水没有污染)但现有技术条件下成本较大。
改善能源结构(如开发氢能源、用酒精代替汽油、西气东输用天然气代替煤气等)、控制有害气体的排放等能有效防治气体污染。
考点3:氧气的性质、制法、用途(1)无色无味气体、不易溶于水,降温可变为淡蓝色液体,甚至变为淡蓝色雪化状同体,氧气通常贮存在蓝色钢瓶中。
化学性质见下表。
2KMnO4 K2MnO4 + MnO2 + O2↑(固固加热型)(组、检、装、夹、点、收、移、熄)2H2O2 H2O+ O2 ↑ (固液不加热型)(Mn02作催化剂“一变两不变”)可用排水法(不易溶于水)或向上捧空气法(密度比空气大,32>29)收集工业上用分离液态空气的方法得到氧气(氧气的沸点比氮气高.物理变化)。
【化学】中考科学中考复习化学部分考点归纳与点拨
中考科学中考复习化学部分考点归纳与点拨考点1:物质的变化、性质、反应类型(1)判别物理变化还是化学变化的依据是:有无新物质生成。
发光、放热、爆炸既可能是化学变化也可能是物理变化。
(2)物质的色、态、味、熔点、沸点、硬度、密度、溶解度属于物理性质,在化学变化中才体现出来的性质属于化学性质(如可燃性、氧化性、还原性、酸碱性等)。
(3)四种基本反应类型是:化合(A+B→AB)、分解(AB→A+B)、置换(C+AB→AC+B)、复分解(AB+CD→AD+CB)氧化还原反应中有关概念的关系得氧——氧化——还原剂(C、CO、H2等);失氧——还原——氧化剂(02、CuO、Fe203等)。
考点2:空气的成分、应用、污染和防治(1)空气成分及体积分数:N278%022l%、稀有气体0.94%、C02 0.03%其他杂质气体0.03%(2)应用:氧气(供给呼吸、支持燃烧)、氮气(作保护气等)、稀有气体(作保护气或电光源来产生各种色光,如氖气一一红色光)(3)污染大气的物质是可吸入颗粒(如沙尘)和有害气体(主要是CO、N02、S02),大气污染引发三大环境问题一一温室效应(C02,但C02不是大气污染物)、酸雨(S02)、臭气空洞(氟氯代烃,即氟里昂)(4)三大化石燃料一一天然气、石油、煤(燃烧都会产生C02,石油在驱动汽车、飞机时尾气中有氮氧化物,煤燃烧会产生S02)。
氢气是最理想的燃料(取之于水来源丰富、等量燃烧放出热量最大、燃烧产物是水没有污染)但现有技术条件下成本较大。
改善能源结构(如开发氢能源、用酒精代替汽油、西气东输用天然气代替煤气等)、控制有害气体的排放等能有效防治气体污染。
考点3:氧气的性质、制法、用途(1)无色无味气体、不易溶于水,降温可变为淡蓝色液体,甚至变为淡蓝色雪化状同体,氧气通常贮存在蓝色钢瓶中。
化学性质见下表。
2KMnO4 K2MnO4 + MnO2 + O2↑(固固加热型)(组、检、装、夹、点、收、移、熄)2H2O2 H2O+ O2 ↑ (固液不加热型)(Mn02作催化剂“一变两不变”)可用排水法(不易溶于水)或向上捧空气法(密度比空气大,32>29)收集工业上用分离液态空气的方法得到氧气(氧气的沸点比氮气高.物理变化)。
【化学】中考科学中考复习化学部分考点归纳与点拨
中考科学中考复习化学部分考点归纳与点拨考点1:物质的变化、性质、反应类型(1)判别物理变化还是化学变化的依据是:有无新物质生成。
发光、放热、爆炸既可能是化学变化也可能是物理变化。
(2)物质的色、态、味、熔点、沸点、硬度、密度、溶解度属于物理性质,在化学变化中才体现出来的性质属于化学性质(如可燃性、氧化性、还原性、酸碱性等)。
(3)四种基本反应类型是:化合(A+B→AB)、分解(AB→A+B)、置换(C+AB→AC+B)、复分解(AB+CD→AD+CB)氧化还原反应中有关概念的关系得氧——氧化——还原剂(C、CO、H2等);失氧——还原——氧化剂(02、CuO、Fe203等)。
考点2:空气的成分、应用、污染和防治(1)空气成分及体积分数:N278%022l%、稀有气体0.94%、C02 0.03%其他杂质气体0.03%(2)应用:氧气(供给呼吸、支持燃烧)、氮气(作保护气等)、稀有气体(作保护气或电光源来产生各种色光,如氖气一一红色光)(3)污染大气的物质是可吸入颗粒(如沙尘)和有害气体(主要是CO、N02、S02),大气污染引发三大环境问题一一温室效应(C02,但C02不是大气污染物)、酸雨(S02)、臭气空洞(氟氯代烃,即氟里昂)(4)三大化石燃料一一天然气、石油、煤(燃烧都会产生C02,石油在驱动汽车、飞机时尾气中有氮氧化物,煤燃烧会产生S02)。
氢气是最理想的燃料(取之于水来源丰富、等量燃烧放出热量最大、燃烧产物是水没有污染)但现有技术条件下成本较大。
改善能源结构(如开发氢能源、用酒精代替汽油、西气东输用天然气代替煤气等)、控制有害气体的排放等能有效防治气体污染。
考点3:氧气的性质、制法、用途(1)无色无味气体、不易溶于水,降温可变为淡蓝色液体,甚至变为淡蓝色雪化状同体,氧气通常贮存在蓝色钢瓶中。
化学性质见下表。
2KMnO4 K2MnO4 + MnO2 + O2↑(固固加热型)(组、检、装、夹、点、收、移、熄)2H2O2 H2O+ O2 ↑ (固液不加热型)(Mn02作催化剂“一变两不变”)可用排水法(不易溶于水)或向上捧空气法(密度比空气大,32>29)收集工业上用分离液态空气的方法得到氧气(氧气的沸点比氮气高.物理变化)。
【化学】中考科学中考复习化学部分考点归纳与点拨
中考科学中考复习化学部分考点归纳与点拨考点1:物质的变化、性质、反应类型(1)判别物理变化还是化学变化的依据是:有无新物质生成。
发光、放热、爆炸既可能是化学变化也可能是物理变化。
(2)物质的色、态、味、熔点、沸点、硬度、密度、溶解度属于物理性质,在化学变化中才体现出来的性质属于化学性质(如可燃性、氧化性、还原性、酸碱性等)。
(3)四种基本反应类型是:化合(A+B→AB)、分解(AB→A+B)、置换(C+AB→AC+B)、复分解(AB+CD→AD+CB)氧化还原反应中有关概念的关系得氧——氧化——还原剂(C、CO、H2等);失氧——还原——氧化剂(02、CuO、Fe203等)。
考点2:空气的成分、应用、污染和防治(1)空气成分及体积分数:N278%022l%、稀有气体0.94%、C02 0.03%其他杂质气体0.03%(2)应用:氧气(供给呼吸、支持燃烧)、氮气(作保护气等)、稀有气体(作保护气或电光源来产生各种色光,如氖气一一红色光)(3)污染大气的物质是可吸入颗粒(如沙尘)和有害气体(主要是CO、N02、S02),大气污染引发三大环境问题一一温室效应(C02,但C02不是大气污染物)、酸雨(S02)、臭气空洞(氟氯代烃,即氟里昂)(4)三大化石燃料一一天然气、石油、煤(燃烧都会产生C02,石油在驱动汽车、飞机时尾气中有氮氧化物,煤燃烧会产生S02)。
氢气是最理想的燃料(取之于水来源丰富、等量燃烧放出热量最大、燃烧产物是水没有污染)但现有技术条件下成本较大。
改善能源结构(如开发氢能源、用酒精代替汽油、西气东输用天然气代替煤气等)、控制有害气体的排放等能有效防治气体污染。
考点3:氧气的性质、制法、用途(1)无色无味气体、不易溶于水,降温可变为淡蓝色液体,甚至变为淡蓝色雪化状同体,氧气通常贮存在蓝色钢瓶中。
化学性质见下表。
2KMnO4 K2MnO4 + MnO2 + O2↑(固固加热型)(组、检、装、夹、点、收、移、熄)2H2O2 H2O+ O2 ↑ (固液不加热型)(Mn02作催化剂“一变两不变”)可用排水法(不易溶于水)或向上捧空气法(密度比空气大,32>29)收集工业上用分离液态空气的方法得到氧气(氧气的沸点比氮气高.物理变化)。
【化学】中考科学中考复习化学部分考点归纳与点拨
中考科学中考复习化学部分考点归纳与点拨考点1:物质的变化、性质、反应类型(1)判别物理变化还是化学变化的依据是:有无新物质生成。
发光、放热、爆炸既可能是化学变化也可能是物理变化。
(2)物质的色、态、味、熔点、沸点、硬度、密度、溶解度属于物理性质,在化学变化中才体现出来的性质属于化学性质(如可燃性、氧化性、还原性、酸碱性等)。
(3)四种基本反应类型是:化合(A+B→AB)、分解(AB→A+B)、置换(C+AB→AC+B)、复分解(AB+CD→AD+CB)氧化还原反应中有关概念的关系得氧——氧化——还原剂(C、CO、H2等);失氧——还原——氧化剂(02、CuO、Fe203等)。
考点2:空气的成分、应用、污染和防治(1)空气成分及体积分数:N278%022l%、稀有气体0.94%、C02 0.03%其他杂质气体0.03%(2)应用:氧气(供给呼吸、支持燃烧)、氮气(作保护气等)、稀有气体(作保护气或电光源来产生各种色光,如氖气一一红色光)(3)污染大气的物质是可吸入颗粒(如沙尘)和有害气体(主要是CO、N02、S02),大气污染引发三大环境问题一一温室效应(C02,但C02不是大气污染物)、酸雨(S02)、臭气空洞(氟氯代烃,即氟里昂)(4)三大化石燃料一一天然气、石油、煤(燃烧都会产生C02,石油在驱动汽车、飞机时尾气中有氮氧化物,煤燃烧会产生S02)。
氢气是最理想的燃料(取之于水来源丰富、等量燃烧放出热量最大、燃烧产物是水没有污染)但现有技术条件下成本较大。
改善能源结构(如开发氢能源、用酒精代替汽油、西气东输用天然气代替煤气等)、控制有害气体的排放等能有效防治气体污染。
考点3:氧气的性质、制法、用途(1)无色无味气体、不易溶于水,降温可变为淡蓝色液体,甚至变为淡蓝色雪化状同体,氧气通常贮存在蓝色钢瓶中。
化学性质见下表。
2KMnO4 K2MnO4 + MnO2 + O2↑(固固加热型)(组、检、装、夹、点、收、移、熄)2H2O2 H2O+ O2 ↑ (固液不加热型)(Mn02作催化剂“一变两不变”)可用排水法(不易溶于水)或向上捧空气法(密度比空气大,32>29)收集工业上用分离液态空气的方法得到氧气(氧气的沸点比氮气高.物理变化)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学中考重难点讲义总结:发光发热现象的变化
问题:发光发热现象是化学变化的标志之一,如碳、铁和石蜡等物质在氧气中燃烧时就伴随发光发热现象。
那么凡是有发光发热现象的变化都一定是化学变化吗?
实验:为了找到有说明力的证据,某同学找来蜡烛并与白炽灯做了下列对比实验。
请完成下表中有关内容的填写:
蜡烛燃烧和白炽灯内钨丝通电时变化情况的比较
实验内容实验现象
结论
(1)点燃蜡烛,分别用干冷烧杯和沾有石灰水的烧杯罩在火焰上。
观察现象,约1 min~2 min后,再吹灭蜡烛①干冷烧杯内壁出现,用手触摸烧杯壁有感觉;②石灰水变;③蜡烛逐渐变。
①蜡烛燃烧时有和放出;②蜡烛燃烧时有和生成。
因此发生的是变化。
(2)观察白炽灯内钨丝的颜色和状态,然后通电,观察现象,约1 min~2 min后,停止通电,比较通电前后钨丝本身是否发生变化①钨丝是色的体;②通电后灯泡发出光。
用手靠近灯泡,有的感觉。
③停止通电后,钨丝颜色和状态变化(填有或没有)①钨丝通电时也有和放出;②通电前后,钨丝本身发生
变化(填有或没有),因此发生的是变化。
