西安建筑科技大学复试试题
西安建筑科技大学考试试卷(共页)评卷人填写.

(3)科学决策与公众参与原则:应当坚持政府组织、专家领衔、部门合作、公众参与、科学决策的原则。
6
4、城市化与城市化水平
城市化:人类生产和生活方式由乡村型向城市型转化的历史过程,表现为乡村人口向城市人口转化以及城市不断发展和完善的过程。又称城镇化、都市化。
城市化水平:衡量城市化发展程度的数量指标,一般用一定地域内城市人口占总人口比例来表示。
5、城市规划区与城市建成区
城市规划区:城市市区、近郊区以及城市行政区域内其他因城市建设和发展需要实行规划控制的区域。
4、“公交优先”的含义及其措施?
“公交优先”即充分发挥公共交通的主导作用。
在国内外一些城市采取了以下一些“公交优先”的措施:如交叉口公交车优先放行、开辟公交车专用道、允许公交车在单向交通道路上逆向行驶、限制小汽车进入市中心区域以及在沿市郊高速公路与城市公交线路的交汇处修建免费停车场、方便小汽车与公交换乘等等。为了最大限度地接近居民、方便乘车,可大胆地将快速公共客运线路引进城区内部,并使住宅区布点与公共客运路线相结合。
3
霍华德不仅提出了田园城市的设想,以图解的形式描述了理想城市的原型,而且他还为实现这一设想进行了细致的考虑,他对资金的来源、土地的分配、城市财政的收支、田园城市的经营管理等都提出了具体的建议。他认为,工业和商业不能由公营垄断,要给私营以发展的条件。但是,城市中的所有土地必须归全体居民集体所有,使用土地必须交付租金。城市的收入全部来自租金,在土地上进行建设、聚居而获得的增值仍归集体所有。
城市建成区:城市行政区内实际已成片开发建设、市政公用设施和公共设施基本具备的地区。
西安建筑科技大学考试试卷标准答案(共6页)A卷评卷人填

西安建筑科技大学考试试卷标准答案(共 6 页)A卷评卷人填写
考试科目:水文学考试时间:
西安建筑科技大学考试标准答案(共 6 页)A卷班级:姓名:学号:。
由t′3到t2的时间段又称为产流历时。
(1分)但河槽集
2
流过程并未停止,它包括雨水由坡面汇入河网,直到全部流经出口断面时为止的整个过程,它的延续时
间最长,比净雨历时和坡地漫流历时都要长得多,一直到t4时刻为止,由这次暴雨产生的洪水过程才算
这段时间称为流域最大汇流时间,以τ表示,即流域最远点A的净雨流到出口断面B所
3 4
西安建筑科技大学考试标准答案(共 6 页)A卷
班级:姓名:学号:
m3(1分)
s
)s
203
0.2
=
⨯(1分)
.
36
m
14
m3(1分)
s
56。
2011年西安建筑科技大学复试真题
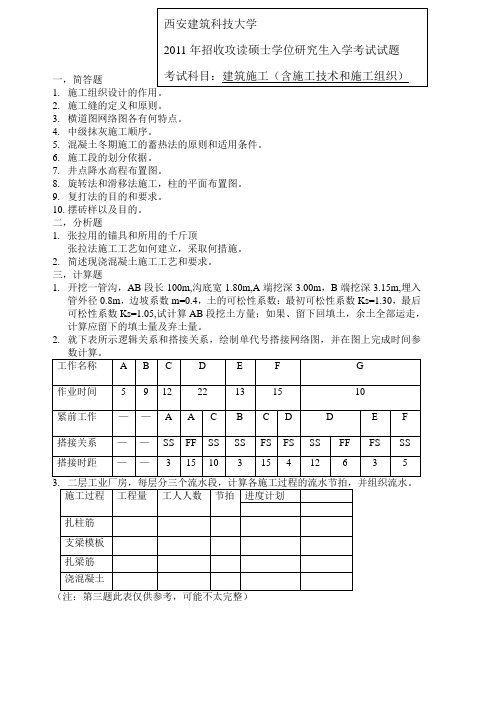
一,简答题
1.
2. 施工缝的定义和原则。
3. 横道图网络图各有何特点。
4. 中级抹灰施工顺序。
5. 混凝土冬期施工的蓄热法的原则和适用条件。
6. 施工段的划分依据。
7. 井点降水高程布置图。
8. 旋转法和滑移法施工,柱的平面布置图。
9. 复打法的目的和要求。
10. 摆砖样以及目的。
二,分析题
1. 张拉用的锚具和所用的千斤顶
张拉法施工工艺如何建立,采取何措施。
2. 简述现浇混凝土施工工艺和要求。
三,计算题
1. 开挖一管沟,AB 段长100m,沟底宽1.80m,A 端挖深3.00m ,B 端挖深3.15m,埋入管外径0.8m ,边坡系数m=0.4,土的可松性系数:最初可松性系数Ks=1.30,最后可松性系数Ks=1.05,试计算AB 段挖土方量;如果、留下回填土,余土全部运走,计算应留下的填土量及弃土量。
2. 就下表所示逻辑关系和搭接关系,绘制单代号搭接网络图,并在图上完成时间参。
西建大04年钢结构复试[1]
![西建大04年钢结构复试[1]](https://img.taocdn.com/s3/m/1e6c5cdace2f0066f5332275.png)
西安建筑科技大学2003年招收攻读硕士学位研究生复试笔试试题(试题附在考卷内交回) 共 4 页考试科目: 钢 结 构 适用专业: 结构工程一、 简答题(共35分):1、画出低碳钢的拉伸试验曲线,标明其主要性能指标。
(3分)2、影响焊接结构疲劳寿命的主要因素有哪些?(3分)3、高强螺栓承压型连接的破坏形式有哪些?如何保证?(5分)4、普通螺栓连接和高强螺栓连接在受弯计算时有何不同?(3分)5、高强度螺栓摩擦型连接受拉时的构件净截面强度验算与其它连接形式的净截面强度验算有何不同?原因何在?(3分)6、理想轴心受压构件和实际轴心受压构件在弯曲失稳时的性能有何不同?(可结合荷载——挠度曲线简要说明)(5分)7、格构式柱绕虚轴弯曲失稳和实腹柱弯曲失稳有何不同?(3分)8、梁的失稳属于哪一类稳定问题?失稳时梁发生了哪些形式的变形?(5分) 9、βmx 的意义是什么?举出两种情况下βmx 的取值。
(5分)二、 填空题(共10分,每空0.5分):1、结构的极限状态分为 (A) 和 (B) 两类。
梁的挠度验算属于(C ) 。
2、轴心受压构件的屈曲变形形式可能有 (A) 、 (B) 和 (C) 三种。
3、轴心受压构件的板件宽厚比是根据 (A) 得到的。
4、nxx xW M γσ=中γx 的物理意义是 (A) 。
5、梁腹板加劲肋类型有 (A) 、 (B) 、短加劲肋和支承加劲肋等。
6、压弯构件的整体破坏形式有 (A) 、 (B) 和 (C) 。
7、影响框架柱平面内计算长度系数的主要因素有 (A) 、 (B) 和 (C) 等。
8、确定轴心受压构件时用的残余应力指的是 (A) 。
9、图1所示二简支梁,除集中荷载位置不同外,其它条件完全相同,图1(a )梁的承载能力比图1(b )(A )。
10、 代表的意义是(B ),三、 计算题(共55分)1、 (10分)验算图2所示牛腿连接的螺栓强度。
已知螺栓为10.9级高强螺栓,承压型连接,d =22mm ,P =190kN ,钢材为Q345B ,接触面喷砂处理, =0.55。
西安建筑科技大学建筑学考研真题

西安建筑科技大学建筑学考研真题西安建筑科技大学建筑学考研真题西安建筑科技大学是一所以建筑学为主要学科的高等学府,在中国的建筑学界有着较高的声誉。
每年,西安建筑科技大学都会组织建筑学考研,吸引了众多学子的关注和参与。
今天,我们就来探讨一下西安建筑科技大学建筑学考研的真题。
首先,我们需要明确一点,考研真题并不是简单的题目集合,而是对考生综合能力的综合考察。
因此,真题并不仅仅是一道题目,而是一个能够全面展示考生知识储备和解决问题能力的工具。
西安建筑科技大学建筑学考研真题通常涵盖了建筑学的各个领域,包括建筑设计、建筑技术、建筑历史等。
这些题目旨在考察考生对建筑学的全面理解和应用能力。
举个例子,一道典型的建筑设计题目可能要求考生根据给定的场地和功能要求,设计一个具有创新性和可持续发展特点的建筑方案。
这个题目要求考生不仅要具备良好的设计思维和创造力,还需要考虑到建筑的实际可行性和环境影响等因素。
这种题目旨在考察考生的设计能力、创新意识和综合分析能力。
除了设计题目,考研真题中还可能包含一些理论性的问题。
比如,一道建筑历史题目可能要求考生分析某个历史时期的建筑风格和文化背景,并评价其对后世的影响。
这种题目要求考生具备扎实的建筑历史知识和批判性思维能力,能够从多个角度对建筑作品进行分析和评价。
此外,考研真题还可能涉及到建筑技术和工程实践方面的问题。
例如,一道建筑技术题目可能要求考生分析某个具体建筑项目的结构设计和施工工艺,并提出改进意见。
这种题目要求考生具备深入理解建筑结构和施工工艺的能力,能够从实践角度出发提出切实可行的解决方案。
总之,西安建筑科技大学建筑学考研真题不仅要求考生具备扎实的专业知识,还要求考生具备创新思维、综合分析和解决问题的能力。
通过解答真题,考生可以不仅了解自己的知识储备和能力水平,还可以提前适应考试的形式和要求。
然而,需要注意的是,真题只是考研备考的一个重要参考资料,不应该成为唯一的备考依据。
西安建筑科技大学考试试卷(共 页)

二、试分析后张法生产预应力构件时可能有哪些应损失?如何进行弥补?(10分)四、试计算上图中④、⑤钢筋的下料长度。
(10分)三、某土方工程场地方格网边长为20米,场地设计标高H0=43.73米。
(1).试列式计算各角点的设计标高和施工高度(填入图中);(2). 列式确定零点位置(必须标明与角点的距离),画出零线,并在图中示出填方区及挖方区;(3).若计算出填方量为26700m3,挖方量为29500m3,可松性系数k s=1.30,k s’=1.05,试计算弃土量。
(12分)六、试绘制三层现浇钢筋混凝土楼盖工程的流水施工进度表。
已知t支模=4d,t扎筋=2d,t浇砼=2d,层间技术间歇为2d。
(10分)五、在图上计算下面双代号网络图的节点时参、工序时参、工序时差,并将其转化为时标网络图。
(10分)一简答题(每题6分,共48分)1. 按工作装置不同单斗挖掘机分为:正铲、反铲、拉铲和抓铲。
(2分)正铲挖掘机的工作特点是:土斗自下向上强制切土,随挖掘的进程向前开行。
反铲挖土机的特点是:土斗自上向下强制切土,随挖随行或后退,主要用于开挖停机面以下的土壤,不需设置进出口通道。
拉铲挖土机的工作特点是:利用土斗自重及拉索拉力切土,随挖随行或后退,主要用于开挖停机面以下的土壤。
抓铲挖土机的工作特点:土斗直上直下,借助土斗的自重切土抓取,用于开挖停机面以下的土壤。
(每种特点1分,共4分)2.复打法的适用范围:当要提高单桩承载力(1.5)或消除缩颈等缺陷时(1.5分),扩大桩径等。
复打法的要求:复打施工必须在第一次灌注的混凝土初凝以前全部完成(1.5分),同时前后两次沉管的轴线必须重合(1.5分)。
3.施工缝:如果由于技术上的原因或设备人力的限制,混凝土的浇注不能连续进行,中间的间歇时间需超过混凝土的初凝时间,则应留置施工缝。
(3分)留置原则:尽可能留置在结构剪力较小且便于施工的部位。
(3分)4.①对水泥的要求:冬期施工为了缩短养护时间,一般应选用硅酸盐水泥或普通硅酸盐水泥,用蒸汽直接养护混凝土时,应选用矿渣硅酸盐水泥。
2019年西安建筑科技大学公共管理硕士MPA考研复试参考书及面试问题预测

2019年西安建筑科技大学公共管理硕士MPA考研复试参考书及面试问题预测育明教育大印老师2019年9月15日【学长解析】北大人大清华北师大北航南开中山武大复旦等全国280多个公共管理硕士MPA 招生院校复试面试问题越来越趋向于考察热点问题,尤其是政策热点问题,比如产业政策争论、垃圾分类、放管服改革等,所以,大家一定要多看一些热点方面的参考书;此外,北大、人大、南开、中山、武大、西安交大、复旦等名校还时常考察社会研究方法问题。
结合以上分析,公共管理硕士MPA考研复试面试参考书如下所示:《公共管理学》,李国正,首都师范大学出版社,2018年版;《公共政策分析》,李国正,首都师范大学出版社,2019年版;《公共管理学:考点热点与真题解析》,首都师范大学出版社,2020年版;《公共政策分析:考点热点与真题解析》,首都师范大学出版社,2020年版;《社会调查研究方法教程》,袁方,北京大学出版社,2006年版。
目录一、2019-2020年公共管理硕士MPA考研复试面试真题及考研复试面试参考书笔记二、2020-2021年公共管理硕士MPA考研面试常见问题及热点总结三、公共管理硕士MPA考研复习技巧四、公共管理硕士MPA考研复试笔记答题模板(类似考研英语模板奥~)具体内容一、2019-2020年公共管理硕士MPA考研复试面试真题及考研复试面试参考书笔记(三)执行手段(2018年中国人民大学)公共政策执行手段是指政策执行机构及其执行者为完成一定的政策任务,达到一定的政策目标,而采取的各种措施和办法。
(1)行政手段:“以力服人”行政手段是指通过各级政府的行政部门,依靠政府权威,采用行政管理的惯用方式,按照系统、层次、区划来实施政策的方法。
特点是强制性、垂直性、无偿性和稳定性。
优点是部署统一、资源集中、协调一致、实施迅速、便捷高效。
缺点是容易产生与“人治”相关的一些弊病,影响横向联系及下级的积极性、创造性。
(2)法律手段:“以律服人”法律手段是指通过各种法律形式来调整政策执行活动中各种关系、贯彻落实政策的方法。
2019-2020年西安建筑科技大学公共管理硕士MPA考研复试参考书及面试问题预测

2019-2020年西安建筑科技大学公共管理硕士MPA考研复试参考书及面试问题预测育明教育大印老师2019年9月15日【学长解析】北大人大清华北师大北航南开中山武大复旦等全国280多个公共管理硕士MPA 招生院校复试面试问题越来越趋向于考察热点问题,尤其是政策热点问题,比如产业政策争论、垃圾分类、放管服改革等,所以,大家一定要多看一些热点方面的参考书;此外,北大、人大、南开、中山、武大、西安交大、复旦等名校还时常考察社会研究方法问题。
结合以上分析,公共管理硕士MPA考研复试面试参考书如下所示:《公共管理学》,李国正,首都师范大学出版社,2018年版;《公共政策分析》,李国正,首都师范大学出版社,2019年版;《公共管理学:考点热点与真题解析》,首都师范大学出版社,2020年版;《公共政策分析:考点热点与真题解析》,首都师范大学出版社,2020年版;《社会调查研究方法教程》,袁方,北京大学出版社,2006年版。
目录一、2019-2020年公共管理硕士MPA考研复试面试真题及考研复试面试参考书笔记二、2020-2021年公共管理硕士MPA考研面试常见问题及热点总结三、公共管理硕士MPA考研复习技巧四、公共管理硕士MPA考研复试笔记答题模板(类似考研英语模板奥~)具体内容一、2019-2020年公共管理硕士MPA考研复试面试真题及考研复试面试参考书笔记三、答题语言(一)是什么1.社区治理社区治理是指在一定的地域范围内由政府与社区自治组织、非营利组织、辖区单位以及社区居民共同管理社区公共事务、推动社区持续发展的活动。
社区治理的优点:(1)不花或者少花政府的钱(2)调动公民积极参与,受到广泛的支持和欢迎缺点:社区治理作为一种政策工具,往往只能作为一种辅助工具来使用。
2.网络治理治理是对合作网络的管理,又可称为网络管理或网络治理。
指的是为了实现和增进公共利益,政府部门和非政府部门等众多公共行动主体彼此合作,在相互依存的环境中分享公共权力,共同管理公共事务的过程。
西安建筑科技大学考试试卷标准答案(共6页) A卷评卷人填

( 2 分:公式 1 分、结果 1 分)
停止时,降雨强度逐渐减小到稳渗率的程度,
地面径流逐渐消失,此即净雨终止的时刻 t2。由 t′3 到 t2 的时间段又称为产流历时。(1 分)但河槽集流过 程并未停止,它包括雨水由坡面汇入河网,直到全部流经出口断面时为止的整个过程,它的延续时间最
长,比净雨历时和坡地漫流历时都要长得多,一直到 t4 时刻为止,由这次暴雨产生的洪水过程才算终 止。由 t2 到 t4 这段时间称为流域最大汇流时间,以 τ 表示,即流域最远点 A 的净雨流到出口断面 B 所花 费的时间(图 6.3b、c)。(1 分)
1956~1985 年的资料,能否用乙系列展延甲系列?若可以,对下列年份的流量值进行展延。(经计算: Q乙 = 净雨深为 R1 = 20mm, R2 = 25mm,R3 = 10mm, f1 = 1.5 km2, f 2 = 3.0
520m3/s, Cv乙 = 0.34; Q乙 = 600m3/s, Cv乙 = 0.31, r = 0.98)。
样、
四、是非题(在每小题后的括号内标出 “√ ”或 “× ”, 每小题 1.5 分,共 9 分)
分层随机抽样 、 均匀抽样 和 适时抽样 ,最好采用前三种形式。
1. 由随机现象的一部分试验资料去研究总体现象的数字特征和规律的学科称为概率论。( × )
5. 能够采用数理统计法的水文资料要具有一定的要求,包括 一致性 、 代表性
a. 1/3;
b. 1/8 ;
3. 下渗率总是 d 。
c.3/8 ;
d.1/6
4. 中泓线:河道各横断面表面最大流速点的连线。
5. 等流时线:落在该线上的净降雨通过坡地漫流和河槽集流到出口断面所需的汇流时间都相等, 称此线为等流时线。
西安建筑科技大学考试试卷(共

二、多项选择题(共10题,每题2分,共20分)在每题给出的选项中至少有二个选项是符合题目要求的,请将正确选项前的字母填在题后的括号内。多选、少选、错选均无分。
1.微观经济学的基本假设包括()
A.市场出清B.完全竞争C.完全理性D.完全信息E.收入分配公平
2.供给的变动()
A.是商品本身价格变动所引起的变动
C、位于边际收益曲线的下方;D、向右下方倾斜;
8.三部门经济中,收入的恒等关系可以表示为()
A、I+S=G+T;B、I+G=S+T;C、I+G+X=S+T+M;D、I=S;
9.平均消费倾向与平均储蓄倾向之和()
A、大于1;B、等于2;C、等于1;D、小于1;
10.在下列情况中,乘数最大的是()
A、MPC=0.6;B、MPC=O.7;C、MPC=MPS;D、MPS=0.8;
2.利润最大化的原则是什么?为什么?
3.简述西方经济学的研究对象。
4.简要说明货币政策的主要内容。
5.什么是边际收益递减规律?这一规律有何现实意义?
六.论述题(每题10分,共20分)
1.根据需求弹性理论解释“薄利多销”和“谷贱伤农”这两句话的含义。
2.什么是通货紧缩?试结合宏观经济学相关原理说明解决这一问题的理论依据和政策选择。
9.宏观经济政策的目标是()
A.充分就业B.物价稳定C.经济增长
D.国际收支平衡E.提高社会福利水平
10.在经济萧条时期,政府可以选择的货币政策是()
A.降低法定准备率
B.中央银行在公开市场上买进政府债券
C.中央银行在公开市场上卖出政府债券
D.降低再贴现率
E.提高再贴现率
西安建筑科技大学电子信息复试真题

西安建筑科技大学电子信息复试真题1、()是工作表中的小方格,它是工作表的基本元素,也是WPS表格独立操作的最小单位。
[单选题] *A.单元格(正确答案)B.单元格区域C.任务窗格2、主机A 向主机B 发送一个(SYN=,seq=)的TCP 报文,期望与主机B 建立TCP 连接,若主机B 收到接受该连接请求,则主机B 向主机A 发送正确的TCP 报文段可能是()中[单选题] *A. (SYN=,ACK=,seq=,ack=)B.(SYN=,ACK=,seq=,ack=)C. (SYN=,ACK=,seq=,ack=)(正确答案)D. (SYN=,ACK=,seq=,ack=)3、计算机的性能主要决定于()。
[单选题] *A.内存容量B.磁盘容量C.CPU型号(正确答案)D.价格高低4、对输入输出设备,输入输出操作的信息传输单位是()。
[单选题] *A.位B.字节C.字(正确答案)D.块5、通过Windows 中"开始"菜单中的"运行"项()。
[单选题] *A.可以运行操作系统的全部命令B.仅可以运行操作系统的内部命令C.可以运行操作系统的外部命令和可执行文件(正确答案)D.仅可以运行操作系统的外部命令6、局域网的特点是:连接范围窄、用户数少、容易分配()。
[单选题] *A连接速率高(正确答案)B连接速率低C连接数量多D连接距离远7、8.在标准ASCII码表中,已知英文字母A的十进制码值是65,英文字母a的十进制码值是()。
[单选题] *A.95B.96C.97(正确答案)D.918、可以检测网络的连通状况的命令是()。
中[单选题] *A.ipconfigB.tracertC.nslookupD.ping(正确答案)9、显示器的参数:1024×768,它表示______。
[单选题] * A:显示器分辨率(正确答案)B:显示器颜色指标C:显示器屏幕大小D:显示每个字符的列数和行数10、TA直通线与TB直通线网速相比较()快。
西安建筑科技大学土木水利复试题

西安建筑科技大学土木水利复试题1、在土方工程施工中有哪些基本要求?并简述其施工特点。
答:土方工程包括土的开挖、运输和填筑等施工过程,有时还要进行排水、降水和土壁支撑等准备工作。
在建筑工程中,最常见的土方工程有:场地平整、基坑(槽)开挖、地坪填土、路基填筑及基坑回填土等。
土方工程的施工具有如下特点:(1)面大量广、劳动繁重、工期长。
(2)施工条件复杂。
根据上述特点,在组织土方工程施工前应详细分析和核对各项技术资料(如实测地形图、工程地质、水文地质勘察资料,原有地下管线和地下构筑物资料及土方工程施工图等)进行现场调查并根据现有施工条件,制订出技术上可行、经济上合理,既能保证工程质量,又能保证施工安全的方案。
2、何谓土的可松性,如何表示?答:自然状态下的土经开挖后土粒松散,体积增大,如再将其全部用以回填,虽经压实但仍不能恢复至与原状土相同的体积。
土的这种经扰动而体积改变的性质称为土的可送性。
土的可送性程度用可送性系数表示,即Ks=V2/V1,Ks'=Va/V1。
Ks-最初可送性系数,Ks’一最后可送性系数,V,-自然状态下土(原状土)的体积,Ve-土经开挖后的松散体积,Va-土经回填压实后的体积。
3、试分析边坡塌方的原因及防治措施。
答:原因:(1)开挖太深,填筑过高,边坡太陡,使边坡内的土体自重增大,从而引起塌方。
(2)雨水、地下水渗入基坑(槽),使土体泡软,土的容重增大,内聚力减小,抗剪强度降低,这是造成塌方的主要因素。
(3)基坑(槽)的边坡顶面临近坡缘大量堆土或停放是机具、材料、或由于动荷载作用,使边坡土体中的剪应力增大,从而使之塌方。
综上所述,边坡塌方的原因主要是边坡内土体的剪应力超过其抗剪强度。
防治塌方的措施:(1)既需注意防止边坡内浸水,也应尽量避免在边坡顶缘附近有附加荷载,否则要加大边坡坡度。
(2)选择合宜的边坡坡度。
(3)加设支撑护壁。
4、简图表示单锚板桩失稳的原因?答:(1)板桩的入土深度不够,在土压力作用下,板桩下部走动而出现坑壁滑坡。
西安建筑科技大学2002-2004混凝土结构研究生复试真题附答案

研究生入学考试及复试试题西安建筑科技大学2002年招收攻读硕士学位研究生入学考试试题考试科目: 钢筋混凝土结构一、名词解释(每题3分,共15分)1.可变荷载的准永久值 2.吊车竖向荷载3.大偏心受拉构件 4.轴压比5.附加偏心距a e二、多项选择题(每题1.5分,共15分)1.对于冷拉钢筋来说,正确的概念应该是:( )。
①钢筋的冷拉只能提高其抗拉屈服强度,但抗压屈服强度将不能提高②在设计中冷拉钢筋宜作为受压钢筋使用③冷拉钢筋在加工时应该先焊接,然后才能进行冷拉④钢筋的冷拉既可以提高其抗拉屈服强度,同时也能提高其抗压屈服强度,并且塑性性能降低很多2.在结构的极限承载能力分析中,不正确的概念是:( )。
①若同时满足极限条件、机动条件和平衡条件的解答才是结构的真实极限荷载②若仅满足机动条件和平衡条件的解答则是结构极限荷载的下限解③若仅满足极限条件和平衡条件的解答则是结构极限荷载的上限解④若仅满足极限条件和机动条件的解答则是结构极限荷载的上限解3.分析偏心受压构件的弯矩—轴力关系曲线可知,控制截面最不利内力选择时的正确概念应该是:( )。
①对于大偏心受压构件,当轴力N 值基本不变时,弯矩M 值越大所需的纵向钢筋越多 ②对于大偏心受压构件,当弯矩M 值基本不变时,轴力N 值越小所需的纵向钢筋越多 ③对于小偏心受压构件,当轴力N 值基本不变时,弯矩M 值越大所需的纵向钢筋越多 ④对于小偏心受压构件,当弯矩M 值基本不变时,轴力N 值越大所需的纵向钢筋越多4.在设计计算螺旋钢箍轴心受压构件的承载力时,不考虑间接钢筋影响的条件是:( )。
①长细比d l /0<12(d 为构件圆形截面的直径)②间接钢筋的换算截面面积0ss A 小于纵向钢筋全部截面面积的25% ③按螺旋钢箍轴心受压构件计算的受压承载力小于按普通钢箍轴心受压构件计算的受压承载力 ④按螺旋钢箍轴心受压构件计算的受压承载力大于按普通钢箍轴心受压构件计算的受压承载力5.为了保证钢筋混凝土受弯构件的安全性,( )。
西安建筑科技大学考试试卷B卷答案与评分标准(共2页)评卷人填写

+
140 1 180 1 [1 − ] ÷ (1 + 14%)3 + [1 − ] ÷ (1 + 14%)8 5 4 14% (1 + 14%) 14% (1 + 14%)
−
20 360 + 12 (1 + 14%) (1 + 14%)12
=180.71(万元)
5 分(说明:计算公式表达正确占 2 分,计算过程 占 2 分;计算结果占 1 分)
项目的自然地理位置是不可移动的,房地产项目不能脱离周围的环境而单独存在,因此强调 位置对房地产投资的重要性。火车站区域位置佳,人流量大,适合做商业用途, “支持投资计划” 的观点是可以理解的,但是没有考虑到火车站改迁后未来区域经济环境变化的风险。 分) (5 但是,在房地产开发中,更应该关注项目的经济地理位置。项目的经济地理位置可以随着社 会经济等因素的变化发生移动,火车站将来要改迁,应当充分考虑到火车站区域的城市经济要素 会发生变化。因此, “建议放弃投资计划”的观点充分考虑到未来经济环境变化带来的风险。 (5 分) 由于房地产资产的不可移动性,实践工作中在进行投资决策时,在关注项目自然地理位置的 同时,应更关注项目的经济地理位置,着重考虑未来的地区环境的可能变化,通过对城市规划、 市政规划等的了解和分析,就可以做到正确并有预见性地选择投资地点。 (10 分)
1 2
答案与评分标准( 西安建筑科技大学考试试卷 B 卷答案与评分标准(共 2 页)
班级: 班级: 姓名: 姓名: 考试科目: 考试科目:房地产开发与经营
解: (1) FNPV = −150 −
学号: 学号:
150 120 20 20 30 − − − − 2 4 9 1 + 14% (1 + 14% ) (1 + 14% ) (1 + 14% ) (1 + 14% )12
西安建筑科技大学2011微原复试题

2011年招收攻读硕士学位研究生入学考试复试试题(答案书写在本试题纸上无效。
考试结束后本试题纸须附在答题纸内交回 ) 微机原理共5页姓名考号一、选择题(每小题1分,共10分)1.内存又称主存,相对于外存来说,它的特点是()。
A.存储量大,价格高,存取速度快B.存储量小,价格低,存取速度慢C.存储量大,价格低,存取速度快D.存储量小,价格高,存取速度快2.断电后存储的资料会丢失的存储器是()。
A.RAM B.ROM C.CD-ROM D.硬盘3.需要进行刷新的存储器是( )。
A.SRAM B.DRAM C.ROM D.EPROM4.以下程序的功能是()。
MOV AH, 09HINT 21HA.在屏幕上显示单个字符B.字符打印C.控制台输入和输出D.在显示器上显示字符串.5.有关伪指令语句叙述不正确的是()。
A.本身不会产生可执行的机器指令代码B.它告诉汇编程序有关源程序的某些信息C.它有时用来说明内存单元的用途D.伪指令在汇编过程中没有经过汇编程序处理.6.若标志寄存器的奇偶标志位PF置“1”反映操作()。
A.结果是偶数B.结果是奇数C.结果中“1”的个数为偶数D.结果中“1”的个数为奇数7.用来表示堆栈指针的寄存器是()。
A.IP B.BP C.SP D.SS8.在DMA方式下,CPU与总线的关系是()。
A.只能控制数据总线B.只能控制地址总线C.成隔离状态D.成短接状态9.一个汇编语言源程序由若干个逻辑段组成,每个逻辑段以()语句开始。
A.BEGIN B.SEGMENT C.END D.START 10.指令MOV AX, [1000H]的源寻址方式是()。
A.变址寻址B.寄存器寻址C.基址变址D.直接寻址二、简答题(25分)1.2010年我国在超级计算机的研发上取得了那些成就?(8分)2.中断控制器8259A上最多可接多少个中断源,它们的优先级别是如何规定的?(4分)3.许多CPU总线都采用了时分复用技术,请说明什么叫时分复用地址/数据总线,它有什么优点?(4分)4.Intel数据收发器8287芯片如图所示,说明每个管脚的功能。
西安建筑科技大学管理科学与工程复试问题及答案

西安建筑科技大学管理科学与工程复试问题及答案1、鱼鳔变大时,鱼肚子会被鱼鳔撑大,鱼就能()。
[单选题] *A.上浮(正确答案)B.下沉C.保持原高度2、动物和植物都是由细胞构成的,微生物不是由细胞构成的。
[单选题] *A.对B.错(正确答案)3、27、自然界的水是循环往复的,所以不必节约用水。
[判断题] *对错(正确答案)4、物体因运动具有的能量是动能;储存在食物,燃烧中的能量是化学能[判断题] *对(正确答案)错5、下面关于能量的说法,正确的一项是()。
[单选题] *A.电风扇在工作时将电能转化为热能B.电视机和电视遥控器使用的电都是由发电厂提供的C.电动机用途很广,大至重型机器,小至儿童玩具,都有其踪迹(正确答案)6、不属于我们的相貌特征的是( )。
[单选题] *A.有耳垂B.平发际C.烫成卷发(正确答案)7、植物的生长需要一定的环境,当环境改变后,植物会努力适应环境的变化。
[判断题] *对(正确答案)错8、下列说法正确的是()。
[单选题] *A.汽车反光镜运用了光在空气中沿直线传播的原理B.我们在小孔成像的实验中看到的像是正立的C.关闭台灯,台灯不能发光,所以关闭后的台灯不是光源(正确答案)9、下列物质中,传热能力最强的物质是( )。
[单选题] *A.铁(正确答案)B.塑料C.卡纸10、物质在发生化学变化时不一定会发生物理变化。
( ) [单选题]对错(正确答案)11、日食是当太阳、地球和月球在同一条直线时,地球在中间挡住了太阳照向月球的光。
[判断题] *对错(正确答案)12、宇宙太遥远、太神秘,对它的探索是科学家的事,我们学生的任务是先学好知识,将来有机会再去关注。
[判断题] *对错(正确答案)13、用弹珠来模拟船上面的货物时,我们会发现弹珠会滚动,导致船容易侧翻,所以可以将船舱设计成分格结构。
[判断题] *对(正确答案)错14、小兰家的“菜园生态系统”主要是由()组成的。
[单选题] *A.菜园里所有的植物和动物B.菜园里所有的动物和阳光C.菜园里所有的生物及非生物(正确答案)15、宇宙有银河系和河外星系两个星系。
最新西安建筑科技大学研究生复试混凝土笔试真题(word版)

西安建筑科技大学研究生复试混凝土笔试真题(w o r d版)------------------------------------------作者xxxx------------------------------------------日期xxxx2014年硕士学位研究生复试笔试试题考试科目:钢筋混凝土结构适用专业:结构工程、防灾减灾工程及防护工程、现代结构理论、桥梁与隧道工程、建筑与土木工程一、名词解释(每小题3分,共15分)1、剪跨比2、塑性铰3、结构的可靠度4、等高排架5、反弯点二、填空题(每空1分,共15分)1、在适筋梁正截面受力的整个过程中,第II阶段是验算的依据,III a状态是计算的依据.2、钢筋混凝土梁的斜截面受剪承载力计算公式是以破坏形态为依据建立的。
3、按弹性理论计算连续梁、板的内力时,中间跨的计算跨度一般取之间的距离;按塑性理论计算时,中间跨的计算跨度一般取。
4、采用D值法计算框架柱的刚度时,梁线刚度越大,则节点的约束能力越强,柱的侧向刚度越。
5、四边支承双向板上均布荷载向两个方向的支承梁传递,其中长边支承梁承受的荷载为分布,短边支承梁承受的荷载为分布.6、全现浇框架计算简图中,框架梁截面形心线近似取至,底层柱底固定于.(本题答案:板底;基础顶面.)7、受弯构件斜截面受剪承载力计算时,验算最小配筋率是为了避免发生破坏;对构件截面尺寸进行验算是为了避免发生破坏.8、双筋梁正截面承载力验算中,当不满足x≥2a′时,说明。
s9、水平荷载作用下,框架结构的侧移由两部分组成:由变形引起的侧移为总体剪切变形,由变形引起的侧移为总体弯曲变形。
三、判断题(每题1分,共10分)1、钢筋混凝土构件中,钢筋与混凝土的粘结强度越好,裂缝间距越大,裂缝宽度越小. ()2、混凝土在双轴复合受压应力状态下,双轴等压时抗压强度不是最大。
( )3、混凝土非均匀受压时,用等效应力图形代替实际压应力分布的等效原则是,混凝土压应力的全力大小相等,合力的作用位置不变。
西安建筑科技大学历年复试试题

西安建筑科技大学历年复试试题2002复试题(给水工程)一,名词解释(每题4分,7选6)1水质标准及水质参数2分子扩散传递3聚合氯化铝的碱化度4自由沉淀5均质滤料6(电渗析的)浓差极化7循环冷却水的浓缩系数二,计算题(每题8分)1某水厂生产规模为50000m3/d,以河水为水源。
河水总碱度0.12mmol/L(按CaO计)。
硫酸铝(含Al2O3为16%)投加量为24mg/L.问为保证硫酸铝水解,每天约需要投加多少千克石灰?(石灰纯度按50%计,剩余碱度为0.35mmol/L(按CaO计))。
2试计算粒径为0.40mm,密度为1.03g/cm3的颗粒沉速。
设平流式沉淀池的有效水深为3.2米,水平流速为0.4m/min。
要将上述颗粒全部从水中去除,沉淀池的长度最少得多少米?此时,粒径为0.36mm的同类颗粒的去除率是多少?(已知水温为15oC,这时水的密度为0.999g/cm33,水的动力粘滞系数为1.55102cm2/)三问答题(每题12分,6选5)1简述DLVO理论,并讨论其使用范围2试述浅沉池理论,并对斜管(板)沉淀池与平流沉淀池的特点进行分析比较3试述滤池小阻力配水系统的均匀配水原理,说明在什么情况下必须采用小阻力配水系统,并说明其基本构造。
4试结合不同的水质特点,分析加氯量与余氯量之间的关系。
(要求绘图说明)5简述混合床除盐的基本原理及特点6写出逆流冷却塔热力计算基本方程,并对方程中参数的物理意义做简要解释2002复试题(排水工程)一名词解释(20分)1水环境容量2BOD污泥负荷率3临界点4.DOC5SVI6底(下)流固体通量Gu7污泥投配率n8污泥比阻r9化学沉淀10吸附等温式二选择(共二十分,少选和多选无分)1污水处理的出路是()A重复利用B排放水体C回灌地下水D灌溉农田E降低BOD,DOC2按物理形态,污水中的污染物质可分为()A有机污染物质B溶解性污染物质C胶体污染物质D无机污染物质E 悬浮固体3水体自净过程中的作用因素有(),净化的主要作用()A物理作用B水生物作用C生化作用D微生物吸附作用E化学和物化作用4一般情况下,污水中悬浮固体颗粒粒径为(),胶体颗粒粒径为(),溶解性污染物质颗粒粒径为()。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第17 次课 2 学时第18 次课 2 学时第19 次课 2 学时第七章气态污染物控制技术基础第一节气体吸收一、吸收机理1. 双膜模型(应用最广)假定:(1)界面两侧存在气膜和液膜,膜内为层流, 传质阻力只在膜内(2)气膜和液膜外湍流流动,无浓度梯度, 即无扩散阻力(3)气液界面上,气液达溶解平衡即:C A i=HP A i(4)膜内无物质积累,即达稳态.2. 渗透模型假定:(1)气液界面上的液体微元不断被液相主体中浓度为C AL的微元置换(2)每个微表面元与气体接触时间都为τ(3)界面上微表面元在暴露时间τ内的吸收速率是变化的3. 表面更新模型假定:(1)各表面微元具有不同的暴露时间,t=0-∞(2)各表面元的暴露时间(龄期)符合正态分布4. 其它模型如:表面更新模型的修正;基于流体力学的传质模型;界面效应模型。
5. 双膜理论(1)双膜模型气相分传质速率N A=k y(y A-y Ai)N A=k y(p A-p Aj)液相分传质速率N A=k x(x Ai- x A)N A=k y(c Aj- c A)总传质速率方程N A =K y (y A - y *A ) N A =K x (x A *-x A )N A =K ai (p A -p A *)(2)气液平衡常见气体平衡溶解度亨利定律:一定温度下,稀溶液中溶质的溶解度与气相中溶质的平衡分压成正比(3)吸收系数吸收系数的不同形式见下图:x AL(4)传质阻力传质阻力-吸收系数的倒数传质阻力=气相传质阻力+液相传质阻力(5)传质过程吸收质与吸收剂;设备、填料类型;流动状况、操作条件二、物理吸收吸收过程如图所示:操作线、平衡线吸收推动力见图。
吸收塔的最小液气比见图三、化学吸收1. 化学吸收的优点:(1)溶质进入溶剂后因化学反应消耗掉,溶剂容纳的溶质量增多(2)液膜扩散阻力降低(3)填料表面的停滞层仍为有效湿表面两分子反应中相界面附近液相内A与B的浓度分布图第20 次课 2 学时●第二节气体吸附●吸附用多孔固体吸附剂将气体(或液体)混合物中的组分浓集于固体表面 吸附质-被吸附物质吸附剂-附着吸附质的物质●优点:效率高、可回收、设备简单●缺点:吸附容量小、设备体积大吸附机理物理吸附和化学吸附物理吸附和化学吸附•同一污染物可能在较低温度下发生物理吸附•若温度升高到吸附剂具备足够高的活化能时,发生化学吸附●吸附剂需具备的特性内表面积大具有选择性吸附作用高机械强度、化学和热稳定性吸附容量大来源广泛,造价低廉良好的再生性能常用吸附剂特性:分子筛特性●操作条件低温有利于物理吸附;高温利于化学吸附增大气相压力利于吸附●吸附质性质、浓度临界直径-吸附质不易渗入的最大直径吸附质的分子量、沸点、饱和性●吸附剂活性单位吸附剂吸附的吸附质的量静活性-吸附达到饱和时的吸附量动活性-未达到平衡时的吸附量常见分子的临界直径气体吸附的影响因素 吸附剂再生吸附剂再生吸附平衡第23 次课 2 学时注:本页为每次课教案首页第九章氮氧化物污染控制主要内容:♌1. 氮氧化物的性质及来源♌2. 燃烧过程中氮氧化物的形成机理♌3. 低氮氧化物燃烧技术♌4. 烟气脱硝技术第一节氮氧化物的性质及来源♌NO x包括:N2O、NO、N2O3、NO2、N2O4、N2O5大气中NO x主要以NO、NO2的形式存在♌NO x的性质:N2O:单个分子的温室效应为CO2的200倍,并参与臭氧层的破坏NO:大气中NO2的前体物质,形成光化学烟雾的活跃组分NO2: 强烈刺激性,来源于NO的氧化,酸沉降♌NO x的来源固氮菌、雷电等自然过程(5×108t/a)人类活动(5×107t/a)▪燃料燃烧占95%。
主要来自:各种锅炉、焙烧炉、窑炉等的燃烧过程;机动车尾气排放。
▪其他: 硝酸生产和各种硝化过程(如化肥厂);冶金行业中的炼焦、烧结、冶炼等高温过程;金属表面的硝酸处理。
95%以NO形式,其余主要为NO2。
▪第二节 燃烧过程NO x 的形成机理♌形成机理1. 燃料型NO x燃料中的固定氮生成的NO x2. 热力型NO x高温下N 2与O 2反应生成的NO x3. 瞬时NO低温火焰下由于含碳自由基的存在生成的NO♌热力型NO x 的形成产生NO 和NO 2的两个重要反应平衡常数和平衡浓度()()2222N O 2NO 11NO O NO 22−−→+←−−−−→+←−−平衡时NO浓度随温度升高迅速增加。
♌ 上述数据说明:1) 室温条件下,几乎没有NO 和NO2生成,并且所有的NO 都转化为NO2; 2) 800K 左右,NO 与NO2生成量仍然很小,但NO 生成量已经超过NO2; 3) 常规燃烧温度(>1500K )下,有可观的NO 生成,但NO2量仍然很小; 4) 平衡时NO 浓度随温度升高而迅速增加; 5) 较低空气过剩系数有利于控制NOx 的形成。
烟气冷却过程中,根据热力学计算,NO x 应主要以NO2的形式存在,但实际90%~95%的NO x 以NO 的形式存在,主要原因在于动力学控制。
NO/NO x Ratioboilervehicles nature gas 0.9~1.0 internal comb. engine 0.99~1.0 coal 0.95~1.06# fuel oil0.96~1.0 diesel engine 0.77~1.0♌ 热力型NO x 形成的动力学——Zeldovich 模型NO 生成的总速率♌ 假定N 原子的浓度保持不变得到代入(6)式得♌ 假定O 原子的浓度保持不变2424552452242p,NO 22452d[NO][N ]([NO]/[O ])2[O]d 1([NO]/[O ])2[O][N ]{1[NO]/([N ][O ])}=1([NO]/[O ])k k k k t k k k K k k -----=+-+425452[O][N ][O][NO][N][NO][O ]k k k k --+=+稳态424552d[N][O][N ][N][NO][O][NO][N][O ]0d k k k k t --=-+-=424525d[NO][O][N ][N][NO][N][O ][O][NO] (6)d k k k k t --=-+-121222N O N O N (4)N O N O O (5)+-+-+⇔++⇔+2O M 2O M (3)+⇔+♌ 最终得♌ 积分得NO 的形成分数Y 与时间t 之间的关系各种温度下形成NO 的浓度-时间分布曲线11(1)(1)exp()c c Y Y Mt +--+=-21/24p,O 21/21/2p,NO 1/21/24p,NO 21/252ed (1)d 2(1)4[N ]()()()[N ][O ][NO]/[NO]Y M Y x CY k K M RT K k K C k Y --=+===1/22e p,NOe 1/2[O ][O]()K RT=在各种温度下NO 浓度随时间的变化曲线(N 2/O 2=40:1)♌ 根据泽利多维奇预测结果:♌ 压力对M 值影响较弱,温度影响较强,即影响NO 生成总量,也影响NO 生成速率; ♌ 在相同停留时间,不同温度下NO 生成速率有显著差别;♌ 为减少NO 生成量,可采取降低火焰区温度和后火焰区温度,减少停留时间的途径。
瞬时NO 的形成:♌碳氢化合物燃烧时,分解成CH 、CH 2和C 2等基团,与N 2发生如下反应♌ 火焰中存在大量O 、OH 基团,与上述产物反应:小结:♌ 低温火焰中生成的NO 的量明显高于泽氏预测的结果. 因此,低温火焰中形成的NO 多为瞬时NO ;♌ 瞬时NO 生成量平均为30g/GJ 。
燃料型NO x 的形成:♌燃料中的N 通常以原子状态与HC 结合,C —N 键的键能较N ≡N 小,燃烧时容易分解,经氧化形成NO x ;♌火焰中燃料氮转化为NO 的比例取决于火焰区NO/O 2的比例;♌燃料中20%~80%的氮转化为NO x 。
2222HCN OH CN H O CN O CO NO CN O CO N NH OH N H O NH O NO H N OH NO H N O NO O+→++→++→++→++→++→++→+22222CH N HCN N CH N HCN NH C N 2CN+→++→++→第24 次课 2 学时第三节低NO x燃烧技术原理♌控制NO x形成的因素空气-燃料比燃烧区温度及其分布后燃烧区的冷却程度燃烧器形状低NO x燃烧技术♌传统低NO x燃烧技术1. 低氧燃烧▪降低NO x的同时提高锅炉热效率▪CO、HC、碳黑产生量增加▪♌2. 降低助燃空气预热温度燃烧空气由27o C 预热到315o C ,NO 排放量增加3 倍3. 烟气循环燃烧采用燃烧产生的部分烟气冷却后,再循环送回燃烧区,起到降低氧浓度和燃烧区温度(主要减少热力型NO x)的作用,以达到减少NO生成量的目的.烟气循环率25%-40%。
♌4. 两段燃烧技术第一段:氧气不足,烟气温度低,NO x生成量很小第二段:二次空气,CO、HC完全燃烧,烟气温度低先进的低NO x燃烧技术♌原理:低空气过剩系数运行技术+分段燃烧技术1. 炉膛内整体空气分级的低NO x直流燃烧器▪炉壁设置助燃空气(OFA,燃尽风)喷嘴▪类似于两段燃烧技术▪要求:▪合理确定燃尽风喷口与最上层煤粉喷口的距离▪燃尽风量要适当▪燃尽风应有足够高的流速,以便能与烟气充分混合.先进的低NO x燃烧技术♌2. 空气分级的低NO x旋流燃烧器既要控制燃料型NOx和热力型NOx的生成,又要具有较高的燃烧效率. 一次火焰区:富燃,含氮组分析出但难以转化二次火焰区:燃尽CO、HC等♌3. 空气/燃料分级的低NO x燃烧器空气和燃料均分级送入炉膛一次火焰区下游形成低氧还原区,还原已生成的NO x为氮气。
第四节烟气脱硝技术♌脱硝技术的难点处理烟气体积大NO x浓度相当低NO x的总量相对较大♌1.选择性催化还原法(SCR )催化剂:贵金属、碱性金属氧化物 还原反应潜在氧化反应♌还原剂: NH 3 (常用) 、H 2S 、 CO♌反应特点:♌使氨能有选择的和气体中的NO X 进行反应,而不和氧反应。
♌常用催化剂: ♌1)贵金属 2)非贵金属的氧化物或盐类 Cu 、Cr 、Fe 、V 、Mn♌优点: ♌1)还原剂基本上不与氧反应,避免了无谓消耗,同时大大减小了反应热,催化床温度变化小易于控制,采用一段流程即可;♌2) 催化剂易得,选择余地大;♌3)还原剂NH 3相对易得,起燃温度低反应热低,床温通常低于3000C,有利于延长催化剂寿命和降低反应器对材料要求。
