武汉大学第五版仪器分析-----红外
武大仪器分析知识点总结考研,期末复习

第一部分:AES,AAS,AFSAES原子发射光谱法是根据待测元素的激发态原子所辐射的特征谱线的波长和强度,对元素进行定性和定量测定的分析方法。
特点:1.灵敏度和准确度较高2.选择性好,分析速度快3.试样用量少,测定元素范围广4.局限性(1)样品的组成对分析结果的影响比较显着。
因此,进行定量分析时,常常需要配制一套与试样组成相仿的标准样品,这就限制了该分析方法的灵敏度、准确度和分析速度等的提高。
(2)发射光谱法,一般只用于元素分析,而不能用来确定元素在样品中存在的化合物状态,更不能用来测定有机化合物的基团;对一些非金属,如惰性气体、卤素等元素几乎无法分析。
(3)仪器设备比较复杂、昂贵。
术语:自吸自蚀•击穿电压:使电极间击穿而发生自持放电的最小电压。
•自持放电:电极间的气体被击穿后,即使没有外界的电离作用,仍能继续保持电离,使放电持续。
•燃烧电压:自持放电发生后,为了维持放电所必需的电压。
由激发态直接跃迁至基态所辐射的谱线称为共振线。
由较低级的激发态(第一激发态)直接跃迁至基态的谱线称为第一共振线,一般也是元素的最灵敏线。
当该元素在被测物质里降低到一定含量时,出现的最后一条谱线,这是最后线,也是最灵敏线。
用来测量该元素的谱线称分析线。
仪器:光源的作用: 蒸发、解离、原子化、激发、跃迁。
光源的影响:检出限、精密度和准确度。
光源的类型:直流电弧交流电弧电火花电感耦合等离子体(ICP)光源蒸发温度激发温度/K 放电稳定性应用范围直流电弧高4000~7000 较差定性分析,矿物、纯物质、难挥发元素的定量分析交流电弧中4000~7000 较好试样中低含量组分的定量分析火花低瞬间10000 好金属与合金、难激发元素的定量分析ICP 很高6000~8000 最好溶液的定量分析ICP原理当高频发生器接通电源后,高频电流I通过感应线圈产生交变磁场(绿色)。
开始时,管内为Ar气,不导电,需要用高压电火花触发,使气体电离后,在高频交流电场的作用下,带电粒子高速运动,碰撞,形成“雪崩”式放电,产生等离子体气流。
武汉大学第五版仪器分析-----红外

距相比)作周期性“简谐”振动,其振动可用经典刚性振动描述:
1 ( 频率 ) 2
1 .......... 或 ( 波数 ) ....... 2c
k
k
k为化学键的力常数(N/cm = mdyn/Å),为双原子折合质量
吸收光子的能量(ha )要与该能量差相等,即a= V时,才可 能发生振转跃迁。例如当分子从基态(V=0)跃迁到第一激发态 (V=1),此时V=1,即a=
条件二:辐射与物质之间必须有耦合作用
电场
无偶极矩变化
磁场
无红外吸收
红外吸收
偶极矩变化
交变磁场
分子固有振动
a
(能级跃迁)
2. 分子振动
C CH3
C CH 3 CH 3
O
C=O=1663cm-1
C=O=1686cm-1
空间效应的另一种情况是张力效应:四元环>五元环>六元 环。随环张力增加,红外峰向高波数移动。
6)物质状态及制样方法 通常,物质由固态向气态变化,其波数将增加。如丙酮在液 态时, C=O=1718cm-1; 气态时 C=O=1742cm-1 ,因此在查阅标准 红外图谱时,应注意试样状态和制样方法。
依存、相互佐证。通过一系列的峰才能准确确定一个基团
的存在。
常见基团的红外吸收带
=C-H O-H CC C=C C=O C-C,C-N,C-O N-O N-N C-F C=N C-H,N-H,O-H C-X
C-H
O-H(氢键)
S-H P-H CN
N-H
3500
3000
2500
2000
武汉大学第五版仪器分析仪器分析讲义

仪器分析讲义绪论(Introduction)仪器分析是化学类专业必修的基础课程之一。
通过本课程的学习,要求学生把握经常使用仪器分析方式的原理和仪器的简单结构;要求学生初步具有依照分析的目的,结合学到的各类仪器分析方式的特点、应用范围,选择适宜的分析方式的能力。
分析化学是研究物质的组成、状态和结构的科学。
它包括化学分析和仪器分析两大部份。
化学分析是指利用化学反映和它的计量关系来确信被测物质的组成和含量的一类分析方式。
测按时需利用化学试剂、天平和一些玻璃器皿。
它是分析化学的基础。
仪器分析是以物质的物理和物理化学性质为基础成立起来的一种分析方式,测按时,常常需要利用比较复杂的仪器。
它是分析化学的进展方向。
仪器分析与化学分析不同,具有如下特点:(1)灵敏度高,检出限量可降低。
如样品用量由化学分析的ml、mg级降低到仪器分析的µL、µg级,乃至更低。
它比较适用于微量、痕量和超痕量成份的测定。
(2)选择性好。
很多仪器分析方式能够通过选择或调整测定的条件,使共存的组分测按时,彼其间不产生干扰。
(3)操作简便、分析速度决,易于实现自动化。
(4)相对误差较大。
化学分析一样可用于常量和高含量成份的分析,准确度较高,误差小于千分之儿。
多数仪器分析相对误差较大,一样为5%,不适于常量和高含量成份的测定。
(5)需要价钱比较昂贵的专用仪器。
§1-1.仪器分析方式的内容和分类(Classification of Instrumental Analysis)分类:1.光学分析法以物质的光学性质为基础的分析方式(1) 分子光谱: 红外吸收可见和紫外分子荧光拉曼光谱(2) 原子光谱: 原子发射AES 原子吸收AAS 原子荧光AFS(3) X射线荧光: 发射吸收衍射荧光电子探针(4) 核磁共振顺磁共振2.电化学分析法溶液的电化学性质用于确信物质化学成份的方式(1)电导法:电导分析法电导确信物质的含量电导滴定法溶液的电导转变确信容量分析的滴定终点。
(完整版)武汉大学版仪器分析知识点总结(适用考中科院的同学)
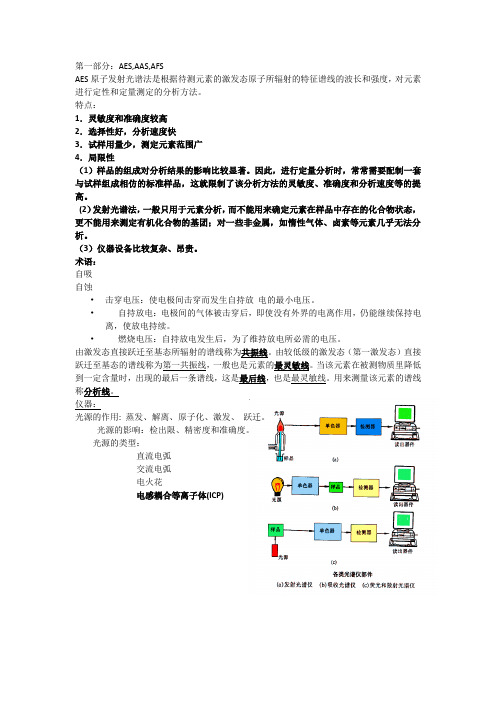
①. 自然宽度ΔυN 它与原子发生能级间路迂时激发态原子的有限寿命有关。 一般情况下约相当于 10-4 Å
②. 多普勤(Doppler)宽度ΔυD 这是由原子在空间作无规热运动所引致的。故又称热变宽。
碰撞变宽:原子核蒸气压力愈大,谱线愈宽。 同种粒子碰撞——赫尔兹马克(Holtzmank)变宽, 异种粒子碰撞——称罗论兹(Lorentz)变宽。 场致变宽:在外界电场或磁场的作用下,引起原子核外层电子能级分裂而使谱线变宽现象称 为场致变宽。由于磁场作用引起谱线变宽,称为 Zeeman (塞曼)变宽。
例如砷、锑、铋、锗、锡、铅、硒和碲等元素。 固体试样
(1). 试样直接插入进样 (2). 电弧和火花熔融法 (3). 电热蒸发进样 (4). 激光熔融法 分光仪棱镜和光栅 检测器:目视法,摄谱法,光电法 干扰:
光谱干扰: 在发射光谱中最重要的光谱干扰是背景干扰。带状光谱、连续光谱以及光学系统的
杂散光等,都会造成光谱的背景。 非光谱干扰:
与试样组成相仿的标准样品,这就限制了该分析方法的灵敏度、准确度和分析速度等的提
高。
(2)发射光谱法,一般只用于元素分析,而不能用来确定元素在样品中存在的化合物状态,
更不能用来测定有机化合物的基团;对一些非金属,如惰性气体、卤素等元素几乎无法分
析。
(3)仪器设备比较复杂、昂贵。
术语:
自吸Biblioteka 自蚀• 击穿电压:使电极间击穿而发生自持放 电的最小电压。
交流电弧 中
火花
低
4000~7000 较差 4000~7000 较好 瞬间 10000 好
定性分析,矿物、纯物质、 难挥发元素的定量分析
试样中低含量组分的定量分 析
武汉大学分析化学(第五版)总结

分析化学(第五版)总结分析化学(第五版)总结第1章绪论分析化学的定义分析化学是发展和应用各种理论、方法、仪器和策略以获取有关物质在相对时空内的组成和性质的信息的一门科学分类标准任务定性分析鉴定物质化学组成(元素、原子团、化合物)定量分析测定物质中有关成分的含量结构分析确定物质化学结构(分子、晶体、综合形态)原理化学分析定义以化学反应为为基础的分析方法分类定性分析定量分析重量分析用称量方法求得生成物W重量滴定分析从与组分反应的试剂R的浓度和体积求得组分C的含量特点仪器简单,结果准确,灵敏度较低,操作繁琐,分析速度较慢,适于常量组分分析(质量分数在1%以上)仪器分析定义以物质的物理或物理化学性质为基础建立起来的分析方法特点灵敏,快速,准确,易于自动化,仪器复杂昂贵,适于微量、痕量组分分析对象无机分析、有机分析、冶金分析、地质分析、环境分析、药物分析、生物分析用量用量及操作规模常量分析>100mg>10ml半微量10~100mg10~1ml微量0.1~10mg0.01~1ml超微量<0.1mg<0.01ml待测组分含量常量分析>1%微量分析0.01%~1%痕量分析<0.01%超痕量分析约0.0001%分析的性质例行分析一般分析实验室对日常生产流程中的产品性质指标进行检查控制的分析仲裁分析不同企业部门间对产品质量和分析结果有争议时,请权威的分析测试部门进行裁判的分析分析方法的选择测定的具体要求,待测组分及其含量范围,欲侧组分的性质获取共存组分的信息并考虑共存组分对测定的影响,拟定合适的分离富集方法,以提高分析方法的选择性对测定准确度、灵敏度的要求与对策现有条件、测定成本及完成测定的时间要求等1.5.1分析化学的过程取样(采样、处理与分解)要使样品具有代表性,足够的量以保证分析的进行试样的制备(分离、富集)掩蔽加掩蔽剂富集沉淀分离、萃取分离、离子交换分离、色谱分离等分析测定要根据被测组分的性质、含量、结果的准确度的要求以及现有条件选择合适的测定方法。
武汉大学《分析化学》(第5版)(上册)笔记和课后习题(含考研真题)详解

武汉大学《分析化学》(第5版)(上册)笔记和课后习题(含考研真题)详解目录内容简介目录第1章概论1复习笔记2课后习题详解1.3名校考研真题详解第2章分析试样的采集与制备1复习笔记2课后习题详解2.3名校考研真题详解第3章分析化学中的误差与数据处理1复习笔记2课后习题详解3.3名校考研真题详解第4章分析化学中的质量保证与质量控制1复习笔记2课后习题详解4.3名校考研真题详解第5章酸碱滴定法1复习笔记2课后习题详解5.3名校考研真题详解第6章络合滴定法1复习笔记2课后习题详解6.3名校考研真题详解第7章氧化复原滴定法1复习笔记2课后习题详解7.3名校考研真题详解第8章沉淀滴定法和滴定分析小结1复习笔记2课后习题详解8.3名校考研真题详解第9章重量分析法1复习笔记2课后习题详解9.3名校考研真题详解第10章吸光光度法1复习笔记2课后习题详解10.3名校考研真题详解第11章分析化学中常用的别离和富集方法1复习笔记2课后习题详解11.3名校考研真题详解第第1章概论1.1复习笔记一、分析化学的定义分析化学是开展和应用各种理论、方法、仪器和策略以获取有关物质在相对时空内的组成和性质的信息的一门科学,又被称为分析科学。
二、分析方法的分类与选择1.分类〔1〕按分析要求定性鉴由哪些元素、原子团或化合物所组成。
定量测定中有关成分的含量。
结构分析:研究物质的分子结构、晶体结构或综合形态。
〔2〕按分析对象无机分析、有机分析。
〔3〕按测定原理化学分析:以物质的化学反响及其计量关系为根底,如重量分析法和滴定分析法等。
仪器分析:通过测量物质的物理或物理化学参数进行分析,如光谱分析、电化学分析等。
〔4〕按试样用量常量分析、半微量分析、微量分析、超微量分析。
〔5〕按工作性质例行分析、仲裁分析。
2.分析方法的选择对分析方法的选择通常应考虑以下几方面:〔1〕测定的具体要求,待测组分及其含量范围,欲测组分的性质;〔2〕获取共存组分的信息并考虑共存组分对测定的影响,拟定适宜的别离富集方法,以提高分析方法的选择性;〔3〕对测定准确度、灵敏度的要求与对策;〔4〕现有条件、测定本钱及完成测定的时间要求等。
武汉大学分析化学第五版总结54页PPT

决于尾数部分的位数,整数部分只代表方次 如:pH=11.02 [H+]=9.6×10-12 二位
3.3 分析化学中的数据处理
• 3.3.1 随机误差的正态分布
• 3.3.2 少量数据的统计处理
t 分布曲线 t xx n
sx
s
平均值的置信区间
xtsx
活度常数、浓度常数、混合常数
5.1.3溶液中的其他相关平衡
物料平衡
电荷平衡 质子条件
强酸(碱)+弱酸(碱)
弱酸(碱)+弱酸(碱) 共轭酸碱对
5.2.酸碱组分的平衡浓度与分布分数δ
5-3.水溶液中pH的计算 计算公式
1.强酸(碱)溶液: 2.一元弱酸(碱)溶液 3.多元酸(碱)溶液 4.混合酸(碱)溶液 5.两性物质
第三章 分析化学中的误差与 数据处理
3.1分析化学中的误差
3.1.1 准确度与精密度 3.1.2 误差与偏差
3.1.2.1 基本概念 3.1.2.2 误差:
绝对误差 相对误差
3.1.2.3 偏差
平均值 平均偏差 标准偏差
样本
总体
x
d
1 n
n
|
i1
xi
x|
xi
n
s
(xi x)2
5.4: 缓冲溶液
缓冲溶液pH值的计算 缓冲溶液的选择原则
5.5: 酸碱指示剂
指示剂变色原理 理论变色点: 理论变色范围 指示剂的选择原则
影响指示剂变色因素
5.6: 酸碱滴定法原理
滴定曲线,sp前,sp时,sp后pH计算 突跃范围,指示剂选择原则 准确滴定判别式 分别滴定判别式
分析化学 第五版 下册 (武汉大学主编 着) 高等教育出版社 课后答案 仪器分析习题答案-光谱分析部分

仪器分析部分作业题参考答案第一章绪论1-21、主要区别:(1)化学分析是利用物质的化学性质进行分析;仪器分析是利用物质的物理或物理化学性质进行分析;(2)化学分析不需要特殊的仪器设备;仪器分析需要特殊的仪器设备;(3)化学分析只能用于组分的定量或定性分析;仪器分析还能用于组分的结构分析;(3)化学分析灵敏度低、选择性差,但测量准确度高,适合于常量组分分析;仪器分析灵敏度高、选择性好,但测量准确度稍差,适合于微量、痕量及超痕量组分的分析。
2、共同点:都是进行组分测量的手段,是分析化学的组成部分。
1-5分析仪器与仪器分析的区别:分析仪器是实现仪器分析的一种技术设备,是一种装置;仪器分析是利用仪器设备进行组分分析的一种技术手段。
分析仪器与仪器分析的联系:仪器分析需要分析仪器才能达到量测的目的,分析仪器是仪器分析的工具。
仪器分析与分析仪器的发展相互促进。
1-7因为仪器分析直接测量的是物质的各种物理信号而不是其浓度或质量数,而信号与浓度或质量数之间只有在一定的范围内才某种确定的关系,且这种关系还受仪器、方法及样品基体等的影响。
因此要进行组分的定量分析,并消除仪器、方法及样品基体等对测量的影响,必须首先建立特定测量条件下信号与浓度或质量数之间的关系,即进行定量分析校正。
第二章光谱分析法导论2-1光谱仪的一般组成包括:光源、单色器、样品引入系统、检测器、信号处理与输出装置。
各部件的主要作用为:光源:提供能量使待测组分产生吸收包括激发到高能态;单色器:将复合光分解为单色光并采集特定波长的光入射样品或检测器;样品引入系统:将样品以合适的方式引入光路中并可以充当样品容器的作用;检测器:将光信号转化为可量化输出的信号。
信号处理与输出装置:对信号进行放大、转化、数学处理、滤除噪音,然后以合适的方式输出。
2-2:单色器的组成包括:入射狭缝、透镜、单色元件、聚焦透镜、出射狭缝。
各部件的主要作用为:入射狭缝:采集来自光源或样品池的复合光;透镜:将入射狭缝采集的复合光分解为平行光;单色元件:将复合光色散为单色光(即将光按波长排列)聚焦透镜:将单色元件色散后的具有相同波长的光在单色器的出口曲面上成像;2-7因为对于一级光谱(n=1)而言,光栅的分辨率为:36005720=×=×===光栅的刻痕密度光栅宽度N nN R 又因为:λλd R =所以,中心波长(即平均波长)在1000cm -1的两条谱线要被该光栅分开,它们相隔的最大距离为:cm -128.036001000===R d λλ2-10原子光谱是由原子外层电子在不同电子能级之间跃迁产生的,而不同电子能级之间的能量差较大,因此在不同电子能级之间跃迁产生的光谱的波长差异较大,能够被仪器分辨,所以显现线光谱;分子光谱的产生既包括分子中价电子在不同电子能级之间跃迁,也包括分子中振动能级和转动能级的跃迁,而振动能级和转动能级之间的能量差较小,在这些能级之间跃迁产生的光谱的波长非常接近,不能被仪器所分辨,所以显现为带光谱。
武汉大学化学系仪器分析课后习题答案

光谱分析导论习题解答1、解:(1)72101067.6101050.111⨯=⨯⨯==-λσ(2)14981047.4107.670/100.3/⨯=⨯⨯==-λνc(3)303010103300/1192=⨯⨯==-σλ(4)80.1)10602.1(1095.6889100.310626.6/1910834=⨯÷⨯⨯⨯⨯===---λνhc h E2、解:由计算公式λν/hc h E ==以及各能级跃迁所处的波长范围可得能量范围分别如下:跃迁类型 波长范围 能量范围/eV 原子内层电子跃迁 10-3nm ~10nm 1.26⨯106~1.2⨯102原子外层电子跃迁 200nm ~750nm 6~1.7 分子的电子跃迁 200nm ~750nm 6~1.7 分子振动能级的跃迁 2.5μm ~50μm 0.5~0.02 分子转动能级的跃迁50μm ~100cm2⨯10-2~4⨯10-7由上表可以看出分子电子能级跃迁1~20eV 分子振动能级跃迁0.05~1eV 分子转动能级跃迁<0.05eV ,其电子光谱,振动光谱以及转动光谱所对应的波长范围分别在紫外-可见区,红外区和远红外微波区。
3、解:棱镜的分光原理是光折射。
由于不同波长的光有其不同的折射率,据此能把不同波长的光分开。
光栅的分光原理是光的衍射与干涉的总效果。
不同波长的光通过光栅作用各有相应的衍射角,据此把不同波长的光分开。
光栅光谱棱镜光谱Sin φ与波长成正比,所以光栅光谱是一个均匀排列的光谱色散率与波长有关,为非均匀排列的光谱 光的波长越短则衍射角越小,因此其谱线从紫到红排列波长越短,其偏向角越大,因此其谱线从红到紫排列复合光通过光栅后,中央条纹(或零级条纹)为白色条纹,在中央条纹两边,对称排列着一级、二级等光谱,由于谱线间距离随光谱级数的增加而增加,出现谱级重叠现象没有谱级重叠现象光栅适用的波长范围比棱镜宽4、解:v cn r i ==θθsin sin ,式中n 为折射率,i θ为入射角,r θ为折射角,c 为光速,v 为玻璃介质中的传播速度。
武汉大学《分析化学》(第5版)(下册)课后习题(光谱分析法导论) 【圣才出品】

第2章 光谱分析法导论2-1 光谱仪一般由几部分组成?它们的作用分别是什么?答:(1)光谱仪的一般由稳定的光源系统、波长选择系统、试样引入系统、检测系统以及信号处理和读出系统组成。
(2)它们的作用分别是:①光源系统:提供足够的能量使试样蒸发、原子化、激发,产生光谱;②波长选择系统(单色器、滤光片):将复合光分解成单色光或有一定宽度的谱带;③试样引入系统:将样品以合适的方式引入光路中并充当样品容器;④检测系统:将光信号转化为可量化输出的信号;⑤信号处理和读出系统:对信号进行放大、转化、数学处理、滤除噪音,然后以合适的方式输出。
2-2 单色器由几部分组成,它们的作用分别是什么?答:(1)单色器的组成部分包括入射狭缝、准直装置、色散装置、聚焦透镜或凹面反射镜、出射狭缝。
(2)各部件的主要作用是:①入射狭缝:采集来自光源或样品池的复合光;②准直装置:将入射狭缝采集的复合光分解为平行光;③色散装置:将复合光色散为单色光(即将光按波长排列);④聚焦透镜或凹面反射镜:将单色元件色散后的具有相同波长的光在单色器的出口曲面上成像;⑤出射狭缝:采集色散后具有特定波长的光入射样品或检测器。
2-3 简述光栅和棱镜分光的原理。
答:(1)光栅的分光原理是光的衍射与干涉的总效果,不同波长的光通过光栅作用各有相应的衍射角,据此把不同波长的光分开;(2)棱镜的分光原理是光折射,由于不同波长的光有其不同的折射率,据此能把不同波长的光分开。
2-4 简述光电倍增管的作用原理。
答:光电倍增管的作用原理为:当光照射到光阴极时,光阴极向真空中激发出光电子。
这些光电子按聚焦极电场进入倍增系统,并通过进一步的二次发射得到倍增放大。
然后把放大后的电子用阳极收集作为信号输出。
2-5 对下列单位进行换算:(1)150pm X 射线的波数(cm -1);(2)Li 的670.7nm 谱线的频率(Hz );(3)3300cm -1波数对应的波长(nm );(4)Na 的588.995nm 谱线相应的能量(eV )。
分析化学(武汉大学 第五版)

造成
例如:沉淀不完全、滴定反应中有干扰离子
减免方法:
对照试验-用同样方法对标样分析,然后将分析结果 与标准值对照,从差值判断方法误差大小
ICM MP China PM
Shanghai
University
② 仪器、试剂误差 -由仪器本身缺陷、试剂不纯、器皿的质量问 题而引起。 例如:蒸馏水不纯、容量瓶刻度不准 减免方法:
ICM MP China PM
二、重量分析
Shanghai
University
1.步骤:称试样w1→溶解→定量转化成难溶 化合物→过滤→洗涤→干燥→灼烧 →称重w2→根据w1、w2间接 计算试 样含量 例:测试样中Ba2+含量 2.特点:速度慢、操作复杂、设备简单 3.要求:分析精度在0.1~0.2%之间
ICM MP China PM
§1-2 分析化学中的误差
Shanghai
University
一、定量分析中的误差和表示法 ⑴ 准确度和误差 准确度—表示分析结果与真值之间的接近 程度。大小用误差E表示 准确度和误差关系: E小,表示测定结果真值接近,准确度高 E大,表示测定结果真值差距大,准确度低 说明:⑴误差有正负 ⑵误差有绝对、相对之分 相对误差能反映准确度的大小
Shanghai
University
◆重量百分数-被测组分在试样中所占白分 数(W/G×100%) ◆体积百分数-100mL溶液中所含被测组分 体积(V/V) ◆如被测组分含量很低,常用ppm、 ppb表 示 1 PPm等于106份试样中含1份被测组分。 1 PPb等于109份试样中含1份被测组分。
ICM MP China PM
⑵ 精密度和偏差
偏差di
Shanghai
武汉大学第五版仪器分析-----红外.48页PPT

61、奢侈是舒适的,否则就不是奢侈 。——CocoCha nel 62、少而好学,如日出之阳;壮而好学 ,如日 中之光 ;志而 好学, 如炳烛 之光。 ——刘 向 63、三军可夺帅也,匹夫不可夺志也。 ——孔 丘 64、人生就是学校。在那里,与其说好 的教师 是幸福 ,不如 说好的 教师是 不幸。 ——海 贝尔 65、接受挑战,就可以享受胜利的喜悦 。——杰纳勒 尔·乔治·S·巴顿
谢谢!
武汉大学第五版仪器分析-----红外.
56、极端的法规,就是极端的不公。 ——西 塞罗 57、法律一旦成为人们的需要,人们 就不再 配享受 自由了 。—— 毕达哥 拉斯 58、法律规定的惩罚不是为了私人的 利益, 而是为 了公共 的利益 ;一部 分靠有 害的强 制,一 部分靠 榜样的 效力。 ——格 老秀斯 59、假如没有法律他们会更快乐的话 ,那么 法律作 为一件
武汉大学分析化学第五版第10章:吸光光度法

溶液的透射比愈大,表示它对光的吸收愈小; 相反,透射比愈小,表示它对光的吸收愈大。
It T I0
入射光 I0
透射光 It
It T I0
T 取值为0.0 % ~ 100.0 % 全部吸收 全部透射 T = 0.0 % T = 100.0 %
物质对光的吸收
物质的颜色与光的关系
光谱示意
复合光
表观现象示意
完全吸收
完全透过
吸收黄色光
10.1.2: 光吸收定律-朗伯-----比耳定律
当一束平行单色光通过任何均匀、非散射的固体、 液体或气体介质时,一部分被吸收,一部分透过介质, 一部分被器皿的表面反射。如图所示,设入射光强度为 I0,吸收光强度为Ia,透过光强度为It,反射光强度为Ir。
10.2 分光光度计及吸收光谱
10.2.1分光光度计
0.575
光源 参比
单色器 A0
吸收池
检测器
显示装置
A= At - A0
样品 At
分光光度计组件
光源 单色器 钨灯,360 ~ 800 nm. 同时配有稳压器
基本要求:光源强,能量分布均匀,稳定
作用:将复合光色散成单色光 棱镜 玻璃, 350 ~ 2500 nm, 石英,185 ~ 4500 nm 光栅 平面透射光栅, 反射光栅 玻璃,光学玻璃,石英 作用:将光信号转换为电信号,并放大 光电管,光电倍增管,光电二极管,光导摄 像管(多道分析器)
1. Lambert--Beer Law 数学表达式: A = K· c b· 定义:当一束单色光通过含有吸光物质的溶 液后,溶液的吸光度A与吸光物质的浓度c及吸 收层厚度b成正比 A1 b1 若:c 一定时 — = — mbert Law A2 b2 A1 c 1 b一定时 — = — ......Beer's Law A2 c 2
武汉大学仪器分析实验总结

仪器分析实验总结一、离子选择性电极测定天然水中的F-1、实验原理:氟离子选择电极是以氟化镧单晶片为敏感膜的电位法指示电极。
氟电极和饱和甘汞电极组成的电池:Ag,AgCl|[10-3mol/L NaF,10-1mol/L NaCl]|LaF3|F-(试液)||Kcl(饱和),Hg2Cl2|HgΦISE=E内参-E M=k±0.059/n lg a外,E M=±0.059/n lg a外,E(电池)=ΦSCE-ΦISE=K-+0.059/n lg a外离子选择性电极测定的是离子的活度,故需控制离子强度(加电解质)。
实验条件控制:(1)PH5.5~6.5,用PH缓冲溶液。
(2)控制溶液离子强度,用电解质。
(3)消除Al3+,Fe3+干扰,用掩蔽剂。
常用PH=6的柠檬酸钠还溶液控制溶液PH 和作掩蔽剂。
PH过低F-易变成HF or HF2-,过高La3+会水解为La(OH)3.所用的单晶为:LaF3·EuF2,单晶中含有F-的空位,膜具有选择性和强制性。
2、关键操作:实验操作:(1)连接氟电极、甘汞电极、mV计并预热。
(2)蒸馏水浸泡氟电极和饱和甘汞电极至读数<-300mV.(3)用逐级稀释法配制浓度为10-2、10-3、10-4、10-5、10-6mol/L的F-标准溶液,测电位(要求每相邻两组电位差小于70mV),无需清洗电极,擦干即可,读数稳定5s即可记数,绘制标准曲线。
(3)一次标准溶液加入法测定水样中F-含量。
3、结果分析:计算水样中F-含量公式:cx=(c s V s/(V x+V s))(10ΔE/S-1)-14、思考题:(1)F-选择电极在使用时应注意哪些问题:一般在低浓度F-溶液中浸泡一定时间进行活化,使用时先放入蒸馏水中至电位小于-300mV方可使用测量,且保证测量溶液的PH在5.5~6.5之间,且擦干时用滤纸吸干几个,不能摩擦膜表面。
(2)为什么要清洗F-电极,使其电极响应值负于-370mV?因为电极由记忆效应,将F-电极清洗至其相应值负于-370mV可排除其离子选择性膜上其他离子的干扰,并平衡F-电极电位。
仪器分析课后习题答案(武大版)

仪器分析课后习题(参考)(部分)第一章绪论1.仪器分析有哪些分析方法?请加以简述。
答:a.光学分析法 b.电化学分析法 c.分离分析法 d.其它分析方法。
光学分析法:分为非光谱法和光谱法。
非光谱法是不涉及物质内部能级跃迁,通过测量光与物质相互作用时其散射、折射等性质变化,从而建立起分析方法的一类光学测定法。
光谱法是物质与光相互作用时,物质内部发生的量子化的能级间的跃迁,从而测定光谱的波长和强度而进行的分析方法。
电化学分析方法:利用待测组分的电化学性质进行测定的一类分析方法。
分离分析方法:利用样品中共存组分间溶解能力、亲和能力、吸附和解析能力、迁移速率等方面的差异,先分离,后按顺序进行测定的一类分析方法。
其它仪器分析方法和技术:利用生物学、动力学、热学、声学、力学等性质测定的一类分析方法。
3.仪器分析的联用技术有何显著优点?答:多种现代分析技术的联用,优化组合,使各自的优点得到发挥,缺点得到克服,尤其是仪器与现代计算机技术智能融合,实现人机对话,不断开拓了一个又一个的研究领域。
第二章分子分析方法2.为什么分子光谱总是带状光谱?答:因为当分子发生电子能级跃迁时,必须伴随着振动能级和转动能级的跃迁,而这些振动的能级和转动的能级跃迁时叠加在电子跃迁之上的,所以是带状光谱。
4.有机化合物分子电子跃迁有哪几种类型?那些类型的跃迁可以在紫外可见光区吸收光谱中反映出来?答:б→б*、П→б*、n→б*、n→б*、n→П*、П→П*。
其中n→б*、n→П*、П→П*类型的跃迁可以在紫外可见光区吸收光谱中反映出。
5.何谓生色团、助色团、长移、短移、峰、吸收曲线、浓色效应,淡色效应、向红基团、向蓝基团?答:深色团:分子中能吸收特定波长的光的原子团或化学键。
助色团:与生色团和饱和烃相连且使吸收峰向长波方向移动,并使吸收强度增强的原子或原子团,如:-OH、-NH2。
长移:某些有机物因反应引入含有未珙县电子对的基团,使吸收峰向长波长的移动的现象。
武汉大学第五版仪器分析.光谱法仪器与光学仪器课件

一定波段的光进入检测系统进行检测
狭缝的选择:
一般来说,狭缝越小,光谱的分辨率越高,越接近真 实光谱.但狭缝太小光信号太弱,检测器难以有效测到光信 号.
所以,如果需要得到高分辨率光谱,可以采用较小宽度 的狭缝.
如果进行定量测定,则适当采用较大宽度的狭缝.
优秀课件,精彩
现代分析仪器多配有计算机完成数据采集、信号处理、 数据分析、结果打印,工作站软件系统;
优秀课件,精彩
15:16:31
无限!
36
2
棱镜的顶角α 越大或折射率n越大,角色散率越大,分开
两条相邻谱线的能力越强,但顶角越大,反射损失也增大,
通常为60度角;
优秀课件,精彩
15:16:31
无限!
19
(2)分辨率
相邻两条靠得很近的谱线分开的能力:
R b dn d
;两条相邻谱线的平均波长;△λ:两条谱线的波长差;
特点:带宽较宽,透射效率低。用于较简单的定量测定, 便宜,较好的热稳定性。
2、干涉滤光片---由两层半透明银膜和银膜间的介电薄膜 (氟化钙或氟化镁)组成。 可获得较窄的辐射宽带。 波长选择性比吸收滤光片好。
优秀课件,精彩
15:16:31
无限!
17
(三)棱镜—根据光的折射现象进行分光
棱镜对不同波长的光具有不同的折射率,波长长的光, 折射率小;波长短的光,折射率大。
15:16:31
无限!
30
(4)光栅与棱镜的比较
作为色散元件,光栅比棱镜要好: 光栅的色散几乎与波长无关 在相同色散率时,光栅的尺寸要小 光栅对棱镜不适用的远紫外远红外区可以用 光栅的杂散辐射,高级光谱干扰等问题已经可以解决 比较高的光栅价格已经降下来
武汉大学仪器分析实验讲义

仪器分析实验讲义武汉大学药学院目录仪器分析实验注意事项 (1)实验一色氨酸紫外吸收光谱定性扫描及定量分析 (2)实验二不同物态样品红外透射光谱的测定 (3)实验三二氯荧光素量子产率的测定 (5)实验四核磁共振波谱法测定乙基苯的结构 (7)实验五循环伏安法测定铁氰化钾的电极反应过程 (9)实验六气相色谱定量分析 (12)实验七高效液相色谱法分离巴比妥与苯巴比妥 (15)实验八毛细管区带电泳(CZE)分离硝基苯酚异构体 (165)实验九液相色谱-质谱联用技术测定饮用水中一氯酚异构体 (19)实验十饮料中咖啡因含量的测定(设计实验) (20)仪器分析实验注意事项1.实验前必须详细预习实验讲义,明了实验目的、原理方法及操作步骤。
2.要听从老师的指导,严格按照实验步骤进行,切勿随意乱动。
3.实验中所遇难题,应先独立思考,再与指导老师共同讨论研究。
4.必须如实记录观察到的现象和实验数据。
5.保持实验环境和仪器的清洁整齐。
6.必须遵守实验室的规则:(1)确保人身安全,使用强酸、强碱、有毒试剂时尤其要细心。
(2)室内不得高声谈笑,必须保持安静的实验环境。
(3)按时到实验室,不迟到,不早退。
(4)爱护仪器,不浪费药品,节约水电,遵守实验室的安全措施。
(5)滤纸、火柴棒、碎玻璃等应投入废物缸,切勿丢入水池内。
(6)各组及同学之间应相互协作,合理安排实验时间及实验内容。
(7)每次实验后由班长安排同学轮流值日,值日要负责当天实验室的卫生,安全和一些服务性工作。
最后离开实验室时,应检查水、电、门窗等是否关闭。
(8)对实验的内容和安排不合理的地方可提出改进意见。
对实验中出现的一切反常现象应进行讨论,并大胆提出自己的看法,做到生动活泼,主动地学习。
(9)实验室禁止吸烟。
实验一色氨酸紫外吸收光谱定性扫描及定量分析一、实验目的1.了解紫外-可见光谱定性分析原理。
2.掌握紫外-可见光谱定性图谱数据的处理方法。
3.熟悉紫外-可见光谱分析仪的定性、定量扫描实验操作方法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C CH 3 CH 3
O
C=O=1663cm-1
C=O=1686cm-1
空间效应的另一种情况是张力效应:四元环>五元环>六元 环。随环张力增加,红外峰向高波数移动。
6)物质状态及制样方法 通常,物质由固态向气态变化,其波数将增加。如丙酮在液 态时, C=O=1718cm-1; 气态时 C=O=1742cm-1 ,因此在查阅标准 红外图谱时,应注意试样状态和制样方法。
制作材料
工作温度
2. 吸收池 红外吸收池使用可透过红外的材料制成窗片;不同的样品状 态(固、液、气态)使用不同的样品池,固态样品可与晶体混 合压片制成。
材 料 NaCl KBr CaF2 CsBr TlBr + TlI
透光范围/m 0.2-25 0.25-40 0.13-12 0.2-55 0.55-40
中介效应(Mesomeric effect):
孤对电子与多重键相连产生的p- 共轭, 结果类似于共轭效应。 当诱导与共轭两种效应同时存在时,振动 频率的位移和程度取决于它们的净效应。
2)氢键效应(X-H)
形成氢键使电子云密度平均化(缔合态),使体系能量下降,
基团伸缩振动频率降低,其强度增加但峰形变宽。
指纹区
500
特征区
5. 影响基团频率的因素
基团频率主要由化学键的力常数决定。但分子结构和外部 环境因素也对其频率有一定的影响。
1)电子效应:引起化学键电子分布不均匀的效应。
诱导效应(Induction effect):取代基电负性—静电诱导—电 子分布改变—k 增加—特征频率增加(移向高波数)。
共轭效应(Conjugated effect):电子云密度均化—键长变长— k 降低—特征频率减小(移向低波数)。
第10章
红外吸收光谱法
Infrared spectrometry
10.1 概述
1. 定义
红外光谱又称分子振动转动光谱,属分子吸收光谱。
样品受到频率连续变化的红外光照射时,分子吸收其中一
些频率的辐射,分子振动或转动引起偶极矩的净变化,使 振-转能级从基态跃迁到激发态,相应于这些区域的透射
光强减弱,记录百分透过率T%对波数或波长的曲线,即
如将原子的实际折合质量(通过Avogaro常数计算)代入,则有
1 2c
k k 1302 ' ( cm 1 ) ' Ar / N A Ar
影响基本振动跃迁的波数或频率的直接因素为化学键力常数 k 和原子质量。 k大,化学键的振动波数高. 如:kCC(2222cm-1)>kC=C(1667cm-1)>kC-C(1429cm-1)(质量相 近)
不同浓度的乙醇CCl4溶液IR光谱
4)费米共振
当一振动的倍频与另一振动的基频接近(2A=B)时,二 者相互作用而产生强吸收峰或发生裂分的现象。
COCl
Ar-C()=880-860cm-1 C=O(as)=1774cm-1
1773cm-1 1736cm-1
5)空间效应 由于空间阻隔,分子平面与双键不在同一平面,此时共轭效 应下降,红外峰移向高波数。 O
下图给出了各种可能的振动形式(以甲基和亚甲基为例)。
理论振动数(峰数) 设分子的原子数为n, 对非线型分子,理 论振动数=3n-6 如H2O分子,其振 动数为3×3-6=3 对线型分子,理 论振动数=3n-5 如CO2分子,其理 论振动数为3×35=4
理论上,多原子分子的振动数应与谱峰数相同,但实际上, 谱峰数常常少于理论计算出的振动数,这是因为: a)偶极矩的变化=0的振动,不产生红外吸收; b)谱线简并(振动形式不同,但其频率相同); c)仪器分辨率或灵敏度不够,有些谱峰观察不到。 以上介绍了基本振动所产生的谱峰,即基频峰(V=±1允 许跃迁)。在红外光谱中还可观察到其它跃迁谱峰(泛频峰): 倍频峰:由基态向第二、三….振动激发态的跃迁(V=±2、 ± 3.); 合频峰:分子吸收光子后,同时发生频率为1,2的跃迁, 此时产生的跃迁为 1+2的谱峰。
分子固有振动
a
(能级跃迁)
2. 分子振动
1)双原子分子振动 分子的两个原子以其平衡点为中心,以很小的振幅(与核间
距相比)作周期性“简谐”振动,其振动可用经典刚性振动描述:
1 ( 频率 ) 2
1 .......... 或 ( 波数 ) ....... 2c
k
k
k为化学键的力常数(N/cm = mdyn/Å),为双原子折合质量
差频峰:当吸收峰与发射峰相重叠时产生的峰 1-2。 泛频峰可以观察到,但很弱,可提供分子的“指纹”。
3. 谱带强度
分子对称度高,振动偶极矩小,产生的谱带就弱;反之则强。
如C=C, C-C因对称度高,其振动峰强度小;而C=X, C-X,因对 称性低,其振动峰强度就大。峰强度可用很强(vs)、强(s)、
光谱仪)(Fourier Transfer, FT)
一、色散型与双光束UV-Vis仪器类似,但部件材料和顺序不同。
红外光谱仪的测量光路
1. 光源 常用的红外光源有Nernst灯和硅碳棒。
类型 Nernst 灯
硅碳棒
特 点 高波数区(> 1000cm-1)有 Zr, Th, Y 1700oC 更强的发射;稳定性好; 氧化物 机械强度差; 但价格较高。 低波数区光强较大;波数 o 1200-1500 C 范围更广; SiC 坚固、发光面积大。
如羧酸 RCOOH(C=O=1760cm-1 ,O-H=3550cm-1); (RCOOH)2(C=O=1700cm-1 ,O-H=3250-2500cm-1) 如乙醇:CH3CH2OH(O=H=3640cm-1 ) (CH3CH2OH)2(O=H=3515cm-1 ) (CH3CH2OH)n(O=H=3350cm-1 ) 3)振动耦合(Coupling) 当两个振动频率相同或相近的基团相邻并由同一原子相连时, 两个振动相互作用(微扰)产生共振,谱带一分为二(高频和低 频)。如羧酸酐分裂为C=O( as1820、 s1760cm-1)
中(m)、弱(w)、很弱(vw)等来表示。
4. 振动频率
1)基团频率
通过对大量标准样品的红外光谱的研究,处于不同有机物分 子的同一种官能团的振动频率变化不大,即具有明显的特征性。
这是因为连接原子的主要为价键力,处于不同分子中的价键
力受外界因素的影响有限!即各基团有其自已特征的吸收谱带。
基团频率位多原子分子 多原子分子的振动更为复杂(原子多、化学键多、空间结构复
杂),但可将其分解为多个简正振动来研究。
简正振动
整个分子质心不变、整体不转动、各原子在原地作简谐振动且
频率及位相相同。此时分子中的任何振动可视为所有上述简谐振 动的线性组合。 简正振动基本形式 伸缩振动:原子沿键轴方向伸缩,键长变化但键角不变的振动。 变形振动:基团键角发生周期性变化,但键长不变的振动。又称 弯曲振动或变角振动。
分子中不同振动能级差为 E振= Vh
吸收光子的能量(ha )要与该能量差相等,即a= V时,才可 能发生振转跃迁。例如当分子从基态(V=0)跃迁到第一激发态 (V=1),此时V=1,即a=
条件二:辐射与物质之间必须有耦合作用
电场
无偶极矩变化
磁场
无红外吸收
红外吸收
偶极矩变化
交变磁场
X-H伸缩振动区:4000-2500cm-1
醇、酚、酸等 O-H 3650~3200 3650~3580 低浓度(峰形尖锐) 3400~3200 高浓度(强宽峰) N-H 3500~3100 胺、酰胺等,可干扰 O-H 峰 饱和(3000 以下)与不饱和(3000 以上) 饱和-C-H -CH3(2960,2870) (3000-2800) -CH2(2930,2850) 不饱和=C-H 末端=CH(3085) C-H 3000 左右 (3010~3040) 不饱和C-H 较弱 (2890)较强 、 (3300) (2890~3300) ArC-H 比饱和 C-H 峰弱,但峰 (3030) 形却更尖锐
红外光谱。
连续h ( I0 ) M M * I t
分子振动转动 跃迁
主要用于化合物鉴定及分子结构表征,亦可用于定量分析。
光谱区与能量相关图
双原子分子能级跃迁示意图
红外光谱的表示方法:
红外光谱以T~或T~ 来表示,下图为苯酚的红外光谱。
T(%)
2. 红外光区划分
近红外(泛频) (0.75~2.5 m) 红外光谱 (0.75~1000m) 中红外(振动区) (2.5~25 m) 远红外(转动区) (25-1000 m) 分区及波长范围 倍频
分子振动转动 (常用区)
分子转动 跃迁类型
3. 红外光谱特点
1)红外吸收只有振-转跃迁,能量低; 2)应用范围广:除单原子分子及单核分子外,几乎所有有 机物均有红外吸收; 3)分子结构更为精细的表征:通过IR谱的波数位置、波峰 数目及强度确定分子基团、分子结构;
4)定量分析;
5)固、液、气态样均可用,且用量少、不破坏样品;
6)分析速度快。
7)与色谱等联用(GC-FTIR)具有强大的定性功能。
10.2 基本原理
1. 产生红外吸收的条件
条件一:辐射光子的能量应与振动跃迁所需能量相等。
根据量子力学原理,分子振动能量E振 是量子化的, 即 E振=(V+1/2)h 为分子振动频率,V为振动量子数,其值取 0,1,2,…
双键伸缩振动区(1900~1200cm-1)
C=O
1900-1650
C=O
C
1680-1620 2000-1650
苯衍生 物的泛 频
强峰。是判断酮、醛、酸、酯及酸酐的 特征吸收峰,其中酸酐因振动偶合而具 有双峰。 峰较弱(对称性较高) 。在 1600 和 1500 附近有 2-4 个峰(苯环骨架振动) ,用于 识别分子中是否有芳环。 C-H 面外、C=C 面内变形振动,很弱, 但很特征(可用于取代类型的表征) 。
