溶液溶解度中考试题
中考化学溶液 溶解度20篇(附带答案解析)经典
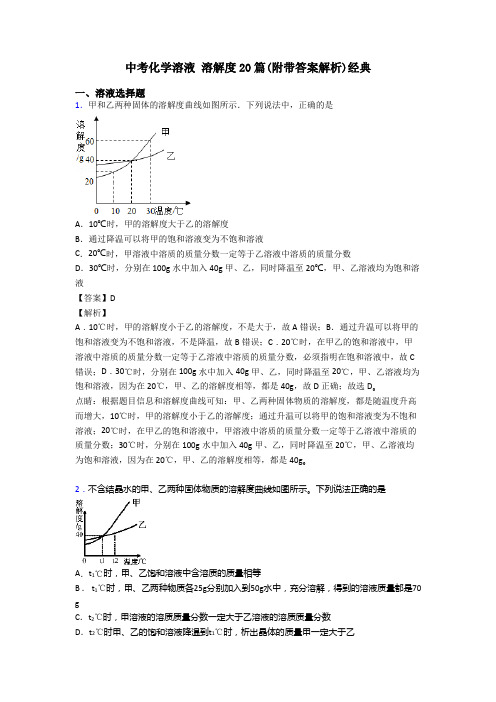
中考化学溶液溶解度20篇(附带答案解析)经典一、溶液选择题1.甲和乙两种固体的溶解度曲线如图所示.下列说法中,正确的是A.10℃时,甲的溶解度大于乙的溶解度B.通过降温可以将甲的饱和溶液变为不饱和溶液C.20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数D.30℃时,分别在100g水中加入40g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液【答案】D【解析】A.10℃时,甲的溶解度小于乙的溶解度,不是大于,故A错误;B.通过升温可以将甲的饱和溶液变为不饱和溶液,不是降温,故B错误;C.20℃时,在甲乙的饱和溶液中,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数,必须指明在饱和溶液中,故C 错误;D.30℃时,分别在100g水中加入40g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液,因为在20℃,甲、乙的溶解度相等,都是40g,故D正确;故选D。
点睛:根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,10℃时,甲的溶解度小于乙的溶解度;通过升温可以将甲的饱和溶液变为不饱和溶液;20℃时,在甲乙的饱和溶液中,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数;30℃时,分别在100g水中加入40g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液,因为在20℃,甲、乙的溶解度相等,都是40g。
2.不含结晶水的甲、乙两种固体物质的溶解度曲线如图所示。
下列说法正确的是A.t1℃时,甲、乙饱和溶液中含溶质的质量相等B.t1℃时,甲、乙两种物质各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70 gC.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数D.t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙【答案】B【解析】A、t1℃时,甲、乙溶解度相等,所以等质量的饱和溶液中含溶质的质量相等,故A错误;B、t1℃时,甲、乙两种物质的溶解度是40g,所以各25g分别加入到50g水中,充分溶解,得到的溶液质量都是70g,故B正确;C、t2℃时,溶液的饱和状态不确定,所以甲溶液的溶质质量分数不一定大于乙溶液的溶质质量分数,故C错误;D、t2℃时甲、乙的饱和溶液的质量不确定,所以降温到t1℃时,析出晶体的质量甲不一定大于乙,故D错误。
2020中考化学 溶液溶解度和溶解度曲线 培优专题练习(含答案)

2020中考化学溶液溶解度及溶解度曲线培优专题练习(含答案)专题训练一一、选择题(本题包括6小题,每小题2分,共12分)1.把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是()A. 碘B. 汽油C. 白糖D. 碳酸钙2.溶液在生活、生产中有广泛的应用。
下列有关溶液的叙述正确的是()A. 均一稳定的液体一定是溶液B. 洗涤剂去油污是乳化现象C. 豆浆、牛奶都是溶液D. 溶液都是无色的3.化学实验常需要配制溶液。
下列说法正确的是()A. 配制溶液时,只能用水作溶剂B. 配制硝酸铵溶液的过程中,溶液的温度会下降C. 用浓硫酸配制稀硫酸时,应将水缓缓注入浓硫酸中D. 将10 g 氯化钠溶于100 g水中,得到质量分数为10%的氯化钠溶液第4题图4.如图是甲、乙的溶解度曲线。
下列说法不正确...的是()A. t1℃时,乙的溶解度大于甲的溶解度B. t2℃时,甲、乙饱和溶液中溶质的质量分数相等C. 降低温度能使接近饱和的甲溶液变为饱和溶液D. t3℃时,75 g甲的饱和溶液中加入50 g水,可以得到质量分数为25%的溶液5.高氯酸钾(KClO()温度/℃20406080溶解度/g 1.68 3.737.313.4A.B. 20 ℃时,将2 g高氯酸钾溶于98 g水可配制2%的溶液C. 60 ℃时,高氯酸钾饱和溶液中溶质的质量分数是7.3%D. 80 ℃的高氯酸钾饱和溶液冷却至40 ℃有结晶现象6.如图为三种物质的溶解度曲线。
下列说法错误..的是()第6题图A. 约在64 ℃时KCl和Na2SO4的溶解度相等B. 在室温至100 ℃区间,随温度升高Na2SO4的溶解度先增大后减小,醋酸钙则相反C. 分离含少量KCl的Na2SO4溶液,采用先蒸发浓缩,再降温结晶的方法D. 在40 ℃时40 g KCl固体溶于60 g水得到40%KCl溶液二、填空及简答题(本题包括4小题,共21分)7.(2分)为了研究物质的溶解现象,设计并进行了如下实验。
溶液 溶解度中考题集锦

A.甲的溶解度大于乙的溶解度 B.t1℃时,50 g 克水中溶解甲最多能形成 65 克溶液 C.t2℃时乙的饱和溶液降温至 t1℃变为不饱和溶液 D.将 t1℃时甲的饱和溶液升温至 t2℃,溶质的质量分数增大
【答案】B 【解析】A.溶解度受温度影响,不指名温度,无法比较溶解的大小;B. t1℃时,甲的溶解 度等于 30g,50 g 克水中溶解甲最多能溶解的溶质为 15g,形成等于 65 克溶液;C. t2℃时 乙的饱和溶液降温至 t1℃时,溶解度变小,溶质析出,得到的仍是饱和溶液;D. 将 t1℃时 甲的饱和溶液升温至 t2℃,溶解度变大,溶质的质量不变,溶质的质量分数不变。 点睛:在溶解度曲线图上,溶剂的量都是 100g,所以分析溶质的质量分数时,只需要比较 溶质 的多少即可。溶解度变大时,溶质不变,溶解度减小时溶质质量等于减小后的溶解度
6.NH4C1 和 Na2SO4 的溶解度表及溶解度曲线如下,下列说法正确的是:( )
A.甲为 NH4C1 B.t2 时,甲溶液的溶质质量分数一定比乙大 C.甲、乙饱和溶液从 t3 降温到 t2,溶质的质量分数都变小 D.等质量的甲、乙饱和溶液从 t1 升温到 t3,为使其溶液恰好饱和,加入的甲、乙固体质量 相等 【答案】D 【解析】A、通过分析溶解度表中的数据可知,氯化铵的溶解度随温度的升高而增大,所 以乙为氯化铵;B、饱和溶液溶质的质量分数=溶解度÷(溶解度+100g)×100%,由图可 知,t2 时,甲乙两物质的溶解度相等,所以两物质的饱和溶液溶质的质量分数相同;不饱 和时,浓度大小关系不确定,C、甲物质饱和溶液从 t3 降温到 t2,溶解度变大,溶质的质量 不变,溶质的质量分数不变;D、t1℃、t3℃时,两物质的溶解度相等,所以等质量的甲、 乙饱和溶液从 t1 升温到 t3,为使其溶液恰好饱和,加入的甲、乙固体质量相等,故 D 正 确.选 D 点睛:在溶解度曲线图上,溶剂的量都是 100g,所以分析溶质的质量分数时,只需要比较 溶质的多少即可。溶解度变大时,溶质不变,溶解度减小时溶质质量等于减小后的溶解度
中考化学化学溶解度大题培优易错难题及详细答案

中考化学化学溶解度(大题培优易错难题)及详细答案一、初中化学溶解度1.M 是硝酸钾或氯化钱中的一种。
硝酸钾和氯化铁的溶解度曲线如图1所示。
某化学兴 趣小组用物质M 进行了如图2所示实验。
下列说法不正确的是()A.物质M 是硝酸钾B.溶液②中溶质质量分数为37.5%C.溶液①②③中,溶质质量分数的关系是②>③>①D.溶液①为不饱和溶液,溶液②和③为饱和溶液【答案】C 【解析】 【分析】 【详解】A 、由图2可知,t2℃时,烧杯②中100g 的水将60g 的M 物质完全溶解,而t2℃时氯化钱的溶解度小于60g,故可以确定M 物质是硝酸钱,故A 正确;B 、溶液②是100g 的水中溶解了 60g 的硝酸钾,故溶质的质量分数为售之x 100% =37.5%,故 B 正确;160gC 、溶液①②④中,②的溶质质量分数为37.5%,①的溶质质量分数为-100% « 28.6%,③的溶质质量分数要比②小,不一定比①大,故C 错误; 150g+60gD 、溶液①经升温蒸发后变为溶液②,12c 时硝酸钾的溶解度是60g,溶液②中刚好是 100g 的水和60g 的硝酸钾,故溶液②刚好是饱和溶液,溶液③中有固体析出,故溶液③ 也是饱和溶液,故D正确。
故选C 。
2.KCI 和KNO3的溶解度表及溶解度曲线如图所示,卜.列说法不正确的是()温度/℃20 30 40 50 溶解度s/gKCI34.0 37.0 40.0 42.6 KNO 331.645.863.985.50 tlt2 温度七图1o o O6 4 2溶解度也图A.甲表示KNCh 溶解度曲线B.温度匕℃应在20〜30℃之间C. 40℃时,lOgKCl 加入20g 水中,可得到33.3%的溶液D. 50°C 时,30gKN03加入50g 水,充分溶解,再降温到30°C,有晶体析出【答案】C 【解析】 【分析】 【详解】A 、通过分析溶解度表中的数据可知,硝酸钾的溶解度受温度变化影响较大,所以甲表示 KNCh 溶解度曲线,故A 正确,不符合题意;B 、20〜30℃,氯化钾的溶解度从34g 增大到37g,硝酸钾的溶解度从31.6g 增大到45.8g,所以温度应在20〜30C 之间,故B 正确,不符合题意;C 、40C 时,氯化钾的溶解度是40.0g,所以lOgKCl 加入20g 水中,有固体剩余,形成的是40 0 g该温度下的氯化钾饱和溶液,故溶液的质量分数为:———^--xl00%«28.6% ,故100 g+40.0 gc 错误,符合题意。
中考化学饱和溶液溶解度

考点19 饱和溶液、溶解度一、选择题1.(10福建省晋江12.)溶解度曲线为我们定量描述物质的溶解性强弱提供了便利。
请你根据下图的溶解度曲线判断下列说法,其中正确的是A.20℃时,甲物质的溶解度大于乙物质的溶解度B.40℃时,两种物质的溶解度相等C.60℃时,将80g甲物质放入100g水中,所得溶液的质量为180gD.60℃时,将等质量的甲、乙两种物质的饱和溶液降温到20℃,析出晶体较多的是乙2.(10福建南安14.)右图是甲、乙两种物质的溶解度曲线,下列说法正确的是A.甲的溶解度受温度影响比乙小B.15℃时甲、乙的溶解度相等C.30℃时乙的溶解度为30gD.升高温度可使接近饱和的甲溶液变为饱和3(2010·辽宁鞍山.)下图为氯化铵和硫酸钠的溶解度曲线。
下列说法中不正确的是A.30℃时,氯化铵、硫酸钠的溶解度相同B.氯化铵的溶解度随温度的升高而增大C.将50℃时硫酸钠的饱和溶液降低温度,始终有晶体析D.将60℃时硫酸钠的饱和溶液降温至40℃,溶质的质量分数不变4.(10邵阳13)右图表示的是a、b两种固体物质的溶解度曲线,下列叙述正确的是A.a的溶解度大于b的溶解度B.a 、b 两物质的溶解度受温度影响都很小C.在t ℃时,a 、b 两物质的饱和溶液中溶质质量分数相等D.当b 中含少量a 时,可用冷却热饱和溶液的方法提纯b5.(10徐州15)根据右图的溶解度曲线判断,下列说法错误的是A50℃时A 物质的溶解度最大B 升温可使C 物质的不饱和溶液变饱和C50℃时把90gA 物质放入100g 水中能得到190g 溶液D 将50℃三种物质的饱和溶液分别降温到20℃时,B 溶液最浓6.(10贵港12下列说法错误的是 ( )A .t2℃时,甲、乙两种物质的溶解度相等B .甲的溶解度随温度的升高而增大C .分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得 的三种溶液中溶质的质量分数大小关系是乙>甲>丙D .t1℃时,丙的饱和溶液中溶质的质量分数为40%7.(10成都11) 右图是a 、b 两种固体物质的溶解度曲线。
人教版中考化学 溶液 溶解度专题复习练习(含解析)

人教版中考化学溶液溶解度专题复习练习(含解析)一、溶液选择题1.甲、乙两种物质的溶解度曲线如图所示。
下列说法正确的是()A.a1℃时甲和乙的饱和溶液,升温到a2℃时仍是饱和溶液B.甲和乙的溶解度相等C.a2℃时,在 100 g 水中加入 60 g 甲,形成 160 g 溶液D.a1℃时,甲和乙各 30 g 分别加入 100 g 水中,均形成饱和溶液【答案】D【解析】A、由图象可知,甲、乙的溶解度随着温度的升高而增大,因此a1℃时甲和乙的饱和溶液,升温到a2℃时变为不饱和溶液,错误;B、物质的溶解度与温度有关,a1℃时,甲和乙的溶解度相等,不是a1℃时,甲和乙的溶解度不等,错误;C、a2℃时,甲的溶解度为50g,在100g水中加入60g甲,形成饱和溶液,并有10g甲溶解不了,错误;D、a1℃时,甲和乙的溶解度均为30g,所以甲和乙各30g分别加入100g水中,均形成饱和溶液,正确。
故选D。
2.甲、乙两种固体物质的溶解度曲线如图所示。
下列有关叙述中错误的是A.t2℃时甲的溶解度比乙的大B.将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大C.升高温度可将甲的饱和溶液变成不饱和溶液D.t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等【答案】B【解析】【分析】由甲、乙两种固体物质的溶解度曲线图可知,甲的溶解度受温度的影响较大,乙的溶解度受温度的影响较小。
【详解】A、由甲、乙两种固体物质的溶解度曲线图可知,t2℃时甲的溶解度比乙的大,故A正确;B、将等质量甲、乙的饱和溶液从t2降到t1,析出甲的质量大,故B不正确;C、甲的溶解度随温度升高而增大,升高温度可以将甲的饱和溶液变成不饱和溶液,故C正确;D、t1℃时,两种物质的溶解度相等,甲和乙的饱和溶液各100g,其溶质的质量一定相等,故D正确。
故选B。
3.氯化铵和硝酸钾溶解度曲线如图所示,下列叙述正确的是( )A.50℃时,氯化铵的溶解度大于硝酸钾B.a℃时,氯化铵与硝酸钾溶液的质量分数相等C.将60℃的硝酸钾饱和溶液降温会变为不饱和溶液D.40℃时,50g水中加入50g硝酸钾,充分搅拌,得到质量分数约为39%的硝酸钾溶液【答案】D【解析】【分析】【详解】A、从图中看出,50℃时,硝酸钾的溶解度大于氯化铵的,故A不正确;B、a℃时,硝酸钾和氯化铵的溶解度曲线相交,此时两物质的溶解度相等,则其饱和溶液的溶质质量分数相等,其不饱和溶液的质量分数是否相等无法确定,故B不正确;C、硝酸钾的溶解度随温度的升高明显增大,将60℃时硝酸钾饱和溶液降温后会析出晶体,剩余的溶液仍然是低温下的饱和溶液,故C不正确;D、40℃时,硝酸钾的溶解度为64g,则50g水中最多溶解硝酸钾32g,所得溶液的溶质质量分数为32g100%39%32g+50g⨯≈,故D正确。
中考化学溶解度计算题及答案[2024年中考化学知识点大全溶解度]
![中考化学溶解度计算题及答案[2024年中考化学知识点大全溶解度]](https://img.taocdn.com/s3/m/49c14c290a4e767f5acfa1c7aa00b52acfc79c9d.png)
1.已知硫酸铜的溶解度为10g/100mL水,试计算溶液中含有的硫酸铜的质量。
答案:溶液中含有硫酸铜的质量为10g.
2.已知硝酸银的溶解度为20g/100mL水,试计算溶液中含有的硝酸银的质量。
答案:溶液中含有硝酸银的质量为20g.
3.已知氯化钠的溶解度为36g/100mL水,试计算溶液中含有的氯化钠的质量。
答案:溶液中含有氯化钠的质量为36g.
4.已知碳酸钠的溶解度为20g/100mL水,试计算溶液中含有的碳酸钠的质量。
答案:溶液中含有碳酸钠的质量为20g.
5.已知氯化铵的溶解度为40g/100mL水,试计算溶液中含有的氯化铵的质量。
答案:溶液中含有氯化铵的质量为40g.
6.已知硫酸铁的溶解度为30g/100mL水,试计算溶液中含有的硫酸铁的质量。
答案:溶液中含有硫酸铁的质量为30g.
7.已知氯化钾的溶解度为50g/100mL水,试计算溶液中含有的氯化钾的质量。
答案:溶液中含有氯化钾的质量为50g.
8.已知硝酸钠的溶解度为25g/100mL水,试计算溶液中含有的硝酸钠的质量。
答案:溶液中含有硝酸钠的质量为25g.
9.已知硝酸铜的溶解度为15g/100mL水,试计算溶液中含有的硝酸铜的质量。
答案:溶液中含有硝酸铜的质量为15g.
10.已知氯化钙的溶解度为40g/100mL水,试计算溶液中含有的氯化钙的质量。
答案:溶液中含有氯化钙的质量为40g.。
2023年中考真题专题溶解度

中考真题专题汇编——溶解度1.(深圳)下图是甲、乙两种固体物质(不含结晶水)旳溶解度曲线。
下列说法对旳旳是(C)A、甲旳溶解度不小于乙旳溶解度B、a1℃时,甲、乙饱和溶液旳温度升温至a2℃时,均有固体析出C、a2℃时,M点对应旳甲溶液不饱和D、a2℃时,乙饱和溶液旳质量分数为20%2.(随州)如图,是甲、乙两种固体物质旳溶解度曲线,下列说法对旳旳是( D )A. 20℃时,甲、乙两种固体物质旳溶解度都是30B. 40℃时,甲旳饱和溶液中溶质质量分数为50%C. 40℃时,将50g乙物质所有溶于水中,恰好能得到150g乙旳饱和溶液D.将130g 20℃甲旳饱和溶液升温到40℃,最多还能溶解甲物质20g3.(孝感)甲、乙两种固体物质(均不含结晶水)旳溶解度曲线如右图所示。
下列说法对旳旳是(B)A. t1℃时,甲旳溶解度不小于乙旳溶解度B.t2℃时,乙旳饱和溶液升温或降温均会析出晶体C.乙溶液从t3℃降温到t1℃,乙溶液中旳溶质质量分数会发生变化D. t3℃时,50g水中加入40g旳甲物质充足溶解可得到90g甲旳饱和溶液4.(苏州)氯化钠和硝酸钾两种固体旳溶解度曲线如右图所示。
下列说法对旳旳是(C)A.硝酸钾旳溶解度不小于氯化钠旳溶解度B.常用冷却结晶旳措施从氯化钠溶液中获得其晶体C.40℃时,将35 g硝酸钾晶体放入50 g水中,充足搅拌后,所得溶液旳溶质质量分数为39.0%D.将20℃旳硝酸钾饱和溶液升温至60℃,溶液旳溶质质量分数增大(忽视水分蒸发)5.(宿迁)右图是甲、乙、丙三种固体物质(均不含结晶水)旳溶解度曲线,下列说法对旳旳是(C)A.t1℃时,甲与丙两种物质旳饱和溶液中溶质质量相似B. 乙中混有少许甲时,应采用降温结晶旳措施提纯乙C.甲属于易溶物质D.t2℃时,30g甲能溶解于50g水中形成80g溶液6.(临沂)甲、乙两种固体物质旳溶解度曲线如右图所示。
下列说法对旳旳是( D )A. 20℃时,甲溶液中溶质旳质量分数一定比乙溶液旳大B.将40℃时甲旳一定量饱和溶液降温至20℃,溶液质量不变C.甲旳溶解度不小于乙旳溶解度D. 40℃时,分别在100g水中各加入30g甲、乙,同步降温至20℃,甲、乙溶液均为饱和溶液7.(泰安)量旳硝酸钾和氣化钾分别加入到各盛有100g水旳两个烧杯中,充足搅拌后现象如图1所示,硝酸钾和氣化钾旳瑢解度曲线如图2所示。
2023河南中考化学专题11 有关溶解度的题(5)

原创好题11 有关溶解度的题1. 硫酸锂( Li2 SO4) 是制造特种高强度玻璃的原料,其在不同温度时的溶解度如下表,下列说法正确的是A. 硫酸锂的溶解度随温度升高而增大B. 20 ℃时,100 g 饱和硫酸锂溶液中含有硫酸锂34. 8 gC. 30 ℃时,硫酸锂的饱和溶液升高温度可变成不饱和溶液D. 40 ℃时,不可能配制溶质质量分数为33. 9%的硫酸锂溶液2. 20 ℃时,KCl 的溶解度为34 g ,某同学向烧杯中依次加入KCl 固体,充分溶解,实验过程如图所示。
下列说法不正确的是A. 氯化钾的饱和溶液中能继续溶解其他物质B. 溶液②为氯化钾的不饱和溶液C. 溶液③中的溶质质量分数为40%D. 溶液③和溶液④的质量相等3. NH4Cl 可用作肥料,20 ℃时按下表配制溶液(20 ℃和40 ℃时NH4Cl 固体的溶解度分别为37. 2 g 和45. 8 g) 。
下列说法正确的是A. ①中溶液属于饱和溶液B. ②与③中溶质质量相等C. ②中溶质的质量分数为35%D. 将③中溶液升温到40 ℃,溶质的质量分数增大4. 下表是氢氧化钠和碳酸钠分别在水和酒精中的溶解度,下列说法不正确的是A. 氢氧化钠在水中的溶解度随温度的升高而增大B. 20 ℃时,氢氧化钠饱和酒精溶液中溶质的质量分数为17. 3%C. 相同温度下, 同种物质在不同溶剂中的溶解度也不同D. 40 ℃时,可用酒精洗涤提纯含有少量氢氧化钠的碳酸钠固体和NaCl 的溶解度曲线,下列说法正确的是5. 如图是MgSO4的溶解度A. NaCl 的溶解度小于MgSO4B. 10 ℃时,将40 g NaCl 固体溶于100 g 水中,得到溶液的质量为140 gC. 将70 ℃时接近饱和的MgSO溶液升温或降温都能转化成饱和溶液4饱和溶液的溶质质量分数为49%D. 50 ℃时,MgSO46. 将60 g 甲固体放入盛有50 g 水的烧杯中充分溶解,测得溶液质量随温度变化的曲线如图。
中考《溶解度》的经典例题及解析

一、饱和溶液与不饱和溶液1.饱和溶液与不饱和溶液的定义在一定温度下,向一定量溶剂里加入某液;当溶质还能继续溶解时,所得到的溶液2.对饱和溶液与不饱和溶液的理解(1)首先,要明确“一定温度”和“一定相转化的。
(2)其次,要明确“某一溶质的”饱和还能溶解KNO 3,此时的溶液是NaCl 的饱的饱和或不饱和溶液。
(3)有些物质能与水以任意比互溶3.饱和溶液与不饱和溶液的转化条件(1)一般规律:此转化条件适合大多数固体物质的溶液(2)特殊情况(如氢氧化钙):极少数物质在一定量水中溶解的最大溶液时,要升高温度;若把饱和溶液转化4.判断溶液是否饱和的方法一般地,可以向原溶液中再加入少量原继续溶解,则说明原溶液是该溶质的不饱和如果有且溶质的量不再减少,未溶解的溶质二、固体的溶解度1.定义在一定温度下,某固态物质在100 g 溶剂里度。
如果不说明溶剂,通常所说的溶解度是2.正确理解溶解度概念需要抓住的四个要(1)条件:一定温度。
因为物质的溶解度溶解度溶液加入某种溶质,当溶质不能继续溶解时,所得到的溶的溶液叫做这种溶质的不饱和溶液。
理解一定量的溶剂”。
因为改变溶剂量或温度时,饱和溶饱和溶液或不饱和溶液。
例如,在一定温度下不能再的饱和溶液,对KNO 3来说就不一定是饱和溶液了互溶,不能形成饱和溶液,如酒精没有饱和溶液。
化条件 的溶液,因为大多数固体物质在一定量水中溶解的最的最大量随温度的升高而降低(如熟石灰),此类物质转化成不饱和溶液,要降低温度。
少量原溶质,如果不能继续溶解,说明原溶液是该溶不饱和溶液。
或者在一定温度下,看该溶液中有没有不的溶质与溶液共存,那么这种溶液就是这种溶质的饱溶剂里达到饱和状态时所溶解的质量,叫做这种固态度是指物质在水里的溶解度。
四个要点溶解度随温度的变化而变化,所以不指明温度时,溶解到的溶液叫做这种溶质的饱和溶饱和溶液与不饱和溶液是可以互不能再溶解NaCl 的溶液,可能液了。
因此必须指明是哪种溶质解的最大量随温度升高而增大。
中考化学溶解度专题复习

1、下表是KNO 3、NaCl在不同温度下的溶解度(单位:g/100g水)温度0102030405060708090100(℃)KNO313.320.93245.86485.5110138169202246 NaCl35.735.83636.336.63737.337.838.43939.8①以上两种物质溶解度的变化受温度影响较大的是________。
②30℃时,KNO3的溶解度是___________。
③KNO3溶液中含有少量NaCl时,可通过____________的方法提纯。
④对③析出的晶体和剩余溶液描述正确的是________(填写编号)。
Ⅰ.剩余溶液一定是KNO3饱和溶液Ⅱ.剩余溶液一定是NaCl不饱和溶液Ⅲ.上述方法可以将两者完全分离Ⅳ.析出的晶体中只含有KNO3⑤在一定温度下,将含69gKNO3、18gNaCl的混合物完全溶解在50g水中。
改变温度使KNO3析出,NaCl不析出,则温度T(℃)的范围是_____________(硝酸钾和氯化钠溶解度互不影响)。
2、溶解度可表示物质溶解性的大小。
①右下图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线。
Ⅰ.20℃时,甲的溶解度________(填“>”、“<”或“=”)乙的溶解度。
Ⅱ.40℃时,乙和丙________(填“能”或“不能”)形成溶质质量分数相同的饱和溶液。
Ⅲ.20℃时,烧杯中分别盛有相同质量甲、乙、丙的饱和溶液,各加入等质量的对应固体,并升温至50℃。
请填写下表。
烧杯中的溶质烧杯中固体的变化甲_____________________________乙固体逐渐减少至全部溶解丙_____________________________②气体的溶解度也有一定的变化规律。
Ⅰ.打开可乐瓶,逸出大量气泡。
由此可见,压强越小,CO2的溶解度越_________。
为增大CO2的溶解度,可采用的一种方法是________。
Ⅱ.不同温度下,氧气的溶解度随压强的变化如右图所示,图中t1对应的温度为40℃,则t2对应的温度________(填编号)。
2024年中考化学专题训练——溶解度

2024年中考化学专题训练——溶解度一、选择题1.要将饱和的KNO3溶液变成不饱和溶液,下列措施中不正确的是A.加水B.升高温度C.与另一不饱和KNO3溶液混合D.加KNO3晶体2.要使二氧化碳气体大量溶解在水里,可以采用的方法是A.降温加压B.升温加压C.降温减压D.升温减压3.不能影响物质溶解度大小的因素为A.温度高低B.溶质、溶剂的量C.溶剂种类D.溶质种类4.下列叙述正确的是A.在饱和溶液中再加入任何物质都不可能溶解B.只有增加溶剂的质量,饱和溶液才可能变成不饱和溶液C.某种溶液可以是稀溶液,但同时又是饱和溶液D.浓溶液一定是饱和溶液5.利用海水晒盐的原理是A.海水受热分解B.升高温度,降低氯化钠在水中的溶解度C.温度升高,使食盐的溶解度增大D.利用阳光和风蒸发水分,使氯化钠成晶体析出6.a、b、c、d四只烧杯中分别盛有10℃、T1℃、T2℃、T3℃不同温度的水各100g,分别向其中加入50g硝酸钾,充分溶解后的情况如下图所示,下列有关判断正确的是A.T1℃<T2℃<T3℃B.T2℃时,硝酸钾的溶解度为50g/100g水C.a、b、c三只烧杯中的溶液都是饱和溶液D.四只烧杯中溶液的溶质质量分数大小关系为:a<b<c=d7.某同学自制汽水(如下图)并记录了心得,下列记录正确的是A.℃中溶质和溶液质量比为1:50B.℃中溶液为碳酸氢钠的不饱和溶液C.℃摇匀放入冰箱后气泡增多D.℃摇匀放入冰箱后有碳酸氢钠析出8.如图为KC1和Na2CO3的溶解度曲线,下列说法错误的是A.T2℃时,Na2CO3饱和溶液质量分数为49.0%B.将两物质的饱和溶液由T1℃升温至T4℃,均无固体析出C.T4℃时,分别将等质量的KC1和Na2CO3溶于水配成饱和溶液,所得溶液的质量前者小于后者D.若KCl溶液中含有少量Na2CO3,可采取蒸发浓缩控制温度T3℃以上降温结晶、过滤等操作提纯9.甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法不正确的是A.甲、乙物质是易溶物质B.t1℃时,甲和丙的饱和溶液中所含溶质质量相等C.将接近饱和的丙溶液变成该温度下的饱和溶液,可采用加入丙物质的方法D.若将t2℃时三种物质等质量的饱和溶液分别降温到t1℃,则析出晶体质量关系是甲>乙>丙10.NaCl和KNO3的溶解度曲线如图所示,下列说法正确的是A.NaCl的溶解度一定大于KNO3B.NaCl的溶解度受温度影响的程度比KNO3大C.40℃时,100gKNO3饱和溶液中含有63.9gKNO3D.将60℃时210gKNO3饱和溶液降温至20℃,析出KNO3晶体78.4g二、实验题11.下表为硝酸钾和氯化钠的部分溶解度数据,某同学进行了如图的溶解实验。
2023中考化学最后冲刺压轴题专练02 溶解度及其应用(解析版)

压轴题02 溶解度及其应用溶解度曲线是中考必考内容,出题概率几乎100%,考查方式有“一线型”、“二线型”、“三线型”、实验与曲线融合型等。
出题方式主要有一下几种:1.溶解度大小的判断及比较2.饱和溶液与不饱和溶液的判断及转化3.改变温度时溶液中各种量的变化情况4.一定温度下配制不同物质的饱和溶液时,溶液质量、溶剂质量、溶质质量的比较5.溶液的稀释6.根据溶解度曲线的升降情况判断提纯方法7.质量分数的计算与比较溶解度曲线的意义:点——曲线上的点表示物质在对应温度时的溶解度,两曲线的交点表示两物质在t℃时的溶解度相等。
线——曲线的走向表示物质的溶解度随温度改变而变化的趋势,曲线的陡缓表示物质溶解度受温度影响的大小。
面——曲线下方的点表示溶液为不饱和溶液,曲线上方的点表示溶液饱和且有未溶解固体 命题角度 1.溶解度大小的判断及比较 溶解度曲线的交点表示两物质在该温度下溶解度相等,同温度下溶解度曲线的交点越高溶解度越大。
2.饱和溶液与不饱和溶液的判断及转化 (1)饱和溶液与不饱和溶液的判断 若g100m m 溶解度溶剂溶质<,为不饱和溶液; 若g100m m 溶解度溶剂溶质=,恰好为饱和溶液; 若g 100m m 溶解度溶剂溶质>,为饱和溶液,且有未溶解的溶质; (2)饱和溶液与不饱和溶液的转化℃温度不变时,改变溶质或溶剂质量不饱和溶液饱和溶液增加溶质或蒸发溶剂增加溶剂℃改变温度时,升温或降温取决于物质的溶解度随温度的变化趋势3.改变温度时溶液中各种量的变化情况改变温度若有溶质析出则溶质质量分数减小,若无溶质析出则溶质质量分数不变4.一定温度下配制不同物质的饱和溶液时,溶液质量、溶剂质量、溶质质量的比较℃溶质的质量与一定时,溶解度越大,配制饱和溶液所需溶剂的质量越小。
℃溶剂的质量一定时,溶解度越大,配制饱和溶液所需溶质的质量越大℃饱和溶液的质量一定时,溶解度越大,所含溶质质量越大,所含溶剂质量越小。
中考化学溶解度练习题含答案

中考化学溶解度练习题含答案一、选择题1.如图所示,分别向盛有100g水的烧杯中加入KNO3,充分溶解。
下列说法正确的是()温度(℃)t1t2KNO3的溶解度(g/100g水)6090A.甲、乙混合后为t1℃的不饱和溶液B.甲、丙溶液中溶质质量相等C.乙升温至t2℃,溶液质量增加D.丙降温至t1℃,有晶体析出答案:B【解析】【分析】溶解度指的是一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。
【详解】A、t1℃硝酸甲的溶解度为60g,即100g溶剂里最多溶解硝酸钾的质量为60g,甲、解析:B【解析】【分析】溶解度指的是一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量。
【详解】A、t1℃硝酸甲的溶解度为60g,即100g溶剂里最多溶解硝酸钾的质量为60g,甲、乙混合后溶剂质量为200g,溶质质量为130g,最多只能溶解120g,属于饱和溶液,故选项不正确;B、根据表中不同温度下的硝酸钾的溶解度可知,甲是t1℃时硝酸钾的饱和溶液,溶解的溶质质量为60g,丙是t2℃硝酸钾的不饱和溶液,溶液中溶质质量为60g,相等,故选项正确;C、由题意可知乙恰好为t1℃的饱和溶液,升温至t2℃,溶液质量不变,故选项不正确;D、t1℃硝酸甲的溶解度为60g,丙降温至t1℃,恰好达到饱和,没有晶体析出,故选项不正确;故选B。
【点睛】固体的溶解度是指在一定温度下,某固体物质在100克溶剂中达到饱和状态时所溶解的质量,根据物质的溶解度即可判断出该温度下一定量的溶液是否饱和;根据物质的溶解度曲线可以判断出物质的溶解度随温度变化的变化情况,从而确定出饱和溶液和不饱和溶液转化时的方法等。
2.根据如图的溶解度曲线判断,下列说法正确的是A.50℃时,A 物质的溶解度为 80B.20℃时,B 的溶解度大于 A 的溶解度C.升温可使 C 物质的饱和溶液变成不饱和溶液D.将 50℃三种物质的饱和溶液分别降温到 20℃时,A 析出固体最多答案:B【解析】【详解】A、50℃时,A物质的溶解度为80g,此选项错误;B、通过分析溶解度曲线可知,20℃时,B的溶解度大于A的溶解度,此选项正确;.C、 C物质的溶解度随温度的降低而增大,所解析:B【解析】【详解】A、50℃时,A物质的溶解度为80g,此选项错误;B、通过分析溶解度曲线可知,20℃时,B的溶解度大于A的溶解度,此选项正确;.C、 C物质的溶解度随温度的降低而增大,所以降温可使C物质的饱和溶液变成不饱和溶液,此选项错误;D、将 50℃三种物质的饱和溶液分别降温到20℃时,饱和溶液的质量不能确定,析出晶体的质量也不能确定,此选项错误。
中考化学--溶解度专题训练含答案

中考化学——19题溶解度(曲线)专题训练1。
(5分)下表列出了KNO3在不同温度下的溶解度.温度/℃0 20 40 60 80 100溶解度/g 13。
3 31.6 63。
9 110 169 246(1)由上表可推出KNO3溶解度曲线的变化规律是。
(2)20℃时,把40 g KNO3放入小烧杯中,然后再加100 g水不断搅拌,形成溶液的质量为 g;该溶液是(填“饱和”或“不饱和”)溶液。
(3)如右图所示,把上述(2)中的小烧杯放到盛水的大烧杯中。
若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,能够使小烧杯中的KNO3溶液溶质的质量分数增大的是(填序号)。
①浓硫酸②硝酸铵③氢氧化钠④冰2.(4分)下表是氯化钠和硝酸钾在不同温度时的溶解度,根据此表回答(1)60℃时,氯化钠的溶解度为g.(2)在30℃时,100g水中加入50g硝酸钾,充分搅拌后得到的溶液质量为g。
(3)欲从海水中获得氯化钠晶体,应采取方法。
(4)由表中数据分析可知,硝酸钾和氯化钠在某一温度时具有相同的溶解度x,则x的取值范围是g.3.(3分)下表是3种物质在不同温度时的溶解度,根据表格信息答题.温度/℃0 20 40 60 80 100溶解度/gNaCl 35.7 36.0 36.6 37。
3 38.4 39.8 KNO313.3 31。
6 63。
9 110 169 246 Ca(OH)20.18 0.16 0。
14 0.12 0。
09 0。
07(1)某饱和溶液随温度升高有固体析出,则该饱和溶液的溶质是(填化学式)。
(2)要配制20℃时的NaCl饱和溶液100g,需要NaCl的质量为g(保留小数点后一位).(3)某KNO3晶体中有少量NaCl、Ca(OH)2杂质,要得到纯净KNO3的方法是:先加热溶解,然后,过滤、洗涤、干燥后得到KNO3晶体。
4、(4分)我国北方有许多盐湖,湖水中溶有大量的Na2CO3和NaCl,那里的人们冬天捞碱(Na2CO3),夏天晒盐(NaCl)。
化学│中考化学溶液 溶解度(有难度)经典

化学│中考化学溶液 溶解度(有难度)经典一、溶液选择题1.图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t 2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )A .t 2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为甲>乙B .将甲、乙两种物质的饱和溶液都从t 2℃将至t 1℃时,两种溶液中溶质的质量分数相等C .向烧杯的水中加NaOH 固体后,只有乙溶液中溶质的质量分数变小D .向烧杯的水中加NH 4NO 3固体后,只有盛放甲溶液的试管中有晶体析出【答案】B【解析】【分析】【详解】A 、图2中两试管底部溶液中都有固体溶质未溶解,因此试管中的溶液均为t 2℃时的饱和溶液,图1显示,t 2℃时甲的溶解度大于乙的溶解度,而饱和溶液中溶质的质量分数=100%+100g溶解度溶解度 ,因此两物质的饱和溶液溶解度大的其饱和溶液的溶质质量分数大,故甲的溶质质量分数大于乙的溶质质量分数,选项A 正确;B 、甲的溶解度随温度的降低而减小,乙的溶解度随温度的降低而增大,将甲、乙两种物质的饱和溶液都从t 2℃将降温至t 1℃时,甲析出晶体,乙的溶解度变大则继续溶解试管内的固体,但溶解固体后是否饱和无法确定,若恰好饱和,则二者的溶质质量分数相等,若溶解后不饱和,则降温后甲的溶质质量分数大于乙的溶质质量分数,故降温后二者的溶质质量分数不一定相等,选项B 错误;C 、氢氧化钠固体溶于水放出大量的热使溶液温度升高,甲物质逐步溶解,溶质的质量分数变大,乙的溶解度减小,析出晶体,溶质质量减小,溶剂不变,所以溶质的质量分数减小,因此只有乙溶液中溶质的质量分数变小,选项C 正确;D 、NH 4NO 3固体溶于水吸收热量使溶液温度降低,甲的溶解度随温度的降低而减小,析出晶体,乙的溶解度随温度的降低而增大,变为不饱和溶液,不会析出晶体,因此只有盛放甲溶液的试管中有晶体析出,选项D 正确。
中考化学化学溶解度综合题及答案解析

A、在t2℃时,a物质的溶解度大于c物质的溶解度,所以a物质的饱和溶液的溶质质量分数大于c物质溶液的溶质质量分数,故A不正确;
B、a、b两种物质的饱和溶液,从t1℃升高到t2℃时,溶解度不变,溶质不变,溶剂不变,所以所得物质溶液溶质的质量分数a<b,故B不正确;
C、t1℃时,100g a、c两物质的溶液中,溶液状态不能确定,所以含a、c的质量不能确定,故C不正确;
故选C。
5.物质甲与乙的溶解度曲线如图所示,下列说法错误的是
A.常温下,乙易溶于水
B.t2℃甲的饱和溶液中溶质的质量分数比乙的饱和溶液大
C.从t2℃降至t1℃,甲溶液中有晶体析出
D.甲的溶解度受温度的影响程度比乙的大
【答案】C
【解析】
【分析】
由物质甲与乙的溶解度曲线可知,甲的溶解度随温度的升高而增大,乙的溶解度随温度的变化基本不变,t1℃时,甲乙两种物质的溶解度相同。
【答案】C
【解析】
A、根据溶解度曲线可知,40℃时,甲的溶解度大于乙的溶解度,正确;B、根据溶解度曲线可知,甲乙物质的溶解度都随温度的升高面增大,正确;C、没有确定溶液的状态,无法判定20℃时,甲乙溶液中溶质的质量分数,错误;D、乙的溶解度随温度降低而减小,将40℃时乙的饱和溶液降温至20℃,有晶体析出,仍然是饱和溶液,正确。故选C。
A、接近饱和的A溶液,降温至10°C时也可能是有晶体析出,故不能说明20℃的A溶液是饱和溶液;
B、蒸发10g水有晶体析出,原溶液可能是饱和溶液,也可能是接近饱和的溶液;故不能说明20℃的A溶液是饱和溶液;
C、由于物质的溶解度一般随着温度的升高而增大,加热到30℃时,一定能溶解A物质,故不能说明20℃的A溶液是饱和溶液;
【答案】A
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
溶液溶解度中考试题1.(4分)下列数据是硝酸钾固体在不同温度时的溶解度。
温度/℃0 20 40 60 80溶解度/g13.3 31.6 63.9 110 169(1)硝酸钾溶液中的溶剂是__________________。
(2)20℃时,向水中加入硝酸钾,充分溶解后得到__________________(填“饱和”或“不饱和”)溶液。
(3)20℃时,向水中加入硝酸钾,若使硝酸钾完全溶解,可以采用的方法是___________________________。
(4)如图所示,小烧杯中盛放的是上述(2)中所得的硝酸钾溶液。
若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是_____________(填字母)。
A.冰B. 浓硫酸C. 硝酸铵D. 干冰E. 氢氧化钠F. 氧化钙2.甲、乙两种固体的溶解度曲线如右图所示。
下列说法中,正确的是A.20℃时,甲溶液中溶质的质量分数一定大于乙溶液B.40℃时,分别在100 g水中加入50 g 甲、乙,所得溶液溶质的质量分数相等C.40℃时,分别在100 g水中加入30 g 甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液D.20℃时,分别在100 g水中加入40 g 甲、乙,加热到40℃时,甲溶液为饱和溶液3.向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。
下列说法正确的是①②③④⑤A.②中A的质量分数最大B.③⑤中A的质量分数相等C.②④⑤的溶液为饱和溶液D.①③④⑤中没有固体存在4.(6分)水和溶液在生命活动和生产、生活中起着十分重要的作用。
⑴“生命吸管”(如右图)是一种可以随身携带的小型水净化器,里面装有网丝、注入了活性炭和碘的树脂等。
其中活性炭起到和过滤的作用。
⑵水常用来配制各种溶液,硝酸钾溶液的溶质为。
⑶农业生产常用溶质的质量分数为10%~20%的NaCl溶液来选种。
现将300 g 25%的NaCl溶液稀释为15%的NaCl溶液,需要加水的质量为 g。
⑷根据下表问题。
温度/℃0 20 40 60 80 100 溶解度/gNaCl 35.7 36.0 36.6 37.3 38.439.84NH Cl29.4 37.2 45.8 55.2 65.6 77.3①60℃时,向两个分别盛有50 g NaCl和4NH Cl的烧杯中,各加入100 g的水,资料:A的溶解度温度/℃20 30 40 50 60溶解度/g 37.2 41.4 45.8 50.4 55.2充分溶解后,为饱和的是 溶液。
②采用一种操作方法,将上述烧杯中的剩余固体全部溶解,变为不饱和溶液。
下列说法正确的是 (填字母序号)。
A .溶质的质量不变B .溶液中溶质的质量分数一定减小C .溶液质量可能不变D .可升高温度或增加溶剂5.甲、乙两种物质的溶解度曲线如右图所示。
下列叙述正确的是A .依据溶解度曲线可判断,甲的溶解度比乙的大B .将甲、乙的饱和溶液从t 2℃降到t 1℃,析出甲的质量大C .将t 2℃时甲的饱和溶液变为不饱和溶液,可采取降温的方法D .t 1℃时,甲和乙的饱和溶液各100g ,其溶质的质量一定相等6.a 、b 、c 三种物质的溶解度曲线如下图所示。
取等质量 ℃的 a 、b 、c 三种物质的饱和 溶液,分别蒸发等量水后恢复至 ℃。
下列说法不正确的是A .原饱和溶液中,溶质的质量分数 a>b=cB .恢复至 t 2℃℃时,析出溶质的质量 a>b=cC .恢复至t 2℃时,三种溶液一定都是饱和溶液D .若继续降温至 t 1℃,三种溶液一定都是饱和溶液7.甲、乙两种固体的溶解度曲线如右图所示,下列说法正确的是A .甲的溶解度大于乙的溶解度B .t 1℃时,甲、乙饱和溶液中溶质的质量分数均为15%C .t 2℃时,将甲、乙的饱和溶液降温至t 1℃,甲析出的固体一定大于乙D .t 2℃时,向30 g 甲、乙中分别加入100 g 水,所得溶液中溶质的质量分数甲一定大于乙8.(2013.兰州市) 下列关于溶液的说法,正确的是 ( )A. 溶液都是无色透明的B. 面粉与水混合可形成溶液C. 饱和溶液不能再溶解任何物质D. 硝酸铵溶解在水中,溶液温度会降低9.(2013.上海市)厨房中的物质放入足量的水中,充分搅拌,不能形成溶液的是 ( )A. 食用油B. 白醋C. 白糖D. 食盐10.(2013.北京市)下列物质放入水中,能形成溶液的是 ( )A .面粉B .牛奶C .白糖D .植物油11.(2013.泸州市)调味品是重要的食品添加剂,将下面调味品加入水中,不能形成溶液的是 ( )A.食盐B.蔗糖C.味精D.芝麻油12.(2013.佛山市)以下说法正确的是( )A.溶液一定是均一、无色、稳定的 B.均一、稳定的液体一定是溶液C.溶液的溶质一定是固体 D.溶液一定是混合物13.(3分)(2013•滨州)关于溶液和乳化的下列说法这种错误的是( )A. 溶液中可以含有多种溶质30 15溶 解 度 /g t 1 t 2 温度/℃ 甲 乙B. 溶液是均一、稳定的混合物C.用汽油洗去衣服上的油污是乳化现象D. 溶液不一定是无色的14.(2013.株洲市)下列物质溶于水时,吸收热量的是()A.NH4NO3固体B.生石灰C.KOH固体D.苛性钠15.(2013.南宁市)把少量下列物质分别加入水中,充分搅拌后,不能形成溶液的是()A.食盐B.蔗糖C.酒精D.花生油16.(2013.昆明市)下列关于溶液的说法正确的是()A.溶液一定是无色的 B.溶质只能是固体物质C.溶液是均一的、稳定的混合物 D.将少量泥土放入水中,充分搅拌,可以得到溶液17. (2013.兰州市)欲配制100g质量分数为10%的氢氧化钠溶液。
下列说法中不正确的是()A. 用托盘天平称取10.0g氢氧化钠B. 氢氧化钠易潮解,应放在玻璃器皿中称量C. 实验中用到的玻璃仪器只有烧杯和量筒D. 将配好的溶液装入试剂瓶中,塞好瓶塞并贴上标签18.(2013.成都)在盛有水的烧杯中加入以下某种物质,形成溶液的过程中,温度下降。
这种物质是()A. 氢氧化钠B.氯化钠C.浓硫酸D.硝酸铵19.(2013.日照市)配制50g质量分数为6%的氯化钠溶液,下列说法不正确的是()A.实验中用到的玻璃仪器有烧杯、量筒、玻璃棒和胶头滴管B.用托盘天平称量所需氯化钠的质量3.0gC.用10mL量筒量取所需水的体积 D.实验步骤是计算、称量、量取、溶解20.(2013.北京市)配制50 g溶质的质量分数为 6%的氯化钠溶液,不需要的仪器是()A.蒸发皿 B.玻璃棒 C.烧杯 D.量筒21(2013.南京市)下列物质加入一定量的水中,能使液体温度明显降低的是()A.硝酸铵 B.氢氧化钠 C.生石灰 D.氯化钠22.(2013.庆阳市)某同学在实验室配制50g6%的氯化钠溶液,图2所示的部分操作其中错误的是()A.取一定量的NaClB.称取3gNaClC.量取47mL水D.溶解23.(2013.佛山市)100克2%NaOH溶液配制等操作正确的是()A.用50mL量筒量取98.0mL水B.将NaOH固体放入小烧杯中,用托盘天平称取2.0gNaOHC.将pH试纸伸入2%NaOH溶液中测得pH=13.7D.10ml2%的NaOH溶液加入10mL水稀释得到1%NaOH溶液24.(2013.烟台市)有关溶液的说法正确的是()A.具有均匀性、稳定性的液体一定是溶液B.配制溶液时,搅拌可以增大固体溶质的溶解度C.饱和溶液的浓度一定比不饱和溶液的浓度大D.融雪剂的原理是利用某些物质水溶液的凝固点低于0℃25(2013.株洲市)下列实验操作正确的是()A.制取蒸馏水时,将温度计水银球插入水中B.过滤时,将玻璃棒靠在三层滤纸的一边C.测某酸性溶液的pH时,先用水将pH试纸润湿D.在“粗盐中难溶性杂质的去除”实验中,将蒸发皿中的溶液直接蒸干26.(2013.佛山市)常温下,将1克物质分别加入100g水中,充分搅拌(或振荡),能配制成溶液的是()A.汽油B.蔗糖C.氯化银D.氧化铁27.(2013•滨州)向如图装置的试管中加入某种物质后,U形管右边支管的红墨水液面降低,左边支管的红墨水液面上升,则加入的物质是()A. 氢氧化钠B. 生石灰C. 浓硫酸D. 硝酸铵28.(2013.成都)20℃时,氯化钠的溶解度为36g。
对这句话理解错误的是()A.20℃时,100g水中最多能溶解氯化钠36gB.20℃时,100g氯化钠饱和溶液中含氯化钠36gC.20℃时,氯化钠饱和溶液中水与氯化钠的质量比为100:36D.20℃时,将36g氯化钠溶解于100g水中,所得溶液为该温度下氯化钠的饱和溶液29.(2013.资阳市)t ℃时,向一支盛有0.15 g熟石灰的烧杯中加入50 g水,充分振荡后静置,烧杯底部仍有未溶解的白色固体。
下列相关叙述正确的是()A.升高温度上层清液变为不饱和溶液B.t ℃时,熟石灰的溶解度为0.3 g C.烧杯中溶液的质量小于50.15 g D.上层清液中溶质质量分数大于0.3% 30.(2013.菏泽市)下列有关溶液的叙述正确的是()A.稀溶液一定是不饱和溶液B.饱和溶液就是不能再溶解如何物质的溶液C.溶质的溶解度都随温度的升高而增大D.溶质在溶解的过程中,有的放出热量,有的吸收热量参考答案1.(1)水(2)饱和(3)加水(或升温)(4)ACD2.C3.D4.⑴吸附⑵KNO⑶ 200 ⑷①NaCl②B35.D6.D7.D8.D9.A 10.C 11.D 12.D13.C14.A15.D16.C17.C18.D19.C20.A21.A22.C23.B24.D 25.B 26.B27.D 28.B 29.C 30.D。
