物理化学实验
物理化学实验

物理化学实验Physical Chemistry Experiment(化学96学时)一、任务和要求1.物理化学实验的主要任务物理化学实验作为化学实验科学的重要分支,是化学专业学生必修的一门独立的基础实验课程。
物理化学实验的主要目的和任务是使学生初步了解物理化学的研究方法,并通过实验熟悉物质物理化学性质与反应规律之间的关系,学会需要的物理化学实验技术,掌握实验数据的处理及实验结果的分析与归纳方法,从而加深对物理化学基本理论和概念的理解,增强解决实际化学问题的能力。
通过结构化学部分的实验,帮助学生生动地理解和总结分子结构与性质的关系,培训学生的一种新的思维体制,以便进入化学领域的更高层次。
2.基本内容和基本要求1.本课程由实验和讲座两个教学环节组成。
实验方面,要求完成20个基础实验,分为16个物理化学实验和4个结构化学实验。
通过本实验使学生初步掌握必要的物理化学和结构化学实验实验方法,熟悉各种物理化学现象,并学会实验数据的归纳和分析方法。
实验讲座的目的在于提高学生解决实际问题的能力,使学生在实验操作训练基础上能对物理化学的实验方法和实验技术有较系统的概括了解。
2.实验内容的选取,包括热力学、电化学、动力学、表面现象、结构化学等部分有代表性的实验,使学生了解物理化学的概貌,另一方面,根据现有仪器设备条件,力求在实验方法和实验技术上得到全面的训练。
3.实验讲座包括物理化学实验基础知识,主要实验方法技术(包括温度的测量和控制、真空技术、电化学测量技术、光化学测量技术、测压技术和数据的计算机处理技术等内容),尽可能反映近代科学研究和实验仪的新成就。
另外要介绍实验的安全防护、误差问题、数据表达方法、文献数据查阅和实验设计思想等。
二、适用专业化学专业。
三、实验内容、实验类型和学时安排实验总学时为96学时,其中物理化学实验为77学时(1-16),结构化学实验为19学时(17-20),分两学期进行。
四、实验内容实验一恒温水浴的组装及性能测试目的要求(1)了解恒温槽的组成,掌握其控温原理(2)学会评价恒温槽的恒温效能。
十二个物理化学中考实验

十二个物理化学中考实验
中考物理化学实验包括多个不同的实验,以下是12个常见中考物理化学实验:
1. 物质密度的测量
2. 测量物体的温度
3. 测量电流和电压
4. 欧姆定律的实验
5. 测量功率和电能
6. 物质燃烧实验
7. 物质溶解实验
8. 物质酸碱性的测定
9. 物质氧化还原实验
10. 物质电解实验
11. 物质表面张力实验
12. 物质光的折射实验
请注意,以上仅为示例,具体考试中涉及的实验会根据地区和考试要求有所不同。
建议查阅所在地区的中考大纲或咨询相关人员,以获取更准确的信息。
物理化学实验

实验一 磺基水杨酸铁配合物稳定常数的测定一.实验目的1.了解比色法测定溶液中配合物的组成和稳定常数的原理。
2.学习分光光度计的使用方法。
二.基本原理磺基水杨酸(SO 3HHOCOOH简化为H 3R ),与Fe 3+可以形成稳定的配合物,配合物的组成随溶液的pH 值的不同而改变。
在pH=2~3时,pH=4~9时,pH=9~11.5时,磺基水杨酸与Fe 3+能分别形成不同颜色且具有不同组成的配离子。
本试验是测定pH=2~3时形成的紫红色的磺基水杨酸铁配离子的组成及其稳定常数。
实验中通过加入一定量的HClO 4溶液来控制溶液的pH 值。
测定配离子的组成时,分光光度法是一种有效的方法。
实验中,常用的方法有两种:一是摩尔比法,一是等摩尔数连续变化法(也叫浓比递变法)。
本实验采用后者,用上述方法时要求溶液中的配离子是有色的,并且在一定条件下只生成这一种配合物,本实验中所用的磺基水杨酸是无色的,Fe 3+溶液很稀,也可以认为是无色的,只有磺基水杨酸铁配离子显紫红色,并且能一定程度的吸收波长为500nm 的单色光。
光密度又称吸光度,是指光线通过溶液或某一物质前的入射光强度与该光线通过溶液或物质后的透射光强度比值的对数,可用分光光度计测定。
光密度与浓度的关系可用比尔定律表示:CL A ε=其中:A 代表光密度;ε代表某一有色物质的特征常数,称之为消光系数;L 为液层厚度;C 为溶液浓度,当液层厚度一定时,则溶液光密度就只与溶液的浓度成正比。
本实验过程中,保持溶液中金属离子的浓度(C M )与配位体的浓度(C R )之和不变(即总摩尔数不变)的前提下,改变C M 与C R 的相对量,配制一系列溶液,测其光密度,然后再以光密度A 为纵坐标,以溶液的组成(配位体的物质的量分数)为横坐标作图,得一曲线,如图1所示,显然,在这一系列溶液中,有一些是金属离子过量,而另一些溶液则是配位体过量,在这两部分溶液中,溶液离子的浓度都不可能到最大值,因此溶液的光密度也不可能达到最大值,只有当溶液中金属离子与配位体的摩尔比与配离子的组成一致时,配离子的浓度才最大,因而光密度才最大,所以光密度最大值所对应的溶液的组成,实际上就是配合物的组成。
物理化学实验
实验1 燃烧热的测定1. 实验目的1.1掌握氧弹量热计的使用;用氧弹量热计测定萘的燃烧热;1.2掌握氧气钢瓶的使用。
2. 实验原理称取一定量的试样置于氧弹内,并在氧弹内充入1.5 ~ 2.0MPa的氧气,然后通电点火燃烧。
燃烧时放出的热量传给水和量热器,由水温的升高(△T)即可求出试样燃烧放出的热量:Q=K·△T式中K为整个量热体系(水和量热器)温度升高1℃所需的热量。
称为量热计的水当量。
其值由已知燃烧热的苯甲酸(标样)确定。
K =Q /△T式中△T应为体系完全绝热时的温升值,因而实测的△T须进行校正。
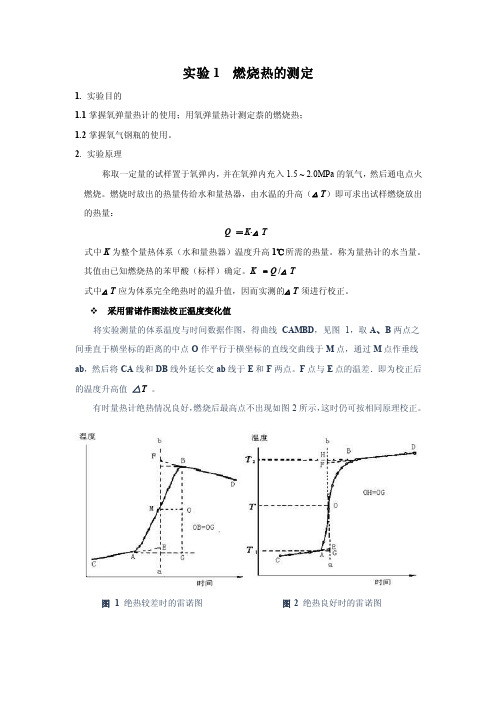
采用雷诺作图法校正温度变化值将实验测量的体系温度与时间数据作图,得曲线CAMBD,见图1,取A、B两点之间垂直于横坐标的距离的中点O作平行于横坐标的直线交曲线于M点,通过M点作垂线ab,然后将CA线和DB线外延长交ab线于E和F两点。
F点与E点的温差.即为校正后的温度升高值△T。
有时量热计绝热情况良好,燃烧后最高点不出现如图2所示,这时仍可按相同原理校正。
图 1 绝热较差时的雷诺图图2 绝热良好时的雷诺图3. 仪器与试剂3.1试剂:分析纯苯甲酸(QV=26480 J·g-1);待测样;引火丝(Ni-Cr丝,QV=8.4 J·cm -1)3.2仪器:HR-15A数显型氧弹量热计一台;压片机(苯甲酸和萘各用一台);精密贝克曼温差温度计(精确至0.01 ℃,记录数据时应记录至0.002 ℃);台秤一台;分析天平一台。
4. 实验步骤4.1水当量的测定(1)打开控制箱预热。
(2)量取10 cm引火丝并准确称重。
(3)在台秤上粗称试样1 g ~ 1.2 g;用压片机压片,同时将燃烧丝压入。
准确称重,减去引火丝重量后即得试样重量。
注意压片前后应将压片机擦干净;苯甲酸和待测试样不能混用一台压片机。
(4)将氧弹盖放在专用架上,将点火丝两端固定在氧弹电极上点火丝切勿接触坩锅,以防短路。
(5)取少量(~2 mL)水放入氧弹中(吸收空气中的N2燃烧而成的HNO3),盖好并拧紧弹盖,接上充气导管,慢慢旋紧减压阀螺杆,缓慢进气至表上指针为1.5 ~ 2.0 MPa。
《物理化学实验》教学大纲

《物理化学实验》课程大纲一、课程基本信息课程名称:(中文):物理化学实验(英文):Physical Chemistry Experiments 课程代码:08S3119B、08S3120B课程类别:专业核心课程/必修课适用专业:材料化学专业课程学时:总学时30(春季学期15学时秋季学期15学时)课程学分:总学分1先修课程:无机及分析化学、无机及分析化学实验、有机化学、有机化学实验、高等数学、普通物理、普通物理实验等选用教材:《物理化学实验》(第三版),复旦大学等编,北京:高等教育出版社,2004年参考书目:1.《化工辞典》(第四版),化学工业出版社,2000年2.《物理化学实验指导书》,长春:东北师范大学出版社,1995年二、课程目标(一)课程具体目标通过本课程的学习,学生达到以下目标:1.加深巩固学生对物理化学基本理论及基本知识的理解。
使学生初步掌握基本实验方法和实验技能,加深对物理化学的重要理论和概念的理解;初步学会处理实验数据、分析与归纳实验现象和表达实验结果。
【毕业要求1工程知识】2.提高学生分析问题和解决实际问题的能力。
提高严谨缜密的科学思维能力,培养学生的创新精神。
【毕业要求2问题分析】3.培养学生实事求是的科学态度和良好的科学素养、工作习惯,并具备初步的团队合作精神。
【毕业要求8职业规范9个人和团队10沟通能力】(二)课程目标与专业毕业要求的关系三、课程学习内容物理化学实验主要设置两种类型的实验:(1)基本操作训练,(2)研究设计性实验。
实验过程包括课前预习讨论、实验操作、实验报告、结果讨论等环节。
学生在实验前必须进行预习,预习报告或设计实验方案经老师批阅后,方可进入实验室进行实验。
(1)基本操作技术作为一门独立开设的基础实验课程,物理化学实验具体到各个部分,教学内容如下:①.热力学和相图部分四个实验:液体摩尔汽化热、燃烧热的测定、二组份简单共熔体系相图、双液系相图。
理解纯液体饱和蒸气压和温度的关系,测定特定温度范围内液体的平均摩尔汽化热及正常沸点;掌握氧弹式量热计测定固体燃烧热的原理;理解热分析法绘制合金体系相图的原理,并对低共熔而组分合金的相机进行分析。
物理化学实验报告_实验报告_

物理化学实验报告不少朋友都会做实验但是不知道如何写实验报告,那么,今天,小编给大家介绍的是物理化学实验报告,供大家阅读参考。
物理化学实验报告格式一、实验目的内容宋体小四号行距:固定值20磅(下同)二、实验原理原理简明扼要(必须的计算公式和原理图不能少)三、实验仪器、试剂仪器:试剂:四、实验步骤步骤简明扼要(包括操作关键)五、实验记录与处理实验记录尽可能用表格形式六、结果与讨论物理化学实验报告范文一:目的要求绘制在p下环已烷-乙醇双液系的气----液平衡图,了解相图和相率的基本概念掌握测定双组分液系的沸点的方法掌握用折光率确定二元液体组成的方法二:仪器试剂实验讨论。
在测定沸点时,溶液过热或出现分馏现象,将使绘出的相图图形发生变化?答:当溶液出现过热或出现分馏现象,会使测沸点偏高,所以绘出的相图图形向上偏移。
讨论本实验的主要误差来源。
答:本实验的主要来源是在于,给双液体系加热而产生的液相的组成并不固定,而是视加热的时间长短而定因此而使测定的折光率产生误差。
三,被测体系的选择本实验所选体系,沸点范围较为合适。
由相图可知,该体系与乌拉尔定律比较存在严重偏差。
作为有最小值得相图,该体系有一定的典型义意。
但相图的液相较为平坦,再有限的学时内不可能将整个相图精确绘出。
四,沸点测定仪仪器的设计必须方便与沸点和气液两相组成的测定。
蒸汽冷凝部分的设计是关键之一。
若收集冷凝液的凹形半球容积过大,在客观上即造成溶液得分馏;而过小则回因取太少而给测定带来一定困难。
连接冷凝和圆底烧瓶之间的连接管过短或位置过低,沸腾的液体就有可能溅入小球内;相反,则易导致沸点较高的组分先被冷凝下来,这样一来,气相样品组成将有偏差。
在华工实验中,可用罗斯平衡釜测的平衡、测得温度及气液相组成数据,效果较好。
五,组成测定可用相对密度或其他方法测定,但折光率的测定快速简单,特别是需要样品少,但为了减少误差,通常重复测定三次。
当样品的折光率随组分变化率较小,此法测量误差较大。
物理化学实验主要教学内容和教学要求

物理化学实验主要教学内容和教学要求大家好,今天我们来聊聊物理化学实验这个话题。
我们要明确一点,物理化学实验可不是什么高深莫测的东西,它就是让我们通过实际操作,去感受科学的魅力,培养我们的动手能力和观察力。
那么,物理化学实验主要包括哪些内容呢?又有哪些教学要求呢?接下来,我们就一一来聊聊。
我们来说说物理化学实验的主要教学内容。
物理化学实验主要包括以下几个方面:1. 基本仪器的使用:比如量筒、烧杯、试管等。
这些都是我们在实验室里经常用到的工具。
学会正确使用这些工具,对于我们今后的学习和工作都是非常重要的。
2. 基本实验操作:比如滴定、萃取、蒸馏等。
这些实验操作虽然看似简单,但其实需要我们掌握一定的技巧。
只有熟练掌握了这些技巧,我们才能在实验中取得更好的效果。
3. 基本理论知识的运用:在实验过程中,我们需要将所学的理论知识运用到实际操作中去。
这样既能巩固我们的理论知识,又能提高我们的实践能力。
4. 实验数据的处理与分析:实验完成后,我们需要对实验数据进行处理和分析。
这不仅能帮助我们了解实验结果,还能锻炼我们的数据处理能力。
接下来,我们来说说物理化学实验的教学要求。
在进行物理化学实验时,我们需要遵循以下几个方面的要求:1. 安全第一:实验室里的危险物品很多,所以我们在进行实验时一定要注意安全。
遵守实验室的安全规定,佩戴好防护用品,确保自己和他人的安全。
2. 严谨认真:实验过程中,我们要做到严谨认真,不允许有任何的马虎。
因为一丝不苟的态度,往往能带来意想不到的收获。
3. 团队协作:实验过程中,我们需要与同学们密切配合,共同完成实验任务。
团队协作能力的培养,对于我们今后的学习和工作都是非常重要的。
4. 勤于思考:在实验过程中,我们要敢于提问,勇于质疑。
通过思考和质疑,我们能更好地理解实验原理,提高自己的学术素养。
5. 善于总结:实验结束后,我们要认真总结实验过程和结果,找出存在的问题和不足,为今后的学习和工作积累经验。
物理化学实验心得

物理化学实验心得在大学的学习生涯中,物理化学实验是一门极具挑战性和启发性的课程。
通过一系列精心设计的实验,我不仅亲身体验了物理化学的理论知识在实际中的应用,还培养了自己的实验技能、科学思维和解决问题的能力。
还记得第一次走进物理化学实验室时,心中充满了好奇和期待。
实验台上整齐摆放着各种仪器设备,如分光光度计、电位差计、恒温槽等等,这些陌生而又神秘的仪器让我感受到了科学的严谨和精细。
在老师的耐心指导下,我们逐渐熟悉了实验仪器的使用方法和操作规范,为后续的实验打下了坚实的基础。
物理化学实验的一大特点就是对实验数据的精确测量和处理。
在实验过程中,我们需要仔细地读取仪器上的数值,记录实验条件和现象,并对数据进行及时、准确的处理。
例如,在燃烧热的测定实验中,我们需要精确测量样品的质量、燃烧前后的温度变化以及周围环境的热交换等数据,然后通过复杂的公式计算出样品的燃烧热。
这个过程不仅需要我们具备扎实的数学基础和运算能力,还需要我们保持高度的耐心和细心,任何一个微小的误差都可能导致实验结果的偏差。
在实验中,误差分析是一个非常重要的环节。
由于实验条件的限制、仪器的精度以及人为操作的因素等,实验数据往往会存在一定的误差。
通过对误差的来源进行分析和评估,我们可以采取相应的措施来减小误差,提高实验结果的准确性。
比如,在凝固点降低法测定摩尔质量的实验中,我们发现搅拌速度不均匀会导致溶液的冷却速度不一致,从而影响凝固点的测量。
于是,我们通过控制搅拌速度,使得溶液在冷却过程中温度均匀下降,有效地减小了误差。
除了数据测量和误差分析,实验方案的设计和优化也是物理化学实验的重要内容。
在进行实验之前,我们需要对实验原理进行深入的理解,根据实验目的和要求,制定合理的实验方案。
在实验过程中,我们还要根据实际情况对实验方案进行调整和优化。
例如,在电动势的测定实验中,最初我们选择的测量电路存在较大的误差,经过与老师和同学的讨论,我们对电路进行了改进,采用了补偿法来测量电动势,大大提高了实验结果的准确性。
物理化学实验

根据不同的实验温度-时间曲线图,可计算出 恒温水浴的灵敏度,并对其性能进行评价。
凝固点降低法测相对分子质量
实验目的:
1 、掌握溶液凝固点的测定技术。 2 、掌握温差测量仪的使用方法。 3 、用凝固点降低法测定萘的相对分子 质量。
二、实验原理
对组成一定的二组分低共熔混合物体系来 说,可以根据其步冷曲线,判断有固体析出时 的温度和最低共熔点的温度。作一系列组成不 同的体系的步冷曲线,找出各转折点,即可画 出二组分体系最简单的相图(温度-组成图)。
不同组成溶液的步冷曲线与对应
相图的关系可从下图看出。
电导法测定水溶性表面活性剂 的临界胶束浓度
一、实验预习(10 %)
实验前预习是顺利完成实验的基本保证,通过预 习,要求对实验基本原理、实验方法、仪器使用、 数据处理等方面的内容做到心中有数,避免盲目 地边看讲义边操作。 具体的预习内容如下: 要求了解实验目的、实验方法、所用仪器设备等, 掌握实验基本原理、实验操作要领以及实验数据 处理方法等。避免实验时的盲目性。
步冷曲线
通常的做法是先将体系 全部熔化,然后让其、时间(t)为横坐标 作图,得步冷曲线。上图是二组分金属体系的一种 常见类型的步冷曲线。当体系均匀冷却时,如果体 系不发生相变,则温度随时间的变化将是均匀的, 冷却也较快(如图中的ab段)。
要求在预习本中预先画出规范的数据记录格式, 包括实验项目,测试内容、测量次数等。 要求对预习时所遇到的难点、疑点和设想等提 出讨论,培养学习的主动性和积极性。 实验预习须在实验前按实验安排进行,没有预 习者需当场预习、通过提问后才能参加实验。 预习内容记录在专门的预习本上,并保留至本 实验课程结束。
物理化学实验

物理化学实验第一篇:物理化学实验物理化学实验大三上学期实验一恒温槽 1.实验原理:恒温槽之所以能维持恒温,主要是依靠恒温控制器来控制恒温槽的热平衡。
当恒温槽因对外散热而使水温降低时,恒温控制器就使恒温槽内的加热器工作,待加热到所需温度时,它又使加热器停止加热,保持恒定水温。
2.实验仪器:玻璃恒温水浴精密数字温度温差仪 3.数据处理:恒温槽灵敏度te=±(t1-t2)/2(t1为最高温度,t2为最低温度),灵敏度曲线(温度-时间)4.课后题:⑴恒温槽主要由哪几个部分组成,各部分作用是什么?答:①浴槽:盛装介质②加热器:加热槽內物质③搅拌器:迅速传递热量,使槽内各部分温度均匀④温度计:观察槽内物质温度⑤感温元件:感应温度,指示加热器工作⑥温度控制器:温度降低时,指示加热器工作,温度升高时,只是加热器停止工作。
⑵对于提高恒温槽的灵敏度,可以哪些方面改进?答:①恒温槽的热容要大些,传热质的热容越大越好。
②尽可能加快电热器与接触温度计间传热的速度,为此要使感温元件的热容尽量小,感温元件与电热器间距离要近一些,搅拌器效率要高。
③做调节温度的加热器功率要小。
⑶如果所需恒定的温度低于室温如何装备恒温槽?答:通过辅助装臵引入低温,如使用冰水混合物冰水浴,或者溶解吸热的盐类盐水浴冷却(硝铵,镁盐等)实验二燃烧焓1实验原理:将一定量的待测物质在氧弹中完全燃烧,燃烧时放出的热量使热量计本身及氧弹周围介质的温度升高,通过测定燃烧前后热量计温度的变化值,就可以算出该样品的燃烧热,其关系式为mQv=C△T-Q点火丝m点火丝。
2仪器与药品:氧弹热量计压片机精密数字温度温差仪萘苯甲酸 3数据处理:雷诺温度校正曲线将燃烧前后历次观测到的水温记录下来,并作图,连成abcd线。
图中b点相当于开始燃烧之点,c点为观测到的最高温度点,由于热量计与外界的热量交换,曲线ab及cd常常发生倾斜。
取b点所对应的温度T1,c点所对应的温度T2,其平均温度(T1+T2)/2为T,经过T点作横坐标的平行线TO',与折线abcd相交于O'点,然后过O'点作垂直线AB,此线与ab线和cd线的延长线交于E,F两点,则E点和F点所表示的温度差即为欲求温度的升高值ΔT。
物理化学实验

实验一 燃烧热的测定一、实验目的1.掌握氧弹卡计的使用方法及测量物质燃烧热的实验技术。
2.了解恒压燃烧热与恒容燃烧热的差别和相互关系。
3.学会绘制雷诺曲线并用图解法校正温度的改变值。
二、实验原理量热法测定有机物的燃烧热是热力学实验的一个基本方法。
测量热效应的仪器称为量热计,用量热计测得的是实验温度下的恒容燃烧热v Q ,从手册上查到的燃烧热数值都是在298.15K ,101.325kPa 条件下的标准摩尔燃烧焓,属于恒压燃烧热p Q 。
热力学第一定律指出了恒压燃烧热与恒容燃烧热之间的关系为g + n p v Q Q RT =∆ (1)式中Δn g 为反应前后气体物质的量之差;R 为气体常数;T 为实验温度。
为了计算相对误差,需要从两个方面对所测的的恒容燃烧热进行转换:首先利用(1)式转换为实验温度下恒压燃烧热,然后根据基希霍夫定律转换为298.15 K 的恒压燃烧热,从而和理论值进行比较。
量热计种类较多,本实验采用氧弹卡计测定萘的燃烧热。
测量的基本原理是能量守恒定律,即样品在体积固定的氧弹中燃烧放出的热、引火丝燃烧放出的热和由氧气中微量的氮气氧化成硝酸的生成热,大部分被水桶中的水吸收;另一部分则被氧弹、水桶、搅拌器及温度计等所吸收。
在量热计与环境没有热交换的情况下,可以写出如下的热量平衡公式:3v HNO m Q f g Vb C T M⋅++=∆点火丝点火丝卡(2) 式中m 为待测物的质量(克);M 为待测物质的摩尔质量; Q v 为待测物的摩尔燃烧热;f 点火丝为点火丝的燃烧热(焦/克);(J 铁丝= -6700 J/g ,J 铜丝= -2500 J/g ,J 镍铬丝= -1400 J/g ,J 棉线= -17500 J/g );g 为点火丝的质量(克); b 为硝酸生成热的滴定校正(每毫升0.1mo l ·dm -3的氢氧化钠相当于-5.983 J 的热值);ΔT 为样品燃烧前后的卡计温度变化值;C 卡为卡计(包括卡计中的水)的水当量,它表示卡计(包括介质)每升高一度所需要吸收的热量。
物理化学实验报告

物理化学实验报告实验目的,通过本实验,掌握物理化学实验的基本操作技能,了解物理化学实验的基本原理和方法。
实验仪器,电子天平、容量瓶、分析天平、热力学仪器等。
实验原理,本实验主要涉及物理化学的热力学和动力学原理。
通过测量不同物质的密度、溶解度、热容量等物理化学性质,来探究物质的基本特性。
实验步骤:1. 密度测量,首先使用电子天平测量样品的质量,然后使用容量瓶测量样品的体积,通过质量和体积的比值计算出样品的密度。
2. 溶解度测量,将样品加入一定量的溶剂中,通过分析天平测量样品在溶剂中的溶解度,探究溶解度与温度、溶剂种类等因素的关系。
3. 热容量测量,利用热力学仪器测量样品在不同温度下的热容量,了解样品在不同温度下的热学特性。
实验结果与分析:通过实验数据的测量和分析,我们得到了样品的密度、溶解度和热容量等物理化学性质。
通过对实验结果的分析,我们可以得出一些结论:1. 样品的密度与其化学成分和结构有关,不同样品的密度差异较大。
2. 样品的溶解度受温度影响较大,随着温度的升高,溶解度也会增加。
3. 样品的热容量随着温度的变化而变化,不同样品的热容量差异较大。
结论:通过本实验,我们深入了解了物理化学实验的基本原理和方法,掌握了测量密度、溶解度和热容量等物理化学性质的技能。
这些知识和技能对我们进一步学习和研究物理化学领域具有重要的意义。
总结:物理化学实验是物理化学学科的重要组成部分,通过实验学习,我们不仅可以掌握基本的操作技能,还可以深入理解物质的基本性质和规律。
希望通过今后的学习和实践,我们能够进一步提高实验技能,为物理化学领域的研究和应用做出贡献。
物理化学实验

物理化学实验(Physical Chemistry Experiment)目的和要求物理化学实验是化学实验科学的重要分支,它综合了化学领域中各分支所需要的基本研究工具和方法。
它与物理化学课程紧密配合,但又是一门独立的、理论性与实践性和技术性很强的课程。
物理化学实验的主要目的是使学生能掌握物理化学实验的基本方法和技能,从而能根据所学的原理设计实验、选择和使用仪器,其次是锻炼学生观察实验现象、正确记录和处理数据、分析实验结果的能力,培养严肃认真、事实求是的科学态度和作风;第三是巩固和加深对物理化学原理的理解,提高学生对物理化学知识灵活应用的创新能力。
为实现厦门大学达到国内一流、国际上有较大影响的综合性大学,应该改革旧的、不适于生产力发展的教学方式和方法,减少验证性实验,把新的科研成果和研究技术引入教学中来,让科研成果充实实验教学内容,同时也为培养科研人才打下坚实基础。
在加强学生动手能力的培养的同时,也应注重学生使用计算机处理数据、进行曲线模拟和分析实验结果的能力。
基本内容和学时分配本课程内容包括实验讲座、实验和考试三个部分。
实验讲座除了绪论及误差与数据处理的内容在实验前专门集中讲解外,其余部分均结合在每个实验中穿插进行,例如在“金属相图”中讲解热电偶的焊接与校正;在“饱和蒸气压测定”及“碳酸钙热分解”实验中讲解真空技术等,一般每个实验前都要讲解近一个小时,把一些相关技术进行讲解和示范。
考试对于化学系学生是笔试为主,笔试与实验成绩比例为3:7。
平时实验成绩分配如下:预习15%、态度5%、卫生5%、操作35%、实验报告15%、实验结果与讨论25%。
实验讲座由绪论、误差与数据处理作为基本知识,安排在学生进入实验室前讲完,学时为4,其他讲座内容是结合各个实验内容,把知识点、仪器的使用等相关知识在每个实验前讲解,每次讲座学时为1。
一、基本知识讲座内容:1. 绪论物理化学实验的目的和要求课程的具体安排课程的预习、实验操作和实验报告的要求物化实验课程的评分标准及考试、考核办法物理化学实验室的规章制度2. 误差和数据处理系统误差的判断和消除法函数的算术平均误差和标准误差,曲线拟合误差的计算有效数字的运算法规和数据的正确表达实验仪器的合理搭配3. 数据的列表与作图规则:数据的列表规则直线图(作图的要求,注意事项,作图的精确度等)曲线图(作曲线图的工具,注意事项,作图精度的表示等)作图技术在数据处理中的地位和运用Lotus-1、2、3程序的计算机数据处理和作图方法二. 实验内容及具体要求1. 恒温槽的装置及性能测试本实验包括温度的测量和控制技术讲座,总学时为7。
物理化学实验内容

物理化学实验内容
1.气体的摩尔质量测定实验:利用气体密度和摩尔质量之间的关系,通过测量气体的密度来计算气体的摩尔质量。
2. 摩尔热容实验:测量气体在不同温度下的热容,从而确定气体的摩尔热容。
3. 热力学第一定律实验:测量气体在恒定体积下的内能变化,验证热力学第一定律。
4. 热力学第二定律实验:通过测量气体在不同温度下的熵变来验证热力学第二定律。
5. 电化学实验:通过电解、电沉积等方法研究电化学反应的原理和规律。
6. 微妙分析实验:利用光谱、色谱等方法对物质进行微妙分析,掌握化学分析中的基本技术。
7. 表面化学实验:研究界面化学现象及其规律,如表面张力、界面吸附等。
8. 晶体学实验:研究晶体结构及其性质,如晶体衍射、晶体生长等。
9. 核磁共振实验:利用核磁共振技术研究物质的结构及其性质,如核磁共振谱、核磁共振成像等。
10. 激光光谱实验:利用激光技术研究分子结构及其振动、转动等动力学过程,如拉曼光谱、荧光光谱等。
- 1 -。
物理化学实验3篇

物理化学实验第一篇:酸碱滴定实验实验目的:1、熟练掌握酸碱滴定的基本原理和实验方法;2、掌握酸碱滴定的计算方法和常见误差的排除方法;3、了解常见酸、碱的性质和运用。
实验原理:酸碱滴定是一种定量分析方法,通常用于测定酸、碱溶液浓度,以及不同物质间的物化性质。
酸碱滴定的原理是在滴定过程中,酸碱指示剂的颜色会随着pH值的变化而改变,从而确定溶液的中和点。
滴定过程中,酸碱相互反应发生,将酸性溶液中的氢离子(H+)与碱性溶液中的氢氧根离子(OH-),发生反应生成水,使pH值由酸性过渡到中性和碱性。
滴定完成后,可以根据所添加的酸、碱的浓度计算出被滴定物质的浓度。
实验步骤:1、准备滴定仪器,将酸、碱分别倒入容量瓶中,用去离子水稀释至预定体积。
并加入相应指示剂。
2、将酸和碱的浓度预估值记录下来,至滴定过程中计算浓度提供参考。
3、用滴管逐滴加入稀硝酸至样品处于酸性,滴定时要轻轻旋转烧杯,预防液面波动。
4、倒入酸性溶液后,进行反应平衡,记录初值,开始滴定碱溶液直至出现终点颜色变化。
注意滴定时,滴液应缓慢、均匀、持续,并充分搅拌与反应。
5、记录终点滴数,计算浓度。
实验注意事项:1、滴定时要每滴排掉,每滴加入时需要旋转烧杯,充分反应。
2、不得用过氧化氢和KMnO4作为氧化剂,否则氧化反应过于剧烈,会产生更多误差。
3、选择合适指示剂,根据所测酸、碱的性质进行选择。
实验结果:本实验掌握了酸碱滴定的基本原理和实验方法,了解常见酸、碱的性质和运用。
在实验过程中,我们成功地测定了不同浓度的酸溶液和碱溶液的浓度,并应用所学知识计算和分析了实验结果,进一步深化了酸碱滴定理论和实践运用。
物理化学试验室试验内容
液体饱和蒸气压的测定
4
验证
该实验通过不断调节液体内部压力,测定该液体在不同压力下的沸点。根据
1
Clapeyon-Clausius方程,T和lg p做图可得一条直线,求直线的斜率,计算出被 测液体的摩尔蒸发热(△Hm)。
5
一级反应一蔗糖的转化
4
综合
本实验要配制10%的蔗糖溶液,取一定体积的蔗糖溶液加入浓度为4mol/L的盐 酸溶液,此时蔗糖开始水解,转化成葡萄糖和果糖。用旋光仪测定不同时间蔗糖 和盐溶液的比旋光度,利用Ig(at-a^)对时间t做图,计算蔗糖溶液的半衰期。
4
醋酸电离常数的测定
4
综合
学习醋酸溶液的配制,酸度计的使用和测定原理,醋酸电离常数的测定 原理和方法。
5
溶度积常数的测定
4
综合
溶度积常数的概念及意义,电导率法测定难溶电解质的溶度积常数的原 理和方法。
6
含铭工业废水的处理
4
综合
掌握利用化学还原法处理含铭工业废水的原理和方法,学习分光光度计 的使用。
7
11
HCl及NaOH标准溶液的配制及标 定
2
验证
学习HCl及NaOH标准溶液的配制方法、标定原理和准确浓度测定。
12
混合碱中各组分含量的测定
4
综合
学习HCl及NaOH标准溶液的配制与标定,掌握双指示剂法测定混合碱的 组成及含量的原理。
13
混合酸中各组分含量的测定
3
综合
掌握双指示剂滴定磷酸及盐酸的混合溶液中各组分的含量。
8
阿司匹林的合成
3
综合
由乙酸酐和水杨酸合成阿司匹林的原理及操作方法。
9
甲基橙的制备
《物理化学实验》课程实验教学大纲

《物理化学实验》课程实验教学大纲课程编号:31590070 学时:27 学分:一、课程的性质和任务《物理化学实验》是一门独立的课程。
是通过实验的手段,研究物质的物理化学性质以及这些物理化学性质与化学反应之间的关系。
物理化学实验课的主要目的是使学生掌握物理化学实验的基本方法和技能;培养学生正确记录实验数据和现象、正确处理实验数据和分析实验结果的能力;掌握有关物理化学的原理,提高学生灵活运用物理化学原理的能力。
通过实验,使学生初步了解物理化学的研究方法,包括实验现象的记录,实验条件的选择,重要物理化学性能的测量,实验数据的处理及可靠程度的判断,实验结果的分析和归纳、主要测试仪器的使用等,从而增强学生解决实际化学问题的能力。
通过物理化学实验的教学,还可以加深对物理化学和物质结构中某些重要的基本理论和概念的理解二、教学内容和方法1、实验前要充分预习,要求明确实验目的,熟悉实验原理,充分了解所用仪器设备的结构与使用方法2、实验过程中要认真仔细严格控制实验条件,仔细观察实验现象,仪器的使用操作要熟练,数据读取方法正确,确保实验数据及测量结果的准确度及精密度。
3、认真记录实验结果,写好实验报告。
真实记录数据,用正确的方法处理所得数据,图表清晰规范,结论合理,逐项写好实验报告中的内容。
物理化学实验课程与物理化学课程同步进行,教学对象为食品科学与工程专业的本科学生,学习时间为一个学期。
三、教学目的要求本课程由实验讲座和实验操作两个环节构成。
实验讲座的主要目的与要求如下:物理化学实验的目的要求,误差理论,数据处理和表达方法,实验预习方法和实验报告的书写方法,计算机辅助教学CAI课件的使用方法。
同时还包括实验室守则,实验室的安全防护,物理化学资料的查阅方法等。
实验操作内容见以下的各实验项目。
四、考试方式及方法平时考察与考试相结合,以独立成绩给予学分。
五、配套的实验教材或指导书物理化学第4版傅献彩高教社93-98物理化学实验复旦大学高教社93-98实验化学,刘约权李贵深高教社2000六、适用专业食品科学与工程(一)实验学时数:3(二)实验项目内容:讲授误差及产生原因与数据处理技术(三)实验室名称:化学中心实验室物理化学实验室实验二硫酸铜溶解热的测定(一)实验学时数:3(二)实验项目内容:1、量热法测定硫酸铜无限稀释摩尔溶解热2、雷诺校正法对搅拌等产生的热交换进行校正,求出由于溶解热而产生的温差(三)主要仪器设备及配套数溶解热测定装置12套(四)实验室名称:化学中心物理化学实验室实验三溶液表面张力的测定(一)实验学时数:3(二)实验项目内容:1、测定乙醇溶液的表面张力2、测定乙醇溶液的表面吸附量3、学会使用压力计(三)主要仪器设备及配套数表面张力测定仪12套(四)实验室名称:化学中心物理化学实验室实验四完全互溶双液系气液平衡相图(一)实验学时数:3(二)实验项目内容:1、沸点的测定2、液体折光率及组成的测定3、阿贝折光仪的使用方法(三)主要仪器设备及配套数:沸点仪、阿贝折光仪等各12套(四)实验室名称:化学中心物理化学实验室实验五液体饱和蒸汽压的测定(一)实验学时数:3(二)实验项目内容:1、测定环己烷不同温度时的饱和蒸汽压2、求算平均摩尔汽化焓及正常沸点3、学会使用压力计主要仪器设备及配套数(三)液体饱和蒸汽压测定装置12套(四)实验室名称:化学中心物理化学实验室实验六电导率法测定弱电解质的电离常数(一)实验学时数:3(二)实验项目内容:1、电导率仪的使用方法2、弱电解质的电离常数的电导法测定(三)主要仪器设备及配套数液体饱和蒸汽压测定装置12套(四)实验室名称:化学中心物理化学实验室实验七原电池电动势的测定(一)实验学时数:3(二)实验项目内容:1、电位差计的工作原理与使用方法2、原电池电动势的测定3、电动势法测定溶液的PH(三)主要仪器设备及配套数电位差计、原电池等各12套(四)实验室名称:化学中心物理化学实验室实验八一级反应动力学评价----蔗糖的转化(一)实验学时数:3(二)实验项目内容:1、用旋光仪测定蔗糖水解液的旋光度2、测定蔗糖水解的速率常数及半衰期(三)主要仪器设备及配套数旋光仪、容量瓶、旋光管等12套(四)实验室名称:化学中心物理化学实验室实验九溶液黏度的测定(一)实验学时数:3(二)实验项目内容:1、用奥氏黏度计测定溶液的黏度2、熟悉恒温槽的原理与控温技术(三)主要仪器设备及配套数奥氏黏度计、超级恒温槽等12套(五)实验室名称:化学中心物理化学实验室实验十物质磁化率的测定(一)实验学时数:3(二)实验项目内容:1、用“古埃法”测定磁化率2、熟悉磁天平的结构和使用技术(三)主要仪器设备及配套数磁天平4套(四)化学中心实验室物理化学实验室实验十一电化学综合测定(一)实验学时数: 3(二)实验项目内容:1、有关电化学性质的测定2、熟悉综合测定仪的结构及使用方法(三)主要仪器设备及配套数电化学综合测定2套(四)化学中心实验室物理化学实验室实验十二凝固点下降法物质摩尔质量的测定(一)实验学时数:3(二)实验项目内容:1、了解凝固点下降法物质摩尔质量的测定原理2、测定物质的摩尔质量(三)主要仪器设备及配套数物质摩尔质量的测定装置12套(四)化学中心实验室物理化学实验室。
物理化学实验技巧

物理化学实验技巧物理化学实验是化学专业中非常重要的一环,通过实验我们可以进一步理解和应用物理化学的原理与知识。
然而,实验过程中的技巧和方法对于实验结果的准确性和可重复性起着决定性的作用。
本文将介绍几个常用的物理化学实验技巧,帮助读者在实验中取得更好的结果。
一、安全操作技巧在进行物理化学实验前,安全始终是首要考虑的因素。
以下是几个安全操作技巧,帮助保证实验过程的安全性:1. 佩戴个人防护用具:实验室中应佩戴实验室规定的个人防护用具,如实验服、护目镜、手套等,以防止实验物质对身体的伤害。
2. 熟悉实验材料的特性:在进行实验前,充分了解实验材料的性质,包括毒性、易燃性等,以便采取相应预防措施。
3. 灵活使用通风设施:实验室应配备良好的通风设施,能够及时排除实验过程中产生的有害气体,确保实验环境的安全。
二、准确实验样品的制备技巧在物理化学实验中,制备准确的实验样品对于实验结果的准确性至关重要。
以下是一些常用的制备技巧:1. 称量准确:使用电子天平进行准确称量,避免因称量误差而导致实验结果的偏差。
2. 溶解技巧:对于固体试剂的溶解,应选择适当的溶剂,并注意溶解温度和溶剂的添加顺序,以便充分溶解。
3. 保存样品:制备好的实验样品应妥善保存,避免受潮和氧化,影响实验的进行。
三、精确实验仪器的使用技巧物理化学实验中使用的仪器对于实验结果的准确性和重复性十分关键。
以下是一些仪器使用的技巧:1. 仪器校准:在实验之前,务必对所使用的仪器进行校准,并确保其准确可靠。
2. 温度控制:对于需要精确温度控制的实验,应使用恒温器或水浴器等仪器,确保温度的稳定性。
3. 读取仪器的误差:在使用仪器时,要准确读取刻度,并考虑仪器的误差范围,以提高实验结果的准确性。
四、实验条件的控制技巧在物理化学实验中,实验条件的控制对于实验结果的可靠性和比较性起着重要作用。
以下是一些实验条件控制的技巧:1. 清洁实验器材:实验之前,应保证实验器材和容器的清洁度,防止杂质对实验结果产生不良影响。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
物理化学实验大三上学期实验一恒温槽1.实验原理:恒温槽之所以能维持恒温,主要是依靠恒温控制器来控制恒温槽的热平衡。
当恒温槽因对外散热而使水温降低时,恒温控制器就使恒温槽内的加热器工作,待加热到所需温度时,它又使加热器停止加热,保持恒定水温。
2.实验仪器:玻璃恒温水浴精密数字温度温差仪3.数据处理:恒温槽灵敏度te=±(t1-t2)/2(t1为最高温度,t2为最低温度),灵敏度曲线(温度-时间)4.课后题:⑴恒温槽主要由哪几个部分组成,各部分作用是什么?答:①浴槽:盛装介质②加热器:加热槽內物质③搅拌器:迅速传递热量,使槽内各部分温度均匀④温度计:观察槽内物质温度⑤感温元件:感应温度,指示加热器工作⑥温度控制器:温度降低时,指示加热器工作,温度升高时,只是加热器停止工作。
⑵对于提高恒温槽的灵敏度,可以哪些方面改进?答:①恒温槽的热容要大些,传热质的热容越大越好。
②尽可能加快电热器与接触温度计间传热的速度,为此要使感温元件的热容尽量小,感温元件与电热器间距离要近一些,搅拌器效率要高。
③做调节温度的加热器功率要小。
⑶如果所需恒定的温度低于室温如何装备恒温槽?答:通过辅助装置引入低温,如使用冰水混合物冰水浴,或者溶解吸热的盐类盐水浴冷却(硝铵,镁盐等)实验二燃烧焓1实验原理:将一定量的待测物质在氧弹中完全燃烧,燃烧时放出的热量使热量计本身及氧弹周围介质的温度升高,通过测定燃烧前后热量计温度的变化值,就可以算出该样品的燃烧热,其关系式为mQv=C△T-Q点火丝m点火丝。
2仪器与药品:氧弹热量计压片机精密数字温度温差仪萘苯甲酸3数据处理:雷诺温度校正曲线将燃烧前后历次观测到的水温记录下来,并作图,连成abcd线。
图中b点相当于开始燃烧之点,c点为观测到的最高温度点,由于热量计与外界的热量交换,曲线ab及cd常常发生倾斜。
取b点所对应的温度T1,c点所对应的温度T2,其平均温度(T1+T2)/2为T,经过T点作横坐标的平行线TO',与折线abcd相交于O'点,然后过O'点作垂直线AB,此线与ab线和cd线的延长线交于E,F两点,则E点和F点所表示的温度差即为欲求温度的升高值ΔT。
EE表示环境辐射进来的热量所造成热量计温度的升高,这部分必须扣除;而FF表示量热计向环境辐射出热量而造成热量计温度的降低,因此这部分必须加入。
经过这样校正后的温差表示由于样品燃烧使热量计温度升高的数值。
必须注意,应用这种作图法进行校正时,量热计的温度和外界环境温度不宜相差太大(最好不超过2~3℃),否则会引起误差。
△cHm=Qp=Qv+RT∑∨B(g)Qv=(C△T-Q点火丝m点火丝)/m误差R=|△cHm理论-△cHm实际|/△cHm理论4.课后题:⑴说明定容燃烧热和定压燃烧热的差别和相互关系答:定容燃烧热是在密闭刚性容器里发生的燃烧热,定压燃烧热则是在具有可移动壁里发生的燃烧热,壁内外压相等,所以燃烧前后其压强不变。
一般来说,燃烧时,会放热,产气,如果是在定容里,那压强就会升高,这会储存一部分能量,所以释放出来的热就比较少。
而定压则不会储存这部分能量,所以会把这部分能量以做体积功的形式释放出来,因此,量会比较大些。
⑵简述装置氧弹和拆开氧弹的操作过程答:装氧弹:拧开氧弹盖,将其内壁擦干净,特别是电极下端的不锈钢接柱更应擦干净。
接着小心的将压好的片状试样的点火丝两端分别紧绕在电极的下端,然后旋紧氧弹盖。
拆开氧弹:首先要把氧弹的出气口打开,放出余气,然后才慢慢旋开盖子。
⑶为什么实验测量得到的温度差值要经过作图法进行校正?答:量热计热量的散失无法避免,这可以是由于环境向量热计辐射进热量而使其温度升高,也可以是由于量热计向环境辐射了热量而使量热计的温度降低。
因此燃烧前后温度的改变值不能直接准确测量,而必须经过作图法进行校正。
因为环境向量热计辐射进热量而使量热计温度升高,这部分温度必须扣除;而量热计向环境辐射了热量而使量热计的温度降低,这部分温度必须加入。
经过校正后的温度差才表示由于样品燃烧使量热计温度升高的数值。
⑷使用氧气刚瓶和减压阀时有哪些注意事项。
答:氧气瓶是高压气体容器,使用时一定要注意安全。
首先要弄清楚怎么使用:连接好氧弹后,旋紧减压阀,使压力表上读数为15atm,充气3分钟,然后旋松减压阀,取下氧弹,关闭氧气刚瓶上端的阀门,操作完毕。
5.注释:实验成功的条件是什么?答:样品是否完全燃烧,燃烧放出的热量尽可能全部传递给量热计和水,几乎不与环境发生热交换。
实验三中和焓1实验原理:1mol一元强酸溶液和1mol一元强碱混合时,所产生的中和热不随酸或碱的种类而改变,因为各组全部电离H+OH=H2O △H中和=-57.36KJ·mol-1 若强碱中和弱酸时,首先是弱酸进行解离,然后进行中和反应:CH3COOH=H+CH3COO. △H 解离H+OH=H2O. △H中和总:CH3COOH+OH=H2O+CH3COO △H △H是弱酸与强碱中和反应总的热效应,它包括中和热和解离热两部分,由盖斯定律可求得△H解离=△H-△H中和2仪器与药品:SWC-ZH中和热(焓)测定装置3数据处理:热量计常数K:K=UIt/△T1=PT/△T1△rH中和=-1000K△T2/CV. △rHm=-1000K△T3/CV△rH解离=△rHm-△rH中和误差R=|△rH解离理论-△rH解离实际|/△rH解离理论4课后题:⑴本实验是用电热法标定热量计的热容C,能否改用其他方法?请设计出一个实验方案来。
答:实验前十分钟,用较小的功率搅拌蒸馏水后,再用远大于之前的功率搅拌蒸馏水,待温度升高0.8○C左右,再转为较小功率,作图得出△T,根据K=PT/△T 求出K值。
⑵试分析影响本实验结果的因素有哪些?答:系统保温效果要好,保温装置要干燥,电流电压值高低,即引入系统热量不要太高太低,同时升温速度不易太快,酸碱充分快速混合⑶中和焓除了与温度、压力有关外,还与浓度有关,如何测量无限稀释时的中和焓?答:在一定的温度下,测得不同浓度的中和热,再做温度与中和热的曲线,通过取极限的方式,测得无线稀释时的中和热。
实验四溶解焓1实验原理:盐类的溶解通常包含晶格的破坏和离子的溶剂化两个同时进行的过程。
前者为吸热过程,后者为放热过程。
溶解热则是两过程热效应的总和,因此,盐溶解过程是吸热还是放热,是由两过程热效应的相对大小所决定的。
溶解热的测定是在绝热式热量计中进行的,根据热量计中温度的变化,即可算出热效应。
最简单的热量计就是保温瓶(杜瓦瓶)。
2.仪器与药品:精密数字温度温差仪溶解热实验装置数字稳压电源3.数据处理:热量计常数K:K=UIt/△T=PT/△TKCL的摩尔溶解焓:△Hm,kcl=(mkcl Ckcl |△T|+K |△T|)Mkcl/mkcl4.课后题:⑴为什么要用雷诺曲线对△T进行校正,如何校正?答:因为热量的散失与增加是无法完全避免的,所以温度的变化值是不准确的,所以需要用雷诺曲线对△T进行校正。
将燃烧前后历次观测到的水温记录下来,并作图,连成abcd线。
图中b点相当于开始燃烧之点,c点为观测到的最高温度点,取b点所对应的温度T1,c点所对应的温度T2,其平均温度(T1+T2)/2为T,经过T点作横坐标的平行线TO',与折线abcd相交于O'点,然后过O'点作垂直线AB,此线与ab线和cd线的延长线交于E,F两点,则E点和F点所表示的温度差即为欲求温度的升高值ΔT。
⑵热量计热容C还可以用什么方法测定?答:用标准物质法测定。
用已知溶解热的盐如(KNO3)使其溶于定量水中,测得溶解前后温度的变化△T,△Hm已知,即可得出C值。
3.实验过程中加样速度应该如何控制,为什么?答:将称量纸卷成漏斗状,匀速而缓慢地倒入药品,使KCL能均匀的溶解,不致由于药品加入太快而使局部温度改变太快。
4.实验时的热量计的摇动速度应如何控制,为什么?答:用手顺时针匀速的摇动热量计,使热量计中的温度均匀传递,使金属探头检测到准确的温度。
5.实验中要尽可能研细药品,目的是什么?答:使药品容易溶解。
实验五甲基红的酸解离平衡常数的测定1实验原理:HMR(酸形式)=H+MR(碱形式)其离解平衡常数:K=[H][MR]/[HMR] PK=PH-㏒[MR]/[HMR]分光光度计法2.仪器与药品:分光光度计PH计标准甲基红溶液3.数据处理:AA=KA,HMR[HMR]L+KA,MR[MR]LAB=KB,HMR[HMR]L+KB,MR[MR]LPK=PH-㏒[MR]/[HMR]误差4.课后题:⑴本实验中,温度对测定结果有何影响?采取哪些措施可以减少因此引起的实验误差?答:温度对PH酸度计测定溶液PH的影响较大,将装有溶液的烧杯置于恒温水浴中。
⑵甲基红酸式吸收曲线的交点,称为“等色点”,讨论在等色点处吸收光和甲基红浓度的关系。
答:两吸收曲线交点时等浓度存在,左侧碱存在形式较多,右侧酸存在形式较多,吸光度和甲基红浓度符合朗伯定律。
⑶为什么要用相对浓度?为什么可以用相对浓度?答:由于HMR和MR两者在可见光谱范围内具有强的吸收峰,溶液离子浓度的变化对它的酸离解平衡常数没有显著的影响,而在简单的缓冲体系中就很容易使颜色在PH=4-6范围内改变,因此比值[MR]/[HMR]可用分光度法测定而求得。
⑷在吸光度测定中,应该怎样选用比色皿?答:选择不同长度的比色皿应视分析样品的吸光度而定,当比色液的颜色较淡时,应选用光程长度较大的比色皿,当比色液的颜色较深时,应选用光程长度较小的比色皿,本实验采用1cm较小的比色皿。
实验六凝固点降低1实验原理:当指定了溶剂的种类和数量后,凝固点降低值取决于所含溶质的数目,即溶剂的凝固点降△低值与溶液的浓度成正比,则△T=To-T=Kf·m(To溶剂凝固点,T溶液凝固点)则MB=Kf·mB/△TfmA2仪器与药品:SWC-LG凝固点实验装置SWC-ⅡD精密数字温度温差仪环己烷萘3.数据处理:△Tf=Tf*-Tf=Kf·bBbB=mB/MB/mAMB=Kf·mB/△TfmA4.课后题:⑴凝固点降低法测定溶质分子摩尔质量的公式在什么条件下才能适用?答:稀溶液中且溶质在溶液中不发生解离和缔合等的情况下才能适用。
⑵什么原因可能造成过冷太甚?若过冷太甚,所测溶液凝固点偏低还是偏高?由此所得的摩尔质量偏低还是偏高?答:溶剂温度过低会造成过冷太甚。
使凝固点偏低,从而使摩尔质量偏低。
⑶在冷却过程中,冷冻管内固、液相之间和冷剂之间有哪些热交换?它们对凝固点的测定有何影响?答:热交换有:冷冻管中液相放出热量而转化为固相,冷剂从冷冻管周围吸收热量。
当析出固相后,温度不回升到平衡温度,不能保持一恒定值,因部分溶剂凝固后,剩余的浓度逐渐增大,平衡温度要逐渐下降,如果溶液的过冷程度不大,可以将温度回升到最高值作为凝固点,若过冷太甚,凝固的溶剂过多,溶液的浓度变化过大,使得凝固点偏低。
