附表1药品不良反应事件报告表
药品不良反应报告表(范例)

药品不良反应/ 事件报告表
首次报告□跟踪报告□编码:
报告类型:新的□严重■一般□报告单位类别:医疗机构□经营企业□生产企业□个人□其他□
13
严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:
1)导致死亡;
2)危及生命;
3)致癌、致畸、致出生缺陷;
4)导致显著的或者永久的人体伤残或者器官功能的损伤;
5)导致住院或者住院时间延长;
6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
新的药品不良反应:是指药品说明书中未载明的不良反应.说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
报告时限
新的、严重的药品不良反应应于发现或者获知之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应30日内报告。
有随访信息的,应当及时报告.
其他说明
怀疑药品:是指患者使用的怀疑与不良反应发生有关的药品。
并用药品:指发生此药品不良反应时患者除怀疑药品外的其他用药情况,包括患者自行购买的药品或中草药等。
用法用量:包括每次用药剂量、给药途径、每日给药次数,例如,5mg,口服,每日2次。
报告的处理
所有的报告将会录入数据库,专业人员会分析药品和不良反应/事件之间的关系.根据药品风险的普遍性或者严重程度,决定是否需要采取相关措施,如在药品说明书中加入警示信息,更新药品如何安全使用的信息等.在极少数情况下,当认为药品的风险大于效益时,药品也会撤市。
14。
药品不良反应事件报告表(附表1)
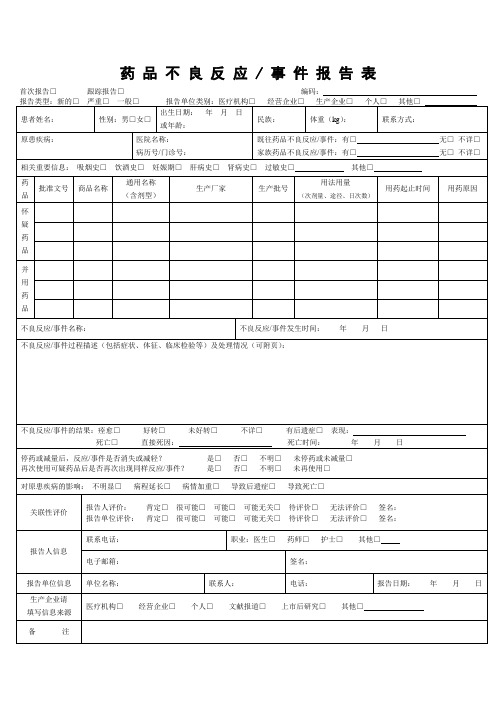
药品不良反应 / 事件报告表首次报告□跟踪报告□编码:
填写说明:
严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:
1) 导致死亡;
2)危及生命;
3)致癌、致畸、致出生缺陷;
4)导致显著的或者永久的人体伤残或者器官功能的损伤;
5)导致住院或者住院时间延长;
6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
新的药品不良反应:是指药品说明书中未载明的不良反应。
说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
报告时限
新的、严重的药品不良反应应于发现或者获知之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应30日内报告。
有随访信息的,应当及时报告。
其他说明
怀疑药品:是指患者使用的怀疑与不良反应发生有关的药品。
并用药品:指发生此药品不良反应时患者除怀疑药品外的其他用药情况,包括患者自行购买的药品或中草药等。
用法用量:包括每次用药剂量、给药途径、每日给药次数,例如,5mg,口服,每日2次。
报告的处理
所有的报告将会录入数据库,专业人员会分析药品和不良反应/事件之间的关系。
根据药品风险的普遍性或者严重程度,决定是否需要采取相关措施,如在药品说明书中加入警示信息,更新药品如何安全使用的信息等。
在极少数情况下,当认为药品的风险大于效益时,药品也会撤市。
药品不良反应和医疗器械不良事件报告登记表

附表1
药品不良反应 / 事件报告表
首次报告□跟踪报告□编码:
报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人□其他□
严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:
1) 导致死亡;
2)危及生命;
3)致癌、致畸、致出生缺陷;
4)导致显著的或者永久的人体伤残或者器官功能的损伤;
5)导致住院或者住院时间延长;
6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
新的药品不良反应:是指药品说明书中未载明的不良反应。
说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
报告时限
新的、严重的药品不良反应应于发现或者获知之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应30日内报告。
有随访信息的,应当及时报告。
其他说明
怀疑药品:是指患者使用的怀疑与不良反应发生有关的药品。
并用药品:指发生此药品不良反应时患者除怀疑药品外的其他用药情况,包括患者自行购买的药品或中草药等。
用法用量:包括每次用药剂量、给药途径、每日给药次数,例如,5mg,口服,每日2次。
报告的处理
所有的报告将会录入数据库,专业人员会分析药品和不良反应/事件之间的关系。
根据药品风险的普遍性或者严重程度,决定是否需要采取相关措施,如在药品说明书中加入警示信息,更新药品如何安全使用的信息等。
在极少数情况下,当认为药品的风险大于效益时,药品也会撤市。
精品
欢迎您的下载,资料仅供参考。
药品不良反应事件报告表

药品不良反应/事件报告表新的严重的一般单位类型:医疗卫生机构单位名称: 部门: 电话: 报告日期:患者姓名: *** 性别: 出生日期: 民族: 体重(kg): 联系方式: ************家族药品不良反应: 有无不详既往药品不良反应情况: 有无不详不良反应/事件名称:食欲不振、恶心、呕吐不良反应发生时间: ****年**月*日医院名称: 病历号/门诊号:不良反应过程描述(包括症状、体征、临床检验等)及处理情况:患者第一天服用该药时稍有不适但能耐受,并无其他反应,等第三天早上食欲不振、恶心呕吐等症状更加明显且不能耐受,体征:血压130/85mmHg,心率:75次/分都正常,嘱托患者停药,随后两天访视一切良好,建议患者服用其他降糖口服药。
怀疑药品商品名称通用名称(含剂型,上市五年内品种用*注明)用药原因用法用量用药起止时间生产厂家批号*** 盐酸二甲双胍***剂型: *** 2型糖尿病用量:次日3次/日用法: 250mg/次从****年*月**日到****年*月**日**************** **********并用药品商品名称通用名称(含剂型,上市五年用药原因用法用量用药起止时间生产厂家批号内品种用*注明)剂型:用量:用法:从到不良反应的结果: 治愈好转有后遗症死亡原患疾病:对原患疾病的影响: 不明显病程延长病情加重导致后遗症导致死亡国内有无类似不良反应(包括文献报道): 有无不详国外有无类似不良反应(包括文献报道): 有无不详关联性评价报告人: 肯定很可能可能可能无关待评价无法评价签名:报告单位: 肯定很可能可能可能无关待评价无法评价签名:不良反应分析1. 用药与不良反应的出现有无合理的时间关系?是否2. 反应是否符合该药已知的不良反应类型?是否不明3. 停药或减量后,反应是否消失或减轻?是否不明未停药或未减量是否不明未再使用是否不明报告人职业: 执业药师报告人职务/职称: 职员报告人签名:。
药品不良反应事件报告表-制表单位国家食品药品监督管理局

附表 1 制表单位�国家食品药品监督管理局药品不良反应/ 事件报告表新的√□ 严重□一般□单位名称�医疗卫生机构□ 生产企业经营企业□ 个人□编码□□□□□□□□□□□□□□□□□□□部门�电话�报告日期2014联系方式年6 月10 日患者姓名:杨红性别�男□女√出生日期1968 年4 月18 日民族汉体重62(kg)家族药品不良反应/事件�有□无√□不详□既往药品不良反应/事件情况�有□ 无□√不详□不良反应/事件不良反应/事件发生时间�年病历号/门诊号�企业填写医院名称�名称�月日不良反应/事件过程描述�包括症状、体征、临床检验等�及处理情况�通用名称�含剂型�监商品名称* 生产厂家批号用法用量用药起止时间用药原因测期内品种用注明�怀疑药品并用药品不良反应/事件的结果�治愈□原患疾病�好转□有后遗症□ 表现�病情加重□死亡□ 直接死因�死亡时间�年月日对原患疾病的影响�不明显□病程延长□导致后遗症□表现�导致死亡□国内有无类似不良反应�包括文献报道��有□无□不详□国外有无类似不良反应�包括文献报道��有□ 无□ 不详□报告人�肯定□很可能□很可能□很可能□很可能□可能□可能无关□可能无关□可能无关□可能无关□待评价□待评价□待评价□待评价□无法评价□无法评价□无法评价□无法评价□签名�签名�报告单位�肯定□可能□关联性评价省级药品不良反应监测机构�国家药品不良反应监测中心�肯定□可能□签名�肯定□可能□签名�报告人职业�医疗机构��医生□药师□护士□其他□报告人职务职称�企业��报告人签名�◇不良反应/事件分析1. 用药与不良反应/事件的出现有无合理的时间关系�2. 反应是否符合该药已知的不良反应类型� 有□ 无□是□ 否□不明□3. 停药或减量后�反应/事件是否消失或减轻�4. 再次使用可疑药品后是否再次出现同样反应/事件�是□否□ 不明□ 未停药或未减量□ 是□ 否□ 不明□未再使用□5. 反应/事件是否可用并用药的作用、患者病情的进展、其他治疗的影响来解释�是□ 否□ 不明□◇严重药品不良反应/事件是指有下列情形之一者� ① 引起死亡□ □ □ □ □② 致畸、致癌或出生缺陷③ 对生命有危险并能够导致人体永久的或显著的伤残 ④ 对器官功能产生永久损伤 ⑤ 导致住院或住院时间延长◇编码规则�省(自治区、直辖市) 市�地区� 县�区� 单位 年代 流水号 □□□□□□□□□□□□□□□□□□□注�省�自治区、直辖市�、市�地区�、县�区�编码按中华人民共和国行政区划代码填写。
药品不良反应登记表格模板

关联性评价
报告人:肯定□很可能□可能□可能有关□待评价□无法评价□签名:
报告单位:肯定□很可能□可能□可能有关□待评价□无法评价□签名:
省级药品不良反应监测机构:肯定□很可能□可能□可能有关□待评价□无法评价□签名:
药品不良反应/事件报告表
新的□严重□一般□医疗卫生机构□生产企业□经营企业□个人□编码
单位名称:部门:电话:报告日期:年月日
患者姓名:
性别:
男□女□
出生日期:
年月日
民族:
体重(㎏)
联系方式:
家庭药品不良反应/事件:有□无□不详□
既往药品不良反应/事件情况:有□无□不详□
不良反应/事件
名称:
不良反应/事件发生时间:
国家药品不良反应监测机构:肯定□很可能□可能□可能有关□待评价□无法评价□签名:
报告人职业(医疗机构):医生□药师□护士□报告人职务职称(企业):报告人签名:
病历号/门诊号
不良反应/事件过程描述(包括症状、体征、临床检验等)及处理情况:
商品名称
通用名称(含剂型,监用药起
止时间
用药原因
怀疑
药品
并用
药品
不良反应/事件的结果:治愈□好转□有后遗症□表现:死亡□直接死因:死亡时间:年月日
原患疾病:
对原患疾病的影响:不明显□病程延长□病情加重□导致后遗症□表现:
药品不良反应事件报告表完整版

报告人职业(医疗机构)
注:严重药品不良反应/事件是指有下列情形之一者:
导致死亡;危及生命;致癌、致畸、致出生缺陷;导致显著的或者永久的人体伤残或者器官功能的损伤;
导致住院或者住院时间延长;
导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
赤峰市药品不良反应监测中心
药品不良反应/事件报告表2012年度
首次报告□跟踪报告□
编号
报告类型
新的□严重□一般□
报告单位类别
医疗卫生机构□生产企业经营企业□个人□
医院名称
病历号/门诊号
联系地址
联系电话
邮编
患者姓名
性别
男□女□
年龄
民族
体重(kg)
联系Байду номын сангаас话
原患疾病
家族药品不良反应/事件
有□无□不详□
既往药品不良反应/事件情况
有□无□不详□
相关重要信息
吸烟史□饮酒史□妊娠期□肝病史□肾病史□过敏史□其他□
药
品
批准文号
商品名称
通用名称
(含剂型)
生产厂家
批号
用法用量
(次剂量、途径、日次数)
用药
起止时间
用药原因
怀
疑
药
品
并
用
药
品
不良反应/事件名称
不良反应/事件发生时间
不良反应/事件过程描述(包括症状、体征、临床检验等)及处理情况(可附页)
填写说明附后
不良反应/事件的结果
治愈□好转□未好转□不详□有后遗症□
表现
死亡□
直接死因
死亡时间
不良反应/事件分析
停药或减量后,反应/事件是否消失或减轻?
药品不良反应报告表(国家)

药品不良反应报告(bàogào)表(国家)制表单位:国家(guójiā)食品药品监督管理局药品不良反应 / 事件报告表新的□严重(yánzhòng)□一般(yībān)□医疗卫生机构(jīgòu)□生产(shēngchǎn)企业经营企业□个人□编码□□□□□□□□□□□□□□□□□□□单位名称:部门:电话:报告日期:年月日◇不良反应/事件(shìjiàn)分析1.用药与不良反应/事件的出现有无合理的时间关系?有□无□2.反应是否符合该药已知的不良反应类型?是□否□不明□3.停药或减量后,反应/事件是否消失或减轻?是□否□不明□未停药或未减量□4.再次使用可疑药品后是否再次出现同样反应/事件?是□否□不明□未再使用□5.反应/事件是否可用并用药的作用、患者病情的进展、其他治疗的影响来解释?是□否□不明□◇严重药品不良反应/事件是指有下列(xiàliè)情形之一者:①引起(yǐnqǐ)死亡□②致畸、致癌或出生(chūshēng)缺陷□③对生命有危险并能够导致人体永久(yǒngjiǔ)的或显著的伤残□④对器官功能产生永久损伤□⑤导致住院或住院时间延长□◇编码规则:省(自治区、直辖市)市(地区)县(区)单位年代流水号□□□□□□□□□□□□□□□□□□□注:省(自治区、直辖市)、市(地区)、县(区)编码按中华人民共和国行政区划代码填写。
单位编码第一位如下填写:医疗机构1、军队医院2、计生机构3、生产企业4、经营企业5。
个人报告单位编码一栏填写6000◇注:通用名称一栏,首次获准进口5年内的进口品种用*注明国家药品不良反应监测中心药品不良反应监测中心通信地址:北京市崇文区法华南(Huánán)里11号楼二层通信地址:邮编:100061邮编:电话:(010)67164979电话:传真:(010)67184951传真:E – mail :report@ E – mail:新的、严重的药品(yàopǐn)不良反应/事件病例报告要求药品生产企业报告(bàogào)要求1.填报(tiánbào)《药品不良反应/事件报告表》;2.产品(chǎnpǐn)质量检验报告;3.药品(yàopǐn)说明书(进口药品还须报送国外药品说明书);4.产品注册、再注册时间,是否在监测期内(进口药是否为首次获准进口5年内);5.产品状态(是否是国家基本药物、国家非处方药、国家医疗保险药品、中药保护品种);6.国内上年度的销售量和销售范围;7.境外使用情况(包括注册国家、注册时间);8.变更情况(药品成分或处方、质量标准、生产工艺、说明书变更情况);9.国内外临床安全性研究及有关文献报道情况;10.除第1、2项以外,其他项目一年之内如无变更,可以免报。
药品不良反应事件报告表

报告基本信息
首次/跟踪报告: 报告类型: □首次报告 □新的 □跟踪报告 □严重 编码: 报告单位类别: 医疗机构
Байду номын сангаас□一般
患者基本信息
患者姓名: 原患疾病: 家族药品不良反应/事件: □不详 既往药品不良反应/事件: □不详 相关重要信息: □吸烟史 □无 □无 □有 □有 □妊娠期 □肝病史 □肾病史 □过敏史 □其他 性别: 民族: 出生年月: 医院名称: 年龄: 体重: 联系方式:
报告单位信息: 单位名称:
报告人评价: 关联性评价: 报告单位评价: □肯定 报告人信息: 联系电话: □很可能 □可能 □可能无关 □待评价 □无法评价 报告单位签名: 报告人签名: 报告日期: □肯定 □很可能 □可能 □可能无关 □待评价 □无法评价 报告人签名:
职业:□医生 □药师 □护士 □其他 联系人: 联系电话:
不良反应/事件结果:
□痊愈
□好转
□未好转 □是
□不详 □否 □否
□有后遗症 □不明 □不明
□死亡
停药或减量后反应/事件是否消失或减轻:
□未停药或未减量 □未再使用 □导致死亡
再次使用可疑药品后是否再次出现同样反应/事件: □是 对原患疾病的影响: □不明显 □病情延长
□病情加重
□导致后遗症
报告人信息
病历号/门诊号:
□饮酒史
怀疑用药
批准文号 商品名称 通用名称 生产厂家 生产批号 用法用量 给药途径 用药起止时间 用药原因
并用药品
批准文号 商品名称 通用名称 生产厂家 生产批号 用法用量 给药途径 用药起止时间 用药原因
不良反应/事件详细信息
不良反应/事件名称: 不良反应/事件发生时间:
药店药品不良反应上报模板 (1)
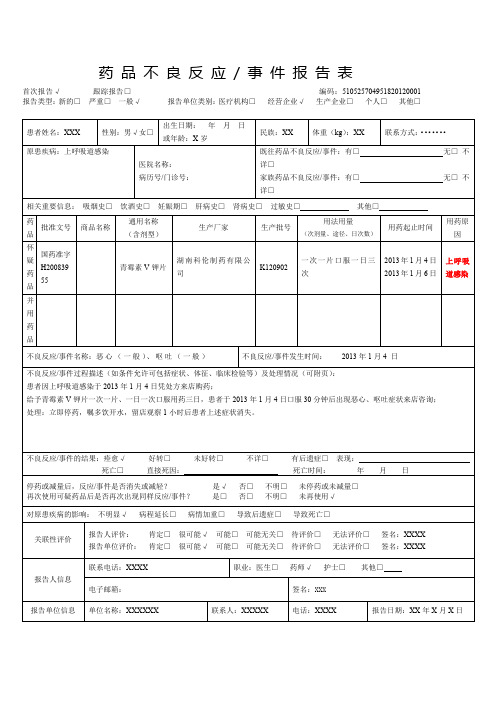
对原患疾病的影响:不明显√病程延长□病情加重□导致后遗症□导致死亡□
关联性评价
报告人评价: 肯定□很可能√可能□可能无关□待评价□无法评价□签名:XXXX
报告单位评价: 肯定□很可能√可能□可能无关□待评价□无法评价□签名:XXXX
给予青霉素V钾片一次一片、一日一次口服用药三日,患者于2013年1月4日口服30分钟后出现恶心、呕吐症状来店咨询;
处理:立即停药,嘱多饮开水,留店观察1小时后患者上述症状消失。
不良反应/事件的结果:痊愈√好转□未好转□不详□有后遗症□表现:
死亡□直接死因:死亡时间:年月日
停药或减量后,反应/事件是否消失或减轻?是√否□不明□未停药或未减量□
医院名称:
病历号/门诊号:
既往药品不良反应/事件:有□无□不详□
家族药品不良反 应/事件:有□无□不详□
相关重要信息:吸烟史□饮酒史□妊娠期□肝病史□肾病史□过敏史□其他□
药品
批准文号
商品名称
通用名称
(含剂型)
生产厂家
生产批号
用法用量
(次剂量、途径、日次数)
用药起止时间
用药原因
怀疑药品
国药准字H20083955
报告人信息
联系电话:XXXX
职业:医生□药师√护士□其他□
电子邮箱:
签名:XXX
报告单位信息
单位名称:XXXXXX
联系人:XXXXX
电话:XXXX
报告日期:XX年X月X日
青霉素V钾片
湖南科伦制药有限公司
K120902
一次一片口服一日三次
2013年1月4日
2013年1月6日
药品不良反应报告表范例 .doc

药品不良反应报告表范例 .doc
药品不良反应记录
日期:xxxx年xx月xx日
药品名称:xxxx
制剂规格:xxxx
生产企业:xxxx
患者信息:
姓名:xxx
性别:xxx
年龄:xxx
病情/疾病诊断:xxx
不良反应记录:
1.反应名称:xxxx
发生时间:xxxx年xx月xx日xx时xx分
反应描述:患者出现了xxxx的症状,包括xxxx。
症状持续时间约为xx小时/天。
患者对此感到不适,并报告给医生。
处理措施:对患者的症状进行了观察,同时给予了xxxx的治疗。
结果:患者在接受治疗后,症状逐渐缓解,并在xx天后完全消失。
2.反应名称:xxxx
发生时间:xxxx年xx月xx日xx时xx分
反应描述:患者出现了xxxx的症状,包括xxxx。
症状持续时间约为xx小时/天。
患者对此感到不适,并报告给医生。
处理措施:对患者的症状进行了观察,同时给予了xxxx的治疗。
结果:患者在接受治疗后,症状逐渐缓解,并在xx天后完全消失。
备注:
1.患者的不良反应于xx年xx月xx日报告给医生,并得到及时处理。
2.对患者的不良反应进行了详细的记录,包括症状的描述、发生时间、处理措施和疗效结果。
3.患者在接受治疗后的症状得到缓解,并无其他严重不良反应发生。
以上是患者使用该药品期间出现的不良反应的详细记录。
如有进一步需要,请及时与我联系。
医师签名:xxxx
日期:xxxx年xx月xx日。
药品不良反应报告表(模板)

药品不良反应/ 事件报告表
严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:
1) 导致死亡;
2)危及生命;
3)致癌、致畸、致出生缺陷;
4)导致显着的或者永久的人体伤残或者器官功能的损伤;
5)导致住院或者住院时间延长;
6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
新的药品不良反应:是指药品说明书中未载明的不良反应。
说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
报告时限
新的、严重的药品不良反应应于发现或者获知之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应30日内报告。
有随访信息的,应当及时报告。
其他说明
怀疑药品:是指患者使用的怀疑与不良反应发生有关的药品。
并用药品:指发生此药品不良反应时患者除怀疑药品外的其他用药情况,包括患者自行购买的药品或中草药等。
用法用量:包括每次用药剂量、给药途径、每日给药次数,例如,5mg,口服,每日2次。
报告的处理
所有的报告将会录入数据库,专业人员会分析药品和不良反应/事件之间的关系。
根据药品风险的普遍性或者严重程度,决定是否需要采取相关措施,如在药品说明书中加入警示信息,更新药品如何安全使用的信息等。
在极少数情况下,当认为药品的风险大于效益时,药品也会撤市。
药品不良反应事件报告表

昌宁县人民医院药品不良反应/事件报告表新的□严重□一般□医疗卫生机构编码5305241单位名称:昌宁县人民医院科室:电话:报告日期:年月日报告人职业(医疗机构):医生□药师□护士□其他□报告人职务职称:报告人签名:科主任审核签名:药品不良反应事件报告表填报要求一、法规要求1.《药品管理法》第七十一条明确规定,“我国实行药品不良反应报告制度”;2.《药品不良反应报告和检测管理办法》中第二、四、十三等条款中对医疗机构的职责做了具体的规定。
强调报告药品不良反应是义务人员应尽的法律义务。
二、报告数量要求:1.百万人口报告数为:不低于170/百万人口;2.住院总人数的5-10%(据统计有5-10%的人员因药品不良反应而住院,住院病人住院治疗期间10-20%的病人发生药品不良反应)。
三、质量要求:1.报表完整不缺项;2.报表真实不虚报;3.钢笔填写;4.时限要求:○1群体不良反应立即填报(3天内),○2新的或严重的不良反应3天内上报,○3一般病例发现之日起一个月内填报;5.不良反应/事件名称:填写使用药品导致的不良反应(例:变态反应,过敏性休克);6.怀疑药品:需填写全名称;7.原患疾病:填写使用该药品的疾病诊断名称;8.不良反应过程描述及处理情况一栏应包括:○1患者基本情况○2就诊主诉○3常规检查(T、BP、P、R等)○4初步诊断○5使用药品情况○6出现药品不良反应时间及反应情况○7处理情况○8转归或结果;9.国内外有无不良反应报道,以说明书(或其他医学期刊记录为准);10.关联性评价:一般不填可能无关一栏;11.不良反应分析:用药与不良反应的出现有无合理的时间关系,应勾“是”。
四、填报要求1.表格填写完整后应有报告人签名,科主任审核后签名,报药剂科审核后网络报告,医务科负责报告情况收集和完成情况督查;2.每位医生每年至少报告一份。
药品不良反应报告表填写范

报告类型:新的严重一般部门:电话:报告日期:年月日
患者姓名
性别:男女
年龄:
民族
联系方式:
体重(kg)
病历号
家族药品不良反应/事件:有无不详
既往药品不良反应/事件情况:有无不详
不良反应/事件名称:
不良反应/事件发生时间:月日
不良反应/事件过程描述(包括症状、体征、临床检验等)及处理情况(可附页):
不良反应/事件的结果:治愈好转未好转不详有后遗症表现:
死亡直接死因:死亡时间:年 月 日
1.停药或减量后,反应/事件是否消失或减轻?是否不明未停药或未减量
2.再次使用可疑药品后是否再次出现同样反应/事件?是否不明未再使用
商品名称
通用名称(含剂型,监测期内品种用*注明)
生产厂家
批号
用法用量
用药起止时间
报告日期: 年 月 日
是否已报告给生产企业使用单位经营或进口单位
备注
若有疑问,请致电:临床药学63157964
用药原因
怀
疑
药
品
合并用药
关联性评价
报告人:肯定□很可能□可能□可能无关□待评价□无法评价□签名:
报告单位:肯定□很可能□可能□可能无关□待评价□无法评价□签名:
报告人信息
姓名:
联系方式:
职业:医生药师护士其他
签名:
电子邮件:
如果不想您的个人信息共享给生产企业,请打√□
报告单位信息
单位名称:
联系人:
电话:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
附表1
药品不良反应/ 事件报告表
首次报告□跟踪报告□编码:
报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人□其他□
严重药品不良反应,是指因使用药品引起以下损害情形之一的反应:
1) 导致死亡;
2)危及生命;
3)致癌、致畸、致出生缺陷;
4)导致显著的或者永久的人体伤残或者器官功能的损伤;
5)导致住院或者住院时间延长;
6)导致其他重要医学事件,如不进行治疗可能出现上述所列情况的。
新的药品不良反应:是指药品说明书中未载明的不良反应。
说明书中已有描述,但不良反应发生的性质、程度、后果或者频率与说明书描述不一致或者更严重的,按照新的药品不良反应处理。
报告时限
新的、严重的药品不良反应应于发现或者获知之日起15日内报告,其中死亡病例须立即报告,其他药品不良反应30日内报告。
有随访信息的,应当及时报告。
其他说明
怀疑药品:是指患者使用的怀疑与不良反应发生有关的药品。
并用药品:指发生此药品不良反应时患者除怀疑药品外的其他用药情况,包括患者自行购买的药品或中草药等。
用法用量:包括每次用药剂量、给药途径、每日给药次数,例如,5mg,口服,每日2次。
报告的处理
所有的报告将会录入数据库,专业人员会分析药品和不良反应/事件之间的关系。
根据药品风险的普遍性或者严重程度,决定是否需要采取相关措施,如在药品说明书中加入警示信息,更新药品如何安全使用的信息等。
在极少数情况下,当认为药品的风险大于效益时,药品也会撤市。
