化学图形符号库
化学名称及符号

水银汞H g白金铂 Pt硫磺硫S金刚石、石墨、木炭碳C白磷、红磷、黄磷磷 P盐酸、盐镪水氢氯酸HCl硝镪水硝酸 HNO3硫镪水硫酸 H2SO4王水浓硝酸、浓盐酸(1:3)HNO3,HCl双氧水过氧化氢 H2O2铅丹、红丹、红铅四氧化三铅 Pb3O4砒霜、信石、白砒、砷华三氧化二砷 As2O3升汞、高汞氯化汞 Hg Cl2朱砂、辰砂、丹砂、银朱硫化汞HgS烧碱、火碱、苛性钠氢氧化钠N aOH苛性钾氢氧化钾 KO H消石灰、熟石灰氢氧化钙Ca(OH)2碱石灰、钠碱石灰氢氧化钠、氧化钙混合 Na OH,Ca O 碳铵碳酸氢铵NH4HC O3盐脑、电气药粉氯化铵NH4Cl硫铵硫酸铵 (N H4)2S O4碳酸气、干冰二氧化碳CO2笑气氧化二氮 N2O硅石、石英、水晶、玛瑙砂子二氧化硅 SiO2矾土、刚玉氧化铝 Al2O3生石灰、煅烧石灰氧化钙CaO锌白、锌氧粉氧化锌ZnO苫土、烧苫土氧化镁MgO苏打、纯碱碳酸铵N a2SO4小苏打、重碱碳酸氢钠 Na HCO3大苏打、海波硫代硫酸钠 Na2S2O3.5H2O褐铁矿2Fe2O3.3H2O芒硝、皮硝、马牙硝结晶硫酸钠 Na2SO4.10H2O泻盐、苦盐硫酸镁 MgSO4.7H2O口碱结晶碳酸钠 NaCO3.10H2O明矾硫酸铝钾 KAl(SO4)2.12H2O皓矾硫酸锌Z nSO4.7H2O胆矾硫酸铜 CuS O4.5H2O红矾重铬酸钾 K2Cr2O7无水芒硝、元明粉硫酸钠 Na2SO4水玻璃、泡花碱硅酸钠 NaSi O3硫化碱、臭碱硫化钠N a2S钾碱、草碱、草木灰碳酸钾 K2CO3硝石、火硝、土硝硝酸钾 KNO3灰锰氧、PP粉高锰酸钾KMnO4冰晶石氟铝酸钠Na3Al F6大理石、方解石、石灰石白垩碳酸钙 CaC O3萤石、氟石氟化钙 Ca F2钙硝石、挪威硝石硝酸钙 Ca(N O3)2电石碳化钙 CaC2铜绿、孔雀石碱式碳酸铜CU2(O H)2CO3重晶石、钡白硫酸钡 Ba SO4钠硝石、智利硝石硝酸钠 NaN O3生石膏、石膏硫酸钙C aSO4.2H2O熟石膏、烧石膏硫酸钙 2Ca SO4.H2O普钙、过磷酸钙磷酸二氢钙、硫酸钙 Ca(H2PO4)2,CaS O4 重钙磷酸二氢钙 Ca(H2PO4)2漂白粉次氯酸钙 Ca(ClO)2氯仿、绿仿三氯甲烷 CHC l3木精甲醇C H3OH甘油丙三醇 C2H5(OH)3石炭酸苯酚C6H5OH蚁酸甲酸 HCO OH草酸乙二酸HOOC-COOH福尔马林甲醛溶液(30%~40%) H CHO尿素碳酰胺 CO(N H2)安息香酸苯甲酸 C6H5COO H赤铜矿氧化亚铜 Cu2O软锰矿二氧化锰MnO2菱铁矿碳酸亚铁F eCO3辉铜矿硫化亚铜C u2S愚人金硫化亚铁 Fe S2铁丹、铁红、赭石、赤铁矿三氧化二铁 Fe2O3磁铁矿、铁黑四氧化三铁 Fe3O4绿矾七水合硫酸亚铁 Fe SO4.7H2O保险粉连二亚硫酸钠Na2S2O4醋酸乙酸C H3COO H常见物质颜色汇总1.红色 Fe(SCN)]2+ (血红色); Cu2O(砖红色); Fe2O3(红棕色); 红磷(红棕色); 液溴(深红棕色); F e(OH)3 (红褐色); I2的CC l4溶液(紫红色); Mn O4-(紫红色);Cu(紫红色); 在空气中久置的苯酚(粉红色).2.橙色: 溴水; K2Cr2O7溶液.3.黄色: Ag I(黄色); Ag Br(浅黄色); K2CrO4(黄色); Na2O2(淡黄色); S(黄色); F eS2(黄色); 久置浓HN O3(溶有NO2);工业浓盐酸(含F e3+); Fe3+水溶液(黄色);久置的K I溶液(被氧化成I2)4.绿色:Cu2(O H)2CO3; F e2+的水溶液; F eSO4.7H2O; Cl2(黄绿色); F2(淡黄绿色); C r2O35.蓝色: Cu(OH)2; Cu SO4.5H2O;Cu2+的水溶液; I2与淀粉的混合物.6.紫色:KMnO4(紫黑色); I2(紫黑色); 石蕊(pH=8--10); Fe3+与苯酚的混合物.7.黑色: F eO, Fe3O4, Fe S, C uS, Cu2S, Ag2S, P bS, CuO, MnO2, C粉.8.白色:Fe(OH)2, AgOH,无水C uSO4, Na2O, Na2CO3, NaHCO3, A gCl, BaSO4, Ca CO3, CaSO3 ,Mg(OH)2, Al(OH)3, 三溴苯酚, M gO, MgCO3, 绝大部分金属等.说明:①元素基本上按周期表的族序数排列;②物质基本上按单质、氢化物、氧化物及其水化物、盐、有机物的顺序排列;③许多物质晶状为无色,粉末状为白色,晶型不同可能有不同颜色;④硫化物和过渡元素化合物颜色较丰富。
化学符号大全

、物质的学名、俗名及化学式⑴金刚石、石墨:C⑵水银、汞:Hg(3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2(5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3(7)氢硫酸:H2S(8)熟石灰、消石灰:Ca(OH)2(9)苛性钠、火碱、烧碱:NaOH(10)纯碱:Na2CO3碳酸钠晶体、纯碱晶体:Na2CO3•10H2O(11)碳酸氢钠、酸式碳酸钠:NaHCO3(也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4•5H2O(13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH有毒、失明、死亡(15)酒精、乙醇:C2H5OH(16)醋酸、乙酸(16."6℃冰醋酸)CH3COOH(CH3COO-醋酸根离子)具有酸的通性(17)氨气:NH3(碱性气体)(18)氨水、一水合氨:NH3•H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2(工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、"CaO、NaOH、Ca(OH)2、"KClO3、"KCl、Na2CO3、"NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、"Fe3O4▲KMnO4为紫黑色3、"红色固体:Cu、Fe2O3、"HgO、红磷▲硫:淡黄色▲ Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)5、"沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、"BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3)等②碱:蓝色↓:Cu(OH)2红褐色↓:Fe(OH)3白色↓:其余碱。
GHS危险性符号

GHS 危险性公示要素(图形符号)适用范围GHS 标签要素中使用了9个危险性图形符号,每个图形符号适用于指定的1个或多个危险性类别以上为物理危害性图标适用危险类别爆炸性物质 自反应物质 有机过氧化物易燃气体 发火液体 易燃气溶胶 发火固体 易燃液体 自燃物质易燃固体 与水放出易燃气体物质自反应物质 有机过氧化物氧化性气体 氧化性固体 氧化性液体高压气体图标以上为健康和环境危害性注意事项:1、危险信息先后排序当某种化学品具有两种及两种以上危险性时,安全标签的象形图、信号词、危险性说明的先后顺序规定如下: (1)象形图先后顺序物理危险象形图的先后顺序,根据GB 12268中的主次危险性确定,未列入GB 12268的化学品,以下危险性类别的危险性总是主危险:爆炸物、易燃气体、易燃气溶胶、氧化性气体、高压气体、自反应物质和混合物、发火物质、有机过氧化物。
其他主危险性的确定按照联合国《关于危险货物运输的建议书规章范本》危险性先后顺序确定方法确定。
适用危险类别急性毒性 皮肤腐蚀/刺激性 严重眼损伤/眼刺激性呼吸或皮肤致敏性特定靶器官系统毒性 (单次接触) 危害臭氧层急性毒性金属腐蚀剂皮肤腐蚀/刺激性 严重眼损伤/眼刺激性呼吸或皮肤致敏性 生殖细胞致突变性 致癌性 生殖毒性 特定靶器官系统毒性(单次接触) 特定靶器官系统毒性(反复接触) 吸入危害性危害水生环境物质对于健康危害,按照一下先后顺序:如果使用了骷髅和交叉骨图形符号,则不应出现感叹号图形符号;如果使用了腐蚀图形符号,则不应出现感叹号来表示皮肤致敏物或者皮肤/眼睛刺激。
(2)信号词先后顺序存在多种危险性时,如果在安全标签上选用了信号词“危险”,则不应出现信号词“警告”。
(3)危险性说明先后顺序所有危险性说明都应当出现在安全标签上,按物理危险、将可危害、环境危害顺序排列。
2、颜色标签内象形图的颜色根据GB 30000.X-2013的规定执行,一般使用黑色图形符号加白色背景,方块边框为红色。
化学常用符号与图标

化学常用符号与图标一、化学式氢气式H2水式H2O 氯化氢式HCl 硝酸式HNO3次氯酸式HClO 硫亚酸式H2SO3硫酸式H2SO4磷酸式H3PO4碳酸式H2CO3硫化氢式H2S 磷化氢式PH3氨式NH3甲烷式CH4硅烷式SiH4水双氧式H2O2偏硅酸式硅酸式H2SiO3硅原酸式H4SiO4氯气式Cl2溴单式Br2碘单式I2氧化钠式Na2O氧过化钠式Na2O2氧化镁式MgO氧化铝式Al2O3氧化铁式Fe2O3氧亚铁式FeO四氧化三铁式Fe3O4氧化钙式CaO二氧化硫式SO2三氧化硫式SO3四氧化二氮式N2O4二氧化氮式NO2一氧化氮式NO氧化铜式CuO氧化银式Ag2O二氧化碳式CO2一氧化碳式CO氢离子式H+钠离子式Na+钾离子式K+银离子式Ag+铵离子式NH+4二氨银式[Ag(NH3)2]+钙离子式Ca2+镁离子式Mg2+铜离子式Cu2+钡离子式Ba2+铁亚离子式Fe2+锌离子式Zn2+铁离子式Fe3+铝离子式Al3+氟离子式F-氯离子式Cl-溴离子式Br-碘离子式I-硝酸根式NO-3硫氢根式HS-碳酸氢根式HCO-3硫亚氢根式HSO-3 硫酸氢根式HSO-4乙酸根式CH3COO-偏铝酸根式AlO-2次氯酸根式ClO-3碘酸根式IO-3氯次酸根式ClO-氢氧根式OH-硫亚酸根式SO2-3 碳酸根式CO2-3 硫酸根式SO2-4 硅酸根式SiO2-3 磷酸根式PO3-4 PO2-3硫离子式S2-硅原酸根式SiO3-4 氧氢化钠式氢氧钠式NaOH 氯钠式NaCl 溴钠式NaBr 碘钠式NaI 硝酸钠式NaNO3乙酸钠式CH3COONa 硫氢钠式NaHS 亚硫钠式NaHSO3碳酸氢钠式NaHCO3偏铝酸钠式NaAlO2次氯酸钠式NaClO 氯酸钠式NaClO3硫酸氢钠式NaHSO4碘酸钠式NaIO3硫酸钠式Na2SO4硫亚酸钠式Na2SO3硅酸钠式Na2SiO3碳酸钠式Na2CO3硫化钠式Na2S 硅原酸钠式Na3SiO4磷酸钠式Na3PO4氧氢化钾式氢氧钾式KOH 氯化钾式KCl 溴化钾式KBr 碘化钾式KI 碘酸钾式KNO3乙酸钾式CH3COOK 硫氢钾式KHS 亚硫钾式KHSO3碳酸氢钾式KHCO3偏铝酸钾式KAlO2次氯酸钾式KClO 氯酸钾式KClO3硫酸氢钾式KHSO4硫酸钾式K2SO4硫亚酸钾式K2SO3硅酸钾式K2SiO3碳酸钾式K2CO3硫化钾式K2S硅原酸钾式K3SiO4磷酸钾式K3PO4氯化银式AgCl 氯化银沉淀式AgCl↓溴化银式AgBr碘化银式AgI 硝酸氨银Ag(NH3)2(NO3)2氯化铵式NH4Cl溴化铵式NH4Br 碘化铵式NH4I 一水合氨式NH3·H2O 硝酸铵式NH4NO3磷酸铵式(NH4)3PO4氧氢化钙式Ca(OH)2氯化钙式CaCl2CaBr2碘化钙式CaI2碳酸钙式CaCO3钙盐:CaSO3CaSO4CaSiO3Ca3(AlO3)2Ca(HCO3)2Ca(HSO3)2Ca(HSO4)2Ca(ClO)2CaSO4 Ca3(PO4)2CaHPO4Ca(H2PO4)2镁盐:MgCl2、MgI2、Mg(NO3)2、MgSiO3、Mg(HSO3)2、Mg3(PO4)2、Mg(H2PO4)2、Mg3N2Cu(OH)2CuCl2CuBr2CuI2CuCO3Cu(NO3)2CuSO3Cu2(OH)2(CO3)2CuSO4Ba(OH)2BaCl2BaBr2BaI2BaCO3Ba(NO3)2BaSO3BaSO4BaSiO3Ba(HCO3)2Ba(HSO3)2Ba(HSO4)2 Ba3(PO4)2BaHPO4Ba(H2PO4)2Fe(OH)2FeCl2FeBr2FeI2Fe(NO3)2FeSO4Zn(OH)2ZnCl2ZnBr2ZnI2ZnCO3ZnSO4Zn(NO3)2Fe(OH)3FeCl3FeBr3Fe(NO3)3硫酸铁式Fe2(SO4)3Al(OH)3AlCl3AlBr3Al(NO3)3硫酸铝式Al2(SO4)3188O二、符号单等 —— 加热等 △—— 一定条件等 一定条件═══ 浓硫酸等 浓硫酸═══ 催化剂等 催化剂═══浓加等 浓硫酸═══加热 高高催等 高温高压═══催化剂 二氧化锰等 二氧化锰═══ 二氧化锰加热等 二氧化锰═══△高温等高温═══ 催加等催化剂═══△ 闪电══单号─→ 加热号△─→ 浓硫酸号浓硫酸───→ 一定条件号一定条件───→ 催化剂号催化剂───→ 浓加号浓硫酸───→△制乙烯号浓硫酸───→170℃ 制乙醚号浓硫酸───→140℃ 二氧化锰号二氧化锰───→ 催化剂───→加压、加热 燃烧═══燃烧══ 电解══ 一定条件逆催化剂逆浓硫酸逆高高逆可逆号浓硫酸△催化剂△ 高温高压△ 高温高压催化剂加热逆 催加逆催化剂△ 浓加逆浓硫酸△ 高高加逆高温高压△期望产物的总质量 ───────生成物的总质量高高催逆 高温高压催化剂H 2OH 2OH 2OH 2O 高温══ 高温─→ 点燃─→ 光照─→ 单逆号 ←─前聚合号——[ 后聚合号——] n 双键号 C —C 叁键号 C ——C 侧二甲苯 ─CH 3─CH 3三甲苯 H 3C ─ ─CH 3| CH 3 三硝基甲苯 ∣CH 3O 2N ─ ─NO 2 | NO 2右斜甲苯 CH3╱ CH3╱ CH3╱ CH3╱ H3C╲H3C ╲左斜甲苯H3C ╲ 竖二甲苯 OH | | CH3羰基式 —O ‖C — 醛基式 —O ‖C —H 羟基式 —OH 羧基式 —O ‖C —OH三、电子式镁电子式 ·Mg · 铝电子式 ··Al · 碳电子式 ··C ·· 氮电子式 · ·· N ·· 氧电子式 · ··O ·· ·氯右电子式 :·· Cl ·· · 氯左电子式 ··· Cl ·· :八电子结构 :··Cl ··: 氨电子式H ·· H :N·· :H :·· Cl ·· :·· Cl ·· : H :·· Cl ·· : 氢左电子式 ·H 氢右电子式 H ·C12 12C C60 12C C 60 碳六十式 C612 126C 碳十二式 沉淀淀↓ 气体体↑二氧化碳电子式 :·· O ·· ::C ::·· O ·· : 氧化钠电子式 Na +[: ·· O·· :]2-Na + 过化钠电子式Na +[: ·· O ·· : ·· O·· :]2-Na +氮气电子式 :N ······N : :·· O ·· ::C ::·· O ·· :Na +[: ·· O ·· :]2-Na + Na +[: ·· O ·· : ·· O ·· :]2-Na+ Na +[: ·· O ·· :H]-Na +[:·· Cl ·· :]-H : ·· O ·· :H :·· Cl ·· ::·· Cl ·· :C :··Cl ··::·· Cl ·· : H 2OH 2OH 2OH 2OH 2OH 2OH 2OH 2OH 2O氧氢化钠电式 Na +[: ·· O ·· : H]- 氯化钠电子式 Na +[:·· Cl ·· :]- 水电H ∶‥O ‥∶ HH ∶‥O ‥∶ H:·· Cl ·· ::·· Cl ·· :C :·· Cl ··::··Cl ·· : 四氯化碳电式:·· Cl ·· ::·· Cl ·· :C :·· Cl ··::·· Cl ·· : 左电子转移号 ·+ · 右电子转移号 · + · 氨电式 H ..H:N ..:H 铵根电式H ·· [H :N ·· :H]+H [:·· Cl ··:]- H | [H -N| -H]+HF ╲F ╱C -F·H H · Na · K · ·Mg ··Ca ···Al ···C ····Si ·· ‥·O · ‥ ···S ·· · ··N ..· ··· Cl ·· : ·· :Cl ···Na ·+ ··· Cl ·· :─→ Na +[:·· Cl ·· :]- 氯钠生式·· Br ·· ·· I ·· ·· O ·· Na ·+ ··· Br ·· : ─→ Na +[:·· Br ··:]- Na · + ··· I ·· : ─→ Na +[:·· I ··:]- CNa · + · ·· O ·· · + ·Na ─→ Na +[:·· O ·· :]2-Na +Na · + · ·· S ·· · + ·Na ─→ Na +[: ·· S ·· :]2-Na +H ·+··· Cl ·· : ─→ H :·· Cl ·· :H · +‥·O · ‥+·H ─→ H :·· O ··: H:·· Cl ·· · + ·Mg · + ··· Cl ·· :─→ [:·· Cl ·· :]-Mg 2+ [:·· Cl ·· :]-H 2OH 2OH 2O·+ · · + · K · + ··· Cl ·· : ─→ K +[:··Cl ·· :]- 氯钠生式K · + ··· Br ·· : ─→ K +[:··Br ·· :]-K · + ··· I ·· :─→ K +[:··I ··:]-K · + ‥·O · ‥ +·K ─→ K +[:·· O ·· :]2-K +K · + · ·· S ·· · +·K ─→ K +[: ·· S ·· :]2-K + H · +··· Cl ·· : ─→ H :··Cl ·· :H · +··· Br ·· : ─→ H :··Br ·· :H · +··· I ·· : ─→ H :··I ··:H · +‥·O · ‥+·H ─→ H :·· O ··: H:·· Cl ·· ·+·Mg ·+··· Cl ·· :─→ [:·· Cl ·· :]-Mg 2+ [:·· Cl ·· :]- [:·· Cl ·· :]-Mg 2+ [:·· Cl ·· :]- :·· I ·· ·+·Mg ·+··· I ·· :─→ [:·· I ·· :]-Mg 2+ [:··I ·· :]- :·· Br ·· ·+·Mg ·+··· Br ·· :─→ [:·· Br ·· :]-Mg 2+ [:··Br ·· :]- :·· Cl ·· ·+·Ca ·+··· Cl ·· :─→ [:·· Cl ·· :]-Ca 2+ [:··Cl ··:]-:·· I ·· ·+·Ca ·+··· I ·· :─→ [:·· I ·· :]-Ca 2+ [:··I ·· :]- :·· Br ·· ·+·Ca ·+··· Br ·· :─→ [:·· Br ·· :]-Ca 2+ [:··Br ·· :]-氯气电式 :·· Cl ·· :·· Cl ·· : :·· Br ·· :·· Br ·· :溴单电式 :·· Br ·· :·· Br ·· : 碘单电式 :·· I ·· :··I ·· : 氮气电式 :N ······N : 氢气电式 H :H Cl 2氯化氢电式 H :·· Cl ·· : H ..H:N ..:H H .. [H :N ..:H]+H 甲烷电式 H ..H :C ..:H H H ..H :Si ..:H HH ·· H :N ·· :H H ·· [H :N ·· :H]+HH ·· H :N ··:H H ·· [H :N ·· :H]+HH | [H -O -H]+电子转移式 2e —∣─────────────↓S + O 2 ═ SO 2 电子转移式2e —∣─────────────↓ S + O 2 ═ SO 2一层结构○+1 )1 ) 二层结构○+1 )2 ))8 ) ○+1 )1 ) ○+1 )2 ))8 ) —CH —∣NH 2CH 2-∣OH ∣CH 2-OH 上CH 2-∣OH∣CH 2-OH 三、 有机域上结构 CH 3—CH —COOH ∣NH 2 —CH —∣NH 2下结构 CH 2-∣OH CH 2-∣OH CH 2-∣OH CH 2-∣OH上下构结 CH -∣OH ∣NH 2 CH -∣OH ∣NH 2CH -∣OH ∣NH 2CH -∣OH ∣NH 2CH -∣OH ∣NH 2CH -∣OH∣NH 2中结构 ∣CH 2-OH ∣CH 2-OH ∣CH 2-OH ∣CH 2-OH署名结构 (C 6H 10O 5)n 纤维素 (C 6H 10O 5)n 淀粉 (C 6H 12O 6)n 葡萄糖 (C 6H 12O 6)n 果糖 (C 12H 22O 11)n 麦芽糖 (C 12H 22O 11)n蔗糖(C 6H 10O 5)n 纤维素分子式结构 HNO 3 C 2H 5O —NO 2硝酸乙酯C 2H 5O —NO 2硝酸乙酯C 2H 5O —NO 2硝酸乙酯C 2H 5O —NO 2硝酸乙酯C 2H 5O —NO 2硝酸乙酯分子结构 CH —ONO 2∣CH 2—ONO 2∣CH 2—ONO 2三层结构 CH —ONO 2∣CH 2—ONO 2∣CH 2—ONO 2反应示意图结构 H 2O ⎩⎪⎨⎪⎧CO 2叶绿素A 酶B O 2催化剂C O2D B H +ENa 2O 2⎩⎨⎧→G 过量CO 2白色沉淀H→F S 点燃I H 2SO 4△水解液NaOH 溶液中和液⎩⎨⎧银氨溶液微热生成银镜碘水无现象 C 6H 5— HO —CH —NH —C ‖O —C 6H 5CH -COOH ∣+H 2O 无机酸C 6H 5— HO —CH —NH 2CH -COOH ∣羟基酸羟基酯结构 CH 3CH ╱╲COO╲OOC╱CHCH 3 CH 3CH ╱╲COO ╲OOC ╱CHCH 3CH 3CH ╱╲COO ╲OOC╱CHCH 3双键结构 H 3C ╲H 3C ╱C =C ╱CH 3╲CH 3 H 3C ╲H 3C ╱C = C ╱╲ C ╱╲ CH 3CH 3 C ╱CH 3╲CH 3横上苯 - 横下苯- - 竖右苯竖左苯对二甲苯 CH 3 -CH 3 CH 3- -CH 3竖苯酚 -OH 横苯酚 OH 竖苯酚 竖方程组结构 竖甲苯竖苯酚 OH |竖苯甲酸COOH|竖甲苯 CH 3|上甲基 CH3| 下甲基 | CH3 右斜甲苯CH3╱ CH3╱ CH3╱ CH3╱ ╱H3C H3C ╲ H3C ╲竖对二苯基 OH || CH3横对二苯基 ——-CH 3-CH 3平二苯基H 3C ──CH 3-CH 3-CH 3 侧二苯基-CH 3-CH 3 三苯基 H 3C ──CH 3| CH3三硝基甲苯 CH3|O 2N ─ ─NO 2 | NO2白藜芦醇 HO - -CH =CH - ╱CH 3╲CH 3横右三甲苯CH - ╱CH 3╲CH 3横左三甲苯 H3C ╲ ╱H3C-CH 3 CHH3C ╲ ╱H3C竖三甲苯 CH3| H 3C ──CH 3 三溴苯酚 Br ─ ─Br | Br双键号 —— 叁键号——合成结构(C 6H 10O 2N 2)C 适当条件CH 3-CH -COOH ∣NH 2↓Na ↓HClA B HHHNO 2D 浓硫酸(C 6H 8O 4)E四、方程组结构 ytxs⎩⎪⎨⎪⎧x ═1y ═2z ═3m ═4 ⎩⎪⎨⎪⎧2x +3y +9z +5m ═555x +7y +11z +9m ═882×(x +y +z +2m )═28 x +y +z +m ═10⎩⎪⎨⎪⎧2x +3y +9z +5m ═55……………………①2×(x +y +z +2m )═28……………………② ⎩⎪⎨⎪⎧x ═ 1y ═ 2⎩⎨⎧银氨溶液微热生成银镜碘水无现象⎩⎨⎧银氨溶液微热生成银镜碘水无现象 银氨溶液微热生成银镜碘水无现象⎩⎨⎧银氨溶液微热生成银镜碘水无现象 同醛基式 -O ║C —H双尖前域⎩⎪⎨⎪⎧x +y ═x +y ═双尖后域⎭⎪⎬⎪⎫x +y ═x +y ═3、⎩⎨⎧x +y ═x +y ═x +y ═4、⎩⎪⎨⎪⎧x +y ═x +y ═x +y ═x +y ═x +y ═双平前域⎣⎢⎡x +y ═x +y ═双平后域⎦⎥⎤x +y ═x +y ═前聚合号——[ 后聚合号 ——] n 聚合号 ——[——] n左合右号 ――――――⎦⎥⎤――― 左分右号 ――――⎣⎢⎡-→-→HO — —∣OH CH 2CH -∣NH 2O -O ║C —HHO - -CH =CH - ╱CH 3╲CH 3 白黎芦醇 HO - -CH =CH - ╱CH 3╲CH 3环氧乙烷O╱ ╲H 2C ――CH 2有机结构域应用 [—]—n C ‖O —NHCH 3CH ╱╲COO ╲OOC╱CHCH 3CHOOCR'∣CH 2OOCR ∣CH 2OOCR'' CHOOCR ∣CH 2OOCR ∣CH 2OOCR CHOOCC 17H 31∣CH 2OOCC 17H 31∣CH 2OOCC 17H 31 催化剂加热、加压CHOOCC 17H 35∣CH 2OOCC 17H 35∣CH 2OOCC 17H 35HO —NO 2硝酸浓硫酸C 2H 5O —NO 2硝酸乙酯227×15.86%12 227×(100%-15.86%-2.20%-18.50%)16CH —ONO 2∣CH 2—ONO 2∣CH 2—ONO 2CH —OH ∣CH 2—OH ∣CH 2—OH —C — ∣CH 3 ∣ CH 3中间结构CH —O —C ‖O—R 2∣CH 2—O —C ‖O —R 1∣CH 2—O —C ‖O —R 3H 2SO 4 CH —OH ∣CH 2—OH ∣CH 2—OHCH —OH ∣CH 2—OOCCH 3∣CH 2—OH 和CH —OOCCH 3∣CH 2—OH ∣CH 2—OH10 g2 0003 g ·mol —1∶12 g 1002 g ·mol —1═①CHOOCC 15H 31∣CH 2OOCC 15H 31∣CH 2OOCC 15H 31 ②CH 2∣CH 2OOCC 17H 35∣CH 2OOCC 17H 35 ③CH —ONO 2∣CH 2—ONO 2∣CH 2—ONO 2Cu(OH)2 KMnO 4 I 2 mol ·L -1 C 17H 35CHOOCC 17H 35∣CH 2OOCC 17H 31∣CH 2OOCC 17H 35 B.CHOOCC 17H 33∣CH 2OOCC 17H 33∣CH 2OOCC 17H 35 C.CHOOCC 17H 33∣CH 2OOCC 17H 33∣CH 2OOCC 17H 31 D.CHOOCC 15H 31∣CH 2OOCC 15H 29∣CH 2OOCC 15H 29—C ‖O —R 被 -P -O ‖O ∣OH 1230 ⎩⎨⎧加碘水溶液变蓝色加C 溶液单质沉淀 加A 溶液△ H -C -H |H ∣H⎩⎨⎧银氨溶液微热生成银镜碘水无现象 ONO 2ONO 2OH⎩⎪⎨⎪⎧→D→C(密度最小的单质)→EC 6H 5— HO —CH —NH —C ‖O —C 6H 5CH -COOH∣C 6H 5— HO —CH —NH 2CH -COOH∣H 2N —CH ∣R 1—C ‖O —N ∣H —CH ∣R 2—C ‖O —N ∣H —CH ∣R 3—C ‖O —N ∣H —CH ∣R 4—C ‖O —OH甘氨酸(C 2H 5NO 2)CH 2—COOH NH 2∣丙氨酸(C 3H 7NO 2)CH 3—CH —COOH ∣NH 2 ,—C ‖O —N ∣H —谷氨酸(C 5H 9NO 4)HOOC —CH 2—CH 2—CH —COOH ∣NH 2⎩⎪⎨⎪⎧2x +3y +9z +5m ═555x +7y +11z +9m ═882×(x +y +z +2m )═28 x +y +z +m ═10 解得⎩⎪⎨⎪⎧x ═1y ═2z ═3m ═4(C 6H 7O 2)—ONO 2ONO 2OH n—NH -↓A CH ∣R -↓B C ‖O -↓CNH -CH ∣R'—C -‖→D OR -CH —C ‖O —OH ∣NH 2+HNO 2R -CH —C ‖O —OH ∣OH+N 2↑+H 2(C 6H 10O 2N 2)C 适当条件CH 3-CH -COOH ∣NH 2↓Na ↓HClA B HHHNO 2D 浓硫酸(C 6H 8O 4)EHS -CH 2—CH —COOH ∣NH 2 HS -CH 2—CH —C ‖O —O -S -CH 2—CH —COOH ∣NH 2∣NH 2 HS -CH 2—CH —COONH 4∣NH 2A.H -C -∣H ∣OH C -∣H ∣OH C -∣H ∣OH C -∣H ∣OH C —C ‖O —H ∣H ∣OHB.H -C -∣H ∣NH 2C -∣H ∣NH 2C -∣H ∣NH 2C -∣H ∣NH 2C —C ‖O —H ∣H ∣NH 2C.H -C -∣H ∣NH 2C -∣H ∣NH 2C -∣H ∣NH 2C -∣H ∣NH 2C —C —‖NH H ∣H ∣NH 2D.H -C -∣H ∣OH C -∣H ∣OH C -∣H ∣OH C -∣H ∣OH C —C —‖NH H ∣H ∣OHCH 2—COOH ∣NH 2、CH 3—CH —COOH ∣NH 2、CH 3—CH 2-CH —COOH ∣NH 2A. CH 2—COOH ∣NH 2B.CH 3—CH —COOH ∣NH 2╲C ‖O ╱ ╲C ‖O ╱ CH 2-CH 2∣ C ——∣H N ∣ CH 2CH 2∣(C 6H 7O 2)—ONO 2OH OH n (C 6H 7O 2)—ONO ONO 2ONO nC. D.HOOC —CH 2—CH 2—CH —COOH ∣NH 2B.C. ——HHD. (C 6H 7O 2)—ONO 2ONO 2OHCH 2-∣OH CH -∣OH CH -∣OH CH -∣OH CH -∣OHCHO 甲CH 2-∣OH CH —CH -∣OH CH -∣OH CH -∣OH CH ∣OH 乙H 2O ⎩⎪⎨⎪⎧CO 2叶绿素A 酶B O 2催化剂C O 2D B H +E Na 2O 2⎩⎨⎧→G 过量CO 2白色沉淀H →F S 点燃I[— [—CH —∣CH 3CH ]—n ∣COOH②CHOOCC 15H 31∣CH 2OOCC 15H 31∣CH 2OOCC 15H 31+HO -P -OH ‖O ∣OH CHOOCC 15H 31∣CH 2O -P -OH ‖O ∣OH ∣CH 2OOCC 15H 31+C 15H 31COOH ③CHOOCC 15H 31∣CH 2O -P -OH ‖O ∣OH ∣CH 2OOCC 15H 31+2NaOH CHOOCC 15H 31∣CH 2O -P -ONa ‖O ∣ONa ∣CH 2OOCC 15H 31+2H 2O(说明:-P -O ‖O ∣OH H 也可代替CHOOCC 15H 31∣CH 2OOCC 15H31∣CH 2OOCC 15H 31中间的—C ‖O—C 15H 31基团。
化学符号大全

化学符号大全文件排版存档编号:[UYTR-OUPT28-KBNTL98-UYNN208]化学符号大全、物质的学名、俗名及化学式⑴金刚石、石墨:C⑵水银、汞:Hg (3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2 (5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3 (7)氢硫酸:H2S (8)熟石灰、消石灰:Ca(OH)2 (9)苛性钠、火碱、烧碱:NaOH (10)纯碱:Na2CO3 碳酸钠晶体、纯碱晶体:Na2CO3?10H2O (11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4?5H2O (13)铜绿、孔雀石: Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH (16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH (CH3COO- 醋酸根离子)具有酸的通性(17)氨气:NH3 (碱性气体)(18)氨水、一水合氨:NH3?H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2 (工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3 、HgO、红磷▲硫:淡黄色▲ Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2 红褐色↓:Fe(OH)3白色↓:其余碱。
(word完整版)化学常见符号大全,推荐文档

化学文档中常见符号集锦说明:将符号复制、粘贴到需要得文档就可。
一、数字顺序:①②③④⑤⑥⑦⑧⑨⑩⑪⑫⑬⑭⑮⑯⑰⑱⑲⑳二、罗马数字:I II III IV V VI VII VIII IX IX三、物理量:焓 ∆H 平均值 -M平均摩尔质量 -r M 平均相对分子质量 -rA 摩尔质量 M ()相对分子质量 M r 相对原子质量 A r 速率v 计量系数ν 密度 ρ 转化率 α体积分数 ϕ 物质的量分数 x 质量分数 w ()四、常见符号 NH 3·H 2O黑点 ● " ´ ° 加热 △ ℃ ≥ ≤ > < 比号 : ÷ × Ω ⋅η ü ℃ 单键 — 双键= 三键 ≡ ~五、希腊字母φ σ ρ π v μ λ ε ∆ δ γ β α六、上下标七、转移电子 4HCl +MnO 2 = MnCl 2+Cl 2↑+2H 2O 2e -MnO 2+4HCl = MnCl 2+Cl 2↑+2H 2O 2e -22↑+2H 2O 得2e -,升2价,被还原八、反应符号: △ 电解 △ 2 2光 △ 点燃 高温 放电 电解 Cu催化剂 催化剂△ 浓硫酸 浓硫酸△浓硫酸140 ℃浓硫酸170 ℃△乙醇一定条件光△高温催化剂高温、高压充电放电+OH -垐?噲?九、其它反应符号常温熔融℃~252电解36微热微热或不加热浓硫酸NaOH平衡时常温灼烧 沸水 熔融 高温煅烧 灼热的Cu水浴加热微生物光合作用水化 酸化 稀盐酸 盐酸酸化 硝酸酸化 浓硝酸 澄清石灰水石灰乳稀氨水 NaOH 溶液 Br 2的CCl 4溶液 AgNO 3溶液 Na 2SO 3溶液 氯水Fe 、水 稀H 2SO 4△NaOH△Cu(OH)2OH - H HClNaOHO 2Cl 2I 22 Cl -Br -I -S -Ⅰ Ⅱ常温沸水浓硫酸催化剂△V 2O 5催化剂T 12。
化学符号大全

化学符号大全、物质的学名、俗名及化学式⑴金刚石、石墨:C⑵水银、汞:Hg (3)生石灰、氧化钙:CaO(4)干冰(固体二氧化碳):CO2 (5)盐酸、氢氯酸:HCl(6)亚硫酸:H2SO3 (7)氢硫酸:H2S (8)熟石灰、消石灰:Ca(OH)2 (9)苛性钠、火碱、烧碱:NaOH (10)纯碱:Na2CO3 碳酸钠晶体、纯碱晶体:Na2CO3•10H2O (11)碳酸氢钠、酸式碳酸钠:NaHCO3 (也叫小苏打)(12)胆矾、蓝矾、硫酸铜晶体:CuSO4•5H2O (13)铜绿、孔雀石:Cu2(OH)2CO3(分解生成三种氧化物的物质)(14)甲醇:CH3OH 有毒、失明、死亡(15)酒精、乙醇:C2H5OH (16)醋酸、乙酸(16.6℃冰醋酸)CH3COOH (CH3COO- 醋酸根离子)具有酸的通性(17)氨气:NH3 (碱性气体)(18)氨水、一水合氨:NH3•H2O(为常见的碱,具有碱的通性,是一种不含金属离子的碱)(19)亚硝酸钠:NaNO2 (工业用盐、有毒)二、常见物质的颜色的状态1、白色固体:MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;铁、镁为银白色(汞为银白色液态)2、黑色固体:石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫黑色3、红色固体:Cu、Fe2O3 、HgO、红磷▲硫:淡黄色▲ Cu2(OH)2CO3为绿色4、溶液的颜色:凡含Cu2+的溶液呈蓝色;凡含Fe2+的溶液呈浅绿色;凡含Fe3+的溶液呈棕黄色,其余溶液一般不无色。
(高锰酸钾溶液为紫红色)5、沉淀(即不溶于水的盐和碱):①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等②碱:蓝色↓:Cu(OH)2 红褐色↓:Fe(OH)3白色↓:其余碱。
6、(1)具有刺激性气体的气体:NH3、SO2、HCl(皆为无色)(2)无色无味的气体:O2、H2、N2、CO2、CH4、CO(剧毒)▲注意:具有刺激性气味的液体:盐酸、硝酸、醋酸。
化学图形符号库 (1)

长颈漏斗 分液漏斗 球形分液漏斗 梨形分液漏斗 三角漏斗
量筒
刻度
酒精灯
铁架台
铁架台(侧面) 铁架台(正面) 铁夹
铁圈(无石棉网) 铁圈(有石棉网)
电池
G Pt Pt Zn Cu
电解池
原电池
棒、夹、塞
玻璃棒
玻璃活塞 玻璃活塞关 滴定管夹
橡皮塞
大试管铁夹橡皮塞
连接管
直玻璃管 直角弯导管(长)直角弯玻璃管(短) 橡胶管
三通
三通口 三通尖嘴 三通短管 三通接口
其它
温度计
水槽
支管U型管 支管试管
干燥器
三脚架
坩埚
坩埚钳
泥三角
燃烧匙
表面皿
酸式
其它
+ H H O H
xSxH
-
H H C H
Ox H
xx
I-Leabharlann Li+Na+
K+
Mg2+
Ca2+
分子
H H
N N
F F
H H C H H
S
Cl Cl
C S
Br Br
I
I
H F
H Cl
H I
H O O H
离子晶体
Na+
-
Cl
Cl
Ca2+
-
Cl
Na+
O
2- +
Na
Na+
2-
S
原子
离子
原子结构示意图
—CH2—CH3
CH CH2=CH
CH CH =CH2
Br
苯1
苯2
—NO2
初中化学常用符号
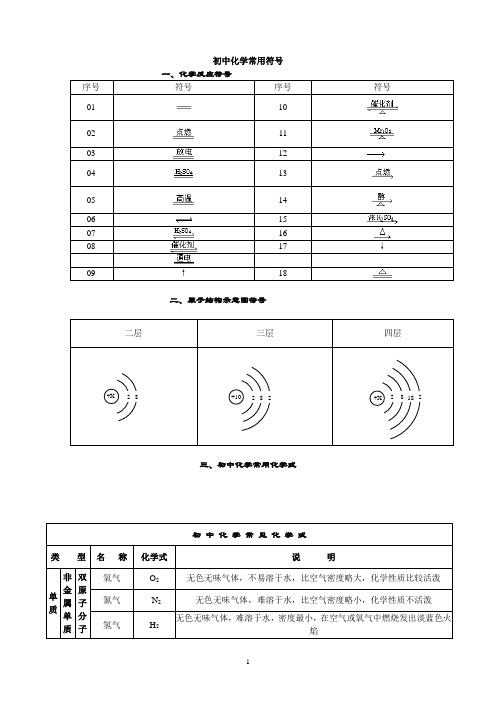
Mg(OH)2 Al(OH)3 Ba(OH)2 NaCl KCl NH4Cl MgCl2 CaCl2 CuCl2 FeCl2 FeCl3 AgCl BaCl2 ZnCl2 AlCl3 Na2SO4 K2SO4 (NH4)2SO4 MgSO4 CaSO4 CuSO4 FeSO4
白色固体,溶于水,水溶液为蓝色
无色无味气体,难溶于水,比空气密度略小,有剧毒,碳或含碳物质不充 分燃烧的生成物,空气的主要污染物之一 无色有刺激性气味有毒的气体, 溶于水并部分与水反应生成亚硫酸, 是空 气的主要污染物之一,也是形成“酸雨”的主要物质之一,煤碳或石油产 品燃烧的生成物,如工厂的废气和汽车排放的尾气里含有二氧化硫 #无色无味固体,与水反应生成硫酸 红棕色有刺激性气味有毒的气体, 溶于水并与水反应生成硝酸, 是空气的 主要污染物之一,也是形成“酸雨”的主要物质之一,煤碳或石油产品燃 烧的生成物,如工厂的废气和汽车排放的尾气里含有二氧化硫 白色固体,难溶于水
F2 Cl2 He Ne Ar C S P Si K Ca Na Mg Al Zn Fe Sn Pb Cu Hg Ag Pt Au H 2O H 2O 2 CO2 实验室制氧气的反应物 无色无味气体,能溶于水,比空气密度大,不支持燃烧,通入澄清石灰水 使之变浑浊
2
无色无味气体,难溶于水,化学性质不活泼
3Mg + 2AlCl3 = 3MgCl2 + 2Al 3Mg + A l 2 ( S O 4 ) 3 3Mg + 2Al (NO3)3 = = 3MgSO4 + 2Al 3Mg (NO3)2+ 2Al
Mg + ZnCl2 = MgCl2 + Zn Mg + Z n S O 4 = MgSO4 + Zn Mg + Zn (NO3)2 = Mg + CuCl2 = Mg (NO3)2+ Zn MgCl2 + Cu
化学符号大全

化学符号大全一、常见元素符号:1.氢元素(H)2.氧元素(O)3.氮元素(N)4.碳元素(C)5.钠元素(Na)6.钾元素(K)7.铁元素(Fe)8.铜元素(Cu)9.锌元素(Zn)10.氟元素(F)11.氯元素(Cl)12.溴元素(Br)13.碘元素(I)14.锂元素(Li)15.硫元素(S)16.磷元素(P)17.铝元素(Al)18.镁元素(Mg)19.银元素(Ag)20.铀元素(U)二、常见离子符号:1.氢离子(H+)2.氧离子(O2-)3.氯离子(Cl-)4.锂离子(Li+)5.钠离子(Na+)6.铜离子(Cu2+)7.铁离子(Fe2+)8.硫离子(S2-)9.铝离子(Al3+)10.鋰離子(Li+)11.鈉離子(Na+)12.鎂離子(Mg2+)13.鈣離子(Ca2+)14.鋅離子(Zn2+)15.氟离子(F-)16.碳酸根离子(CO32-)17.硫酸根离子(SO42-)18.硝酸根离子(NO3-)19.氨基离子(NH4+)20.铵离子(NH4+)三、常见化合物符号:1.水(H2O)2.乙醇(C2H5OH)3.二氧化碳(CO2)4.盐酸(HCl)5.硫酸(H2SO4)6.硝酸(HNO3)7.碳酸(CO3)8.醋酸(CH3COOH)9.氨水(NH3)10.氢氧化钠(NaOH)11.氯化钠(NaCl)12.硝酸铵(NH4NO3)13.硝酸钾(KNO3)14.硫酸铜(CuSO4)15.硫酸亚铁(FeSO4)16.碳酸钙(CaCO3)17.氯化铁(FeCl3)18.氢碘酸(HI)19.石蜡(C25H52)20.点燃气(C3H8)以上仅是一小部分常见的化学符号和化合物,实际上化学符号体系非常复杂广泛,涉及到大量的元素、化合物、离子和反应物等。
化学符号的使用可以使科学家们在实验和研究中更方便快捷地记录、表示和表达。
同时,它还帮助科学家们更好地理解元素之间的化学性质和反应规律。
不同国家和地区对化学符号的命名和使用也有一定的差异,因此,在学习和使用化学符号时,需要遵守相应的国际化学命名规则和约定。
化学常用符号与图标

精心整理化学常用符号与图标一、化学式氢气式水式氯化氢式硝酸式次氯酸式硫亚酸式硫酸式磷酸式碳酸式硫化氢式磷化氢式氨式甲烷式硅烷式水双氧式偏硅酸式硅酸式硅原酸式氯气式溴单式碘单式氧化钠式氧过化钠式氧化镁式氧化铝式氧化铁式氧亚铁式四氧化三铁式氧化钙式二氧化硫式三氧化硫式四氧化二氮式二氧化氮式一氧化氮式氧化铜式氧化银式二氧化碳式一氧化碳式氢离子式钠离子式钙盐:O浓加等高高催等二氧化锰等二氧化锰加热等高温等催加等单号加热号浓硫酸号一定条件号催化剂号浓加号制乙烯号制乙醚号二氧化锰号一定条件逆催化剂逆浓硫酸逆高高逆加热逆催加逆浓加逆高高加逆高高催逆单逆号←─前聚合号双键号CC叁键号CC侧二甲苯─CH3,─CH)3三甲苯 CH 3),)三硝基甲苯),O 2N ─ ─NO 2,) 右斜甲苯 左斜甲苯 竖二甲苯羰基式—),C )—醛基式—),C )—H 羟基式—OH羧基式—),C )—OH三、电子式镁电子式·Mg ·铝电子式··碳电子式··氮电子式··氧电子式··氯右电子式:·氯左电子式·:八电子结构::氨电子式),H ::H ):::H ::氢左电子式·H 氢右电子式H ·C12C60C 60碳六十式C612碳十二式沉淀淀↓气体体↑·HH ),· ),·K ·+·:K ·+·:K ·+·:K ·++·K ·+H ·+·:H ·+·:H ·+·:H ·++·:·+·:·+·:·+·:·+·Ca ·+·:[::]-Ca 2+[::]-:·+·Ca ·+·:[::]-Ca 2+[::]-:·+·Ca ·+·:[::]-Ca 2+[::]-氯气电式::::::溴单电式:::碘单电式:::氮气电式:NN :氢气电式H :H氯化氢电式H ::),H::H )),[H ::H]+,H )甲烷电式),H ::H ,H )),H ::H ,H )),H ::H )),[H ::H]+,H)电子转移式),S+O 2═SO 2,)电子转移式),S+O 2═SO 2,)一层结构二层结构上三、有机域上结构下结构上下构结中结构署名结构分子式结构—,硝酸乙酯)—,硝酸乙酯)—,硝酸乙酯)—,硝酸乙酯)—,硝酸乙酯)分子结构三层结构反应示意图结构ABCDE,白色沉淀H,→FI))))水解液中和液生成银镜,无现象))))—,)C6H5),)+H2O))))羟基酸羟基酯结构横对二苯基——平二苯基─,)三苯基同醛基式-),C,)—H双尖前域双尖后域)3、4、双平前域)))双平后域)前聚合号后聚合号聚合号左合右号)―――左分右号)HO-CH=CH-白黎芦醇CH=CH-环氧乙烷有机结构域应用n )中间结构和)∶,2)═①②③—,)R 被溶液变蓝色,单质沉淀))H 2N ——,)——,)——,)——,)OH ,—,)—解得⑵取代;不能;其组成和数量均发生了变化⑶①2NaCl +2H 2O,电解,)2NaOH +↑+↑ ②CH 3COOH +ClCH 2COOH +HCl26.⑴缩聚⑵+n H 2O n (C 6H 7O 2)— n⑶CH2—n,∣,COOH),水解,);;;;╱╱。
(完整)化学常见符号大全,推荐文档

化学文档中常见符号集锦说明:将符号复制、粘贴到需要得文档就可。
一、数字顺序:①②③④⑤⑥⑦⑧⑨⑩⑪⑫⑬⑭⑮⑯⑰⑱⑲⑳二、罗马数字:I II III IV V VI VII VIII IX IX三、物理量:焓 ∆H 平均值 平均摩尔质量 平均相对分子质量 摩尔质量 M ()-M -r M -r A相对分子质量 M r 相对原子质量 A r 速率v 计量系数ν 密度 ρ 转化率 α 体积分数 ϕ 物质的量分数 x 质量分数 w ()四、常见符号 NH 3·H 2O黑点 ● " ´ ° 加热 △ ℃ ≥ ≤ > < 比号 : ÷ × Ω η ü ℃⋅单键 — 双键= 三键 ≡ ~五、希腊字母φ σ ρ π v μ λ ε ∆ δ γ β α六、上下标-----2 = MnCl 2+Cl 2↑+2H 2O2+Cl 2↑+2H 2O↑+2H 2O八、反应符号:℃放电电解℃MnO 22℃光℃点燃高温放电电解℃Cu催化剂催化剂℃浓硫酸浓硫酸℃浓硫酸140 ℃浓硫酸170 ℃℃乙醇一定条件光℃高温催化剂高温、高压催化剂充电放电+H OH-A AA A AA九、其它反应符号熔融400℃~500℃V 2O 52电解1000 ℃ Na 3AlF 6浓硫酸NaOH 平衡时常温灼烧沸水熔融高温煅烧灼热的Cu水浴加热微生物光合作用水化酸化稀盐酸盐酸酸化硝酸酸化浓硝酸澄清石灰水石灰乳稀氨水NaOH 溶液Br 2的CCl 4溶液AgNO 3溶液Na 2SO 3氯水Fe 、水稀H 2SO 4℃℃NaOH℃Cu(OH)2OH -H HClNaOHO 2Cl 2I 2水H 2OCl -Br -I -S ℃℃常温沸水℃催化剂℃V 2O 5催化剂T 1T 2。
化学常见符号大全

化学常见符号大全The Standardization Office was revised on the afternoon of December 13, 2020化学文档中常见符号集锦说明:将符号复制、粘贴到需要得文档就可。
一、数字顺序:①②③④⑤⑥⑦⑧⑨⑩⑪⑫⑬⑭⑮⑯⑰⑱⑲⑳二、罗马数字:I II III IV V VI VII VIII IX IX三、物理量: 焓∆H 平均值 -M平均摩尔质量 -r M 平均相对分子质量 -r A 摩尔质量 M () 相对分子质量 M r 相对原子质量 A r 速率v 计量系数ν 密度 ρ 转化率 α体积分数 ϕ 物质的量分数 x 质量分数 w ()四、常见符号 NH 3·H 2O黑点 " ´ ° 加热 △ ℃ ≥ ≤ > < 比号 : ÷ × Ω ⋅η ü ℃ 单键 — 双键= 三键 ≡ ~五、希腊字母φ σ ρ π v μ λ ε ∆ δ γ β α 六、上下标七、转移电子 4HCl +MnO 2 = MnCl 2+Cl 2↑+2H 2O 2e -MnO 2+4HCl = MnCl 2+Cl 2↑+2H 2O2e -22↑+2H 2O 得2e -,升2价,被还原八、反应符号:△高温放电电解催化剂△22△光△点燃高温放电电解△Cu催化剂催化剂△浓硫酸浓硫酸△浓硫酸140 ℃浓硫酸170 ℃△乙醇一定条件光△高温催化剂高温、高压充电放电+OH -九、其它反应符号常温沸水400℃~500252电解1000 ℃ Na 3AlF 6点燃或光照微热微热或不加热浓硫酸NaOH 平衡时常温灼烧沸水熔融高温煅烧灼热的Cu水浴加热微生物光合作用水化酸化稀盐酸盐酸酸化硝酸酸化浓硝酸澄清石灰水石灰乳稀氨水NaOH 溶液Br 2的CCl 4溶液AgNO 3溶液Na 2SO 3氯水Fe 、水稀H 2SO 4△△NaOH△Cu(OH)2OH - H HClNaOHO 2Cl 2I 2水H 2OCl -Br -I -SⅠⅡ常温沸水浓硫酸△催化剂V 2O 5催化剂T 1T 2。
化学字母公式符号大全

化学字母公式符号大全
在化学中,有许多用于表示元素、化合物和化学反应的符号和公式。
以下是化学字母公式符号的一些常见示例:
1.元素符号:
-H:氢
-He:氦
-Li:锂
-Be:铍
-B:硼
-C:碳
-N:氮
-O:氧
-F:氟
-Ne:氖
-Na:钠
-Mg:镁
-Al:铝
-Si:硅
-P:磷
-S:硫
-Cl:氯
-K:钾
-Ca:钙
-Fe:铁
-Cu:铜
-Zn:锌
-Ag:银
-Au:金
2.化合物和离子:
-H2O:水
-CO2:二氧化碳
-NH3:氨
-NaCl:氯化钠
-CaCO3:碳酸钙
-HCl:盐酸
-CH4:甲烷
-C6H12O6:葡萄糖
-NO3-:硝酸根离子
-SO42-:硫酸根离子
-OH-:羟基离子
3.化学反应方程式:
-H2+O2→H2O:氢气加氧气生成水
-CH4+2O2→CO2+2H2O:甲烷燃烧生成二氧化碳和水
-2H2O→2H2+O2:水分解生成氢气和氧气
这只是一些常见的化学字母公式符号示例,化学中还有更多的符号和公式表示法。
根据不同的化合物和化学反应类型,符号和公式可能会有许多不同的组合和表示方法。
初三化学符号大全

初三化学符号大全一、元素符号元素符号是表示化学元素的一种缩写形式,由元素的拉丁名字或拉丁名字的首字母组成,有时也是用来缩写元素中的拉丁名字的前两个字母,为了避免混淆,符号一般采用英文大写字母。
1. 金属元素符号金属元素是指具有金属性质的元素,如铁(Fe)、铜(Cu)、锌(Zn)等。
2. 非金属元素符号非金属元素是指不具有金属性质的元素,如氧(O)、氮(N)、硫(S)等。
二、化合物符号化合物符号是用来表示多个元素组成的物质的缩写形式,化合物符号通常由元素符号和其相应的下标表示。
1. 水(H2O)水是由氢元素和氧元素构成的化合物,其化学符号为H2O。
2. 二氧化碳(CO2)二氧化碳是由碳元素和氧元素构成的化合物,其化学符号为CO2。
三、常见的基本化学符号基本化学符号是指常见的元素的符号,如H代表氢元素,C代表碳元素等。
1. H(氢)氢是最轻的元素,在化学中的化学符号为H。
2. He(氦)氦是第二轻的元素,在化学中的化学符号为He。
3. C(碳)碳是生命中的基本元素之一,在化学中的化学符号为C。
4. O(氧)氧是空气中最重要的元素之一,在化学中的化学符号为O。
5. N(氮)氮是主要构成空气的元素之一,在化学中的化学符号为N。
6. Na(钠)钠是一种金属元素,在化学中的化学符号为Na。
7. Cl(氯)氯是一种非金属元素,在化学中的化学符号为Cl。
8. Fe(铁)铁是一种常见的金属元素,其化学符号为Fe。
四、离子符号离子是指带有正电荷或负电荷的原子或分子,通过失去或获得电子而形成。
1. 阴离子阴离子带有负电荷,如氧化物离子(O2-)。
2. 阳离子阳离子带有正电荷,如氯离子(Cl+)。
五、常见的物质符号除了化学元素和化合物的符号外,还有一些物质的符号也很常见。
1. H2SO4(硫酸)硫酸是一种常见的化学物质,它的化学符号为H2SO4。
2. NaCl(氯化钠)氯化钠是食盐的化学名字,其化学符号为NaCl。
3. CH4(甲烷)甲烷是一种简单的烷烃化合物,其化学符号为CH4。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
连接管
直玻璃管 直角弯导管(长)直角弯玻璃管(短) 橡胶管 三通 三通口 三通尖嘴 三通短管 三通接口
其它
温度计 水槽 支管U型管 支管试管
干燥器
三脚架
坩埚
坩埚钳
泥三角 燃烧匙 表面皿 酸式
其它
本内容仅供参考,如需使用,请根据自己实际情况更改后使用!
碳还原氧化铜
制取与收集氢气
一氧化碳还原氧化铜
排气、水法收集氧气
二氧化碳通入澄清的石灰水
氢气还原氧化铜
固体加热气体干燥
固液不加热制气
启普发生器
制氢简易装 置
简易启普发 生器
蒸馏烧瓶成套装置
尾气吸收氯气、氯化氢气体
固固加热造气
固固不加热造气
固液加热造气
向下排空气法
制氯气的成套装置
CH–ONO2
甘油
| CH2–ONO2
OH
三溴苯酚 | Br–– ––Br
C17H35COOCH2 |
C17H35COOCH |
C17H35COOCH2
CH2–OH | CH–OH | CH2–OH
| Br
环
苯环 苯环1 苯环2 杂环1 杂环2 O 三元环 四元环 五元环 六元环 八元环 任意苯环
蒽
萘
苯磺酸
—SO3H
羰基 O C
多环化合物
三键
xx
xx
xx xx
xx
原子
xx xx
H
Hx
He
He
Li
Lix
x
C
Cx
x
N
Nx
x
xx
O xO x
xx
xx
xx
F xF
xx
xx
xx
xx
xx
Ne Ne Na Na x M g Mg
xx
Al
Alx
Si
S ix
x
P
xx
Px
x
xx
S xS x
xx
xx
Cl
xx
C lx
放映结束 感谢各位批评指导!
让我们共同进步
CH2=CH2 CH CH CH2=CH CH =CH2
乙烯 乙炔 1,3-丁二烯 环戊二烯
聚合物
聚乙烯 聚苯乙烯
CH2-CH2 n CH-CH2 n
聚1,3丁二烯 聚异戊二烯 酚醛树脂
CH2-CH=CH—CH2 n
CH2-C=CH—CH2 n CH3
OH CH2 n
衍生物
硬脂酸甘油酯
硝化甘油 CH2–ONO2 |
HOOH
H HC H
H
S CS
H Cl H I
离子晶体
Na+
-
Cl
C l -Ca2+
-
Cl
Na+ O 2N- a+
Na+ S 2-
原子
离子
原子结构示意图
+26 2 8 14 2
天平 烧杯
瓶类
集气瓶 锥形瓶 平底烧瓶 蒸馏烧瓶 圆底烧瓶 (带塞液体)
滴瓶
空滴瓶
容量瓶 洗气瓶 洗气瓶1 洗气瓶2 洗气瓶液体 储气瓶 集气装置1 集气装置2 烧瓶固体 烧瓶液体
xx
xx
Ar
xx
Ar
xx
K
Kx
C a Ca
xx
Br
B rx
xx xx
I
xx
Ix
xx xx
离子
xx
x
H+
H xNxH H
-
xOxH
xx xx
2-
OxO
H+
HO H
-
xS xH
H HC
H
OxH
3-
N
2-
O
-
F
-
I
Li+
Na+ K+ Mg2+ Ca2+
Ba2+ Al3+
分子
HH N N
F F Cl Cl Br Br I I H F
失 e-
失电子
上弯箭头 下弯箭头
高温
通电
△
电解
电炉
点燃
△
△
催化剂
充电
△
放电
催化剂
催化剂 △
浓硫酸 △
浓硫酸 170℃
催化剂 高温高压
催化剂 加热
催化剂
浓硫酸 140℃
MnO2 △
§
V2O5
△←↑→↓
500℃
苯
甲苯 —CH3 乙苯 —CH2—CH3 Br 溴苯
苯1 苯2 苯1 苯2 硝基苯 —NO2
管类
试管 胶头滴管 碱式滴定管 酸式滴定管 硬质玻璃管 硬质玻璃管加热
试管架
试管中液体 牛角管
冷凝管
漏斗
长颈漏斗 分液漏斗 球形分液漏斗 梨形分液漏斗 三角漏斗
量筒
刻度
酒精灯
铁架台
铁架台(侧面) 铁架台(正面) 铁夹 铁圈(无石棉网) 铁圈(有石棉网)
电池
Pt
Pt
电解池
G
Zn
Cu
原电池
棒、夹、塞
制乙烯
洗气瓶
硫酸铜洗气瓶
气体收集装置
排水法
向上排空气法 向下排空气法
气体发生装置
U型管制氢简易装置
制氢简易装置
制乙炔
固体干燥装置
干燥管
U型干燥管
尾气处理装置
双通管加热
水冷却装置
坐标系
Y X
坐标纸
可能用到的相对原子质量
H:1 Na:23 Mg:24 Al:27 Fe:56 K:39 Cu:64 Ag:108 C:12 O:16 S:32 Cl:35.5 Br:80
