大学有机化学总复习
大一有机化学复习

H2N-
CHO 对-醛基苯胺;对-氨基苯甲醛
HO-CH2CH2-NH2 2-氨基乙醇;2-羟基乙胺
三、有机物主要化学性质
熟悉各类有机物的主要化学性质,相互变化关系, 掌握各类化合物的鉴别方法.
四、用化学方法鉴别化合物 鉴别就是利用有机化合物化学性质之间的差异来
26、油脂的碘值大小说明; 油脂的碘值大说明油脂的C=C键多;碘值小说明油脂 的C=C键多少。
27、产生旋光性的原因: 分子有手性;或分子不对称性
28、旋光异构体数目:
分子有n个手性C原子,旋光异构体数目≤ 2n
29、消除反应
按扎依切夫规则进行,生成取代基多的烯。
例如: CH3CHOH-CH2CH3 -H2O
CH2=CH-OH
CH2=CH-C·H2
P~π共轭
22、共轭体系特点(共轭效应) 有大π键;体系稳定;外电场作用下交替极化;
23、蛋白质沉淀原理 破坏了蛋白质微粒的电荷及水化膜
24、蛋白质变性原理 破坏了蛋白质的空间结构(2~4级结构)
25、油脂的皂化值大小说明:
油脂的皂化值大说明油脂的平均分子量小;油脂 的皂化值小说明油脂的平均分子量大。
X RCOOH > RCOOH >Y RCOOH
有吸电子基
有斥电子基
例:F-CH2COOH > CH3COOH > CH3-CH2COOH;
CH3OH >CH3CH2OH >( CH3)2CHOH> (CH3)3OH ;
伯醇
仲醇
叔醇
=
6、碱性大小 NH
R4NOH 、 H2N-C-NH2(胍) > >( R2NH , RNH2 , R3N )> NH3 > Ar-NH2 > RCO-NH2(酰胺)
大学有机化学复习总结(全)-大学有机化学

大学有机化学复习总结(全)-大学有机化学有机化学是一门非常重要的学科,它涉及到许多领域,如药物研发、材料科学等。
在大学有机化学课程中,我们需要掌握许多基本概念和理论知识,以便更好地理解这门学科。
我们需要了解有机化合物的基本结构。
有机化合物由碳原子和氢原子组成,它们可以通过共价键连接在一起。
有机化合物还可以含有氧、氮、硫等元素。
在学习有机化学时,我们需要掌握不同类型的有机化合物,如烷烃、烯烃、炔烃、芳香烃等。
我们需要了解有机化学中的一些基本反应类型。
例如,加成反应是指两个或多个分子结合在一起形成一个新的分子。
消除反应是指一个分子中的一个键被破坏,同时形成两个新的键。
取代反应是指一个分子中的一个原子被另一个原子或基团所取代。
这些反应类型在有机合成中非常重要,因为它们可以帮助我们设计和构建新的有机化合物。
接下来,我们需要了解有机化学中的一些高级概念和理论。
例如,共轭体系是指一个分子中的π电子云分布在不同的平面上。
这种体系在药物研发中非常常见,因为它们可以影响药物的生物活性和稳定性。
另外,我们还需要了解一些高级的合成方法和技术,如催化反应、高通量筛选等。
我们需要进行有机化学实验来加深对这门学科的理解。
在实验中,我们可以观察到许多有趣的现象和结果,例如产物的颜色、形态等。
这些实验可以帮助我们更好地理解有机化学的理论知识,并且提高我们的实验技能。
大学有机化学是一门非常重要的学科,它涉及到许多领域。
在学习这门学科时,我们需要掌握许多基本概念和理论知识,并且进行相关的实验来加深对这门学科的理解。
希望这篇文章能够帮助你更好地理解大学有机化学这门课程。
(完整版)大学有机化学知识点总结.doc

有机化学复习总结一.有机化合物的命名1.能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH>- SO3H>- COOR>- COX>- CN>- CHO> >C= O>- OH(醇 ) >- OH(酚 ) >- SH>- NH2>- OR> C = C>- C≡C-> ( -R>- X>- NO2),并能够判断出Z/E 构型和 R/S 构型。
2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
立体结构的表示方法:COOH CH 31)伞形式: C 2)锯架式:H H OHH OHOHH3C C 2 H 5H H COOHH HH4)菲舍尔投影式:H OH 3)纽曼投影式:H H HCH 3H H H H5)构象 (conformation)(1)乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2)正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是 e 取代的椅式构象。
多取代环己烷最稳定构象是 e 取代最多或大基团处于 e 键上的椅式构象。
立体结构的标记方法1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型,在相反侧,为 E 构型。
CH 3 Cl CH 3 C 2 H 5C C C CH C 2H 5 H Cl(Z) - 3 -氯- 2 -戊烯(E) - 3 -氯- 2 -戊烯2、顺 / 反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
CH3 CH3 CH3 H CH3 CH3 H CH3C C C CH H H CH3 H H CH3 H顺- 2-丁烯反- 2-丁烯顺- 1,4-二甲基环己烷反- 1,4-二甲基环己烷3、 R/S 标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。
大学有机化学复习提纲

C*构型的确定,从离序数最小基的最远方向 看,其余3基的序数由大到小为顺时针记作‘R’, 反时针记作‘S’
4、多官能团化合物的命名 • 当化合物中含有多个官能团时,一般按下列顺
序,选取其中最优者为主体名,其余作取代基 (个别有例外)。
• 一些主要官能团按优先递减排序如下: —COOH,—SO3H,—COOR,—COCl, —CONH2,—CN,—CHO,=C=O(酮), —OH , —SH , —NH2 , ——C≡C— , —C=C—
• THF、NBS、TNT、DMSO、DMF等
二、有机化合物结构
• 1、同分异构 • 2、构象分析 • 3、结构理论
1、同分异构
• 异构体类型: 构造异构(C架、位置、官能团) 立体异构(顺反、对映)
• 异构体书写: 一般常见物质或结构较简单物质的同
分分异异构构体体等。如写分子式为C5H10、C5H12同 • 互变异构现象:酮式—烯醇式互变异构、
• 卤仿反应:
• R-CO-CH3 + NaOX (X2 + NaOH)
R-
COOH
• 酰胺重排:
• R-CONH2 +Br2 +OH— • 缩合逆反应:
R-NH2
• R2C=CH-CHO +OH—(H2O) + CH3CHO
R2C=O
• 成环反应
• 三元环:
•
碳 烯 插 入 C=C + CH2I2 + Cu-
• 羧酸衍生物的水解、醇解、氨解反应
• 重氮化反应可使芳环氨基转换成其他 原子或原子团
• 烯加水成醇,炔加水成醛酮,烯与炔 加HX或X2成卤代物、加HOX成卤代醇、 催化加氢成烷,烯硼氢化氧化水解生成 反马氏规则的醇,炔硼氢化氧化水解成 醛(酸化水解成烯)
大学有机化学归纳

有机化学复习总结一、试剂的分类与试剂的酸碱性1、自由(游离)基引发剂在自由基反应中能够产生自由基的试剂叫自由基引发剂(free radical initiator),产生自由基的过程叫链引发。
如:Cl2、Br2是自由基引发剂,此外,过氧化氢、过氧化苯甲酰、偶氮二异丁氰、过硫酸铵等也是常用的自由基引发剂。
少量的自由基引发剂就可引发反应,使反应进行下去。
2、亲电试剂简单地说,对电子具有亲合力的试剂就叫亲电试剂(electrophilic reagent)。
亲电试剂一般都是带正电荷的试剂或具有空的p轨道或d轨道,能够接受电子对的中性分子,如:H+、Cl+、Br+、RCH2+、CH3CO+、NO2+、+SO3H、SO3、BF3、AlCl3等,都是亲电试剂。
在反应过程中,能够接受电子对试剂,就是路易斯酸(Lewis acid),因此,路易斯酸就是亲电试剂或亲电试剂的催化剂。
3、亲核试剂对电子没有亲合力,但对带正电荷或部分正电荷的碳原子具有亲合力的试剂叫亲核试剂(nucleophilic reagent)。
亲核试剂一般是带负电荷的试剂或是带有未共用电子对的中性分子,如:OH-、HS-、CN-、NH2-、RCH2-、RO-、RS-、PhO-、RCOO -、X-、H2O、ROH、ROR、NH3、RNH2等,都是亲核试剂。
在反应过程中,能够给出电子对试剂,就是路易斯碱(Lewis base),因此,路易斯碱也是亲核试剂。
4、试剂的分类标准在离子型反应中,亲电试剂和亲核试剂是一对对立的矛盾。
如:CH3ONa + CH3Br→CH3OCH3 + NaBr的反应中,Na+和+CH3是亲电试剂,而CH3O-和Br-是亲核试剂。
这个反应究竟是亲反应还是亲核反应呢?一般规定,是以在反应是最先与碳原子形成共价键的试剂为判断标准。
在上述反应中,是CH3O-最先与碳原子形成共价键,CH3O-是亲核试剂,因此该反应属于亲核反应,更具体地说是亲核取代反应。
大学有机化学期末复习总结

有机化学期末复习总结一、有机化合物的命名命名是学习有机化学的“语言”,因此,要求学习者必须掌握。
有机合物的命名包括俗名、习惯命名、系统命名等方法,要求能对常见有机化合物写出正确的名称或根据名称写出结构式或构型式。
1、俗名及缩写:要求掌握一些常用俗名所代表的化合物的结构式,如:木醇、甘醇、甘油、石炭酸、蚁酸、水杨醛、水杨酸、氯仿、草酸、苦味酸、肉桂酸、苯酐、甘氨酸、丙氨酸、谷氨酸、巴豆醛、葡萄糖、果糖等。
还应熟悉一些常见的缩写及商品名称所代表的化合物,如:RNA、DNA、阿司匹林、福尔马林、尼古丁等。
2、习惯命名法:要求掌握“正、异、新”、“伯、仲、叔、季”等字头的含义及用法,掌握常见烃基的结构,如:烯丙基、丙烯基、正丙基、异丙基、异丁基、叔丁基、苄基等。
3、系统命名法:系统命名法是有机化合物命名的重点,必须熟练掌握各类化合物的命名原则。
其中烃类的命名是基础,几何异构体、光学异构体和多官能团化合物的命名是难点,应引起重视。
要牢记命名中所遵循的“次序规则”。
4、次序规则:次序规则是各种取代基按照优先顺序排列的规则(1)原子:原子序数大的排在前面,同位素质量数大的优先。
几种常见原子的优先次序为:I>Br>Cl>S>P>O>N>C>H(2)饱和基团:如果第一个原子序数相同,则比较第二个原子的原子序数,依次类推。
常见的烃基优先次序为:(CH3)3C->(CH3)2CH->CH3CH2->CH3-(3)不饱和基团:可看作是与两个或三个相同的原子相连。
不饱和烃基的优先次序为: -C≡CH>-CH=CH2>(CH3)2CH-次序规则主要应用于烷烃的系统命名和烯烃中几何异构体的命名烷烃的系统命名:如果在主链上连有几个不同的取代基,则取代基按照“次序规则”一次列出,优先基团后列出。
按照次序规则,烷基的优先次序为:叔丁基>异丁基>异丙基 >丁基>丙基>乙基>甲基。
大学有机化学复习重点总结(各种知识点

大学有机化学复习重点总结(各种知识点1、烷烃的自由基取代反应 X2的活性:F2 >Cl2 >Br2 >I2 选择性:F2 < Cl2 < Br2< I22、烯烃的亲电加成反应活性 R2C=CR2 > R2C=CHR>RCH=CHR > RCH=CH2 > CH2=CH2 > CH2=CHX3、烯烃环氧化反应活性 R2C=CR2 > R2C=CHR> RCH=CHR > RCH=CH2 > CH2=CH24、烯烃的催化加氢反应活性:CH2=CH2 >RCH=CH2 >RCH=CHR > R2C=CHR > R2C=CR2 卤代烃的亲核取代反应SN1 反应:SN2 反应:成环的SN2反应速率是:v五元环 > v六元环 > v中环,大环 > v三元环 > v四元环定位基定位效应强弱顺序:邻、对位定位基:-O->-N(CH3)2>-NH2>-OH>-OCH3>-NHCOCH3>-R >-OCOCH3>-C6H5>-F>-Cl>-Br >-I间位定位基:-+NH3>-NO2>-CN>-COOH>-SO3H>-CHO>-COCH3>-COOCH3>-CONH2 转]有机化学鉴别方法《终极版》找了很久有机化学鉴别方法的总结1烷烃与烯烃,炔烃的鉴别方法是酸性高锰酸钾溶液或溴的ccl4溶液(烃的含氧衍生物均可以使高锰酸钾褪色,只是快慢不同)2烷烃和芳香烃就不好说了,但芳香烃里,甲苯,二甲苯可以和酸性高锰酸钾溶液反应,苯就不行3另外,醇的话,显中性4酚:常温下酚可以被氧气氧化呈粉红色,而且苯酚还可以和氯化铁反应显紫色5可利用溴水区分醛糖与酮糖6醚在避光的情况下与氯或溴反应,可生成氯代醚或溴代醚。
醚在光助催化下与空气中的氧作用,生成过氧化合物。
7醌类化合物是中药中一类具有醌式结构的化学成分,主要分为苯醌,萘醌,菲醌和蒽醌四种类型,具体颜色不同反应类型较多一、各类化合物的鉴别方法1、烯烃、二烯、炔烃:(1)溴的四氯化碳溶液,红色腿去(2)高锰酸钾溶液,紫色腿去。
有机化学基础知识点总复习资料

有机化学基础知识点总复习资料有机化学是研究有机化合物及其反应的一门学科。
它是化学中非常重要的一个分支,不仅与生物化学、药物化学等领域密切相关,也在工业生产中得到广泛应用。
以下是有机化学基础知识点的总复习资料。
1. 有机化合物的结构:有机化合物是由碳元素与氢元素及其他元素组成的化合物。
碳元素的四个电子外壳能级使其能够与其他元素形成共价键,从而构成复杂的化合物结构。
有机化合物的基本结构有直链、支链、环状和立体异构等。
2. 功能团:功能团是有机化合物中特定结构的部分,可以决定化合物的性质和反应。
常见的功能团有羟基、羰基、胺基、酮基、酰基等。
不同的功能团会导致有机化合物具有不同的化学性质。
3. 同分异构体:同分异构体是指分子式相同但结构不同的有机化合物。
同分异构体的存在使得有机化合物的种类非常丰富。
常见的同分异构体有结构异构体、空间异构体和性质异构体等。
4. 有机化合物的命名:有机化合物命名有系统命名和常用命名两种方法。
系统命名是根据化合物的结构和功能团来命名,常用命名则是使用常见的化合物名来命名。
常见的命名方法包括IUPAC命名法和功能团命名法。
5. 有机化合物的物理性质:有机化合物的物理性质包括熔点、沸点、溶解度等。
这些性质受到分子间力的影响,如氢键、分子间作用力等。
不同的分子结构和功能团会导致有机化合物具有不同的物理性质。
6. 有机化合物的化学性质:有机化合物的化学性质主要表现为它们能够发生反应,并在反应中产生新的化合物。
常见的有机化学反应包括酯化、醇酸酸解、氧化还原反应等。
不同的功能团和结构会决定有机化合物的反应性质。
7. 反应机理:反应机理是研究有机化合物反应过程的重要内容。
它是通过观察反应速率、催化剂和中间体等信息,来推测反应的步骤和反应物之间的作用方式。
反应机理对于理解有机反应的本质和预测反应结果非常重要。
8. 烯烃的反应:烯烃是一类含有双键的有机化合物,它们具有丰富的反应性质。
烯烃的常见反应包括加成反应、聚合反应、环加成反应等。
大学有机化学知识点总结

大学有机化学知识点总结有机化学复总结一.有机化合物的命名1.能够用系统命名法命名各种类型化合物,包括烷烃、烯烃、炔烃、烯炔、脂环烃、芳烃、醇、酚、醚、醛、酮、羧酸、羧酸衍生物、多官能团化合物,并能够判断Z/E构型和R/S构型。
2.根据化合物的系统命名,写出相应的结构式或立体结构式,包括伞形式、锯架式、菲舍尔投影式、纽曼投影式。
立体结构的表示方法包括Z/E标记法、顺/反标记法和R/S标记法。
立体结构的标记方法1.Z/E标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z构型,在相反侧,为E构型。
2.顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
3.R/S标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。
然后将最不优先的基团放在远离观察者,再以次观察其它三个基团,如果优先顺序是顺时针,则为R构型,如果是逆时针,则为S构型。
有机化学反应及其特点有机化学反应可以分为不同的类型,包括自由基取代、自由基加成、亲电加成、亲电取代、亲核取代、离子型反应、亲核加成、消除反应、协同反应、还原反应和氧化反应。
每种类型的反应都有其特点和规律。
马氏规律是亲电加成反应的规律,即亲电试剂总是加到连氢较多的双键碳上。
过氧化效应是自由基加成反应的规律,即卤素加到连氢较多的双键碳上。
空间效应是体积较大的基团总是取代到空间位阻较小的位置。
定位规律是芳烃亲电取代反应的规律,包括邻、对位定位基和间位定位基。
查依切夫规律是卤代烃和醇消除反应的规律,主要产物是双键碳上取代基较多的烯烃。
休克尔规则是判断芳香性的规则,存在一个环状的大π键,成环原子必须共平面或接近共平面,π电子数符合4n+2规则。
霍夫曼规则是季铵盐消除反应的规律,只有烃基时,主要产物是双键碳上取代基较少的烯烃(动力学控制产物)。
当β-碳上连有吸电子基或不饱和键时,则消除的是酸性较强的氢,生成较稳定的产物(热力学控制产物)。
大学有机化学知识点总结

⼤学有机化学知识点总结有机化学复习总结⼀.有机化合物的命名1. 能够⽤系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍⽣物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。
2. 根据化合物的系统命名,写出相应的结构式或⽴体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
⽴体结构的表⽰⽅法:1)伞形式:CCOOHOHH 3 2)锯架式:CH 3OH HHOH 2H 53)纽曼投影式:H H 4)菲舍尔投影式:COOHCH 3OH H5)构象(conformation)(1) ⼄烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环⼰烷构象:最稳定构象是椅式构象。
⼀取代环⼰烷最稳定构象是e 取代的椅式构象。
多取代环⼰烷最稳定构象是e 取代最多或⼤基团处于e 键上的椅式构象。
⽴体结构的标记⽅法1. Z/E 标记法:在表⽰烯烃的构型时,如果在次序规则中两个优先的基团在同⼀侧,为Z 构型,在相反侧,为E 构型。
2、顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同⼀侧,则为顺式;在相反侧,则为反式。
3、 R/S 标记法:在标记⼿性分⼦时,先把与⼿性碳相连的四个基团按次序规则排序。
然后将最不优先的基团放在远离观察者,再以次观察其它三个基团,如果优先顺序是顺时针,则为R 构型,如果是逆时针,则为S 构型。
注:将伞状透视式与菲舍尔投影式互换的⽅法是:先按要求书写其透视式或投影式,然后分别标出其R/S 构型,如果两者构型相同,则为同⼀化合物,否则为其对映体。
大学有机化学复习总结(全)-大学有机化学

大学有机化学复习总结(全)-大学有机化学大家好,我是你们的有机化学老师,今天我要给大家讲一下大学有机化学的复习总结。
我要告诉大家一个秘密,其实有机化学并不可怕,只要你用心去学,一定会有所收获。
好了,不多说了,让我们开始吧!一、基础知识1.1 烷基和烯基烷基和烯基是有机化学的基础,它们是构成有机分子的基本单元。
烷基是由碳、氢和一个或多个氧原子组成的链状烃基,常见的烷基有甲烷、乙烷、丙烷等。
烯基是由碳、氢和一个氧原子组成的支链状烃基,常见的烯基有乙烯、丙烯等。
1.2 烃的取代反应烃的取代反应是指在烃分子中加入一个或多个原子或原子团的过程。
例如,将一个氢原子加到甲烷分子中,就可以得到甲基甲烷(CH3)。
这个过程可以用下面的方程式表示:CH3 + H2 → CH3CH21.3 羟基和胺的反应羟基和胺的反应是指羟基与胺分子中的氨基反应生成酰胺的过程。
这个反应在医药工业中有广泛的应用,例如制备青霉素等抗生素。
这个过程可以用下面的方程式表示:NH2 + OH -> NH2OHNH2OH + RCOOR' -> RCOOR' + NH3 + H2O二、官能团及其性质2.1 羧酸和酚的性质羧酸和酚都是含有羧基(-COOH)的化合物,它们的性质有很多相似之处。
例如,它们都可以发生酯化反应、酰胺化反应等。
羧酸和酚还可以通过缩合反应形成醚类化合物。
例如,苯酚可以与甲醛缩合生成环氧树脂。
2.2 醛和酮的性质醛和酮都是含有羰基(C=O)的化合物,它们的性质有很多相似之处。
例如,它们都可以发生氧化反应、还原反应等。
醛和酮还可以通过缩合反应形成高分子化合物。
例如,甲醛可以与苯酚缩合生成酚醛树脂。
三、合成路线设计3.1 基本合成路线设计方法合成路线设计是有机化学研究的核心内容之一。
基本的合成路线设计方法包括以下几个步骤:确定目标产物;选择合适的原料;设计反应条件;优化合成路线;进行实验验证。
在设计合成路线时,要充分考虑原料的来源、价格、易得性等因素。
大学有机化学知识点总结资料

有机化学复习总结一.有机化合物的命名 1. 能够用系统命名法命名各种类型化合物:,芳烃,包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),多官能团化合物(官能团优先顺序:醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺)C>-NH2OR >OH(酚)>-SH>->->>--COOH>-SO3HCOOR>-COX>-CN>-CHO>C=O>-OH(醇) R/S构型。
X>-NO2),并能够判断出Z/E构型和≡=C>-CC->(-R>-Fischer根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式, 2.。
投影式)立体结构的表示方法:CH COOH3HOH C 2)伞形式:)锯架式:1H H OHOHCH3HC52HHCOOH HHH OHH纽曼投影式:3)4)菲舍尔投影式:HHHCHHHH3H(conformation))构象5(1)乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2)正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
式构象。
多e取代的椅(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是e键上的椅式构象。
取代环己烷最稳定构象是e取代最多或大基团处于立体结构的标记方法构型,1.Z/E标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型。
在相反侧,为E ClCHCHCH5233CCCC HCHHCl52(Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;、2在相反侧,则为反式。
1CHHCHCHCH333HCHCH333CC HHHHCHHCHH33-二甲基环己烷-二甲基环己烷反-1,42反--丁烯顺-1,4-丁烯顺-2标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。
大学有机化学知识点总结

有机化学复习总结一.有机化合物的命名1. 能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。
2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
立体结构的表示方法:1)伞形式:COOHOHH 3 2)锯架式:CH 3OHHHOH 2H 53)纽曼投影式:H H 4)菲舍尔投影式:COOH3OH H5)构象(conformation)(1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是e 取代的椅 式构象。
多取代环己烷最稳定构象是e 取代最多或大基团处于e 键上的椅式构象。
立体结构的标记方法1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型,在相反侧,为E 构型。
CH 3C H C 2H 5CH 3C CH 2H 5Cl(Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯2、 顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
CH 3C CHCH 3HCH 3CCH HCH 3顺-2-丁烯反-2-丁烯333顺-1,4-二甲基环己烷反-1,4-二甲基环己烷3、 R/S 标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。
大学有机化学知识点总结教材
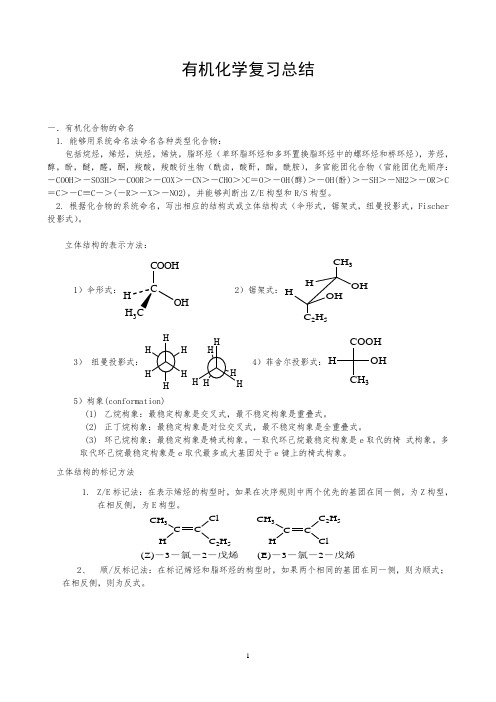
有机化学复习总结一.有机化合物的命名1. 能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。
2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
立体结构的表示方法:1)伞形式:COOHOHH 3 2)锯架式:CH 3HHOH 2H 53)纽曼投影式:H H 4)菲舍尔投影式:COOHCH 3OH H5)构象(conformation)(1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是e 取代的椅 式构象。
多取代环己烷最稳定构象是e 取代最多或大基团处于e 键上的椅式构象。
立体结构的标记方法1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型,在相反侧,为E 构型。
CH 3C H C 2H 5CH 3C CH 2H 5Cl(Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯2、 顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
CH 3C CHCH 3HCH 3CCH HCH 3顺-2-丁烯反-2-丁烯333顺-1,4-二甲基环己烷反-1,4-二甲基环己烷3、 R/S 标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。
大学有机化学期末复习总结_2

大学有机化学期末复习总结大学有机化学期末复习总结大学有机化学期末复习总结本课程的学习即将结束,现将全书的重点内容按命名、结构理论、基本反应、化合物转化及合成方法、鉴别等几个专题进行总结归纳,供同学们复习时参考。
一、有机化合物的命名命名是学习有机化学的“语言”,因此,要求学习者必须掌握。
有机合物的命名包括俗名、习惯命名、系统命名等方法,要求能对常见有机化合物写出正确的名称或根据名称写出结构式或构型式。
1、俗名及缩写要求掌握一些常用俗名所代表的化合物的结构式,如:木醇、甘醇、甘油、石炭酸、蚁酸、水杨醛、水杨酸、氯仿、草酸、苦味酸、肉桂酸、苯酐、甘氨酸、丙氨酸、谷氨酸、巴豆醛、葡萄糖、果糖等。
还应熟悉一些常见的缩写及商品名称所代表的化合物,如:RNA、DNA、阿司匹林、煤酚皂(来苏儿)、福尔马林、扑热息痛、尼古丁等。
2、习惯命名法要求掌握“正、异、新”、“伯、仲、叔、季”等字头的含义及用法,掌握常见烃基的结构,如:烯丙基、丙烯基、正丙基、异丙基、异丁基、叔丁基、苄基等。
3、系统命名法系统命名法是有机化合物命名的重点,必须熟练掌握各类化合物的命名原则。
其中烃类的命名是基础,几何异构体、光学异构体和多官能团化合物的命名是难点,应引起重视。
要牢记命名中所遵循的“次序规则”。
⑴几何异构体的命名烯烃几何异构体的命名包括顺、反和Z、E两种方法。
简单的化合物可以用顺反表示,也可以用Z、E表示。
用顺反表示时,相同的原子或基团在双键碳原子同侧的为顺式,反之为反式。
如果双键碳原子上所连四个基团都不相同时,不能用顺反表示,只能用Z、E表示。
按照“次序规则”比较两对基团的优先顺序,较优基团在双键碳原子同侧的为Z型,反之为E型。
必须注意,顺、反和Z、E是两种不同的表示方法,不存在必然的内在联系。
有的化合物可以用顺反表示,也可以用Z、E表示,顺式的不一定是Z型,反式的不一定是E型。
例如:CH3-CH2BrC=C(反式,Z型)HCH2-CH3CH3-CH2CH3C=C(反式,E型)HCH2-CH3脂环化合物也存在顺反异构体,两个取代基在环平面的同侧为顺式,反之为反式。
大学有机化学综合复习(附答案)

有机化学综合复习题集(附答案)1.写出下列反应的主要产物:2.解释下列现象:(1) 为什么乙二醇及其甲醚的沸点随分子量的增加而降低?(2)下列醇的氧化(A )比(B )快?(3) 在化合物(A )和(B )的椅式构象中,化合物(A )中的-OH 在e 键上,而化合物(B )中的-OH 却处在a 键上,为什么? 3.下列邻二醇类化合物能否用高碘酸氧化,为什么?若能,写出反应的产物。
(1).(CH 3)3CCH 2OH(2).(CH 3)2C3)OH OH+(3).OH(4).OHNaBr,H SO (5).OH(6).OH22(7).CH 3C 2H 5HOH PBr (8).OCHCH2CH3(9).33A()O (2)Zn,H 2OB(10).33125(2)H 3O 33H IO (11).OHOH22OO(A)(B)CH 2OH CH 2OHCH 2OCH 3CH 2OCH 3CH 2OCH 3CH 2OHb.p.CC(A)OH(B)OOOH3OH(1)(2)(3)(4)4.写出下列化合物在酸催化下的重排产物,并写出(1)在酸催化下的重排反应机理。
5.醋酸苯酯在AlCl 3存在下进行Fries 重排变成邻或对羟基苯乙酮:(1) 这两个产物能否用水蒸汽蒸馏分离?为什么? 为什么在低温时(25℃)以生成对位异构体为主,高温时(165℃)以生成邻位7.推测下列反应的机理:8.RCOOCAr 3型和RCOOCR 3型的酯,在酸催化水解时,由于可以生成稳定的碳正离子,可发生烷-氧键断裂。
请写出CH 3COOCPh 3在酸催化下的水解反应机理。
9.光学活性物质(Ⅰ)在酸存在下水解,生成的醇是外消旋混合物。
请用反应机理加以解释。
10.观察下列的反应系列: (1).(2).(3).C(C 6H 5)2OH OH(C 6H 5)2C C(CH 3)2OHOH OHOCOCH 3AlCl 2OHCOCH 3OHCOCH 3+(1).(2).(3).(4).OH +OH(5).OCH 2CHCH 2OC OO 3C 6H 5CH 2CH 323-C 6H 5CH 22CH 3(S)( )+( )根据反应机理,推测最终产物的构型是R 还是S ?11.(1)某化合物C 7H 13O 2Br ,不能形成肟及苯腙,其IR 谱在2850~2950cm -1有吸收峰,但3000 cm -1以上无吸收峰,在1740 cm -1有强吸收峰,δH (ppm ):1.0(3H ,三重峰),4.6(1H ,多重峰),4.2(1H ,三重峰),1.3(6H ,双峰),2.1(2H ,多重峰),推断该化合物的结构式,并指出谱图上各峰的归属。
(完整版)大学有机化学知识点总结
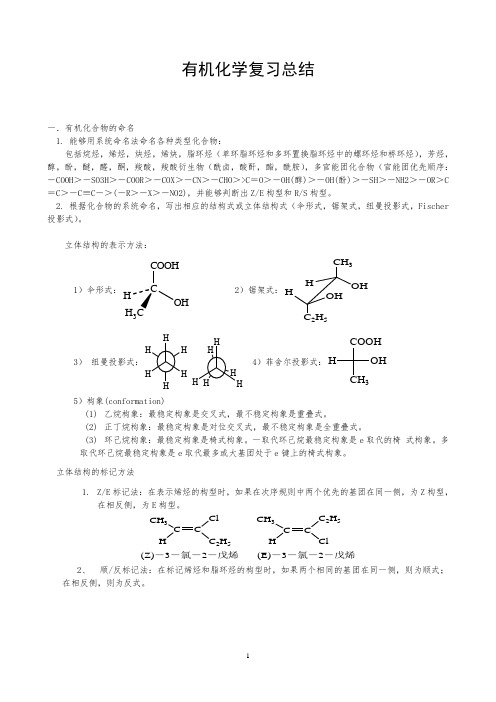
有机化学复习总结一.有机化合物的命名1. 能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。
2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
立体结构的表示方法:1)伞形式:CCOOHOHH 3 2)锯架式:CH 3OH HHOH C 2H 53)纽曼投影式:H H 4)菲舍尔投影式:COOHCH 3OH H5)构象(conformation)(1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是e 取代的椅 式构象。
多取代环己烷最稳定构象是e 取代最多或大基团处于e 键上的椅式构象。
立体结构的标记方法1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型,在相反侧,为E 构型。
CH 3C H C 2H 5CH 3C CH 2H 5Cl(Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯2、 顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
CH 3C CHCH 3HCH 3CCH HCH 3顺-2-丁烯反-2-丁烯333顺-1,4-二甲基环己烷反-1,4-二甲基环己烷3、 R/S 标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。
大学有机化学知识点总结
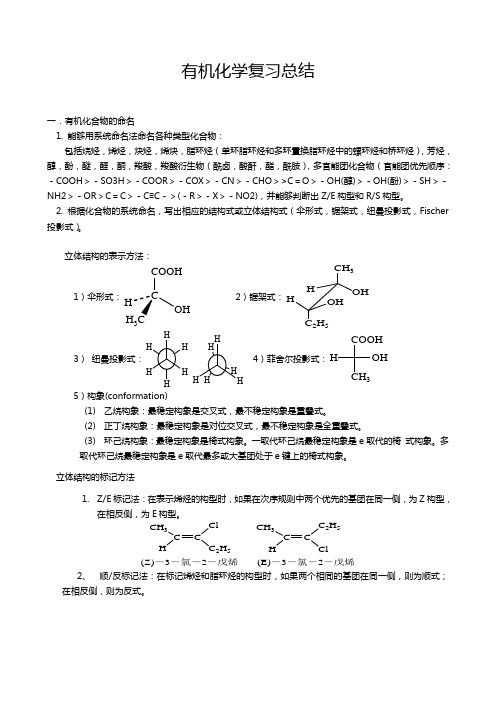
有机化学复习总结一.有机化合物的命名1. 能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C ≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。
2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
立体结构的表示方法:1)伞形式:COOHOHH 3 2)锯架式:CH 3OHHHOH C 2H 53)纽曼投影式:4)菲舍尔投影式:COOH3OH H5)构象(conformation)(1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是e 取代的椅 式构象。
多取代环己烷最稳定构象是e 取代最多或大基团处于e 键上的椅式构象。
立体结构的标记方法1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型,在相反侧,为E 构型。
CH 3CHC 2H 5CH 3CHC 2H 5Cl(Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯2、 顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
CH3C CHCH3HCH3C CHHCH3顺-2-丁烯反-2-丁烯333顺-1,4-二甲基环己烷反-1,4-二甲基环己烷3、R/S标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。
大学有机化学期末复习总结

大学有机化学期末复习总结有机化学期末复习总结一、有机化合物的命名命名是学习有机化学的“语言”,因此,要求学习者必须掌握。
有机合物的命名包括俗名、习惯命名、系统命名等方法,要求能对常见有机化合物写出正确的名称或根据名称写出结构式或构型式。
1、俗名及缩写:要求掌握一些常用俗名所代表的化合物的结构式,如:木醇、甘醇、甘油、石炭酸、蚁酸、水杨醛、水杨酸、氯仿、草酸、苦味酸、肉桂酸、苯酐、甘氨酸、丙氨酸、谷氨酸、巴豆醛、葡萄糖、果糖等。
还应熟悉一些常见的缩写及商品名称所代表的化合物,如:RNA、DNA、阿司匹林、福尔马林、尼古丁等。
2、习惯命名法:要求掌握“正、异、新”、“伯、仲、叔、季”等字头的含义及用法,掌握常见烃基的结构,如:烯丙基、丙烯基、正丙基、异丙基、异丁基、叔丁基、苄基等。
3、系统命名法:系统命名法是有机化合物命名的重点,必须熟练掌握各类化合物的命名原则。
其中烃类的命名是基础,几何异构体、光学异构体和多官能团化合物的命名是难点,应引起重视。
要牢记命名中所遵循的“次序规则”。
4、次序规则:次序规则是各种取代基按照优先顺序排列的规则(1)原子:原子序数大的排在前面,同位素质量数大的优先。
几种常见原子的优先次序为:I>Br>Cl>S>P>O>N>C>H(2)饱和基团:如果第一个原子序数相同,则比较第二个原子的原子序数,依次类推。
常见的烃基优先次序为:(CH3)3C->(CH3)2CH->CH3CH2->CH3- (3)不饱和基团:可看作是与两个或三个相同的原子相连。
不饱和烃基的优先次序为: -C≡CH>-CH=CH2>(CH3)2CH-次序规则主要应用于烷烃的系统命名和烯烃中几何异构体的命名烷烃的系统命名:如果在主链上连有几个不同的取代基,则取代基按照“次序规则”一次列出,优先基团后列出。
按照次序规则,烷基的优先次序为:叔丁基>异丁基>异丙基>丁基>丙基>乙基>甲基。
大学有机化学总复习

(一) 烷烃的同分异构现象
分子式相同而结构不同的现象。
同分异构
构造异构
碳架异构
位置异构 官能团异构 互变异构
原子的连接方式和顺 序不同
构象(键的旋转产生)
立体异构 构型 顺反异构(键的不能旋转产生)
分子中原子和基团在
旋光异构(手性产生)
空间的排布不同
1
1. 乙烷的构象
小于两个H 的 von der waals 半 径(1.2Å)之和, 有排斥力
R C
R'
R" C
H
KMnO4(浓,热), H 或 K2Cr2O7, H
R
R"
CO+OC
R'
OH
13
② 臭氧氧化 ◇ 将烯烃氧化成酮或醛
R C
R'
R" C
H
(1) O3 (2) H2O, Zn
R
R"
C O+ O C
CH3 + HBr CH3
催化加H2
BrCH2CH2CH2Br
CH3 CH3 CH C CH3
CH3 Br
属离子型加成反应,三元环较四元环容易开环。 不对称小环与HX加成时,环的破裂发生在含氢 最多和含氢最少的碳原子之间,且卤原子加到 含氢较少的碳原子上。
6
●多元取代环己烷优势构象的书写规律
◇ 取代基尽可能在e键上 ◇ 体积大的取代基尽可能在e键上 ◇ 同时要满足顺反异构和位置 例1 写出顺-1-甲基-4-异丙基环己烷的优势构象。
OCH3 H 主要产物
CH3 CH CH2 H OH 次要产物
Markovnikov规则:氢原子总是加在含氢较多的双键碳上
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(1)弱酸和它的共轭碱形成的缓冲溶液 pHpKaOlo{gc({共 c(酸轭 )/c)O /c碱 }O}
(2)弱碱和它的共轭酸(NH3∙H2O~NH4Cl) pOHpKbOlo{gc({共 c(碱轭 )/c)O /c酸 }O}
pH14pKb(B)lgc(cB (B H))
37
9. 标准溶度积
2. 复合反应 与基元反应
♥ 复合反应 :通过两个或多个反应步骤而完成的反应, 也叫非基元反应
♥ 基元反应 :复合反应的每一个反应步骤,为组成一切 化学反应的基本单元
♥ 通常确定反应机理就是确定化学反应由哪些基元反应 所组成
3
几种简单级数反应的速率方程及特征
级数
0
1
2
微分式
dcA dt
k0
范特霍夫规则 反应物浓度一定时,温度每升高 10℃,反应速率增加为原来的2~4倍。
阿仑尼乌斯公式:
Ea
k Ae RT
活化能
速率常数
指前因子
7
ln{k}lnA Ea RT
由T1、T2温度时的速率常数k1、k2,求活化能:
ln{k1}lnARETa1 ln{k2}lnARETa2 ln{k2}ln{k1}R E T a2R ET a1
ln{ {kk1 2} }E RaT 11T 12E RaTT 21 T2 T1
8
7. 活化能对反应速率的影响
阿仑尼乌斯提出:在基元反应中,只有少数能量较 高的分子直接相互作用才能发生反应。这些能量较 高的分子称为活化分子。
活化分子的平均能量与普通分子的平均能量之 差称为反应的活化能。
rH m E a (正 ) E a '(逆 )
由稳定单质生成1mol化合物时的热效应。
18
第四章 热力学第二定律 与化学反应的方向和限度
19
一、热3.奥力斯学特第瓦二德定(律W的.三Os种tw表al述d)::
1. 1850年,克劳休斯(R.Clausius): 不可能将热从低温物体传
2到. 18高51温年物,体开,尔而文不(引L起.K其elv它in变):
Q
K
O sp
25
九、多重平衡规则: ① 若反应4=反应1+反应2+反应3,则
K4Ө=K1Ө ·K2Ө ·K3Ө
②若反应4=反应1+反应2-反应3,则 K4Ө =(K1Ө ·K2Ө )/ K3Ө
③若反应3 = n反应1- m反应2,则 K3Ө =(K1Ө)n·/(K2Ө )m
26
十、 化学反应等温式
等温等压下,对于任一理想气体反应
的能量 。 功不是状态函数
6. 热力学能U
热力学能(内能)U,它是系统内部能量的总和,包 括分子运动的平动能、分子内的转动能、振动能、 电子能、核能以及各种粒子之间的相互作用位能 等。
热力学能变化只与始态、终态有关,与变化 途径无关。状态函数!
13
7. 热力学第一定律
热力学第一定律的实质是能量守恒与转
32
2. 酸碱的强弱
def
pKaOlogKaO
pK aO越 小 , 酸 性 越 强 。
pKbOdeflogKbO pK b O越 小 , 碱 性 越 强 。
3. 水的离子积常数
def
Kw O1.01014 pKpw O Ka O plK ogb O Kw O pK w O 1414
33
4. 溶液的pH值
化不。可能从单一热源吸热,使热完全转变为功 而不引起其它变化。
第二类永动机不可能造成
20
二、 熵
S称做熵, 熵是系统混乱度的量度,体系的混乱度越
低,有序性越高,熵值就越低。
熵是状态函数,单位是J·K-1。
Q
r
1850年克劳修斯提出:
T
Qr: 在状态1和状态2之间进行的任何恒温 可逆过程,系统所吸收或放出的可逆热量
10. 溶度积和溶解度之间的换算
1
s
K
O sp
nnmm
mn
cO
同一类型的电解质,K
O sp
越小,溶解度越小。不
同类型的难溶电解质,不能直接用 K
O sp
比较。
39
11. 溶度积规则
沉淀溶解反应 A n B m (s)
n A m m B n
化学反应等温式rG mrG m ORTlnQRTlnK Q sO p
总复习
1
第一章 气 体
1. 理想气体
(1)条件:高温、低压 (2)状态方程式: pV nRT
2. 分压定律和分体积定律
(1) 道尔顿分压定律 (2) 阿马格分体积定律
3. 真实气体状态方程(了解):
p
an2 V2
(V
nb)
nRT
2
第二章 化学动力学基础
1. 反应机理
也称反应历程,是化学反应实际经历的步骤
溶解 AgCl(s)
沉淀Leabharlann Ag+(aq) + Cl- (aq)
此时溶液是饱和溶液,是多相平衡。其平衡常数为:
K s O p ( A g C l) { c ( A g ) /c O } { c ( C l ) /c O }
K
O sp
称为溶度积常数,简称溶度积。它反应了物质
的溶解能力。它是温度的函数。
38
K a(H 12 C 3 ) O c (H 3 O c ( H )2 C c (H 3 ) O - 3C ) 4 .2 O 1 70
第 H 二 - 3 (C a H 步 2 O q O )( H : 3 O l ( )a C q 3 2 - (O ) a
K a( 2 H 2 C 3 ) O c (H 3 c O (H )c ( - 3 C C )3 2 - ) O O 4 .7 1 10 1
dD(g) + eE(g)
gG(g) + hH(g)
rG m rG m O RlT n [[p p ((G E ))//p pO O ]]e g [[p p ((D H ))//p p O O ]]d h
Q [p(G )/pO ]g[p(H )/pO ]h [p(B )/pO ]B
[p(E )/pO ]e[p(D )/pO ]d B
化定律。
UQW
14
8. U + pV = H ——焓,状态函数 H = H2 - H1 ——焓变 则:Qp = H 即,在定压且非体积功为零的过程中,
封闭系统从环境吸收的热等于系统焓的增 加。
吸热H 反 0,应 放热H 反 0应
15
9. 标准状态
热力学中规定:标准状态是在温度T及 标准压力p Ө(p Ө=100kPa)下的状态,简称 标准态,用右上标“Ө”表示。
rG mrG m ORlT n Q
rG m RlT n K O RlT n Q RlT n K Q O
以上二式称化学反应等温式。
27
当反应达到平衡时,rGm=0。则: rG m O RlT n [[p p e e((q G q E ) )//p p O O ] ]e g [[p p e e((q q D H ))//p p O O ]]d h
31
第五章 水溶液中的离子平衡
1. 酸碱质子理论: 凡能释放出质子(H+)的物质都是酸(质子的给予体) ; 凡是能接受质子(H+)的物质都是碱(质子的接受体)。
酸
H+ + 碱 HAc的共轭碱是Ac- ,
共轭酸碱
Ac-的共轭酸HAc。
酸较其共轭碱多一个质子。
根据质子理论,酸碱反应的实质是两个共轭酸碱对 之间质子的转移反应。
def c(H) pH log
cO
5. 一元弱酸、弱碱的解离平衡
KaOcO / c
溶液被稀释时, 增大—稀释定律
H+浓度简化计算公式 c(H)c cKaOcO
34
6. 多元弱酸、弱碱的解离平衡
第H 2 一 C 3 (O a H 步 2 O q)( H : 3 O l ( )a H q - 3 (C ) a
8. 催化剂
9
第三章 热力学第一定律与热化学
10
1. 系统和环境
系统:被研究对象。
环境:系统外与其密切相关的部分。
2. 状态和状态函数
状态:系统的宏观性质的综合表现。 状态函数:描述系统性质的物理量。(p,V,T)
特点:①状态一定,状态函数一定。 ② 状态变化,状态函数也随之而变,且 状态函数的变化值只与始态、终态 有关,而与变化途径无关。
Ka1 103 Ka2
溶液中H的 3O主要来自于第一反步应解
c(H3O)的计算可按一元解弱离酸平的衡
做近似处理。
35
7 同离子效应
在弱电解质溶液中,加入具有相同离子的强电解质, 使得弱电解质解离度降低的现象,叫同离子效应。
8. 缓冲溶液
当加入少量强酸,强碱或稀释时,保持pH值基本不 变的溶液称为缓冲溶液。它一般由弱酸和它的共轭碱 ( 如 HAc~NaAc) ; 弱 碱 和 它 的 共 轭 酸 ( 如 NH3∙H2O~NH4Cl) 组成。
T: 热源的绝对温度T
Q
②不可逆过程Q<Qr,
T
21
三、 热力学第三定律
热力学第三定律:温度趋于0K时,任何完美晶体 的熵值都等于零。
任一化学反应的标准摩尔熵变
rSm O(298. 1 5B K Sm O )(B,29)8.15K
B
四、吉布斯函数G
0 自发过程
(G)T△,p,WG'0=Δ00H-平 不 T△衡 可S态 能标 发志 生或可逆G过ib程bs等温方程
令:
K O [p e(G q)/p O ]g [p e(q H )/p O ]h [p e(q B )/p O ]B
