有机化学 第04章 苯和芳香烃
高二化学苯和芳香烃

一、苯的分子结构
二、苯的物理性质 三、苯的化学性质 四、苯的存在
• 一、定义 • 二、通式 • 三、物理性质递变规律 • 四、化学性质 • 五、同分异构体
苯的同系物 一、概念:苯的同系物:
只含有一个苯环,在组成上比苯多一个或 若干个“-CH2-”原子团的烃。 二、通式:CnH2n-6(n≥6)
⑵能使酸性高锰酸钾褪色
1ml苯
0.5mlKMnO4(H+)溶液
振荡
上层:无色
下层紫红色不褪
1ml苯 0.5ml溴水 振荡
上层橙黄色 下层几乎无色
结论:苯与酸性高锰酸钾、溴水都不反 应,由保洁家具技巧 简介 你搬家时一定要注意保护好贵重物品和家具,家具主要包括沙发、书柜、衣柜、床、钢琴、餐桌、椅子等,这些都属于大件物品,搬家时也是最难搬的,通常需要2-4人才能搬运,同时也是最易 脏的。脏了该怎么做呢?方法 用蛋清擦拭弄脏了的真皮沙发,可用一块干净的绒布蘸些蛋清擦拭,既可去除污迹,又能使皮面光亮如初。 用牙膏擦拭冰箱外壳。冰箱外壳的一般污垢,可用软布蘸少许牙膏慢慢擦拭。如果污迹较顽固,可多挤一些牙膏再用布反复擦拭。冰箱即会恢复光洁。因为牙膏中含有研磨剂,去污力非常强。 蘸牛奶擦木制家具。取一块干净的抹布在过期不能饮用的牛奶里浸一下,然后用此抹布擦抹桌子、柜子等木制家具,去污效果非常好,后再用清水擦一遍。油漆过的家具沾染了灰尘,可用湿纱布 叶渣去擦,或用冷茶水擦洗,会更加光洁明亮。 白萝卜擦料理台切开的白萝卜搭配清洁剂擦洗厨房台面,将会产生意想不到的清洁效果,也可以用切片的小黄瓜和胡萝卜代替,不过,白萝卜的效果佳。 酒精清洗毛绒沙发?毛绒布料的沙发可用毛刷蘸少许稀释的酒精扫刷一遍,再用电吹风吹干,如遇上果汁污渍,用1茶匙苏打粉与清水调匀,再用布沾上擦抹,污渍便会减退。 苹果核去油污?厨房里的水池常常有一层油污,碰巧刚吃完苹果就可用果核将油垢擦洗掉,这是因为果核中含有果胶,而果胶则具有去除油垢的作用。 用盐去地毯上的汤汁有小孩的家庭,地毯上常常滴有汤汁,千万不能用湿布去擦。应先后用洁净的干布或手巾吸干水分,然后在污渍处撒些食盐,待盐面渗入吸收后,用吸尘器将盐吸走,再用刷 毯即可。 冰块去除口香糖。有些孩子喜欢吃口香糖,不小心会弄到地毯上。粘在地毯上的口香糖很不容易取下来,可把冰决装在塑料袋中,覆盖在口香糖上,约30分钟后,手压上去感觉硬了,取上冰决, 刷就可刷下。 巧用保鲜膜这是一则懒人小妙方。在厨房临近灶上的墙面上张贴保鲜膜。由于保鲜膜容易附着的特点,加上呈透明状,肉眼不易察觉,数星期后待保鲜膜上沾满油污,只需轻轻将保鲜膜撕下,重 一层即可,丝毫不费力。对于平日忙碌的主妇们,倒不失为一个方便偷懒的好方法。 原木家具光洁法。原木家具可用水质蜡水直接喷在家具表面,再用柔软干布抹干,家具便会光洁明亮。如果发现表面有刮痕,可先涂上鱼肝油,待一天后用湿布擦拭。此外,用浓的盐水擦拭,可 朽坏,延长家具的寿命。 / 华语作文
有机化学-第六版-第04章-芳香烃

(2)加成反应
+2H2 Pt
+3H2,Pt
萘
二、蒽和菲
8 9 7 6
5 10
蒽
四氢化萘
1
4
23
十氢化萘
6
5
7
8
4 3 2 1 菲 10 9
C
D
AB
环戊烷并氢化菲
(环戊烷并多氢菲)
三、休克尔(Hückel)规则:
Aromaticity and Hückel Rules
['hʌkl]
具有共平面的离域体系的单环多烯化合物中, 若参与形成 π 键的电子数等于4n+2 (n=0,1,2,3…),此化合物就具有 芳香性。
Antibonding
Cyclooctatetraene
Bonding
8 p electrons; 3 bonding orbitals are filled; 2
nonbonding orbitals are each half-filled.
MO Diagram
1,3-Cyclopentadiene Benzene
Antibonding
Benzene
Bonding
6 p electrons fill all of the bonding orbitals. All p antibonding orbitals are empty.
p-MOs of Cyclobutadiene (Square Planar)
视频教学:苯的溴代实验
• 卤代:
Cl
+
Cl2
FeCl3 50-60oC
+ HCl
• 硝化:
NO2
+ HONO2 H2SO4
大学有机化学课件第四章 芳香烃

定条件下还是能加成的。
加氢:
加氯: 3.氧化反应 苯环侧链的氧化: 烃基苯侧链可被高锰酸钾或重铬酸钾的酸性或碱性溶液或稀硝酸所氧化,并在与苯环直接相连 的碳氢键开始,如果与苯环直接相连的碳上没有氢时,不被氧化。氧化时,不论烷基的长短,最后 都变为羧基,苯环不容易氧化。
苯环的氧化:
第四节 苯环的亲电取代定位规律 一、定位规律 1. 定位基在苯环上引入新的取代基时,其进入苯环的位置,主要决定于原有取代基的性质。这个原有 的取代基称为定位基。 2. 定位基类型 第一类:邻、对位定位基,使反应容易进行,并使新导入基主要进入苯环的邻、对位。 如:-NH2、-ph、- N(CH3)2 、-NHCOCH3 、-OH、- OCH3 第二类:间位定位基,使反应难于进行,并使新导入基进入苯环的间位。 + 如:-COOH 、-NO2 、- N(CH3)3 、-CF3 第三类:使反应较难进行,又使新基导入邻位或对位。 如:-F、- Cl、- Br 、-CH2Cl 二、定位规律的解释 1. -COOH 、-NO2 、- N(CH3)3 、-CF3等。 这类定位基与苯环直接连接的原子都具有一定的正电荷,吸引苯环上的电子,使苯环上的电子 云降低,使亲电取代反应较难进行。以硝基为例,硝基的π轨道和苯环构成π-π共轭体系,由于 氧、氮的电负性强于碳,使共轭体系的电子云移向硝基。诱导效应和共轭效应协同作用的结果,降 低了苯环的电子云密度,其中以邻、对位为甚,而间位相对来说降低的少一些。
+ 3H 2
二、近代物理方法测定苯的结构
+Q
应该 Q=120×3=360KJ/mol,而实际上苯的氢化热=208 KJ / mol,比理论值低 152 KJ / mol 。
1.近代物理方法测定苯的结构: (1)6 个碳组成一个平面正六边形,6 个氢与 6 个 碳都在同一个平面上。 (共平面性) (2)所有键角都是 120° (3)碳碳键键长为 0. 139nm. 2.轨道杂化理论: 苯环所有碳原子都是采用 SP2 杂化,每个碳原子以三个杂化轨道分别与相邻的碳原子和氢原子形成 三个σ键。每个碳原子的未参与杂化的 P 轨道都垂直于碳环的平面。相邻的两个 P 轨道彼此从侧面 重叠,形成一个封闭的共轭体系,这个封闭的共轭体称为大π键,由于π电子高度离域,从而使键 达到完全平均化。
有机化学-芳香烃

CH3
HNO3
HOAc
CH3
CH3 CH3
NO2 +
+
NO2
NO2
63% 34% 3%
Cl
Cl
Cl
Cl
HNO3
H2SO4
NO2 +
+ NO2
30%
NO2
69% 1%
(2) 第二类定位基─间位定位基
使新进入苯环的取代基主要进入它的 间位,并使苯环致钝。
例如: −CF3, −N(CH3)3+, −NO2, −CN, −SO3H, −CHO, −COCH3, −COOH, −COOCH3, −CONH2, −NH3+。
NO2
NO2
CH3 C CH3 CH3 无 α-H
KMnO4 H+
COOH
氧化剂: KMnO4 铬酸等
4.2.4 苯环上亲电取代反应的定位规则
Y
一取代苯:
芳环上的取代基既影响亲电 取代反应的速率又决定着亲电试 剂进入芳环的位置。
1. 两类定位基
芳环上的取代基分为两类:
(1)第一类定位基 ─ 邻、对位定位基 使得新进入苯环的取代基主要进入它的
均化,闭合共轭
苯
苯的分子结构 体系(环状大π键)
6 个C–C σ键: sp2–sp2相互交盖,6 个C –H σ键: sp2–1s 相互交盖。 6 个2p 轨道的对称轴垂直于环所在平面, 彼此相互平行,两侧进行侧面交盖,形成闭合的π轨道。 6个π电子离域在六个C原子上。由此形成一个闭合的
共轭体系。
2. 苯的构性相关分析
CH3
CH3
CH3
CH3
1,2-二甲苯 邻二甲苯 o-二甲苯
有机化学第四篇芳香烃
第四章芳香烃芳烃,也叫芳香烃,一般是指分子中含苯环结构的碳氢化合物。
现代芳烃的概念是指具有芳香性的一类环状化合物,它们不必然具有香味,也不必然含有苯环结构。
分类:芳香烃按照分子中是不是含有苯环,可分为苯系芳烃和非苯系芳烃。
苯系芳烃按所含苯环的数量和结合方式分为单环芳烃、稠环芳烃和多环芳烃。
1.单环芳烃:指分子中仅含一个苯环的芳烃,包括苯、苯的同系物和苯基取代的不饱和烃。
例如:CH3CH2CH3CH=CH2苯甲苯乙苯苯乙烯2.多环芳烃:指分子中含两个或两个以上苯环的芳烃,多环芳烃按照分子中苯环的连接方式不同分为多苯代脂肪烃,联苯烃和稠环芳烃(1)多苯代脂肪烃:能够看做脂肪烃分子中两个或两个以上氢原子被苯基取代的化合物。
CH2HC CH二苯甲烷1,2-二苯乙烯(1)联苯烃:指两个或两个以上苯环别离以单键相连而成的多环芳烃例如:联苯1,4-三联苯(2)稠环芳烃:两个或两个以上苯环彼此共用两个碳原子而成的多环芳烃,例如:萘蒽菲3.非苯芳烃:指分子中不含苯环的芳香烃,例如:环戊二烯负离子环庚三烯正离子第一节单环芳烃一,单环芳烃的异构现象和命名苯是最简单的单环芳烃。
单环芳烃包括苯、苯的同系物和苯基取代的不饱和烃。
1.异构现象(1)烃基苯有烃基的异构例如:CH2CH2CH3CHCH3CH3(2)二烃基苯有三种位置异构例如:RR'RRR'R'(3)三取代苯有三种位置异构例如: R R'RRR''R''R''R'R'2. 命名(1)苯基的概念芳烃分子去掉一个氢原子所剩下的基团称为芳基(Aryl)用Ar 表示。
重要的芳基有:CH 2(C 6H 5CH 2-)苄基(苯甲基),用Bz 表示苯基, 用Ph 或 表示ф(2)一元取代苯的命名a 当苯环上连的是烷基(R-),-NO 2,-X 等基团时,则以苯环为母体,叫做某基苯。
例如:CH CH 33NO 2Cl异丙基苯叔丁基苯硝基苯氯苯b 当苯环上连有-COOH ,-SO 3H ,-NH 2,-OH ,-CHO ,-CH=CH 2或R 较复杂时,则把苯环作为取代基。
有机化学41

第四章 芳 香 烃Ⅰ 学习要求1. 熟练掌握用系统命名法命名芳香烃和芳香族化合物。
2. 掌握和熟练应用芳环的亲电取代反应及侧链氧化反应。
3. 了解亲电取代反应的影响因素,熟练应用亲电取代反应定位规律判断反应的主要产物,芳环的化学活性和确定合成路线。
4. 了解芳香性的概念,掌握休克尔规则,熟练应用休克尔规则判断环状共轭烯烃有无芳香性。
Ⅱ 内容提要一.苯的结构与芳香性1.苯的分子式为C 6H 6,有较大的不饱和性。
苯分子中每个碳原子以sp 2杂化轨道与相邻的两个碳原子组成碳碳σ键,与一个氢原子组成碳氢σ键,六个碳原子和六个氢原子都在同一平面内,构成平面六边形。
六个碳原子上各自未杂化的含有单电子的且垂直于环平面p 轨道,相互轴向平行重叠形成闭合的离域大π键。
2.苯分子中碳碳键长完全平均化,形成的完全离域的闭合共轭体系,其离域能为150kJ ·mol ﹣1,使得苯环具有很好的热力学稳定性。
在通常的反应条件下,苯环的结构保持不变,不易被氧化,不易被加成,较易于发生苯环上的取代反应。
3.苯环上具有较多的π电子且具有较大的可极化性,可与缺电子的亲电试剂作用,发生亲电取代反应。
苯环上连有供电子基(致活基团)时,亲电取代反应活性增加,主要产物为邻、对位取代产物;苯环上连有吸电子基(致钝基团)时,亲电取代反应的活性降低,主要产物为间位取代产物。
4.苯分子的特定结构及特殊性质称为芳香性,芳香性是芳香烃化合物的共性,其他芳环具有和苯环相似的化学性质。
如果符合以下两点条件,则该体系具有芳香性:①具有平面环状的闭合共轭体系。
②该闭合共轭体系中离域的π电子数等于(4n + 2)个(n = 0,1,2,3…。
一般n ≤6)。
这就是休克尔(Hückel)规则。
二.芳烃的化学性质1.苯环上的亲电取代反应FeX 3NO 2S O 3H X AlCl 3R (RCO)2AlCl 3COR+ X 2+ 浓HNO + 浓H 2SO + R X+ RC OX卤代反应,反应不可逆,通常用Cl 2,Br 2。
有机化学:第四章芳香烃

治学善质疑,心灵悟真谛
2.稠环芳香烃 分子中无独立苯环,两个或多个苯环稠合。
C C
萘
C
C
C
C
蒽
C
C
C
C
菲
马敬中 华中农业大学理学院
治学善质疑,心灵悟真谛
二、单环芳烃的构造异构和命名
1.苯的同系列,通式是CnH2n-6(4个不饱和度) 具有侧连异构和位置异构。
CH2CH2CH3
H3C
CH3
CH
CH2CH3
马敬中 华中农业大学理学院
治学善质疑,心灵悟真谛
2)付-克烃基化反应的重排
卤代烷具有三个碳以上时,常产生重排产物。
H3C Cl
AlCl 3
CH3
+
CH3
CH3
重排由不稳定碳正离子中间体稳定性引起。
H
CH3 CH CH2
重排
CH3 CH CH3
马敬中 华中农业大学理学院
治学善质疑,心灵悟真谛
没有更稳定的离子中间体产生,就没有重排产物。
5)卤代苯亲电取代生成邻对位两种产物
Br
HNO 3
H2SO 4
Cl Cl Br
FeCl 3
Br H2SO 4
+ Br Br NO 2
+ Br Br Cl
+ Br Br SO 3H
NO 2 Cl SO 3H
马敬中 华中农业大学理学院
治学善质疑,心灵悟真谛
6)硝基苯亲电取代只生成一种间位产物
NO 2
NO 2
HNO 3 H2SO 4
NO 2
Cl Cl FeCl 3
O2N
NO 2 Cl
NO 2
苯和芳香烃(比武课件)

随着人们对石油和化学品的需求越来越大,对苯和芳香烃的研究也越来越深入。现在,它们 已经成为现代工业的重要组成部分。
苯的结构和性质
苯的分子结构
苯环由六个碳原子和六个氢原 子组成。这个结构始终保持着 共面,具有高度稳定性。
物理性质
苯是一种无色透明液体,带有 类似于香味的气味。它可以溶 于许多有机溶剂,例如酒精和 乙醚。
结论
1 重要性和未来发展
芳香烃是许多重要化学品的基础,它们在人类日常生活中发挥着至关重要的作用。为了 更好地利用化学产业的优势,我们需要更进一步的研究和发展。
2 影响
虽然芳香烃对人类生活和环境产生了很多积极影响,但它们也会对环境产生一定程度的 影响,并且需要妥善处理。
芳香烃的合成和应用
合成方法
芳香烃可以通过多种途径合成, 包括加氢、缩合、取代等反应。 通常,它们从石油或天然气中 提炼和合成。
应用领域
芳香烃广泛应用于医药、日常 化学品、材料科学、塑料制造、 日用香水等领域。
人工合成和天然芳香烃 的比较
天然芳香烃通常用于医疗和天 然香料方面,而人工合成的芳 香烃更多用于化工、塑料和其 它工业领域。
化学性质
苯是一种很稳定的分子,但它 可以发生芳香性亲电取代反应、 芳香性负离子反应等多种反应。
芳香烃的命名和结构
1
命名规则
芳香烃的命名原则主要是基于其分子的结构和对应的化学官能团。
2
典型的芳香烃结构
许多天然和人工合成的芳香烃都包括苯环,例如萘和苯并芘。
3
结构和构象
芳香烃的分子由苯环和其他取代基、环和链组成。它们可以有不同的三维空间构 象。
苯和芳香烃
苯和芳香烃是许多化学品的基础,从塑料到医药,从水果到芳香香水都有应 用。这个比武课件将会探讨它们的结构、性质、合成和应用。
有机化学第四章 芳香烃

1 价键理论
此时每个碳原子上剩有一 H 个未参与杂化 参与杂化的 轨道, 个未 参与杂化 的 p 轨道 , H120° 其对称轴垂直碳环所在 平面,并彼此平行,于 两侧相互交盖重叠,形 H H 成一个闭合的π 成一个闭合的 π键 , 这样 处于该 π 键中的 π 电子能 高度离域, 够 高度离域 , 使 π 电子云 完全平均化。分子整体 能量降低,分子稳定。 能量降低,分子稳定。
CH3
CH3 甲苯
CH2CH3 乙苯
CH2CH2CH2CH3
CH3
CH3
CH3CH2
对二甲苯
邻甲乙苯
13
苯同系物的命名
• 3 苯环上连有三个相同基团时,用连、偏、均来 表示相对位置。 表示相对位置。 • 要求必须是三个相同基团才能用连、偏、均来表 才能用连 示此三基团的相对位置。
CH3 CH3 CH3
H H
0.110nm
0.140nm
8
• 由于苯形成了一个环状π键,使6个碳-碳键、6 个碳-氢键都相同,其碳-碳键较烷烃中短,比 烯烃中碳-碳双键长,导致其性质与烷烃、烯烃 都有较大区别,苯的这种难加成、难氧化、易取 难加成、难氧化、 代的性质,就被称为芳香性。 现在一般用
表示苯,以示苯中 个碳 个碳- 表示苯,以示苯中6个碳-碳键并无
3 芳烃衍生物的命名
当苯环上连有-OH、-CHO、-COOH、- 当苯环上连有-OH、-CHO、-COOH、- 、-CHO、-COOH 、-NO 、-SO 、-X NH2、-NO2、-SO3H、-X等基团时我们又该 如何命名这样的化合物呢? 如何命名这样的化合物呢? 首先仍然是选择一个母体。 首先仍然是选择一个母体。 一般我们按一定的次序选择一个最优先的基团 选择一个最优先的基团, 一般我们按一定的次序选择一个最优先的基团, 并将它与苯一起作为一个完整的母体。 并将它与苯一起作为一个完整的母体。其它都作 为取代基来看。 为取代基来看。 这一次序我们称为“ 优先次序 ”,它与在烯烃一 完全没有任何关系。 章中介绍的“ 次序规则 ”完全没有任何关系。 一些常见基团的优先次序如下: 一些常见基团的优先次序如下:
芳香烃-有机化学

单环芳烃的物理性质
相对密度
单环芳烃的相对密度小于 1,但比同碳数的 脂肪烃和脂环烃大,一般在 0.86~0.9。
单环芳烃的物理性质
沸点
苯的同系物中每增加一个 -CH2-单位,沸点 平均增高约25℃。如苯、甲苯、乙苯、正丙 苯和正丁苯的沸点分别为80.1℃、110.6℃, 130℃,159.2℃ 和 183℃。含同碳数的各 种异构体的沸点很接近,如邻、间和对二甲 苯的沸点分别为 144.4℃,139.1℃ 和 138.2℃ 。
长0.140nm(0.154/0.137)。如何解释呢? 杂化轨道理论: 碳 sp2杂化和共轭大π键
H H
120 。
0.108nm H
sp2
H
H 0.140nm
H
6个P电子高度离域
π
6 6
电子环流 效应,没 有头和尾
强调离 域
苯的6个碳碳键完全相同,无单双 键的区别,苯结构式另一写法:
结构特征:
四 单环芳烃的化学性质
苯环上电子云密度高, 易被亲电试剂进攻,泳衣 品牌发生亲电取代反应。 而烯烃易进行的是亲电加 成。 苯环的特殊结构——环状的共轭大π键,决定 了苯环的特殊稳定性——芳香性——易于亲电 取代,不易加成、氧化。
1、亲电取代反应
硝化反应
浓H2SO4的作用——促使NO2 +离子(硝基正离子)的生成
第四章 芳 香 烃
芳香的含义? • 通常把苯及其衍生物总称为芳香族化合物。
过去:天然产物中许多物质有芳香气味,分子中都含有苯环。 • 芳香族碳氢化合物简称芳香烃或芳烃,一般指分子中 含有苯环结构的烃,通式符合C 现在:是指有芳香性的化合物。 nH2n-6(n≥6)。 • 另外还有符合休克尔规则的非苯芳烃。
《有机化学(第二版)》第4章:芳香烃

C2H5
19:46
傅-克反应
① 烷基化反应
+ C2H5Br
AlCl3
+ HBr
76%
19:46
傅-克烷基化反应历程
.. CH3CH2—Cl: + AlCl3 C2H5-Cl -AlCl3 ..
CH3CH2+ + AlCl4ˉ H + CH3CH2
α:1、4、5、8—电子云密度次之 β:2、3、6、7—电子云密度最低 γ:9、10—电子云密度最高
19:46
9.10—位电子云密度最高,反应活性最强。
O HNO3
O
O + O O O O O
19:46
3.菲(C14H10)
10 1 2 3 4 5 6 9 8 7
菲的化学性质与蒽相似,反 应主要发生在9、10位。
苯与亲电试剂 E+作用时,生成π- 络合物,
从苯环的π- 体系获得两个π电子,与苯环的
一个碳原子形成σ- 络合物,σ- 络合物不稳 定,容易失去一个质子,重新形成六个π电 子离域的闭合共轭体系。
19:46
2.亲电取代反应
(1) 卤代反应 卤 素:Cl2 、Br2 催化剂:Fe 、 FeX3
CH CH2
②不论有多少支链,氧化都在原支链位置上生成苯甲酸 ③叔丁苯不含α-H的抗氧化能力强,不易被氧化。 苯环在氧化剂 V2O5存在下可被氧化
V2O5
400~500℃
2
CH—C CH—C
O
+ 9O2
O + 4CO2 + 4H2O
O
顺丁烯二酸酐
苯和芳香烃中小学PPT教学课件

○ 56__________,从“ ○ 57__________”到○ 58____________、从5○9
__________到 6○0 __________,从“ ○ 61 __________”到 ○ 62
__________,从○ 63__________到6○4 __________,代表着农业生产
二、产业活动中的地域联系
1.产业活动的地域联系包括⑯__________联系、⑰
________联系、⑱__________联系等联系方式。
2.商贸联系可分为一国范围内的⑲__________和国与国之
间的⑳__________。由于存在2○1__________、○ 22__________和2○3
答案:B
考点2 产业活动中的地域联系 1.产业活动中的地域联系
2.生产协作的基本类型
3.商贸联系的发展、分类以及与物流业 的关系
针对训练2 下列关于工业联系的叙述,正确 的是( )
①为汽车厂生产各种零部件的工厂间存在着 生产联系
②绝大多数产品从原料开始的全部加工过程 是在一个工厂里独立完成的
注意实验:石油的分馏
第一节 产业活动的区位条件和 地域系及农业区位因素与农业地域
类型
考纲点击
1.了解不同产业活动的区位条件的差异,理 解自然条件对农业、工业以及商业和服务业等经 济活动的影响的表现。
2.了解产业活动中地域联系的形式及其特点。
3.通过活动和案例,说明自然、社会经济因 素及其发展变化对农业区位的影响。
针对训练3 “下表是中美两国的两个苹果 产区与北半球苹果生长最适宜区的气候条件和生 产成本的相关资料。”据表回答问题。
力的要求是不同 的。一些农业生 产对劳动力的数 量需求大,而有 的对劳动力的素
有机化学 第4章芳香烃

卤代反应
NO2
SO 3 H
R
酰基化 反应* 反应
硝化反应
磺化反应
烷基化反应
1.卤代反应 1.卤代反应
+ Br 2 Fe 或 FeBr 3 Br + HBr
卤代反应机制: 卤代反应机制: (1)产生亲电试剂Br+: 产生亲电试剂Br
Fe + Br2 FeBr 3 + Br2 FeBr 3 Br + FeBr 4
4. 烷基化反应
H + CH 3CH2 Cl
无水AlC l 3
25 ℃
CH 2 CH 3 + HCl
此反应又称付瑞德尔-克拉夫茨 此反应又称付瑞德尔-克拉夫茨(Friedel付瑞德尔 Crafts)烷基化反应,简称“付-克”烷基化反应。 烷基化反应,简称“ 烷基化反应 烷基化反应。 在“付-克”烷基化反应中,当烷基大于2 烷基化反应中,当烷基大于2 个碳原子时,则发生碳链异构化作用。例如: 个碳原子时,则发生碳链异构化作用。例如:
CH3 + HNO 3
H2 SO 4 30℃ ℃
CH3 NO2
CH3
CH3
+
NO2
+
NO 2
(59%) %
(37%) %
(4%)
硝基苯硝化时,须提高温度, 硝基苯硝化时,须提高温度,并增加硝酸的浓 主产物为间-二硝基苯。 度,主产物为间-二硝基苯。
NO2 + HNO 3
H2 SO 4 95~100℃ ℃
1. 一烷基苯 一烷基苯命名时,多以苯为母体, 一烷基苯命名时,多以苯为母体,烷基为取 代基,称为“某苯” 例如: 代基,称为“某苯”。例如:
高中化学有机化学-苯-芳香烃

苯芳香烃一、苯的物理性质苯是无色有特殊气味的液体,密度比水小,不溶于水,苯的沸点80.1C(易挥发),熔点5.5C (结冰,无色晶体),有毒二.苯的分子结构1.分子式C6H6苯是不饱和烃。
2.苯的结构凯库勒式:苯分子是平面正六边形结构,平面形分子,12个原子共平面。
各个键的键角都是120°。
因为苯不能使酸性高锰酸钾溶液褪色,苯与溴水混合不加成。
结论:苯与一般的不饱和烃在性质上有很大的差异,苯分子中的碳碳键是介于碳碳单键与碳碳双键之间的独特的键。
用下式表示更好:既有烷烃的性质又有不饱和烃的性质3.芳香族化合物芳香族化合物:分子里含有一个或多个苯环的化合物属于芳香族化合物。
芳香烃:分子里含有一个或多个苯环的烃,苯是最简单的芳香烃。
苯的同系物:分子里含有一个苯环,侧链是烷基的烃。
三、苯的化学性质和用途易于取代,难于加成。
㈠、取代反应:①卤代用的是液溴,不是溴水,铁粉的作用:催化(真正的催化剂是FeBr3),将反应的混合物倒入水中的现象是什么?[有红褐色的油状液体沉于水底,表面有油状苯,还有红色溴]。
溴苯的物理性质如何?[比水重,不溶于水,油状]。
如何除去溴苯中的溴?[水洗,再用10%烧碱溶液洗,再干燥,蒸馏]②苯的硝化反应条件:混酸,水浴温度:50-60C;浓硫酸的作用:催化剂,吸水剂;倒入水中,硝基苯的物质性质如何?硝基苯——无色油状液体,不溶于水比水重,毒性。
③磺化反应苯磺酸:中强酸。
㈡苯的加成反应苯分子的碳碳键不是典型的双键,不容易发生加成反应,在特定条件下也能发生加成反应,注意发生加成反应的条件(1)加氢+ 3H2→环己烷(2)加氯+3Cl2→C6H6Cl6㈢、苯的氧化反应2C6H6+ 15O2→12CO2+ 6 H2O 现象:火焰明亮,有黑烟,含C% = 92.3%遇到酸性高锰酸钾四、苯的同系物1. C7H8、C8H10、C9H12用—CH3取代苯分子中的H原子,得到的分子其分子式是C7H8,其结构式是用—CH2CH3取代,得到的分子其分子式是C8H10,其结构式是,乙苯C8H10有几种同分异构体?含有苯环的同分异构体有4种:1+3用—C3H7取代,得到的分子其分子式是C9H12,其结构式是C9H12有几种同分异构体?含有苯环的同分异构体有:2+3+3它们都是苯的同系物,苯的同系物的通式是C n H2n-6。
汪小兰有机化学第四章芳香烃

有机
芳烃的分类
二. 来源 1. 煤焦油中提取
炼焦时将煤干馏得焦炭及副产品煤焦油,煤 焦油组成十分复杂,含有大量的芳香族化合物, 通过分馏可得到多种芳香族化合物:
煤焦油分馏产物
馏分 轻油 酚油 萘油 重油 蒽油 沥青
➢不能解释苯为什么表现出难加成、易 取代的化学特性;
➢不能解释苯的几何结构
苯结构的近代概念
碳原子都是sp2杂 化
六个碳原子和六个 氢原子都在同一平 面上
六个碳原子组成一 个正六边形
碳碳键长完全相等 (0.140nm)
所有键角都是120º
H H
H
H H
H
现代杂化理论: SP2杂化,大键(离域),共 轭体系,离域能为150kj/mol, 而一般有机反 应有机活化化学能反仅应60的~8活0k化j/能mo,l,故由破于坏共共轭轭能体远系大的亲于 电加成与氧化反应均很难。
说起苯的六碳环结构, 人们自然都会想
起凯库勒(德1829-1896)著名的仲夏夜之梦,
他通过梦的启迪而认识到苯的环状结构, 并被
公认为发现苯环结构的鼻祖。事实上, 奥地利
一位中学教师洛斯密德(Loschmidt 1821-
1895)在1861年出版的<<化学研究>>中就
提出了包括苯环在内的与现代分子模型相近
苯环结构的稳定性亦可用其氢化热数据来 进一步证明: 环己烯/环己二烯/苯分别加氢, 产物都是环己烷, 氢化热数据分别为: 119.7/-213.5/208.4kj/mol( 苯 氢 化 热 远 小 于 环己烯氢化热的三倍, 其差值150即是共轭能, 同样环己二烯氢化热亦能反映这种共轭效应) 。
《苯与芳香烃》课件

芳香烃的密度通常较小,介于0.75-0.95 g/cm³之 间。
不同的芳香烃具有不同的沸点,范围从80°C到 400°C。
芳香烃在非极性溶剂中溶解度较好,但在水中几 乎不溶。
芳香烃的化学性质
1
取代反应
2
芳香烃中的氢原子可以被其他官能团或
原子(如卤素)取代。
3
燃烧反应
芳香烃可以燃烧,释放出大量的热能和 二氧化碳。
煤焦油蒸馏
一些芳香烃可以通过煤焦油的蒸馏分离得到。
苯和芳香烃的应用
苯的应用
芳香烃的应用
• 苯是重要的溶剂,广泛用于化学工业。 • 苯与其他化合物反应,可制备各种有机化合物。 • 苯用作食品和香水中的香精。
• 芳香烃可以作为化学原料制造塑料、橡胶和 涂料等产品。
• 某些芳香烃具有药用价值,用于制造药物。 • 芳香烃可以用作香料和香氛产品。
2 环境监测
建立芳香烃污染的环境监 测网络,及时发现和控制 污染源。
3 法律法规
制定和执行相关的法律法 规,对芳香烃的排放和使 用进行限制和监管。
苯和芳香烃的检测方法
实验室分析
使用色谱、质谱和光谱等仪器对苯和芳香烃进行定 量检测。
气体检测仪器
使用气体检测仪器对苯和芳香烃的浓度进行实时监 测。
《苯与芳香烃》PPT课件
苯和芳香烃是有机化学中重要的化合物。本课件将介绍苯和芳香烃的结构、 性质、生产方法、应用以及与环境和健康相关的风险。
什么是苯和芳香烃
苯
苯是一种具有特殊化学性质的芳香烃,由六个碳原子和六个氢原子组成的环状化合物。
芳香烃
芳香烃是一类含有苯环或苯类结构的有机化合物,具有持久的香气和稳定的结构。
有机化学 第四章 芳香烃
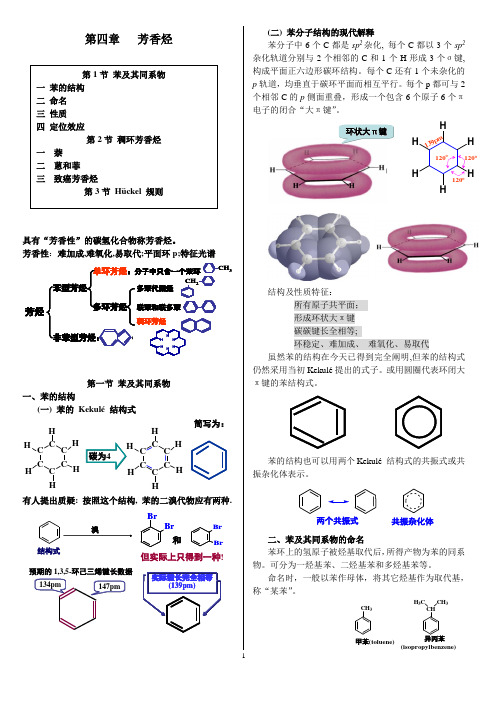
第四章 芳香烃具有“芳香性”的碳氢化合物称芳香烃。
芳香性:难加成,难氧化,易取代;平面环p;特征光谱单环芳烃苯型芳烃多环芳烃非苯型芳烃芳烃3第一节 苯及其同系物一、苯的结构(一) 苯的 Kekulé 结构式简写为:H HH HHHH H碳为4有人提出质疑: 按照这个结构, 苯的二溴代物应有两种.结构式溴BrBrBr Br和但实际上只得到一种!预期的1,3,5-环己三烯键长数据134pm147pm(二) 苯分子结构的现代解释苯分子中6个C 都是sp 2杂化, 每个C 都以3个sp 2杂化轨道分别与2个相邻的C 和1个H 形成3个σ键,构成平面正六边形碳环结构。
每个C 还有1个未杂化的p 轨道,均垂直于碳环平面而相互平行。
每个p 都可与2个相邻C 的p 侧面重叠,形成一个包含6个原子6个π电子的闭合“大π键”。
o结构及性质特征:所有原子共平面; 形成环状大π键 碳碳键长全相等;环稳定、难加成、 难氧化、易取代虽然苯的结构在今天已得到完全阐明,但苯的结构式仍然采用当初Kekulé提出的式子。
或用圆圈代表环闭大π键的苯结构式。
苯的结构也可以用两个Kekulé 结构式的共振式或共振杂化体表示。
个共振式共振杂化体二、苯及其同系物的命名苯环上的氢原子被烃基取代后,所得产物为苯的同系物。
可分为一烃基苯、二烃基苯和多烃基苯等。
命名时,一般以苯作母体,将其它烃基作为取代基,称“某苯”。
3H 3C 3甲苯(toluene) 异丙苯(isopropylbenzene)二烃基苯有三种异构体,用邻或1,2-;间或1,3-;对或 1,4- 表示;间-二甲苯1,3-二甲苯m -二甲苯m -xylene对-二甲苯1,4-二甲苯p -二甲苯p -xylene 邻-二甲苯1,2-二甲苯o -二甲苯o -xylene CH 3CH 3CH 3CH 3CH 33具有三个相同烃基的取代苯也有三种异构体。
如:连-三甲苯1,2,3-三甲苯偏-三甲苯1,2,4-三甲苯均-三甲苯1,3,5-三甲苯CH 3CH 3CH 3CH 3CH 33CH 3H 3CCH 3(1,2,3-trimethylbenzene)若苯环上连接不同的烷基时,烷基名称的排列顺序按“优先基团”后列出的原则,其位置的编号应将简单的烷基所连的碳原子定为1-位,并以位号总和最小为原则来命名。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
为什么卤素是邻对位定位基却是致钝的基团?
Cl
虽然p-π共轭效应使苯环 上电子密度有所增高(如右 图),但由于卤素的电负性 较强,总的效应是使苯环上 电子密度降低。因此,卤素 对苯环在亲电取代反应中有 致钝作用。
pπ
八. 稠环芳烃
1. 萘 (C10H8)
142.1
1)结构
136.3pm
142.3
141.8
C60F18
水溶性的C60聚合物
将C60转化为水溶性是研究球碳化学的一个重要战略方向。 最近,韩国人通过如图的方式用环糊精包裹 C60的二胺侧链使 聚合物水溶化获得成功。有人期望此成果会加快C60作为药物 分子胶囊的开发,或者可以设计成分子马达或其他超分子器 件。
我国科学家“拍摄”首张C60化学键图 象
第四章 环烃
Ⅱ. 苯和芳香烃
第四章 环烃
Ⅱ. 苯和芳香烃
苯型芳香烃 例: 芳香烃 非苯型芳香烃 例: O
+
...
...
一. 芳香烃的分类和命名
1. 单环芳烃 之一取代苯
1) 苯为母体 2)苯为取代基
CH3
NO2
CH(CH3)2
COOH
NH2
OH
甲苯
硝基苯
异丙苯
苯甲酸
苯胺
苯酚
2. 单环芳烃 之二取代苯
-NR2 _NHR _ R _Ar; _X
_
NH2
_
OH;
_
NHCOR
_
OCOR;
(1) 含有未共用电子对的原子与芳环成键,形成大键 ; (2) 含有电子的基团; (3) 可通过诱导效应或超共轭效应产生给电子效应的烷基等。
Ⅱ类 间位定位基——致钝的定位基。
NR3 __ CHO
__+ __
__
NO2
__
CF3
__
CCl3
__
CN
__
SO3H
__
CR O
COOH
__
COOR
(1) 与苯环相连的原子有极性双键; (2) 与苯环相连的是带正点荷的原子或强的吸电子基。
二取代苯的定位效应
1)原有取代基定位效应一致,第三个取代基进入它们共同确 定的位置。
CH3 (>99%)
COOH
COOH Br
NO2
(100%)
H2SO4 (95%)
NO2(deact.) [O]
NO2 COOH COOH
NH2(act.) COOH [O] COOH
③还原反应
Na, lig.NH3 ROH
Birch还原
1,4-二氢萘
2.蒽和菲 (C14H10)
3 8 7 6 5 10 4
9
1 2 6 3 7
5
4
2 1 10
环闭共轭体系(大键);
1)两基团相同
2)两基团不同
OH
有三种异构体:邻(o)、间(m)、对(p)
一个加苯环作母体,另一个作取代基
CH3 CHO NH2
Cl SO3H
间氯苯酚
对甲苯磺酸
邻氨基苯甲醛
3. 多环芳烃
1)多苯代 脂肪烃 2) 联 苯
5
CH=CH
CH
1,2-二苯乙烯
6'
1 1'
三苯甲烷
6 5 4 2 3
6
5'
4'
+ HCl
可用于制备芳香酮、双官能团化合物或直链取代烷基苯。 反应的局限性是 芳环上有吸电子基如: 硝基、羰基等不发生傅克酰化反应。
5. 烷基苯的侧链氧化
CH3 KMnO4 COOH CH2CH2CH3 [O] COOH
有H的烷基苯,都氧化成苯甲酸。 6. 烷基侧链的卤代
CH2CH3 Br2 CH-CH3 Br
休克尔(Hü ckel)规则
环闭的共轭体系,共轭体系中成环的原子处于同一平面,
其 电子数为4n+2时(n=0,1,2,3...整数),具有芳香性。
6 1
10 2
14 3
14 电子数 3 n
1. 卤代反应
+ Br2 FeBr3 Br + HBr
2. 硝化反应
+ 浓HNO3 浓H2SO4 ~55 C
C60
C70
波意耳(Boyel) 怀疑派化学家 1661年 确立元素概念.
新的巴基球家族
它们是不是 碳的同素异 形体?
会发光的巴基球
纯粹的C60分子以及它 的许多衍生物会猝灭 光子。然而,美国加 州大学最近在C60环上 接上6个四氢吡咯环 ( 图上 ) ,得到具有 Th 点群对称性的球碳衍 生物与聚乙烯咔唑 ( PVK—— Polyvinylcarbazole ) 以及联萘口恶二唑 ( BND , Bisnaphthyloxadiazole ) 的复合物通以电流会 像发光二极管(图下) 一样发出白光。
七. 定位规律与电子效应
给电子诱导效应( +I) 电子效应 诱导效应 ( I) 共轭效应 ( C) 吸电子诱导效应( -I)
pπ 共轭
ππ 共轭
+
诱导效应:σ 电子的偏移。用→表示方向。
δ δ δ δ δ
+
δ
+
δ
-
CH3
CH2
CH2
CH2
Cl
Cl
共轭效应:由于相邻P轨道的重叠而产生, 共轭的结果是使电子密度趋于 平均化。
4 3
1
NO2
2
CH3 2-甲基-4'-硝基联苯
2'
3'
1,3-联三苯
8 9 1 2 9 8 10 1 2 6
3) 稠环芳烃
8 7 6 5 4 1 2 3 7 6
3
5 10 4
7 5
4 3
萘
蒽
菲
二. 苯的结构和表达式
不反应 C 6H 5 KMnO4 H Br2 FeBr3
+
C 6H 6
Br2 CCl4
中国科技大学侯建国教授等利用扫描隧道显微镜 技术,将C60分子组装在一单分子膜上,在5K温度下 冻结分子热振动,在国际上首次“拍摄”了能够清 楚分辨碳原子间单不完全等同;
电子云不完全平均化;离域能 ~255kJ/mol。
2) 化学性质
① 亲电取代 (反应条件较温和,取代主要发生在α 位。)
H E
+
H
E
H
+
+
其它贡献较 小的共振式
E
其它贡献较小的共振式
Br 卤化 + Br2
CH3COOH (75%)
NO2 硝化 + HNO3
不反应
C6H5Br
凯库勒(kekule)结构式:
平面分子 正六边形 碳碳键长均等:140pm ; 键角120o
H H H H H sp2 H
Csp2 , C-C键和C-H键; p轨道, 键 ; 电子云分布在平面上下; 环闭共轭体系; 能量降低稳定、 键长平均化。
三. 物理性质(自学) 四. 化学性质
压扁了的球碳
1996 年 俄 国 和 英 国 的 研究者报道过合成了氟化的 C60F18 。用 19F NMR 证实所 有氟原子都在球碳的同一半 球上。最近,单晶衍射证实, 这种氟化的C60是一个“压扁 了 的 ” 球 ( 图 ) [Angew Chem Int Ed 39 , 3273 , (2000)]。而且,在被压扁 的中心是碳的六元环,其 CC 键的长度完全相等,表明 这个六元环是一个完全的芳 香环。这是第一次发现在球 碳上存在类苯环。因该化合 物的特殊结构,有望被开发 为光子器件或者光电器件。
o
NO2 + H2O
3. 磺化反应
SO3H + H2SO4 (10%SO3) + H2O
4. 傅-克(Friedel-Crafts)反应 1)傅-克烷基化反应
+ CH3CH2Cl AlCl3 0~5oC CH2CH3 + HCl
2)傅-克酰基化反应
O + CH3CCl AlCl3 ( 无水 )
O C-CH3
(100%)
与烷烃的卤代一样,是按游离基历程进行反应的。
五. 亲电取代反应的历程
sp2 + E
+
sp3 H + E -H
+
sp2 E
E
+
亲电试剂
络合物
络合物
产物
用极限式表示中间体:
H
+
H E
+
+
H E
E
六. 苯环上取代基的定位规律(定位效应)
Ⅰ类 邻对位定位基——致活的定位基(除卤素外)
SO3H
(80%)
(20%)
2)两个取代基定位效应相矛盾,由基团致活能力顺序判断第 三个基团取代的位置。
①.两个基团不同类,定位效应受邻对位取代基控制。
CHO
CH3
OH
NO2
②.两个取代基为同一类,定位效应受致活能力较强的基
团控制。
OH (100%)
CH3
CH3
NHCOCH3
③.两个取代基定位效应接近,难预测主要产物,为混合物。
离域能:苯>萘>菲>蒽
9,10位化学活性较大。
O
8
9
HNO3
O
Na ROH
3.致癌芳烃
8 7 6 5 10 4 9 1 2 3
6 5 1 2
CH3
CH3
5,10-二甲基-1,2-苯并蒽
5 4 3 9 1 10 6 7 8
1,2,5,6-二苯并蒽
