年产10万吨甲醇初步设计——课程设计
最新年产10万吨煤合成甲醇工厂设计

年产10万吨煤合成甲醇工厂设计1 概述甲醇是重要的有机化工原料之一,是碳一化学的母体,广泛应用于生产塑料、纤维、橡胶、染料、香料、医药和农药等方面,也是一种重要的有机溶剂,由甲醇延伸的化工产品达数百种,在发达国家其产量仅次于乙烯、丙烯和苯,居第四位。
另外,甲醇是一种易挥发的无色透明液体,它与现实中使用的液体燃料具有极为相似的燃烧性能,它既具有燃烧性能好、辛烷值高、抗爆性能好等特点,又具有生产原料非常广泛的优势。
因此,早在20 世纪70 年代初,欧美的一些发达国家就将甲醇列为替代燃料,并开始了不同方式的研究开发与推广应用工作。
我国在这方面的起步工作也较早,20 世纪70 年代初期就有少数大专院校、科研单位和个别汽车制造企业开始了甲醇燃料的开发与应用工作,并取得了一定的进展。
综上所述,根据目前我国资源结构及能源供应的现状,大力发展煤炭洁净技术,对于调整和改善我国的能源结构,促进经济发展会起到更加积极的作用。
2 甲醇合成技术的发展1923 年德国首次用CO+H2 合成气在锌铬催化剂、高温高压下实现了甲醇合成工业化之后,甲醇生产便迅速发展,甲醇合成的方法也不断出现新的成就,最初采用的锌铬催化剂,甲醇合成反应温度在360~400 ℃,反应压力为20~30 MPa。
后来由于脱硫技术的发展及铜系催化剂研究与应用的成功,在较低的反应温度(240~300 ℃),较低的压力(5 MPa)下,即可获得较高的甲醇产率。
相对于锌铬系催化剂,铜系催化剂不仅活性好,而且选择性高,减少了副反应,不仅改善了甲醇质量,降低了原料气消耗,而且因反应压力低,工艺设备的制造比高压法更容易,投资少,能耗约降低了1/4,单位产品的成本较低,低压甲醇合成具有显著的优越性。
目前,国内外新上的单醇系统全采用低压工艺。
甲醇生产的另一个重要发展动向就是装置的大型化。
20 世纪90 年代以来,国外新建甲醇装置生产能力一般在50~80 万t/a,进入21 世纪后进一步提升至100 万t/a 以上,沙特国际石化公司(Sipchem)和伊朗国家石化公司(NPC)2004 年投产的甲醇装置均为100 万t/a。
年产10万吨甲醇工艺设计

甲醇是一种重要的有机化工品,广泛应用于合成有机化合物、涂料、塑料等工业领域。
甲醇工艺设计的关键目标是实现高产量、高质量的甲醇生产,同时考虑能源消耗、环境污染和安全性等方面的要求。
本文将对一种年产10万吨甲醇工艺设计进行详细介绍,包括原料选择、反应过程、设备选型、能源消耗和环境污染控制等方面。
1.原料选择甲醇的主要原料为天然气或煤炭。
在本工艺设计中,我们选择优质天然气作为甲醇的主要原料。
天然气中的甲烷通过蒸汽重整反应生成合成气,包括一氧化碳和氢气。
该合成气经过净化处理后,进入甲醇合成反应器进行反应。
2.反应过程甲醇的合成反应是一种催化反应,主要基于甲醇合成催化剂的作用。
在本工艺设计中,我们选择了高效的铜锌氧化物催化剂,能够在相对低的温度和压力下实现高效率的甲醇合成。
反应过程主要包括气相反应和液相吸收两个步骤。
气相反应器中,一氧化碳和二氧化碳与氢气发生反应生成甲醇。
反应后的气体进入液相吸收器,通过溶剂的吸收和分离,将甲醇从废气中回收。
3.设备选型甲醇生产设备主要包括气体净化、蒸汽重整、合成反应、分离和脱水等装置。
对于年产10万吨甲醇的工艺设计,我们选用了适宜的设备类型和规格,确保设备能够满足预期产量和质量要求。
例如,气体净化装置采用活性炭吸附和分子筛吸附的组合方式,提高气体净化效果。
合成反应器采用多床催化剂装置,提高反应效率和催化剂的使用寿命。
分离装置采用精馏和吸附等工艺,实现甲醇的回收。
4.能源消耗甲醇生产需要消耗大量的能源,包括天然气和蒸汽等。
为了降低能源消耗和提高能源利用效率,我们在工艺设计中采取了多项措施。
例如,在蒸汽重整过程中,我们采用余热回收技术,将废弃热量回收利用。
在合成反应过程中,我们优化反应条件和催化剂的使用方式,降低能源消耗。
此外,我们还考虑了电力和水的节约措施,提高整体能源利用效率。
5.环境污染控制甲醇生产过程中会产生废气、废水和废渣等污染物。
为了控制环境污染,我们在工艺设计中采取了多项措施。
年产十万吨甲醇设计

年产十万吨甲醇设计学号:题目:院(部)系所学专业年级、班级完成人姓名指导教师姓名专业技术职称年月日论文原创性保证书我保证所提交的论文都是自己独立完成,如有抄袭、剽窃、雷同等现象,愿承担相应后果,接受学校的处理。
专业:班级:签名:年月日摘要本设计重点描述了甲醇合成工艺流程。
甲醇是重要的化工原料和燃料,应用于多个领域。
首先简单地介绍了甲醇的生产发展、甲醇合成的反应热力学和动力学、甲醇反应需要的催化剂、甲醇合成工艺和甲醇的发展前景。
其中,甲醇合成催化剂和工艺选择关系着甲醇合成产量。
中低压、铜基催化剂的条件有利于甲醇合成。
紧接着介绍了甲醇合成工艺。
甲醇合成首先要进行造气。
造气选用煤作原料,得到的粗煤气经脱硫、脱碳等净化操作后进入合成塔合成甲醇。
甲醇合成工艺选择Luigi低压合成,合成气于5MPa、220℃下进入Luigi管壳式反应器。
从合成塔得到的粗甲醇必须要进行精馏。
本设计需要将原料粗甲醇精制到含醇量99.95%的纯度。
根据现代对甲醇精馏工艺设计的了解,甲醇三塔精馏技术以其能耗低、产品质量好的优点领先于其他工艺。
所以本设计采用三塔精馏工艺。
再接着对甲醇的生产合成和精馏过程进行了详细的物料衡算。
最后进行了常压精馏塔的计算,包括设备选型、塔的外形设计以及塔板流体力学验算。
通过本次设计,对合成甲醇以及提纯甲醇有更深刻的认识。
关键词:甲醇;合成;工艺设计;三塔精馏;常压塔AbstractThis design for methanol synthesis processes were described emphatically. Methanol is an important chemical raw material and fuel, is applied to the fields. First simply introduces the methanol production development, the reaction thermodynamics and kinetics of methanol synthesis, methanol reaction requires a catalyst, methanol synthesis process and the development prospects of methanol. Methanol synthesis catalyst and process selection is one of the relationship between the yield of methanol synthesis. In conditions of low pressure, copper base catalyst for methanol synthesis. Followed by methanol synthesis process was introduced. Gasification methanol synthesis should first. Gasification coal as raw materials, the raw coal gas after desulfurization and decarbonization purification operation into the synthesis of methanol synthesis tower. Choose Luigi low-pressure synthesis methanol synthesis process, synthesis gas in 5 mpa, 220 ℃ under into Luigi tubular reactor. From the crude methanol synthesis tower has to be distillation. This design need to be material crude methanol refining to the alcohol content of 99.95% purity. According to the modern understanding of the methanol distillation process design, methanol tower distillation technology for its low energy consumption, product quality good advantage ahead of other technology. So this design USES three tower distillation process. We'll go on with the production of methanol synthesis and material balance of distillation process in detail. Finally, the calculation of atmospheric distillation column was carried out, including equipment type selection, design of the tower and tray hydrodynamics calculation. Through the design, for methanol synthesis and purification of methanol has a more profoundunderstanding.Keywords:methanol;synthetic ;process design ;three tower distillation ;atmospheric column目录第一章前言 (1)1. 概述 (1)1.1 生产及技术发展 (1)2. 甲醇合成 (2)2.1 合成反应热力学 (2)2.2 合成反应动力学 (3)2.3 合成反应催化剂 (3)2.4 合成工艺 (4)2.5 合成甲醇的目的和意义 (5)第二章工艺概述 (6)1. 造气工段 (6)1.1 原料 (6)1.2 原料气的制备 (7)1.3 工艺概述 (7)1.4 净化工段 (8)2. 合成工段 (8)3. 精馏工段 (9)第三章工艺计算 (12)1. 甲醇生产的物料平衡计算 (12)1.1 合成塔物料平衡计算 (12)1.2 甲醇精馏的物料平衡计算 (15)第四章常压精馏塔计算 (18)1.基础数据 (18)2. 塔板数的计算 (19)2.1 处理能力 (19)2.2 最小理论板数 (19)2.3 最小回流比 (20)2.4 理论板数 (20)2.5 进料位置 (20)2.6 全塔效率的估算 (20)3. 精馏段与提馏段的体积流量 (21)3.1 精馏段 (21)3.2 提馏段 (23)4. 塔径计算 (24)4.1 精馏段 (24)4.2 提馏段 (25)5. 塔内件设计 (26)5.1 溢流堰的设计 (26)5.2 溢流装置 (26)5.3 塔板布置及浮阀数目与排列 (27)6. 塔板流体力学验算 (29)6.1 塔板压降 (29)6.2 液泛 (29)6.3 雾沫夹带 (30)7. 塔板负荷性能图 (31)7.1 雾沫夹带线 (31)7.2 液泛线 (31)7.3 液相负荷上限线 (32)7.4 漏液线 (32)7.5 液相负荷下限线 (33)8. 常压塔工艺计算汇总 (34)9. 常压塔塔高计算 (35)第五章 Aspen Plus 的模拟计算 (36)第一章前言1. 概述甲醇是最简单的化学品之一,是重要的化工基础原料和清洁液体燃料,广泛应用于有机合成、染料、医药、农药、涂料、汽车和国防等工业中。
年产10万吨煤合成甲醇工厂设计要点

年产10万吨煤合成甲醇工厂设计要点煤合成甲醇工厂设计要点煤合成甲醇工厂是利用煤作为原料制备甲醇的生产设备。
煤作为一种丰富的化石燃料,具有储量大、价格低廉以及可再生的特点,因此利用煤来生产甲醇具有较大的经济和环境优势。
下面我们将介绍设计一个年产10万吨煤合成甲醇工厂的要点。
1. 工艺选择煤合成甲醇工厂的工艺选择对于整个工厂的设计有至关重要的影响。
目前常见的工艺路线有间接法、直接法和半直接法等。
在选择工艺路线时需要考虑甲醇产率、甲醇纯度、能耗和设备投资等因素,综合比较各种工艺路线的优势和劣势,选择适合的工艺路线。
2. 原料处理煤是煤合成甲醇工厂的主要原料,但煤中含有许多杂质,如灰分、硫分、氮分等,需要进行原料处理。
原料处理的主要目的是去除杂质,提高煤的纯度,减少后续工艺过程中的能耗和设备磨损。
原料处理的主要工艺包括煤炭碎煤、煤炭洗选、煤泥脱水等。
3. 反应和分离煤合成甲醇的反应过程是核心环节,主要包括原料气化、合成气净化、合成气变换和甲醇合成等。
在反应过程中,需要注意反应温度、反应压力、反应速率等参数的控制,以保证反应的高效进行。
在分离过程中,主要包括甲醇的分离和副产物的回收利用。
4. 能源利用煤合成甲醇工厂需要大量的能源供应,包括煤炭燃烧产生的热能、原料气化产生的合成气以及电力等。
在能源利用上需要考虑能源的高效利用和节能减排。
通过合理设计能源系统,进行余热回收、废气处理和烟气排放控制等措施,以减少能源消耗和环境污染。
5. 设备选型煤合成甲醇工厂设备的选型对于工艺的高效运行和产品质量的保证至关重要。
设备选型需要考虑设备的质量、性能、可靠性和维修保养等方面。
此外,还需要考虑设备的运行安全和环境保护要求,选择符合国家标准和行业规范的设备。
6. 自动化控制煤合成甲醇工厂的生产过程复杂,需要进行自动化控制来实现对生产过程的监控和调控。
自动化控制系统可以实现对设备运行状态、工艺参数和产品质量等方面的实时监测和调节,提高生产效率和产品质量。
年产10万吨甲醇工厂模拟设计

目录1甲醇生产的主要原料及生产工艺 (1)1.1甲醇生产主要原料及合成方法 (1)1.2甲醇合成工艺流程简介 (2)2生产工艺物料衡算 (3)2.1设计条件及参数 (4)2.2生产工艺物料衡算 (5)3生产工艺热量衡算 (6)3.1合成塔的热量计算 (7)3.2入塔气换热器的热量计算 (8)3.3水冷器热量的计算 (9)4生产工艺的流程设计计算及设备选型 (9)4.1甲醇合成塔的设计选型 (9)4.1.1传热面积计算 (10)4.1.2催化剂用量计算 (11)4.1.3传热管数计算 (11)4.1.4合成塔计算 (11)4.1.5折流板计算 (12)4.1.6管板计算 (12)4.1.7支座计算 (12)4.1.8合成塔设计汇总表 (13)4.2甲醇合成工段设备一览表 (13)5参考文献 (13)甲醇生产的主要原料及生产工艺1.1甲醇生产主要原料及合成方法我国甲醇生产制造原料气的原料有气体、液体和固体原料。
气体原料有天然气、焦炉气、乙炔尾气、炼厂气、高炉气等。
液体原料有石脑油、重油、渣油等。
固体原理有焦炭、无烟煤、褐煤等[1]。
目前甲醇生产技术主要采用低压法和中压法两种工艺,并且以低压法为主,这两种方法生产的甲醇约占世界甲醇产量的80%以上。
高压法:(19.6-29.4Mpa)是最初生产甲醇的方法,采用锌铬催化剂,反应温度360-400℃,压力19.6-29.4Mpa。
高压法由于原料和动力消耗大,反应温度高,生成粗甲醇中有机杂质含量高,而且投资大,其发展长期以来处于停顿状态。
低压法:(5.0-8.0 Mpa)是20世纪60年代后期发展起来的甲醇合成技术,低压法基于高活性的铜基催化剂,其活性明显高于锌铬催化剂,反应温度低(240-270℃)。
在较低压力下可获得较高的甲醇收率,且选择性好,减少了副反应,改善了甲醇质量,降低了原料消耗。
此外,由于压力低,动力消耗降低很多,工艺设备制造容易。
中压法:(9.8-12.0 Mpa)随着甲醇工业的大型化,如采用低压法势必导致工艺管道和设备较大,因此在低压法的基础上适当提高合成压力,即发展成为中压法。
年产10万吨甲醇工艺设计

甲醇是一种无色、易挥发的液体,是一种重要的化工原料。
甲醇可用作溶剂、防冻剂、燃料等,并且也是合成多种化学品的重要原料。
本文将介绍一种年产10万吨甲醇的工艺设计。
1.原料选择甲醇的主要原料是天然气或煤炭。
在本设计中,采用天然气作为原料,主要原因是天然气作为清洁能源,不仅含有丰富的甲烷,而且还有其他杂质,如醇、醛和硫化物等。
2.甲醇生产工艺流程甲醇的生产过程主要分为气化、合成气净化、变换反应、甲醇的分离和精制等环节。
气化:天然气通过一系列的处理后,首先进入气化炉进行气化反应,将甲烷转化成一氧化碳和氢气。
合成气净化:气化产生的合成气中含有一氧化碳、二氧化碳、氢气等杂质,需要通过一系列净化步骤,去除杂质,如一氧化碳的选择性氧化、水蒸气转化等,使得合成气的组成符合变换反应的要求。
变换反应:减少二氧化碳的含量并提高一氧化碳的转化率,需要进行一系列变换反应。
主要反应有水汽变换反应和低温甲醇合成反应。
甲醇的分离和精制:合成后的甲醇进入精制塔,通过分离和纯化操作,去除杂质和溶剂,获得高纯度的甲醇。
3.工艺优化为了提高甲醇的生产效率和降低成本,可以对工艺进行优化。
提高合成气的利用率:在气化炉中,采用高效的催化剂和反应条件,提高一氧化碳和氢气的产率。
减少能量消耗:通过余热回收系统,对高温废气和废水进行换热,降低能量消耗。
优化反应条件:根据反应的动力学特性,确定最佳反应温度和压力,提高甲醇的选择性和收率。
改进分离和纯化技术:对精制塔进行优化设计,提高甲醇的回收率和纯度。
4.安全措施甲醇是一种易燃易爆液体,在生产过程中需要采取一系列安全措施,包括防火、防爆、通风和泄漏处理等。
此外,还需要定期检查和维护设备,确保工艺安全可靠运行。
综上所述,本文介绍了年产10万吨甲醇的工艺设计,包括原料选择、工艺流程、工艺优化和安全措施。
通过对工艺的优化和改进,可以提高甲醇的生产效率和质量,并降低生产成本,达到经济效益和环境效益的双重目标。
年产10万吨低压法甲醇精制工段设计

年产10万吨低压法甲醇精制工段设计(生物与化学工程学院10化学工程与工艺班)摘要:本设计所用的低压法采用51—1型铜基催化剂,合成压力为5MPa°以天然气为原料,利用铜基催化剂合成粗甲醇后再经过三塔精憎合成纯度更髙的甲醇。
再通过査阅相关的精餾工艺资料;在实习车间观摩实际操作过程;并整合与精馅相关的文献,从物料和热量衡算,设备选型与il•算的角度,设计出符合生产要求的精憾工艺路线。
关键词:甲醇;低压法:精制:工段设汁引言甲醇在现代工业中占着及其重要的地位,他不仅仅是碳一化工的基本原料,而且在无论是在化工、医药,还是在轻工纺织行业都有着广泛的应用。
甲醇用途广泛,加工后可以作为优质燃料。
其衍生物也用途广泛,诸如屮醛、醋酸、氯甲烷等现代工业的基础产品都能通过甲醇的加工得到,现今,我国已有三十多种工业产品是通过甲醇的一次加工得到的,同时,在市场需求的不断扩张下,如何生产出高质量、高纯度的甲醇产品,已经影响到了每个甲醇生产企业的生存能力。
工艺原理:造气工段:使用二步造气法⑴CH4+H2O (气)-CO+3H2 AH=-205.85kJ/molCH4+O2—CO2+2H2 AH =+109.45kJ / molCH4+7 Ch-CO+2H2 AH =+35.6kJ / molCH4+2H2-CO2+2H2O AH =+802.3kJ / mol合成工段:鲁奇低压工艺法,在5MPa,铜基催化剂条件下合成。
主反应:CO+2H2—CH3OH AH=+102.37kJ/mol副反应:2CO+4H2—CH3(O)+H2O AH =+200.3kJ / molCO+3H2—CH4+H2O AH =+115.69kJ / mol 4CO+8H2—C4H9OH+3H2OAH =+49.62kJ / molCO2+H2-CO+H2O AH =-42.92kJ / mol (1) 因为除了(1)反应之外,所有反应都增加了反应物CO的消耗,从反应平衡的角度考虑,必须抑制除(1)外所有副反应的进行,以此增加CO反应物的物质的量,利于反应向合成甲醇方向进行,增加产率。
甲醇化工设计课程设计

甲醇化工设计课程设计一、教学目标本课程的教学目标是让学生掌握甲醇化工设计的基本原理和方法,能够运用所学知识进行简单的甲醇化工设计。
具体来说,知识目标包括:了解甲醇的性质、用途和生产方法;掌握甲醇化工设计的基本原理和方法;了解甲醇化工生产过程中的安全和环保要求。
技能目标包括:能够运用所学知识进行甲醇化工设计的计算和分析;能够阅读和理解甲醇化工相关的技术资料;能够进行简单的甲醇化工工艺流程设计。
情感态度价值观目标包括:培养学生对甲醇化工行业的兴趣和热情;培养学生严谨的科学态度和良好的职业道德;培养学生可持续发展意识和环保意识。
二、教学内容本课程的教学内容主要包括甲醇的性质和用途、甲醇化工设计的基本原理和方法、甲醇化工生产过程中的安全和环保要求等。
具体来说,教学大纲如下:1.甲醇的性质和用途:介绍甲醇的物理性质、化学性质和生物性质,以及甲醇在化工生产中的应用。
2.甲醇化工设计的基本原理和方法:讲解甲醇化工设计的基本原理,如化学反应原理、物质传递原理、能量传递原理等,以及甲醇化工设计的方法,如流程设计、设备选型、参数计算等。
3.甲醇化工生产过程中的安全和环保要求:介绍甲醇化工生产过程中的安全措施和环保要求,如防火、防爆、防毒、防腐蚀等。
三、教学方法本课程的教学方法采用讲授法、案例分析法和实验法相结合的方式。
具体来说:1.讲授法:通过教师的讲解,让学生了解甲醇的性质和用途、甲醇化工设计的基本原理和方法、甲醇化工生产过程中的安全和环保要求等。
2.案例分析法:通过分析实际案例,让学生掌握甲醇化工设计的计算和分析方法,提高学生的实际操作能力。
3.实验法:通过实验操作,让学生了解甲醇化工生产过程中的安全和环保要求,培养学生的实验技能和动手能力。
四、教学资源本课程的教学资源包括教材、参考书、多媒体资料和实验设备等。
具体来说:1.教材:选用权威、实用的甲醇化工设计教材,为学生提供系统的理论知识。
2.参考书:提供相关领域的参考书籍,拓展学生的知识面。
年产10万吨甲醇初步设计——课程设计
绪论1.1概述1.1.1甲醇的意义及作用甲醇作为及其重要的有机化工原料,是碳一化学工业的基础产品,在国民经济中占有重要地位。
长期以来,甲醇都是被作为农药,医药,染料等行业的工业原料,但随着科技的进步与发展,甲醇将被应用于越来越多的领域。
1.1.2甲醇的生产工艺及发展1.1.2.1 生产的发展世界甲醇工业的发展总体上说,世界甲醇工业从90年代开始经历了1991-1998的供需平衡,1998-1999的供大于求,从2000年初至今的供求基本平衡三个基本阶段。
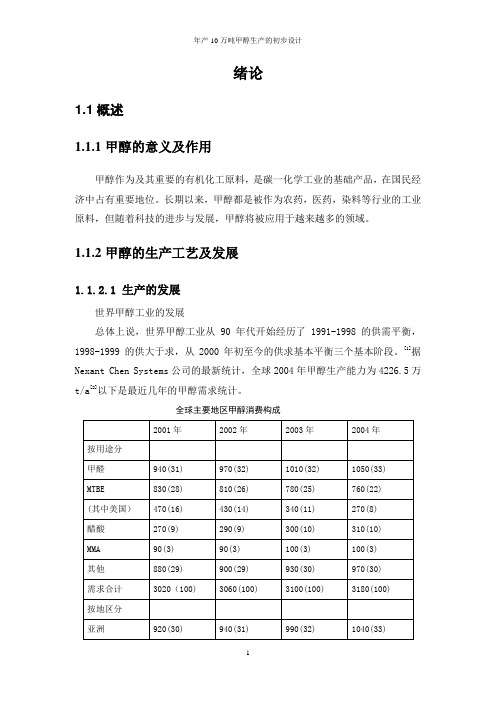
[1]据Nexant Chen Systems公司的最新统计,全球2004年甲醇生产能力为4226.5万t/a[2]以下是最近几年的甲醇需求统计。
全球主要地区甲醇消费构成从上表可以看出,到2004年为止,甲醇仍主要用于制造甲醛和MTBE。
用于制造甲醛的甲醇用量随年份成增长趋势,而MTBE 的需求量则逐年降低。
亚洲需求量增长比较迅速,与此相反,北美地区需求则在减少。
2)我国甲醇工业发展我国的甲醇工业经过十几年的发展,生产能力得到了很大提高。
1991年,我国的生产能力仅为70万吨,截止2004年底,我国甲醇产能已达740万吨,117家生产企业共生产甲醇440.65万吨,2005年甲醇产量达到500万吨,比2004年增长22.2%,进口量99.1万吨,因此下降3.1%。
1.1.2.2生产技术的发展1)装置大型化于上世纪末相比,现在新建甲醇规模超过百万吨的已不再少数。
在2004——2008年新建的14套甲醇装置中平均规模为134万t/a,其中卡塔尔二期工程项目高达230万t/a。
最小规模的是智利甲醇项目,产能也达84万t/a,一些上世纪末还称得上经济规模的60万t/a装置因失去竞争力而纷纷关闭。
2)二次转化和自转化工艺合成气发生占甲醇装置总投资的50%—60%,所以许多工程公司将其视为技术改进重点。
已经形成的新工艺在主要是Syenetix(前ICI)的先进天然气加热炉转化工艺(AGHR),Lurgi的组合转化工艺(CR)和Tops e的自热转化工艺(ATR) 3)新甲醇反应器的合成技术大型甲醇生产装置必须具备与其规模相适应的甲醇反应器和反应技术。
年产甲醇课程设计

年产甲醇课程设计一、课程目标知识目标:1. 学生能理解甲醇的化学性质、制备原理及年产量的计算方法。
2. 学生掌握甲醇生产过程中的关键设备、工艺流程及其在国民经济中的应用。
3. 学生了解我国甲醇产业的发展现状及趋势。
技能目标:1. 学生能够运用化学知识解决实际生产中与甲醇相关的问题,具备一定的实际操作能力。
2. 学生能够通过查阅资料、数据分析等方法,对甲醇产业进行简单的评价和分析。
3. 学生能够运用数学知识,对甲醇年产量进行计算和预测。
情感态度价值观目标:1. 培养学生对化学学科的兴趣和热情,提高对化学在生产实践中的认识。
2. 增强学生的环保意识,使其关注甲醇生产过程中的环境保护和资源利用。
3. 培养学生的团队协作能力和创新精神,使其在学习过程中主动探究、积极思考。
课程性质:本课程属于化学与化工类课程,以实践性和实用性为主,结合理论知识,培养学生的实际操作能力和分析问题、解决问题的能力。
学生特点:学生为高中生,具有一定的化学基础,对实际生产过程有一定的好奇心,善于思考,但可能缺乏实际操作经验。
教学要求:教师需结合学生特点,采用理论教学与实践操作相结合的方式,引导学生主动探究,注重培养学生的实际操作能力和综合素质。
在教学过程中,关注学生的情感态度价值观的培养,使学生在掌握知识的同时,形成正确的价值观。
通过分解课程目标为具体的学习成果,为后续的教学设计和评估提供依据。
二、教学内容1. 甲醇的化学性质与制备原理- 课本章节:第二章有机化合物,第四节醇、酚、醚- 内容:甲醇的分子结构、物理性质、化学性质;甲醇的合成方法及反应原理。
2. 甲醇生产设备及工艺流程- 课本章节:第三章化工设备,第六节合成塔与反应器- 内容:甲醇生产中的关键设备(合成塔、冷却器、压缩机等)及其工作原理;工艺流程及操作要点。
3. 甲醇年产量计算与应用- 课本章节:第四章化学反应工程,第九节反应速率与化学平衡- 内容:甲醇合成反应的化学平衡;根据反应速率计算年产甲醇的产量;甲醇在国民经济中的应用。
化工设计任务书范文

化工设计任务书范文一、项目名称年产 10 万吨甲醇合成工艺设计二、项目背景甲醇是一种重要的有机化工原料,广泛应用于化工、医药、农药、燃料等领域。
随着经济的发展和能源需求的增长,甲醇的市场需求不断扩大。
本项目旨在设计一套年产 10 万吨甲醇的合成工艺,以满足市场需求。
三、设计依据1、原料供应原料气组成:氢气(H₂)70%,一氧化碳(CO)20%,二氧化碳(CO₂)5%,氮气(N₂)5%。
原料气压力:25 MPa原料气温度:40℃2、产品规格甲醇产品纯度:≥999%甲醇产品含水量:≤01%3、公用工程条件冷却水温度:25℃冷冻水温度:-15℃蒸汽压力:10 MPa(饱和蒸汽)四、设计原则1、采用先进、成熟、可靠的工艺技术,确保生产过程安全、稳定、高效。
2、充分考虑环境保护和节能减排,符合国家相关法规和标准。
3、优化工艺流程和设备选型,降低投资成本和运行费用。
4、考虑装置的灵活性和可扩展性,以适应市场变化和未来发展的需求。
五、工艺流程设计1、合成气制备原料气经过脱硫、脱碳等净化处理,去除其中的杂质。
净化后的原料气通过压缩提高压力,以满足合成反应的要求。
2、甲醇合成合成气在催化剂的作用下进行甲醇合成反应。
反应产物经过冷却、分离,得到粗甲醇。
3、甲醇精馏粗甲醇经过精馏塔精馏,去除其中的杂质,得到高纯度的甲醇产品。
六、设备选型1、压缩机选用离心式压缩机,根据原料气流量和压力要求确定型号和规格。
2、合成反应器采用绝热式固定床反应器,根据反应条件和生产能力确定尺寸和结构。
3、精馏塔选用板式精馏塔,根据分离要求和物料特性确定塔板数和塔径。
4、换热器根据热量交换需求选择合适的换热器类型和规格,如管壳式换热器、板式换热器等。
5、泵根据物料流量和扬程要求选择离心泵或柱塞泵等。
七、车间布置1、按照工艺流程和设备特点,合理布置设备,确保物料输送顺畅,操作方便。
2、充分考虑安全距离和防火防爆要求,设置必要的安全设施和通道。
3、考虑设备检修和维护的空间需求,便于设备的安装和拆卸。
年产10万吨甲醇精馏工段设计毕业设计-年产10万吨甲醇的设计

毕业设计设计题目:年产10万吨甲醇精馏工段工艺设计毕业设计(论文)原创性声明和使用授权说明原创性声明本人郑重承诺:所呈交的毕业设计(论文),是我个人在指导教师的指导下进行的研究工作及取得的成果。
师的指导下进行的研究工作及取得的成果。
尽我所知,尽我所知,除文中特别加以标注和致谢的地方外,不包含其他人或组织已经发表或公布过的研究成果,也不包含我为获得也不包含我为获得 及其它教育机构的学位或学历及其它教育机构的学位或学历而使用过的材料。
对本研究提供过帮助和做出过贡献的个人或集体,均已在文中作了明确的说明并表示了谢意。
均已在文中作了明确的说明并表示了谢意。
作 者 签签 名:名: 日 期:期:期: 指导教师签名:指导教师签名: 日日 期:期:使用授权说明本人完全了解本人完全了解 大学关于收集、保存、使用毕业设计(论大学关于收集、保存、使用毕业设计(论文)的规定,即:按照学校要求提交毕业设计(论文)的印刷本和电子版本;学校有权保存毕业设计(论文)的印刷本和电子版,并提供目录检索与阅览服务;学校可以采用影印、缩印、数字化或其它复制手段保存论文;在不以赢利为目的前提下,学校可以公布论文的部分或全部内容。
或全部内容。
作者签名:作者签名: 日日 期:期:期:学位论文原创性声明本人郑重声明:所呈交的论文是本人在导师的指导下独立进行研究所取得的研究成果。
除了文中特别加以标注引用的内容外,除了文中特别加以标注引用的内容外,本论文本论文不包含任何其他个人或集体已经发表或撰写的成果作品。
对本文的研究做出重要贡献的个人和集体,究做出重要贡献的个人和集体,均已在文中以明确方式标明。
均已在文中以明确方式标明。
均已在文中以明确方式标明。
本人完本人完全意识到本声明的法律后果由本人承担。
全意识到本声明的法律后果由本人承担。
作者签名:作者签名:日期:日期: 年年 月月 日日学位论文版权使用授权书本学位论文作者完全了解学校有关保留、使用学位论文的规定,同意学校保留并向国家有关部门或机构送交论文的复印件和电子版,允许论文被查阅和借阅。
年产10万吨煤合成甲醇的工艺设计

精细化工工艺学设计说明书年产10万吨煤合成甲醇的工艺设计起止日期:2011 年11 月28 日至2011 年12 月16 日学生姓名班级学号成绩指导教师(签字)包装与材料工程学院(部)2011年12 月16 日目录一、概述 (1)1.1甲醇的应用情况介绍 (1)1.2 甲醇的合成方法 (1)1.2.1常用的合成方法 (1)1.2.2其他方法 (2)1.2.3本设计所采用的合成方法 (2)二.工艺概述 (2)2.1 造气工段 (2)2.2 净化工段 (3)2.3 合成工段 (3)2.3.1合成工段工艺 (3)2.3.2反应热力学 (4)2.4 精馏工段 (4)三.生产工艺及主要设备计算 (4)3.1 合成塔物料平衡计算 (5)3.2合成塔能量计算 (9)3.3 常压塔主要尺寸确定 (14)3.3.1.壁厚 (14)3.3.2.封头 (14)3.3.3裙座 (14)3.3.4塔高设计 (14)3.3.5接管设计 (14)3.3.5.1.塔顶甲醇蒸汽出口管 (14)3.3.5.2.回流液进口管 (15)3.3.5.3塔底出料管 (15)3.3.5.4进料管 (16)3.3.5.5.再沸器蒸汽入口管 (16)四.参考文献 (17)五.结束语 (18)一、概述1.1甲醇的应用情况介绍甲醇作为及其重要的有机化工原料,是碳一化学工业的基础产品,在国民经济中占有重要地位。
长期以来,甲醇都是被作为农药,医药,染料等行业的工业原料,但随着科技的进步与发展,甲醇将被应用于越来越多的领域。
1.2甲醇的合成方法1.2.1常用的合成方法当今甲醇生产技术主要采用中压法和低压法两种工艺,并且以低压法为主,这两种方法生产的甲醇约占世界甲醇产量的80%以上。
高压法:(19.6-29.4Mpa)是最初生产甲醇的方法,采用锌铬催化剂,反应温度360-400℃,压力19.6-29.4Mpa。
高压法由于原料和动力消耗大,反应温度高,生成粗甲醇中有机杂质含量高,而且投资大,其发展长期以来处于停顿状态。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
年产10万吨甲醇初步设计——课程设计绪论1.1概述1.1.1甲醇的意义及作用甲醇作为及其重要的有机化工原料,是碳一化学工业的基础产品,在国民经济中占有重要地位。
长期以来,甲醇都是被作为农药,医药,染料等行业的工业原料,但随着科技的进步与发展,甲醇将被应用于越来越多的领域。
1.1.2甲醇的生产工艺及发展1.1.2.1 生产的发展世界甲醇工业的发展总体上说,世界甲醇工业从90年代开始经历了1991-1998的供需平衡,1998-1999的供大于求,从2000年初至今的供求基本平衡三个基本阶段。
[1]据Nexant Chen Systems公司的最新统计,全球2004年甲醇生产能力为4226.5万t/a[2]以下是最近几年的甲醇需求统计。
全球主要地区甲醇消费构成2001年2002年2003年2004年按用途分甲醛940(31) 970(32)1010(32)1050(33)MTBE 830(28) 810(26)780(25)760(22)(其中美国)470(16)430(14)340(11)270(8)醋酸270(9) 290(9) 300(10) 310(10 )MMA 90(3) 90(3) 100(3) 100(3)其他880(29) 900(29)930(30)970(30)需求合计3020(100)3060(100)3100(100)3180(100)按地区分亚洲920(30) 940(31)990(32)1040(33)北美1000(33) 1000(33)980(31)970(31)西欧630(21) 640(21)650(21)670(21)其他470(16) 480(16)490(16)500(16)需求合计3020(100)3060(100)3110(100)3180(100)从上表可以看出,到2004年为止,甲醇仍主要用于制造甲醛和MTBE。
用于制造甲醛的甲醇用量随年份成增长趋势,而MTBE 的需求量则逐年降低。
亚洲需求量增长比较迅速,与此相反,北美地区需求则在减少。
2)我国甲醇工业发展我国的甲醇工业经过十几年的发展,生产能力得到了很大提高。
1991年,我国的生产能力仅为70万吨,截止2004年底,我国甲醇产能已达740万吨,117家生产企业共生产甲醇440.65万吨,2005年甲醇产量达到500万吨,比2004年增长22.2%,进口量99.1万吨,因此下降3.1%。
1.1.2.2生产技术的发展1)装置大型化于上世纪末相比,现在新建甲醇规模超过百万吨的已不再少数。
在2004——2008年新建的14套甲醇装置中平均规模为134万t/a,其中卡塔尔二期工程项目高达230万t/a。
最小规模的是智利甲醇项目,产能也达84万t/a,一些上世纪末还称得上经济规模的60万t/a装置因失去竞争力而纷纷关闭。
2)二次转化和自转化工艺合成气发生占甲醇装置总投资的50%—60%,所以许多工程公司将其视为技术改进重点。
已经形成的新工艺在主要是Syenetix(前ICI)的先进天然气加热炉转化工艺(AGHR),Lurgi的组合转化工艺(CR)和Tops e的自热转化工艺(ATR) 3)新甲醇反应器的合成技术大型甲醇生产装置必须具备与其规模相适应的甲醇反应器和反应技术。
传统甲醇合成反应器有ICI的冷激型反应器,Lungi的管壳式反应器,Topsdpe的径向流动反应器等,近期出现的新合成甲醇反应器有日本东洋工程的MRF--Z反应器等,而反应技术方面则出现了Lurgi推出的水冷一气冷相结合的新流程。
4)引入膜分离技术的反应技术通常的甲醇合成工艺中,未反应气体需循环返回反应器,而KPT则提出将未反应气体送往膜分离器,并将气体分为富含氢气的气体,前者作燃料用,后者返回反应器。
5)液相合成工艺传统甲醇合成采用气相工艺,不足之处是原料单程转化率低,合成气净化成本高,能耗高。
相比之下,液相合成由于使用了比热容高,导热系数大的长链烷烃化合物作反应介质,可使甲醇合成在等温条件下进行。
1.1.3产品的性质及用途1.1.3.1物理性质甲醇在常温下为无色透明具有酒精气味的挥发性液体,冰点-97.68℃,沸点64.7℃,自燃点470℃,闪点12℃。
甲醇与空气混合形成爆炸混合物,爆炸极限为5.5-36.5%(V)。
甲醇可与水、乙醇、乙醚等互溶。
与乙醇不同,甲醇不和水形成恒沸混合物,因此甲醇与水的混合物可以用分馏方法分开。
甲醇不同于其它醇,有剧毒,易燃烧,饮后会使人眼睛失明,量多可致死,吸入甲醇蒸汽或长期与甲醇蒸汽接触,也会引起中毒。
掺有甲醇的酒精称为变性酒精,不能饮用。
1.1.3.2化学性质甲醇含有一个甲基与一个羟基。
因它含有羟基,所以具有醇类的典型反应,因它含有甲基,所以又能进行甲基化反应。
甲醇可以与一系列物质反应,所以甲醇在工业上有着十分文广泛的应用。
a.甲醇氧化生成甲醛、甲酸甲醇在空气中可被氧化为甲醛,然后被氧化为甲酸CH3OH + 1/202=HCHO+H2OHCHO + 1/202=HCOOHb.甲醇与氨以一定比例混合,在370-420℃,5.0-20.0MPa压力下,以活性氧化铝为催化剂进行合成,得一甲胺、二甲胺、三甲胺、再经精馏,可得一、二、三甲胺产品。
CH3OH+NH3=CH3NH2+ H2O2CH3OH+NH3=(CH3)2NH+ 2H2O3CH3OH+NH3=(CH3)3N+ 3H2Oc.甲醇羰基化,生成醋酸甲醇与一氧化碳在碘化钴均相催化剂存在,压力65.0 MPa温度250℃下,或者在非均相铑催化剂(以碘为助催化剂)存在,压力3.0-4.0 MPa 温度180℃,能合成醋酸。
CH3OH+CO=CH3OOCHd.甲醇酯化,生成各种酯类化合物e.甲醇与甲酸生成甲酸甲酯CH3OH+HCOOH=HCOOCH3+H2Of.甲醇与硫酸反应生成硫酸氢甲酯、硫酸二甲酯CH3OH+H2SO4=CH3HSO4+H2O2CH3OH+H2SO4=(CH3)2SO4+H2Og.甲醇氯化,生成氯化甲烷甲醇与氯气混合,以氯化锌为催化剂可生成一、二、三氯甲烷,直至四氯甲烷。
CH3OH+Cl2+H2=CH3+HCL+H2CH3CL+Cl2=CH2Cl2+HCLCH2CL2+Cl2=CHCl3+HCLCHCL3+Cl2=CCl4+HCLh.甲醇与氢氧化钠反应,生成甲酸钠甲醇与氢氧化钠在85-100℃,下反应脱水可生成甲醇钠。
CH3OH+NaOH=CH3Ona+H2Oi.甲醇的脱水在高温下,在ZSM-5型分子筛或5-15埃的金属硅铝催化剂下,甲醇可脱水生成二甲醚。
CH3OH=(CH3)2O+H2Oj.甲醇与苯反应,生成甲苯在340-830℃下,甲醇与苯在催化剂存在下生成甲苯。
CH3OH+C6H6=C6H5CH3+H2Ol.甲醇与二硫化碳(CS2)反应,生成二甲基硫醚,再与硫酸氧化生成二甲基亚砜。
4CH3OH+CS2=2(CH3)2S+C02+2H2O3(CH3)2S+2HNO3=3(CH3)2SO+2NO+H2Om.甲醇的裂解甲醇在加温加压下,可在催化剂上分解为CO和H2CH3OH=CO+2H21.1.3.2产品的用途甲醇作为化工原料,主要用于生产甲醛,其消耗量占目前甲醇总产量的近一半,其次用作甲基化剂,生产甲胺,甲烷氯化物、丙烯甲酯、甲基丙烯酸甲醇酯、对苯二甲酸二甲酯等。
甲醇羰基化可生产醋酸、醋酐、甲酸甲酯、碳酸二甲酯等,甲醇也可生产敌百虫、甲基对硫磷、多菌灵等农药。
甲醇经生物发酵可以生产甲醇蛋白,用作饲料添加剂。
近年来,随着一碳化学的发展,由甲醇出发合成乙二醇、乙醇、乙醛等工艺路线正在日益受到注意。
由甲醇与异丁烯反应生产甲醇叔丁基醚的技术发展很快,产量逐年增大。
甲醇也是优良的能源和车船用燃料,它可以与汽油混合作为汽车燃料,也可以直接用作车船用燃料。
1.1.4 厂址选择1.1.4.1厂址选择原则厂址选择是十分重要的环节是工业布局的最终环节和工业基本建设的前期工作,也是工业项目可行性研究的组成部分。
它根据工业地区布局和新建项目设计任务书的各项要求,由规划与设计部门共同承担,在实地踏勘及区域性技术经济调查的基础上,对各地建设条件分析评价,并选择若干个能基本满足建厂要求的厂址方案作定性与定量相结合的技术经济综合论证,从而确定最优的建设地点和具体厂址。
厂址选择通常分为两个阶段:①确定选址范围和建厂地点。
侧重考虑厂址的外部区域经济技术条件,包括:距离原材料、燃料动力基地和消费地的远近;与各地联系的交通运输条件;当地的厂际生产协作条件;供水、排水及电源的保证程度;原有城镇基础和职工生活条件;有否可供工业进一步发展、工业成组布局和城镇发展的场地;是否与城镇规划及区域规划相协调;土地使用费用、建筑材料来源及施工力量等。
②确定厂址最后具体位置。
主要考虑项目设计任务书和厂区总平面布置的有关要求及投资约束条件。
包括:厂址场地条件,如建设用地的面积与外形、地势坡度、工程地质与水文地质状况、地震裂度、灾害性威胁(如洪水、泥石流等),土地征用的数量、质量及处理难度,厂址下有无矿藏等;距水源地的远近和给排水的扬程;修建铁路专用线与厂外公路等交通设施的工程量与投资;供电、供热设施的工程量及投资;距已有城镇生活区与公共服务设施的远近;“三废”排放对城镇和周围环境的影响及环保费用等。
厂址一经选定,不仅对所在地区的经济发展、城镇建设和环境质量产生重要影响,而且直接关系到新建项目的基本建设投资和建厂速度,并长期影响企业的经营、管理等经济效果。
1.1.4.2本次设计的厂址选择本次甲醇生产厂址选择在黑龙江省大庆市让胡路区马鞍山。
大庆市位于黑龙江省西部,松嫩平原中部,是一座以石油、石化和高科技产业著称的新兴城市,是祖国北方一颗璀璨的明珠,被誉为“绿色油化之都,天然百湖之城,北国温泉之乡”。
让胡路区资源优势突出,发展潜力巨大,特别是农业资源开发、化工产业发展前景广阔。
自然资源丰富有优质草原76万亩、耕地12万亩、水面6万亩、森林21万亩、湿地2.1万亩;让胡路区石化资源得天独厚,是全国最大的石油石化生产基地,辖区共有各类石油化工企业94家,天然气储备9.75亿立方米、原油3000万吨,有各类化工原料及中间体29大类、78个品种,聚丙烯轻烃等年生产能力达百万吨;存量资产优良,有可利用闲置资产37处,包括工业厂房、办公楼、商服、铁路专用线、冷暖库等资产,总净值4000多万元,总面积385.4万平方米.甲醇生产主要以大庆油田丰富的天然气资源为原料。
得天独厚的原料优势,先进的生产工艺,现代化的质量监测手段,严格的内部管理。
高于国家标准的内控标准,为产品质量提供了可靠的保证。
该厂址选择距离火车站只有 2公里,厂内可设火车专用线、汽车装车场及300余节铁路罐车、10余辆公路槽车,产品运输十分便利。
