美国《Ⅰ、Ⅱ期浸润性乳腺癌保乳手术的切缘指南》要点解读pdf
乳腺癌中文版NCCN指南(v.2版)

• 病理检查
初次活检为 手术活检
降低风险措施 监测
小叶原位癌 不伴其他癌
导管原位癌 (DCIS)
降低乳腺癌风 险的咨询,见 NCCN乳腺癌 降低风险指南
根据 • NCCN乳腺癌降低
风险指南 以及 • NCCN乳腺癌筛查
和诊断指南进行 监测
见NCCN DCIS指南 (DCIS-1)
浸润性 乳腺癌
检查
• 病史和体检 • 全血细胞计数,血小板计数 • 肝功能检查和碱性磷酸酶 • 双侧乳房X线摄片,乳腺超声检查 • 病理检查 • 明确肿瘤ER、PR及HER-2状况 • 遗传性乳腺癌高危患者进行遗传学咨询 • 乳腺MRI (可选),特别对于经X线摄片查出的隐匿性肿瘤 • 必要时进行生育咨询 • 心理评估(见NCCN 忧伤管理指南)
IIIC期: 任何T、N3、M0
IV期: 任何T、任何N、 M1
M0:无远处转移的临床或影像学证据 M1:通过传统临床和影像学方法发现的远处转移和/或组织学证实超过0.2cm的转移灶
NCCN对证据和共识的分类
1类
基于高水平证据(如随机对照试验)提出的建议,专家组一致同意。
2A类 基于低水平证据提出的建议,专家组一致同意。 2类
关于导管原位癌中阴性病理切缘的定义还存在很大分歧。分歧的产生有以下几个原因:疾病存在异质性、难以区分增生的 不同状况、切缘位置的解剖考虑,以及缺乏有关导管原位癌预后资料的前瞻性资料。
• 专家普遍认为,大于10 mm的切缘属阴性(但此切缘宽度也许过大,而且可能影响美观) • 小于1 mm的切缘被认为不足够 • 对于范围在1~10 mm之间的切缘,一般切缘越宽,局部复发率越低。但是对于位于乳腺纤维-腺分界部
原发肿瘤≤0.5 cm或 原发肿瘤微浸润
美国临床肿瘤学会乳腺导管原位癌保留乳房手术切缘指南

·国外医学·美国临床肿瘤学会乳腺导管原位癌保留乳房手术切缘指南DOI :10.3877/cma.j.issn.1674-0807.2016.06.015作者单位:400038重庆,第三军医大学西南医院乳腺外科(黎君彦、齐晓伟);618000四川省德阳市人民医院乳腺外科(黎君彦)尽管保留乳房治疗(breast conserving therapy ,BCT )在乳腺导管原位癌(ductal carcinoma in situ ,DCIS )中应用广泛,但目前还没有对最佳的无瘤切缘宽度形成共识。
资料显示,大约每3例行BCT 的DCIS 患者中就有1例需要再次手术。
针对上述问题,肿瘤外科学会(Society of Surgical Oncology ,SSO )、美国放射肿瘤学会(American Society for Radiation Oncology ,ASTRO )和美国临床肿瘤学会(American Society of Clinical Oncology ,ASCO )通过一项涵盖20项研究的系统评价(纳入7883例患者)和其他已发表数据,制定了新版DCIS 保留乳房手术+全乳放射切缘共识指南,并于2016年8月15日在线发表在《临床肿瘤学杂志》(J Clin Oncol )上,现将该指南摘译如下。
一、阳性切缘问题:切缘阳性是否增加同侧乳腺肿瘤复发(ipsilateral breast tumor recurrence ,IBTR)率?全乳放射治疗(whole-breast irradiation ,WBRT )会降低这种风险吗?推荐:阳性切缘定义为切缘被墨汁染色。
切缘阳性会显著增加IBTR风险,这种风险的增加不能被WBRT 抵消。
推荐强度:强。
证据强度:强(随机对照试验Meta 分析;观察性研究Meta 分析;单个随机对照研究)。
对于阳性切缘,一致认为其预示着潜在的切除不完全和IBTR风险增加。
2020年《美国外科年鉴》解读:早期乳腺癌保乳总生存期优于全乳切除

2020年《美国外科年鉴》解读:早期乳腺癌保乳总生存期优于全乳切除手术治疗是影响乳腺癌患者生存预后的重要因素,如何更好地选择手术方式使早期的乳腺癌患者获得更佳的生存结局?早期乳腺癌患者,其手术方式大体可分为乳腺癌根治手术与保乳手术两种。
这两种手术方式所取得的不同生存结局,一直是乳腺外科医师所争论探讨的话题。
目前,对于早期乳腺癌治疗方式的推荐,主要参考的是著名的NSABP B-06试验,该研究选取了2163例早期乳腺癌患者(1976~1984),证实了乳房保乳手术联合放射治疗与全乳根治性切除具有几乎等效的生存结局,该试验20年随访结果于2002年公布于著名期刊《新英格兰医学杂志》。
另外,近10多年来的多项研究均证明,对于早期乳腺癌患者,乳房保乳手术联合放疗相比全乳切除术可以提高患者的总生存期。
但这些研究未将乳腺癌的共病情况及肿瘤特征纳入评价指标,包括HER-2受体状态、是否同时应用化疗或内分泌药物治疗等。
且近年来乳腺癌辅助治疗方法不断地发生着改变与创新,现代乳腺外科诊治水平正飞速发展,故在此情况下,多种肿瘤相关指标的评价及非手术治疗方法的联合应用是否会对两种手术治疗方式后患者总生存期的评价产生影响引人思考。
2020年7月13日,美国《肿瘤外科年鉴》在线发表了涉及20余万例乳腺癌患者的大数据分析报告,该报告利用美国国家癌症数据库近10年来的早期乳腺癌患者数据,对他们的5年、7年的总生存结局进行了对比分析。
作者首先从美国国家癌症数据库提取2004~2015年间的患者数据,获取了I~II期乳腺癌女性患者共计431899 例数据,其中302299 例进行了乳腺癌保乳治疗(乳房肿块切除术+放疗),129600 例进行了乳房全切除术。
考虑到评价参数较多,为减少数据偏差与混杂变量的影响,采用倾向评分匹配,根据年龄、种族、合并症评分、肿瘤部位、左侧右侧、单侧双侧、组织学类型、分级、肿瘤大小、局部淋巴结状态、淋巴血管浸润、激素受体状态、化疗和内分泌治疗等特征,按1∶1的比例,匹配对之间最大允许差值为10%,并以总生存期为主要结局衡量指标。
2017年St.Gallen国际乳腺癌会议内外科热点问题解读

2017年St.Gallen国际乳腺癌会议内外科热点问题解读郑亚兵;俞洋;王晓稼【摘要】两年一度的St.Gallen国际乳腺癌会议与专家共识是对过去2年来乳腺癌领域所出现的新的治疗证据的盘点和总结.第15届St.Gallen国际乳腺癌会议就早期乳腺癌新辅助化疗、辅助化疗、辅助内分泌治疗、辅助靶向治疗的“加减法”进行了充分的讨论与表决,外科领域就保乳手术、前哨淋巴结活检术的适应证和禁忌证等问题以及新辅助化疗后的保乳术和前哨淋巴结活检进行了重点讨论;会议注重“对患者利益最大化,损害最小化”的原则,使乳腺癌综合治疗更加“精准”和“个体化”.本文对内外科的热点问题作一解读.【期刊名称】《健康研究》【年(卷),期】2017(037)004【总页数】5页(P361-365)【关键词】乳腺肿瘤;治疗;共识;解读【作者】郑亚兵;俞洋;王晓稼【作者单位】浙江省肿瘤医院肿瘤内科,浙江杭州310022;浙江省肿瘤医院肿瘤内科,浙江杭州310022;浙江省肿瘤医院肿瘤内科,浙江杭州310022【正文语种】中文【中图分类】R737.92017年3月15—18日第15届St.Gallen国际乳腺癌会议在美丽的奥地利首都维也纳盛大召开。
今年大会的主题是在早期乳腺癌的治疗决策上如何做到根据临床病理特征和分子分型进行加法和减法的合理应用,从而最大程度避免治疗不足或治疗过度,实现“量体裁衣”的个体化治疗。
会议最后一天,来自全球53位乳腺癌专家组成员对200余个乳腺癌诊治领域的热点问题进行投票表决,并形成了专家共识。
本文将对内外科治疗部分的共识进行解读。
1.1 辅助内分泌治疗的“加法”与“减法” 对于绝经前激素受体阳性的早期乳腺癌患者,加与不加卵巢功能抑制(Ovarian Function Suppression,OFS)一直存有争议。
两个关键性临床研究(SOFT[1]和TEXT[2])结果给出了答案:对于年轻的(<35岁)、淋巴结转移数目较多的(≥4枚以上)、化疗后仍保持绝经前状态的患者,建议加用OFS,至于是OFS联合三苯氧胺(TAM)还是联合芳香化酶抑制剂(AI),TEXT研究的结果提示OFS联合AI比OFS联合TAM有更好的DFS获益。
NCCN临床实践指南关于期转移复发乳腺癌部分解读讲课文档

• 对于绝经后妇女,抗雌激素治疗无效或超过1 年以上的抗雌
激素治疗,选项包括芳香酶抑制剂,或选择性雌激素受体调 节剂,或ER 调节剂。一些研究显示,芳香化酶抑制剂可能比他
莫昔芬有更好的获益,但差异不大。
第十七页,共31页。
对于既往抗雌激素治疗或一年内有抗雌激素治疗的绝 经后病人,证据支持选择性使用芳香化酶抑制剂作 为首选一线治疗复发性疾病。
清扫术,但可以考虑行再次前哨淋巴结活检术代替腋窝清扫术。
第五页,共31页。
1.3远处转移病灶的局部处理: 新版指南建议如果出现下列临床状况如脑转移、软脑膜及脉络膜转移、胸腔积液、心包积液
、胆道梗阻、输尿管梗阻、即将发生的病理性骨折、脊髓压迫及局部骨或软组织转移, 如给病人造成巨大痛苦,则外科手术、放射治疗或区域性化疗(如鞘内注射甲氨蝶呤) 可考虑作为局部控制的手段。 新版指南甚至支持包括考虑对于复发、转移病灶附加的局部高温照射治疗(3 类)
第八页,共31页。
• 新版指南建议Ⅳ期、转移复发乳腺癌在考虑综合治疗时,首先 根据是否存在骨转移对其进行分类,然后对这两个亚群进一步
按照肿瘤激素受体和人表皮生长因子受体2(HER2)状态再进
行分类。
第九页,共31页。
2.1 骨转移的综合治疗 破骨细胞活性的治疗价值在于防止骨转移病人骨折的发生;需要针对骨 疼痛、脊髓压迫进行放射治疗;同时处理高钙血症等骨骼相关事件。双 膦酸盐类药物唑来膦酸或帕米膦酸二钠已用于这一目的,对于预防骨骼 相关事件,二者均有广泛的临床试验支持。双膦酸盐类药物使用是基于 化疗或内分泌治疗基础上的;对于溶解性骨转移唑来膦酸可能优于帕米 膦酸二钠。目前的临床试验结果支持达2 年的使用双磷酸盐。
第二十二页,共31页。
乳腺癌指南解读PPT课件

浸润性乳腺癌I-IIIA(T3N1)
二、全乳切除术 后 (普通组织学类型:导管癌,小叶癌,混合型癌,化生型癌)
1.激素受体阴性,HER-2阳性 T≤0.5cm,pN0 :辅助化疗+曲妥珠单抗(2B类)(2011版是不用辅助治疗)。
T≤0.5cm,pN1mi或0.6<T≤1cm:辅助化疗+曲妥珠单抗。
T>1cm 或淋巴结阳性(>2mm的淋巴结转移灶):辅助化疗+曲妥珠单抗(1类)。
2.三阴乳腺癌 T≤0.5cm,pN0 :不用化疗。 T≤0.5cm,pN1mi或0.6<T≤1cm :考虑辅助化疗。 T>1cm 或淋巴结阳性(>2mm的淋巴结转移灶) :辅助化疗(1类)。
进 入 随 访
浸润性乳腺癌 I-IIIA(T3N1)
考虑进一步化疗和/或术前放疗
缓解
未缓解
1.化疗有效继续化疗 2.如ER和/或PR阳性则后续内分泌治疗 3.如果HER-2阳性,完成至多1年的曲妥珠单抗治疗
进入 随访
个性化治疗
浸润性乳腺癌
术后治疗( I-IIIA(T3N1) )
浸润性乳腺癌I-IIIA(T3N1)
一、保乳术后(普通组织学类型:导管癌,小叶癌,混合型癌,化生型癌) 1.对高龄低危患者可免放疗。(高龄低危患者:70岁及以上、雌激素受体(ER)阳性、临床腋窝淋巴结阴性、
浸润性乳腺癌
术前治疗(Ⅱa-IIIA T3N1M0、除了肿瘤大小外均符合保乳术要求)
浸润性乳腺癌
术前治疗(Ⅱa-IIIA T3N1M0 、除了肿瘤大小外均符合保乳术要求)
术前化疗(绝经后的激素受体阳性患者可考虑单用内分泌治疗)
任何时间PD
PR,无法切除
Ⅰ~Ⅱ期三阴乳腺癌患者保乳治疗后的预后探讨

Ⅰ~Ⅱ期三阴乳腺癌患者保乳治疗后的预后探讨吕平;崔秀洁【摘要】目的探讨分析Ⅰ~Ⅱ期三阴乳腺癌患者保乳治疗后的预后.方法在本院2014年1月至2016年1月接诊的Ⅰ~Ⅱ期三阴乳腺癌保乳治疗患者中选取90例作为本次研究的对象,采用数字表格法随机分为对照组和观察组,每组各45例.对照组采用改良根治术,观察组采用保乳术治疗,术后对两组患者进行2年随访,比较两组的术后复发率、癌细胞远端转移率及生存率等预后情况.结果观察组患者手术时间、术中出血量、平均引流量、术后并发症及住院时间等手术指标均明低于对照组(P<0.05);经过术后2年的随访了解,两组患者局部复发率、癌细胞远端转移率、术后1、2年生存率比较无明显差异;两组比较差异无统计学意义(P>0.05).结论Ⅰ~Ⅱ期三阴乳腺癌患者保乳治疗效果确切,预后较好,安全性较高.【期刊名称】《中国医药指南》【年(卷),期】2018(016)003【总页数】2页(P98-99)【关键词】Ⅰ~Ⅱ期三阴乳腺癌;保乳治疗;复发率;癌细胞远端转移率;生存率【作者】吕平;崔秀洁【作者单位】朝阳市中心医院肿瘤内科,辽宁朝阳122000;朝阳市中心医院肿瘤内科,辽宁朝阳122000【正文语种】中文【中图分类】R737.9乳腺癌是临床上常用的恶性肿瘤,三阴乳腺癌(TNBC)是指患者的雌激素受体(ER)、孕激素受体(PR)及人表皮生长因子受体(HER-2)的免疫组化检验结果呈阴性的一种乳腺癌[1]。
具有非常高的发病率,占乳腺癌发病率的10%~15%,而且其恶性程度相当高,具有病灶侵蚀性强、易复发、易转移、治疗预后差等特性[2]。
乳腺癌传统治疗采用改良根治术和放、化疗,具有安全性较高,预后较好的特点,有较好的临床治疗效果,是目前治疗早期乳腺癌的主要方法。
随着保乳治疗的逐步推广,在早期治疗中己成为首选治疗方法[3]。
其手术创面小,能最大限度保留做为女性性特征的乳房外观,消除患者形体及心理的遗憾。
Ⅰ、Ⅱ期乳腺癌保乳手术后的护理

中 图分 类号 : 436 R 7.
文献 标 识码 : B
文章 编 号 :0 6- 1 (0 1 1- 02 0 1 0- 4 12 1 )1 04 - 3 6 第 2 … 乳 腺 癌 外科 手 术经 历 了局部 切 除 术 、 a t 根 治 术 、 大 位 。 H le sd 扩 根 治 术 、 良根 治术 及 保 留乳 房 的局 部 切 除加 腋 窝 淋 巴 结 清 扫术 改
・
4 ・ 2
T ODAY NURS No e e , 0 1 No1 E, v mb r 2 1 , . 1
I Ⅱ期乳腺癌 保乳手术后的护理 、
余玲 霞
摘要 总结 了 I、 Ⅱ期乳腺癌 患者保乳手术后 的护理 经验 , 主要 包括心理护理 、 病情观察、 口及 负压 引流的护理、 能锻 炼、 伤 功 术后 综 合治疗的护理及 出院指 导等 , 为全 面、 认 系统、 规范化的护理是提 高患者生存 质量 的重要保障。
治 疗 护理 。 22 诱 导 排尿 .
老 年 急性 尿 潴 留是 泌 尿科 比较 常见 的病 症 , 者 常 常 急 诊人 患 院, 迫切 要 求 排 出尿 液 解 除 痛 苦 。 组 5 例 尿潴 留 患 者 经 过 心 理 本 0 护 理 、诱 导 排尿 法 和 穿刺 抽 尿 法等 综 合 护理 后 均 及 时排 出尿 液 ,
痊愈出院 , 无泌尿道感染等并发症的发生 。 泌尿科护士面对老年
急 性 尿潴 留患 者 应 以尊 敬 和爱 护 的态 度 、 柔 与 熟 练 的技 巧 进 行 轻 排 泄 后 的清 洁 , 意 保护 其 隐 私 , 时安 慰 老年 人 不 必 担 心 , 快 注 同 很
浸润性乳腺癌保乳治疗临床指南

浸润性乳腺癌保乳治疗临床指南1浸润性乳腺癌保乳治疗的外科技术1.1开展保乳治疗的必要条件⑴开展保乳治疗的医疗单位应该具备相关的技术和设备条件以及外科、病理科、影像诊断科、放疗科和内科的密切协作(上述各科也可以分布在不同的医疗单位)。
⑵患者在充分了解乳腺切除治疗与保乳治疗的特点和区别之后,本人具有明确的保乳意愿。
⑶患者客观上有条件接受保乳手术后的放疗以及相关的影像学随访,如乳腺X线、B超或MRI检查等(必须充分考虑患者的经济条件、居住地的就医条件及全身健康状况等)。
1.2保乳治疗的适宜人群主要针对具有保乳意愿且无保乳禁忌证的患者。
1.2.1临床Ⅰ期、Ⅱ期的早期乳腺癌肿瘤大小属于T1和T2分期,尤其适合肿瘤最大直径不超过3 cm,且乳房有适当体积,肿瘤与乳房体积比例适当,术后能够保持良好的乳房外形的早期乳腺癌患者。
1.2.2Ⅲ期患者(炎性乳腺癌除外)经术前化疗或术前内分泌治疗充分降期后也可以慎重考虑。
1.3保乳治疗的绝对禁忌证⑴同侧乳房既往接受过乳腺或胸壁放疗者。
⑵病变广泛或确认为多中心病灶,且难以达到切缘阴性或理想外形。
⑶肿瘤经局部广泛切除后切缘阳性,再次切除后仍不能保证病理切缘阴性者。
⑷患者拒绝行保留乳房手术。
⑸炎性乳腺癌。
1.4保乳治疗的相对禁忌证⑴活动性结缔组织病,尤其硬皮病和系统性红斑狼疮或胶原血管疾病者, 对放疗耐受性差。
⑵肿瘤直径>5 cm者。
⑶靠近或侵犯乳头(如乳头Paget’s病)。
⑷广泛或弥漫分布的可疑恶性微钙化灶。
1.5保乳治疗前的谈话⑴经大样本临床试验证实(超过1万名患者),早期乳腺癌患者接受保留乳房治疗和全乳切除治疗后生存率以及发生远处转移的概率相似。
⑵保留乳房治疗包括保留乳房手术和术后的全乳放疗,其中保留乳房手术包括肿瘤的局部广泛切除加腋窝淋巴结清扫或前哨淋巴结活检。
保留乳房治疗还需要配合必要的全身治疗,例如化疗和(或)内分泌治疗。
⑶术后全身性辅助治疗基本上与乳房切除术相同,但因需配合全乳放疗,可能需要增加相关治疗的费用和时间。
乳腺癌保乳手术原发灶切缘的评估

乳腺癌保乳手术原发灶切缘的评估概述乳腺癌是常见的女性恶性肿瘤之一,手术是治疗乳腺癌的主要方法之一。
对于早期乳腺癌,保乳手术已成为常规手术方式之一。
在保乳手术中,完整地切除原发灶并保护乳房组织,是一个挑战性的手术操作。
原发灶切缘是判断手术切除效果的重要指标,评估原发灶切缘是否干净是判断病人术后预后的重要指标。
评估方法术前评估1.术前超声检查:术前超声检查对乳腺内的病变进行评估,包括病变的大小、位置、数量、形态、密度、内部回声等信息,以指导手术的切除范围和手术方式。
此外,术前还应进行乳腺磁共振检查(MRI),确保完整掌握病变情况。
2.临床体检:包括检查乳房以及腋窝淋巴结情况等。
3.组织学检查:从病变部位进行乳腺细胞穿刺或者活检,确定病变是何种性质,以支持后续手术。
术中评估1.快速病理:快速病理是术中原发灶切缘的评估方法之一,通常在原发灶切除并包扎止血后,立即取出原发灶组织标本进行冰冻切片,由病理学家快速判断切缘是否清晰,以便及时调整手术切缘范围,避免误切、未切或切缘不清的情况。
2.生物蛋白芯片检测:该技术可以检测肿瘤标志物,同时还可以评估细胞的浸润深度和淋巴结转移情况。
该技术能够识别肿瘤细胞在局部组织中的分布情况,从而评价原发灶切缘的清晰度。
3.磁共振成像(MRI):MRI是一种术中三维成像技术,可以提供高分辨率的图像,非常适合于颅内和骨盆内的成像。
该技术可以评估手术切除部位周围的结构和分布情况。
术后评估1.手术部位细胞学检查:取出术后切断的组织标本,进行组织学检查,以评估原发灶切缘是否干净,是否存在病变残留或者血管侵犯情况。
2.病理学检查:确定原发灶的病理类型、大小、浸润深度并确认有无淋巴结转移,以及是否需要化疗、放疗等辅助治疗方式。
结论乳腺癌保乳手术是乳腺癌治疗的重要手术方式之一,但手术切缘是否清楚直接关系到患者的预后,对于保乳手术来说更为重要。
因此,在确定手术的范围和方法后,进行术前、术中及术后的多种方法进行原发灶切缘的评估,以便及时采取个性化的手术措施,保障手术临床治疗效果的有效实施。
Ⅰ、Ⅱ期乳腺癌的保乳治疗:国内临床对照试验的Meta分析的开题报告

Ⅰ、Ⅱ期乳腺癌的保乳治疗:国内临床对照试验的Meta分析的开题报告一、背景与意义:乳腺癌是女性最常见的恶性肿瘤,其中Ⅰ、Ⅱ期乳腺癌患者常规的治疗方式为保乳手术。
保乳手术的优点是能够保留患侧乳房,有利于提高患者的生活质量,但这种方法的风险也比较大,容易造成局部复发。
因此,对于Ⅰ、Ⅱ期乳腺癌患者是否进行保乳手术,一直是国内外学者探讨的课题,而目前尚无一个权威的标准。
中国临床医学研究中心及其合作单位“乳腺癌保乳手术治疗国内临床对照试验”(以下简称“对照试验”)旨在比较保乳手术和根治手术之间的疗效和安全性,为制定我国Ⅰ、Ⅱ期乳腺癌患者的手术治疗标准提供科学依据。
因此,本研究旨在对“对照试验”中关于保乳手术的临床对照试验进行Meta分析,探讨保乳手术在Ⅰ、Ⅱ期乳腺癌患者中的疗效和安全性,为临床提供更具参考价值的证据。
二、研究目的:①比较保乳手术和根治手术在治疗Ⅰ、Ⅱ期乳腺癌方面的效果,如局部复发率、总体生存率、恶性转归率;②对保乳手术相关的安全问题进行分析,如切缘阳性率、服务关系恶性转化率;③探讨性别、年龄、期别等因素对保乳手术效果和安全性的影响。
三、研究方法:1.论据来源:通过PubMed、Embase、Cochrane Library、Wanfang、中国知网等中英文数据库检索相关文献,同时还需手动检索国内外相关期刊,以获取尽可能多的试验和重要临床研究。
2.数据筛选:按照“对照试验”的入选标准筛选相关文献,首先根据标题和摘要进行筛选,符合研究对象的文献进行全文查阅,对符合研究对象和研究目的要求的相关文献进行筛选。
3.数据提取和数据质量评估:使用Cochrane Collaboration Workbench软件提取数据,对文献质量进行评估,包括随机性、盲法、完成度、选择偏差、掩盖偏差、检测偏差、其他偏差等方面进行评估,并综合自己的判断确定每篇文献的评分。
4.统计分析:打分后将选出的文献进行Meta分析,计算合并相对风险(RR)、合并无偏标准差(SD)、合并均值差(MD)和95%置信区间(CI),并将结果采用RevMan5.3软件做图,进行荟萃分析。
2014美国乳腺癌保乳手术切缘新指南解读

一、指南内容简介近日,外科肿瘤学会(SSO)、美国放射肿瘤学会(ASTRO)共同制定乳腺癌手术切缘新指南。
目前早期乳腺癌再切除率高达20%~25%,该指南的发布或可使接受乳房肿瘤切除术的早期乳腺癌患者的再次手术率降低。
指南规定,在多学科综合治疗时代,采用“切缘无肿瘤累及”作为浸润性癌的安全手术切缘标准;并指出,常规临床实践中采用比无瘤切缘更广泛的切缘或不可取。
“安全手术切缘的定义一直存在争议。
所以,制定一份明确的指南,以最大限度减少不必要的手术,同时保证外科手术、放射治疗的良好疗效,是十分必要的。
”SSO前任主席、指南共识小组共同主席、Memorial Sloan-Kettering癌症中心乳腺外科主任Monica Morrow表示。
“我们希望,该指南最终可使接受保乳手术的早期乳腺癌患者的高再切除率显著下降。
”指南共识小组共同主席、美国耶鲁癌症中心Meena Moran指出,“对于早期乳腺癌女性,手术联合放疗、激素治疗和(或)化疗后疾病控制良好。
因此,绝大多数再切除术是不必要的。
”Moran认为,再切除术常在首次乳房肿瘤切除术后数周进行,此时患者伤口已开始愈合。
这是因为外科医生在切除术中取出组织样本后,交由病理科医生检查并报告病理,再将结果反馈给外科医生,然后外科医生与患者讨论并作出再次手术与否的决定。
而且一般情况下,患者资料需经肿瘤专家小组审查。
显然,再切除术可能导致其他治疗(如化疗或放疗)延迟,并给患者带来心理压力、不适/疼痛、费用增加等伤害。
“最大的问题是,若有大量肿瘤负荷残留,不能经化疗、放疗或激素治疗控制,可能导致复发。
需要担心的是局部复发引致再切除,同时还应考虑是否确有必要再切除。
”她说。
新指南是由乳腺专家小组基于临床证据达成的共识。
“虽然该指南应用仍需根据患者个体化情况,但应让医生和患者相信,在特定情况下放弃再切除术是可行的,从而避免过度治疗。
”Moran补充说。
二、国内专家述评邵志敏教授保乳手术是一门充满矛盾的艺术复旦大学附属肿瘤医院邵志敏教授保乳手术是一门艺术,充满矛盾的艺术,只有完美的掌控、调和其中的矛盾,才能更好的诠释这门艺术学科。
浸润性乳腺癌保乳手术切缘的研究进展

真 实 性 产 生 影 响 。本 文 就 浸 润 性 乳 腺 癌 保 乳 手 术 最 佳 的 阴 性 切 缘 阈 值 及 不 同 切 缘 评 估 方 法 的 研 究 进 展 进 行 综 述 。
Байду номын сангаас
【关 键 词 】 浸 润 性 乳 腺 癌 ;保 乳 手 术 ; 切 缘 评 估 ;阴 性 切 缘 阈 值 ;综述
评 法。 1 . 1 垂直切取法垂直切取法是目前应用最广泛的切 缘 评 估 方 法 ,其 操 作 方 法 是 外 科 医 生 切 除 手 术 标 本 后 用 缝 线 标 记 方 位 ,病 理 科 医 生 用 六 种 不 同 颜 色 的 染 料 标 记 各 个 面 ,沿 肿 物 垂 直 基 底 面 切 成 两 部 分 ,平 行 切 取 组 织 片 ,在 显 微 镜 下 观 察 切 缘 中 肿 瘤 距 离 切 取 前 后 内 外 墨 染
2 广 西 医 科 大 学 第 一 附 属 医 院 胃 肠 腺 体 外 科 ,南 宁 市 5 3 0 0 2 1 )
【提 要 】 保 乳 手 术 联 合 术 后 放 疗 已 成 为 早 期 乳 腺 癌 的 标 准 治 疗 方 式 。 在 保 乳 手 术 中 ,切 缘 阴 性 时 即 可 认 为 该 手 术 肿
【中 图 分 类 号 】 C 7 3 7 . 9 【文 献 标 识 码 】 A
D O I :1 0 . 1 1 6 7 5 / j . issn. 0 2 5 3 - 4 3 0 4 . 2 0 1 8 . 07. 2 8
【文 章 编 号 】 0 2 5 3 - 4 3 0 4 (2 0 1 8 )0 7 - 0 8 3 3 - 0 6
1 乳腺癌保乳手术切缘评估方法
乳腺癌保乳手术实施成功的关键在于获得阴性切 缘 ,准 确 、可 靠 的 切 缘 评 估 方 法 至 关 重 要 ,假 阳 性 率 高 的 切 缘 评 估 方 法 会 造 成 不 必 要 的 二 次 手 术 、较 大 的 组 织 切 除 量 、较 低 的 保 乳 成 功 率 以 及 较 差 的 美 容 效 果 ,假 阴 性 率 高 的 切 缘 评 估 方 法 易 造 成 切 缘 残 留 癌 ,从 而 使 患 者 术 后局部复发率增高。 目前国际上并无标准的切缘评估 法 ,临 床 中 常 用 的 方 法 有 垂 直 切 取 法 、切 缘 离 断 取 材 法
最新2021版NCCN乳腺癌指南更新要点(全文)
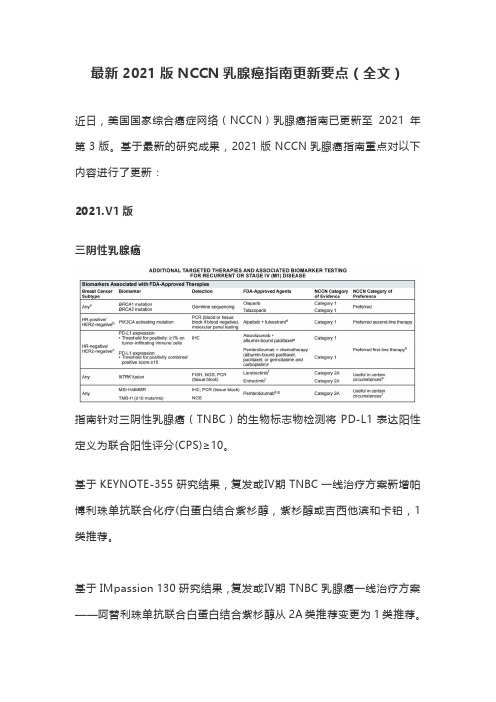
最新2021版NCCN乳腺癌指南更新要点(全文)近日,美国国家综合癌症网络(NCCN)乳腺癌指南已更新至2021年第3版。
基于最新的研究成果,2021版NCCN乳腺癌指南重点对以下内容进行了更新:2021.V1版三阴性乳腺癌指南针对三阴性乳腺癌(TNBC)的生物标志物检测将PD-L1表达阳性定义为联合阳性评分(CPS)≥10。
基于KEYNOTE-355研究结果,复发或Ⅳ期TNBC一线治疗方案新增帕博利珠单抗联合化疗(白蛋白结合紫杉醇,紫杉醇或吉西他滨和卡铂,1类推荐。
基于IMpassion 130研究结果,复发或Ⅳ期TNBC乳腺癌一线治疗方案——阿替利珠单抗联合白蛋白结合紫杉醇从2A类推荐变更为1类推荐。
指南指出,虽然一线治疗已有数据,但是如果之前没有使用过PD-L1抑制剂治疗,那么这些方案可用于二线及其后续治疗。
如果使用PD-L1抑制剂治疗时疾病进展,那么没有数据支持使用其他PD-L1抑制剂进行下一线的治疗。
HR阳性乳腺癌对于芳香酶抑制剂5年+卵巢抑制或切除的绝经前激素受体(HR)阳性的乳腺癌患者,指南新增考虑再用芳香酶抑制剂3~5年。
对于接受芳香酶抑制剂辅助治疗的绝经后(自然或诱发)HR阳性患者,考虑双膦酸盐或地舒单抗辅助治疗。
HER2阳性乳腺癌以下从“首选方案”移至“某些情况下有用”:AC→TH(多柔比星+环磷酰胺→紫杉醇+曲妥珠单抗,各种疗程);AC→THP(多柔比星+环磷酰胺→紫杉醇+曲妥珠单抗+帕妥珠单抗,各种疗程)删除脚注:回顾研究证据表明,对于HER2阳性肿瘤患者,蒽环类化疗方案可能优于非蒽环类方案。
修改脚注e:由于医学原因(例如过敏反应),对于某些患者,紫杉类(例如多西他赛、紫杉醇、白蛋白结合紫杉醇)可以互相替代。
如果替代每周紫杉醇或多西他赛,那么紫杉醇每周剂量不应超过125mg/m²。
(删除白蛋白结合紫杉醇)。
对于复发或IV期的HER2阳性乳腺癌的全身治疗,在其他推荐方案中,恩美曲妥珠单抗(T-DM1)改为1类推荐意见。
2021版CSCO乳腺癌指南:HER2+早期乳腺癌新辅助治疗更新要点解读(全文)

2021版CSCO乳腺癌指南:HER2 +早期乳腺癌新辅助治疗更新要点解读(全文)2021版CSCO乳腺癌指南关于HER2 +早期乳腺癌术前新辅助治疗的更新聚焦于三方面:新辅助治疗适应证、新辅助治疗I级推荐、新辅助治疗后辅助治疗选择。
新辅助治疗适应证:将临床分期与分子分型相结合作为依据2021版CSCO指南仍然强调,术前新辅助治疗的适应证应结合肿瘤分子分型、临床分期及患者意愿个体化确定。
这一理念也是CSCO于2018年率先在国内提出的,即对于HER2 +乳腺癌的患者,若肿瘤二2cm(T>2)或有淋巴结转移(N>1 ),推荐给予新辅助治疗。
满足以下条件之一者可选择术前新辅助药物治疗:1. 肿块较大(> 5cm )2. 胶窝淋巴细够3. HER-2阳性4. 三阴性新辅助治疗的适应证不再仅仅依据临床分期,而应结合肿瘤分子分型、临床分期及患者意愿个体化确定5.有保乳意愿,但肿瘤大小与乳房体积比例大难以保乳者注O:1. 若孚扇原发月黝大小2.0~5.0cm之间,应综合其他生物学指标选择是否先行药物治疗.2. 专家组成员认同,仅以HER-2阳性或三阴性,作为乳腺癌术前新辅助药物治疗选择的标准时,肿瘤应大于2cm ;或可以加入严格设计的临床硏究.图1 2021版CSCO指南关于术前新辅助治疗的适应证对于美国国家综合癌症网络(NCCN)指南,2018版仍然仅依据临床分期确定新辅助治疗适应证;2020版和2021版则指出,对于HER2 +、三阴性乳腺癌,若"2或N",推荐给予新辅助治疗。
可见,CSCO指南提出的分子分型与临床分期相结合的理念比NCCN 指南早了 2 年。
NCCN 指南(2018版)NCCN Guidelines Version 3.2018 Invasive Breast CancerPREOPERATIVE 8Y8TEMIC THERAPY FOR OPERABLE DISEASE WORKUP CLINICALSTAGE图2 2018版和2020版NCCN 指南推荐然而,2021版美国临床肿瘤学会(ASCO )指南指出,对于T1a 和T1b 的患者,不应常规给予新辅助治疗。
降低乳腺癌再手术率主要内容

降低乳腺癌再手术率主要内容众所周知,乳腺癌是女性肿瘤患者的主要死因。
乳腺癌复发更堪称是女性肿瘤患者的噩梦,在美国每年有10%-50% 的乳腺癌患者因肿瘤复发而接受再手术治疗。
这不仅会降低乳腺癌患者的生存质量,还给患者家庭和社会带来了巨大的经济负担。
那么问题来了,有什么措施可以降低乳腺癌患者的再手术率?2015 年5 月美国乳腺外科医生协会(ASBS)召开了一场多学科共识会议,与会者包括乳腺癌治疗和护理领域专家及患者代表,旨在讨论如何降低乳腺癌患者术后的再手术率。
该会议最终以投票方式确定了10 条可以降低乳腺癌再手术率的建议,并于2015 年7 月将其发布在Annals of Surgical Oncology 上。
1. 术中严格遵循SSO-ASTRO 指南进行肿瘤边缘切除。
2014 年美国肿瘤外科协会- 美国放射肿瘤学会(SSO-ASTRO)发布的指南:(1)建议「切缘无肿瘤累及」作为Ⅰ、Ⅱ期浸润性乳腺癌保乳手术安全切缘标准;(2)常规临床实践中采用比无瘤切缘更广泛的切缘或不可取;(3)早期乳腺癌手术联合放疗、激素治疗和/ 或化疗后疾病控制良好,大多数的再切除术没有必要。
与指南后,再手术率降低了40%,该建议对乳腺癌再手术有最直接的影响。
2. 术前成像诊断。
术前成像诊断的常规技术是乳房X 射线检查,辅助技术是超声检查。
不常用的候选技术是断层扫描和磁共振成像。
3. 乳腺组织微创活检。
该建议意味着患者在术前要进行遗传学风险评估、内科肿瘤学检查、整形外科学咨询和腋窝淋巴结检查。
4. 多学科小组会诊。
在术前应明确患者癌灶病变数量、肿瘤形状、癌灶与皮肤和胸腔壁的距离、癌灶是否扩展到乳头,以便最大程度的保证肿瘤切除边缘阴性。
5. 触诊阴性乳房病变的定位。
对于触诊阴性的乳房病变,建议采取放射性粒子、术中超声和穿刺定位等手段确定病变的具体位置。
6. 借用重建外科技术。
通过切除更大体积的组织以降低阳性边缘出现的概率,从而降低乳腺癌患者的再手术率。
乳腺癌保乳手术原发灶切缘的评估

乳腺癌保乳手术原发灶切缘的评估【摘要】总结近20年来乳腺癌保乳手术原发灶切缘评估处理的主要临床证据,并详细介绍了评估方法。
【关键词】乳腺肿瘤乳腺癌保乳手术切缘(margin)是指原发灶切除后标本的边缘与癌组织间的镜下最短距离。
获得原发灶切除后阴性切缘是乳腺癌保乳手术的一项基本要求,其目的是切除病变乳腺中的可见肿瘤组织,并希望用其后的放射治疗清除可能存在于余下乳腺组织中的隐性病灶或镜下可见病灶。
在理论上,术后残余肿瘤组织在相对乏氧的疤痕环境中,更有可能耐受放射治疗而生存。
大量事实业已证明,切缘阳性会明显地增加保乳手术的局部复发率。
因此,如何正确地评估和处理原发灶手术切缘,是保乳手术实施过程中的一个非常关键的问题。
1 安全手术切缘的界定尽管大量研究均显示保乳手术的切缘状态与局部复发有关。
但到目前为止,还没有一个得到普遍认同的阴性切缘距离定义。
Gould和Robinson[1]总结了手术标本的检查处理过程及切缘取材的差异,认为其中许多因素均会影响到对切缘状态的评估结果。
实际上,即使是在同一个保乳手术随机化临床研究中,在评估切缘状态时也存在相当的实际差异。
对切缘状态的评估结果不同,是可能导致实际复发率差异的一个原因。
但无论如何,较广的切缘应该能显著减少局部复发率,这一点已为米兰癌症研究所的研究证实[2,3]。
他们将705例2.5cm的肿瘤分为象限切除(quadrantectomy)(整块切除原发灶及2cm~3cm的周围组织,包括表皮及其下胸大肌筋膜)和肿块切除(lumpectomy)两组。
两组术后均予45Gy的全乳照射剂量及15Gy 的增强照射剂量放射治疗。
尽管两组的7年生存曲线无显著性差异,但象限切除组较之肿块切除组复发率更低(分别为5.3%、13.3%)。
切缘状态病理学检查显示,象限切除组178例中有8例被确定为阳性(4.5%)。
肿块切除组289例中有46例(16%)被确定为阳性。
两组切缘阳性病例的局部复发率相比,后者比前者增高(分别为12.5%、17.4%)。
保乳手术阴性切缘切取次数与早期乳腺癌患者临床预后的相关性

保乳手术阴性切缘切取次数与早期乳腺癌患者临床预后的相关性钱炜伟;倪毅【摘要】目的:探讨早期乳腺癌保乳术中获得阴性切缘所需切取次数与患者预后的相关性.方法:收集2009年1月至2016年10月在江苏省南通市第三人民医院行保乳治疗的早期乳腺癌患者的临床资料,回顾性分析获得阴性切缘切取次数与患者年龄、肿块大小、淋巴结状态、激素受体状态、HER-2状态、病理类型及患者预后的相关性.结果:共入组287例接受保乳治疗的早期乳腺癌患者,其中191例(66.6%)经1次切取即获得阴性切缘,65例(22.6%)经2次切取获得阴性切缘,31例(10.8%)经3次及以上切取获得阴性切缘.肿块大小(P=0.010)、病理类型(P<0.001)及HER-2状态(P=0.034)与获得阴性切缘切取次数相关.中位随访5年的局部复发率在1次切取患者(6.3%)、2次切取患者(9.2%)及3次及以上切取患者(25.8%)间差异有统计学意义(P=0.002);而3组患者间中位随访5年的远处转移率(P=0.989)及总生存率(P=0.326)差异无统计学意义.结论:肿块大小、病理类型、HER-2状态与保乳患者获得阴性切缘所需切取次数相关,切取次数与术后局部复发率正相关,但与患者远处转移及总生存率无明显相关.%Objective:To analyze the correlation between re-excision frequency of breast-conserving surgery negative margins and clinical prognosis of patients with early-stage breast cancer.Methods:We collected the clinical information of early breast cancer patients treated with breast conserving therapy in the Third People's Hospital of Nantong City, Jiangsu Province, from January 2009 to October 2016.We analyzed the relationship between the frequency of re-excision and patient age, tumor size, lymph node status, hormone receptor status,Her-2, pathological type and prognosis of patientsretrospectively.Results:In this study, 287 patients with early breast cancer who underwent breast-conserving therapy were included.191 (66.6%) patients acquired negative margins by one excision, 65 (22.6%) patients by twice excision, and 31 (10.8%) patients by thrice or more.Tumor size(P=0.010), pathological type (P< 0.001), and HER-2 state (P=0.034) corrected with the frequency of re-excision.The median follow-up time was 5 years.Local recurrence rates were 6.3%, 9.2%, and 25.8% for one excision group, twice excision group, and thrice or more excision group, respectively and statistical difference was found among the three groups (P=0.002).No statistical difference was found among the three groups with regard to distant metastasis rates (P=0.989) and overall survival rates(P=0.326).Conclusions:Tumor size, type of pathology, HER-2 status were correlated with the frequency of re-excision required for negative margins in the breast-conserving patients.The frequency of re-excision is positively correlated with local recurrence rates, but had no significant relationship with distant metastasis and overall survival rates.【期刊名称】《中国临床医学》【年(卷),期】2017(024)003【总页数】4页(P423-426)【关键词】早期乳腺癌;保乳手术;阴性切缘;切取次数;预后【作者】钱炜伟;倪毅【作者单位】南通市第三人民医院甲乳科, 南通 226001;南通市第三人民医院甲乳科, 南通 226001【正文语种】中文【中图分类】R737.9乳腺癌是女性最常见的恶性肿瘤[1]。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
中国实用外科杂志 2014 年 4 月 第 34 卷 第 4 期
· 295 ·
临床问题 阳性切缘绝对增加 IBTR 风险吗?放疗、系 统治疗和好的肿瘤生物学可以降低这风 险? 较宽的切缘是否降低 IBTR?
内分泌、生物靶向治疗或化疗等对 IBTR 的 影响?没有接受这些系统治疗者是否需要 更宽的切缘? 不良的生物学亚型(如三阴性乳腺癌)是否 需要较宽的切缘? 切缘宽度是否取决于实施 WBRT? 切缘存在 LCIS 是否需再切除?ILC 是否需 要较宽的切缘?切缘多形 LCIS 的意义? <40 岁的年轻乳腺癌病人需较宽的切缘 吗? 肿瘤标本中有 EIC 的意义以及对切缘的影 响?
Interpretation of the American Guidelineቤተ መጻሕፍቲ ባይዱon Margins for
Breast- Conserving Surgery in Stages Ⅰ and Ⅱ Invasive
Breast Cancer
WU Ke-jin. Department of General
Oncology (ASTRO) issued the guideline on margins for
beast-conserving surgery in stage I and Ⅱ invasive breast
cancer. A multidisciplinary consensus panel developed the
注:引自参考文献[1-3]
表 1 临床指南推荐总结
推荐 切缘阳性至少增加 2 倍 IBTR 风险,且并不随着实 施放疗、系统治疗和好的生物学情况而降低
切 缘 阴 性 ,即“ 切 缘 无 肿 瘤 累 及 ”可 有 益 于 避 免 IBTR,更宽的切缘对此无助而不予推荐 应用系统综合治疗可减少 IBTR,但没有证据表明 较宽的切缘不需要这种治疗
接受 WBRT 和综合治疗支持等,因此得到的结论只可应用 于背景相似的病例。另外一些特殊情况并未列入该荟萃 分析,如近切缘残留可疑微钙化者、Ⅲ期乳腺癌、接受新辅 助化疗者、单纯 DCIS 以及只接受部分乳腺放疗或未经放疗 的病人等等。因此,不能将该指南简单理解为“切缘无肿 瘤累及就是安全切缘”。每例病人应该由多学科小组进行 综合评估后决定治疗方案。
作者单位:上海交通大学医学院附属新华医院普外科, 上海 200092
E-mail:kejinwu@
《Ⅰ、Ⅱ期浸润性乳腺癌保乳手术的切缘指南》(以下简称 指 南)同 时 发 表 在 临 床 肿 瘤 学 杂 志(Journal of Clinical Oncology)、国 际 放 射 肿 瘤 学·生 物 学·物 理 学 杂 志 (International Journal of Radiation Oncology Biology Physics) 和外科肿瘤学年鉴(Annals of Surgical Oncology)上。至此, 一直存在多方争议的关于早期浸润性乳腺癌保乳手术的 安全切缘问题终于有了一个比较明确的共识。本文简述 该指南要点以飱读者。
widely clear margins than no ink on tumor adopted common in
the clinical work is not necessary.
Keywords breast cancer; breast-conserving surgery;
surgical margin
综上所述,由该指南非常及时地明确了阴性切缘的定 义,不仅有益于临床医师的工作,也为病人提供了医学信 息,使其能更好地了解自身病情。但是任何指南总归存在 某些局限性,临床医师在实践过程中,应加强多学科合作, 重视肿瘤病人的个体化治疗。
参考文献
[1] Moran MS, Schnitt SJ, Giuliano AE, et al. Society of Surgical Oncology-American Society for Radiation Oncology consensus guideline on margins for breast-conserving surgery with whole-breast irradiation in stages I and II invasive breast cancer [J]. Int J Radiat Oncol Biol Phys, 2014, 88(3):553-564.
[2] Moran MS, Schnitt SJ, Giuliano AE, et al. Society of Surgical Oncology-American Society for Radiation Oncology consensus guideline on margins for breast-conserving surgery with whole-breast irradiation in stages I and II invasive breast cancer [J]. J Clin Oncol, 2014,[Epub ahead of print].
guideline. Based on the results of meta-analysis, it is clear
that the use of no ink on tumor as the standard for an adequate
margin in early invasive breast cancer is reasonable. More
Surgery, Xinhua Hospital, Shanghai Jiaotong University School
of Medicine, Shanghai 200092, China
Abstract From February to March in 2014, Society of
Surgical Oncology (SSO) and American Society for Radiation
切缘宽度不取决于生物学亚型
WBRT 的选择不依赖于切缘宽度 浸 润 性 小 叶 癌 无 需 较 宽 的 切 缘 ;切 缘 有 经 典 的 LCIS 非再切除指证;切缘多形 LCIS 的意义不确定 没有证据显示较宽的切缘降低年轻乳腺癌的 IBTR
没有证据显示当切缘阴性时增加这类病例的 IBTR
证据级别 Meta 分析和来自前瞻性试验和回顾 性研究的 2 级数据
· 294 ·
中国实用外科杂志 2014 年 4 月 第 34 卷 第 4 期
指南解读
文章编号:1005-2208(2014)04-0294-02
美国《Ⅰ、Ⅱ期浸润性乳腺癌保乳手术的切缘指南》 要点解读
吴克瑾
【摘要】 2014 年 2—3 月,外科肿瘤学会(Society of Surgical Oncology,SSO)和美国放射肿瘤学会(American Society for Radiation Oncology,ASTRO)颁布了由多学科领域专家共同 制定的《Ⅰ、Ⅱ期浸润性乳腺癌保乳手术的切缘指南》。指 南基于荟萃分析结果,提出在多学科合作治疗中,“切缘无 肿瘤累及”可作为Ⅰ、Ⅱ期浸润性乳腺癌的安全手术切缘 标准,临床上通常采用的比无瘤切缘更广泛的切缘并无必 要。 【关键字】 乳腺癌;保乳术;手术切缘 中图分类号:R6 文献标志码:A
1 指南简介 为明确乳腺癌保乳手术切缘宽度与同侧乳腺肿瘤复发
(ipsilateral breast tumor recurrence,IBTR)的相关性,制定保 乳手术及术后辅助放疗的手术切缘指南,由数名包括乳腺 外科、肿瘤内科、放疗以及病理学等多学科临床医师,甚至 病人代表组成了专家委员会,共同撰写指南,该指南获得 专家委员会的一致通过,并在听取了编外专家的反馈建议 后最终成文,经 SSO 和 ASTRO 批准。
Meta 分析、回顾性研究
多项随机试验、Meta 分析
多项回顾性研究
回顾性研究 回顾性研究
来自前瞻性试验和回顾性研究的 2 级数据 回顾性研究
2 指南解读 2.1 手术切缘标准界定合理 切缘复发是保乳术后局部 肿瘤复发的主要表现之一。在诸多影响切缘复发的因素 中最主要的是由于切缘不够导致的肿瘤残留,而此恰恰为 外科医师可控的一个重要环节。本次基于特定人群的荟 萃分析纳入了多项 1 级证据水平数据和大型回顾性研究资 料,提供了令人信服的证据。根据该荟萃分析得到结果而 制定的早期乳腺癌保乳手术的切缘指南获得了广泛认 同。本指南提出的采用“切缘无肿瘤累及”作为早期浸润 性乳腺癌保乳手术切缘标准体现了安全性和合理性,让 “特定情况下放弃再切除术”有据可依,从而避免过度治 疗。该指南可能潜在改变目前的临床工作常规,在降低再 手术率的同时保证良好疗效,可最大限度减少不必要的手 术进而减少手术创伤。 2.2 规定的切缘标准易于临床实施 现行的保乳手术阴 性切缘宽度有 1~10 mm,尺度不一,大多数操作建议集中 在 2~5 mm。“阴性切缘到底达到多少宽度才足够”一直是 临床医师讨论的热点。临床实践中,外科医生很难在术中 精准地把握这几个毫米的差别。临床常用的标识所切除 标本切缘的方法包括墨水染色法、简单易行的 5 点标记法 (即在切除标本的上、下、内、外和底部各点标记)等,传统 切缘判断多以肿瘤距切缘的最短距离和切缘的病理点状 取材为准,有较大的随意性和不确定性。指南规定的墨水 染色技术使保乳手术切缘的评估较为客观、可靠。“切缘无 肿瘤累及”直接成为病理判断的惟一指标,从而使切缘问 题得以明确,更易于临床实施。 2.3 指南存在一定局限性 指南是由乳腺专家委员会根 据临床证据达成的共识,但本次荟萃分析基于特定的人 群,如早期浸润性乳腺癌(Ⅰ、Ⅱ期浸润性乳腺癌)病人,且
专家委员会针对手术切缘宽度与 IBTR,采用荟萃分析 方法,收集了包含 28 162 例病人的 33 个研究,时间跨度从 1965 年至 2013 年 1 月,中位随访时间为 79.2 个月,中位 IBTR 发生率为 5.3%。入选或排除标准:(1)Ⅰ、Ⅱ期浸润性 乳腺癌病人,不包括接受新辅助化疗的或单纯导管原位癌 (ductal carcinoma in situ,DCIS)病人;(2)所有实施 BCT 病 人 均 接 受 辅 助 全 乳 放 疗(whole-breast radiation therapy, WBRT);(3)镜下切缘必须定量报告;(4)必须呈现年龄资 料;(5)至少中位随访时间为 4 年。Meta 分析结果发现,手 术切缘阳性与 IBTR 发生风险成倍增加具有明显相关性,必 需再次进行手术切除;切缘阴性则无需再手术;系统性综 合治疗可降低局部复发风险,但是没有证据表明较宽的切 缘可以不需要综合治疗;无论何种生物学亚型、切缘尚存 小叶原位癌(lobular carcinoma in situ,LCIS)、浸润性小叶癌 (invasive lobular carcinoma,ILC)、含有广泛的导管内癌成 分(extensive intraductal component,EIC)的浸润性癌以及年 轻乳腺癌,都没有证据表明需要较宽的切缘。基于 Meta 分 析的 8 项辨证推荐建议详见表 1。指南规定,在多学科合作 和综合治疗前提下,“切缘无肿瘤累及”可作为Ⅰ、Ⅱ期浸 润性乳腺癌的安全手术切缘标准,而目前临床实践中通常 采用的比无瘤切缘更广泛的切缘并不可取。
