有机化学课件_徐寿昌版_12--13章
有机化学课件(徐寿昌)

的顺序和空间排列方式不同.) 例1:乙醇和二甲醚 CH3CH2-OH, CH3-O-CH3
例2:丁烷和异丁烷 CH3CH2CH2CH3, CH3CH(CH3)CH3
◎碳化合物含有的碳原子数和原子种类越多,它的同
分异构体也越多。如: C7H16的同分异构体数 9 个;
★键的极性大小主要取决于成键两原子的电负性
值之差,与外界条件无关,是永久的性质。
电负性:一个元素吸引电子的能力。
偶极矩:正电中心或负电中心的电荷与两个电荷中心之
间的距离d的乘积. (方向性:正到负,一般用符号 表示。 qd (D,德拜)
■ 在两原子组成的分子中,键的极性就是分子的极性,键
的偶极矩就是分子的偶极矩。
它原子所形成的两个共价键之间的夹角.
(3)键能 ——气态原子A和气态原子B结合成A-B分
子(气态)所放出的能量,也就是气态分子A-B离解 成A和B两个原子(气态)时所吸收的能量.
键能泛指多原子分子中几个同类型键的离解能的
平均值.
离解能 :一个共价键离解所需的能量 .指离解特定共
价键的键能.(在多原子分子中,即使相同的键其解
一.有机化合物和有机化学
◎1806年柏则里斯(Berzelius)首先提出(有机
化学)名词,以区别于其它矿物质的化学 ——
无机化学
◎1828年,魏勒(F.Wöhler)在实验室由氰酸铵
(NH4OCN)合成尿素(NH2CONH2),促进了有机
化合物的人工合成:
O N H O C N 4 H H NC N 2 2
C8H18的同分异构体数可达18个;
C10H22的同分异构体数可达75个。
2.性质上:① 容易燃烧 ② 热稳定性差 ③ 熔点、沸点低 ④ 难溶于水; ⑤ 反应速度慢 ⑥ 副反应多 三、有机化合物中的共价键 共价键广泛存在于有机物中,也可说共价键 是有机物的结构基础。关于共价键,目前有两 种常用的理论: ◎1、价键理论 从“形成共价键的电子只处于形成共价键两原子 之间” 的定域观点出发。
徐寿昌主编《有机化学》(第二版)_0

徐寿昌主编《有机化学》(第二版)篇一:徐寿昌主编(第二版)-课后1-13章习题答案1第一章有机化合物的结构和性质无课后习题第二章烷烃1.用系统命名法命名下列化合物:1.(CH3)2CHC(CH3)22.CH3CH2CH2CH2CH3CH3CHCH3CH3CH(CH3)22,3,3,4-四甲基戊烷3-甲基-4-异丙基庚烷23.178CH3CH2C(CH3)2CH2CH3CH3CHCH3CH2CH36322223345CH33,3-二甲基戊烷 2,6-二甲基-3,6-二乙基辛烷6532146.8.6754212,5-二甲基庚烷2-甲基-3-乙基己烷7.2,4,4-三甲基戊烷 2-甲基-3-乙基庚烷2.写出下列各化合物的结构式:1.2,2,3,3-四甲基戊烷2,2,3-二甲基庚烷CH3CH3CH3CH2CH333CH3CH32CH2CH2CH333、 2,2,4-三甲基戊烷4、2,4-二甲基-4-乙基庚烷CH3CH333CH3CH3CH3CHCH2CCH2CH2CH335、 2-甲基-3-乙基己烷6、三乙基甲烷CH3CH3CHCHCH2CH2CH32CH3CH3CH2CHCH2CH32CH37、甲基乙基异丙基甲烷 8、乙基异丁基叔丁基甲烷CH3CHCH(CH3)22CH3CH3CH2CHC(CH3)3CH2CHCH3CH33.用不同符号表示下列化合物中伯、仲、叔、季碳原子11.100343210012CH312CH3CH31CH2.13323)33312.3.4.5.6.5.不要查表试将下列烃类化合物按沸点降低的次序排列:(1) 2,3-二甲基戊烷(2) 正庚烷 (3) 2-甲基庚烷 (4) 正戊烷 (5) 2-甲基己烷解:2-甲基庚烷>正庚烷> 2-甲基己烷>2,3-二甲基戊烷> 正戊烷(注:随着烷烃相对分子量的增加,分子间的作用力亦增加,其沸点也相应增加;同数碳原子的构造异构体中,分子的支链愈多,则沸点愈低。
有机化学徐寿昌第二版第12章醛和酮核磁共振

◆醛酮的红外光谱
羰基化合物在1680~1850cm-1处有一个强的羰基伸 缩振动吸收峰。醛基C-H在2720cm-1处有尖锐的特征 吸收峰。
乙醛的红外光谱
1
2
羰基若与邻近基团发生共轭,则羰基吸收频率降低: 苯乙酮的红外光谱
12.4.1 亲核加成反应 ◆烯烃的加成一般为亲电加成. ◆醛、酮的加成为亲核加成,易与HCN、NaHSO3、
R1 R2
例如:
C=C
R1 R2
+Ph3P=O
=O + Ph3P=CH2
=CH2
CH3CH=CHCHO+ Ph3P=C(CH3)2
CH3CH=CHC=C(CH3)2
该反应1945年由德国化学家Wittig发现,对有机合成特别是 维生素类的合成做出了巨大贡献。1979年Wittig 在82岁时获得了 Nobel化学奖.
◆反应历程(亚硫酸氢根离子为亲核试剂):
O
◆ -羟基磺酸钠与等摩尔的NaCN作用,则磺酸基可 被氰基取代,生成 -羟基腈,避免用有毒的氰化氢, 产率也比较高。
PhCHONaHSO3PhCHSO3NaNaCNPhCHCNHCl/△ PhCHCOOH
OH
OH
OH
பைடு நூலகம்
◆醛酮与NaHSO3的加成反应活性: 甲醛>乙醛>苯甲醛>丙酮>环戊酮>苯乙酮(不反应).
◆希夫碱还原可得仲胺。在有机合成上常利用芳醛与 伯胺作用生成希夫碱,再还原来制备仲胺。
⑦醛酮与Wittig试剂的加成:
Wittig试剂为磷的内蓊盐,即磷叶立德.由三苯基磷 与卤代烷反应得到磷盐.磷盐与碱作用得到Wittig试 剂: Ph3P+—C-R1(R2). 反应通式为:
徐寿昌主编《有机化学》(第二版)-课后1-13章习题答案
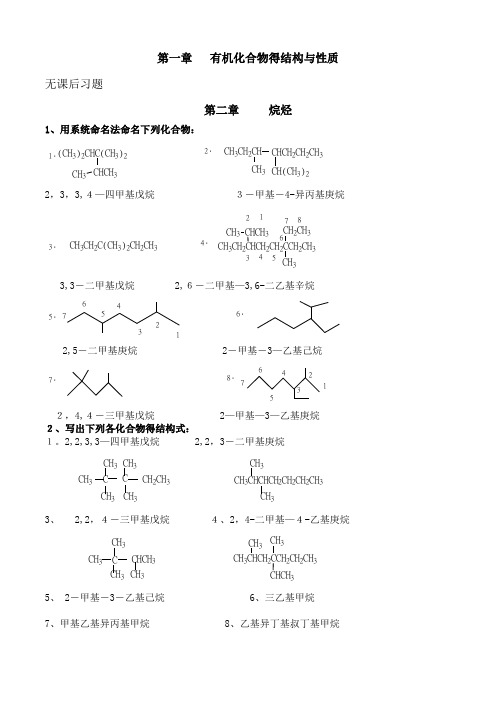
第一章 有机化合物得结构与性质无课后习题第二章 烷烃1、用系统命名法命名下列化合物:1.(CH 3)2CHC(CH 3)2CHCH 3CH 32.CH 3CH 2CH CHCH 2CH 2CH 3CH 3CH(CH 3)22,3,3,4—四甲基戊烷 3-甲基-4-异丙基庚烷3.CH 3CH 2C(CH 3)2CH 2CH 34.CH 3CH 3CH 22CH 2CCH 2CH 3CHCH 3CH 3CH 2CH 3123456783,3-二甲基戊烷 2,6-二甲基—3,6-二乙基辛烷5.12345676.2,5-二甲基庚烷 2-甲基-3—乙基己烷7.8.12345672,4,4-三甲基戊烷 2—甲基—3—乙基庚烷2、写出下列各化合物得结构式:1。
2,2,3,3—四甲基戊烷 2,2,3-二甲基庚烷CH 3CCCH 2CH 3CH 3CH 3CH 3CH 3CH 3CH 3CHCHCH 2CH 2CH 2CH 3CH 33、 2,2,4-三甲基戊烷 4、2,4-二甲基—4-乙基庚烷CH 3C CHCH 3CH 3CH 3CH 3CH 3CHCH 2CCH 2CH 2CH 33CH 3CH 35、 2-甲基-3-乙基己烷6、三乙基甲烷7、甲基乙基异丙基甲烷 8、乙基异丁基叔丁基甲烷CH3CHCH(CH3)2 CH2CH3CH3CH2CH C(CH3)3CH2CHCH3CH33、用不同符号表示下列化合物中伯、仲、叔、季碳原子3CH2CCH32CH3CCH3CH31.0010111112CH342.43001323)3342.3.4.5.6.1.5、不要查表试将下列烃类化合物按沸点降低得次序排列:(1)2,3-二甲基戊烷(2)正庚烷(3)2-甲基庚烷(4)正戊烷(5) 2-甲基己烷解:2-甲基庚烷>正庚烷〉 2-甲基己烷〉2,3-二甲基戊烷>正戊烷(注:随着烷烃相对分子量得增加,分子间得作用力亦增加,其沸点也相应增加;同数碳原子得构造异构体中,分子得支链愈多,则沸点愈低。
有机化学课件徐寿昌全精品PPT

根据IUPAC命名法,烷烃的命名基于其碳原 子数和结构。直链烷烃称为正烷烃,带有支 链的称为异烷烃。
物理性质
化学性质
烷烃通常为无色、无味、非极性的气体或液 体,不溶于水,易溶于有机溶剂。
烷烃的主要化学反应包括燃烧、卤化、裂化 等。
烯烃
定义与通式
烯烃是含有至少一个碳碳双键的 烃类化合物,通式为CnH2n。
机理
通常通过离子型或自由基型机理进行,与取 代反应和加成反应密切相关。
实例
乙醇在浓硫酸存在下发生消除反应,生成乙 烯和水。
重排反应
01
定义
有机分子中原子或基团的位置发生 重新排列的反应。
机理
通常涉及碳正离子、碳负离子或自 由基等中间体的形成和重排。
03
02
种类
频哪醇重排、贝克曼重排、霍夫曼 重排等。
有机化合物分类及命名
分类
按照碳架分类、按照官能团分类、按 照性质分类等。
命名
系统命名法、普通命名法、衍生物命名 法等,遵循IUPAC命名规则。
有机化学发展历史
早期历史
从天然有机物的提取和利用开始,如糖、油脂、染料等。
现代发展
合成有机化学的兴起,如塑料、橡胶、药物等人工合成有机物 的广泛应用。
有机化学在现实生活中的应用
物理性质
芳香烃通常为无色或淡黄色的液体或固体, 具有特殊的芳香气味,不溶于水,易溶于 有机溶剂。
命名与结构
芳香烃的命名基于其苯环数和取代基的种 类和位置。苯环是芳香烃的核心结构,具 有特殊的稳定性和芳香性。
化学性质
芳香烃的主要化学反应包括取代、加成、 氧化等。由于苯环的稳定性,芳香烃通常 比脂肪烃更难发生化学反应。
实例
有机化学课件(徐寿昌__全)2

◎异烷基:
CH3CH(CH2)n CH3
(n0) 型的烷基叫
异烷基,用“iso-”表示。
eg:异戊基
CH3CHCH2CH2 CH3
◎叔烷基:去掉一个叔氢原子所得的烷基。
用“t-”或“tert-”表示。
eg:叔丁基
CH3 CH3 C CH3
常用基团的英文简写
Me—甲基;
n-Pr—正丙基; n-Bu—正丁基; t-Bu—叔丁基(三级丁基); Ar—芳基; Ph—苯基;
CH3
CH2CH3 H H CH3 H H
H3CH2C C H
重叠式、交叉式构象比较:
交叉式构象因两个碳原子上的氢原子距离最大,其排斥力较 小,分子内能最低,因而较稳定,为优势构象。
重叠式
重叠式
12.6kJ/mol
交叉式
交叉式
交叉式
乙烷分子各种构象的能量曲线
二.丁烷的构象
丁烷C(2)-C(3)键旋转引起的各构象的能量变化
甲烷的四面体结构
◎sp3杂化轨道:
基态 1s22s22px12py1
1s22s12px12py12pz1
激发态
一个s轨道与三个p轨道形成四个sp3杂化轨道
甲烷的四个C-H 键:
键——凡是成键电子云对键轴呈圆柱形对称的键均称为 键.以 键相连的两个原子可以相对旋转而不影响电子云的分 布.
5' CH
2
3 CH 2
2 1 CHCH 3 CH 3
6' CHCH 3
7'
2,5-二甲基-4-异丁基庚烷
CH 3
CH 2CH 3
7 6
CH 3
5 4
3 2
1 7
有机化学课件徐寿昌

碳氢化合物的衍生物
研究烃的衍生物,如醇、醛、酮、羧 酸等有机化合物的结构和性质。
有机化学的发展历史
01
02
03
萌芽时期
从远古时期人们使用天然 有机物开始,到18世纪化 学家开始研究有机物的组 化学家李 比希和法国化学家贝采利 乌斯为代表,建立了有机 化学的基本理论和方法。
醇、酚、醚具有氧化反应、酯化反应、醚化反应等化学性质。其中,氧化反应是醇的重要反应之一,可用于合成 醛、酮等化合物;酯化反应是醇和羧酸的重要反应之一,可用于合成酯类化合物;醚化反应则是醇与醇之间的重 要反应之一,可用于合成醚类化合物。
醛、酮、醌
醛的分类和命名
酮的分类和命名
醌的分类和命名
醛、酮、醌的物理 性质
品质。
环境领域
研究有机污染物的来源 、迁移转化和治理方法
,保护生态环境。
02 有机化合物的结构与性质
有机化合物的结构特点
碳原子的四价性
碳原子最外层有四个电子 ,可以形成四个共价键, 是有机化合物结构多样性 的基础。
碳链和碳环
碳原子之间可以通过共价 键形成碳链和碳环,构成 有机化合物的基本骨架。
官能团
醛、酮、醌的物理性质 与其结构密切相关,一 般具有较低的沸点和熔 点,且随着分子量的增 加,沸点和熔点逐渐升 高。此外,它们还具有 一定的溶解性和极性。
醛和酮具有还原性、氧 化反应、缩合反应等化 学性质;而醌则具有氧 化性、还原性以及亲电 取代反应等化学性质。 这些反应在有机合成中 具有重要的应用价值。
醚的分类和命名
醚是氧原子连接两个烃基的化合物 ,根据烃基的不同,醚可分为单醚 、混醚等。醚的命名遵循系统命名 法。
醇、酚、醚
醇、酚、醚的物理性质
有机化学徐寿昌12PPT课件

• -羟基磺酸钠与等摩尔的NaCN作用,则磺酸基可被氰
基取代,生成 -羟基腈,避免用有毒的氰化氢,产率也
比较高。
-
22
•3 与醇加成
•将醛溶液在无水醇中通入HCl气体或其他无水强酸, 则在酸的催化下,醛能与一分子醇加成,生成半缩醛。 半缩醛不稳定,可以和另一分子醇进一步缩合,生成 缩醛:
• 也可用希腊字母表示靠近羰基的碳原子,其次为、 、…...
-
8
例如:
(2)芳香醛、酮的命名,常将脂链作为主链,芳环为取 代基:
-
9
(3) 二元酮命名时,两个羰基的位置除可用数字标明外, 也可用、、…表示它们的相对位置, 表示两个羰 基相邻, 表示两个羰基相隔一个碳原子:
-
10
3、根据来源采用俗名:
CH3CH=CHCHO
CH=CHCHO
巴豆醛(2-丁烯醛) 肉桂醛(3-苯基丙烯醛)
CHO OH
水杨醛(邻羟基苯甲醛)
-
11
第二节 醛酮的物理性质
• 室温下,甲醛为气体, 12 个 碳 原 子 以 下 的 醛 酮 为液体,高级醛酮为固 体。 • 低级醛有刺鼻的气味, 中 级 醛 ( C8~C13 ) 则 有 果香。
C=C 和 C=O 的区别
相同:①都含有一个δ 键,一个π 键
②碳都是sp2 杂化
不同点:
C=C
电子云分布均匀
C=O δδ
电子云分布不均匀
-
1
醛和酮在许多性质上都很相似,但结构上醛的羰基上 连有氢原子,而酮的羰基碳上连有两个有机基团。 这种结构上的区别影响了他们的化学性质:
醛十分容易被氧化,而酮很难被氧化 醛比酮更容易发生加成反应。
有机化学第二版徐寿昌主编,第十二章习题答案

第十二章 醛酮和核磁共振一、命名下列化合物:1.CH 3CHCH 2CHO CH 2CH 32.(CH 3)2CH C OCH 2CH 33.C OCH 34.CH 3OC OH 5.CHO6.C OCH 37.CH 2=CH C OCH 2CH 38.CH 3CH 2CHOC 2H 5OC 2H 59.NOH10.CH 3CH 2CH 3C OC O11.(CH 3)2C=N NO 2NH2二、 写出下列化合物的构造式:1、2-丁烯醛2、二苯甲酮3、2,2-二甲基环戊酮COCH 3CH3CH 3CH=CHCHOC O4、3-(间羟基苯基)丙醛5、甲醛苯腙6、丙酮缩氨脲CH 2CH 2CHOOHH 2C=NNHCH 3CH 3C=N NH C ONH 27、苄基丙酮 8、α-溴代丙醛CH 2CH 2CH 2CH 3C OCH 3CH CHOBr9、三聚甲醛(P292) 10、邻羟基苯甲醛CH 2OCH 2CH 2O CHO OH三、 写出分子式为C 5H 10O 的醛酮的同分异构体,并命名之。
CH 3CH 2CH 2CH 2CHOCH 3CH 3CHCH 2CHOCH 3CH 2CHCHOCH 3(CH 3)CCHOCH 3CH 2CH 2CH 3CH 3CH 2CH 2CH 3CH 3CH(CH 3)2C OC OC O酮: 2-戊酮 3-戊酮 3-甲基-2-丁酮四、 写出丙醛与下列各试剂反应所生成的主要产物:1,NaBH 4在氢氧化钠水溶液中 2,C 6H 5MgBr 然后加H 3O +CH 3CH 2CH 2OHCH 3CH 2CHC 6H 5OH3.LiAlH 4 ,然后加水 4,NaHSO 3 5, NaHSO 3然后加NaCNCH 3CH 2CH 2OHOHCH 3CH 23NaCH 3CH 2CHCNOH6,稀碱 7,稀碱,然后加热 8,催化加氢 9,乙二醇,酸OHCH 3CH 2CHCHCHOCH 3CH 3CH 2CH=CCHOCH 3CH 3CH 2CH 2OH CH 3CH 2O O CH2CH 210,溴在乙酸中 11,硝酸银氨溶液 12,NH 2OH 13,苯肼Br CH 3CH 3CH 2COONH 4CH 3CH 2CH=NOH CH 3CH 2CH=NNH五、对甲基苯甲醛在下列反应中得到什么产物? 1.(P287)六、苯乙酮在下列反应中得到什么产物?1.COCOCOCOCH3CH3CH3CH3+HNO3H2SO4COCONO2CH3O-+HCCl3+NaBH4CHCH3OH+MgBrCOMgBrCH3C6H5CH3CC6H5OHH O+2.3.4.七、下列化合物中那些能发生碘仿反应?那些能和饱和亚硫酸氢钠水溶液加成?写出反应式。
第13章 羧酸及其衍生物

HOCH2CH2CH2CH2COOH
d
-羟基戊酸
CH3CH2C CHCOOH CH3
-甲基--戊烯酸
1.用系统命名法命名下列化合物:
1. CH 3(CH 2)4COOH .
1
CH3(CH 2)4COOH
2.CH 3CH(CH 3)C(CH 3)2COOH
2.CH 3CH(CH 3)C(CH 3)2COOH
CH3 (CH3)2CHCH2 CHCOOH
COOH OCCH3 O
阿司匹林(解热镇痛药)
布洛芬(抗炎镇痛药)
生命活动与之息息相关
― 生物体内大多数代谢反应都发生在羧基等官能Байду номын сангаас或强烈的受其影响的 邻位上
第十三章
羧酸及其衍生物
(一)羧酸
13.1 羧酸的结构、分类和命名 13.1.1 羧酸的结构
O
分子中含有
丁酸
丁酸 丁酸
5 23 1 2 1 4 5 34 3 5 4 2 1 C H3 CC H CCH CCHCOOHC3,OH 3,,4-二甲基戊酸 H H CH CH O4- 二甲基戊酸 C H3 C H H2 CH22COOH 34- 二甲基戊酸 3 - 二甲基戊酸 -二甲基戊酸 - 二甲基戊酸 CH3 CCH C H H3 C H CH33 3 3
C3H7CHO C3H7CH CN 醛出发制备带有其他官能团的羧酸:
HCN C3H7CHO OH C3H7CH CN H2O, HCl
HCN
OH H2O, HCl
OH C3H7CH
OH C3H7CH COOH
COOH
C3H7CHO
HCN (NH4)2CO3
有机化学课件(徐寿昌全)1-2024鲜版

状态
常温下,低级卤代烃多为气体或液体,高级卤代烃多为固体。
溶解性
低级卤代烃易溶于有机溶剂,部分可溶于水。随着碳链增长,溶解 度逐渐降低。
密度
卤代烃的密度一般比水大。
31
卤代烃的化学性质
01
亲核取代反应
卤代烃中的卤素原子可被亲核试剂取代,生成相应的醇、醚、胺等化合
物。例如,卤代烃与氢氧化钠水溶液反应,可生成相应的醇和卤化钠。
2024/3/28
27
芳香烃的来源和制备
2024/3/28
来源
芳香烃广泛存在于石油、煤焦油等天然资源中,也可通过化 学合成方法制备。
制备
工业上主要通过石油裂解、煤焦油分馏等方法获得芳香烃原 料,再经过精制、分离等步骤得到不同种类的芳香烃产品。 实验室中可通过有机合成方法制备特定的芳香烃化合物。
28
医疗卫生
环境保护
有机化学在医疗卫生领域也发挥着重要作 用,如合成药物、生物医用材料等都需要 有机化学的支持。
随着环境保护意识的提高,有机化学也致力 于开发环保型化学品和材料,减少对环境的 污染和破坏。
2024/3/28
6
02
烷烃
2024/3/28
7
烷烃的结构和命名
结构特点
碳原子间以单键相连,其 余价键被氢原子饱和。
20世纪中叶至今,随着现代化学 理论和实验技术的发展,有机化 学的研究领域不断拓宽和深化, 与其他学科交叉融合,形成了许
多新的分支领域。
2024/3/28
5
有机化学与生产生活的关系
农业生产
工业生产
有机化学为农业生产提供了大量的农药、 化肥等化学品,提高了农作物的产量和品 质。
有机化学在工业领域有着广泛的应用,如 合成纤维、塑料、橡胶、涂料等材料的生 产都离不开有机化学。
有机化学徐寿昌版PPT课件

(3) 乙炔的键
• C : 2s22p2 2s12px12py12pz1 • 乙炔的每个碳原子还各有两个相互
垂直的未参加杂化的p轨道, 不同碳 原子的p轨道又是相互平行的. • 一个碳原子的两个p轨道和另一个碳原子对应的两 个p轨道,在侧面交盖形成两个碳碳键.
(4) 乙炔分子的圆筒形 电子云 • 杂化轨道理论:两个成键轨道(1, 2),两个反键轨道
为反式加成.
例2:
HCCH + HCl
Cu2Cl2 或HgSO4
H2C=CH-Cl 氯乙烯
•亚铜盐或高汞盐作催化剂,可加速反应的进行.
例题
H C C H +HBr H 2 CC HB r+HBr H3C CHB 2 r
Cl
H3CC CHH HC g2lCH3lC C
HCl
CH2 HgCl2
H3C
C
4.2 炔烃的结构 (1) 乙炔的结构 •乙炔分子是一个线形分子,四个原子都排布在同一 条直线上. •乙炔的两个碳原子共用了三对电子.
•烷烃碳: sp3杂化 •烯烃碳: sp2杂化 •炔烃碳: sp杂化
(2) 乙炔分子中的 键
•由炔烃叁键一个碳原子上的两个sp杂化轨道所组成 的键则是在同一直线上方向相反的两个键. •在乙炔中,每个碳原子各形成了两个具有圆柱形轴 对称的 键.它们是Csp-Csp和Csp-Hs.
OO
CH3(CH2)7CC(CH2)7COOH
KMnO4 H2O
CH3(CH2)7-C-C-(CH2)7COOH
pH=7.5
92%~96%
•利用炔烃的氧化反应,检验叁键的存在及位置
•这些反应产率较低,不宜制备羧酸或二酮.
4.4.4 聚合反应 •只生成几个分子的聚合物
2024年徐寿昌有机化学课件-(版)

徐寿昌有机化学课件-(附件版)徐寿昌有机化学课件是一份全面、系统的有机化学教学资料,由我国著名有机化学家徐寿昌教授编写。
本课件涵盖了有机化学的基本理论、基本知识和基本技能,旨在帮助学习者系统地掌握有机化学的基本原理和实验技能,为进一步深入研究有机化学领域奠定坚实的基础。
一、课件特点1.系统性:本课件按照有机化学的知识体系进行编排,从有机化合物的结构、性质、反应机理到有机合成等方面进行了全面、系统的阐述,使学习者能够建立起完整的有机化学知识框架。
2.科学性:课件内容严格遵循有机化学的基本原理,注重理论与实践相结合,使学习者能够深入理解有机化学的基本概念和基本理论。
3.实用性:本课件紧密结合有机化学实验,注重培养学习者的实验技能和实际操作能力,使学习者能够熟练掌握有机化学实验的基本方法和技巧。
4.启发性:课件中穿插了大量典型实例和问题,引导学习者积极思考、自主学习,培养学习者的创新能力和解决问题的能力。
二、课件内容1.有机化学基本概念:介绍有机化学的定义、研究对象、特点等基本概念,使学习者对有机化学有一个初步的认识。
2.有机化合物的结构:阐述有机化合物的键合特征、分子结构、同分异构现象等,使学习者掌握有机化合物的基本结构特点。
3.有机化合物的性质:分析有机化合物的物理性质、化学性质,以及官能团对化合物性质的影响,使学习者了解有机化合物的性质规律。
4.有机化学反应:介绍有机化学反应的类型、机理、影响因素等,使学习者掌握有机化学反应的基本原理。
5.有机合成:阐述有机合成的基本原理、策略和典型反应,使学习者了解有机合成的基本方法。
6.有机化学实验:详细介绍有机化学实验的基本操作、实验技术和方法,以及实验安全知识,培养学习者的实验技能。
7.有机化学与生活:分析有机化学在生物、医药、食品、能源等领域的应用,使学习者认识到有机化学与日常生活的密切关系。
三、课件使用建议1.学习者应按照课件的结构顺序进行学习,逐步掌握有机化学的基本原理和实验技能。
有机化学徐寿昌优质公开课获奖课件

途。
03
五元杂环化合物的合成方法
包括Diels-Alder反应、环化反应等多种合成方法。
六元杂环化合物
吡啶、嘧啶和吡嗪的结构 与性质
六元杂环化合物中,吡啶、嘧啶和吡嗪是常见 的类型,它们具有不同的电子云密度和反应活 性。
吡啶类化合物的合成方法
包括吡啶环的构建、官能团的引入等合成策略。
六元杂环化合物的应用
重氮和偶氮化合物
1 重氮和偶氮化合物的结构和命名
阐述重氮和偶氮化合物的结构特点、分类以及命名规则。
2 重氮和偶氮化合物的物理性质
介绍重氮和偶氮化合物的物理性质,如颜色、溶解性等。
3 重氮和偶氮化合物的化学性质
详细讲解重氮和偶氮化合物的化学性质,包括放出氮气反 应、偶联反应、还原反应等。
4 重氮和偶氮化合物的合成方法
炔烃的结构和性质
包括炔烃的异构现象、稳 定性、加成反应等,以及 与烯烃的性质比较。
芳香烃及其衍生物
芳香烃的结构和性质
01
包括苯及其同系物的结构特点,以及它们的物理和化学性质,
如取代反应、氧化反应等。
芳香烃衍生物的合成和性质
02
包括硝化反应、磺化反应、卤化反应等合成方法,以及衍生物
的物理和化学性质。
详细讲解芳香族硝基和亚硝基化合物的化学性质,包括还原反应、亲 核取代反应等。
芳香族硝基和亚硝基化合物的合成方法
介绍芳香族硝基和亚硝基化合物的合成方法,如硝化反应、还原反应 等。
06
杂环化合物和生物碱
杂环化合物概述
杂环化合物的定义和分类
含有一个或多个杂原子的环状有机化合物,根据杂原子种类和数 量可分为不同类型。
有机化学徐寿昌优质公开课 获奖课件
徐寿昌主编《有机化学》-课后1-13章习题答案

第一章有机化合物的结构和性质无课后习题第二章烷烃1. 用系统命名法命名下列化合物:2,3,3,4-四甲基戊烷 3 -甲基-4-异丙基庚烷3 ,3-二甲基戊烷 2 ,6-二甲基-3,6-二乙基辛烷2,5-二甲基庚烷22 ,4,4-三甲基戊烷2 2. 写出下列各化合物的结构式:1.2,2,3,3-四甲基戊烷23、 2 ,2,4-三甲基戊烷45、2 -甲基-3-乙基己烷7、甲基乙基异丙基甲烷8-甲基-3-乙基己烷-甲基-3-乙基庚烷,2,3-二甲基庚烷、2,4-二甲基-4-乙基庚烷 6 、三乙基甲烷、乙基异丁基叔丁基甲烷3. 用不同符号表示下列化合物中伯、仲、叔、季碳原子4. 下列各化合物的命名对吗?如有错误的话,指出错在那里?试正确命名之2—乙基丁烷正确:3—甲基戊烷2, 4—2甲基己烷正确:2, 4—「甲基己烷3—甲基十二烷正确:3—甲基^一烷4- 丙基庚烷正确:4—异丙基辛烷4—二甲基辛烷正确:4, 4—二甲基辛烷1,1 , 1—三甲基一3—甲基戊烷正确:2, 2, 4—三甲基己烷5. 不要查表试将下列烃类化合物按沸点降低的次序排列:⑴2 , 3—二甲基戊烷(2)正庚烷(3) 2 —甲基庚烷⑷正戊烷(5) 2 —甲基己烷解:2—甲基庚烷〉正庚烷> 2 —甲基己烷>2, 3—二甲基戊烷>正戊烷(注:随着烷烃相对分子量的增加,分子间的作用力亦增加,其沸点也相应增加;同数碳原子的构造异构体中,分子的支链愈多,则沸点愈低。
)6•作出下列各化合物位能对旋转角度的曲线,只考虑所列出的键的旋转,并且用纽曼投影式表示能峰、能谷的构象。
(1)CH3-CI4旋转角度:00 600 1 200能(2) (CH3)3C-C(CH)3(3) CHCH -CH能峰能谷能7. 用Newman投影式写出1, 2—二溴乙烷最稳定及最不稳定的构象,并写出该构象的名称解:对位交叉式构象全重叠式构象最稳定最不稳定8. 下面各对化合物那一对是等同的?不等同的异构体属于何种异构?旋转角度:0 0600 1200得四种一氯化产物,(4)只得两种二氯衍生物,分别这些烷烃的构造式。
有机化学课件徐寿昌
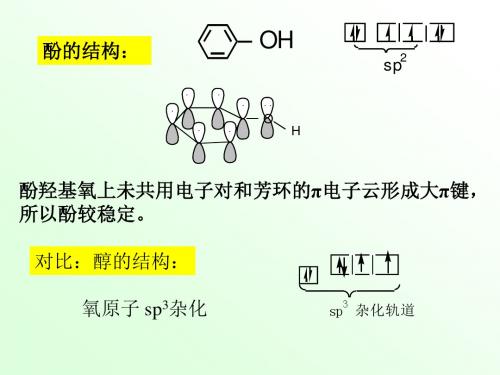
(二) 芳环上的亲电取代反应 • 羟基是强的邻对位定位基,使苯环活化。 1、卤化反应—酚很容易发生卤化。
•苯酚与溴水作 用,生成 2,4,6三溴苯酚白色 沉淀
白色沉淀 (~100%)
•溴水过量,生成黄色 的四溴苯酚析出
黄色沉淀
•邻、对位上有磺酸基 团时,可同时被取代
• 一元取代物对
溴苯酚的生成
(低温,非极性溶剂)
• 酚具有酸性的原因——氧原子以SP2(与醇醚不同)杂化轨道 参与成键,它的一对未共用电子的 P轨道与苯环的 6个 P轨道平行, 并且共轭,氧原子的负电荷分散到整个公轭体系中,氧的电子云 密度降低,减弱了O-H键,氢原子容易离解成为质子。
• 酚具有极高的亲电反应活性的原因 ——氧原子的P电子分
散到苯环上,增加了苯环的电子云密度,加强了亲电反应活性。
•对氯苯酚、邻氯 苯 酚 和 2,4- 二 氯 苯酚的生成
2,4-二氯苯酚
(注意:温度和氯用量,不用溶剂)
•2,4,6 -三氯苯酚的 生成
(水溶液)
2、硝化反应——酚很容易硝化 • 稀硝酸,室温
•浓硝酸,室温
•邻硝基苯酚和对硝基苯酚可 用水蒸气蒸馏 方法分开
注意这 种结构
•邻 硝 基 苯 酚 分 子 形成分子内六元环 的螯和物,对硝基 苯酚只能通过分子 间的氢键缔和。
中含有
答: ( 1 )加入与 FeCl3 ,显色(蓝色),表明有酚羟
基存在; (2)将邻羟基苯甲醇分别与NaHCO3和NaOH作用,该 物质不溶于 NaHCO3 而溶于 NaOH ,酸化后又能析出, 表明该物质显弱酸性(进一步证明有酚羟基)。 (3)与卢卡斯试剂反应生成混浊(证明有醇羟基,酚微 溶于水)
pKa
吸电子基团的硝基愈 多,酸性愈强。
徐寿昌主编《有机化学》(第二版)-课后1-13章习题答案
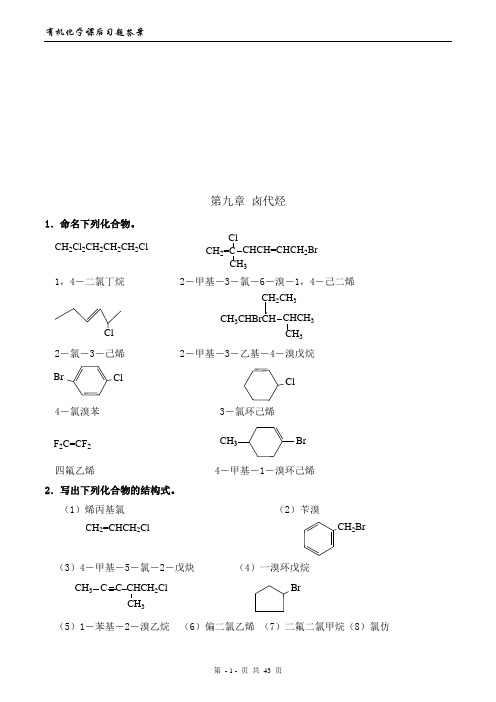
第九章 卤代烃1.命名下列化合物。
CH 2Cl 2CH 2CH 2CH 2ClCH 2=C CHCH=CHCH 2BrCH 3Cl1,4-二氯丁烷 2-甲基-3-氯-6-溴-1,4-己二烯CH 3CH 2CH 3CHCH 3CH 32-氯-3-己烯 2-甲基-3-乙基-4-溴戊烷ClBrCl4-氯溴苯 3-氯环己烯F 2C=CF 2CH 3Br四氟乙烯 4-甲基-1-溴环己烯 2.写出下列化合物的结构式。
(1)烯丙基氯 (2)苄溴CH 2=CHCH 2ClCH 2Br(3)4-甲基-5-氯-2-戊炔 (4)一溴环戊烷CH 3C C CHCH2ClCH 3Br(5)1-苯基-2-溴乙烷 (6)偏二氯乙烯 (7)二氟二氯甲烷(8)氯仿CH 2CH 2BrCL 2C=CH 2CCl 2F 2HCCl 33.完成下列反应式:CH 3CH=CH 2+HBrCH 3CHCH 3Br CH 3CHCH 3CN (1)CH 3CH=CH 2+HBr ROORCH 3CH 2CH 2Br H 2O(KOH)CH 3CH 2CH 2OH (2)CH 3CH=CH 2+Cl 25000CClCH 2CH=CH 2Cl +H O ClCH2CHCH 2ClOH (3)+Cl 2ClCl2KOH(4)KICH 3COCH 3I(5)CH 3CH CHCH CH 3OHPCl 5CH 3CH CHCH 3CH 3ClNH 3CH 3CHCH 3NH 2CH 3(6)(CH 3)3CBr +KCN25CH 2=C(CH 3)2(7)CH 3CHCH 3OHPBr CH 3CHCH 3AgNO 3/C 2H 5OHCH 3CHCH 3ONO 2(8)C 2H 5MgBr +CH 3CH 2CH 2CH 2C CHCH 3CH 3+CH 3CH 2CH 2CH 2C CMgBr(9)ClCH=CHCH 2Cl +CH 3COONa 3ClCH=CHCH 2OOCCH 3+NaCl (10)CHCH+25ClC=C ClH Cl Cl 2CHCHCl 22Cl (11)CH2Cl+3CH2CH2CH2CH2CH2OC2H5CNNH2IOH(12)4.用方程式表示CH3CH2CH2CH2Br与下列化合物反应的主要产物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
12.2.5 芳烃侧链的氧化
芳烃侧链上的-活泼易被氧化.
控制条件可生成相应的芳醛和芳酮(注意选择适当
的催化剂)。
12.2.6 羰基合成
烯烃与CO和H2在某些金属的羰基化合物催化下,与
110~200℃、10~20 MPa下,发生反应,生成多一个 碳原子的醛。
(主要)
• 羰基合成的原料多采用双键在链端的 -烯烃,其产 物以直链醛为主(直:支 = 4:1)。
例 1:
例 2:
12.2.3 同碳二卤化物水解 生成相应的羰基化合物,该法主要制备芳香族醛酮 (因为芳环侧链上-容易被卤化。) 例 1:
例 2:
补充: •用甲苯及其他必要的有机、无机试剂合成:
注意
12.2.4 傅-克酰基化反应
芳烃在无水三氯化铝催化下,与酰卤或酸酐作用,
生成芳酮:
苯甲酰氯
第十二章 醛和酮
醛和酮均含有羰基官能团:
羰基碳原子上至少连有一个氢原子的叫醛: 叫醛基。
—CHO 或
• 羰基碳原子上同时连有两个烃基的叫酮。
O R H an aldehyde
O R R an ketone
12.1 醛、酮的结构和命名 (1)醛酮的结构
易受亲核试剂进攻, 发生亲核加成
sp2
羰基π电子云示意图 甲醛的结构
• 低级醛酮易溶于水。丙酮能溶解很多有机化合物, 是很好的有机溶剂。
12.4 醛酮的化学性质 12.4.1 加成反应 烯烃的加成一般为亲电加成; 醛 酮 的 加 成 为 亲 核 加 成 , 易 于 HCN 、 NaHSO3 、 ROH、RMgX等发生亲核加成反应。
(1)与氰化氢加成
(氰醇)
羰基与羟基互换
例 5 :醇在适当的催化剂条件下脱去一分子氢,生成 醛酮。
• 该反应得到的产品纯度高,但为一吸热反应,工业上常 在脱氢的同时,通入一定量的空气,使生成的氢与氧结 合放出的热量供脱氢反应。这种方法叫氧化脱氢法。
12.2.2 炔烃水合
在汞盐催化下,生成羰基化合物,除乙炔外,其他
炔烃水合均生成酮:
偶极矩 2.27D
偶极矩 2.85D
(2)醛酮的命名
(1)
脂肪族醛酮命名 : 以含有羰基的最长碳链为主链 , 支链作为取代基,主链中碳原子的编号从靠近羰基 的一端开始(酮需要标明位次):
• 也可用希腊字母表示靠近羰基的碳原子,其次为、 、…...
例如:
(2)芳香醛、酮的命名,常将脂链作为主链,芳环为取 代基:
OH C H3C H2C HC H 3 OH O C H3C H2C C H 3 O
例 2:
C rO3 H2S O4 Na2C r2O7 H2S O4
OH CHCH2CH3
H2C rO4
O CCH2CH3
例3:以三氧化铬和吡啶的络合物为催化剂制醛产率高:
例4:欧芬脑尔氧化法 (主要制酮):含有不饱和C=C 双键的醛氧化,需采取特殊催化剂,如:丙酮-异丙醇 铝(或叔丁醇铝)或三氧化铬-吡啶络合物作氧化剂达 到此目的。
则在酸的催化下,醛能与一分子醇加成,生成半缩醛。 半缩醛不稳定,可以和另一分子醇进一步缩合,生成 缩醛:
半缩醛反应历程:
质子化
• 半缩醛在酸催化下,可以失去一分子水,形成一个 碳正离子,然后再与另一个醇作用,最后生成稳定的 缩醛:
缩醛的反应历程:
缩醛对碱和氧化剂都相当稳定。由于在酸催化下生 成缩醛的反应是可逆反应,故缩醛可以水解成原来的 醛和醇:
(注意:苯甲醛可以,但苯乙酮不与之反应)
反应历程(亚硫酸氢根离子为亲核试剂):
• 该反应是个可逆反应,常被用来分离和提纯某些羰 基化合物:
• -羟基磺酸钠与等摩尔的NaCN作用,则磺酸基可被氰 基取代,生成 -羟基腈,避免使用有毒的氰化氢,产率 也比较高。
( 3)与醇加成
将醛溶液在无水醇中通入 HCl 气体或其他无水强酸,
二苯甲酮
• 该反应也是一个芳环上的亲电取代反应:
傅-克酰基化反应历程:
加酸处理得酮
芳烃与直链卤烷发生烷基化反应,往往得到重排产 物,但酰基化反应没有重排现象:
在AlCl3-Cu2Cl2催化剂下,芳烃与CO、HCl作用可在环 上引入一个甲酰基的产物,叫 伽特曼-科赫反应 。
补充:完成下列转换
伽特曼-科赫反应
(3) 比较简单的酮还常用羰基两边烃基的名称来命名:
(4) 二元酮命名时 ,两个羰基的位置除可用数字标明外 , 也可用、、…表示它们的相对位置, 表示两个羰 基相邻, 表示两个羰基相隔一个碳原子:
12.2 醛酮的制法 12.2.1 醇的氧化和脱氢
伯醇和仲醇氧化或脱氢反应,可分别生成醛、酮。 例 1:
12.3 醛酮的物理性质 室温下,甲醛为气体, 12 个碳原子以下的醛酮 为液体,高级醛酮为固 体。 低级醛有刺鼻的气味, 中 级 醛 ( C8~C13 ) 则 有 果香。 低级醛酮的沸点比相对 分子量相近的醇低。 (分子间无氢键)。
醛酮沸点与烷烃沸点的比较
由于羰基是个极性基团,分子间偶极的静电引力比 较大,所以醛酮的沸点一般比相对分子量的非极性化 合物(如烃类)高。
• 在有机合成中常利用缩醛的生成ቤተ መጻሕፍቲ ባይዱ水解来保护醛基。
醛与二元醇反应生成环状缩醛:
例如: 制造合成纤维“维尼纶”:
聚乙烯醇
甲醛
聚乙烯醇缩甲醛 纤维(维尼纶)
酮也能与醇生成半缩酮或缩酮,但反应较为困难。 而酮和1,2-或1,3-二元醇比较容易生成环状缩酮:
丙酮氰醇 (78%)
-甲基丙烯酸甲酯(90%)
• 第二步包含:水解、酯化和脱水等反应。
伽特曼-科赫反应
氯甲基化反应
(2)与亚硫酸氢钠加成 醛和脂肪族甲基酮(或七元环以下的环酮)与之 反应,生成 -羟基磺酸钠:
• -羟基磺酸钠易溶于水,不溶于饱和亚硫酸氢钠。将 醛酮与过量的饱和亚硫酸氢钠水溶液混合在一起,醛和 甲基酮很快会有结晶析出。可以此来鉴别醛酮。
• 在碱性溶液中反应加 速,在酸性溶液中反 应变慢:
-
CN- 离子为强的亲核试剂,它与羰基的加成反应历程:
注意:由于氰化氢剧毒,易挥发。通常由氰化钠和无 机酸与醛(酮)溶液反应。pH值约为8有利于反应。
羟基腈是一类很有用的有机合成中间体。氰基 -CN 能水解成羧基,能还原成氨基。 例如: 有机玻璃 —聚-甲基丙烯酸甲酯的单体的合成:
