无机材料科学基础 24常见硅酸盐的晶体结构【精选】
硅酸盐晶体结构(无机材料科学)

一、岛状结构 镁橄榄石( Mg2[SiO4]或 2MgO· 2) SiO 二、组群状结构 绿宝石(Be3Al2[Si6O18] 或 3BeO· 2O3 · Al 6SiO2) 三、连状结构 透辉石CaMg [Si2O6] 的结构(CaO· MgO· 2SiO2 ) 四、层状结构(层状结构矿物的特点) 1、高岭石结构( Al2O3•2SiO2 •2H2O 或Al4[Si4O10](OH)8) 2、 蒙脱石(微晶高龄石)的结构(Al2[Si4O10](OH)8•nH2O理论式)
双四面体
三元环
四元环
六元环
5
(3) 链状 单链 :[SiO4]彼此共用两个顶点, 在一维方向上连结成无限的长链, 每一四面体仍有2个活性氧,借 此与存在于链间的金属离子相连, Si/O=1:3; 双链 :双链是由两个单链通过共 用氧平行连接而成,或者看成是 单链通过一个镜面反映而得。 Si/O=4:11
21
辉石类硅酸盐(如透辉石,玩火辉石)含有[Si2O6]n4n单链,链与链之间通过金属正离子相连接,最常见的为 Mg2+和Ca2+ ,也有被其他正离子取代的情况,Mg2+可被 Fe2+代替,(Mg2++Ca2+)可被(Na++Al3+), (Na++Fe3+), (Li++Al3+)等离子对所取代。 角闪石类硅酸盐含有[Si4O11]n6n-双链,如斜方角闪石 (Mg,Fe)7 [Si4O11]2(OH)2,透闪石 Ca2Mg5[Si4O11]2(OH)2, 具有硅氧链的硅酸盐矿物,因链内Si-O键要比链之间 的M-O键强得多,所以这类矿物易沿链(或带)方向 劈裂为柱状或纤维状。 以透辉石为例说明该类矿物的结构。
硅酸盐晶体结构

五、层状结构
单网层相当于一个硅氧层加上一个水铝石或水 镁石层,称为1:1层。复网层相当于两个硅氧 层中间加上一个水铝石或水镁石层,称为2:1 层,见图。
根据水铝石或水镁石层中八面体空隙的填充情 况,结构又分为三八面体型和二八面体型。前 者八面体空隙全部被金属离子所占据,后者只 有2/3的八面体空隙全部被金属离子所填充。
四、链状结构
1、链的类型、重复单元与化学式 硅氧四面体通过共用氧离子相连,在
一维方向延伸成链状,依照硅氧四面体共 用氧离子数目的不同,这种链又可以分为 单链和双链。
链于链之间是通过其它阳离子按一定 的配位关系连结起来。
四、链状结构
单链:如果两个硅氧四面体通过共用两个顶
点向一维方向无限延伸,则形成单链状。单 链结构以[Si2O6]4-为结构单元不断重复,结构 单元的化学式为[Si2O6]。
2)岛状结构晶体:
岛状结构的硅酸盐晶体有锆石英 Zr[SiO4]、镁橄榄石Mg2[SiO4]、蓝晶石 Al2O3•SiO2、莫来石3Al2O3•2SiO2以及水 泥熟料中的γ-C2S、β-C2S和C3S等
3)举例:镁橄榄石Mg2[SiO4] 结构说明:正交晶系Pbmm空间群;晶格常 数,a0=0.476nm,b0=1.021nm, c0=0.598nm, 晶胞分子数Z=4;镁橄榄石结构中,O2-离子 近似六方最紧密堆积排列, Si4+离子填于四面 体空隙的1/8,Mg2+离子填于八面体空隙的1/2。 孤立的[SiO4]四面体之间通过镁氧八面体相连; 每个O2-连接一个Si4+和三个Mg2+,电价平衡。
架状
4
骨架
[SiO2]
1:2
石英SiO2
[(AlxSi1-x)O8] x
硅酸盐晶体结构

ڻ以SiO2为例讨论,SiO2分
为三类晶型(石英、鳞石 英、方石英)七种变体。
目录
上页
下页
退出
(1)α-方石英结构
立方晶系,Fd3m 空间群, a=0.705nm,Si4+在立方 晶胞中的配置与金刚石 构造中的相同,而 O2-位于每两个 Si4+之间, Si4+、O2-均作面心立方排 列。
结构式Mg6[Si4O10](OH)
8
结构组成:相当于在高 岭石结构中,用Mg2+取 代Al3+,为保持电价平
衡,需用3个Mg2+取代2
个Al3+
目录
上页
下页
退出
4、叶腊石类 (属三层结构) 主要有叶腊石、蒙脱石、 滑石。
叶腊石
构成:将高岭石的双层结
构再加上一层[SiO4]四面
体层。
成分:Al2O3· 4SiO2· 2O H
目录 上页 下页 退出
3)四面体不相连,八面体共棱相连。
4)Si-O形成[SiO4]四面体,弧立存在,由
[MgO6]连接起来。 5)Si-O→[SiO4],Mg-O→[MgO6]
目录
上页
下页
退出
(2)
结构特点
1)各[SiO4]4- 是单独存在的,其顶角相互地朝上朝下。 2)各[SiO4]4-四面体只通过O-Mg-O键连接一起。
目录
上页
下页
退出
(2)叶蛇纹石 又称岫玉, 形成于镁质碳酸岩的变质大 理石中,全国最大的蛇纹石 玉矿在辽宁省岫岩县哈达碑 镇瓦沟,岫岩玉以绿色为主, 还有红、黄、白、青、蓝、 紫色和墨绿、淡黄、乳白色。 可谓七彩斑斓,五光十色。 硬度一般介于3.5至5之间。
《硅酸盐晶体结构》PPT课件

镁橄榄石 Mg2[SiO4] 镁铝石榴石 Al2Mg3[SiO4]3 硅钙石 Ca3[Si2O7] 蓝锥矿 BaTi[Si3O9] 斧石
Ca2Al2(Fe,Mn)BO3[Si4O12](OH) 绿宝石 Be3Al2[Si6O18] 透辉石 CaMg[Si2O6] 透闪石 Ca2Mg5[Si4O11]2(OH)2 滑石 Mg3[Si4O10](OH)2 石英 SiO2 钾长石 K[AlSi3O8] 方钠石 Na[AlSiO4] 4/3H2O
三、组群状结构
2个、3个、4个或6个[SiO4] 通过共用氧相连接形成单独硅 氧络阴离子团(有限硅氧四面体群),它们之间再通过其它金 属离子连接。
(1)桥氧(或公共氧、非活性氧):有限四面体群中连 接两个Si4+的氧,其电价已饱和,一般不再与其它正离子配位
(2)非桥氧(或非公共氧、活性氧):只有一侧与Si4+
属斜方晶系,空间群Pbnm
晶胞参数 a=0.476nm,b=1.021nm,c=0.599nm
晶胞分子数 Z=4
O2-近似于六方最紧密堆积排列(即ABAB……层 序堆积),Si4+填充1/8四面体空隙;Mg2+填充1/2八面 体空隙
(a) (100)
面上的 投影图
(c) 立体 侧视图
(b)(001)面上的投影图
硅酸盐晶体结构特点:
• 基本结构单元:[SiO4]四面体。Si-O-Si键为夹角不 等折线,一般145o左右;
• [SiO4] 每个顶点,即O2-最多为两个[SiO4] 所共用; • 两相邻[SiO4] 之间只能共顶而不能共棱或共面连接; • [SiO4] 中心Si4+可部分被Al3+ 所取代。
硅酸盐晶体分类方法:
硅酸盐晶体结构

▲▲
如果八面体以共棱方式相连,但O2被3个正离子所共用,这种八面体称为三
八面体,即 全部八面体空隙都被正离
子填充,[MgO6] 就属此种情况。
材料科学基础
• 不管是二八面体还是三八面体,八面
体层网络中仍有一些O2-不能与Si4+配位 (活性氧),因而剩余电价就要由H+来 平衡,所以层状结构中都有OH-出现。
五、层状矿物
层状结构是[SiO4]之间通过三个桥氧相 连,在二维平面无限延伸构成的硅氧四面 体层。
结构基元:[Si4O10]4- 化学式:[Si4O10]n4n- Si/O: 4:10 共用O2-数: 3
(a)立体图
(b)投影图
层状结构硅氧四面体
层的类型:
按照硅氧层中活性氧的空间取向不同,硅氧
第二节 硅酸盐晶体结构
一、概述 1、硅酸盐晶体化学式的写法
氧化物法:将所用氧化物由低价到高价按比例写 出,(最后写H2O) 无机络盐法:低价离子→高价离子→氧→(OH)基
Mg2[SiO4]
2、硅酸盐晶体结构的特点
1)[SiO4]是硅酸盐晶体结构的基础;
2)硅酸盐结构中的Si4+之间不存在直接的键,
通过金属正离子连接,最常见的是Mg2+和Ca2。
角闪石类硅酸盐含有双链[Si4O11],如斜方角
闪石(Mg,Fe)7[Si4O11]2(OH)2和透闪石
Ca2Mg5[Si4O11]2(OH)2等。
例:透辉石, CaMg[Si2O6]
结构与性质的关系:
介电性 解理性Si-O键要比M-O键要强
石英 磷石英 方石英 熔体
870 C 1470 C 1723 C
硅酸盐晶体结构

长石族 结构特点:
长石的结构中的四个面体[TO4](T代表Si或Al)相互共顶,形成一个四联环。四联环与四联
环又相互共用角顶,连接成曲轴状的链,平行于a轴伸展,链与链之间,又以桥氧相接,形成 整个三维的骨架。
主要
种: K[AlSi3O8]
透长石 Sanidine 正长石 Orthoclase 微斜长石 Microcline 斜长石 (钠长石_奥长石_中长石_拉长石_培长石_钙长石)
PS:翡翠的A货、B货和C货的含意
层状结构硅酸盐
滑石
化学组成:
Talc Mg3[Si4O10](OH)2
晶体形态:偶见假六方或菱形的片状单晶体。
物理性质:无色透明或白色,硬度1,{001}解理完全,比重2.58~2.83, 能耐
火。
鉴定特征:低硬度,有滑感,较浅的颜色以及片状形态。
架状结构硅酸盐
层状结构硅酸盐
翡翠(jadeite), 也称翡翠玉、翠玉、缅甸玉,是 玉的一种。 翡翠的正确定义是以硬玉矿物为主的辉石类矿物组 成的纤维状集合体。但是翡翠并不等于硬玉。翡翠 是在地质作用下形成的达到玉级的石质多晶集合体, 主要由硬玉或硬玉及钠质(钠铬辉石)、钠钙质辉 石(绿辉石)组成,可含有角闪石、长石、铬铁矿、 褐铁矿等。
参考文献: 高等无机结构化学 麦松威,周公度,李伟基 北京大学出版社 第二版 化学中的多面体 周公度 北京大学出版社 结构和物性 周公度 高等教育出版社 第三版 维基百科
感谢聆听
3、链状硅氧骨干
硅氧四面体彼此之间共用两个角顶构成延伸 的单链[Si2O6]4硅氧四面体部分共用两个角顶,部分共用三 个角顶相互联接构成延伸的双链[Si4O11]6-
4、层状硅氧骨干
硅氧四面体共用三个角顶构成二向延展 的平面层状[Si4O10]4-
晶体结构硅酸盐晶体结构

晶体结构硅酸盐晶体结构晶体结构是指晶体中原子、离子或分子的排列方式。
硅酸盐晶体是指以硅酸根为基础的晶体,其中硅离子(SiO_4^4-)与其他阳离子形成网络结构。
硅酸盐晶体结构的研究对于了解晶体的物理性质以及在材料科学中的应用具有重要意义。
硅酸盐晶体结构可以分为四类:随机硅酸盐、连续硅酸盐、不连续硅酸盐、氟硅酸盐。
随机硅酸盐晶体结构是指硅酸盐中的硅酸根离子(SiO_4^4-)和其他离子随机排列的结构。
这类结构的特点是硅酸根离子之间没有明确的排列规律,并且硅酸根离子与其他离子之间的距离也比较随机。
随机硅酸盐晶体结构可以用来制备玻璃等非晶态材料。
连续硅酸盐晶体结构是指硅酸盐中的硅酸根离子(SiO_4^4-)按照一定的排列规律形成的结构。
这类结构的特点是硅酸根离子之间有明确的连接方式,形成一维、二维或三维的网络结构。
连续硅酸盐晶体结构具有较高的晶体度和结晶度,可以用来制备陶瓷等工程材料。
不连续硅酸盐晶体结构是指硅酸盐中的硅酸根离子(SiO_4^4-)与其他离子之间有插入不连续的阳离子,形成硅酸盐层状结构。
这类结构的特点是硅酸根离子之间有明确的排列规律,但是硅酸根离子与其他离子之间的距离不均匀。
不连续硅酸盐晶体结构可以用来制备硅酸钙等复合功能材料。
氟硅酸盐晶体结构是指硅酸盐中的硅酸根离子(SiO_4^4-)的一部分或全部被氟离子(F^-)取代的结构。
这类结构的特点是硅酸根离子与氟离子之间有明确的排列规律,并且形成独特的晶体结构。
氟硅酸盐晶体结构具有特殊的光学、电学和热学性质,可以用来制备光学器件、电子器件和热障涂层等材料。
总之,硅酸盐晶体结构的研究对于深入了解晶体的性质、设计新型材料以及开发新的应用具有重要意义。
随着材料科学的进步和技术的发展,我们对硅酸盐晶体结构的理解将进一步深化,为新材料的开发和应用提供更多的可能性。
硅酸盐晶体结构

(3) 层状硅酸盐 layered silicates
9
二、硅酸盐矿物的分类
2、根据Si-O四面体在空间的连接情况
(4) 架状硅酸盐 network silicates
10
三、硅酸盐的结构
1、岛状硅酸盐 Island silicates (limited Si-O group) (1) 单一硅氧团(孤立有限硅氧团)
举例:
• 能“爆米花”的矿物和岩石
• 能吸水膨胀的膨润土
20
4、骨架状硅酸盐 Network silicates
(1). 硅石 silica(石英) SiO2 硅氧四面体在空间组成的三维网 络状结构
方石英结构特征:
• FCC点阵,Si4+排成金刚石结构, O2-位于<111>方向上 的一对Si4+之间,形成桥氧; Si4+位于O2-的四面体间隙, O2-四面体在空间通过桥氧相连,形成三维网络结构 • 所有的氧均为桥氧
13
(2) 含成对的硅氧团
• = O/Si=3.5
• 硅钙石 Ca3(Si2O7),即3CaO· 2SiO2,正交晶系
14
(3) 含环状硅氧团
• 三节环:(Si3O9)6- • 四节环:(Si4O12)8-
• 六节环:(Si6O18)12-
= O/Si=3
代表性矿物:
绿柱石 Be3Al2[Si6O18] 堇青石 cordierite 2MgO· 2O3· 2Al 5SiO2
15
2、链状硅酸盐 Chained silicates
由大量的[SiO4]4-共顶连接而成的一维结构
(1) 单链:结构单元[SiO3]2-, = O/Si=3
无机材料科学基础-之-硅酸盐的晶体结构

C0 Si
Al(Mg) H2O
C0 Si
Al(Mg)
H2O
(A) (B)
39
(5)层状结构中, 如果在Si—O四面体 层中,部分Si4+离子 被A13+离子代替,或 Al—O八面体层中, 部分A13+离子被Mg2+ 或Fe2+离子代替时, 则结构单位中电荷就 不平衡,有多余的负 电荷出现。这时,可 以进入一些电价低而 离子半径大的水化阳 离子(如K+,Na+等) 来平衡多余的负电荷。
桥氧、非活性氧: 两之间个共[Si用O的4]四氧面离体子。
非桥氧、活性氧、 自由氧:只与一个 [SiO4]四面体中的 Si4+配位的氧。
非桥氧、活性 氧、自由氧
桥氧、非活 性氧
6
二、分类 硅酸盐晶体种类繁多,是构成地壳的主要矿
物,也是水泥、普通陶瓷、玻璃、耐火材料等传 统硅酸盐工业的主要原料。各种硅酸盐晶体结构 共同的特点是结构中都含有硅氧四面体[SiO4], 硅酸盐晶体结构就是以这些[SiO4]作为基本结构 单元,由它们相互连接构筑起来的,并且它们之 间的不同连接方式,就决定了硅酸盐晶体的结构 类型,分为:岛状、组群状、链状、层状和架状。 硅酸盐晶体种类归纳于下表。
C0 Si
Al(Mg) H2O
(A)
40
(6)如果结构中取 代主要发生在Al—O八 面体中,进入层间的 阳离子与层的结合并 不很牢固,在一定条 件下可以被其它阳离 子交换。可交换量的 大小即称为阳离子交 换容量。
如果取代发生在Si—O 四面体中,且量较多 时,进入层间的阳离 子与层之间有离子键 作用,则结合较牢固。
25 -9
52 59
75 9
关于硅酸盐晶体结构

硅酸盐晶体结构的共同特点:
(1)构成硅酸盐晶体的基本结构单元[SiO4]四面体。SiO-Si键是一条夹角不等的折线,一般在145o左右。
(2)[SiO4]四面体的每个顶点,即O2-离子最多只能为两 个[SiO4]四面体所共用。
(3)两个相邻的[SiO4]四面体之间只能共顶而不能共棱或 共面连接。
1、镁橄榄石Mg2[SiO4]结构
属斜方晶系,空间群Pbnm;晶胞参数a=0.476nm ,b=1.021nm,c=0.599nm;晶胞分子数Z=4。如图13-1、1-3-2、1-3-3所示。
镁橄榄石结构中,O2-离子近似于六方最紧密堆 积排列,Si4+离子填于四面体空隙的1/8;Mg2+离子填 于八面体空隙的1/2。
三、组群状结构
组群状结构是2个、3个、4个或6个[SiO4]四面体通 过共用氧相连接形成单独的硅氧络阴离子团,如图1-3-4 所示。硅氧络阴离子团之间再通过其它金属离子连接起 来,所以,组群状结构也称为孤立的有限硅氧四面体群 。
双四面体 [Si2O7]6-
三节环 [Si3O9]6-
四节环 [Si4O12]8-
结构与性质的关系:结构中每个O2-离子同时 和1个[SiO4]和3个[MgO6]相连接,因此,O2-的电价 是饱和的,晶体结构稳定。由于Mg-O键和Si-O键都 比较强,所以,镁橄榄石表现出较高的硬度,熔点 达到1890℃,是镁质耐火材料的主要矿物。同时, 由于结构中各个方向上键力分布比较均匀,所以, 橄榄石结构没有明显的解理,破碎后呈现粒状。
二、岛状结构
[SiO4]四面体以孤岛状存在,各顶点之间并不互相 连接,每个O2-一侧与1个Si4+连接,另一侧与其它金属 离子相配位使电价平衡。结构中Si/O比为1:4。
【精品】硅酸盐晶体结构

目的要求:1.了解固体中各类结合键的特性,明确键性与晶体结构的关系及其对固体性质的影响。
2.掌握最紧密堆积原理(等径球体)和两种堆积方式(六方、立方)及其晶胞特点。
3.掌握晶胞、离子半径、配位数、配位多面体、离子极化等概念。
4.能理解当正离子极化力不强,负离子的极化性不大时,负离子多面体的形状主要由正离子半径和负离子半径之比来决定。
5.能理解CsCl、NaCl、立方ZnS、CaF2、CaCO3的晶体结构。
6.理解鲍林规则的内容,并能分析不复杂的离子化合物晶体结构符合鲍林规则各条规则。
7.明确硅酸盐矿物的分类依据及各类结构(岛状、组群状、链状、层状、架状)的特征,清楚几种典型矿物(镁橄榄石、高岭石、蒙脱石、石英)结构特点及对性质的影响。
重点:最紧密堆积原理、晶胞、离子半径、配位数、配位多面体、离子极化、鲍林规则典型离子晶体、硅酸盐晶体的结构难点:典型离子晶体结构、硅酸盐晶体的结构的特点1.晶体:如立方体岩盐,菱面体天然菱镁矿(单晶:晶体慢慢冷却形成)非晶体:玻璃、松香、沥青等(无定形)(玻璃:SiO2原料熔化,急冷形成)有的物质如石英SiO2,可成为晶体亦可成为非晶体性质与结构紧密相关,如何区分晶体与非晶体?①各向异性晶体对光、电、磁、热以及抵抗机械和化学作用在各个方向上是不一样的。
晶体的各向异性是区别于物质其它状态最本质性质。
②固定熔点晶体在熔化时必须吸收一定的熔融热才能转变为液态(同样在凝固时放出同样大小的结晶热),随时间的延长,温度升高,当晶体开始熔解,温度停止上升,此时所加的热量,用于破坏晶体的格子构造,直到晶体完全熔解,温度才开始继续升高③稳定性晶体能长期保持其固有状态而不转变成其它状态。
这是晶体具有最低内能决定的,内能小,晶体内的质点规律排列,这是质点间的引力斥力达到平衡,结果内能最小,质点在平衡位置振动,没有外加能量,晶体格子构造不破坏,就不能自发转变为其它状态,处于最稳定状态,而非晶体就不稳定,如玻璃有自发析晶(失透)倾向。
2-2硅酸盐晶体结构
无机材料科学基础
一、硅酸盐晶体的一般特点及分类
硅酸盐结构的一般特点:
r (1)据鲍林第一规则,si /rO =0.041/0.140=0.293 ,Si4+的配位数为 4,形成[SiO 4]四面体。Si-O之间的平均距离为0.160nm, 此值小于硅氧离子半径之和0.181nm,说明硅氧键并非简单 的离子键,尚含有相当成分的共价键,一般认为,离子键和 共价键各占50%。Si4+之间不直接相连,而必须通过O2-相 连。
表 硅酸盐晶体结构分类
Si:O 公用氧 硅氧骨干 类型 例子
无机材料科学基础
1:4
0
[SiO4]4[Si2O7]6[Si3O9]6[Si4O12]8-
孤岛状
1:3.5 1
1:3 2 2
有 双四面体 限 硅 三元环 氧 四元环 基 团
镁橄榄石Mg2[SiO4] 硅钙石Ca3[Si2O7]
蓝锥矿BaTi[Si3O9] 斧石 Ca2Al2(Fe,Mn)BO3[Si4O12](OH) 绿宝石Be3Al2[Si6O18]
其它同类型晶体:蓝晶石Al2O3· 2、莫来石 SiO
3Al2O3· 2以及水泥熟料中的-C2S、-C2S和C3S等。 2SiO
无机材料科学基础
橄榄石
• 自然界中,橄榄石(Peridot或 Olivine)因具有橄榄绿色而得名, 以酷似祖母绿色者最佳,次为浓绿 色和黄绿色,为八月诞辰石,产于 河北,吉林。
Neo-: from Greek Means:island
无机材料科学基础
(1)镁橄榄石(Mg2SiO4)(Olivine)
• 基本特征:斜方晶系,Pbnm空间群。晶格常数 a=0.467nm,b=1.020nm,c=0.598nm,每个晶胞中有4 个“分子”,故可以写成Mg8Si4O16。 • 按鲍林第一规则: r /r =0.041/0.140=0.293 • 所以Si4+的配位数为4,形成[SiO4]四面 rMg 体; /rO =0.065/0.140=0.464 ,所以Mg2+的配位数为 6,形成[MgO6]八面体。 • 按鲍林第三规则,[SiO4]四面体应该孤立存在, 而[MgO6]八面体可以共棱。
硅酸盐晶体结构

结构稳定,熔点高达1800℃,是一类重要的耐火材料。 同时在各个方向上结合力分布差异不大,所以没有显 著的解理,常呈粒状。
示意图
无机材料科学基础
50
OH 0 100
OH 50
OH 0
50
13
50
50 75
50
镁橄榄石在(100)面投影
• 按鲍林第一规则: rsi4+ /rO2- =0.041/0.140=0.293 • 所以Si4+的配位数为4,形成[SiO4]四面
体;rMg2+ /rO2- =0.065/0.140=0.464 ,所以Mg2+的配位数为 6,形成[MgO6]八面体。 • 按鲍林第三规则,[SiO4]四面体应该孤立存在, 而[MgO6]八面体可以共棱。
75 Al 50
0 50 13
50
镁橄榄石结构中的同晶取代:
无机材料科学基础
➢ 镁橄榄石中的Mg2+可以被Fe2+以任意比例取代,形成铁 橄榄石(FexMg1-x)SiO4固溶体。
➢ 部分Mg2+被Ca2+取代,则形成钙橄榄石CaMgS水iO泥4。的主要 ➢ 如果Mg2+全部被Ca2+取代,则形成-Ca2SiO4组,成即矿-物C2S之,一
无机材料科学基础
一、硅酸盐晶体的一般特点及分类
硅酸盐结构的一般特点:
(1)据鲍林第一规则,r si
4+
/rO2-
=0.041/0.140=0.293,Si4+的配位数为
4,形成[SiO4]四面体。Si-O之间的平均距离为0.160nm,
此值小于硅氧离子半径之和0.181nm,说明硅氧键并非简单
晶体结构硅酸盐晶体结构

晶体结构硅酸盐晶体结构晶体结构是指晶体中原子、分子或离子的排列方式。
硅酸盐是指含有硅和氧的化合物,其中硅酸的结构单元是硅酸四面体SiO4硅酸盐晶体结构的研究对理解晶体性质和应用具有重要意义。
下面将以一些典型的硅酸盐晶体结构为例进行介绍。
1.石英晶体:石英是一种含有二氧化硅(SiO2)的典型硅酸盐晶体。
其晶体结构是由硅酸四面体和氧离子构成的三维结构。
硅酸四面体通过共用氧离子形成一个网络状结构。
当硅酸四面体都以角的方式连接在一起时,形成了石英的六方晶体结构。
2.长石晶体:长石是一种常见的硅酸盐矿物,由硅酸盐层状结构和钠、钾等阳离子构成。
其中,硅酸盐层状结构由硅酸四面体构成,每个硅酸四面体都与相邻的四个硅酸四面体共享角,形成了一层平面。
这些硅酸四面体层通过钠、钾等阳离子填充在它们之间,形成了长石的晶体结构。
3.方解石晶体:方解石是一种含有碳酸根离子(CO3)的硅酸盐晶体。
它由硅酸盐八面体和碳酸根离子构成。
硅酸盐八面体和碳酸根离子通过共用氧离子形成一个三维网状结构。
方解石的晶体结构中,硅酸盐八面体与碳酸根离子是按照一定比例交替排列的。
硅酸盐晶体结构研究的重要性在于它对晶体的物理和化学性质起着决定性的作用。
晶体中原子、分子或离子的排列方式决定了晶体的特定性质,如硬度、折射率、导电性等。
此外,晶体结构的研究还可以为合成新型功能材料提供参考,如电子器件、光学材料等。
在实际应用中,硅酸盐晶体结构的研究被广泛用于材料科学、地球科学和无机化学等领域。
例如,在材料科学中,通过改变硅酸盐晶体结构可以调控材料的性质,用于制备新型材料。
在地球科学中,硅酸盐晶体结构的研究可以帮助我们了解地壳中的硅酸盐矿物形成的过程。
此外,硅酸盐晶体结构的研究还对于监测和预测地震等地质灾害具有重要意义。
总之,硅酸盐晶体结构的研究对于理解晶体性质和应用有着重要的意义。
不同的硅酸盐晶体具有不同的结构,其特定的结构决定了晶体的特定性质。
通过研究硅酸盐晶体结构,可以为合成新型材料以及地球科学等领域提供重要的参考。
硅酸盐材料的晶体结构及性能研究

硅酸盐材料的晶体结构及性能研究一、引言硅酸盐材料是一类包括玻璃、陶瓷、水泥等广泛应用的无机非金属材料,在人类社会的发展中扮演着不可或缺的角色。
它们作为优秀的结构材料,除了具有高耐热、耐磨、抗腐蚀、电绝缘等特性外,还具有良好的机械性能、化学稳定性以及光学、磁学等特殊性质,因此受到了越来越多的关注。
二、硅酸盐材料的晶体结构1.硅酸盐晶体结构基础硅酸盐晶体结构是由硅酸盐骨架和充填物组成的,硅酸盐骨架由正四面体的二氧化硅离子和正六面体的金属氧离子组成,形成六面体和四面体交替排列的层状结构。
充填物是指填在硅酸盐骨架中的氧化物或其他物质,如钙、铝、钠、镁等离子。
硅酸盐材料的晶体结构与骨架中硅酸盐单元和充填物的类型、数量、配位等因素密切相关。
2.硅酸盐材料的结构类型目前已知的硅酸盐材料有上千种,其中最常见的结构类型包括四面体硅酸盐、正交硅酸盐、层状硅酸盐、环状硅酸盐、正八面体硅酸盐等。
四面体硅酸盐是最简单的硅酸盐结构,材料中的硅酸盐骨架仅包含硅氧四面体,没有充填物;正交硅酸盐中的硅酸盐骨架和充填物呈长方形和正方形排列,层状硅酸盐和环状硅酸盐则是表现出层状或球形的稳定晶体结构。
3.硅酸盐材料晶体结构变形硅酸盐材料的晶体结构往往在外界条件下发生变形,即晶体的过程中出现了晶格畸变。
晶格畸变包括晶格缺陷、错位、位错、拉伸、压缩等,可以影响硅酸盐材料的物理性能、结构稳定性以及反应性能。
三、硅酸盐材料的性能研究1.硅酸盐材料的物理性能硅酸盐材料的物理性能主要包括热膨胀系数、导热性、电性能、磁性能、光学和声学性能等。
其中最具代表性的是玻璃这一特殊物理性能。
玻璃由于不规则的结构和无序的排列,出现了随机散射、透明度、折射率等物理现象,充分发挥了玻璃的优越性能。
2.硅酸盐材料的化学性能硅酸盐材料的化学性能是指材料在化学反应中的化学活性能力。
它主要包括酸碱稳定性、氧化还原稳定性和水解稳定性等。
硅酸盐材料的化学性质决定了它在不同环境下的应用范围,具有极其广泛的应用价值。
简述硅酸盐晶体的基本结构特点

硅酸盐晶体是一类具有硅氧四面体结构基本单元的结晶物质,具有多种不同的结构特点。
以下是对硅酸盐晶体基本结构特点的简要描述:1. 硅氧四面体结构硅酸盐晶体的基本结构特点之一就是其由硅氧四面体构成的结构。
硅酸盐晶体的结构单位是由一个硅原子和四个氧原子构成的硅氧四面体。
在这种结构中,一个硅原子通过共价键连接着四个氧原子,形成了一个类似于四面体的结构。
这种硅氧四面体的结构单位是硅酸盐晶体结构的基础,它决定了硅酸盐晶体的物理化学性质和结构特征。
2. 多样的配位结构硅酸盐晶体的另一个结构特点是其具有多样的配位结构。
在硅氧四面体结构的基础上,硅酸盐晶体可以通过不同的配位方式形成多种不同的晶体结构。
硅酸盐晶体中的硅原子和氧原子可以通过共价键、离子键或氢键等不同的配位方式结合在一起,形成了不同的晶体结构。
这种多样的配位结构使得硅酸盐晶体拥有丰富多彩的物理化学性质,适应了不同的应用领域和需求。
3. 多种晶体形态硅酸盐晶体还具有多种不同的晶体形态。
基于硅酸盐晶体的结构特点和配位结构,硅酸盐晶体可以形成多种不同的晶体形态,包括直角棱柱形、六方柱形、正四面体形等。
这些不同的晶体形态反映了硅酸盐晶体内部结构的多样性和复杂性,也为其在不同领域的应用提供了丰富的选择。
4. 特殊的物理化学性质硅酸盐晶体的基本结构特点还表现在其特殊的物理化学性质上。
由于硅氧四面体结构的存在,硅酸盐晶体具有较高的热稳定性、化学稳定性和机械强度,这使得硅酸盐晶体在陶瓷、玻璃等领域有着广泛的应用。
不同的配位结构和晶体形态也赋予了硅酸盐晶体不同的光学、电学和磁学性质,为其在光学器件、电子器件等领域的应用提供了可能性。
硅酸盐晶体具有独特的硅氧四面体结构、多样的配位结构、多种不同的晶体形态以及特殊的物理化学性质。
这些结构特点赋予了硅酸盐晶体丰富的应用前景和发展空间,使其成为当代材料科学领域中备受关注和研究的重要材料之一。
5. 应用领域的多样性硅酸盐晶体在多个领域都有广泛的应用,其中最为显著的是在玻璃和陶瓷工业中。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
镁橄榄石 Mg2[SiO4] 镁铝石榴石 Al2Mg3[SiO4]3 硅钙石 Ca3[Si2O7] 蓝锥矿 BaTi[Si3O9] 斧石
Ca2Al2(Fe,Mn)BO3[Si4O12](OH) 绿宝石 Be3Al2[Si6O18] 透辉石 CaMg[Si2O6] 透闪石 Ca2Mg5[Si4O11]2(OH)2 滑石 Mg3[Si4O10](OH)2 石英 SiO2 钾长石 K[AlSi3O8] 方钠石 Na[AlSiO4] 4/3H2O
上一讲主要内容回顾
1 离子晶体的结构及其影响因素 2 鲍林规则 3 二元化合物的典型晶体结构
2.4 硅酸盐的晶体结构
一、硅酸盐晶体组成表征、结构特点及分类
二、岛状结构
三、组群状结构 四、链状结构 五、层状结构 六、架状结构
2.4 硅酸盐晶体结构
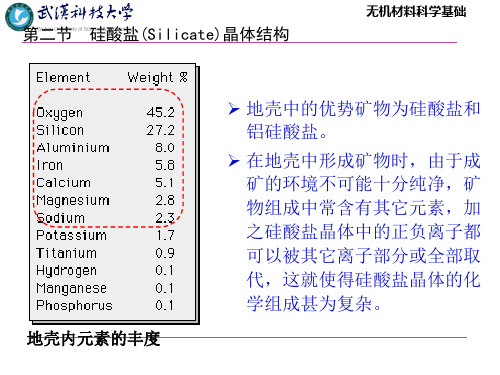
地壳中:铝 7.45 wt%
硅 26.0wt% 氧 49.130wt % 优势矿物:硅酸盐 铝硅酸盐 基本结构单元构造 基本结构单元之间连接 结构和性质上特征等
双四面体 [Si2O7]6-
三节环 [Si3O9]6-
四节环 [Si4O12]8-
六节环 [Si6O18]12-
孤立的有限硅氧四面体群
组群状结构中Si/O比:2:7或1:3 双四面体:硅钙石Ca3[Si2O7]
铝方柱石 Ca2Al[AlSiO7] 镁方柱石Ca2Mg[Si2O7] 三节环:蓝锥矿BaTi[Si3O9] 六节环:绿宝石Be3Al2[Si6O18]
镁橄榄石Mg2[SiO4]结构
属斜方晶系,空间群Pbnm 晶胞参数 a=0.476nm,b=1.021nm,c=0.599nm 晶胞分子数 Z=4 O2-近似于六方最紧密堆积排列(即ABAB……层 序堆积),Si4+填充1/8四面体空隙;Mg2+填充1/2八面 体空隙 每个[SiO4] 被[MgO6] 隔开,呈孤岛状分布
绿宝石Be3Al2[Si6O18]结构
六方晶系,空间群P6/mcc,
晶胞参数:a=0.921nm,c=0.917nm 晶胞分子数Z=2,如图1-34。
基本结构单元是由6个[SiO4] 组成六节环,其中1 个Si4+和2个O2-处在同一高度,环与环相叠。
镁橄榄石结构与性质的关系
(1)结构中每个O2-同时和1个[SiO4]和3个 [MgO6]相连接,其电价饱和,晶体结构稳定;
(2)Mg-O键和Si-O键均较强,则表现出较 高硬度,熔点达到1890℃,是镁质耐火材料的主要矿 物;
(3)结构中各个方向上键力分布较均匀,则无 明显解理,破碎后呈现粒状。
三、组群状结构
二、岛状结构
[SiO4] 以孤岛状存在,各顶点之间互不连接,每 个O2-一侧与1个Si4+连接,另一侧与其它金属离子相 配位使电价平衡。结构中Si/O比为1:4。
如:锆石英Zr[SiO4]、镁橄榄石Mg2[SiO4]、蓝 晶石Al2O3·SiO2、莫来石3Al2O3·2SiO2以及水泥熟料 中-C2S、-C2S(Ca2SiO4)和C3S(Ca3SiO5)等。
(2)若上图(b)中25、75的Mg2+被Ca2+取代,则形成钙 橄榄石CaMgSiO4;
(3)若Mg2+全部被Ca2+取代,则形成-Ca2SiO4(即-C2S ),其中Ca2+配位数为6。由于配位规则,在水中几乎为惰性
注意:另一种岛状结构的水泥熟料矿物-Ca2SiO4(即C2S)属单斜晶系,其中Ca2+有8和6两种配位。由于其配位不规 则,化学性质活泼,能与水发生水化反应。
一、硅酸盐晶体组成表征、结构特点及分类
硅酸盐晶体化学组成复杂,常采用两种方法表征: 氧化物表示法 无机络盐表示法(结构式)
氧化物表示法:按一定比例和顺序写出构成硅酸盐 晶体所有氧化物,先1价碱金属氧化物,其次2价、3价金 属氧化物,最后SiO2。
如,钾长石化学式: K2O·Al2O3·6SiO2; 无机络盐表示法:按一定比例和顺序全部写出构成 硅酸盐晶体所有离子,再用 [ ]将相关络阴离子括起,先 是1价、2价金属离子,其次Al3+和Si4+,最后O2-或OH-。 如,钾长石:K[AlSi3O8]。
六节环 单链 双链 平面层
骨架
络阴离子
[SiO4]4-
[Si2O7]6[Si3O9]6[Si4O12]8-
[Si6O18]12[Si2O6]4[Si4O11]6[Si4O10]4[SiO2]0 [AlSi3O8]1[AlSiOBiblioteka ]1-Si/O实例
1 :4
2 :7 1 :3 1 :3
1 :3 1 :3 4 :11 4 :10
以不同Si/O比对应基本结构单元[SiO4] 之间不 同结合方式,分为五种方式:
岛状 组群状 链状 层状 架状 对应Si/O由1/4→1/2,结构趋于复杂。
硅酸盐晶体结构类型与Si/O比的关系
结构 类型 岛状
[SiO4]4-共 用 O2-数
0
1
组群状
2
链状 层状 架状
2 2,3
3
4
形状
四面体
双四面体 三节环 四节环
2个、3个、4个或6个[SiO4] 通过共用氧相连接形成单独硅 氧络阴离子团(有限硅氧四面体群),它们之间再通过其它金 属离子连接。
(1)桥氧(或公共氧、非活性氧):有限四面体群中连 接两个Si4+的氧,其电价已饱和,一般不再与其它正离子配位
(2)非桥氧(或非公共氧、活性氧):只有一侧与Si4+ 相连接的氧
(a) (100) 面上的 投影图
(c) 立体 侧视图
(b)(001)面上的投影图
镁橄榄石晶体结构(1)
镁橄榄石晶体结构(2)
(a)(100)面上的投影图
镁橄榄石晶体结构(3)
(b)(001)面上的投影图
镁橄榄石晶体结构(4)
镁橄榄石结构中的同晶取代
(1)Mg2+被Fe2+以任意比例取代,则形成橄榄石( FexMg1-x)SiO4固溶体;
硅酸盐晶体结构特点:
基本结构单元:[SiO4]四面体。Si-O-Si键为夹角不 等折线,一般145o左右;
[SiO4] 每个顶点,即O2-最多为两个[SiO4] 所共用; 两相邻[SiO4] 之间只能共顶而不能共棱或共面连接; [SiO4] 中心Si4+可部分被Al3+ 所取代。
硅酸盐晶体分类方法:
