Ag在碱性介质中作氧还原催化剂综述
Ag在碱性介质中作氧还原催化剂综述

Ag在碱性介质中作氧复原催化剂综述本文较为全面地归纳了氧复原反响中使用的各种银基催化剂:纯银、碳载银、银合金、银-过渡金属氧化物。
论述了催化剂的机理、优缺点。
此外,简要阐述了银基催化剂的一些合成方法,并介绍了催化剂的形貌、PH值、成分对氧复原反响的影响,最后对银基催化剂的研究现状进展了小结并指出今后可能应用的领域,展示出良好的应用前景。
一、在碱性介质中的ORR机理在碱性溶液中,Yeager认为ORR主要有4e和2e两种反响途径:(1) 直接4e 反响途径O2+2H2O+4e→4OH-ψ°=0.401 V a(2) 2e-2e 逐步反响途径O2+H2O+2e→HO2-+OH-ψ°=-0.065 V bHO2-+H2O+2e→3OH-ψ°=0.867 V c中间产物HO2-或可发生歧化反响2HO2-→2OH-+O2 d反响b, c合起来即是反响a, 因此这种反响途径又可叫做准4e反响途径或连续4e反响途径,其中, 反响c被认为是速控步骤. 如果ORR按2e-2e逐步反响途径进展, 那么将主要面临两个问题: (1) 假设反响c没有进展,那么阴极反响的转移电子数减半, 能量密度降低; 而且电池的输出电压、功率性能也相应下降, (2)在碱性溶液中稳定的HO2-容易在催化剂的作用下发生反响d, 从而降低催化剂活性。
所以, 能直接催化氧复原按反响a的途径进展就显得尤为重要; 另一方面, 考虑到燃料电池的实用化, 催化材料也应具有在碱性溶液中寿命长和制作本钱低、储量丰富等特点, 而在上述的催化材料中,银是少数同时具有上述三项优点的催化材料之一。
但是, Ag 的这种4e反响途径与Pt还是有区别的,已有研究说明Ag在催化复原氧的过程中有过氧化氢产物, 在卤素离子的影响下, 这种现象就更加明显。
除此之外, Ag不仅具有良好的耐碱性, 而且在碱性电解质中随着OH-升高(0.1~11.1 mol/L)反而能提升Ag的催化活性。
炭载Pt_Ag双金属催化剂对甲醇氧化反应的电催化

炭载Pt-Ag 双金属催化剂对甲醇氧化反应的电催化毕丽晓刘增花孔德生郁章玉*冯媛媛*(曲阜师范大学化学与化工学院曲阜273165)摘要以NaBH 4为还原剂,将K 2PtCl 6和AgNO 3前体进行共还原制备了一系列具有不同组成的碳载Pt m Ag /C合金催化剂(m 为Pt /Ag 原子比,m 为0.05 1.0),在酸性介质中考察了该系列催化剂对甲醇氧化反应的电催化性能。
与单组分Pt /C 催化剂相比,系列Pt m Ag /C 催化剂呈现出较高的催化氧化甲醇的活性与抗CO 毒化能力,而且该催化剂的性能与其组成密切相关。
随m 值增加,Pt m Ag /C 催化剂对甲醇氧化反应的质量比催化活性(MSA )、本征催化活性(IA )与稳定性均逐步增加,当m =0.5时催化活性达到最高,其MSA 和IA 分别是Pt /C 催化剂的5.1和4.8倍。
关键词铂,银,去合金,酸性介质,甲醇电氧化中图分类号:O646文献标识码:A文章编号:1000-0518(2013)01-0107-07DOI :10.3724/SP.J.1095.2013.200532012-02-21收稿,2012-04-17修回山东省优秀中青年科学家奖励基金(BS2011NJ009)、山东省自然科学基金(ZR2010EM026)资助项目通讯联系人:郁章玉,教授;Tel /Fax :0537-*******;E-mail :zyu@mail.qfnu.edu.cn ;研究方向:表面电化学共同通讯联系人:冯媛媛,副教授;Tel :0537-*******;Fax :;E-mail :yfeng@mail.tsinghua.edu.cn ;研究方向:电催化直接甲醇燃料电池(DMFCs )具有低污染、无噪音以及燃料来源方便等特点,在未来的电子、通讯和交通等许多方面被认为是最佳的低温绿色替代能源[1-2]。
然而,迄今为止,该类燃料电池仍未得到大规模的商业化应用,原因之一在于甲醇氧化过程中涉及到的多电子转移过程会产生一些类CO 中间产物,这些物质很容易吸附在Pt 表面,占据Pt 的活性位,致使催化剂中毒[3-4]。
ag基氧还原催化剂

ag基氧还原催化剂
Ag基氧还原催化剂是指以银(Ag)为主要活性组分的催化剂,用于促进氧还原反应的进行。
氧还原反应是电化学反应的一种,在燃料电池、金属-空气电池等新能源领域有重要应用。
Ag基氧还原催化剂通常由Ag纳米颗粒、载体材料和助剂组成。
其中,Ag 纳米颗粒是催化剂的活性组分,负责催化氧还原反应;载体材料是用来支撑和稳定Ag纳米颗粒的结构材料,常用的载体材料包括碳黑、碳纳米管和金属氧化物等;助剂则可以增强催化剂的活性和选择性,常用的助剂包括铂、钯等贵金属元素。
Ag基氧还原催化剂具有较高的催化活性和稳定性,尤其在低温条件下表现出较好的性能。
此外,Ag基催化剂还可以通过优化制备条件、添加助剂等方式进一步改善其催化性能。
目前,Ag基氧还原催化剂的研究已经成为电化学和新能源领域的研究热点之一。
未来,随着对Ag基氧还原催化剂的深入研究和改进,有望进一步提高其催化活性和稳定性,为燃料电池、金属-空气电池等新能源技术的发展提供更加有效的技术支持。
《非贵金属Fe-N-C电催化剂的制备及其氧还原性能研究》范文

《非贵金属Fe-N-C电催化剂的制备及其氧还原性能研究》篇一非贵金属Fe-N-C电催化剂的制备及其氧还原性能研究一、引言随着全球能源危机和环境问题的日益突出,电化学能源转换与存储技术受到了广泛关注。
其中,氧还原反应(ORR)作为燃料电池和金属空气电池等电化学设备的核心反应,其催化剂的性能直接决定了设备的性能。
传统的贵金属基催化剂如铂(Pt)具有出色的ORR活性,但其高成本和稀缺性限制了其大规模应用。
因此,开发非贵金属基的ORR催化剂,特别是Fe-N/C催化剂,成为了当前研究的热点。
本文旨在研究非贵金属Fe-N/C电催化剂的制备方法及其氧还原性能。
二、材料与方法(一)材料准备本实验所需的材料包括铁源(如硫酸亚铁)、氮源(如氨水或三聚氰胺)、碳源(如炭黑或生物质)等。
(二)催化剂制备本实验采用高温热解法制备Fe-N/C电催化剂。
具体步骤包括:将铁源、氮源和碳源混合均匀,然后进行高温热解处理,得到Fe-N/C电催化剂。
(三)性能测试采用循环伏安法(CV)和线性扫描伏安法(LSV)等电化学测试方法,对所制备的Fe-N/C电催化剂的氧还原性能进行测试。
三、实验结果与分析(一)Fe-N/C电催化剂的制备结果通过高温热解法成功制备了非贵金属Fe-N/C电催化剂。
通过对制得的催化剂进行XRD、SEM等表征手段,发现催化剂中存在明显的Fe-N键和良好的碳结构。
(二)氧还原性能分析对所制备的Fe-N/C电催化剂进行CV和LSV测试,发现其在碱性溶液中表现出较好的氧还原性能。
通过对比不同条件下的CV和LSV曲线,分析了铁源、氮源、碳源的配比及热解温度等因素对氧还原性能的影响。
实验结果表明,适量的铁源和氮源以及适宜的热解温度有利于提高催化剂的氧还原性能。
(三)性能对比分析将所制备的Fe-N/C电催化剂与商业Pt/C催化剂进行性能对比。
在相同条件下测试,发现Fe-N/C电催化剂在碱性溶液中的氧还原性能与商业Pt/C相当,甚至在某些条件下表现出更优异的性能。
Au、Ag、Pd、Cu、Ni纳米催化剂设计构筑与催化氧化还原研究中期报告

Au、Ag、Pd、Cu、Ni纳米催化剂设计构筑与催化
氧化还原研究中期报告
纳米催化剂在催化氧化还原反应中具有独特的催化性能,能够提高
化学反应速率和选择性,并降低反应温度和能量消耗。
因此,纳米催化
剂广泛应用于环境治理、能源转化和化工生产等领域。
本次研究中,我们选择了五种常见的金属纳米颗粒(Au、Ag、Pd、Cu、Ni)作为催化剂,并针对其设计构筑和催化氧化还原反应进行了研究。
首先,在纳米催化剂的设计构筑方面,我们采用了两种方法:一种
是化学还原法,另一种是溶液相沉淀法。
通过比较两种方法的催化性能,发现化学还原法制备的纳米催化剂具有更高的催化活性和选择性。
其次,在催化氧化还原反应中,我们测试了五种纳米催化剂对环境
污染物(如苯酚、硝基苯和甲醛)和能源转化物(如乙醇和甲烷)的催
化氧化反应活性。
测试结果表明,在相同条件下,不同金属纳米颗粒的
催化活性存在明显差异,其中Pd纳米催化剂的催化活性最高,可以实现高效率、低能耗的氧化还原反应。
综上所述,本次研究为纳米催化剂的设计构筑和催化氧化还原反应
研究提供了重要的实验数据和理论基础,为开发高效率、低能耗的催化
剂提供了有益的参考。
Ag-Al2O3催化剂选择性催化还原稀薄燃烧NOx的研究

Ag-Al2O3催化剂选择性催化还原稀薄燃烧NOx的研究罗永明;郝吉明;傅立新;宁平【期刊名称】《环境工程》【年(卷),期】2004(022)006【摘要】本研究主要考察了丙烯为还原剂,溶胶-凝胶和共沉淀两种方法制备的Ag-Al2O3催化剂的活性,实验结果表明Ag(5)-Al2O3(SG)催化剂具有最高的活性.同时详细考察了C3H6浓度、NO浓度和空速等因素对Ag(5)-AlO3(SG)催化剂活性的影响,实验结果表明该催化剂在高空速条件下仍然具有良好的性能.此外,还考察了乙烯、丙烷和辛烷为还原剂,Ag(5)-Al2O3(SG)催化剂的活性,实验结果表明以辛烷为还原剂,该催化剂还原NOx的活性,特别是低温活性明显提高.【总页数】4页(P39-42)【作者】罗永明;郝吉明;傅立新;宁平【作者单位】昆明理工大学环境科学与工程学院,昆明,650093;浙江大学(西溪校区),催化研究所,杭州,310028;清华大学环境科学与工程系,北京,100084;清华大学环境科学与工程系,北京,100084;昆明理工大学环境科学与工程学院,昆明,650093【正文语种】中文【中图分类】X701【相关文献】1.Pd/TiO2催化剂上氢气选择性催化还原NOx的研究 [J], 张祎旸;曾慧;贾斌;王智华;刘志明2.柴油车NH3选择性催化还原NOx催化剂研究进展 [J], 施赟;王晓祥;李素静;李伟;单胜道;庄海峰;王群3.CeOx对低温选择性催化还原脱硝催化剂FeOx-MnOx/TiO2的改性研究 [J], 肖雨亭; 吴鹏; 王玲; 张亚平4.SO2-4功能化处理对Fe2O3催化剂上氨选择性催化还原Nox性能的促进机理研究 [J], 王慧敏; 马延平; 陈西颖; 许思远; 陈金定; 张秋林; 赵宾; 宁平5.Cu-SAPO-18催化剂氨选择性催化还原NOx钾中毒机理的研究 [J], 孟繁伟;高琦;叶青;李晨曦因版权原因,仅展示原文概要,查看原文内容请购买。
Ag Ag2WO4催化剂光催化还原CO2
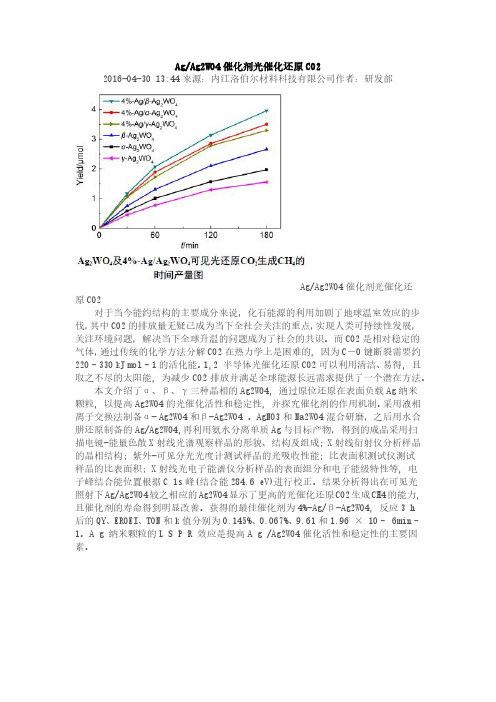
Ag/Ag2WO4催化剂光催化还原CO22016-04-30 13:44来源:内江洛伯尔材料科技有限公司作者:研发部Ag/Ag2WO4催化剂光催化还原CO2对于当今能约结构的主要成分来说,化石能源的利用加剧了地球温室效应的步伐,其中CO2的排放量无疑已成为当下全社会关注的重点,实现人类可持续性发展,关注环境问题,解决当下全球升温的问题成为了社会的共识。
而CO2是相对稳定的气体,通过传统的化学方法分解CO2在热力学上是困难的, 因为C―O键断裂需要约220–330 kJ mol–1的活化能。
1,2 半导体光催化还原CO2可以利用清洁、易得, 且取之不尽的太阳能, 为减少CO2排放并满足全球能源长远需求提供了一个潜在方法。
本文介绍了α、β、γ三种晶相的Ag2WO4, 通过原位还原在表面负载Ag纳米颗粒, 以提高Ag2WO4的光催化活性和稳定性, 并探究催化剂的作用机制。
采用液相离子交换法制备α- Ag2WO4和β-Ag2WO4 。
AgNO3和Na2WO4混合研磨,之后用水合肼还原制备的Ag/Ag2WO4,再利用氨水分离单质Ag与目标产物,得到的成品采用扫描电镜-能量色散X射线光谱观察样品的形貌、结构及组成; X射线衍射仪分析样品的晶相结构; 紫外-可见分光光度计测试样品的光吸收性能; 比表面积测试仪测试样品的比表面积; X射线光电子能谱仪分析样品的表面组分和电子能级特性等, 电子峰结合能位置根据C 1s峰(结合能284.6 eV)进行校正。
结果分析得出在可见光照射下Ag/Ag2WO4较之相应的Ag2WO4显示了更高的光催化还原CO2生成CH4的能力, 且催化剂的寿命得到明显改善。
获得的最佳催化剂为4%-Ag/β-Ag2WO4, 反应3 h后的QY、EROEI、TON和k值分别为0.145%、0.067%、9.61和1.96 × 10– 6min–1。
A g 纳米颗粒的L S P R 效应是提高A g /Ag2WO4催化活性和稳定性的主要因素。
Ag在碱性介质中作氧还原催化剂综述

Ag在碱性介质中作氧还原催化剂综述本文较为全面地归纳了氧还原反应中使用的各种银基催化剂:纯银、碳载银、银合金、银-过渡金属氧化物。
论述了催化剂的机理、优缺点。
此外,简要阐述了银基催化剂的一些合成方法,并介绍了催化剂的形貌、PH值、成分对氧还原反应的影响,最后对银基催化剂的研究现状进行了小结并指出今后可能应用的领域,展示出良好的应用前景。
一、在碱性介质中的ORR机理在碱性溶液中,Yeager认为ORR主要有4e和2e两种反应途径:(1) 直接4e 反应途径O2+2H2O+4e→4OH-ψ°=0.401 V a(2) 2e-2e 逐步反应途径O2+H2O+2e→ HO2-+OH-ψ°=-0.065 V bHO2-+H2O+2e→3OH-ψ°=0.867 V c中间产物HO2-或可发生歧化反应2HO2-→2OH-+O2 d反应b, c合起来即是反应a, 因此这种反应途径又可叫做准4e反应途径或连续4e反应途径,其中, 反应c被认为是速控步骤. 如果ORR按2e-2e逐步反应途径进行, 则将主要面临两个问题: (1) 若反应c没有进行,则阴极反应的转移电子数减半, 能量密度降低; 而且电池的输出电压、功率性能也相应下降, (2)在碱性溶液中稳定的HO2-容易在催化剂的作用下发生反应d, 从而降低催化剂活性。
所以, 能直接催化氧还原按反应a的途径进行就显得尤为重要; 另一方面, 考虑到燃料电池的实用化, 催化材料也应具有在碱性溶液中寿命长和制作成本低、储量丰富等特点, 而在上述的催化材料中,银是少数同时具有上述三项优点的催化材料之一。
但是, Ag 的这种4e反应途径与Pt还是有区别的,已有研究表明Ag在催化还原氧的过程中有过氧化氢产物, 在卤素离子的影响下, 这种现象就更加明显。
除此之外, Ag不仅具有良好的耐碱性, 而且在碱性电解质中随着OH-升高(0.1~11.1 mol/L)反而能提升Ag的催化活性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Ag在碱性介质中作氧还原催化剂综述本文较为全面地归纳了氧还原反应中使用的各种银基催化剂:纯银、碳载银、银合金、银-过渡金属氧化物。
论述了催化剂的机理、优缺点。
此外,简要阐述了银基催化剂的一些合成方法,并介绍了催化剂的形貌、PH值、成分对氧还原反应的影响,最后对银基催化剂的研究现状进行了小结并指出今后可能应用的领域,展示出良好的应用前景。
一、在碱性介质中的ORR机理在碱性溶液中,Yeager认为ORR主要有4e和2e两种反应途径:(1) 直接4e 反应途径O2+2H2O+4e→4OH-ψ°=0.401 V a(2) 2e-2e 逐步反应途径O2+H2O+2e→ HO2-+OH-ψ°=-0.065 V bHO2-+H2O+2e→3OH-ψ°=0.867 V c中间产物HO2-或可发生歧化反应2HO2-→2OH-+O2 d反应b, c合起来即是反应a, 因此这种反应途径又可叫做准4e反应途径或连续4e反应途径,其中, 反应c被认为是速控步骤. 如果ORR按2e-2e逐步反应途径进行, 则将主要面临两个问题: (1) 若反应c没有进行,则阴极反应的转移电子数减半, 能量密度降低; 而且电池的输出电压、功率性能也相应下降, (2)在碱性溶液中稳定的HO2-容易在催化剂的作用下发生反应d, 从而降低催化剂活性。
所以, 能直接催化氧还原按反应a的途径进行就显得尤为重要; 另一方面, 考虑到燃料电池的实用化, 催化材料也应具有在碱性溶液中寿命长和制作成本低、储量丰富等特点, 而在上述的催化材料中,银是少数同时具有上述三项优点的催化材料之一。
但是,Ag 的这种4e反应途径与Pt还是有区别的,已有研究表明Ag在催化还原氧的过程中有过氧化氢产物, 在卤素离子的影响下, 这种现象就更加明显。
除此之外, Ag不仅具有良好的耐碱性, 而且在碱性电解质中随着OH-升高(0.1~11.1 mol/L)反而能提升Ag的催化活性。
比如: ORR还原产物为OH-而基本不生成HO2-, 当在较高浓度碱性电解质中Ag电极催化ORR的性能要优于Pt的催化性能, 且Ag的质量密度约为Pt的一半, 则同样的载量, Ag的比表面积将大于Pt, 有利于增大表观总电流。
1.PH值的影响之前的研究表明,对于像Pt和Ag这样的金属,ORR的速率决定步骤是:O2a + e- O2- ; ψ°=0.562±0.03V e在Ag(111)表面,此步骤e的电势值在PH=0至13之间并不随PH值增大而改变,体现出PH 的独立性,导致e步骤的反应过电势η值只从PH=0的1.53V减小到PH=14的0.7V。
在e步骤后,ORR发生的是直接生成OH-或者生成中间产物HO2-。
我们可通过Tafel曲线来揭示这个现象:基于催化剂为Pt的过电势,Tafel曲线中出现了两个明显的区域:在低过电势区域中,曲线斜率为-60mV/dec,表现出-30mV/PH单元的依赖性;而在高过电势区域中,曲线斜率为-120mV/dec,并无PH值的依赖性。
在低过电势区域,Tafel斜率-60mV/dec,是由ORR 中间产物的而引起的氧化物中间物覆盖在Pt催化剂表面,呈现出的是Temkin吸附等温线。
在高电势区域,Tafel斜率为-120mV/dec,吸附主要由Langmur吸附等温线控制,在此电位之下,主要的氧化物都都消失。
类似Pt,碱性电解质中,在Ag的表面发生ORR同样是4e 过程,反应顺序一样,Tafel曲线也同样具有两个明显的斜率区域,因此,基于实验数据,有利地证明Ag作为催化剂的机理和Pt类似。
但不同的是在Pt催化剂中,Pt在低的过电势时呈现出强的PH值依赖性,而Ag却没有PH的依赖性。
所以,当PH值升高时,更有利于许多非Pt催化剂反应,因此在采用碱性电解液的金属空气电池中,阴极的空气电极催化剂可以完全不用Pt,而采用如Ag、MnO x、金属氮化物和复合金属氧化物等廉价材料。
于是分别在0.1M KOH和0.1M HClO4中进行RRDE测试,探索PH值对Ag(111)的ORR 机理的影响。
在酸性环境中,在低的过电势下,2e机理占主导,高的过电势下,2e和4e过程都存在于反应之中。
若从酸性变为碱性环境,则其过电势减小400mV,同时ORR发生的是4e过程,所产生的H2O2量极少。
在碱性电解质中,Tafel曲线呈现的两个明显的区域,在低过电势下,曲线斜率为-85mV/dec,在高的过电势下,曲线斜率为-125mV/dec。
这些数据都是表明在碱性介质中Ag表面发生的ORR跟Pt类似的有利支撑。
然而,对于Pt来说,无论是在酸性还是碱性介质中,表面发生的都是4e过程占主导地位。
从表观上来看,Pt和Ag上的ORR均按4e反应途径进行,而微观上看氧分子在两种材料上的吸附却有所差异,比如Pt只需要2个原子就能达到要求,而Ag却需要3-4个,且吸附能力不强,那么,微小干扰就会影响到催化效果。
而在HClO4中,由于ClO4- 和Cl-在很宽的电势范围都可以在Ag上吸附,从而加大了ORR的超电势,且产物H2O2的比率显著增加,但并不是说杂质的吸附都会对ORR产生不利的影响,如果吸附选择物得当,或许还能产生正面的影响。
例如,一个很有趣的例子,2012年,Casarin等根据自己的技术将酞菁铁(FePc)吸附在Ag(110)上构成修饰表面[FePc/Ag(110)] ,通过STM测试发现Fe原子以顶位或短桥位吸附在Ag(110)表面之上,呈长方矩形或倾斜矩阵排列,他们通过在330K、超高真空环境下使用离子枪喷射质子的方式模拟燃料电池中还原态氧得到氢形成水或过氧化氢的过程,经过一系列的测试和计算表明,以倾斜矩阵方式排列的FePc几乎不能吸附和还原氧,而以短桥位、长方矩阵形式排列的FePc对氧的还原效果最好,氧气在该催化剂上实现了可逆的氧化还原过程,且一个可逆过程循环完后,催化剂的组分、形貌等几乎完全回到初始状态。
在最初吸附氧后,吸附形式发生转变,由Fe原子顶位吸附转换为Fe原子与两个氧原子共同以短桥位吸附在Ag(110)表面,此时,Fe原子被大酞菁环所掩盖,这种催化剂材料可替代Pt称为低温燃料电池中的高效、长寿命阴极催化剂。
因此,吸附物的选择以及它在银催化剂表面的吸附行为会对ORR产生重要影响,ClO4- 和Cl-的吸附是占用了氧分子在Ag表面的吸附位,阻止了氧气还原(负催化剂),而顶位吸附的FePc不但没有占用,反而促进了氧的吸附和还原(正催化剂),因此,基于ClO4- 和Cl-、FePc等吸附物种与Ag(110)形成的表面以及这些表面所表现出的催化效果的事实,预示着通过选择不同物种对银表面进行化学修饰,就可能得到新型化学修饰电极,在这个角度上看,可以认为是催化剂实施的一种功能和结构的调控,这有可能成为新型催化剂的研究方向。
2.晶面效应Blizanac等采用RRDE方法对Ag催化剂的ORR进行研究,发现不同的晶面结构所造成的ORR活性也不一样,在相同的温度和过电势下,ORR活性顺序Ag(110)>Ag(111)>Ag(100)。
然而,在不同温度和不同的过电势下,ORR的活化能的最大值仍然为(100)晶面,最小值为(110)晶面。
这些晶面的不同所引起的ORR活性不同可通过OH和O2在这些晶面上的吸附平衡理论来解释:Ag(110)晶面对OH具有强吸附作用,由于OH高度覆盖在Ag表面,按理应该表现出的是低的ORR活性,但是由于Ag(110)对O2同样具有很强的亲和力, 因此呈现出Ag(110)的高ORR活性。
另一方面,对于Ag(100)来说,无论是O2和OH,都表现出弱的亲和力,因此呈现出低的ORR活性。
可是,OH在Pt(hkl)和Ag(hkl)晶面上吸附是不同的,主要表现OH在Ag(hkl)吸附层上的吸附是可逆的,而OH在Pt(hkl)表面的吸附是先进行可逆吸附,后进行不可逆吸附。
因此,由于存在可逆与不可逆的相互转换,从而导致在阴极和阳极之间进行扫描时Pt(hkl)晶面上出现电流滞后的现象,而在Ag (hkl)上却无法观察到ORR电流滞后现象。
所以,结合Ag(hkl)的可逆伏安法性质以及没有ORR电流滞后现象,使得OH在Ag上的吸附要弱于Pt,但不能否认的是Ag对O2的亲和力足够使得O-O键断裂,导致一个4e氧还原反应过程。
Wang等人通过计算和实验方法的相互结合,对Ag的纳米十面体和纳米立方体的晶面效应进行ORR研究,发现Ag的纳米十面体结构被10个Ag(111)晶面所环绕,而Ag的纳米立方体结构是由6个Ag(100)晶面所环绕。
K-L方程计算得出Ag的纳米十面体的电子转移数n=3.8,纳米立方体的电子转移数n=3.1和3.7。
所以说,纳米十面体结构Ag(110)的ORR是4e过程,而纳米立方体Ag(100)主要遵循的是2e过程。
不同之处就在于中间产物OH*在两个晶面上的不同的吸附行为。
通过DFT计算,发现在Ag(100)晶面上OH*的吸附能越高使得O2和OOH*的可利用位置越少,最终阻碍ORR的动力学性质。
3.尺寸效应Ag的催化活性随着其颗粒尺寸大小的减小而增大。
Li等人合成出尺寸大小范围为2~9nm之间的Ag/C催化剂,平均颗粒大小为5.4nm。
将纳米颗粒(NPs)平均大小为5.4nm的Ag/C催化剂应用到由两个不同阴极组成的阴离子交换膜电池上,发现有良好的催化活性,高的能量密度和低的过电势。
同样地,将这些NPs通过沉积法沉积到Vulcan XC-72上,对其催化剂进行RRDE和CV法进行测试来研究其ORR机理。
计算表明,Ag/ Vulcan XC-72的电子转移数n=3.94,而Pt/C的电子转移数n=3.91。
另一方面,通过T afel 曲线可以看出,如图1所示,Ag/ Vulcan XC-72和Pt/C都有两个明显的区域:在低的过电势下,Ag/ Vulcan XC-72曲线斜率为50.4mV/dec,而Pt/C的曲线斜率为46mV/dec;在高的过电势下,Ag/ Vulcan XC-72曲线斜率为125.4mV/dec,而Pt/C的曲线斜率为128.5mV/dec。
相似的T afel曲线表明Ag/ Vulcan XC-72和Pt/C具有相似的催化剂ORR 机理。
另外,Singh和Buttry对多晶银(PC)和平均直径为4.5nm的Ag纳米颗粒(Ag NP)分别在0.1M KOH溶液中进行CV和RDE扫描测试,通过测试和K-L方程进行计算电子转移数n值,发现两种催化剂的n值在3-4之间,Ag NP具有更大的n值,而块状的Ag具有低的n值,这可能是由于更多的缺陷表面造成OH强吸附而成,所以阻碍了ORR动力学性质。
