第10章 羟基酸和羰基酸
第十章 羟基酸和酮酸习题

第十章羟基酸和酮酸一.学习要求1、掌握羟基酸和酮酸的命名;羟基酸和酮酸的重要化学性质;α-酮酸的转氨基反应、β-酮酸的脱羧反应及其酮式分解和酸式分解;乙酰乙酸乙酯活泼亚甲基的化学性质,酮式-烯醇式互变异构体的化学性质。
2、熟悉柠檬酸在酶催化下转变成α-酮戊二酸的反应,酮体组成及其应用。
3、了解重要羟基酸和酮酸的性质和用途。
二.本章要点羟基酸和酮酸同属于取代羧酸(substituted acid),在有机合成和生命代谢中都是十分重要的化合物。
取代羧酸为多官能团化合物,其分子中既含有羧基,又有其它官能团,在化学性质上不仅具有单官能团的典型反应,而且还具有分子中不同官能团之间相互影响的一些特殊性质。
因此掌握他们的特殊性质是本章要点。
(一)羟基酸的结构和命名羟基酸的俗名应用广泛,因为这些化合物的历史远比有机化合物命名原则的历史长,更为人们熟悉。
如柠檬酸、苹果酸、水杨酸等。
羟基酸的系统命名也要掌握。
(二)羟基酸的化学性质在化学性质上,酸性、热不稳定性是多官能团之间相互影响所表现出来的特性。
1.羟基酸的酸性在脂肪酸分子中引入羟基-I效应能显著增加酸的强度;而邻羟基苯甲酸的酸性较强,则是几种影响因素共同作用的结果,包括形成分子内氢键而使邻-羟基苯甲酸的负离子稳定。
2.受热分解羟基酸加热时,因羟基的相对位置不同而脱水产物各异。
β-羟基酸脱水生成α,β-不饱和酸反应应用较广泛。
邻羟基苯甲酸加热脱羧生成苯酚。
(三)酮酸的命名酮酸的系统命名是以羧酸为母体,酮基作为取代基,用“氧代”表示并标出位置。
普通命名常用某酮酸或俗名。
(四)酮酸的化学性质 1. 脱羧反应 β-酮酸易脱羧。
2. α-酮酸的氨基化反应α-酮酸的氨基化反应在生物体内都是酶催化完成,因而具有重要的意义。
临床上,用简单的化学反应测定血清中谷丙转氨酶的活性,就是根据α-酮戊二酸转氨基反应与谷丙转氨酶有关而设计的。
(五)酶催化下酮酸和醇酸的相互转变酮酸 醇酸β-羟基丁酸、β-丁酮酸和丙酮的总称为酮体。
羟基酸和酮酸

第10 章羟基酸和酮酸本章重点介绍羟基酸和酮酸命名,相互影响的性质、酸性;脱水反应;转氨作用;脱羧反应;酮酸分解反应;醇酸和酮酸的体内化学过程;前列腺素的结构;酮式- 烯醇式互变异构羧酸分子中烃基上的氢原子被其他原子或原子团取代所形成的化合物称为取代羧酸( substituted carboxylic acid )。
根据取代基的种类不同,取代羧酸可分为卤代羧酸( halogeno acid)、羟基酸( hydroxy acid )、羰基酸( carbonyl acid )以及氨基酸( amino acid )等几类;羟基酸又可分为醇酸( alcoholic acid )和酚酸( phenic acid ),羰基酸又可分为醛酸( aldehydo acid)和酮酸( keto acid )。
取代羧酸分子中除含羧基外,还含其它官能团,因此它是一类具有复合官能团的化合物。
各官能团除具有其特有的典型性质外,由于不同官能团之间的相互影响,还具有某些特殊反应和生物活性。
卤代酸不作专题介绍,氨基酸将在第17 章中讨论,本章只讨论羟基酸和酮酸。
羟基酸广泛存在于动植物体内,它们中有的是动植物体内进行生命活动的物质,有的是合成药物的原料,有的可作为食品的调味剂。
酮酸是人体内糖、脂肪和蛋白质等代谢过程中产生的中间产物。
因此在有机合成及生物代谢中羟基酸和酮酸都是极其重要的化合物。
你在学完本章以后,应该能够回答以下问题:1 .氨基酸的结构特点是什么?可分为几类?如何命名?2 .酸的结构特点分别是什么?可分为几类?如何命名?3.羟基酸和酮酸的重要化学性质是什么?4.哪些因素影响羟基酸酸性?5.α-酮酸的分解为什么比β-酮酸难解?6.何为酮式—烯醇式互变异构现象?酮式—烯醇式互变异构现象产生的原因及条件是什么?7. α- 酮酸氨基化反应的生物学意义是什么?10. 1 羟基酸的结构和命名温习提示:羧酸的命名及结构羟基酸是分子中既含有羟基又含羧基两种官能团的化合物。
10-第十章_羟基酸和酮酸

-I
OH
-I +C
OH
Pka 4.17
3.00
4.12
4.54
酸性: o->m->p-
第十章 羟基酸和酮酸
9/40
C O O O H
解释:
C O
OH O H
+ H
水杨酸
水杨酸阴离子
a.o-羟基苯甲酸可形成分子内氢键,增大O-H极性, 利于H+离解,形成稳定的-COO (分散负电荷)。 b.o-羟基苯甲酸结构中,由于空阻使-COOH与苯环 不共面,+C效应弱,能形成稳定的-COO ,酸性↑。 c.m-羟基甲酸,+C效应传递受阻,-I起作用,使 传递距离较大,-I效应较弱,酸性略大于苯甲酸。 d.p-羟基苯甲酸,+C>-I,使O-H极性减小,电 离度↓,酸性<苯甲酸。
CH3-CH-COOH OH
2(α)-羟基丙酸
2(α)-hydroxy propanoic acid
HOOCCH2CHCOOH OH 羟基丁二酸(苹果酸)
malic acid
乳酸 lactic acid
羟基 (hydroxy)
第十章 羟基酸和酮酸
5/40
OH OH HOOCCH-CHCOOH 2,3-二羟基丁二酸 (酒石酸)
第十章 羟基酸和酮酸
19/40
CH3COCOOH
2-氧代丙酸 (丙酮酸)
pyruvic acid (acetone acid)
CH3COCH2COOH 3(β)-氧代丁酸 3(β)-丁酮酸
(β-butanone acid)
乙酰乙酸
acetoacetic acid
O HOOCCCH2COOH 2-氧代丁二酸 丁酮二酸 butanone diacid 草酰酸
有机化学课件——Chapter 10 羟基酸和酮酸

第十章 羟基酸和酮酸
Hydroxy Acids and Keto Acids
1
导言
¾ 取代羧酸: 羧酸分子中烃基上的氢原子被其他原子或官能团取代 后的化合物.
¾ 常见取代羧酸: 卤代酸、羟基酸、氧代酸(酮酸)和氨基酸.
R CH COOH
X
卤代酸(halogeno acid)
烯醇型分子存在的条件
OO CH3CCH2COCH2CH3
酮型(93%)
H
O
O
C
C
CH2CH3
H3C
CH
O
烯醇型(7%)
分子中的亚甲基氢受两个吸电子基团影响而酸性增强。 形成烯醇型产生的双键应与羰基形成π-π共轭,使共 轭体系有所扩大和加强,能量有所降低。 烯醇型可形成分子内氢键,构成稳定性更大的环状螯合物。
NADH + H+
NAD+ + H2O
NH3+
HOOCCH2CH2COCOOH + NH3 α -酮戊二酸
谷氨酸脱氢酶
-OOCCH2CH2CHCOO谷氨酸
有机化学课件
31
第10章 羟基酸和酮酸
4. 酶催化下醇酸和酮酸的相互转化
OH
苹果酸脱氢酶
HOOCCH2CHCOOH
苹果酸
O HOOCCH2CCOOH
O
= =
OH HO-C
R-CH +
HC-R
C OH HO
-2H2O △
O
¾ β-醇酸分子内脱水成共轭烯酸
O
O=
R-CH C
交酯
O=C CH-R
O
CH3CH2CHCH2COOH OH COOH H OH
羟基酸和酮酸

223 第10章羟基酸和酮酸本章重点介绍羟基酸和酮酸命名相互影响的性质、酸性脱水反应转氨作用脱羧反应酮酸分解反应醇酸和酮酸的体内化学过程前列腺素的结构酮式-烯醇式互变异构等。
羧酸分子中烃基上的氢原子被其他原子或原子团取代所形成的化合物称为取代羧酸substituted carboxylic acid。
根据取代基的种类不同取代羧酸可分为卤代羧酸halogeno acid、羟基酸hydroxy acid、羰基酸carbonyl acid以及氨基酸amino acid等几类羟基酸又可分为醇酸alcoholic acid和酚酸phenic acid羰基酸又可分为醛酸aldehydo acid和酮酸keto acid。
取代羧酸分子中除含羧基外还含其它官能团因此它是一类具有复合官能团的化合物。
各官能团除具有其特有的典型性质外由于不同官能团之间的相互影响还具有某些特殊反应和生物活性。
卤代酸不作专题介绍氨基酸将在第17章中讨论本章只讨论羟基酸和酮酸。
羟基酸广泛存在于动植物体内它们中有的是动植物体内进行生命活动的物质有的是合成药物的原料有的可作为食品的调味剂。
酮酸是人体内糖、脂肪和蛋白质等代谢过程中产生的中间产物。
因此在有机合成及生物代谢中羟基酸和酮酸都是极其重要的化合物。
你在学完本章以后应该能够回答以下问题1 氨基酸的结构特点是什么可分为几类如何命名2 酸的结构特点分别是什么可分为几类如何命名3 羟基酸和酮酸的重要化学性质是什么 4 哪些因素影响羟基酸酸性5 α-酮酸的分解为什么比β-酮酸难解6 何为酮式—烯醇式互变异构现象酮式—烯醇式互变异构现象产生的原因及条件是什么7 α-酮酸氨基化反应的生物学意义是什么101 羟基酸的结构和命名温习提示羧酸的命名及结构羟基酸是分子中既含有羟基又含羧基两种官能团的化合物。
羟基连接在脂肪烃基上的羟224 基酸称为醇酸alcoholic acid连接在芳环上的羟基酸称为酚酸phenolic acid。
第十章 羟基酸 酮酸
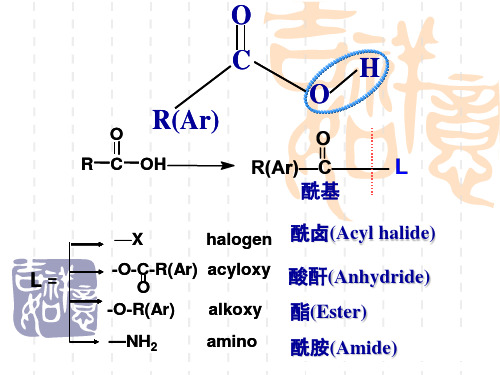
CH3CH2CH2COOH pKa 4.83 CH3CH2CHCOOH OH 3.65 CH3CHCH 2COOH OH 4.41
CH3CH2CHCOOH > CH3CHCH2COOH OH
H O CH3 C O CH2 C OC2H5 O CH3 C C H 烯醇式分子内的氢键 O C OC2H5
H O CH3 C O CH2 C OC2H5 O CH3 C C O C OC2H5
O
O
H 烯醇式分子内的氢键
凡分子中含有“ C CH2 G ”
O
O
( G为
, C OR , CN , C H , NO2 ) 结构的化合物都能发生酮式-烯醇互变异构
CH2 H2C COOH α -酮戊二酸
草酰琥珀酸
5. 水杨酸及其衍生物(柳酸) COOH 水杨酸(柳酸) OH 水杨酸具有杀菌能力,其酒精溶液可以治疗由霉 菌引起的皮肤病。它的钠盐可用作食品的防腐剂,同 时也是治疗风湿性关节炎的药物。
COOH OCOCH 3
乙酰水杨酸 (阿司匹林)
作用:解热镇疼。 APC(复方阿司匹林):阿司匹林、非那西丁、咖啡因
COOH OH > OH
> CH3CH2CH2COOH
COOH
OH
COOH >
OH 羟基与羧基间的距离越大,酸性越弱。 一般情况:
醇酸和酚酸中的羟基不能与Na2CO3 成盐
COOH OH + Na2CO3 COONa OH
2. 氧化反应 由于α- 醇酸中的羟基受羧基的影响,它比醇 中的羟基容易氧化。
α-酮酸的氨基化反应
《羟基酸和酮酸》课件

化工原料
某些酮酸可用作化工原料,如丙二酸、丁二酸 等,用于生产塑料、合成纤维等。
农业应用
酮酸可以作为植物生长调节剂,促进植物生长和发育。
羟基酸和酮酸的比较与选择
性质差异
羟基酸具有亲水性,而酮酸具有亲脂性,因此两者在溶解性和化学 性质上有所不同。
应用领域
羟基酸主要应用于护肤、食品和制药领域,而酮酸则更多应用于生 物合成、化工和农业领域。
选择依据
根据实际需求选择合适的羟基酸或酮酸。例如,在护肤品中通常选择 羟基酸,而在制药工业中可能更倾向于使用酮酸作为合成原料。
04 羟基酸和酮酸的合成方法
羟基酸的合成方法
醛酸合成法
利用醛和羧酸在催化剂作用下合成醛酸,是工业上广泛应用的方 法。
酯化法
通过羧酸与醇的酯化反应生成酯,再经水解得到羟基酸。
羧酸酯还原法
将羧酸酯在还原剂作用下还原成羟基酸,常用的还原剂有氢气、 金属钠等。
酮酸的合成方法
羧酸酯氧化法
将羧酸酯在氧化剂作用下氧化成酮酸,常用 的氧化剂有过氧化氢、硝酸等。
酮酯合成法
利用酮与羧酸酯在催化剂作用下合成酮酯, 再经水解得到酮酸。
羧酸还原法
将羧酸在还原剂作用下还原成酮酸,常用的 还原剂有氢气、金属钠等。
羟基酸和酮酸作为重要的有机化合物,其研究和 应用领域将继续拓展,特别是在生物医药、环保 、新能源等领域。
2
随着技术的进步,羟基酸和酮酸的制备工艺将不 断优化,提高生产效率和降低成本。
3
针对羟基酸和酮酸的生理活性研究将更加深入, 有望发现更多新的应用领域和用途。
THANKS 感谢观看
不同种类的羟基酸具有不同的颜色和外观,可用于初 步鉴别。
羟基酸的化学性质
第十章取代羧酸

( 以符号 I 表示 )。
H
CH3CH2CH2Cl
H
δ+
C H
+ δ+ δ + δ δ
C H C H Cl
H
H
产生原因:成键原子的电负性不同 。
本 特 质:极性共价键产生的电场引起邻近价键电荷 的偏移。 点:沿碳链传递,随碳链增长迅速减弱或消失。 比较标准:以H原子为标准。
C
X
C
H
C
Y
吸电子诱导效应 比较标准 -I效应 I=0 诱导效应的相对强弱
γ等标明羟基的位置。一些醇酸常用俗名。
CH2 COOH HO C CH2 COOH 3-羧基-3-羟基戊二酸(柠檬酸,枸橼酸) citric acid COOH
HO
CH HC
COOH COOH 3-羧基-2-羟基戊二酸(异柠檬酸) isocitric acid
CH2 COOH
(二) 醇酸的物理性质(自学)
一、酮酸的分类和命名
根据酮基和羧基的相对位置不同,酮酸可分为α、 β、γ ……酮酸。 酮酸的命名也是以羧酸为母体,酮基作取代基。
CH3 C COOH O -丙酮酸 pyruvic acid CH3 C O -丁酮酸 -butanone acid CH2COOH HOOC C CH2COOH O 丁酮二酸(草酰乙酸) butanone diacid
二、酮酸的化学性质 (一)酸性 由于羰基氧吸电子能力强于羟基,酮酸 的酸性强于相应的醇酸,更强于相应的羧酸, 并且α-酮酸比β-酮酸的酸性强。
CH3 C COOH CH3 C CH2COOH CH3 CH COOH > > OH O O
> HOCH2CH2COOH > CH3CH2COOH
第十章+有机酸(修改稿)

C H 3C HC H C O O H+H 2O
H O O C C H C H 2 C O O H O H
H
C O O H
CC
H O O C
H
+H 2 O
CH 2=CHCOOH 丙烯酸
脂环酸 芳香酸
COOH
环己基甲酸
COOH
苯甲酸
--
二元酸
HOOC COOH 乙二酸
HOOCCH=CHCOOH 丁烯二酸
COOH COOH
1,2-环戊基二甲酸
COOH COOH
邻苯二甲酸
2. 羧酸的命名 羧酸的系统命名法与醛的命名相似,只需相应地将“醛”
字改成“酸”字。 (1)饱和脂肪酸的命名
(3)生成酸酐 一元羧酸(除甲酸外)与脱水剂(如 P2O5)共热时,两分子羧酸可脱去一分子水,生成酸酐。
O
O
OO
RC O H +H O C RP Δ 2O 5 R C OC R+H 2O
酸酐
二元羧酸可发生分子内脱水生成环酸酐,如丁二酸脱水 可生成丁二酸酐,邻苯二甲酸脱水可生成邻苯二甲酸酐。
--
(4)生成酰胺 羧酸分子中羧基上的羟基被氨基(—NH2) 取代生成的化合物叫做酰胺。在羧酸中通入氨气或加入碳酸 铵得到羧酸的铵盐,铵盐加热后分子内失水即可生成酰胺。
羟基连在芳香烃上h3chccohohocoohoh22羟基丙酸乳酸邻羟基苯甲酸水杨酸羟基丙酸乳酸邻羟基苯甲酸水杨酸1结构一羟基酸的结构和命名2命名脂肪族羟基酸找主链编号写名称羰基co永远是1号位标注羟基oh位置将羟基看成取代基包含羧基在内的最长碳链h3chccohoho22羟基丙酸乳酸hch2cccohohhooo羟基丁二酸苹果酸23羟基丁二酸苹果酸23二羟基丁二酸酒石酸二羟基丁二酸酒石酸hcchhohoccooohohcoohhoohoh2命名芳香族羟基酸以苯甲酸为母体编号写名称一羟基酸的结构和命名c原子永远是1号位coohoh邻羟基苯甲酸345三羟基苯甲酸没食子酸三羟基苯甲酸没食子酸二酮酸的结构和命名分子含有羧基和酮基两种官能团的化合物称为酮酸
第十章 羟基酸和酮酸
Organic Chemistry
第十章 羟基酸和酮酸
Hydroxy Acid and Carbonyl Acid
[重点]
1、羟基酸和酮酸分类和命名。
2、醇酸、酚酸和酮酸的酸性。
3、β-醇酸的脱水;α-醇酸、α-酮酸与
Tollens试剂的反应;β-酮酸的分解。
4、酚酸与FeCl3的显色。
P257-258习题:1(1,2,3,4,5,6)、2(1,4,6)、3、
OH
排序: ③ ② ① ⑤ ④ 2、①CH3COOH ② F3CCOOH ③ HCOOH ④Cl3CCOOH 排序: ② ④ ③ ① 3、① ② ③
OH
CH2OH COOH
④ H2CO3 排序: ② ④ ③ ①
二、用化学方法鉴别下列化合物: 1、草酸
乙酸 托伦试剂 甲酸 乙醛 × KMnO4/H+ 褪色(草酸) × Ag Ag × (乙酸)
4.
CH3COCH2COOC2H5
(5)α-戊酮二酸(3-草酰丙酸)
(6)β-羟基戊酸
2、 1. CH3CHCH2COOH
1.
PBr3
CH3CHCH2COBr Br
OH
O (4) HOOCCH2COCOOH
OH COOH
CH3CCOOH + CO2
O O C COOH CH3
(6)
+ CH3COCl
+ HCl
3、
1. 乙酰水杨酸 水杨酸 水杨酸甲酯 乙酰乙酸乙酯 NaHCO3
CO2 CO2 (-) (-)
FeCl3
(-) 紫色 (-) 黄色
(-) 紫色 紫色 (-)
I2 / NaOH
2. 丙酮酸 草酰乙酸甲酯 2,4 - 戊二酮 丙酮 NaHCO3
【北京大学】《医用有机化学》第10章-醇酸和酮酸--一等奖课件

COOH
OH
3.0
HO
OH
4.12
4.54
《医用有机化学》
北京大学
1.酸性
.. 酚酸:酸性由位置决定。
O
COOH
OH
C OH
CO
..
..
H O
HO
OH
+C
-I
分子内氢键,
-I
-I
增加了羧基中
氧氢键极性。
《医用有机化学》
北京大学
1.酸性
COOH NO2
COOH
COOH
NO2 COOH
间位只存在 -I效应
CH3CHCH2CH2COOH OH
+ H2O OO
γ-戊内酯
CH2CH2CH2CH2COOH OH
+ H2O
OO
δ-戊内酯
《医用有机化学》
北京大学
3.醇酸加热脱水反应
g-醇酸比d-醇酸更易脱水,通常室温下即
可失水成内酯,因此游离的γ-醇酸很难存在, 通常以γ- 醇酸盐的形式保存。
O
+ NaOH O
北京大学
2.α-酮酸的氨基化反应
α-酮酸与氨在催化剂(如生物体内的酶)作用下 可转变成α-氨基酸,称为α-酮酸的氨基化反应。
O NH3
H3C C COOH 酶
NH H3C C COOH H
NH3 H3C CH COO
生物体内,α-酮酸与α-氨基酸在各种转氨酶的作用下 可以发生相互转换,产生新的α-酮酸与α-氨基酸。如:
RCHCOOH
OH
OO R C C OH
《医用有机化学》
北京大学
一、羟基酸的分类和和命名
1、羟基酸的分类 羟基酸可分为醇酸和酚酸两类:
大学课件有机化学-第10章

学习要求: 1.熟练掌握羟基酸、羰基酸的命名 2.熟练掌握羟基酸、羰基酸的化学性质 3.了解互变异构现象
第一节 一、概述 1.含义
羟基酸
2.分类
烃基不同 醇酸 酚酸 羟基的位置: α - 醇酸 、β- 醇酸 、 δ - 醇酸 γ - 醇酸 、
3.命名
CH3CHCOOH OH
COOHCHCH2COOH OH
N O H 酰胺式 常见的互变异构体: C C=N OH
亚胺醇式 7.5% (烯醇式) 80% (烯醇式)
CH 3COCH 2COOC 2H5
CH 3COCH 2COCH 3
CH3COCH(COOC2H5)2 69% (烯醇式)
H2 C H2C H2C C O O
γ-羟基丁酸
γ-丁内酯
3.醇酸的氧化反应 醇酸中的羟基同醇一样可被氧化。α-醇酸中
的羟基受羧基的影响,比醇中的羟基易被氧化,
与吐伦试剂作用即可被氧化成α-羰基酸:
OH CH3CHCOOH [O]
O CH3CCOOH
4. α-醇酸的分解反应
浓 H SO 2 4 RCHCOOH RCHO + H2O + CO OH
CH3COCH2COOH
室温
三、重要的羰基酸 1.乙醛酸
2.丙酮酸 3.乙酰乙酸
四、互变异构现象 β-酮酸酯如乙酰乙酸乙酯
O CH3CCH2COOC2H5
具有酮和羧酸酯的性质,如与HCN、 NaHSO3
等试剂加成;能与苯肼生成苯腙等。此外与金属 钠作用放出氢气;能与FeCl3溶液发生颜色反应, 能与溴加成而使溴水褪色。
CH 3COCH 2COOH β -丁酮酸
丙酮酸
(3- 丁酮酸或乙酰乙酸)
羟基酸和酮酸PPT课件

丙酮酸 乙酰乙酸
CH3 C COOH 是人体内糖、脂肪、蛋白质代谢的中间产物。 易脱羧生成乙醛,还原生成乳酸。
O
O
2021
9
问题7:人体内酮体积蓄过多会产生什么 后果?如何解决?
酮体含量过多会使血液酸性增强,造成酸 中毒。
酸中毒可以用乳酸钠或碳酸氢钠来纠正。
2021
10
常见的酸
结构简式
用途
乳酸
CH3 CH COOH
(α—羟基丙酸剂。乳酸钠纠 正酸中毒。乳酸钙治疗因缺钙引起的佝偻病。 乳酸是人体内糖代谢的产物。
苹果酸 (羟丁二酸)
柠檬酸 (3—羟基—
3—羧基戊 二酸)
水杨酸 (邻羟基苯甲
酸)
HO CH COOH CH2 COOH
CH2 COOH HO C COOH
CH2 COOH
COOH OH
有酸味。 糖代谢的中间产物。
人体内糖代谢的中间产物。 柠檬酸钠盐有防止血液凝固的作用,用作抗凝剂。 柠檬酸铁铵是常用的补血剂,用于治疗缺铁性贫血。
人体内脂肪代谢的中间产物。酸性比醋酸强,
性20质21不稳定,易发生脱羧反应生成丙酮;也11
CH3 C CH2 COOH 可还原生成β—羟丁酸。
羟基酸和酮酸
2021
1
复习引入
问题1:羟基酸和酮酸的结构特点
2021
2
问题2:分析下列哪些是羟基酸?哪些是酮酸?
2021
3
问题3:观察下述羟基酸中,哪些能发生氧化反 应?若能,则他们的氧化产物是什么?
有机化学 第10章 羟基酸和羰基酸

NADH+ H+
NAD+ + H2O
HOOCCH2CH2COCOOH
a-酮戊二酸
谷氨酸脱氢酶
+
NH3 OOCCH2CH2CHCOO
谷氨酸
式中NAD为烟酰胺腺嘌呤二核苷酸(辅酶 I),在反应中起递氢作用。
在生物体内a-酮酸和a-氨基酸在转氨酶的作用下可发
生相互转化,即a-氨基酸的a-氨基借助转氨酶的催化
RCHC OH + H O O H HO C CHR
O + 2H2O O
R
O
O
b-醇酸加热时分子内脱水生成α,β-
不饱和酸
RCH CHCOOH OH H
RCH CHCOOH
g-醇酸和d-醇酸加热时分子内脱水形成内酯
CH2CHO H
O
CH2 C OH
O
O
g-醇酸易发生分子内脱水,室温下失水成形成稳
作用转移到酮酸的酮基上,结果原来的氨基酸生成相
应的酮酸,而原来的酮酸则形成相应的氨基酸,这种
反应称为转氨基作用(transamination)。
+
NH3
GPT
HOOCCH2CH2COCOOH + H3C CH COO
a-酮戊二酸
丙氨酸
+
NH3
O
OOCCH2CH2CHCOO + H3C C COOH
谷氨酸
裂,生成两分子羧酸盐
O R C CH2COOH
+2 NaOH (浓) )
RCOONa + CH3COONa
10.6 醇酸和酮酸的体内化学过程
体内的醇酸和酮酸均为糖、脂肪和蛋白 质代谢的中间产物,这些中间产物在体 内各种酶的催化下,发生一系列化学反 应(如氧化、脱羧及脱水等),在反应过 程中,伴随着氧气的吸收、二氧化碳的 放出以及能量的产生,为生命活动提供 了物质基础。
第10章 羟基酸和羰基酸

第10章 羟基酸和酮酸10.1 基本要求● 掌握羟基酸和酮酸的结构和命名● 掌握醇酸的化学性质(酸性、氧化反应、α、β、γ-醇酸的脱水反应,酚酸的脱羧反应) ● 掌握酮酸的化学性质(还原作用、β-酮酸的酮式分解和酸式分解、α-酮酸的氧化反应、α-酮酸在稀H 2SO 4和浓H 2SO 4下的分解反应,α-酮酸的氨基化反应)● 掌握乙酰乙酸乙酯的酮型—烯醇型互变异构现象 ● 掌握酮体的概念● 了解醇酸和酮酸的体内化学过程;了解α-酮酸氨基化反应的生物学意义 ● 熟悉医药学上重要的羟基酸和酮酸的性能与生物活性10.2 基本知识点10.2.1 羟基酸的结构和命名羧酸分子中烃基上氢原子被羟基取代后的化合物称为羟基酸(羟基酸分为醇酸和酚酸) 醇酸的命名:羧酸为母体,羟基为取代基,并用阿拉伯数字或希腊字母α、β、γ 等标明羟基的位置。
一些来自自然界的羟基酸多采用俗名。
酚酸的命名:以芳香酸为母体,标明羟基在芳环上的位置。
例如:α-羟基丙酸(2-羟基丙酸)羟基丁二酸2-hydroxypropanic acid hydroxybutanedioic acid乳酸(lactic acid) 苹果酸 (malic acid)邻羟基苯甲酸 间羟基苯甲酸 对羟基苯甲酸o -hydroxybenzoic acid m -hydroxybenzoic acid p -hydroxybenzoic acid10.2.2 羟基酸的物理性质常见的醇酸多为晶体或粘稠的液体,在水中的溶解度和熔点较相应碳原子数的醇和酸大,多数醇酸具有旋光性。
酚酸都为晶体,多以盐、酯或糖苷的形式存在于植物中。
10.2.3 羟基酸的化学性质羟基酸具有醇、酚和酸的通性。
由于羟基和羧基的相互影响又具有特殊性,而且这些特殊性质因两官能团的相对位置不同又表现出明显的差异。
1. 酸性 醇酸中羟基表现出-I 效应,因此醇酸的酸性强于相同碳原子数的羧酸,羟基离羧C H 3CH OHCOOHHOOC CH 2CH OHCOOHCOOH OHCOOHOHCOOHOH基越近,酸性越强;反之越弱。
羟基酸和酮酸

OCCH3
CH3CCH2CCH3
+
COOH
CH3COOH
水杨酸具有止痛、退热、抗风湿、杀菌等功效,其 酯——乙酰水杨酸,药名Asprine。
阿司匹林有“世纪神药”之美誉
CH3-C-CH2COOC2H5 CH3-C=CHCOOC2H5 酮式 (92.5%) 酮式 (92.5%) 烯醇式 (7.5%) 酮式 (92.5%) 烯醇式 (7.5%) 酮式(92.5%) 烯醇式 (7.5%) 烯醇式 (7.5%) 酮式 (92.5%) 烯醇式 (7.5%) 酮式(92.5%) 烯醇式 (7.5%) 能与钠作用放出氢气; 能与钠作用放出氢气; 能与羟胺、苯肼反应,生成肟、苯腙等; 能与钠作用放出氢气; 能与羟胺、苯肼反应,生成肟、苯腙等; 能与钠作用放出氢气; 能与羟胺、苯肼反应,生成肟、苯腙等; 羟胺、苯肼反应,生成肟、苯腙等; 能与钠作用放出氢气; 能与钠作用放出氢气; 能与羟胺、苯肼反应,生成肟、苯腙等; 能与羟胺、苯肼反应,生成肟、苯腙等;
O
O OO O
CH3-C-CH COOC H CH -C-CH COOC H CH -C-CH COOC H -C-CH COOC H CH -C-CH COOC H 2 2 5 2 3 2 2 5 3 2 2 55 3 2 5
O
OH OH OH OH OH
OH
CH CH -C=CHCOOC CH -C=CHCOOC CH H5 3 2 5 3-C=CHCOOC 2H5 3-C=CHCOOC 3CH 2H5 2H5 3-C=CHCOOC 2H
解释:酚酸的酸性受诱导效应、共轭 效应和邻位效应的影响。
Organic Chemistry
University of South China
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C、HOOCCH2COOCH3
D、苯酚
5、下列化合物中烯醇式程度最小的是( D )
A、C6H5COCH2COCH3 C、CH3COCH2COOCH3
B、CH3COCH2COCH3 D、CH3COCH2CH3
有机化学
药学院化学教研室
10.5.2 α-酮酸的氨基化反应(不作要求) 10.5.3 α-酮酸的氧化反应(不作要求)
有机化学
10.5.4 酮酸的分解药反学应院化学教研室
1、-酮酸的分解反应
❖ -酮酸分子中的碳—碳键容易断裂,因而与稀硫酸 或浓硫酸共热时可发生分解反应。
脱羧反应
脱羰反应 (不作要求)
有机化学
❖酚酸:
>
>
>
有机化学
❖ 解释:
药学院化学教研室
分子内的氢键,使负离 子稳定,酸性↑↑ -OH在间位,以诱导效应为主 (共轭受到阻碍),由于距离大, 吸电子诱导较弱,酸性↑
-OH在对位,共轭效应> 诱导效应,
-OH斥电子(总效应),酸性有↓ 机化学
10.3.2 醇酸的氧化反应药(了学解院化)学教研室
O OH H O CH3
α-羟基丙酸
H3C O O + H2O
O O CH3
丙交酯
2.β-醇酸(分子内脱水生成α,β-不饱和酸(烯酸)
共轭体系(稳定)
有机化学
3.γ-醇酸(分子内的酯化生成环状内药酯学)院化学教研室
O CH2 C OH CH2CH2O H
γ-醇酸
O O
γ-丁内酯
因此游离的γ-醇酸很难存在,通常以盐的形式保存。
❖ α-醇酸分子中的羟基受羧基吸电子效应的影响, 比醇更易被氧化
❖ 醇酸在体内的氧化通常在酶的催化下进行
H
CH3 C COOH
[O]
CH3 C COOH
OH
[H]
O
乳酸
丙酮酸 有机化学
10.3.3 醇酸的脱水药反学应院化学教研室
1.α-醇酸(分子间脱水生成交酯)
H3C O H HO O
CH
C
C
CH
COOH OH
200~220℃
OH + CO2
COOH
200℃
+ CO2
HO
OH
HO
OH
OH
OH
10.3.5 α-醇酸的分解反应(不作要求)
有机化学
10.4 羰基酸的结构和药学命院名化学教研室
❖羰基酸(又称氧代酸),包括醛酸和酮酸两类,最简 单的醛酸是乙醛酸,最简单的酮酸是丙酮酸。
丙醛酸
2 -丁酮酸 α-丁酮酸
OH
O
H3C药学C 院CH化学C教O研C室2H5
为什么乙酰乙酸乙酯的烯醇式稳定?
1、它的烯醇式有-共轭体系的存在,稳定。
2.它的烯醇式能借分子内氢键形成六元环结构,更增
加了它的稳定性。
OH O
H3C C CH C O C2H5
3、乙酰乙酸乙酯中亚甲基的氢原子,由于同时受到酮 基和酯基两个吸电子基影响,-氢原子更加活泼,易 脱落,也有利于烯醇式的形成。
有机化学
4.δ -醇酸(分子内的酯化生成环状药内学酯院)化学教研室
△
δ -醇酸
δ –戊内酯
❖δ-醇酸较难生成内酯,生成的δ-内酯也容易开环。 ❖某些中草药的有效成分常常含有内酯结构
❖羟基和羧基相隔五个C以上,受热生成链状聚酯。
有机化学
10.3.4 酚酸的脱羧反应药(了学解院化)学教研室
❖ 酚酸的羧基处于羟基的邻位或对位时,受热后 易脱羧 。
2、 -酮酸的分解反药应学院化学教研室
❖ 受羰基和羧基-I效应的影响,易发生分解反应。
O
微热
R C CH2COOH
O R C CH3 + CO2↑
❖ -酮酸的受热脱羧反应生成酮,称为酮式分解反应。
❖ -酮酸比-酮酸更易脱羧,由于两个吸电子基团连 在同一个碳上,而羰基的吸电子效应大于羧基,使 电子转移有利于引起脱羧。
羟基丁二酸 苹果酸
2,3-二羟基丁二酸 酒石酸
有机化学
药学院化学教研室 3-羧基-3-羟基戊二酸 柠檬酸(p242命名较少见)
❖酚酸:羟基酸分子中羟基直接连在芳环上
邻羟基苯甲酸 水杨酸
3,4,5-三羟基苯甲酸 没食子酸
有机化学
10.2 羟基酸的物理性质(了药解学院)化学教研室
1、醇酸:水溶性通常都大于相应的脂肪酸或醇。 2、酚酸:多为晶体,有的微溶于水,有的易溶于水
❖ ②③性质表明乙酰乙酸乙酯还应具有不饱和键和烯醇的
性质。O
O
OH
O
H3C C CH2 C O C2H5
(酮式)
H3C C CH C O C2H5
(烯醇式) (7.5%)
能够互相转变的两种异构体之间存在的动态平衡现象 称为互变异构现象。相互转变的异构体称为互变异构体。
有机化学
O
O
H3C C CH2 C O C2H5
酸式分解
酮式分解
(两分子羧酸盐) (酮+CO2)
有机化学
药学院化学教研室
10.6 醇酸和酮酸的体内化学过程 (不作要求)
10.7 前列腺素(不作要求)
有机化学
10.8 酮式-烯醇式互药变学异院构化学教研室
O
O
乙酰乙酸乙酯是β-丁酮酸
H3C C CH2 C O C2H5 (乙酰乙酸)的乙醇酯。
①与羰基试剂反应,②使溴水褪色③使FeCl3溶液显色
3 -丁酮酸(β-丁酮酸) 乙酰乙酸
α-丁酮二酸 草酰乙酸
有机化学
10.5 酮酸的化学性药质学院化学教研室
❖ 既有-C=O 性质,也有-COOH 性质,如酸性;也有 相互影响产生的特殊化学性质,如分解反应
10.5.1 酸性
❖ 羰基氧吸电子能力强于羟基,因此酮酸的酸性强于 相应的醇酸
>
>
>
>
有机化学
10.3 羟基酸的化学性质
❖既有-OH的性质,又有-COOH的性质 ❖酚酸可以使FeCl3显色
①酸性
③脱水 ④脱羧反应 ②羟基的氧化
有机化学
10.3.1 酸性 药学院化学教研室
❖醇酸: ①羟基的吸电子诱导效应,使酸性: 卤代酸 > 羟基酸 > 羧酸 ②羟基离羰基愈远,对酸性的影响愈少。 α-羟基酸 > β-羟基酸 > γ-羟基酸
有机化学
药学院化学教研室 ❖ -酮酸更易脱羧的原因还有:羰基还能与羧基
氢形成氢键。(了解)
有机化学
药学院化学教研室
❖β-酮酸与浓碱共热时, α-碳原子和β-碳原子之间 发生断裂,生成两分子的羧酸盐,
❖该反应称酸式分解反应
O
浓NaOH
R C CH2 COOH △
O R C ONa + CH3COONa + H2O
药学院化学教研室
H OO
OH O
H3C Br
稳定
OC2H5 H有机化学
练习:选择题
药学院化学教研室
1、下列化合物中既能发生酮式分解,又能发生酸式分解的是
( B)
A、α-丁酮酸
B、β-丁酮酸
C、β-羟基丁酸 D、α-酮戊二酸
2、加热脱水生成α,β-不饱和酸的是( D )
A、δ-羟基戊酸
B、乳酸
C、γ-羟基丁酸 D、β-羟基丁酸
3、①苯甲酸 ②邻羟基苯甲酸 ③对羟基苯甲酸,酸性从大到小
顺序是(B )
A、① > ② > ③
B、②> ① > ③
C、③ > ② > ①
D、②> ③ > ①
有机化学
药学院化学教研室
4、下列化合物中不能与FeCl3起显色反应 ( C )
A、HOOCCOCH2COOH B、CH3COCH2COOH
有机化学
药学院化学教研室 ❖酮式要转变为烯醇式(稳定)条件:
亚甲基旁的两个吸电子基中至少要有一个羰基。 ❖丙二酸,很难转为烯醇式。原因没有羰基
有机化学
练习:
药学院化学教研室
1、烯醇式的稳定性: ① > ② > ③ > ④
原因:
❖
上连有吸电子基或共轭体系扩大时,
烯醇式较稳定
有机化学
2、与溴的反应(了解)
药学院化学教研室
第10章 羟基酸和羰基酸
有机化学
药学院化学教研室 ❖ 羧酸分子中烃基上的氢原子被其他官能团取代
后的生成物称为取代羧酸。取代羧酸可分为卤 代酸、羟基酸、羰基酸或氨基酸。
有机化学
10.1 羟基酸的结构药和学命院化名学教研室
❖醇酸:羟基酸分子中羟基连在脂肪烃基上
α-羟基丙酸(2-羟基丙酸) 乳酸
