硫酸安普霉素可溶性粉(成品)检验记录
硫酸安普霉素及其制剂的研究进展

硫酸安普霉素及其制剂的研究进展摘要:硫酸安普霉素是新一代氨基糖苷类抗生素,具有抗菌活性高、抗菌谱广、对细菌内酰胺酶稳定性好等特点,在临床上被广泛用于治疗敏感菌引起的感染性疾病。
但由于其存在吸收差、半衰期短等问题,限制了其在临床上的应用。
近年来,随着药物制剂技术的不断发展,硫酸安普霉素的生物利用度得到了较大提高。
本文对硫酸安普霉素及其制剂研究进展进行综述,包括硫酸安普霉素的药代动力学研究及用药剂量的选定、硫酸安普霉素的抗菌活性及其作用机制、硫酸安普霉素的稳定性进行了研究,为进一步提高硫酸安普霉素的生物利用度及更好地发挥其临床价值提供参考。
关键词:硫酸安普霉素;制剂;研究进展引言:安普霉素是美国开发的畜禽专用抗菌药物,又名“阿泊拉霉素”,是一种由暗黑链霉菌族菌产生的氨基环醇类抗菌药物,主要通过影响原核生物的核蛋白合成来抑制细菌增殖,对革兰氏阴性菌(如大肠埃希菌、沙门氏菌)有很强的抗菌活性,而且不容易发生耐药,市场前景广阔,目前国内已有多个厂家开发成功。
一、硫酸安普霉素的药代动力学研究及用药剂量的选定药代动力学研究表明,硫酸安普霉素主要经胆汁、尿液、粪便和胎盘吸收,口服给药后,药物很快分布到血浆和组织中,在血液中浓度迅速增加。
因此,硫酸安普霉素的给药方法和剂量的选定应根据其药代动力学特性和临床特点而定。
硫酸安普霉素主要经肝脏代谢,肝脏是其主要的代谢器官,药物主要经肝脏代谢为半合成状态。
有研究表明,硫酸安普霉素在口服后约有90%可由肾脏清除。
因此,从药物排泄和消除的角度看,口服硫酸安普霉素的最大生物利用度为仅为10%。
在相同给药剂量下,口服给药硫酸安普霉素的生物利用度仅为静脉注射的60%左右。
因此,硫酸安普霉素静脉给药应为其最常用的给药方式。
临床实践表明,在静脉注射硫酸安普霉素时,由于药物快速清除使疗效迅速提高并保持较长时间。
临床上使用硫酸安普霉素静脉注射治疗慢性淋巴细胞白血病时,一次给药后可维持数周至数月以上的疗效。
硫酸安普霉素及其制剂的研究进展

1、安普霉素概况安普霉素(Apramycin)亦称阿泊拉霉素,由黑暗链霉菌族菌产生的一种氨基环醇类抗生素,通过干扰原核生物核蛋白质的合成而抑制细菌的繁殖。
安普霉素在活体内外,可有力阻止蛋白质合成的易位阶段,该化合物以硫酸盐在兽医上应用。
具有广谱抗菌活性的畜禽专用安普霉素是美国于60年代研制出的一类抗生素,对畜禽感染的革兰氏阴性菌有较强抗菌活性,特别是对其他抗生素耐药的大肠杆菌和沙门氏菌等有强抗菌作用,且不易产生耐药性,有广泛的市场前景和需求,国内先后有多家进行了研制。
我国学者近年来对国产安普霉素进行了试验研究。
报道显示了对仔猪黄白痢的治疗效果良好,可以预混剂或粉针形式应用。
以中国科学院武汉植物研究所王有为研究员为首的科研人员针对国家畜牧养殖业的需求,着重解决畜禽的肠道感染和耐药性问题,在安普霉素单组分高产菌种筛选认证、免疫屏障促生长机制、安全应用技术等方面作出了创新性贡献,通过诱变筛选出了稳定高产的单组分安普霉素生产菌种,研究出成熟的生产工艺,对安普霉素的药理学、毒理学、动物临床、对猪与鸡生产性能的影响及饲用安全性等进行了全面、系统的研究,取得了创新性成果,并获得了二类新兽药证书[1]。
据《中国农村科技》2001年8期报道,中国农业科学院兰州畜牧与兽药研究所与沈阳药科大学合作开发研制的硫酸安普霉素,对畜禽多种致病菌均有很强的抑杀作用。
主要用于治疗由大肠杆菌、沙门氏菌、巴氏杆菌、链球菌引起的多种畜禽传染病,尤对猪、鸡白痢病有良好的治疗效果,据数千例病例的疗效统计,对仔猪白痢的治愈率在94%以上。
徐忠赞等以一定浓度添加于饲料中。
应用表明,以0.01%浓度饲料添加硫酸安普霉素预混剂,治疗仔猪白痢用量少,治愈率高,此外还可促进增重,提高饲料转化率;另据其介绍,以含量40%的硫酸安普霉素治疗时,配成20mg/ml的水溶液,患猪每天口服3ml,每日l次,连用7天,在第5天时患猪停止腹泻,精神好转,食欲恢复,治愈率为93.3%。
硫酸安普霉素可溶性粉生产工艺规程

硫酸安普霉素可溶性粉生产工艺规程目录1 产品概述2 处方和依据3 工艺流程图4 制剂工艺过程及工艺条件5 原辅材料的预处理6 原辅材料质量标准和检查方法7 中间产品质量标准和检查方法8 成品质量标准和检查方法9 包装规格、包装材料质量标准10 说明书、产品文字说明和标志11 工艺要求12 设备一览表和主要设备生产能力13 技术安全与劳动保护14 劳动组织15 原辅料消耗定额16 包装材料消耗定额17 动力消耗定额18 综合利用与环境保护目的:制定本标准的目的是规范硫酸安普霉素可溶性粉生产过程,对一定数量的成品所需的起始原辅料和包装材料,以及工艺、加工说明、技术参数、注意事项等进一步标准化。
适用范围:适用于硫酸安普霉素可溶性粉生产全过程。
责任人:质量部部长、生产部部长、车间主任。
内容:1 产品概述:本品为硫酸安普霉素可溶性粉。
1.1 产品特点:1.1.1性状:本品为黄褐色粉末。
1.1.2 规格:50g:安普霉素5g1.1.3 贮藏:遮光,密闭,在干燥处保存。
1.1.4有效期:二年1.1.5批准文号:2.处方和依据2.1处方:50g硫酸安普霉素: 5g(以安普霉素计)无水葡萄糖:加至50g2.2处方依据:3生产工艺流程图及环境区域划分示意图4 制剂工艺过程及工艺条件4.1总述:按生产指令领取硫酸安普霉素原料药和预处理过的无水葡萄糖,将硫酸普霉素与无水葡萄糖用等量递增法混合均匀,定量分装即可。
4.2分述:4.2.1投料量:为处方量的整数倍。
5 原辅材料的预处理5.1 按生产指令单领取无水葡萄糖粉的预处理按粉碎机操作规程操作,粉碎,使完全通过80目筛。
过筛结束后,检查合格将粉碎好的药粉装入洁净容器,称量、记录,挂上标签,注明品名、批号、数量、日期等,填写中间产品交接单,转入下工序。
进行物料平衡计算,收率97.0%~99.9%。
5.2 称量配料:按生产指令单称取硫酸安普霉素和无水葡萄糖5.3混合:将上述称量好的药粉置V型混合机中,按等量递增法充分混合,每次预混10分钟,总混30分钟,检验含量均匀度合格后,装入洁净不锈钢桶密封并标明名称、规格、批量(或数量)等,填写中间产品交接单,转入中间站。
硫酸安普霉素可溶性粉 杆菌特效

硫酸安普霉素预混剂
【兽药名称】通用名:硫酸安普霉素预混剂
英文名:Apramycin sultate premix
汉语拼音:Liusuan anpumeisu yuhunji
【主要成份】硫酸安普霉素
【性状】本品为白色或类白色粉末。
【药理作用】本品抗菌谱广,对革兰氏阴性菌特别是对其他抗生素耐药的大肠杆菌和沙门氏杆菌等致病菌有相当强的抗菌作用,对革兰氏阳性菌(某些链球
菌)、密螺旋体和某些支原体也有较好的抗菌作用。
内服给药吸收差,
肌注后吸收迅速。
【适应症】抗菌药:主要用于畜禽细菌(如大肠杆菌、沙门氏杆菌、巴氏杆菌)及支原体感染,临床上适用于禽顽固性大肠杆菌引起的心包炎、肝周炎、气囊炎、卵黄
性腹膜炎、肠炎以及沙门氏菌引起的白痢、伤寒等症;也可治疗犊牛和仔猪
肠杆菌和沙门氏菌引起的腹泻
【用法用量】混饲:每1000kg饲料添加本品300-500g,每日两次,连用3-5天。
混饮:每1kg水加入本品0.33g(本品100g兑水300kg),每日2次,集中用药,连用3-5天,预防量减半。
【注意事项】与青霉素类或头孢类联合有协同作用,不宜与氨基甙类合用(增强毒性)【不良反应】按标准使用无不良反应
【停药期】鸡7日,猪21日。
【规格】100g:安普霉素3g(300万单位)
【包装】100g /袋
【贮藏】密闭、干燥处保存。
【执行标准】《中国兽药典》2005年版。
硫氰酸红霉素可溶性粉(成品)检验记录

检验结论:
粒度
取本品,通过筛孔为0.45毫米(40目)的颗粒不得少于99%。
检验结论:
含量测定:硫氰酸红霉素可溶性粉室温:℃湿度:%
效价测定:硫氰酸红霉素可溶性粉
主要分析仪器
名称
型号
精度
编号
分析天平
0.0001
电热恒温培养箱
高压蒸汽灭菌锅
试验菌:短小芽孢杆菌
培养基:胨5g
牛肉浸出粉3g
成品检验报告单
文件编号:00第4页共4页
检品名称
硫氰酸红霉素可溶性粉
检验单号
商品名
请验部门
生产日期
生产批号
生产总量
取样数量
批号
取样人
送检日期
年月日
报告日期
年月日
检验依据
<<硫氰酸红霉素可溶性粉内控质量标准(成品)>>
检验项目标准规定检验结果项目结论
(1)性状本品应为白色
或类白色粉末规定
(2)鉴别(1)(2)(3)应呈正反应规定
有限公司
成品检验记录首页
文件编号:00第1页共4页
检品名称
硫氰酸红霉素可溶性粉
检验单号
商品名
请验部门
生产日期
生产批号
生产总量
取样数量
批号
取样人
送检日期
年月日
报告日期
年月日
检验依据
<<硫氰酸红霉素可溶性粉内控质量标准(成品)>>
性状
本品为类白色或类白色粉末。
检验结果:
鉴别
(1)取本品约0.1g,加硫酸10ml,缓缓摇匀,即显红棕色。
项目结论
硫酸新霉素可溶性粉成品检验记录

1、性状类白色至淡黄色粉末规定
2、鉴别(1)应为正反应规定
(2)应符合规定规定
3、酸碱度应为4.0-7.5规定
4、干燥失重不得过6.0%规定
5、含量测定应为标示量的
92.0%-108.0%规定
检验结论:
本品按<<硫酸新霉素可溶性粉内控质量标准(成品)>>检验,结果规定。
检验结果:
(2)取本品,加水制成每1ml中含新霉素13mg的溶液照薄层色谱法试验。供试品溶液所显主斑点的颜色和位置应与标准品溶液的主斑点相同。
检验结果:
酸碱度
取本品,加水制成每1ml中含新霉素10ml的溶液,依法测定,PH值应为4.0-7.5。
检查结果:
干燥失重
取本品,以五氧化二磷为干燥剂,在60℃减压干燥至恒重减失重量不得过6.0%。
有限公司
成品检验记录首页
文件编号:00第1页共3页
检品名称
硫酸新霉素可溶性粉
检验单号
批号
规格
请验车间
取样人
取样地点
取样数量
送检日期
年月日
报告日期
年月日
检验依据
<<硫酸新霉素可溶性粉内控质量标准(成品)>>
性状
本品为类白色至淡黄色粉末。
检验结果:
鉴别
(1)取本品,加水制成每1ml中含新霉素13mg的溶液,加盐酸溶液2ml,在水浴中加热10分钟,加8%氢氧化钠溶液2ml与2%乙酰丙酮水溶液1ml,置水浴中加热5分钟,放冷后,加对二甲氨基苯甲醛试液1ml,即显樱桃红色。
检验结论:
本品按<<硫酸新霉素可溶性粉内控质量标准(成品)>>检验,结果规定。
硫酸新霉素可溶性粉(成品)检验操作规程

GMP管理文件
一、目的:为规定硫酸新霉素可溶性粉生产过程中的质量控制和
检验操作要求,特制定此操作规程。
二、适用范围:适用于硫酸新霉素可溶性粉成品的检验。
三、责任者:生产部经理、检验员、生产人员
四、正文:
质量标准:见硫酸新霉素可溶性粉(成品)内控质量标准
操作内容:
性状本品为白色或类白色粉末。
检查酸度取本品,加水制成每1ml中含10mg的溶液,依法测定,pH 值应为4.0~7.5。
干燥失重取本品,在60℃减压干燥至恒重,减失重量不得过6.0%。
含量测定精密称取本品适量,照硫酸新霉素项下的方法测定。
即得。
10%阿莫西林可溶性粉内控质量标准+硫酸安普霉素可溶性粉中间产品内控标准检验操作规程

阿莫西林可溶性粉中间产品质量标准本品为阿莫西林与无水葡萄糖配制而成。
含阿莫西林(C16H19N3O5S)应为标示量的93.0%~107.0%。
【性状】本品为白色或类白色粉末。
【检查】溶解性取本品50mg,加水100ml,搅拌,应溶解。
水分取本品,照水分测定法(第三法A)测定,含水分不得过5.0%。
外观均匀度取供试品适量,置光滑纸面上,平铺约5cm2,将其表面压平,在亮的背景下观察,应呈均匀的色泽、无花纹与色斑。
【含量测定】照高效液相色谱法测定.色谱条件与系统适用性试验用十八烷基硅胶为填充剂;以0.05mol/L磷酸二氢钾溶液(用2mol/L氢氧化钾溶液调节pH值至5.0±0.1-乙腈(96:4)为流动相;检测波长为254nm.理论板数按阿莫西林峰计算不低于1700。
测定法取本品适量,精密称定,加磷酸盐缓冲液(pH5.0)溶解并稀释成每1ml 中约含0.6mg的溶液,滤过,精密量取续滤液20ul,注入液相色谱仪,记录色谱图;另取阿莫西林对照品适量,同法测定。
按外标法以峰面积计算出供试品中阿莫西林的含量。
【规格】100g:10g. (按C16H19N3O5S·3H2O计算)【贮藏】遮光,密封保存。
硫酸安普霉素可溶性粉中间产品内控标准检验操作规程【标准依据】《中国兽药典》2010版一部本品为硫酸安普霉素与枸橼酸钠配置而成。
含安普霉素(C21H14N5O11)应为标示量的93.0%~107.0%。
【性状】本品为微黄色至黄褐色粉末。
【检查】酸碱度仪器与试剂天平、PH计、烧杯、移液管、标准缓冲溶液取本品0.5g,加水10ml溶解后,依法测定,pH值应为5.0~8.0。
干燥失重仪器与用具天平、快速水分测定仪、毛刷。
取本品,用快速水分测定仪测定,减失重量不得过8.0%。
溶解性仪器及试剂天平、烧杯、玻璃棒、水取本品1.0g,加水50ml,搅拌,应全部溶解。
【效价测定】仪器及试剂双碟、陶瓦盖、钢管、恒温培养箱、移液管、刻度吸管、容量瓶、称量瓶、毛细滴管、电子分析天平、镊子、游标卡尺、灭菌水精密称取本品适量,加灭菌水定量制成每1ml中约含10000单位的溶液,照抗生素检定法测定。
二剂量法测硫酸安普霉素可溶性粉含量的不确定度评定

生长发 育 , 提高饲料 利用率 , 短饲养 周期 。硫 酸安 缩 普霉素可溶 性粉作 为一种较 新 的兽药 产 品 ,为确保
广东饲 料 第 1 9卷第 9期
21 0 0年 9月
二 量 测 酸 普 素 溶 粉 量 不 定 评 剂 法 硫 安 霉 可- 含 的 确 度 定 陛
伍 绍 登 庄 淑 丽
( 广东省兽药 与饲料监察总所 , 广东广州 5 0 3 ) 2 0 1
【 中图 ̄ ]8 97 S 5 .9 [ 文献标识码] A 【 文章编号】0 5 8 l (o 0 O — 0 5 0 1O — 6 3 2 l )9 0 3 — 4
31 . 标所 有 的各抑 菌 圈 直径 引起 的 相对 . 11低 . 标准 不确 定度 uf1 e )l S r
・
3 ・ 5
广东饲料 第 1 卷第 9 9 期 21 年 9 00 月
1 2 3 4 5 6 u 亍 ) =u T )T : .×1一 7 8 9 ( / 4 n 6 0 (
111 0 . %硫酸 安普 霉素 可溶性 粉 .1
1 仪 器设 备 . 2
s: 1 为低 标 所 有 的各 抑 菌 圈直 径 总 和 s : 高标 所 有 的 各 抑 菌 圈直 径 总 和 2为
1 . 器 。Z 一 0I 抑 菌 圈 自动 测 量 分 析 . 1仪 2 Y 30V 仪 、rsa9S 2 2 电 子 天 平 、 MMTT培 养 Pee 2 M一 0A ME I
1 . 析试 剂与 溶液 3分
硫酸安普霉素质量标准+硫酸安普霉素检验操作规程
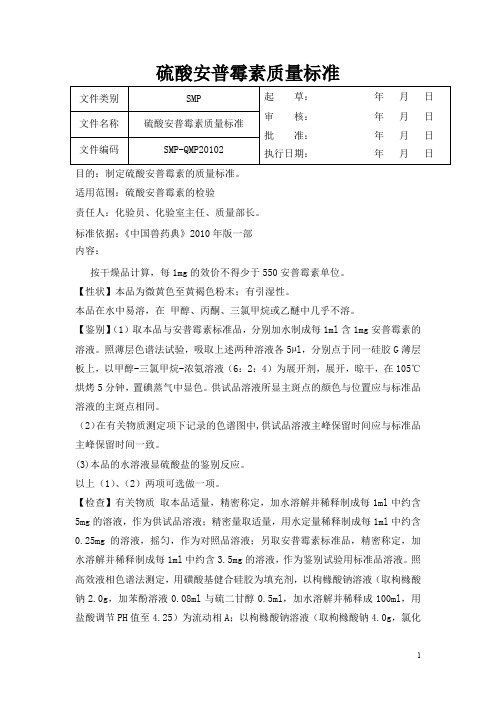
硫酸安普霉素质量标准 文件类别SMP 起 草: 年 月 日 审 核: 年 月 日 批 准: 年 月 日 执行日期: 年 月 日 文件名称硫酸安普霉素质量标准 文件编码 SMP-QMP20102 目的:制定硫酸安普霉素的质量标准。
适用范围:硫酸安普霉素的检验责任人:化验员、化验室主任、质量部长。
标准依据:《中国兽药典》2010年版一部内容:按干燥品计算,每1mg 的效价不得少于550安普霉素单位。
【性状】本品为微黄色至黄褐色粉末;有引湿性。
本品在水中易溶,在 甲醇、丙酮、三氯甲烷或乙醚中几乎不溶。
【鉴别】(1)取本品与安普霉素标准品,分别加水制成每1ml 含1mg 安普霉素的溶液。
照薄层色谱法试验,吸取上述两种溶液各5µl,分别点于同一硅胶G 薄层板上,以甲醇-三氯甲烷-浓氨溶液(6:2:4)为展开剂,展开,晾干,在105℃烘烤5分钟,置碘蒸气中显色。
供试品溶液所显主斑点的颜色与位置应与标准品溶液的主斑点相同。
(2)在有关物质测定项下记录的色谱图中,供试品溶液主峰保留时间应与标准品主峰保留时间一致。
(3)本品的水溶液显硫酸盐的鉴别反应。
以上(1)、(2)两项可选做一项。
【检查】有关物质 取本品适量,精密称定,加水溶解并稀释制成每1ml 中约含5mg 的溶液,作为供试品溶液;精密量取适量,用水定量稀释制成每1ml 中约含0.25mg 的溶液,摇匀,作为对照品溶液;另取安普霉素标准品,精密称定,加水溶解并稀释制成每1ml 中约含3.5mg 的溶液,作为鉴别试验用标准品溶液。
照高效液相色谱法测定,用磺酸基健合硅胶为填充剂,以枸橼酸钠溶液(取枸橼酸钠2.0g ,加苯酚溶液0.08ml 与硫二甘醇0.5ml ,加水溶解并稀释成100ml ,用盐酸调节PH 值至4.25)为流动相A ;以枸橼酸钠溶液(取枸橼酸钠4.0g ,氯化钠4.0g 与苯酚溶液0.08ml ,加水溶解并稀释成100ml ,用盐酸调节PH 值至7.4)为流动相B ;柱后衍生反应温度为120℃;以茚三酮溶液为衍生化试剂;按下表进行线性梯度洗脱;检测波长为568nm 。
硫酸安普霉素可溶性粉质检报告
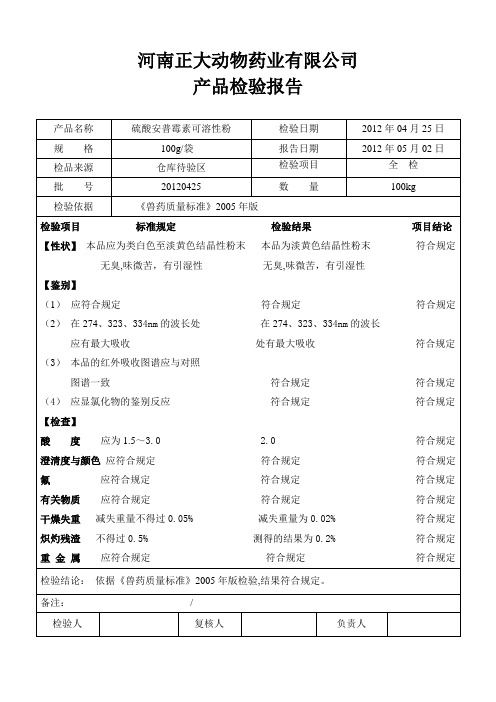
产品检验报告产品名称硫酸安普霉素可溶性粉检验日期2012年04月25日规格100g/袋报告日期2012年05月02日检品来源仓库待验区检验项目全检批号20120425 数量100kg检验依据《兽药质量标准》2005年版检验项目标准规定检验结果项目结论【性状】本品应为类白色至淡黄色结晶性粉末本品为淡黄色结晶性粉末符合规定无臭,味微苦,有引湿性无臭,味微苦,有引湿性【鉴别】(1)应符合规定符合规定符合规定(2)在274、323、334nm的波长处在274、323、334nm的波长应有最大吸收处有最大吸收符合规定(3)本品的红外吸收图谱应与对照图谱一致符合规定符合规定(4)应显氯化物的鉴别反应符合规定符合规定【检查】酸度应为1.5~3.0 2.0 符合规定澄清度与颜色应符合规定符合规定符合规定氟应符合规定符合规定符合规定有关物质应符合规定符合规定符合规定干燥失重减失重量不得过0.05% 减失重量为0.02% 符合规定炽灼残渣不得过0.5% 测得的结果为0.2% 符合规定重金属应符合规定符合规定符合规定检验结论:依据《兽药质量标准》2005年版检验,结果符合规定。
备注:/检验人复核人负责人产品检验报告产品名称氟苯尼考可溶性粉检验日期2012年04月25日规格 100g/袋报告日期 2012年05月02日检品来源仓库待验区检验项目全检生产批号20120425 数量100kg检验依据《兽药质量标准》2005年版检验项目标准规定检验结果项目结论【性状】本品应为白色或类白色粉末本品为白色粉末符合规定【鉴别】(1)在266nm的波长处在266nm的波长处吸收最大符合规定应有最大吸收(2)沉淀的红外吸收图谱应与对照品的图谱一致。
符合规定符合规定【检查】粒度本品应全部通过二号筛符合规定符合规定干燥失重取本品,在105℃干燥至恒重,减失重量不得过9.7%。
减失重量为0.3% 符合规定其他应符合预混剂项下有关的各项规定符合规定符合规定装量平均装量不少于100g,每袋装量应为99g~102g。
10%硫酸安普霉素可溶性粉工艺验证方案+生产工艺规程
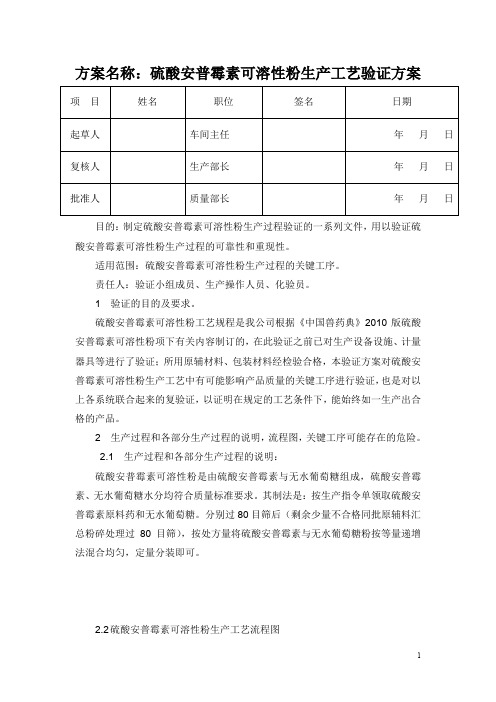
方案名称:硫酸安普霉素可溶性粉生产工艺验证方案目的:制定硫酸安普霉素可溶性粉生产过程验证的一系列文件,用以验证硫酸安普霉素可溶性粉生产过程的可靠性和重现性。
适用范围:硫酸安普霉素可溶性粉生产过程的关键工序。
责任人:验证小组成员、生产操作人员、化验员。
1 验证的目的及要求。
硫酸安普霉素可溶性粉工艺规程是我公司根据《中国兽药典》2010版硫酸安普霉素可溶性粉项下有关内容制订的,在此验证之前已对生产设备设施、计量器具等进行了验证;所用原辅材料、包装材料经检验合格,本验证方案对硫酸安普霉素可溶性粉生产工艺中有可能影响产品质量的关键工序进行验证,也是对以上各系统联合起来的复验证,以证明在规定的工艺条件下,能始终如一生产出合格的产品。
2 生产过程和各部分生产过程的说明,流程图,关键工序可能存在的危险。
2.1 生产过程和各部分生产过程的说明:硫酸安普霉素可溶性粉是由硫酸安普霉素与无水葡萄糖组成,硫酸安普霉素、无水葡萄糖水分均符合质量标准要求。
其制法是:按生产指令单领取硫酸安普霉素原料药和无水葡萄糖。
分别过80目筛后(剩余少量不合格同批原辅料汇总粉碎处理过80目筛),按处方量将硫酸安普霉素与无水葡萄糖粉按等量递增法混合均匀,定量分装即可。
2.2硫酸安普霉素可溶性粉生产工艺流程图2.3 关键工序可能存在的危险。
2.3.1过筛:因无水葡萄糖易结块、原料粒度大不符合要求影响产品质量,因此通过过80目筛验证原辅料需不需要过筛。
2.3.2 混合:混合为硫酸安普霉素可溶性粉生产中的一道重要工序,混匀与否直接影响着成品的质量,为防止有效成分含量有偏差,因此应对混合搅拌工序进行验证。
2.3.3 分装:此工序为硫酸安普霉素可溶性粉的成型工序,因为装量差异在生产时不可能一直测定,只能每隔20分钟测定一次,装量可能在两次测定之间发生较大偏差。
因此应对分装工序进行验证。
2.3.4 包装:包装为硫酸安普霉素可溶性粉最后一道生产工序,包装的好坏直接影响产品的质量,因此应对包装的过程全面验证,用以证明现行的工艺条件能始终如一生产出合格的产品。
测量硫酸安普霉素不确定度的评定

中。
U () ( 0 + ( ) + ( ) + ( ) + 2J = V ) I 耐 d ( ) 酽( ) ( ) 耐 () 3
公 式计 算其 不确 定 管引起 的相对 标 准不确 ... O l
2 测 量 数 学 模 型
随着 社 会 进 步与 科 学 技术 的发 展 , 界 对 实 验 业 室提供 的数据 有效 性 、 学 性 、 科 公正性 和可靠 性 提 出 了更 高 的要求 。IO I C 7 2 S / 1 0 5标 准 明确 规定 检测 实 E 验室 应具 有并应 用 评定 测量 不确 定 度 的程序 。在 国
u s1: ( ) = . x 03 1 7 1- 8
定 度为 U( of V )l e :
u v ) 、 U ( 1十 ( ) ( 0= / 2 ) 低 标所 有 的各 吸光 值 引 起 的相 对 标 准 不 确 定
度( A类不 确定 度 ) :
u s) 【 S1 Sl1 7 1-05 8 3 9 1。 (1 , I . x 03 . = . x 0 ( ) = 8 / 6 2
!
S l 05 3 .7 05 4 .6 05 8 .6
! 兰竺
05 7 .6 05 .68
5一 T 的加 样顺 序加 样 ,加 好 后 每管 再分 别 加入 带 2 2
菌 培 养 基 90 Ⅱ ,盖 上 塞 子 ,放 人 预 热 至 3 ℃ 的 . l 0l 7
T: 。低样 所有 的各吸 光值 总 和 ;
采 用《 国药 典)0 5年 版第 二部 附 录第 8 页 中 ) 0 2 1
抗 生素 浊 度 法 , 对硫 酸 安 普 霉 素可 溶 性 粉 进 行 含量
测定 , 并对 其 测量 不 确 定 度进 行 分 析 。精 密称 取 硫
【精品】硫酸安普霉素可溶性粉工艺规程

硫酸安普霉素可溶性粉工艺规程制订人审核人批准人制订日期批准日期执行日期烟台金海药业有限公司目录2、处方和依据3、粉剂生产工艺流程及环境区域划分示意图4、工艺过程及条件4.1生产前准备:a.专人检查确认该品种的批生产指令及相应的配套文件,如批记录等是否准备齐全,并是现行文件b.设备器具和现场是否有“清场合格证”c。
对设备状况进行检查,挂有“合格”、“已清洁”、“已消毒”标志的设备方可使用。
4。
2粉碎工序4.2.1工艺过程4。
2。
1。
1认真核对硫酸安普霉素和枸橼酸钠品名、批号等是否与生产指令相符,并有检验合格报告单,确认无误后经清洁或脱去外包装提入暂存室。
将内容物连同内包装一起取出放在干净的容器内,并正确填写盛装单放在该容器内(可扎在袋口上).4.2.1.2对硫酸安普霉素和枸橼酸钠进行检查,用五号筛试筛,应全部通过五号筛,如不符合要求,则按生产工艺要求,粉碎至规定细度,并用振荡筛进行过筛。
如符合要求,则可不粉碎。
4。
2。
1.3粉碎后的物料装入洁净容器中,贴上标志,注明名称、规格、批号、数量、日期、操作者等。
4.2.1。
4.每批物料粉碎结束后,须对粉碎机进行清洗,以防止改变品种时相互污染. 4。
2。
2工艺条件及质量控制点4.2.2。
1粉碎岗位应有除尘设施,并控制尾气排放中粉尘不得超标。
4。
2.2.2当水分过高时,要先干燥后再粉碎4.2.2.3.粉碎后药粉应全部通过五号筛.4.3干燥4.3。
1因硫酸安普霉素和枸橼酸钠水分含量低,无需烘干.4.4称量、配料工序4.4。
1工艺过程4。
4。
1.1直接使用的硫酸安普霉素和枸橼酸钠须清洁或除去外包装.4。
4.1.2.称量人认真校对物料名称、批号、数量等,确认无误后按规定的方法和生产指令定额称量,记录并签名。
需要进行计算后称量的物料,计算结果先经复核无误后再称量。
4.4。
1.3称量必须复核,复核人校对称量后的物料的名称、重量,确认无误后记录、签名.4.4.1.4称好的硫酸安普霉素和枸橼酸钠分别装于洁净容器中,备用。
二剂量法测硫酸安普霉素可溶性粉含量的不确定度评定

二剂量法测硫酸安普霉素可溶性粉含量的不确定度评定
伍绍登;庄淑丽
【期刊名称】《广东饲料》
【年(卷),期】2010(019)009
【摘要】@@ 硫酸安普霉素为氨基糖苷类抗生素,主要作用于细菌的核糖体30s 亚基,抑制蛋白质的正常合成,使细菌细胞膜通透性增强,导致细胞内的重要物质外漏而引起细菌死亡,对多数革兰氏阴性菌如大肠杆菌、沙门氏菌及部分阳性菌如金黄色葡萄球菌和支原体等都有很强的抗菌作用,与其他氨糖苷类药物无交叉抗药性.【总页数】4页(P35-38)
【作者】伍绍登;庄淑丽
【作者单位】广东省兽药与饲料监察总所,广东广州,510230;广东省兽药与饲料监察总所,广东广州,510230
【正文语种】中文
【中图分类】S859.79
【相关文献】
1.微生物浊度法测硫酸安普霉素及其制剂含量的研究 [J], 陈智慧;李小燕
2.微生物浊度法测定硫酸安普霉素可溶性粉含量的研究方法 [J], 玛尔江;沙吾烈;古丽曼;木尼热
3.强普生拓和硫酸安普霉素可溶性粉对仔猪白痢的治疗试验 [J], 朱楼英;何海健
4.硫酸安普霉素可溶性粉中非法添加乙酰甲喹的HPLC-PDA检测方法的建立 [J],
戴青;于丽娜;张璐;韩宁宁;徐嫄;赵晖
5.好益特硫酸安普霉素可溶性粉 [J],
因版权原因,仅展示原文概要,查看原文内容请购买。
硫酸安普霉素可溶性粉(成品)检验操作规程

GMP管理文件
一、目的:为规定硫酸安普霉素可溶性粉生产过程中的质量控制
和检验操作要求,特制定此操作规程。
二、适用范围:适用于硫酸安普霉素可溶性粉成品的检验。
三、责任者:生产部经理、检验员、生产人员
四、正文:
质量标准:见硫酸安普霉素可溶性粉(成品)内控质量标准
操作内容:
性状本品为微黄色至黄褐色粉末。
鉴别照硫酸安普霉素项下的鉴别(1)项试验,显相同的结果。
检查酸度取本品0.5g,加水10ml溶解后,依法测定, pH值应为5.2~7.9。
干燥失重取本品,在105℃干燥4小时,减失重量不得过7.0%。
硫酸安普霉素可溶性粉中非法添加乙酰甲喹的HPLC-PDA检测方法的建立

硫酸安普霉素可溶性粉中非法添加乙酰甲喹的HPLC-PDA检测方法的建立戴青;于丽娜;张璐;韩宁宁;徐嫄;赵晖【期刊名称】《中国兽药杂志》【年(卷),期】2017(051)002【摘要】为检测硫酸安普霉素可溶性粉中非法添加的乙酰甲喹,以十八烷基硅烷键合硅胶为填充剂,磷酸盐缓冲液(取磷酸二氢钠3.0 g,加水1000 mL使溶解,加三乙胺0.5 mL,用饱和氢氧化钠溶液调节pH值至7.0)-甲醇为流动相,二极管阵列检测器(PDA),建立了HPLC-PDA检测方法,并采用峰纯度检查和光谱相似度检查辅助对照品比对方法,对非法添加药物进行确证.在此液相色谱条件下,乙酰甲喹与其他物质峰分离良好.按外标法以峰面积计算,乙酰甲喹的平均回收率为98.1%,RSD为0.3%.该检测方法简便、准确、可靠,可用于测定硫酸安普霉素可溶性粉中非法添加的乙酰甲喹.%A method for the determination of mequindox in the apramycin sulfate soluble powder was developed by the high performance liquid chromatography with photo-diode array detector (HPLC-PDA).It was tested with C18 column,using phosphate buffer solution (taking the sodium dihydrogen phosphate 3.0 g,add 1000 mL water to dissolve,and add 0.5 mL triethylamine,adjusting pH to 7.0 by sodium hydroxide saturated solution) and methanol as the mobile phase.Peak purity test and spectrum similar test were helped to identify the mequindox.The mean recovery of mequindox was 98.1%,and RSD was 0.3%,respectively.Inconclusion,the method is simple,accurate and reliable for the determination of mequindox in apramycin sulfate soluble powder.【总页数】5页(P19-23)【作者】戴青;于丽娜;张璐;韩宁宁;徐嫄;赵晖【作者单位】中国兽医药品监察所,北京 100081;中国兽医药品监察所,北京100081;中国兽医药品监察所,北京 100081;中国兽医药品监察所,北京 100081;中国兽医药品监察所,北京 100081;中国兽医药品监察所,北京 100081【正文语种】中文【中图分类】S859.83【相关文献】1.乙酰甲喹与硫酸安普霉素治疗仔猪黄痢病的效果观察 [J], 刘文杰2.乙酰甲喹与硫酸安普霉素治疗仔猪黄痢病的疗效观察 [J], 雷万均3.HPLC-PDA法同时测定硫酸新霉素可溶性粉中非法添加4种化学药物 [J], 熊玥;宋慧敏;汪云花;孙瑶;石慧慧4.阿莫西林可溶性粉中非法添加氟苯尼考的HPLC-PDA检测方法的建立 [J], 王轩;韩宁宁;杨秀玉;戴青;汪霞;赵晖5.氟苯尼考粉中非法添加乙酰甲喹的检测方法研究 [J], 文英会;邱天宝;刘占通;吴慧豪因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4、粒度应符合规定规定
5、酸碱度应为5.0-8.0规定
(4)含量测定:
含安普霉素应为标
示量的92.0%~108.0%。。规定
检验结论:
本品按<硫酸安普霉素可溶性粉内控质量标准(成品)>>检验,结果
规定。
备注:
负责人:复核人:检验人:
检验结论:
含量测定:硫酸安普霉素素可溶性粉室温:℃湿度:%
效价测定:硫酸安普霉素可溶性粉
主要分析仪器
名称
型号
精度
编号
分析天平
0.0001
电热恒温培养箱
高压蒸汽灭菌锅
试验菌:枯草芽孢杆菌
培养基:胨5g
牛肉浸出粉3g
磷酸氢二钾3g
琼脂15-20g
水至1000ml
调节PH值,使灭菌后为7.8~8.0
复核人:检验人:
检验结果:
酸碱度
取本品0.5g,加水10ml溶解后,依法测定,pH值应为5.0-8.0
检验结果:
检查
装量
样品号
1
2
3
药+包装重
包装重
药重
平均
标准规定
每袋装量不得少于标示量,平均装量不得少于标示量。
项目结论
干燥失重
天平室温度℃ 湿
瓶+药重W1
干燥后瓶+药重W2
复核人:检验人:
样品稀释:
测量结果:(1) (2)平均值:
标准规定:
含安普霉素应为标示量的92.0%~108.0%
检验结论:
本品按<<硫酸安普霉素可溶性粉内控质量标准(成品)>>检验,结果
规定。
备注:
复核人:检验人:
有限公司
成品检验报告单
文件编号:00第4页共4页
检品名称
硫酸安普霉素可溶性粉
检验单号
商品名
请验部门
生产日期
有限公司
成品检验记录首页
文件编号:00第1页共4页
检品名称
硫酸安普霉素可溶性粉
检验单号
商品名
请验部门
生产日期
生产批号
生产总量
取样数量
批号
取样人
送检日期
年月日
报告日期
年月日
检验依据
<<硫酸安普霉素可溶性粉内控质量标准(成品)>>
性状
本品为微黄色至黄褐色粉末。
检验结果:
鉴别
取本品与安普霉素标准品,分别加水制成每1ml中含1mg的溶液。照薄层色谱法试验,吸取上述两种溶液各5ul,分别点于同一硅胶G包层板上,以甲醇-三氯甲烷-浓氨溶液(6:2:4)为展开剂,展开,晾干,在105℃烘烤5分钟,置碘蒸汽中显色,供试品溶液所显主斑点的颜色和位置应与标准品溶液的主斑点相同。
检验单号
商品名
请验部门
生产日期
生产批号
生产总量
取样数量
批号
取样人
送检日期
年月日
报告日期
年月日
检验依据
<<硫酸安普霉素可溶性粉内控质量标准(成品)>>
检验项目标准规定检验结果项目结论
(1)性状应为微黄色至
黄褐色粉末规定
(2)鉴别应呈正反应规定
(3)检查
1、外观均匀度应色泽均匀规定
2、干燥失重不得过7.0%规定
4、粒度应符合规定规定
5、酸碱度应为5.0-8.0规定
(4)含量测定:
含安普霉素应为标
示量的92.0%~108.0%。。规定
检验结论:
本品按<硫酸安普霉素可溶性粉内控质量标准(成品)>>检验,结果
规定。
备注:
负责人:复核人:检验人:
有限公司
成品检验报告单
文件编号:00第4页共4页
检品名称
硫酸安普霉素可溶性粉
生产批号
生产总量
取样数量
批号
取样人
送检日期
年月日
报告日期
年月日
检验依据
<<硫酸安普霉素可溶性粉内控质量标准(成品)>>
检验项目标准规定检验结果项目结论
(1)性状应为微黄色至
黄褐色粉末规定
(2)鉴别应呈正反应规定
(3)检查
1、外观均匀度应色泽均匀规定
2、干燥失重不得过7.0%规定
3、装量应符合规定规定
有限公司
成品检验记录附页
文件编号:00第2页共4页
干燥
失重
计算公式
W1- W2
干燥失重=
W1- W0
干燥失重(%)
平均值(%)
标准规定
减失重量不得过7.0%
项目结论
外观均匀度
取本品适量,平铺于光滑纸上,成5cm2,将表面压平,在亮的背景下观察,呈
均匀色泽,无花纹与色斑。
检验结论:
粒度
本品应全部通过二号筛。
有限公司
成品检验记录附页
文件编号:00第3页共4页
样品制备:
精密称取本品适量,加灭菌水定量制成每1ml中约含1000单位的溶液,照抗生素微生物检定法测定。
对照品制备:
精密称取安普霉素对照品适量,加灭菌水制成每毫升中约含1000单位的溶液。
培养条件:
标准品效价:标准品取量(g):
标准品稀释:
样品估计效价:样品取量(g):(1) (2)
