几种抗肿瘤筛选模型简介
抗肿瘤药物筛选方法及体内药效学评价体系

抗肿瘤药物筛选方法及体内药效学评价体系引言:肿瘤是一种严重威胁人类健康的疾病,对其进行系统研究和筛选出有效的抗肿瘤药物至关重要。
本文将介绍抗肿瘤药物筛选方法和体内药效学评价体系,以期加强抗肿瘤药物的研发和应用。
一、抗肿瘤药物筛选方法1.高通量筛选平台(HTS):利用微孔板和机器人技术,大规模、高效地筛选化合物或草药中的抗肿瘤活性物质。
通过测定细胞增殖、细胞周期、转移能力和凋亡等参数,筛选出具有抗肿瘤活性的化合物。
2.化学方法与计算机辅助筛选:利用化学合成技术,设计和合成一系列的化合物,通过计算机模拟和数据库筛选,选出具有潜在抗肿瘤活性的化合物。
3.多维数据整合筛选方法:采用多个筛选指标,综合多种方法对候选化合物进行研究和评价。
如细胞毒性数据、抗肿瘤活性数据、药代动力学参数等,加强对候选化合物的筛选和评价。
1.细胞系体内实验:将候选化合物通过体外培养的肿瘤细胞系,进行细胞毒性和细胞凋亡等实验,评估化合物的抗肿瘤活性。
2.小鼠移植瘤体内实验:将人体肿瘤移植到小鼠体内,观察化合物对肿瘤生长和转移的影响,评价化合物的抗肿瘤活性。
3.药物代谢动力学研究:通过给小鼠或大鼠静脉或口服投给候选化合物,进行药物代谢动力学研究,包括体内分布、代谢和排泄等过程,从而了解化合物在体内的代谢和消除。
4.药物安全性评价:通过给小鼠、大鼠或犬等动物进行长期或短期的给药实验,观察化合物对动物的毒性反应和安全性,评价化合物的毒性作用。
5.疗效评价体系:根据体内实验结果,评估化合物对肿瘤的疗效,包括肿瘤体积、肿瘤抑制率、生存期延长等指标。
结论:抗肿瘤药物的筛选和评价是抗肿瘤药物研发过程中的重要环节。
高通量筛选平台、化学方法与计算机辅助筛选和多维数据整合筛选方法是目前常用的药物筛选方法。
体内药效学评价体系则包括细胞系体内实验、小鼠移植瘤体内实验、药物代谢动力学研究、药物安全性评价和疗效评价。
通过这些方法和体系,可以筛选出活性强、毒副作用小、疗效好的抗肿瘤药物,为临床治疗提供有力支持。
一种新的快速简便的抗肿瘤药物筛选模型

一种新的快速简便的抗肿瘤药物筛选模型
许文思;彭剑;王吉成;陈秀华;钱蓓丽
【期刊名称】《中国抗生素杂志》
【年(卷),期】2001(026)001
【摘要】本研究利用DNA修复缺陷的大肠埃希氏菌343/591和正常的大肠埃希氏菌343/636的差异性DNA修复特性,建立了液体悬浮法和琼脂固体筛选方法,用于抗肿瘤药物的筛选。
这两种方法简便易行,其中琼脂固体筛选方法与抗生素生物鉴定杯碟法一样简单,适合于大量筛选各种来源的抗肿瘤药物。
【总页数】4页(P15-18)
【作者】许文思;彭剑;王吉成;陈秀华;钱蓓丽
【作者单位】上海医药工业研究院;上海医药工业研究院;上海医药工业研究院;上海医药工业研究院;上海医药工业研究院
【正文语种】中文
【中图分类】R965.1
【相关文献】
1.一种基于荧光图像的体外抗肿瘤药物快速筛选方法 [J], 聂晓静;赵筱萍;王毅
2.海洋放线菌杀虫抗生素的一种快速筛选模型 [J], 胡志钰;刘三震;黄浩;黄耀坚;苏
文金
3.产生物表面活性剂菌种的一种快速筛选模型 [J], 宁长发;沈薇;孟广荣;杨树林
4.一种简便快速测量折射率的新方法研究 [J], 李春江; 李陆余; 杨靖垒; 李廷荣; 向
文丽
5.国际电传邮政——与国外联系的新渠道——快速、简便、廉价 [J], 陶辅文因版权原因,仅展示原文概要,查看原文内容请购买。
抗肿瘤药物体内筛选试验标准操作规程(SOP)

抗肿瘤药物体内筛选标准操作规程概述:抗肿瘤药物是指能够直接杀伤或抑制肿瘤细胞生长或增殖的一类药物,作用机制包括抑制肿瘤细胞核酸或蛋白质的合成、干扰大分子物质代谢、干扰微管系统、抑制拓扑异构酶等.本操作规程包括与抗肿瘤药物申请临床试验和申请上市有关的非临床有效性和安全性研究的内容,其中着力强调非临床有效性和安全性之间的关联性,以及非临床研究和临床试验之间的关联性。
旨在一方面为抗肿瘤药物的非临床研究提供技术参考;另一方面,通过技术要求引导科学有序的研发过程,使国内此类药物的研发更趋规范和合理。
本操作规程仅代表目前对抗肿瘤药物非临床研究的一般性认识.具体药物的非临床研究应在本指导原则的基础上,根据药物的自身特点制订研究方案。
研究目的:建立一套包括抗肿瘤药物体内作用的药效学研究和评价体系及相应的标准操作规程以及抗肿瘤药物安全性和作用新机制的研究.①有效性研究抗肿瘤药物有效性研究的目的主要在于探索受试物的作用机制、作用强度、抗瘤谱等,为之后的安全性评价以及临床试验中适应症、给药方案的选择提参考信息。
②安全性评价安全性评价的目的主要包括:(1)估算 I 期临床试验的起始剂量;(2)预测药物的毒性靶器官或靶组织;(3)预测药物毒性的性质、程度和可逆性;(4)为临床试验方案的制订提供参考.研究计划:(a)小鼠急性毒性测试按照急性毒性测试的常规方法,选用昆明种小鼠,通过腹腔注射方式给药,测定体外抗肿瘤活性突出的化合物的半数致死量(LD50),参考给药小鼠体重变化情况,评价化合物的急性毒性,并确定小鼠体内抗肿瘤活性测试的给药剂量。
(b)小鼠体内抗肿瘤活性测试根据动物体内抗肿瘤活性测试的标准方法,选用昆明种小鼠,皮下接种肉瘤S180或肺癌H22瘤株,选择体外活性突出且急性毒性较低的化合物,设定合适的剂量通过腹腔注射方式给药,以临床常用抗肿瘤药物环磷酰胺作为阳性对照药物,测定肿瘤生长抑制作为体内活性评价指标。
(c)专利保护范围内的化合物的继续合成申请保护范围较大的专利,合成部分可能具有良好活性的新的化合物,拓展研究范围,发现活性更强的化合物,并申请新的发明专利。
常见肿瘤动物模型一览

接种措施(无菌操作)
1.实体瘤
冻存旳瘤株
移入宿主体内
瘤源动物
7~10d
增殖
取得瘤块
制备瘤块
给动物接种
受体动物
实体瘤接种法:瘤块接种法、瘤细胞悬液接种法、培养细胞接种法、活细胞接 种措施等
瘤块接பைடு நூலகம்法
选用接种后7~10d生长状态良好旳瘤源动物,颈椎脱臼处死,消毒操 作部位皮肤。切开皮肤,剥离出接种用旳瘤块,剔除非肿瘤组织和坏死 组织,选用生长良好而无变性坏死、淡红色(黑色素瘤则呈黑色或黑紫 色)、鱼肉装旳瘤组织,在无菌平皿内剪成2mm3小块。平皿放置在冰块 上,平皿内放置少许灭菌旳PBS或其他营养液。
发癌率可达40% ,DEN总量达1176mg,观 察时间为六个月时,发癌率可达94% ,其中 支气管鳞状细胞癌占41%。
• ②乌拉坦注后3个月肺腺癌发生率为100%, 且多数为多发性,诱发肺肿瘤旳部位和组织分 型与人类肺肿瘤相近似。
• 2.食管癌(Carcinoma of esophagus)
• [简述]:亚硝胺在体内经过代谢,产生重碳烷, 使核酸或其他分子发生烷化而致癌.不对称亚 硝胺口服或胃肠外给药,均能诱发大鼠食管癌。
二、诱发性肿瘤动物模型
定义:使用致癌原因(Carcinogens)在试验条件下诱发动物发生肿瘤旳
动物模型。
原理:利用外源性致癌原因引起细胞遗传特征异常而呈现出异常生长和
高增殖活性,形成肿瘤。
诱发性肿瘤模型动物选择
用于诱发试验性肿瘤旳动物种类诸多,以啮齿动 物旳使用最多、应用最广,涉及多种大鼠、小鼠、 豚鼠等
瘤细胞悬液接种法
每次接种旳动物数量较多时可采用此法。详细措施是:无菌操作取 出瘤块,将数个瘤块混合后剪成小块,放入玻璃匀浆器中,加无菌生理 盐水向一种方向转动研磨后,经滤网过滤,加生理盐水稀释成1:3~1:4 (肿瘤g:生理盐水ml)旳瘤细胞悬液,用台盼兰染色法计数活细胞数, 用1ml注射器注射到接种部位,每个接种点接种0.2ml(一般含 1×106~1×107个细胞数)。一般接种到腋窝皮下,每只动物可选用多种 接种点。
抗肿瘤药物筛选及临床实验

抗肿瘤药物筛选及临床实验责任编辑:luanchaojibing,作者:佚名文章来源:本站原创点击数:更新时间:2005-10-24 14:54:02(—)抗肿瘤药物的筛选1.体内筛选方法体内筛选方法是药物应用于有移植性肿瘤的动物进行实验的方法。
肿瘤模型是进行药物筛选的先决条件。
一个理想的用于药物筛选的肿瘤模型应具备的条件是:①对临床疗效有预告性;②快速、经济;③指标明确、客观;④重现性好,结果可信赖。
常用于鼠类,近年来在体内试验方面,裸鼠被广泛应用于抗肿瘤药物的筛选,目前已成功地将官颈癌、卵巢癌、乳腺癌、结肠癌、肺癌等10余种人体肿瘤移植于裸鼠,国内已成功地建立了卵巢癌裸鼠皮下移植瘤和腹水瘤模型,并已用于科研和临床。
在体内试验方面需注意:①给药途径。
因腹腔给药假阳性较多见,因此要筛选一种药物是否对一种移植肿瘤确实有效,需应用两种以上不同的给药途径,并且三次实验结果均显示标准抗癌活性时才能判定有效。
②在每一种给药途径中,还需观察不同剂量的抗肿瘤活性,以揭示有效抗肿瘤药物的量效关系。
2.体外筛选方法因体内筛选需要的技术条件高,故大批筛选或粗选时多采用体外筛选。
(1)人肿瘤集落形成法:该方法是将单细胞悬液,接种到含软琼脂的培养基中,培养一定时间后一部分肿瘤细胞能够在琼脂中生长,形成集落。
通过药物处理组和对照组的细胞集落生成数量比较,可作为肿瘤化疗的药物敏感试验。
每次可用多个平面筛选8一10种药物,以找出对肿瘤细胞最敏感的药物。
此法快速、经济、选择性高,而且结果可靠,故在临床用药选择和抗肿瘤药物开发上将得到广泛应用。
该方法缺点是活肿瘤组织单细胞悬液的制备比较困难,并且集落形成的成功率不够高,故在方法学上需待完善。
ALberts等以此法指导69例复发转移卵巢癌的治疗,结果临床有效率为54%;经验治疗组的有效率为20%;而以。
HCTA中抗药的药物治疗的有效率为8%。
(2)三磷酸腺苷生物发光法(ATP法):其基本原理是ATP为细胞内能量的基本来源,其浓度与活细胞量有关。
几种抗肿瘤筛选模型简介

镰刀菌模型筛选步骤
将镰刀菌接种在土豆培养基上,28℃培养1~2周 后,加入无菌水刮下孢子,摇匀过滤;以土豆液体 培养基稀释成1×104/mL孢子的孢子液, 然后 将50μL待筛样品,分别加到96孔板,第1行各孔 中(从第3列开始,第1、2列作空白对照),每1列从 第1行开始依次稀释到最后一孔(即第8行),然后 在28℃培养16h,在倒置显微镜下观察孢子及菌 丝体生长形态变化情况,根据上述活性指标,判 断活性,计算最小活性浓度。
MTT法
MTT法是一种检测细胞生存和增殖状态 的方法,该方法以其简单、快速、准确等优点被 用于细胞毒和淋巴因子生长抑制的定量检测,尤 其在肿瘤化疗药敏实验中广泛使用。其原理是 MTT可被活细胞线粒体中的脱氢酶还原为蓝 色的甲基化合物,再经适当溶剂溶解后,其吸光 度与活细胞数相关,从而可作为检测活细胞数的 指标。因此MTT法可用于细胞毒活性物质的 筛选。
DDRT法(different DNA repair test)
试验菌株 343/591为赖氨酸和生物素营养缺陷型并具 有发酵乳糖能力和DNA修复缺陷的菌种;343/636为不 能发酵乳糖的脯氨酸营养缺陷型菌株并具有紫外线损 伤和DNA修复能力。 DDRT法是一种利用两个菌株对DNA损伤修复的差异 性建立的方法,可以用来检测试验物的DNA毒性。 343/591为DNA修复缺陷菌株,而343/636菌株具有紫外 线损伤和DNA修复能力,因而通过两个菌株的修复能力 不同可以检测出受试物的DNA毒性。因而DDRT法可 用于筛选得到作用于DNA的抗肿瘤活性菌株。
DDRT法的步骤
343/636和343/591菌株分别接种于含5ml蛋白胨-肉汤培 养基中; 在37℃振荡培养16h; 用分光光度计测 450nm处的343/591和343/636的OD值,用蛋白胨-肉汤 培养基稀释343/636菌液使其OD值与343/591相同; 在100ml中性红琼脂培养基中加入1ml菌液后倒入平皿 中静置1h; 将所要测定的放线菌发酵液和受试物滴 加在覆盖于琼脂培养基上直径为8mm的滤纸片上; 37℃培养24h,以丝裂霉素为标准药物对照,根据发酵液 产生的抑菌圈大小的差异来判定其对DNA造成损伤 的大小及是否有抗肿瘤活性.
免疫疗法相关肿瘤模型介绍

免疫疗法相关肿瘤模型介绍导读前两期我们介绍了常见的肿瘤动物模型,考虑到肿瘤免疫疗法不同于普通抗癌药物的作用方式和评价体系,有必要在此单独介绍一下肿瘤免疫疗法研究领域常用的肿瘤动物模型。
为此,笔者专门搜集和整理了一些相关资料,以当前较为成熟的CAR-T/TCR-T以及免疫检查点阻断技术为例,对免疫疗法肿瘤模型的特点、常用实验动物及细胞株、建立方法以及药物评价方式等关键点做个简要介绍,以期为有志于从事肿瘤免疫疗法研究的同行们提供些许参考。
背景在当今众多的癌症治疗手段中,免疫疗法无疑是近年来最为吸引人们眼球的“明星”治疗手段,普遍引起学术界及医学界的强烈关注和研究兴趣。
随着以T细胞受体T细胞技术(TCR-T)、嵌合抗原受体T细胞技术(CAR-T)以及免疫检查点阻断技术(Immune Checkpoint Blockade)为代表的新兴肿瘤免疫疗法不断取得临床上的突破和成功,奇迹频现,捷报频传,持续更新着人们对机体免疫系统潜在的强大肿瘤杀伤能力的认知,进一步提高人们战胜恶性肿瘤的信心,当然也持续激发着科研人员对“肿瘤免疫疗法”这一强大抗癌利器的研究和开发热情。
而对于肿瘤免疫疗法的研究,离不开相关动物模型的选择和建立。
事实上,目前已经取得临床成功的肿瘤免疫疗法中,无一例外都已经过大量严格的临床前动物实验进行验证、评估和预测。
可见,相关动物模型的建立对于肿瘤免疫疗法的开发和应用是至关重要且必不可少的。
免疫疗法相关肿瘤模型一、以CAR-T/TCR-T为代表的细胞过继性疗法(Adoptive Transfer)常用肿瘤动物模型细胞过继性疗法是指将供体(donor)细胞(此处主要是T淋巴细胞)经体外刺激活化或者基因修饰后再次回输入受者(Recipient)体内,从而达到相关治疗目的的治疗方式。
供体细胞可以是来源于受者自身,也可以来自于其他个体,前者称为自体移植(Autograft),后者则有两种情况,如果受者与供者属于相同种属,称为同种异体移植(Allograft),反之则为异种移植(Heterograft)。
2024福建省执业药师继续教育答案-抗肿瘤药物筛选的新模型

抗肿瘤药物筛选的新模型——人源类器官(答案在文末)温馨提示:福建华博施教机构的执业药师继续教育考试题为随机抽取题库内部分题目进行考试,该文档列出了该科目的所有考试题目及答案。
若5次未通过考核,则需重新学习该课视频课程。
1、PDO可以取自肿瘤发展过程中的()阶段,而且只需要一小部分肿瘤组织即可在体外进行培养和扩增。
()A.前期B.中期C.后期D.任何2、肿瘤诱导的免疫抑制作用,与机体抗肿瘤作用的平衡影响肿瘤清除或是进展的结局。
()A.正确B.错误3、(多选题)属于免疫治疗的方法有()。
A.集落刺激因子B.白介素C.干扰素D.单抗4、肿瘤细胞系培养条件复杂,体外能够无限增殖,适宜于大规模的药物筛选。
()A.正确B.错误5、()11月,伦琴发现了神秘之光X线。
A.1865年B.1875年C.1885年D.1895年6、PDX肿瘤模型的优点有()。
A.很大程度保留肿瘤异质性B.移植成功率高C.所需肿瘤样本小D.成本低7、对恶性肿瘤的现代治疗,始于()世纪末外科脱胎换骨之后率先对癌症发起的战斗。
A.17B.18C.19D.208、(多选题)恶性肿瘤常用治疗方法包括()。
A.手术B.药物治疗C.放疗D.按摩保健9、化疗不仅是一种姑息疗法或辅助疗法,还已经发展为一种根治性的方法和手段。
()A.正确B.错误10、公元前()古埃及的木乃伊便已有了肿瘤存在的证据。
()A.1000年B.2000年C.3000年D.4000年11、(多选题)人源类器官的特点有()。
A.与对应的器官拥有类似的组织结构、重现部分生理功能B.稳定的表型和遗传学特征C.兼顾个性化和高通量的需求,可以体传代、复苏和冻存,可操作性强D.是发病机制、药物筛选的强有力工具E.肿瘤个体化精准治疗的优秀体外模型12、类器官只可来源于肿瘤组织,不可来源于正常成体组织。
()A.正确B.错误13、()Cushing首次进行脑瘤手术。
()A.1900年B.1910年C.1920年D.1930年14、以下哪种药物是CYP酶强诱导剂,应尽量避免与肺癌靶向药物联用?()A.伊曲康唑B.伏立康唑C.胺碘酮D.利福平15、以下哪种药物是CYP酶强抑制剂,应尽量避免与肺癌靶向药物联用?()A.伊曲康唑B.卡马西平C.苯巴比妥D.苯妥英16、以下哪种药物是以HER2为靶点的小分子口服抗肿瘤靶向药物?()A.吉非替尼B.吡咯替尼C.厄洛替尼D.埃克替尼E.克唑替尼17、以下哪种药物是以HER2为靶点的大分子抗肿瘤靶向药物?()A.恩美曲妥珠单抗B.吡咯替尼C.厄洛替尼D.埃克替尼18、根据《中华人民共和国医师法》的条文,关于超说明书用药四个前提条件,缺一不可:()A.药品具有循证医学证据B.没有其他更安全有效、经济合理的治疗手段C.患者知情同意D.医院建立了相关的管理机制19、特殊情况下抗肿瘤药物使用采纳的循证医学证据包括:()A.特殊情况下抗肿瘤药物使用采纳的循证医学证据包括:B.其他国家或地区药品说明书中已注明的用法C.国际权威学协会或组织发布的诊疗规范D.国际权威学协会或组织发布的临床诊疗指南参考答案。
肿瘤药物筛选指标

肿瘤药物筛选指标肿瘤药物筛选指标主要包括以下几个方面:客观缓解率(ORR):ORR是肿瘤体积缩小达到预先规定值(通常是30%)并能维持最低时限要求的患者比例,是完全缓解(CR,即肿瘤完全消失不见)和部分缓解(PR,即肿瘤缩小达到30%及以上)比例之和,不包括疾病稳定,ORR属于短期疗效评价指标。
通俗理解,ORR也叫做有效率,是指患者接受某种治疗后肿瘤缩小达到30%及以上的人数比例,ORR越高意味着使用该疗法达到肿瘤缩小的患者越多。
疾病控制率(DCR):DCR是肿瘤经治疗后获得缓解(PR+CR)和疾病稳定(SD,即肿瘤缩小没有达到30%,但也没有达到进展的程度)的患者比例,同样是一个短期疗效评价指标。
通俗理解,DCR是指患者接受某种治疗后肿瘤得到控制,没有继续进展的人数比例,DCR越高意味着使用该疗法肿瘤稳定,疾病不进展的患者越多。
无进展生存期(PFS):指患者从随机分组到疾病进展或任何原因死亡的时间,就是患者通过治疗后病情没有进展或耐药的时间,一般PFS越长,意味着患者有质量的生存时间越长,活得越好。
再通俗的说,PFS非常接近于患者朋友常问的服用某药能维持多久不复发,或是出现耐药时间。
临床价值:PFS是目前很多研究设置的主要观察指标或成为“主要研究终点”。
在III期对照研究中,如果研究药物相比对照药物(一般用目前指南推荐的标准治疗药物)能延长PFS,表明药物能有效的延缓肿瘤的增大及转移,患者可以从该药治疗明显获益。
总生存期(OS):指患者从进入随机分组到研究中至患者因任何原因死亡的时间,就是患者通过治疗后活了多久:OS越长意味着患者活得越久。
除了以上四个指标外,还有其他指标如总缓解率、中位缓解期、中位生存期等也可以作为肿瘤药物筛选的指标。
需要注意的是,这些指标只是对疗效的初步评估,对于具体的治疗方案和药物选择还需要结合患者的具体情况和医生的专业意见进行综合考虑。
抗肿瘤药物的筛选方法

抗肿瘤药物的筛选方法1.细胞毒性筛选:通过使用细胞系或动物模型,评估候选药物对肿瘤细胞的毒性效应。
这些细胞系通常来自于肿瘤组织或细胞株库。
可以使用MTT试剂或其他细胞代谢活性测定方法来评估药物对细胞生存能力的影响。
2. 细胞增殖和凋亡分析:通过评估候选药物对肿瘤细胞增殖的影响,可以确定其抗肿瘤效应。
此外,还可以使用凋亡标记物如Annexin V和Casapese-3评估候选药物对肿瘤细胞的凋亡诱导效应。
3.细胞周期分析:肿瘤细胞与正常细胞相比,在细胞周期的控制上存在差异。
通过评估候选药物对肿瘤细胞周期的影响,可以确定其抗肿瘤机制。
流式细胞仪是一种用于进行细胞周期分析的常见工具。
4. 迁移和侵袭分析:肿瘤侵袭和迁移是肿瘤生长和转移的重要步骤。
通过使用Boyden室和Transwell孔板,可以评估候选药物对肿瘤细胞迁移和侵袭的抑制效果。
5.血管生成抑制分析:肿瘤生长和转移需要新的血管生成。
通过评估候选药物对血管生成的抑制效果,可以确定其抗肿瘤机制。
常见的评估方法包括管状结构形成、血管内皮细胞迁移和血管内皮细胞增殖等。
6.体内动物模型:通过使用小鼠或其他动物模型,评估候选药物对体内肿瘤生长和转移的影响。
这些模型可以是异种移植肿瘤模型、转基因肿瘤模型或者荷瘤小鼠模型等。
7.药代动力学和安全性评估:候选药物需要进行药代动力学和毒理学评估,以确定其在体内的药物代谢、分布和排泄情况,以及其对正常细胞和组织的安全性。
8.临床试验:在药物筛选的最后阶段,候选药物需要进行临床试验,以评估其对人体肿瘤的疗效和安全性。
这些试验通常分为三个阶段:I期试验用于评估药物的安全性和耐受性,II期试验用于评估药物的有效性和适应症,III期试验用于验证药物的疗效和安全性,并与标准治疗进行比较。
总体而言,抗肿瘤药物的筛选方法是一个复杂的过程,需要通过多种实验评估和临床试验来确定候选药物的疗效和安全性。
这些方法可以帮助研究人员在众多候选药物中筛选出最有潜力的抗肿瘤药物,为肿瘤患者的临床治疗提供更有效和安全的选择。
抗肿瘤药物的体外体内模型权威验证评价

抗肿瘤药物的体外体内模型权威验证评价肿瘤是一种严重威胁人类健康的疾病,而抗肿瘤药物的研发是治疗肿瘤的重要手段之一。
为了评估抗肿瘤药物的疗效和安全性,科学家们通常会使用体外体内模型进行验证评价。
这些模型可以模拟肿瘤细胞内的药物作用和体内的药物代谢,为药物研发提供重要的参考依据。
下面将介绍几种常用的体外体内模型,并对其权威性验证评价进行讨论。
一、细胞模型细胞模型是研究抗肿瘤药物作用机制和疗效评估的重要工具。
常见的细胞模型包括肿瘤细胞系、原代肿瘤细胞和3D细胞培养模型。
1. 肿瘤细胞系:肿瘤细胞系是从患者的肿瘤组织中分离和培养出来的细胞系。
它能够长期稳定地生长,在体外模拟肿瘤细胞的特性和药物反应。
通过测定细胞的增殖、凋亡和迁移能力,可以对抗肿瘤药物的治疗效果进行初步评估。
2. 原代肿瘤细胞:原代肿瘤细胞是从患者新鲜手术标本中分离和培养出来的细胞。
与肿瘤细胞系相比,原代肿瘤细胞更接近真实的肿瘤环境,具有更高的生物学真实性。
因此,原代肿瘤细胞模型被广泛应用于抗肿瘤药物的体外评估。
3. 3D细胞培养模型:3D细胞培养模型是一种能够模拟肿瘤组织结构和功能的模型。
它通过在细胞培养基中添加支撑基质,使细胞能够在三维空间中生长和相互作用。
这种模型更接近于真实的肿瘤微环境,能够更准确地评估抗肿瘤药物的疗效和毒副作用。
二、动物模型除了细胞模型外,动物模型也是评估抗肿瘤药物疗效和安全性的重要手段。
常见的动物模型包括小鼠模型、大鼠模型和人源异种移植瘤模型。
1. 小鼠模型:小鼠模型是最常用的抗肿瘤药物研发模型之一。
小鼠体内的肿瘤模型可以通过移植肿瘤细胞、异种移植瘤或基因敲除等方式得到。
通过观察肿瘤的生长抑制、体重变化和生存率等指标,可以评估抗肿瘤药物的疗效和毒副作用。
2. 大鼠模型:大鼠模型与小鼠模型类似,但由于其体型较大,更适合用于评估肿瘤治疗手术的效果。
大鼠模型还可以用于评估肿瘤转移和药物代谢等指标,为抗肿瘤药物的疗效评估提供更全面的信息。
抗肿瘤药物筛选

2021/3/2
4
当前,体外抗肿瘤活性实验选用人癌细胞株,按常 规细胞培养法进行培养,使用四氮唑蓝(MTT)还原 法,磺罗丹明B染色法或集落形成法等测定药物抗 癌作用.
本实验除了用于抗肿瘤药物的初步筛选外,还用于 了解候选化合物的抗瘤谱,为随后进行体内抗肿瘤 实验(如剂量范围.肿瘤类别等)提供参考.
2021/3/2
10
★噬箘体法
包括抗噬箘体法和溶原性菌诱导法两种. 细菌的噬箘体核酸大部分为双链DNA,干扰DNA
代谢的抗生素(如放线菌素.博来霉素)常也抑制噬 箘体在细菌细胞内的生长,从而出现抗噬箘体现象.
T4噬箘 体吸附 在大肠 杆菌细 胞
2021/3/2
11
2021/3/2
12
应用诱导溶源性菌前噬箘体的方法筛选.
2021/3/2
14
★抗代谢法
抗代谢物在含无机氮 源的合成培养基中显示抗癌 作用,而在普通有机氮源的营养培养基中无抗癌作 用.利用这个特点,选择无机氮源实验有抗菌作用 的物质,作为抗代谢的初筛方法.
2021/3/2
15
★精原细胞法
1. 建立精原细胞法的依据
造精过程可分为下列阶段:A型精原细胞、B型精原细 胞、静止期初级精母细胞、初级精母细胞(细线期.偶线 期.粗线期.双线期.终变期) 、次级精母细胞、精子细胞 (园核精子细胞.长核精子细胞) 、精子.在造精细胞系列
中,对放射最为敏感的是B型精原细胞,其次是A型精原细胞,
然后依次为精子细胞、
精母细胞、精子.
2021/3/2
16
精原细胞法阳性和抗肿瘤作用的相关性尤以在抗 生素和植物药中较为明显.
用精原细胞法检测72种抗生素,精原细胞法阳性的 13种抗生素,据已报道资料均属抗肿瘤抗生素,其 中9种在临床上有一定疗效.
抗肿瘤药物评价技术

体外抗肿瘤活性试验
美国NCI抗肿瘤药物体外筛选使用的60种人类细胞
白血病(6株):CCRF-CEM、HL-60、K562、MOLT-4、RPMI-8226、SR 肺癌(9株):A549、EKVX、HOP-62、HOP-92、NCI-H23、NCI-H226、NCI-H322、 MNCI-H460、NCI-H522 乳腺癌:BT-549、HS578T、MCF-7、MCF-7/ADR、MDA-MB-231、ATCC、 MDA-MB-435、MDA-N、T-47D 卵巢癌:IGROV1、OVCAR-3、OVCAR-4、OVCAR-5、OVCAR-8、SK-OV-3 肾癌:786-0、A498、ACHN、CAKI-1、RXF-393、SN12C、TK-10、UO-31 前列腺癌:DU-145、PC-3 中枢神经系统肿瘤:SF-268 、SF-295 、SF-539、 SFB-19 、SFB-75、U251 黑色素瘤:M14、MALME-3M、SK-MEL-2、SK-MEL-5、SK-MEL-28、UACC-62、 UACC-257、LOCIMV
体外抗肿瘤活性试验
注意事项
体外筛选其他方法:MTS法、刃天青法 以线粒体为作用靶点的受试物不宜采用四氮唑盐还原法 溶媒对照组与阴性对照组比较,OD值应在±5%,且无统 计学差异 应考虑到受试物在水溶液中的稳定性,比如环磷酰胺在水溶液 中的半衰期为3h 脂溶性的受试物常用DMSO助溶,但DMSO终浓度不低于0.1% 测出的OD值有事会出现假阴性(加MTT等染色剂时更换培养基)
体外抗肿瘤活性试验
生长曲线测定法
试验原理:在最适条件下,肿瘤细胞在培养液中呈指数生长,如取细胞 数的对数与培养时间作图可得一条直线,故称此时为对数生长期。随着细 胞密度不断增高,由于代谢产物的积聚及营养物的消耗,细胞生长逐渐减 慢以致停止,此时称高坪期或稳定期。因此药物对细胞生长的影响可通过 生长曲线反映出来 。 方法要点: 将浓度为10000个细胞/ml的对数生长期细胞悬液按每瓶5ml 种至25ml的培养瓶,或按每孔100微升种至96孔板,并加受试样品适量, 培养后分别于即刻和1、2、3、4、5、6、7d进行检测。前者可采用台盼 蓝染色计数活细胞,后者可采用MTT法或SRB法读取OD值,并据此进行 作图与计算。 观测指标 1、倍增时间(TD),将实际生在曲线进行直线回归求出0和t时刻 的理论细胞数N0和N t,据此计算:TD=0.301t/(log N t—log N0);2 增殖细胞杀伤率(%)=( N0—N0’)/ N0×100%;3 细胞生长饱和密度 (N s),代表高坪期每毫升细胞数的均数。
恶性肿瘤的疾病模型与药物筛选

恶性肿瘤的疾病模型与药物筛选恶性肿瘤是一种具有高度恶性和侵袭性的疾病,对人类健康构成严重威胁。
为了更好地研究恶性肿瘤的病理过程以及寻找有效的治疗方法,科学家们开发了多种不同的疾病模型并进行药物筛选。
本文将介绍几种常见的恶性肿瘤模型以及药物筛选的方法。
一、大鼠肿瘤模型大鼠肿瘤模型是最早被广泛应用于恶性肿瘤研究的模型之一。
通过移植人类肿瘤细胞株到大鼠体内,可以观察和研究肿瘤生长、转移以及对治疗药物的反应。
这种模型具有较高的可重复性和可操作性,可以提供更接近人类疾病的环境。
二、小鼠转基因模型小鼠转基因模型是通过基因工程技术将特定的致癌基因或抑癌基因转入小鼠体内,使其发生肿瘤变化。
这种模型可以模拟出人类肿瘤的发生机制,并且对于研究肿瘤的早期发展和治疗药物的疗效评估具有重要意义。
三、细胞系模型细胞系模型是将体外细胞培养技术与肿瘤研究相结合的模型。
科学家们将人类肿瘤细胞分离培养,并通过不同的培养条件模拟肿瘤在体内的生长环境。
这种模型具有较强的实验控制性和高效性,可以为药物筛选提供大量的样本。
四、三维组织工程模型三维组织工程模型是近年来发展起来的一种新型肿瘤模型。
将肿瘤细胞与支架材料相结合,形成具有结构和功能特性的肿瘤组织。
这种模型能够模拟真实的肿瘤组织结构和肿瘤微环境,对药物的筛选和治疗效果评估能提供更可靠的数据。
针对恶性肿瘤的药物筛选主要包括体外筛选和体内筛选两个阶段。
体外筛选主要利用细胞系模型或三维组织工程模型进行,通过评估药物对肿瘤细胞的抑制作用或诱导细胞凋亡的能力来初步筛选药物。
而体内筛选则需要将合适的肿瘤模型移植到动物体内,观察和评估药物对肿瘤生长、转移以及患者生存率的影响。
随着科学技术的不断发展,越来越多的新的恶性肿瘤模型和药物筛选方法不断涌现。
例如人工智能在肿瘤筛选方面的应用,有望为研究人员提供更准确、高效的药物筛选策略。
总之,恶性肿瘤的疾病模型与药物筛选是推动肿瘤研究和治疗进步的重要手段。
科学家们根据疾病的特点选择合适的模型,通过系统、全面地筛选药物,为寻找更有效的抗肿瘤药物提供科学依据,以期最终提高恶性肿瘤患者的生存率和生活质量。
肿瘤药物筛选指标

肿瘤药物筛选指标
肿瘤药物筛选指标是用来评估一种药物在治疗肿瘤方面的疗效和安全性的指标。
常用的肿瘤药物筛选指标包括:
1. 抑制肿瘤细胞增殖的能力:通过观察药物对肿瘤细胞增殖的抑制作用,来评估药物的抗肿瘤活性。
2. 细胞凋亡诱导能力:药物是否能够诱导肿瘤细胞发生凋亡,从而抑制肿瘤的生长和扩散。
3. 抗血管生成作用:肿瘤生长需要新的血管生成来供给营养和氧气,药物是否能够抑制肿瘤相关的血管生成过程,从而抑制肿瘤的生长。
4. 细胞周期调控作用:药物是否能够影响肿瘤细胞的周期进程,使其停滞在某个特定的周期,从而阻止肿瘤细胞的增殖。
5. 选择性毒性:药物是否对肿瘤细胞具有较高的选择性毒性,即对肿瘤细胞有较强的杀伤作用,而对正常细胞的毒性较小。
6. 药物代谢和排泄特性:药物在体内的代谢和排泄特性对其疗效和安全性具有重要影响,需要评估药物的代谢速度和代谢产物的活性。
7. 动物模型研究结果:药物在动物模型中的疗效和安全性结果可以为临床前研究提供重要参考。
8. 临床试验结果:药物在临床试验中的疗效和安全性结果是决定药物是否能够作为肿瘤治疗药物的关键指标。
以上仅为常见的肿瘤药物筛选指标,根据具体研究目的和药物特性,还可以选择其他相关指标进行药物筛选。
抗肿瘤药物筛选

继续培养; (5)24或48h以后,加入MTT溶液,再培养3-6h,停止培养,弃
取培养基,加入DMSO,每孔150ul,轻微震荡混匀; (6)把96孔板放入酶标仪中,490nm测定吸光度。
CCK-8法
④大白鼠饲养与药物刺激
用常规方法饲养大白鼠,用适当计量的 药物喂养大白鼠,不同的时间取大白鼠的适当 器官(根据所筛选的药物而定),抽提刺激前 后的mRNA。
⑤刺激前后的mRNA的制备即标记 ⑥芯片杂交及扫描 ⑦数据分析及生物信息学分析
用表达效。
体内:动物眼角膜囊 地鼠颊囊 裸鼠外耳皮下 鸡胚绒毛尿囊膜
鸡胚绒毛尿囊膜模型
鸡胚的生物学构造
尿囊
卵黄囊
对照组
低浓度药物实验组
中浓度药物实验组
高浓度药物实验组
操作步骤:
(1)于实验前72h孵育受精蛋
(2)实验进行前以照蛋箱透照孵育的种蛋,凡已正常发育的 种蛋可照见胚胎的影子,用铅笔做记号,弃取未发育种蛋
以提高疗效。
常用宿主动物: 裸小鼠
(“活的试管”)
特点:先天无毛,无胸腺,T淋巴细胞功能完全缺失, 对异种移植不产生排斥反应。
缺点:费用高,饲养条件高,不宜大量繁殖。一般不 用于初筛。
应用:观察药物对癌细胞逆转作用,抑制增殖及诱导 凋亡作用。
C57BL/6小鼠
特点:黑毛,体型小,性情温顺,易饲养,药 敏性好,为研究Lewis肺癌首选。
2.基本技术路线
①基因的选择与实验设计
根据表达谱数据库选择5000-10000个与发育及疾 病相关的基因,制备药物筛选芯片。
②芯片的制备
抗肿瘤体内筛选模型
8周
瘤
BalB/c 裸鼠 皮下实体瘤或静脉血液
8周
瘤
BalB/c 裸鼠 皮下实体瘤或静脉血液
8周
瘤
ICR 小鼠或 KM 小鼠 皮下实体瘤或
6周
腹水瘤
ICR 小鼠或 KM 小鼠 皮下实体瘤或
6周
腹水瘤
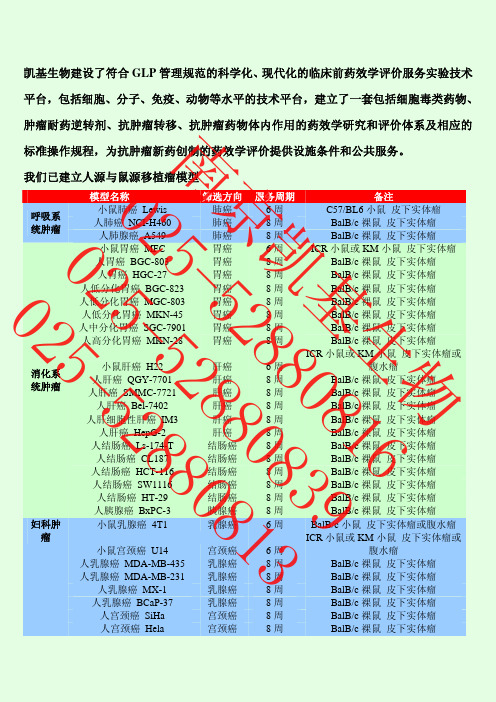
凯基生物建设了符合 GLP 管理规范的科学化、现代化的临床前药效学评价服务实验技术
平台,包括细胞、分子、免疫、动物等水平的技术平台,建立了一套包括细胞毒类药物、
南 肿瘤耐药逆转剂、抗肿瘤转移、抗肿瘤药物体内作用的药效学研究和评价体系及相应的
标准操作规程,为抗肿瘤新药创制的药效学评价提供设施条件和公共服务。
宫颈癌
8周
BalB/c 裸鼠 皮下实体瘤
人卵巢癌 A2780
卵巢癌
8周
BalB/c 裸鼠 皮下实体瘤
人卵巢癌 SK-OV-3
卵巢癌
8周
BalB/c 裸鼠 皮下实体瘤
人肾癌 Ketr-3
肾癌
8周
BalB/c 裸鼠 皮下实体瘤
生殖系
统肿瘤
南 头颈部
肿瘤
0 京 皮肤肿 2 瘤 0 025 5-5 凯基 白血病 25 -5 28 生 其它肿 -52882088810388309816 物 瘤
6周 8周 8周 8周 8周 8周 8周 8周 8周 8周 8周 8周 6周
6周 8周
备注
C57/BL6 小鼠 皮下实体瘤 BalB/c 裸鼠 皮下实体瘤 BalB/c 裸鼠 皮下实体瘤 ICR 小鼠或 KM 小鼠 皮下实体瘤 BalB/c 裸鼠 皮下实体瘤 BalB/c 裸鼠 皮下实体瘤 BalB/c 裸鼠 皮下实体瘤 BalB/c 裸鼠 皮下实体瘤 BalB/c 裸鼠 皮下实体瘤 BalB/c 裸鼠 皮下实体瘤 BalB/c 裸鼠 皮下实体瘤 ICR 小鼠或 KM 小鼠 皮下实体瘤或
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2003/6/27
于志斌
前言
近年来,国内外在海洋生物抗肿瘤活性物质筛选和研 究上已取得了初步的成果。NCI每年筛选的出3万个新 的抗肿瘤化合物这些化合物绝大多数具有独特的化学 结构和明显的抗癌、抗病毒作用, 有以影响DNA、 RNA、蛋白质为主的,也有以干扰有丝分裂或诱导细 胞内信息分子的改变为主的。除了一些新的化合物, 在一些老的化合物中也发现很多具有抗肿瘤的活性。 活性化合物的筛选关键问题之一在于选择有效的活性 筛选模型。 本文对MTT法、DDRT法、稻瘟霉法以及镰刀菌 等几种筛选模型进行简单的介绍。
镰刀菌模型筛选步骤
将镰刀菌接种在土豆培养基上,28℃培养1~2周 后,加入无菌水刮下孢子,摇匀过滤;以土豆液体 培养基稀释成1×104/mL孢子的孢子液, 然后 将50μL待筛样品,分别加到96孔板,第1行各孔 中(从第3列开始,第1、2列作空白对照),每1列从 第1行开始依次稀释到最后一孔(即第8行),然后 在28℃培养16h,在倒置显微镜下观察孢子及菌 丝体生长形态变化情况,根据上述活性指标,判 断活性,计算最小活性浓度。
DDRT法(different DNA repair test)
试验菌株 343/591为赖氨酸和生物素营养缺陷型并具 有发酵乳糖能力和DNA修复缺陷的菌种;343/636为不 能发酵乳糖的脯氨酸营养缺陷型菌株并具有紫外线损 伤和DNA修复能力。 DDRT法是一种利用两个菌株对DNA损伤修复的差异 性建立的方法,可以用来检测试验物的DNA毒性。 343/591为DNA修复缺陷菌株,而343/636菌株具有紫外 线损伤和DNA修复能力,因而通过两个菌株的修复能力 不同可以检测出受试物的DNA毒性。因而DDRT法可 用于筛选得到作用于DNA的抗肿瘤活性菌株。
稻瘟霉模型
近年来,人们发现大量的抗真菌和抗肿瘤化合物有明显的致 稻瘟霉菌丝弯曲作用或抑制发芽管生长作用,说明化合物使稻瘟霉 分生孢子或菌丝形态生长异常(卷曲、膨胀、菌丝分枝过多或念珠 状等)或生长抑制与其抗真菌、抗肿瘤活性之间存在一定的相关性。 因此,利用稻瘟霉这一模型筛选抗真菌、抗肿瘤活性菌株有一定的 实验依据。 稻瘟霉为一种植物病原真菌,中间有2个横隔为多细胞丝状真菌, 其个体比较大,形状特殊,呈亚梨形,易于观察;在沙氏培养液中进行 培养只需14~16h,因此非常快速;用96孔平板进行定量,操作程序 简单、易于掌握;菌种引进后由自己传代培养,比较经济;此外,用样 量少,重现性好,决定其作为初筛模型的优越性。
稻瘟霉活性筛选指标
抑制孢子芽萌发,孢子基本保持原有状态为抑制活性,用“×”表示 (a);孢子不萌发、萌发或菌丝生长,但形态发生严重变化,为强变 形活性,用“+++”表示(b);孢子萌发或菌丝生长,但形态发生中等强 度的变化,为中等变形活性,用“++”表示(c)。菌丝生长,但生长状态 异常,为弱变形活性,用“+”表示(d);菌丝正常生长为阴性,用“-”表 示(e)。
MTT法
MTT法是一种检测细胞生存和增殖状态 的方法,该方法以其简单、快速、准确等优点被 用于细胞毒和淋巴因子生长抑制的定量检测,尤 其在肿瘤化疗药敏实验中广泛使用。其原理是 MTT可被活细胞线粒体中的脱氢酶还原为蓝 色的甲基化合物,再经适当溶剂溶解后,其吸光 度与活细胞数相关,从而可作为检测活细胞数的 指标。因此MTT法可用于细胞毒活性物质的 筛选。
小结
这几种抗肿瘤筛选模型,具有相同的优点: 灵敏度高、重现性好、用量少、费用低、操作 简便、快速、安全等特点,是很好的初筛模型, 可广泛用于抗肿瘤活性物质的筛选。例如稻瘟 霉筛选模型和镰刀菌筛选模型,几乎相同的仪 器设备,而且操作简单,一般实验室即可实现; 与价格昂贵的流式细胞仪相比费用要低很多。 微生物的次级代谢产物是生物活性物质的 重要来源,开展新药的研究与开发,就必须加 强其生物活性物质的筛选。
镰刀菌筛选模型
中国热带农业科学院热带作物生物技 术国家重点实验室在筛选抗镰刀菌抗生 素时发现镰刀菌也可应用于抗肿瘤、抗 真菌活性物质的筛选,为此他们建立了镰 刀菌筛选模型, 应用于海洋微生物抗肿瘤 活性物质的筛选。 镰刀菌活性筛选指标与稻瘟霉指标相同。
植物类药物HH、VCR、HCPT可能是通过与细胞微管蛋白结合使其不 能形成纺锤体,促进微管解聚而抑制细胞周期中M期的有丝分裂。抗 代谢药物5- FU可能是通过阻碍S期的DNA合成,从而抑制孢子萌 发或使菌丝变形。烷化剂CTX、金属络合物DDP以及抗生素类药物 MMC则可能是通过直接破坏增殖期或Go期的细胞DNA,从而影响菌 丝的生长。结果表明,上述7种抗癌药在一定程度上均影响镰刀菌分生 孢子或菌丝生长,因此镰刀菌筛选模型可用于抗肿瘤活性物质筛选。
MTT法的基本步骤
细胞培养至90%铺底(处于对数生长期),用胰酶消化液消化收集细 胞,吹打制成单细胞悬液,苔芬蓝染色计算活细胞数,接种细胞于96 孔板中,每孔加200µ l悬浮细胞液,在37℃ CO2培养箱培养过夜。第 二天加入各稀释度的菌株发酵液20 µ l,继续培养3d,倒去培养 液,PBS洗1遍,加入MTT(0.2mg/ml)100 µ l,在37℃培养4h,然后 去除MTT,加DMSO与甘氨酸NaOH缓冲液(9∶1)200 µ l,摇 床摇0.5~1h,酶标仪测定570nm吸光值。其中四孔做全培液空白 对照,四孔做细胞悬浮液对照,每样平行测试3孔,以阿霉素为标准参 照.。计算抑制率: 抑制率=100%×(OD对照-OD实验)/OD对照 发酵液活性以ID50衡量,ID50为抑制率为50%时,发酵液所稀释 的倍数;抗癌药物的活性以IC50衡量,IC50为抑制率为50%时,样品 的浓度。
稻瘟霉筛选模型的步骤
将稻瘟霉接种在土豆培养基上,在27℃下培养12d左 右,收集分生孢子,混悬在10mL无菌水中,过滤除去菌丝 体得孢子悬液,孢子悬液中加入300μL沙氏液体培养基 后,以每孔50μL的量加入到96孔培养板的各孔中。将 各菌株的发酵液分别过滤除去菌丝体,取50μL滤液分 别加到96孔板的第1行各孔中(从第3列开始,第1、2列作 空白对照),每1列从第1行开始依次稀释到最后一孔(即 第8行),然后27℃培养16h,在倒置显微镜下观察孢子及 菌丝体生长形态变化情况,根据上述活性指标,判断活性, 计算最小活性浓度。
DDRT法的步骤
343/636和343/591菌株分别接种于含5ml蛋白胨-肉汤培 养基中; 在37℃振荡培养16h; 用分光光度计测 450nm处的343/591和343/636的OD值,用蛋白胨-肉汤 培养基稀释343/636菌液使其OD值与343/591相同; 在100ml中性红琼脂培养基中加入1ml菌液后倒入平皿 中静置1h; 将所要测定的放线菌发酵液和受试物滴 加在覆盖于琼脂培养基上直径为8mm的滤纸片上;37℃培养24h,以丝裂霉素为标准药物对照,根据发酵液 产生的抑菌圈大小的差异来判定其对DNA造成损伤 的大小及是否有抗肿瘤活性.
