cp2020中国药典硫酸镁标准
硫酸镁钠钾口服用浓溶液中苯甲酸钠测定方法

硫酸镁钠钾口服用浓溶液中苯甲酸钠测定方法
苯甲酸钠照高效液相色谱法(中国药典2020年版四部通则0512)测定。
供试品溶液精密量取本品5ml(约相当于苯甲酸钠2.8mg),置50ml量瓶中,加水稀释至刻度,摇匀。
对照品溶液取苯甲酸钠对照品适量,精密称定,加水溶解并稀释制成每1ml中约含苯甲酸钠50μg的溶液。
色谱条件用十八烷基硅烷键合硅胶为填充剂;以0.02mol/L醋酸铵溶液-甲醇(80:20)为流动相;检测波长为230nm;柱温为40℃;流速为每分钟1.0ml;进样体积10μl。
系统适用性要求理论板数按苯甲酸峰计算不低于2000。
测定法精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。
限度供试品溶液色谱图中,如有与苯甲酸钠保留时间一致的色谱峰,按外标法以峰面积计算,应为标示量的80%~120%(每瓶177ml含苯甲酸钠0.1g )。
典型图谱:。
硫酸镁的理化性质及危险特性
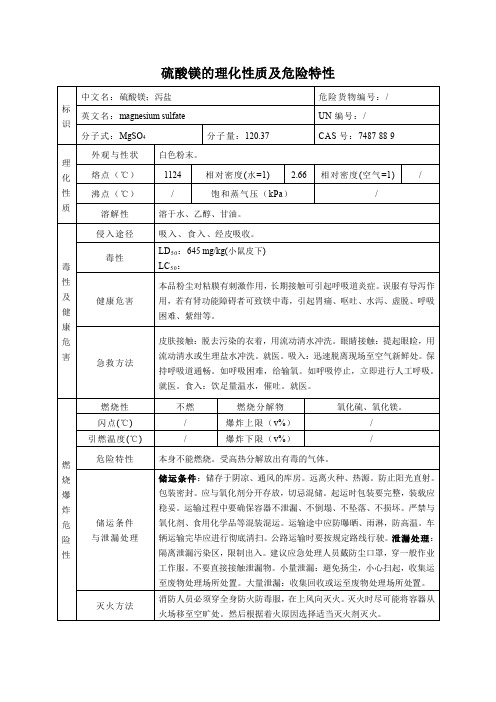
燃烧性
不燃
燃烧分解物
氧化硫、氧化镁。闪点(℃)/爆炸上限(v%)/
引燃温度(℃)
/
爆炸下限(v%)
/
危险特性
本身不能燃烧。受高热分解放出有毒的气体。
储运条件
与泄漏处理
储运条件:储存于阴凉、通风的库房。远离火种、热源。防止阳光直射。包装密封。应与氧化剂分开存放,切忌混储。起运时包装要完整,装载应稳妥。运输过程中要确保容器不泄漏、不倒塌、不坠落、不损坏。严禁与氧化剂、食用化学品等混装混运。运输途中应防曝晒、雨淋,防高温。车辆运输完毕应进行彻底清扫。公路运输时要按规定路线行驶。泄漏处理:隔离泄漏污染区,限制出入。建议应急处理人员戴防尘口罩,穿一般作业工作服。不要直接接触泄漏物。小量泄漏:避免扬尘,小心扫起,收集运至废物处理场所处置。大量泄漏:收集回收或运至废物处理场所处置。
硫酸镁的理化性质及危险特性
标识
中文名:硫酸镁;泻盐
危险货物编号:/
英文名:magnesium sulfate
UN编号:/
分子式:MgSO4
分子量:120.37
CAS号:7487-88-9
理化性质
外观与性状
白色粉末。
熔点(℃)
1124
相对密度(水=1)
2.66
相对密度(空气=1)
/
沸点(℃)
/
饱和蒸气压(kPa)
灭火方法
消防人员必须穿全身防火防毒服,在上风向灭火。灭火时尽可能将容器从火场移至空旷处。然后根据着火原因选择适当灭火剂灭火。
/
溶解性
溶于水、乙醇、甘油。
毒性及健康危害
侵入途径
吸入、食入、经皮吸收。
毒性
LD50:645 mg/kg(小鼠皮下)
纯化水标准(版中国药典)

纯化水【1】【试剂】10%氯化钾:取10g氯化钾溶加100ml水使溶解,即得。
稀硫酸:取硫酸57ml,加水稀释至1000ml,即得。
应含H2SO4 9.5%~10.5%甲基红指示剂:取甲基红0.1g,加0.05mol/L氢氧化钠溶液 5.3ml使溶解,再加水稀释至100ml,即得。
溴麝香草酚蓝指示剂:取溴麝香草酚蓝0.1g,加0.05mol/L氢氧化钠溶液3.2,ml使溶解,再加水稀释至200ml,即得。
0.1%二苯胺硫酸溶液:取0.1g二苯胺,加入100ml硫酸(98%)使之溶解,即得。
稀盐酸:取盐酸243ml,加水稀释至1000ml,即得。
应含HCl9.5%~10.5%高锰酸钾滴定液(0.02mol/L):取高锰酸钾3.2g,加水1000ml,煮沸15分钟,密塞,静置2天以上,用垂熔玻璃滤器过滤,摇匀。
高锰酸钾滴定液标定:准确称取于摄氏110度烘过两小时的草酸钠0.2g,置于烧杯中,加5%硫酸120ml,加热至80-90摄氏度,用高锰酸钾标准溶液滴至微红色(在1分钟内不消失)即为终点。
c=5m/v*0.0670式中c-高锰酸钾标准溶液的浓度(mol/L); m-称取草酸钠重量(g); v-滴定时消耗高锰酸钾溶液体积(ml);0.0670-Na2C2O4(草酸分子量)/2*1/1000。
本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【性状】本品为无色的澄清液体;无臭。
【检査】酸碱度取本品10ml,加甲基红指示液2滴,不得显红色;另取10ml,加溴麝香草酚蓝指示液5滴,不得显蓝色。
硝酸盐取本品5ml置试管中,于冰浴中冷却,加10%氯化钾溶液0.4ml与0.1%二苯胺硫酸溶液0.1ml,摇匀,缓缓滴加硫酸5ml,摇匀,将试管于50°C水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100ml,摇匀,精密量取1ml ,加水稀释成100ml,再精密量取10ml,加水稀释成100ml,摇匀,即得(每lml相当于1μg NO 3)]0.3ml,加无硝酸盐的水4.7ml,用同一方法处理后纯化水的颜色比较,不得更深(0.000006%)。
2020版药典植物类33种禁用农药残留

2020版药典植物类33种禁用农药残留检测方法2020年6月,《中国药典》2020年版正式出版。
33种禁用农药正式列入2020版《中国药典》四部通则《0212药材和饮片检定通则》。
2020版药典在四部通则《2341 农药残留量测定法》中新增第五法“药材及饮片(植物类)中禁用农药多残留测定法”。
第五法要求采用气相色谱-串联质谱法和液相色谱-串联质谱法,对药材及饮片(植物类)33种禁用农药及其代谢物,异构体共54个残留物进行测定。
1.气相色谱-串联质谱法色谱条件用(50%苯基)-甲基聚硅氧烷为固定液的弹性石英毛细管柱(柱长为30m,柱内径为0.25mm,膜厚度为0.25um)。
进样口温度250℃,不分流进样。
载气为高纯氦气(He)。
进样口为恒压模式,柱前压力为146kPa。
程序升温:初始温度60℃,保持1分钟,以30℃/min升至120℃,再以每分钟10℃的速率升温至160℃,再以每分钟2℃的速率升温至230℃,最后以每分钟15℃的速率升温至300℃,保持6分钟。
质谱条件以三重四极杆串联质谱仪检测;离子源为电子轰击源(EI),离子源温度250℃。
碰撞气为氮气或氩气。
质谱传输接口温度250℃。
质谱监测模式为多反应监测(MRM),各化合物参考保留时间、监测离子对、碰撞电压(CE)见表6。
为提高检测灵敏度,可根据保留时间分段监测各农药。
2.高效液相色谱-串联质谱法色谱条件以十八烷基硅烷键合硅胶为填充剂(柱长10cm,内径为2.1mm,粒径为2.6um);以0.1%甲酸溶液(含5mmol/L甲酸铵)为流动相A,以乙-0.1%甲酸溶液(含5mmol/L甲酸铵)(95:5)为流动相B,按下表5进行梯度洗脱;流速为每分钟0.3ml,柱温为40℃。
质谱条件以三重四极杆串联质谱仪检测;离子源为电喷雾(ESI)离子源,正离子扫描模式。
监测模式为多反应监测(MRVD,各化合物参考保留时间、监测离子对、碰撞电压(CE)见表7。
硫酸镁注射液说明书

硫酸镁注射液说明书(总3页) -CAL-FENGHAI.-(YICAI)-Company One1-CAL-本页仅作为文档封面,使用请直接删除硫酸镁注射液说明书请仔细阅读说明书并在医师指导下使用【药品名称】通用名称:硫酸镁注射液英文名称:Magnesium Sulfate Injection汉语拼音:Liusuanmei Zhusheye【成份】本品主要成份为:硫酸镁;辅料为:注射用水。
分子式:MgSO4·7H2O分子量:246.48【性状】本品为无色的澄明液体。
【适应症】可作为抗惊厥药。
常用于妊娠高血压。
降低血压,治疗先兆子痫和子痫,也用于治疗早产。
【规格】10ml:2.5g【用法用量】1.治疗中重度妊娠高血压征、先兆子痫和子痫首次剂量为2.5~4g,用25%葡萄糖注射液20ml稀释后,5分钟内缓慢静脉注射,以后每小时1~2g静脉滴注维持。
24小时总量为30g,根据膝腱反射、呼吸次数和尿量监测。
2.治疗早产与治疗妊娠高血压用药剂量和方法相似,首次负荷量为4g;用25%葡萄糖注射液20ml稀释后5分钟内缓慢静脉注射,以后用25%硫酸镁注射液60ml,加于5%葡萄糖注射液1000ml中静脉滴注,速度为每小时2g,直到宫缩停止后2小时,以后口服β肾上腺受体激动药维持。
3.治疗小儿惊厥肌注或静脉用药:每次0.1~0.15g/kg,以5%~10%葡萄糖注射液将本品稀释成1%溶液,静脉滴注或稀释成5%溶液,缓慢静注。
25%溶液可作深层肌注。
一般儿科仅用肌注或静脉用药,安全。
【不良反应】1.静脉注射硫酸镁常引起潮红、出汗、口干等症状,快速静脉注射时可引起恶心、呕吐、心慌、头晕,个别出现眼球震颤,减慢注射速度症状可消失。
2.肾功能不全,用药剂量大,可发生血镁积聚,血镁浓度达5mmol/L时,可出现肌肉兴奋性受抑制,感觉反应迟钝,膝腱反射消失,呼吸开始受抑制,血镁浓度达6mmol/L时可发生呼吸停止和心律失常,心脏传导阻滞,浓度进一步升高,可使心跳停止。
硫酸镁的正确使用

整理课件
24
硫酸镁不建议用在保胎 的争论(4)
在芝加哥Lying-In 医院进行的一项围产期死亡率对照研究 发现,从1986-1999年随着硫酸镁剂量累计超过48g的时 候,胎儿死亡风险增加,并具有统计学差异。与较低剂量 比较,死亡和剂量最佳比例是4.7(95% 的可信度在1.1– 20.0之间)。48g大剂量,通常在常规保胎剂量4-6g,随后 2-4g/小时,持续24小时。并不是所有研究均发现硫酸镁 对婴儿和胎儿的伤害,其中一个研究还发现了可能的益处。 然而在这些试验中使用硫酸镁剂量小于其一般用于保胎的 剂量。(剂量经常超过50g 24小时),在有益和有害之间 存在着一个狭窄的治疗窗。
肌注和静脉注射,药物均由肾脏排出,排出的 速度与血镁浓度和肾小球滤过率相关
【资料来源】:中国药典2005年版及临床用药须知2005年版
整理课件
5
硫酸镁使用中观察指标
膝腱反射必须存在 呼吸不少于16次/分 尿量不少于17ml/h(24小时尿量不少于
400ml)
【资料来源】:中国药典2005年版及临床用药须知2005年版
【资料来源】:中国药典2005年版及临床用药须知2005年版
整理课件
17
药物相互作用
同时静注钙剂时,可减弱本品的中枢抑制和骨骼 肌松弛作用
本品可加强氯丙嗪、氯氮革等药物的中枢抑制作 用。故服用中枢抑制药中毒需导泻时,应改用硫 酸钠
与其他具有神经肌肉阻断的药物合用时,可致严 重的神经肌肉传导阻滞
8
整理课件
9
临时医嘱
5%Glucose 100ml
25%Magsulfate 20ml ivdrip(入泵) (30分 钟内滴完 )
5%Glucose 500ml
硫酸镁

【药物名称】硫酸镁 Magnesium Sulfate[国家基本药物]【药物类别】泻药【药物别名】硫苦、干燥硫酸镁、苦盐、泻利盐、泻盐、药用硫酸镁 Addex-Magnesium、Epsom Salt、Epsonite、Mag. Sulfas、Magnesii Sulfatis·7H2O。
分子量:246.48。
性状:本品为无色结晶;无臭,味苦、咸;【分子式成分】分子式:MgSO4有风化性。
在水中易溶,在乙醇中几乎不溶。
【制剂规格】注射液:10ml:1g、10ml:2.5g、20mL:2g;灌肠剂:50%;结晶粉剂:50、500g/袋。
【药理毒理】本品的具体作用如下:(1)导泻作用:本品口服不被肠道吸收,可使肠腔内渗透压提高,阻止水分被肠壁吸收,肠内保留大量水分引起肠道扩张,刺激牵张感受器而增强肠蠕动;同时本品可促使肠壁释放胆囊收缩素,后者能刺激肠道的分泌和运动,增强本品的致泻作用。
本品导泻作用强而迅速,其作用速度和强度受药物浓度的影响,空腹服用并同时大量饮水,可加速和增强下泻作用。
(2)利胆作用:本品小剂量可使奥狄(Oddi)括约肌松弛,胆囊收缩,增强胆汁引流,起利胆作用。
(3)对中枢神经系统的作用:本品注射给药,可提高细胞外液中镁离子浓度,抑制中枢神经系统的活动,抑制运动神经-肌肉接头乙酰胆碱的释放,并抑制运动神经元终板对乙酰胆碱的敏感性,从而产生镇静、降低或解除横纹肌收缩的作用,也能降低颅内压。
(4)对心血管系统的作用:本品注射给药,可直接舒张外周血管平滑肌,并引起交感神经节冲动传递障碍,从而导致血管扩张,血压下降。
同时,本品静脉给药,还可延长心脏传导系统的有效不应期,提高室颤阈值,并使心肌复极均匀,减少或消除折返激动,有利于快速性室性心律失常的控制。
(5)对子宫的作用:本品对子宫平滑肌收缩也有抑制作用,可用于治疗早产。
(6)消炎去肿:本品50%溶液外用热敷患处,有消炎去肿的作用。
硫酸镁质量标准及检测方法
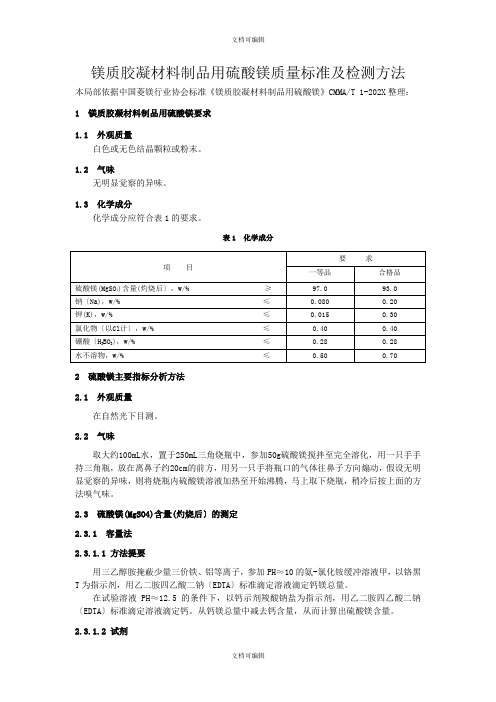
镁质胶凝材料制品用硫酸镁质量标准及检测方法本局部依据中国菱镁行业协会标准《镁质胶凝材料制品用硫酸镁》CMMA/T 1-202X整理:1 镁质胶凝材料制品用硫酸镁要求1.1 外观质量白色或无色结晶颗粒或粉末。
1.2 气味无明显觉察的异味。
1.3 化学成分化学成分应符合表1的要求。
表1 化学成分2 硫酸镁主要指标分析方法2.1 外观质量在自然光下目测。
2.2 气味取大约100mL水,置于250mL三角烧瓶中,参加50g硫酸镁搅拌至完全溶化,用一只手手持三角瓶,放在离鼻子约20cm的前方,用另一只手将瓶口的气体往鼻子方向煽动,假设无明显觉察的异味,则将烧瓶内硫酸镁溶液加热至开始沸腾,马上取下烧瓶,稍冷后按上面的方法嗅气味。
2.3 硫酸镁(MgSO4)含量(灼烧后〕的测定2.3.1 容量法2.3.1.1 方法提要用三乙醇胺掩蔽少量三价铁、铝等离子,参加PH≈10的氨-氯化铵缓冲溶液甲,以铬黑T为指示剂,用乙二胺四乙酸二钠〔EDTA〕标准滴定溶液滴定钙镁总量。
在试验溶液PH≈12.5的条件下,以钙示剂羧酸钠盐为指示剂,用乙二胺四乙酸二钠〔EDTA〕标准滴定溶液滴定钙。
从钙镁总量中减去钙含量,从而计算出硫酸镁含量。
2.3.1.2 试剂1〕氨水溶液:1+2;2〕三乙醇胺溶液:1+3;3〕氨-氯化铵缓冲溶液甲〔PH≈10〕: 20g NH4Cl〔A.R.〕溶于水,参加80ml 25%NH3·H2O 〔A.R.〕溶液,再用水稀释至1L,摇匀;4〕氢氧化钠溶液:50g/L;5〕乙二胺四乙酸二钠〔EDTA〕标准滴定溶液:c(EDTA) ≈0.05mol/L;6〕乙二胺四乙酸二钠〔EDTA〕标准滴定溶液:c(EDTA) ≈0.02mol/L;7〕铬黑T指示剂;8〕钙示剂羧酸钠盐指示剂。
2.3.1.3 分析步骤1〕试验溶液的制备称取约10g硫酸镁试样,精确至0.001g,置于250ml烧杯中,参加100ml水溶化。
制药用水简介

制药用水简介制药用水通常指制药工艺过程中用到的各种质量标准的水。
制药用水是制药生产过程的重要原料,参与了整个生产工艺过程,包括原料生产、分离纯化、成品制备、洗涤过程、清洗过程和消毒过程等。
因此,在制药生产过程中,制药用水系统是至关重要的组成部分。
制药用蒸汽系统是湿热灭菌的一种介质,主要应用于注射用水系统、湿热灭菌柜、生物反应器、配液罐、管路系统、过滤器等重要设备与系统的灭菌。
常见的制药用蒸汽系统主要为纯蒸汽系统,纯蒸汽的冷凝水直接与设备或物品表面接触,或者接触到用以分析物品性质的物料,纯蒸汽冷凝后的水质需满足注射用水质量标准,因此,制药用蒸汽系统也是医药行业无菌生产工艺过程中一个非常重要的组成部分。
制药用水和制药用蒸汽的质量从药品生产质量管理规范(GMP)和药典的角度来看非常重要,从良好的工程管理规范(GEP)和经济的角度来看也同样重要,制药生产企业必须证明其所使用的制药用水系统与制药用蒸汽系统能始终如一地提供达到质量标准的制药用水与制药用蒸汽。
通常情况下,制药行业将制药用水系统与制药用蒸汽系统统称为制药用水系统,简称水系统。
制备制药用水的本质是减少或消灭潜在的污染源,欧盟和WHO将制药用水中的杂质列为潜在杂质来源之一,基于这个问题的考虑,本书提出如何进行制药用水制备、储存与分配系统的设计并确保污染风险得到控制。
1.1 制药用水的分类对制药用水的定义和用途,通常以药典为准,各国药典对制药用水通常有不同的定义、不同的用途规定。
从使用角度分类,制药用水主要分为散装水与包装水两大类。
散装水特指制药生产企业按相关生产工艺自制的制药用水,例如,中国药典认可的散装水包括纯化水和注射用水;欧盟药典认可的散装水包括散装纯化水、草药提取用水和注射用水;美国药典认可的散装水包括散装纯化水、血液透析用水和注射用水等。
包装水也称成品水,特指按制药工艺生产的包装成品水,例如,中国药典收录了灭菌注射用水;欧盟药典收录了包装纯化水和灭菌注射用水等;美国药典收录了抑菌注射用水、灭菌吸入用水、灭菌注射用水、灭菌冲洗用水和灭菌纯化水等多种产品水(表1)。
硫酸镁检测SOP

硫酸镁检测SOP1. 目的规范硫酸镁的检测操作,确保检测的准确性。
2. 范围本标准适用于硫酸镁的测定。
3. 定义无4. 职责4.1.QC负责本规程的起草、修订、培训及执行。
4.2.QA、QC组长、质量管理部经理负责本规程的审核。
4.3.质量总监负责批准本规程。
4.4.QA负责本规程执行的监督。
5. 引用标准《中华人民共和国药典》6. 材料见程序7. 流程图无8. 程序8.1.性状:本品应为无色结晶;无臭,味苦、咸;有风化性。
在水中易溶,在乙醇中几乎不溶。
8.2.鉴别8.2.1.原理:镁离子遇氢氧根离子可生成白色氢氧化镁沉淀或胶体,此沉淀或胶体在氯化铵试液中能生成络合物而使沉淀溶解,此络合物在弱酸中即可分解,白色沉淀出现。
镁离子遇氢氧根离子可生成白色氢氧化镁沉淀或胶体,此沉淀或胶体遇碘即可生成红棕色碘化镁沉淀。
钡离子与硫酸根离子反应,可生成不溶于盐酸或硝酸的白色沉淀。
硫酸根离子与铅离子反应生成硫酸铅白色沉淀,此白色沉淀能在强碱溶液中溶解。
硫代硫酸根离子与盐酸能生成白色沉淀,而硫酸根与盐酸不能生成白色沉淀。
8.2.2.仪器及设备:电子天平、100ml烧杯、中试管、100ml容量瓶等。
8.2.3.试剂及配制:氨试液,取浓氨溶液40ml,加水使成100ml,即得。
氯化铵试液,取氯化铵10.5g,加水溶解使成100ml,即得。
磷酸氢二钠试液,取磷酸氢二钠结晶12g,加水使溶解成100ml,即得。
氢氧化钠试液,取氢氧化钠4.3g,加水使溶解成100g,即得。
碘试液,取用碘滴定液(0.1mol/L)。
硫酸镁溶液,取硫酸镁20g,加水使溶解成100ml,即得。
氯化钡试液,取氯化钡的细粉5g,加水使溶解成100ml。
醋酸铅试液,取醋酸铅10g,加新沸过的冷水溶解后,滴加醋酸使溶液澄清,再加新沸过的冷水使成100ml,即得。
8.2.4.操作步骤:取已配制好的硫酸镁溶液20ml于中试管中,滴加氨试液,即生成白色沉淀;滴加氯化铵试液,沉淀溶解;再加磷酸氢二钠试液1滴,振摇,即生成白色沉淀,分离,沉淀在氨试液中不溶解。
硫酸镁的MSDS

硫酸镁;泻盐
标
识
中文名:
硫酸镁;泻盐
英文名:
Magnesium sulfate;Epsom salts
分子式:
MgSO4
分子量:
120.37
CAS号:
7487-88-9
RTECS号:
OM4500000
穿工作服。
手防护:
戴防护手套。
其他:
工作现场禁止吸烟、进食和饮水。工作后,淋浴更衣。注意个人清洁卫生。
泄漏处置:
隔离泄漏污染区,周围设警告标志,建议应急处理人员戴好口罩、护目镜,穿工作服。小心扫起,避免扬尘,运至废物处理场所。也可以用大量水冲洗,经稀释的污水放入废水系统。如大量泄漏,收集回收或无害处理后废弃。
灭火方法:
不燃。
包装与储运
危险性类别:
危险货物包装标志:
包装类别:
储运注意事项:
储存于阴凉、通风仓间内。远离火种、热源。保持容器密封。应与氧化剂、食用化工原料分开存放。搬运时要轻装轻卸,防止包装及容器损坏。分装和搬运作业要注意个人防护。
毒性危害
接触限值:
中国MAC:未制订标准
前苏联MAC:2mg/m3
美国TLV—TWA:未制订标准
美国TLV—STEL:未制订标准
侵入途径:
吸入食入
毒性:
LD50:645mg/kg(小鼠皮下)
LC50:
健康危害:
本品粉尘对粘膜有刺激作用,长期接触可引起呼吸道炎症。误服有导泻作用,若有肾功能障碍者可发生镁中毒,发生胃痛、呕吐、水泻、虚脱,呼吸困难、紫绀等。
硫酸镁

理化性质
物理性质
化学性质Biblioteka 溶解性:易溶于水,微溶于乙醇、甘油、乙醚,不溶于丙酮。
稳定性:无水硫酸镁易吸水,七水硫酸镁易脱水 毒性:低毒 毒理学数据:小鼠皮下: LD50 645 mg/kg(小鼠皮下);小鼠腹腔:670-733mg/kg 刺激性:本品可能引起引起胃痛、呕吐、水泻、虚脱、呼吸困难、紫绀等
用于制革、炸药、肥料、造纸、瓷器、印染料、铅酸蓄电池等工业。硫酸镁和其他钾、钙、氨基酸盐、硅酸 盐等矿物质一样,可以用作浴盐。
肥料:在农业和园艺,硫酸镁是用来改良缺镁的土壤(镁是一个叶绿素分子的基本要素),最常见的用于盆 栽植物,或含镁作物,如马铃薯,玫瑰,西红柿,辣椒和大麻。施用硫酸镁的优势超过其他硫酸镁镁土壤改良剂 (如白云质石灰)是它的高溶解性。
主要用途
建材 医药
工业 农业
硫酸镁溶于水后可与轻烧粉反应形成硫氧镁水泥。硫氧镁水泥具有较好的防火性、保温性、耐久性和环保性, 应用在防火门芯板、外墙保温板、硅质改性保温板、防火板等诸多领域 。
(1)硫酸镁可抑制中枢神经系统,松弛骨骼肌,具有镇静、抗痉挛以及减低颅内压等作用。常用于治疗惊厥、 子痫、尿毒症、破伤风及高血压脑病等。多以10%硫酸镁10毫升深部肌肉注射或用5%葡萄糖稀释成2%~2.5%的溶 液缓慢滴注。但应注意直接静脉注射或大剂量肌肉注射硫酸镁很危险,一般25%硫酸镁每次最多用15毫升即可。 使用时应注意观察病人呼吸和血压情况,膝反射迟钝是镁离子足量的重要标志。
制备方法
以氧化镁、氢氧化镁、碳酸镁、菱苦土等为原料加硫酸分解或中和而得。也有以生产氯化钾副产为原料,与 制溴后含镁母液按比例混合,冷却结晶分离得粗硫酸镁,再加热过滤、除杂、冷却结晶得工业硫酸镁。还可用苦 卤加热浓缩、结晶分离而得或氧化镁及石膏水悬浮液碳化制得。
HG∕T5737-2020化妆品用硫酸镁(报批稿)

化妆品用硫酸镁1范围本标准规定了化妆品用硫酸镁的要求、试验方法、检验规则、标志、标签、包装、运输、贮存。
本标准适用于化妆品用硫酸镁,主要用于浴盐、香皂、沐浴液、洗面奶等,也用作化妆品和洗护用品的添加剂。
2规范性引用文件下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB/T191—2008包装储运图示标志GB5009.15食品安全国家标准食品中镉的测定GB5009.17—2014食品安全国家标准食品中总汞及有机汞的测定GB5009.75—2014食品安全国家标准食品添加剂中铅的测定GB5009.76食品安全国家标准食品添加剂中砷的测定GB/T6678化工产品采样总则GB/T6682—2008分析实验室用水规格和试验方法GB/T8170数值修约规则与极限数值的表示和判定HG/T3696.1无机化工产品化学分析用标准溶液、制剂及制品的制备第1部分:标准滴定溶液的制备HG/T3696.2无机化工产品化学分析用标准溶液、制剂及制品的制备第2部分:杂质标准溶液的制备HG/T3696.3无机化工产品化学分析用标准溶液、制剂及制品的制备第3部分:制剂及制品的制备3分子式和相对分子质量分子式:MgSO4相对分子质量:120.36(按2018年国际相对原子质量)MgSO4·H2O相对分子质量:138.38(按2018年国际相对原子质量)MgSO4·7H2O相对分子质量:246.47(按2018年国际相对原子质量)MgSO4·n H2O(n是水合作用的平均值,为2~6之间的整数)4要求4.1外观:白色或无色结晶颗粒或粉末。
4.2化妆品用硫酸镁按本标准规定的试验方法检测应符合表1的规定。
表1技术要求项目指标硫酸镁(MgSO4)(以灼烧干基计)w/%≥99.0灼烧减量w/%无水硫酸镁(MgSO4)≤ 3.0一水硫酸镁(MgSO4·H2O)13.0~16.0七水硫酸镁(MgSO4·7H2O)40.0~52.0硫酸镁干燥品(MgSO4·n H2O)22.0~33.0铅(Pb)w/%≤0.0005镉(Cd)w/%≤0.0005汞(Hg)w/%≤0.0001砷(As)w/%≤0.0002pH(10g/L溶液) 5.5~9.5总有机碳a(TOC)w/%≤0.003a天然法不要求,天然法指由盐湖中得到的苦卤经自然蒸发浓缩成粗硫酸镁,再经纯化、重结晶、干燥得到的化妆品用硫酸镁。
硫酸镁简介

硫酸镁简介目录•1拼音•2英文参考•3国家基本药物•4硫酸镁基本信息o 4.1识别o 4.2性质o 4.3结构o 4.4相关化学品•5起源•6用途o 6.1农业o 6.2医药o 6.3有机化学o 6.4其他用途•7危险性o7.1急救措施o7.2消防措施o7.3泄漏应急处理o7.4操作处置与储存o7.5接触控制/个体防护•8硫酸镁药典标准o8.1品名▪8.1.1中文名▪8.1.2汉语拼音▪8.1.3英文名o8.2分子式与分子量o8.3来源含量o8.4性状o8.5鉴别o8.6检查▪8.6.1酸堿度▪8.6.2溶液的澄清度▪8.6.3氯化物▪8.6.4炽灼失重▪8.6.5铁盐▪8.6.6钙▪8.6.7锌盐▪8.6.8重金属▪8.6.9砷盐o8.7含量测定o8.8类别o8.9贮藏o8.10制剂o8.11版本•9硫酸镁说明书o9.1药品名称o9.2英文名称o9.3硫酸镁的别名o9.4分类o9.5剂型o9.6硫酸镁的药理作用o9.7硫酸镁的药代动力学o9.8硫酸镁的适应证o9.9硫酸镁的禁忌证o9.10注意事项o9.11硫酸镁的不良反应o9.12硫酸镁的用法用量o9.13硫酸镁与其它药物的相互作用o9.14专家点评•10硫酸镁中毒o10.1临床表现o10.2诊断o10.3治疗•11参考资料•附:o*硫酸镁相关药品说明书其它版本1拼音liú suān měi2英文参考Epsom salt,magnesium sulfate,MGW,salamarum[湘雅医学专业词典]3国家基本药物与硫酸镁有关的国家基本药物零售指导价格信息序号基本药物目录序号药品名称剂型规格单位零售指导价格类别备注 639 90 硫酸镁注射剂 2.5g:10ml 瓶(支) 1.1 化学药品和生物制品部分*△ 640 90 硫酸镁注射剂 1g:10ml 瓶(支)0.55 化学药品和生物制品部分注:1、表中备注栏标注“*”的为代表品。
《保健食品原料目录 营养素补充剂(2020年版)》

2.0
化醇
维生素 D3 中国药典《维生素 D3》
所有人群
计,µg)
孕妇
2.0
乳母
2.0
1—3
0.1
GB14751《维生素B1(盐酸硫 盐酸硫胺素
胺素)》
所有人群
4—6
0.2
7—10
0.2
维生素 B1
维生素 B1
11—13
0.3
(以硫胺
素计,mg) 14—17
0.3
中国药典《硝酸硫胺》
硝酸硫胺素
所有人群
适宜 人群
1—3
4—6 7—10
柠檬酸钙 GB1903.14《柠檬酸钙》 葡萄糖酸钙 GB15571《葡萄糖酸钙》
所有人群 所有人群
11—13
乳酸钙
GB1886.21《乳酸钙》 4 岁以上人群
14—17
钙
磷酸氢钙 GB1886.3《磷酸氢钙》
所有人群 Ca(以Ca计, 成人
mg)
磷酸二氢钙 GB25559《磷酸二氢钙》 4 岁以上人群
磷酸三钙 (磷酸钙)
GB25558《磷酸三钙》
所有人群
孕妇
硫酸钙
GB1886.6《硫酸钙》
所有人群
L-乳酸钙 GB25555 《L-乳酸钙》 所有人群 甘油磷酸钙 中国药典《甘油磷酸钙》 4 岁以上人群
乳母
柠檬酸苹果 GB1903.18《柠檬酸苹果 4 岁以上人
酸钙
酸钙》
群
碳酸镁
GB25587《碳酸镁》
《琥珀酸亚铁》 GB 1903.38《琥珀酸亚铁》
4 岁以上人 群
11—13
3.5
14—17
3.5
成人
5.0
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
cp2020中国药典硫酸镁标准
《中华人民共和国药典》是中国的药典标准,该药典对硫酸镁的规定如下:
英文名称:Magnesium Sulfate
化学名称:硫酸镁
分子式:MgSO4·7H2O
性状:无色结晶或白色颗粒,无臭,微苦味。
溶解性:可溶于水,微溶于醇。
在真空下加热至约120℃失去结晶水,贮于沙密瓶中。
含量测定:称取本品约0.5g,加入少量去离子水,加热溶解,冷却后定容首次溶液,取首次溶液10ml,加水稀释为50ml,振摇均匀。
按《一般分析法》中多硼酸盐复杂零价卤素滴定法第四法测定硫酸镁(Mg)的含量。
含量要求:
- MgSO4·7H2O含量:≥99.0%。
- pH值(对10%溶液):5.0-9.0。
水分:检查样品的含水量,不应超过12.0%。
重金属:每克不得超过20微克。
理化规格:
- 显微物:应符合塔斯曼蓝试验的要求。
- 替代溶出物:未使用。
- 显微水质:不得超过0.2ml。
以上是《中华人民共和国药典》对硫酸镁标准的要求,用于质量标准和质量控制。
请注意,该标准仅适用于中国境内的药品生产和销售。
其他国家或地区的标准可能会有所不同,请根据当地法规和标准执行。
