光化学——电子转移.ppt
光化学反应中的电子转移过程研究

光化学反应中的电子转移过程研究光化学反应是一种利用光能进行化学反应的方法,其主要过程涉及到光吸收、电子激发和电子转移等方面。
其中,电子转移过程是一个比较基础的科学问题,也是研究光化学反应机制的重要内容之一。
本文将探讨光化学反应中的电子转移过程的研究进展。
一、电子转移电子转移是指电子从一个分子传递到另一个分子的过程。
在光化学反应中,电子转移是光能变化的一个重要形式,也是反应机制的一个关键环节。
通常来说,光能可以激发一个分子中的电子,使得这个电子从基态跃迁到激发态。
在激发态下,这个电子可以与其他分子中的电子进行相互作用,从而实现电子转移。
二、电子转移过程的研究在电子转移过程中,电子的运动状态、电子云的转移等都是需要研究的内容。
目前,研究人员通过理论模拟和实验方法来探究电子转移的机理和动力学过程。
1.理论模拟理论模拟是一种基于计算机程序的方法,可以模拟分子中的电子转移过程。
目前,理论模拟主要采用量子化学理论和分子动力学模拟方法。
量子化学理论可以计算分子中每个原子的能级和电子构型,从而预测电子转移的概率和动力学过程。
而分子动力学模拟则可以模拟分子系统中的运动和相互作用,可以揭示分子中电子转移的能量和结构变化。
2.实验方法实验方法主要包括光谱学、超快激光技术和电化学技术等。
光谱学可以测量分子的吸收和发射光谱,观察分子的激发态和基态之间的电子转移。
超快激光技术则可以测量分子中电子转移的时间尺度和动力学过程。
电化学技术可以通过外界电场来控制分子中电子的位置、能量和方向,从而研究电子转移的过程。
三、电子转移过程的应用电子转移过程的研究不仅有理论的意义,还有实际应用价值。
电子转移可应用于制备新型材料、开发光触媒、设计新型电子器件等。
例如,通过研究电子转移过程,可以发现激发态分子发射的光子具有特殊的能量和波长,从而可以制备自发光材料和荧光染料等。
另外,电子转移还是光触媒反应中的关键步骤,通过研究电子转移过程,可以改善光触媒的效率和稳定性。
光合电子传递

Nobel Prize Winners In photosynthesis research
Paul D. Boyer and John E. Walker (1997, Chemistry): ATP合成. Rudolph Marcus (1992, Chemistry): Electron transfer theory: Hartmut Michel; Robert Huber; and Johannes Deisenhofer (1988, Chemistry): X-ray structure of bacterial reaction center. Peter Mitchell (1978, Chemistry): chemi-osmotic theory Robert Burns Woodward (1965, Chemistry): Total synthesis of chlorophyll Melvin Calvin (1961, Chemistry): Carbon-dioxide assimilation Richard Kuhn (1938, Chemistry): carotenoids; vitamins [Germany] Paul Karrer (1937, Chemistry): Carotenoid structure; flavins, etc Hans Fischer (1930, Chemistry): Chlorophyll chemistry; etc Richard Martin Wilstatter (1915, Chemistry): Chlorophyll purification
Emerson 增益效应
红光+远红光
高等有机化学课件-光化学

光化学反应可以将水中的有机物分解成无害的物质,降低水体污 染。
藻类控制
光化学反应可以抑制藻类的生长,保持水体的生态平衡。
光化学在土壤污染治理中的应用
土壤修复
光化学反应可以分解土壤中的有害物质,降低土壤污染程度。
农药降解
光化学反应可以分解农药,减少农药对环境和农作物的危害。
重金属固定
光化学反应可以将重金属固定在土壤中,防止重金属迁移和污染地 下水。
羧酸及其衍生物的光化学反应在合成高分子材料和功能材料方面具有重要 应用。
03
光化学合成
光化学合成方法
Байду номын сангаас
直接光化学合成
01
利用光能直接引发有机反应,通常需要使用高能量的光源,如
紫外光。
间接光化学合成
02
通过光敏剂或催化剂将光能转化为化学能,引发有机反应。这
种方法通常需要较低能量的光源,如可见光。
组合光化学合成
自由基和离子反应
在光化学反应中,自由基和离子是常见的活性物 种,它们参与的反应类型和机理各不相同。
光化学合成的应用
有机合成
利用光化学合成方法可以合成多种有 机化合物,如烯烃、芳香烃、醇、醛 等。
药物研发
光化学合成方法可用于合成药物中间 体或活性成分,提高药物的生产效率 和纯度。
生物成像和探针
利用光敏剂或荧光探针标记生物分子 ,可以用于生物成像和检测生物分子 的结构和功能。
高等有机化学课件-光化学
目录
• 光化学基础 • 有机光化学反应 • 光化学合成 • 光化学反应动力学 • 光化学在环境科学中的应用
01
光化学基础
光化学基本概念
01
光化学是研究光与物质相互作用及其相关能量转换 、信息转换的学科领域。
光催化氧化过程PPT课件

– 与无机离子的反应
电子转移
O C H d O H C 2 d O N H iO H N 2 i O T H 3 iO H T 4 i O H C2 3-O O H C-3O O H Br -3 O OH Br 3O
10
– 与无机离子的反应
夺氢反应
O H HC -3 H O 2O C-3O O H- 4 S H O 2 O S- 4 O O H H-3 S O H 2O S-3 O
<500
100± 20 < 3 × 1 0 -5 < 4 × 1 0 -2 (3 ± 1 )× 1 0 -2 (3± 3) × 103
K · OH M -1s -1 7 .8 × 1 0 9 3 .9 × 1 0 9 3 .0 × 1 0 9 7 .5 × 1 0 9 1 .3 × 1 0 8 1 .6 × 1 0 7 1 .4 × 1 0 6 3 .1 × 1 0 8 2 .2 × 1 0 10 3 .2 × 1 0 9 8 .5 × 1 0 7 7 .7 × 1 0 6 3 .1 × 1 0 8 1 .6 × 1 0 10
活泼自由基:·OH, ·OOH, ·O2-
27
0 Vacuum
E (NHE)
-2
SiC SrTiO3
-2
CdS
-4 CdSe
ZnO WO3TiO2
ZnS
BaTiO3
3.0
Fe2O3
SnO2
0
3.2
CdO
1.7 2.5
-6
3.2 3.2 3.2
3.7
3.2 2.2
2.1 2
3.8
-8 4
28
常用的半导体光催化剂:TiO2、CdS、 ZnO、WO3、Fe2O3、SnO2、SrTiO3等 其中催化活性最高: TiO2 、CdS、ZnO CdS、ZnO在光照时不稳定,金属离子溶 出;其优势在能隙较小,可吸收可见光。 TiO2 :不发生光腐蚀;耐酸碱性好,化学 性质稳定;对生物无毒性;来源丰富;能 隙较大(3.2ev,最大入射波长为 387.5nm),有很强的氧化还原能力;
光致电子转移
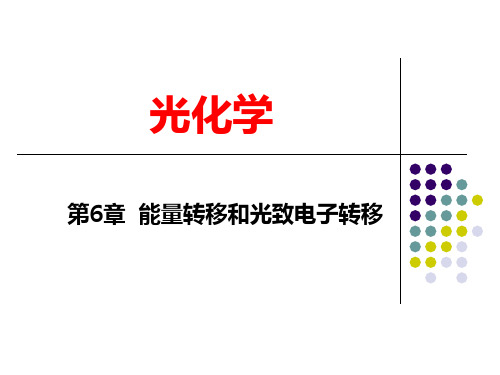
能量转移的可逆性
实际能量转移速率常数:
D hv D A
A *
k ET k ET
D A*
kiD D
kiA A
A i
k
ob ET
kET ET
k kET ( A ) ki k ET [ D]
在溶液中的能量转移
在溶液中的能量转移更多的是通过电子交换机 制进行的 。过程如下:
三重态敏化剂的性质
(1)强的吸光能力;
(2)高的系间串越量子产率φst; (3)较高的三重态能量; (4)较长的三重态寿命; (5)敏化剂的吸收光谱与受体吸收光谱重叠小; (6)化学惰性。
三重态猝灭剂的性质
(1)小的吸光能力; (2)低的三重态能量; (3)短的三重态寿命; (4)化学惰性。
敏化剂一般可以用作猝灭剂,
k kD kq [Q]
ob D
1
Sen hv Sen Sen A Sen A
3 3
三重态敏化剂的光物理性质
化合物 丙酮 苯乙酮 二苯酮 ES
355.6 330.5 313.8
ET
326.4 309.6 288.7
△E
29.2 20.9 25.1
τs
τT 10-5
电子组态
ket kJe
2R L
(2) Ket与受体的吸光性能无关; (3)介质黏度显著影响能量转移; (4)能量转移过程遵循Winger自旋守恒规则。
6.3.3 通过化学键的能量转移
结构特点:给体与受体通过钢性桥联结起来。
O
C
n
通过化学键的能量转移
O
CH3
C
电子转移的表示方法

BIG DATA EMPOWERS TO CREATE A NEW
ERA
• 电子转移基本概念 • 箭头表示法 • 曲线表示法 • 符号表示法 • 数值表示法 • 实例解析与应用探讨
目录
CONTENTS
01
电子转移基本概念
BIG DATA EMPOWERS TO CREATE A NEW
发展具有推动作用。
02
箭头表示法
BIG DATA EMPOWERS TO CREATE A NEW
ERA
箭头方向规定
在化学反应中,箭头的方向通常指向电子流动的方向,即从 电子供体指向电子受体。
在电化学中,箭头的方向通常指向电流的方向,即从正极指 向负极。
箭头使用场景
01
02
03
化学反应机理
在描述化学反应机理时, 箭头表示法可以清晰地展 示电子的转移路径和方向。
电化学过程
在描述电池、电解池等电 化学过程时,箭头表示法 可以表示电流的流动方向 和电子的转移情况。
物理化学过程
在描述光化学反应、氧化 还原反应等物理化学过程 时,箭头表示法也可以用 来表示电子的转移。
箭头优缺点分析
优点
直观性:箭头表示法能够直观地展示电子 的转移路径和方向,便于理解和记忆。
简洁性:相比于其他表示方法,箭头表示法更 加简洁明了,不会引入过多的符号和标记。
原子或分子吸收能量后,电子从原子 或分子中逸出,形成带正电荷的离子。
电子转移意义
电子转移是化学反应的基础, 对于理解化学反应的机理和本
质具有重要意义。
电子转移过程伴随着能量的 吸收和释放,对于研究化学 反应的热力学和动力学性质
具有重要意义。
现代光化学-6-能量转移和光致电子转移
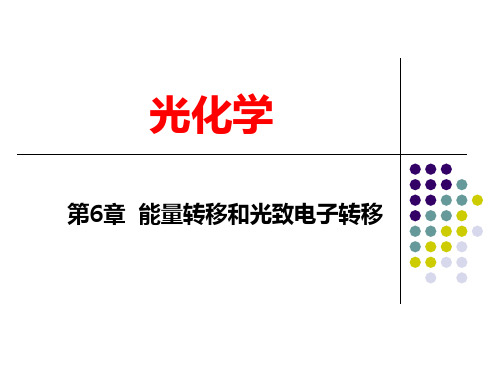
kst k p kET [ A]
p [T1]
kst k p
1
kET
(
kst
1
kp
)[
A]
1
k ET T
[
A]
Stern-Volmer 方程
三重态-三重态能量转移
当存在能量转移时,给体三重态寿命:
e T
kp
kts
1
kET [ A]
1
e T
kp
kts
kET
6.3.2 无辐射的能量转移
无辐射的能量转移过程不是光的发射与吸收, 可以表示为:
D* A (D*... A) D A*
波函数表示:
i (D*)( A) (D)( A*) f
两个状态之间跃迁的速率常数:
ket i | H | f i | He | f i | Hc | f
单重态-单重态的能量转移
对于单重态-单重态的能量转移,辐射机制、 共振机制和电子交换机制都是允许的。
D*(S1) A(S0 ) D(S0 ) A*(S1)
单重态-单重态的能量转移
S1 f
kET ISC
IC
T1
S1 ISC
f
IC
T1
S0 D
S0 A
f
(D)
kf
kic
kf kst
kET [ A]
给体发射的量子产率φe; D*与A发生作用的距离L和[A]; 受体A的吸光能力εA;
D*的发射光谱与A的吸收光谱的重叠程度J。
J 0 IDdv
辐射机制能量转移发生的概率
P
[ A]L e
0 ID dv
辐射能量转移的特点
可以使给体的发射光谱发生改变; 能量转移过程不影响给体的辐射寿命; 能量转移速率常数不依赖与介质的黏度; 一般为单-单或三-单过程; 能量转移效率受容器大小和形状的影响。
光化学——电子转移

• ]]]\]
光诱导电子转移的应用
一、模拟光合作用 自然界的光合作用过程能够非常高效的转化和
存储太阳光能量。光合作用中最重要的光能转换 过程是通过原初反应和电荷稳定过程实现的。原 初反应电荷分离产生高化学活性的正、负离子自 由基分别推动一系列电子转移的氧化还原反应。 因此原初电荷分离过程是光系统实现光能转换为 化学能的关键。大量的模拟工作都是围绕光合作 用反应中心的电荷分离过程,试图在人工模拟体 系中得到长寿命的电荷分离态。
图3
更直观地描述了溶液中电子转移反应的不同 过程。首先激发态分子或与基态分子或在溶 液中碰撞形成相遇络合物。
这种络合物可以直接发生电子转移而生成溶 剂隔离离子对(SSIP) ,也可以先生成激基复 合物再发生电子转移生成紧密离子对(CIP) 其中中,经过SSIP正负电荷 分离并扩散生成自由的正负离子自由基, 但是多数情况下,电子转移生成的紧密离 子对或溶剂隔离离子对还没来得及分开, 热力学允许的电子回传就在短距离内快速 地发生了,又回到了给体和受体的基态从 而浪费了能量。
一个激发的分子与其基态相比通常是一 个更好的电子供体(Donor)或者电子受体 (Acceptor),通过电子的转移,它会“敏化” 或者永久改变其邻近分子的化学物理性质。
电子转移的分类
典型的 PET 体系是由三部分组成 包含电子给体(D)的主体分子 通过一间隔基 B(或是桥基) 和电子受体(A)相连而成。
体系吸收光后,既可以是 D 被激发,也 可以是A被激发。如果D被激发,生成D*A,D的 HOMO 轨道上的一个电子将被提升到 LUMO轨道。
如果 A 被激发,情况完全一样,只不过 这时要求 D 的 HOMO 轨道能级高于 A。相应 轨道的能级。
总之,无论 D 和 A 谁被激发,最后都能 得到电荷分离的 D+A-态。D+A-态是不稳定 的,其 LUMO 轨道上的电子将会跃迁回 HOMO 轨道,从而发出荧光,体系回到基 态。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
当 DBA 体系吸收光发生激发后,其电荷要 重新分布,导致了分子在基态和激发态时 的光吸收和发射、反应活性、氧化还原性 质等方面的差异。
光诱导电子转移基本理论 目前,光诱导电子转移基本理论主要上有两种:
一是直接以反应自由能变化值ΔG0的正负直接判断电子转移
反应能否发生的能否发生的Rehm-Weller方程
二是以电子转移反应的活化能和自由能的相对大小来判断电
子转移反应能否发生的Marcus理论。
1956年,Marcus提出了电子转移反应 理论。该理论认为:电子转移反应速率取 决于电子给体与电子受体间的距离,反应 自由能的变化以及反应物与周围溶剂重组 能的大小,电子转移速率常数可表示为:
一个激发的分子与其基态相比通常是一 个更好的电子供体(Donor)或者电子受体 (Acceptor),通过电子的转移,它会“敏化” 或者永久改变其邻近分子的化学物理性质。
电子转移的分类
典型的 PET 体系是由三部分组成 包含电子给体(D)的主体分子 通过一间隔基 B(或是桥基) 和电子受体(A)相连而成。
FRET在生物学上的应用
荧光共振能量转移(FRET)(Fluorescence / Förster resonance energy transfer) 是比较分子间距离与分子直径的有效工具, 广泛用于研究各种涉及分子间距离变化的 生物现象, 可以定量测量两个发光基团之间的距离, 在蛋白质空间构象、蛋白与蛋白间相互作 用、核酸与蛋白间相互作用以及其它一些
• ]]]\]
光诱导电子转移的应用
一、模拟光合作用 自然界的光合作用过程能够非常高效的转化和
1992年10月14日瑞典皇家科学院宣布1992年诺贝 尔化学奖授予美国加州理工学院Rudolph A.Marcus教授,以表彰1956—1965年期间他在 “电子转移过程理论”方面所作出的重要贡献。
光诱导电子转移(PET)是光化学的一 个重要分支,它是研究光激发分子作为强 氧化剂和强还原剂的化学物理性质的一门 学科。
体系吸收光后,既可以是 D 被激发,也 可以是A被激发。如果D被激发,生成D*A,D的 HOMO 轨道上的一个电子将被提升到 LUMO轨道。
如果 A 被激发,情况完全一样,只不过 这时要求 D 的 HOMO 轨道能级高于 A。相应 轨道的能级。
总之,无论 D 和 A 谁被激发,最后都能 得到电荷分离的 D+A-态。D+A-态是不稳定 的,其 LUMO 轨道上的电子将会跃迁回 HOMO 轨道,从而发出荧光,体系回到基 态。
电子转移理论模型的示意图。从图中可以看出
Marcus曲线分为三个区域,且各个区域与电子转 移的机理密切相关:
-ΔG<λ:ΔG0越负,ΔG*越小,相应的电子转移 速率越大,属于Marcus正常区; -ΔG≈λ: ΔG*最小为零,相应的电子转移速率最 大;
-速Δ率G>越λ :小,ΔG属0于越反负转,区ΔG。*越大,相应的电子转移
Байду номын сангаас
式中:
ΔG0为电子转移反应的自由能变化值; λ为电子转移前后电子给体与受体的内部结 构以及周围溶剂分子的取向调整所需要的 重组能;
HDA为电子转移前后的电子轨道偶合常数, 一般取决于电子给体和受体的中心距离而 与介质的性质无关。
通过对电子转移反应速率的研究,推出一
个极为简单的公式,可用以描述电子转移 反应活化能G*与反应中自由能变化ΔG0以 及总的重组能λ之间的关系:
第五章 电子转移
电子转移是最基本和最重要的化学反应 之一。它在物理学(半导体,显微扫描技 术)、合成(光)化学、分子生物学 (DNA 的降解与修复,酶催化等)、超分 子化学、材料科学以及显像技术等领域扮 演着极为重要的角色。
大半个世纪以来,人们对电子转移反应进 行了卓有成效的实验和理论研究。在过去的 二十多年,诺贝尔化学奖被多次授予给从事 电子转移相关工作的科学家,这不仅反映了 电子转移在这些领域中的突出地位和重要作 用,而且也说明它巨大的科学和实用价值。
1983年授予H.Taube的诺贝尔化学奖,表彰他在 无机化学体系中氧化还原反应机制的开创性研究;
1988年由H.Michel,J.Deisenhofer及R.Huber共 享,诺贝尔化学奖表彰他们在阐明细菌光合作用 反应中详细机理方面的贡献,而这一过程所涉及 的机制也与光诱导的电子转移过程相关。
方面的研究中得到广泛应用。
J(λ)表示光谱重叠积分
FRET的应用: ⑴、可用于研究蛋白质以及蛋白复合体的结构和 空间构象与布局
⑵、研究蛋白质的折叠 蛋白质折叠是一个非常繁杂的过程,因为它涉及 到大量的途径来将无数去折叠构象连接成为唯一 的天然构象。在用实验方法来探索各个途径所占 比例的漫长过程中,FRET已经能够测量自由状态 的单分子蛋白折叠的表面自由能特征,这些数据 在其他方法是难以得到的。
图3
更直观地描述了溶液中电子转移反应的不同 过程。首先激发态分子或与基态分子或在溶 液中碰撞形成相遇络合物。
这种络合物可以直接发生电子转移而生成溶 剂隔离离子对(SSIP) ,也可以先生成激基复 合物再发生电子转移生成紧密离子对(CIP) 其中SSIP和CIP相互平衡
在强极性溶剂中,经过SSIP正负电荷 分离并扩散生成自由的正负离子自由基, 但是多数情况下,电子转移生成的紧密离 子对或溶剂隔离离子对还没来得及分开, 热力学允许的电子回传就在短距离内快速 地发生了,又回到了给体和受体的基态从 而浪费了能量。
当分子被激发后,它处于高能且不稳定状 态,很容易失活重新回到基态。
光化学反应过程
所有的光化学反应都是从基态分子吸 收光子开始的。当基态分子吸收可见或者 紫外光后,处于最高占据轨道(HOMO)上的 电子就将跃迁到具有更高能级的空轨道 (LUMO+n,n=1,2,3…)上。
电荷分离态的实现
将 D 和 A 连接起来构成超分子,假定 D 和 A 之间耦合很小(如图 )。
