2009年四川大学无机化学考研真题-考研真题资料
2009年315化学农考研真题

8.配位滴定中, Fe 、 Al 对铬黑 T 有 A.僵化作用 C.沉淀作用 B.氧化作用 D.封闭作用
3+
3+
,则反应 C= 9.等温等压下,已知反应 A=2B 的 r H m (1)及反应 2A=C 的 r H m (2) 4B 的 r H m 为 A.2 r H m (1)- r H m (2) B. r H m (2)-2 r H m (1) C. r H m (1)+ r H m (2) D.2 r H m (1)+ r H m (2) 10.某有色物质溶液,测得其吸光度为 A1,第一次稀释后测得吸光度为 A2,再稀释一次, 测得吸光度为 A3,已知 A1-A2=0.500,A2-A3=0.250。透光度比值 T3 /T1 应为 A.5.62 B.5.16 C.3.16 D.1.78
5.测得某种新合成有机酸的 p K a 为 4.35,其 K a 为 A.4.467×10-5 C.4.5×10-5
B.4.47×10-5 D.5×10-5
2
6.Mg OH 2 和 MnCO3 的 Ksp 数值相近, 在 Mg OH 2 和 MnCO3 两份饱和溶液中 Mg 和 Mn
-1
15.电势分析中,pH 玻璃电极的内参比电极一般为 A.标准氢电极 B.Ag-AgCl 电极 C.铂电极 D.银电极 16.化合物 与 HBr 反应,生成的主要产物是
17.化合物
的构型是
A. 2 R,3S
B. 2 S , 3S
C. 2 R , 3 R
D. 2 S , 3R
18.下列化合物中,取代基与苯环形成 p 共轭体系的是 A.氯苯 B.氯化苄 C.苯甲酸 D.苯磺酸 19.苯乙醛与甲醛在稀碱作用下加热生成的主要产物是
18最近几年无机考研真题

近几年来某些综合大学无机化学考研试题汇编复旦大学无机化学考研试题汇编一完成并配平以下反映式:1 BrO3- + XeF2 + H2O →2 SnS + (NH4)2S2 →3 BF3 + H2O →4 K2MnO4 + H2O →5 FeC2O4→6 [Co(NH3)6]2+ + O2 + H2O →7 BF3 + LiAlH4 →8 Pb(OH)3- + ClO- →9 Bi(OH)3 + Cl2 + NaOH →10 XeO3 + O3 + H2O →11 (NH4)2Cr2O7 →12 CaCO3 + H2O + Cl2→13 Pb3O4 + HCl →14 NH3 + CO2 →15 Zn + NH3 + H2O →二用反映式表示以下制备进程,注明必要反映条件及步骤,辅助原料自选。
1 以为NaNO3要紧原料制备NaNO2;2 以SO2,NaOH,锌粉为原料制备保险粉;3 由CuCl2制备CuCl;4 利用配体取代反映制备cis-[PtCl2(NH3)2]。
可供选择的原料为[Pt(NH3)4]SO4、Na2[PtCl4]、NH3、NH4Cl,说明选择原料的依据;5 以H3PO4和NaOH为原料制备三聚磷酸钠;6 以粗硅为原料制取超纯硅;7 以Ba(IO3)2为原料制备偏高碘酸;8 试举两例实验室制备CO的合理方式。
三简答题:1 什么缘故硼砂(Na2B4O5(OH))溶液具有缓冲作用?2 如何制取纯HD?(D=21H)3 锝在周期表中处于什么位置?写出锝最高氧化态的含氧酸的分子式。
4 稀土元素的离子和化合物的颜色主若是由什么引发的?稀土元素作为优良磁性材料的依据是什么?5 多硼烷中可能存在哪几种类型的化学键?丁硼烷(B4H10)中有哪几种类型的化学键?6 写出[PtCl2(NO2)(NH3)(en)]Cl的名称,并画出内界可能的几何异构体。
7 如何说明NH3是Lewis碱而NF3却不具有Lewis碱性?8 何谓沸石分子筛?以人工合成A型分子筛为代表,讨论它们的组成、结构、性质和应用。
张祖德《无机化学》(修订版)配套题库名校考研真题碱金属和碱土金属【圣才出品】

第11章氢、碱金属和碱土金属一、选择题1.将NaH放入H2O中,可得到()。
[华南理工大学2016研]A.NaOH、H2、O2B.NaOH、O2C.NaOH、H2D.Na2O2、H2【答案】C2.下列氢化物中,在室温下与水反应不产生氢气的是()。
[华南理工大学2015研]A.NaBH4B.CaH2C.PH3D.SiH4【答案】C【解析】A项,NaBH4+2H2O=NaBO2+4H2↑;B项,CaH2+2H2O=Ca(OH)2+2H2↑;D项,SiH4+3H2O=H2SiO3↓+4H2↑。
C项,PH3与水不发生反应。
3.从锂到铯,单质熔点的变化规律是()。
[华南理工大学2015研]A.由低到高B.由高到低C.两边低中间高D.没有规律【答案】B4.下列各物质中,熔点最低的是()。
[华南理工大学2015研]A.LiClB.BeCl2C.NaClD.BaCl2【答案】B5.盛Ba(OH)2溶液的瓶子在空气中放置一段时间后,内壁蒙上一层白色薄膜,欲除去这层薄膜,最合适的洗涤溶液是()。
[北京交通大学2014研]A.硫酸溶液B.水C.氢氧化钠溶液D.盐酸溶液【答案】D【解析】盛Ba(OH)2溶液的瓶子在空气中放置一段时间后,Ba(OH)2可以吸收空气中的CO2,从而生成难溶的BaCO3,使其内壁蒙上一层白色薄膜。
D项,BaCO3可溶于HCl,反应如下:32222BaCO HCl BaCl H O CO +=++↑6.钙在空气中燃烧所得到的产物之一用水润湿后,所放出的气体是()。
[北京科技大学2012、2014研]A.O 2B.N 2C.NH 3D.H 2【答案】C 【解析】钙在空气中燃烧可发生反应:3Ca+N 2→Ca 3N 2。
其燃烧产物用水润湿后,反应:()32232632Ca N H O Ca OH NH →↑++7.和水反应得不到H 2O 2的是()。
[厦门大学2013研]A.K 2O 2B.Na 2O 2C.KO 2D.KO 3【答案】D 8.下列物质中碱性最强的是()。
2009河北师大考研真题——无机化学

专业名称 无机化学 物理化学 考试科目 无机化学 *考生必须将答案写在答题纸上,试题纸上答题无效。
(允许考生用计算器)一、单向选择题(本题共40分,每小题2分)1.对于A ,B 两种混合气体,下列公式中不正确的是 ( )A. p 总V 总= n 总RTB. p A V A = n A RTC. p 总V A = n A RTD. p A V 总= n A RT2.下列物质固化时,形成分子晶体的是 ( )A. CO 2B. NaBrC. FeD. Si3.AgCl 的溶度积常数为K sp , [Ag(CN)2]-的稳定常数是K 稳,则:AgCl(s)+2CN [Ag(CN)2]-+Cl -的平衡常数K 等于 ( )A. K spB. K spC. K sp /K 稳D. K sp ·K 稳4.下列氟化物分子中,分子的偶极矩不为0的是 ( )A .PF 5B .BF 3C .IF 5D .XeF 45.已知 ϕ(Ni 2+/Ni)=-0.23V , ϕ(Zn 2+/Zn)=-0.7628V ,则在标准状态下反应 Zn 2++ Ni =Zn + Ni 2+ 自发进行的方向是 ( )A .向左B .向右C .不能确定D .维持现状,保持平衡6.对热力学系统的变化过程,下列物理量的变化值与变化途径有关的是( )A .UB .HC .TD .W7.在一定条件下,一个反应达到平衡的标志是 ( )A. 各反应物和生成物的浓度相同B. 0f m G ϑ∆=C. 各物质浓度不随时间改变而改变D. 正逆反应速率常数相等8.0.4 mol/L HAc 溶液中H +浓度是0.1 mol/L HAc 溶液中H +浓度的 ( )倍A. 1B. 2C. 3D. 49.配合物[Pt(NH 3)2Cl 2]的磁矩为0,有2种异构体,Pt 的杂化方式为( )A .sp 3B . dsp 3C . dsp 2D . d 2sp 310.下列分子或离子的键长比较结果正确的是( )A. 22O O +>B. 22O O -<C. 22N N +>D. 22N N +<11.下列各套量子数中,不合理的一组是 ( )A .(3 1 +2 +1/2)B .(2 1 +1 +1/2)C .(2 1 –1 –1/2)D .(3 2 –1 –1/2)12.设AgCl 在H 2O 中、在0.01mol/L 的CaCl 2中、在0.01mol/L NaCl 中、在0.01mol/L KNO 3中、在0.05mol/L AgNO 3中的溶解度分别为S 0、S 1、S 2、S 3、S 4。
【内部资料】四川大学2009年研究生考试录取统计
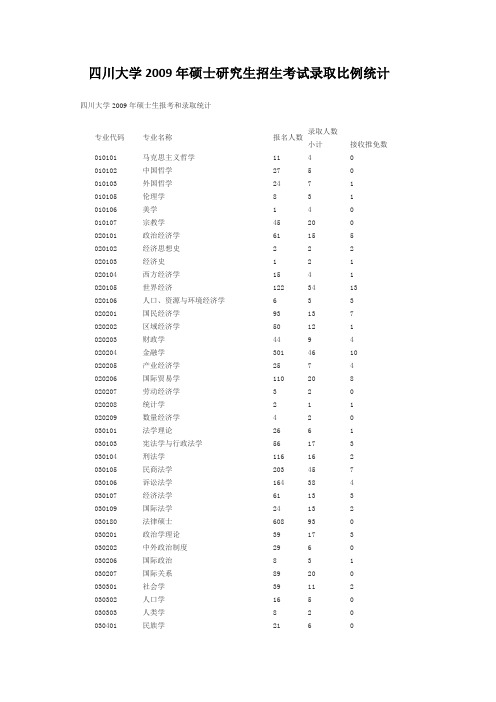
四川大学2009年硕士研究生招生考试录取比例统计四川大学2009年硕士生报考和录取统计专业代码专业名称报名人数录取人数小计接收推免数010101 马克思主义哲学11 4 0 010102 中国哲学27 5 0 010103 外国哲学24 7 1 010105 伦理学8 3 1 010106 美学 1 4 0 010107 宗教学45 20 0 020101 政治经济学61 15 5 020102 经济思想史 2 2 2 020103 经济史 1 2 1 020104 西方经济学15 4 1 020105 世界经济122 34 13 020106 人口、资源与环境经济学 6 3 3 020201 国民经济学93 13 7 020202 区域经济学50 12 1 020203 财政学44 9 4 020204 金融学301 46 10 020205 产业经济学25 7 4 020206 国际贸易学110 20 8 020207 劳动经济学 3 2 0 020208 统计学 2 1 1 020209 数量经济学 4 2 0 030101 法学理论26 6 1 030103 宪法学与行政法学56 17 3 030104 刑法学116 16 2 030105 民商法学203 45 7 030106 诉讼法学164 38 4 030107 经济法学61 13 3 030109 国际法学24 13 2 030180 法律硕士608 93 0 030201 政治学理论39 17 3 030202 中外政治制度29 6 0 030206 国际政治8 3 1 030207 国际关系89 20 0 030301 社会学39 11 2 030302 人口学16 5 0 030303 人类学8 2 0 030401 民族学21 6 0030405 中国少数民族艺术12 3 3 030501 马克思主义基本原理35 11 1 030503 马克思主义中国化研究26 11 0 030505 思想政治教育64 14 0 040106 高等教育学72 10 0 040203 应用心理学223 18 4 040301 体育人文社会学11 3 0 040302 运动人体科学8 1 0 040303 体育教育训练学105 22 2 040304 民族传统体育学 2 2 0 050101 文艺学81 20 3 050102 语言学及应用语言学306 34 3 050103 汉语言文字学78 27 3 050104 中国古典文献学32 12 7 050105 中国古代文学188 25 3 050106 中国现当代文学165 27 4 050107 中国少数民族语言文学 5 0 0 050108 比较文学与世界文学160 31 9 050120 文艺与传媒31 4 0 050121 文化批评20 7 0 050122 文学人类学23 11 4 050123 佛教语言文学 5 6 0 050124 广播影视文艺学26 4 1 050201 英语语言文学242 45 11 050202 俄语语言文学7 5 2 050205 日语语言文学41 18 3 050211 外国语言学及应用语言学477 63 22 050301 新闻学286 45 8 050302 传播学313 51 9 050401 艺术学93 23 8 050403 美术学191 36 6 050404 设计艺术学261 36 13 060101 史学理论及史学史 4 1 0 060102 考古学及博物馆学51 13 5 060103 历史地理学25 4 0 060104 历史文献学14 4 0 060105 专门史52 11 2 060106 中国古代史49 16 3 060107 中国近现代史165 31 3 060108 世界史64 18 5 060123 中国儒学9 1 0 070101 基础数学121 31 12 070102 计算数学31 11 6 070103 概率论与数理统计34 9 6070104 应用数学26 4 1 070105 运筹学与控制论26 5 3 070120 不确定性处理的数学24 5 3 070121 信息安全22 5 3 070201 理论物理35 8 2 070202 粒子物理与原子核物理53 15 1 070203 原子与分子物理130 45 1 070205 凝聚态物理101 39 8 070207 光学165 39 5 070208 无线电物理12 6 2 070220 生物医学物理 3 2 0 070221 应用电子物理12 6 2 070222 高压科学与技术24 12 0 070301 无机化学29 10 1 070302 分析化学88 25 5 070303 有机化学115 38 11 070304 物理化学20 17 4 070305 高分子化学与物理30 16 5 070320 绿色化学32 11 0 070321 化学生物学30 26 2 071001 植物学93 30 5 071002 动物学23 12 1 071005 微生物学197 33 7 071007 遗传学104 37 7 071009 细胞生物学138 51 6 071010 生物化学与分子生物学189 54 7 071012 生态学20 9 4 071020 生物信息学27 4 0 071021 生物安全29 6 0 071022 结构生物学 1 0 0 077301 物理电子学23 10 2 077401 计算机系统结构23 4 1 077402 计算机软件与理论206 57 13 077403 计算机应用技术549 179 27 077501 环境科学197 38 4 080102 固体力学7 3 2 080103 流体力学 2 1 1 080104 工程力学 5 2 1 080201 机械制造及其自动化136 36 11 080202 机械电子工程21 9 8 080203 机械设计及理论52 24 13 080204 车辆工程12 2 0 080300 光学工程12 17 4 080401 精密仪器及机械13 5 3080402 测试计量技术及仪器33 10 3 080501 材料物理与化学40 24 4 080502 材料学238 100 26 080503 材料加工工程129 52 12 080520 高分子科学与工程148 50 5 080521 纳米材料与纳米技术18 8 1 080522 复合材料28 6 0 080601 冶金物理化学 1 1 1 080602 钢铁冶金7 5 1 080603 有色金属冶金7 4 3 080706 化工过程机械31 12 9 080801 电机与电器11 1 0 080802 电力系统及其自动化127 37 17 080803 高电压与绝缘技术 4 1 1 080804 电力电子与电力传动45 5 2 080805 电工理论与新技术33 5 1 080902 电路与系统51 22 4 080903 微电子学与固体电子学25 9 4 080904 电磁场与微波技术15 9 4 081001 通信与信息系统288 49 11 081002 信号与信息处理148 48 9 081101 控制理论与控制工程43 11 5 081102 检测技术与自动化装置34 10 4 081104 模式识别与智能系统19 15 4 081280 软件工程47 4 4 081302 建筑设计及其理论22 10 5 081303 城市规划与设计28 16 6 081304 建筑技术科学12 4 1 081401 岩土工程25 21 6 081402 结构工程51 16 12 081403 市政工程15 7 4 081501 水文学及水资源53 13 5 081502 水力学及河流动力学55 29 12 081503 水工结构工程73 20 8 081504 水利水电工程17 7 2 081505 港口、海岸及近海工程 3 1 0 081520 水电建设工程管理16 6 0 081521 城市水利与水安全 3 2 0 081701 化学工程43 14 3 081702 化学工艺115 37 6 081703 生物化工33 16 8 081704 应用化学62 25 6 081705 工业催化 4 3 0 081720 制药工程48 16 6081721 化工安全工程与技术9 4 2 082102 纺织材料与纺织品设计11 3 2 082103 纺织化学与染整工程8 5 1 082104 服装11 5 4 082203 发酵工程7 4 1 082204 皮革化学与工程21 21 8 082504 人机与环境工程 2 1 0 082703 核技术及应用9 5 1 082802 农业水土工程26 7 1 083001 环境科学 1 1 0 083002 环境工程76 18 7 083100 生物医学工程49 30 13 083120 医学信息工程 5 1 1 083201 食品科学43 13 8 090403 农药学16 5 1 090706 园林植物与观赏园艺50 15 3 090707 水土保持与荒漠化防治 6 2 1 097202 粮食、油脂及植物蛋白工程 1 0 0 097203 农产品加工及贮藏工程20 10 1 100101 人体解剖与组织胚胎学 4 4 0 100102 免疫学17 7 1 100103 病原生物学11 3 0 100104 病理学与病理生理学90 20 4 100105 法医学61 13 7 100120 医学生物化学及细胞生物学24 6 0 100121 医学神经生物学 1 0 0 100122 医学生理学与时间生物学15 3 0 100201 内科学414 72 8 100202 儿科学68 10 2 100203 老年医学20 6 0 100204 神经病学87 11 0 100205 精神病与精神卫生学57 6 1 100206 皮肤病与性病学76 7 0 100207 影像医学与核医学81 14 0 100208 临床检验诊断学27 8 2 100209 护理学110 12 4 100210 外科学480 64 3 100211 妇产科学208 26 3 100212 眼科学84 9 0 100213 耳鼻咽喉科学51 8 0 100214 肿瘤学103 27 3 100215 康复医学与理疗学13 2 0 100216 运动医学10 1 0 100217 麻醉学96 23 2100218 急诊医学12 2 0 100220 循证医学8 6 0 100221 移植科学与工程学7 5 5 100222 临床药物与器械评价科学 4 0 0 100223 眼视光学 6 2 2 100225 人类重大疾病生物治疗 4 2 1 100301 口腔基础医学8 14 1 100302 口腔临床医学331 77 0 100401 流行病与卫生统计学67 31 7 100402 劳动卫生与环境卫生学12 9 2 100403 营养与食品卫生学71 17 3 100404 儿少卫生与妇幼保健学11 3 1 100405 卫生毒理学 4 2 0 100420 健康与社会行为学11 4 1 100421 公共卫生检验学27 13 4 100602 中西医结合临床29 8 0 100701 药物化学101 36 6 100702 药剂学77 30 10 100703 生药学15 6 2 100704 药物分析学85 20 2 100705 微生物与生化药学9 4 0 100706 药理学59 25 5 100720 临床药学26 9 2 100721 药事管理学 4 1 0 100722 天然药物化学26 11 5 107200 生物医学工程25 28 1 120100 管理科学与工程131 37 15 120124 医院管理与卫生政策 4 3 3 120201 会计学182 27 9 120202 企业管理451 48 15 120203 旅游管理283 55 9 120204 技术经济及管理48 10 3 120280 工商管理硕士571 398 0 120401 行政管理447 93 2 120402 社会医学与卫生事业管理42 14 5 120403 教育经济与管理142 32 0 120404 社会保障164 54 4 120405 土地资源管理131 20 1 120501 图书馆学25 13 3 120502 情报学61 26 6 120503 档案学20 10 4。
2009川大数学分析及答案

四川大学2009年攻读硕士学位研究生入学考试题一、(每题7分,共28分)求下列极限1. ∑=∞→nk k nn Cn2ln 1lim解:定理(∞∞型Stolz 公式,数列极限)设}{n x 严格递增(即N n ∈∀,有1+<n n x x ),且+∞=∞→n n x lim . 若1)a x x y y n n n n n =----∞→11lim(有限数),则a x y nnn =∞→lim . 2)a 为∞+或∞-,结论任然成立. 因2n ↗∞+,用Stolz 公式1211ln lim 12ln lim )1(ln ln lim ln 1lim 00122010102+-++=+=-+-=∑∑∑∑∑=∞→=+∞→=+=+∞→=∞→n k n n n C C n n C C C n nk n nk kn k n n nk kn n k k n n n k k n n 12ln )1ln()1(lim12)1ln()1ln(lim 11+-++=+-+-+=∑∑∑+=∞→==∞→n kn n n k n n n k n nk n k n (再次用Stolz 公式)212)11ln(lim )12()12()ln ln (]ln )1ln()1[(lim111=+=--+---++=∞→=+=∞→∑∑nn n k n k n n n n k n n k n n2. )(sin lim 22n n n +∞→π 解:)111(sin )(sin )(sin 22222++=-+=+nn n n n n ππππ 初等函数在有定义的地方皆连续12s i n l i m )111(s i n l i m )(s i n l i m 2222==++=+∞→∞→∞→πππn n n nn n3. dtt t t dtt x x x ⎰⎰-+→0230)sin (sin lim 2解:x x x x x x x x x x x x x dt t t t dtt x x x x x x sin 2lim )sin ()(2)(sin lim )sin ()(sin 2lim )sin (sin lim 30232223202320002302-=-⋅=-=-++++→→→→⎰⎰1226lim cos 16lim 22020==-=++→→x x x x x x4. xx xe x x cos 11lim 0----→ 解:泰勒公式∑∞==++++++=032!!!3!21n nn xn x n x x x x e ,(+∞<<∞-x ) +----++--+-++=+!)]1([)2)(1(!3)2)(1(!2)1(1)1(2n n x x x ααααααααααα,(11<<-x )∑∞=-=+-+-+-+-=022642)!2()1()!2()1(!6!4!21cos n n n n n n x n x x x x x ,(+∞<<∞-x ) )](!4)(!2)(1[)(!2)121(21)(2111)(21lim cos 11lim 24222220x o x x x o x x xx o x x x x xe x x x ++--+-+-+--+++=----→→3)(24181)(2lim 222220-=+--+=→x o x x x o x x二、(每题10分,共40分)计算下列积分 (1)dxdy y x yx D⎰⎰--+222,其中}1:),{(222≤+∈=y x R y x D 解:2222)221()221(412----=--+y x y x y x 当),(y x 在41)221()221(22=-+-y x 内和上时0222≥--+y x yx ,记作1D ; 当),(y x 在41)221()221(22=-+-y x 外,且在122≤+y x 内时0222<--+y x y x ,记作2D 则dxdy y x yx dxdy y x y x I D D ⎰⎰⎰⎰--+---+=21)2()2(2222 2122222)2()2(2211I I d x d y y x y x d x d y y x y x I DD D D -=--+---+=⎰⎰⎰⎰=+ d x d y y x y x I D ⎰⎰--+=1)2(221 令θcos 221r x =-、θsin 221r y =- πθπ321)81(213201=-=⎰⎰dr r r d I d x d y y x yx I D⎰⎰--+=)2(222 令θcos r x =、θsin r y = πθθθπ21)2c o s s i n (1032202-=-+=⎰⎰dr r r d Iπ169221=-=I I I(2)ds yz l⎰,其中l 是球面2222a z y x =++与平面1=++z y x 的交线。
华南理工大学 华南理工2009年866无机化学 考研真题及答案解析

2. 试用杂化轨道理论说明PCl3(键角 101°)分子中心原子的杂化轨道类型及其成键 情况。(6 分) 3. 写出d4和d6构型的中心离子在八面体强场和八面体弱场中的电子排布式。(4 分)
二、填空 (每空 1 分,共 47 分)
1.在配制FeSO 4溶液时,常向溶液中加入一些 其目的是
和
,
。
2.变色硅胶中含有化合物
,其颜色由蓝变红是发生了反应:
。
3.向CrCl 3溶液中加入Na2CO 3溶液,产生的沉淀组成为
为
。
,沉淀的颜色
4.向K 2MnO 4溶液中不断通入CO 2,会发生
别是
和
。
(12 分)2. (1)在 20mL 0.10mol L-1MgCl2 溶液中,加入 10mL 0.2mol L-1 NH3·H2O溶
液,能否生成Mg(OH)2 沉淀?(2)若在原MgCl2 溶液中,先加入 1.069g NH4Cl(忽
略体积变化),然后再加入上述 10mL NH3·H2O溶液,能否生成沉淀?已知:Kb\ (NH3)
(A)PCl5 ; (B)BCl3 ; (C)CCl4 ; (D)SiCl4 。 27.欲除去CuSO4酸性溶液中的少量Fe3+离子,最好加入 (A)NH3·H2O ; (B)Na2S ; (C)Cu2 (OH) 2CO3 ; (D)Cu粉 。 28.AgNO3溶液与NaH2PO4溶液混合后生成的沉淀是 (A)Ag2HPO4 ; (B)Ag2O ; (C)AgH2PO4 ; (D)Ag3PO4 。 29.常温下以液态形式存在的化合物是 (A)TiOSO4 ; (B)TiCl4 ; (C)TiO2 ; (D)BaTiO3 。 30.下列化合物中,不为黄色的是 (A)BaCrO4 ; (B)PbCrO4 ; (C)Ag2CrO4 ; (D)PbI2 。 31.在FeCl3与KSCN的混合液中加入过量NaF,其现象是 A)变为无色 ; (B)产生沉淀 ; (C)颜色加深 ; (D)无变化 。 32.下列新制备的沉淀中在空气中放置,颜色不发生变化的是 (A)Mn(OH) 2 ; (B)Fe(OH)2 ; (C)Co(OH) 2 ; (D)Ni(OH) 2 。
四川大学考研真题2009年环境科学

四川大学
2009年攻读硕士学位研究生入学考试试题考试科目:环境学导论
考试代码:838#
适用专业:环境科学环境资源
一名词解释(每题4分,共40分)
热岛效应食物网环境污染危险废弃物适度人口
VOCS Leq BaP PM2.5 CFCS
二简答题(每题10分,共50分)
1,简述生态系统的组成?
2,目前世界上土地资源退化和减少的主要原因有哪些?
3,森林生态系统在生物圈中有哪些主要作用?
4,请分析矿业开发对环境的影响有哪些?
5,农药污染物的主要特点及其产生的主要环境问题有哪些?
三问答题(第1 2 题每题25分,第三题10分,共60分)
1,试从外部性理论的观点出发,举例并分析说明环境恶化的经济原因?
2,什么是生态城市?生态城市应该满足什么要求?我国目前正在开展全国的生态市建设规划活动,这是科学发展观在城市规划与建设中的体现。
请你从环境科学专业角度分析生态城市建设中如何处理好经济发展,社会进步与生态环境保护的关系。
3,喜鹊曾是各地最常见的鸟类之一,广布与各市,县,乡镇的山林,田园,城镇,是人们熟悉的一种留鸟。
喜鹊是杂食性的鸟类,又常在耕地,菜园,果园中觅食,喜欢将巢筑在高大的乔木上。
但从上个世纪70年代末在现在,短短二十多年,喜鹊就在四川盆地中消失了。
进入90年代四川盆地已成为喜鹊的罕见地,盆周山地,川西南山地为部分布区,川西高原为广布区。
喜鹊消失地域占四川总面积的三分之一。
从生态学的角度讲,鸟类是生态环境变化最敏感的指示者,鸟类数量的变化,对生态环境监测与保护和可持续利用,意义重大。
请你总结生态环境的可能变化分析喜鹊种数数量变化的可能原因。
名校无机化学历年考研真题汇总

三 简答题:
1 B4O5(OH)42- + 5H2O == 2H3BO3 + 2B(OH)4-.水解产生的酸(H3BO3)和碱(B(OH)4-)能够抵抗 外来少量碱和酸,故具有缓冲作用。
2 NaH + D2O == NaOD + HD↑ 3 第五周期,ⅦB 族,HTcO4。 4 f-f 跃迁,核外不成对电子多,以及电子轨道磁矩对顺磁性的贡献。
为例,写出它们在酸性溶液中与氧气反应的方程式。
14 镧系元素位于周期表的什么位置?填写下表:
ⅡA 族 ⅢB 族 ⅣB 族
周期 5
周期 6
镧
周期 7
15 指出下列分子或离子的几何构型及中心原子的杂化态:
BF4- 2 TeF4 3 BrF4- 4 XeOF4 5 ClO3F 6 Fe(CO)5 7 IOF3 8 Cu(H2O)42+
10 H2SO2, H2SO3, H2SO5, H2S2O3, H2S2O4, H2S2O5, H2S2O6, H2S2O7, H2S2O8. 次硫酸 亚硫酸 过一硫酸 硫代硫酸 连二亚硫酸,焦亚硫酸 连二硫酸 焦硫酸,过二硫酸
3
11 (1) 紫红色;
(2) △0=20300cm-1; (3) 由于 John-Teller 效应,使激发态 2eg 谱项分裂成 2 个能级的缘故。 12 NH3和 N(CH3)3 结构相似,均为三角锥形,但三甲硅胺却为平面三角形。因为除形成σ键外, 每个硅原子的 3d 空轨道能与 N 的孤对电子占据的 p 轨道相互重迭,形成π42 键,因而平
β笼构成更大的α笼。由于这些笼具有一定的孔径和孔体积,以及笼内的静电作用,可
四川大学《939生物化学与分子生物学(自主命题)》历年考研真题专业课考试试题

二、选择题(20个,每个2分,40分) 1 由三脂酰甘油(TG)、磷脂酰丝氨酸(PS)和磷脂酰胆碱(PC) 组成的一个脂混合物被注入一个硅胶柱子,并用极性逐渐增强的溶剂进 行洗脱他们从柱子上洗脱下来的先后次序为( )。 A.TG→PS→PC
3 谷氨酸脱氢酶依赖于( )存在,才能催化谷氨酸-α-酮戊二酸。 A.NAD+或NADP+ B.FAD或FMN
C.磷酸吡哚醛 D.CoA
2014年四川大学939生物化学考研 真题
2015年6年四川大学939生物化学考研 真题
2015年四川大学939生物化学考研真题 2016年四川大学939生物化学考研真题 2017年四川大学939生物化学(自主命题)考研真题
1998年四川大学生物化学考研真 题
1999年四川大学生物化学考研真 题
2000年四川大学生物化学考研真 题
2001年四川大学345生物化学考研 真题
6 水合茚三酮
2013年四川大学939生物化学考研 真题(部分)
一、名词解释(5个,每个3分,15分) 1 Super-secondary structure (Motif) of protin
2 Northern blot
3 Ploycistronic Mrna
4 Suicide substrate
目 录
1998年四川大学生物化学考研真题 1999年四川大学生物化学考研真题 2000年四川大学生物化学考研真题 2001年四川大学345生物化学考研真题 2002年四川大学345生物化学考研真题 2005年四川大学439生物化学考研真题 2006年四川大学439生物化学考研真题 2007年四川大学439生物化学考研真题 2008年四川大学939生物化学考研真题 2009年四川大学939生物化学考研真题 2010年四川大学939生物化学考研真题 2011年四川大学939生物化学考研真题(回忆版) 2012年四川大学939生物化学考研真题(部分) 2013年四川大学939生物化学考研真题(部分) 2014年四川大学939生物化学考研真题
无机化学610考研真题

无机化学610考研真题无机化学610考研真题是考研复习中的重要内容之一。
无机化学作为化学科学的一个重要分支,研究非有机物质的结构、性质和变化规律,对于理解化学反应机理和开发新材料具有重要意义。
下面将从考研真题的特点、备考方法以及相关知识点的重点梳理等方面进行探讨。
一、考研真题的特点无机化学610考研真题的特点主要体现在以下几个方面:1. 考查知识点广泛:无机化学作为化学的一个重要分支,涉及的知识点较多。
考研真题往往涵盖了无机化学的各个方面,如元素周期表、配位化学、晶体结构等。
2. 题目形式多样:无机化学610考研真题的题目形式多样,不仅有选择题,还有填空题和简答题等。
这些题型要求考生对知识点的理解和应用能力都有一定的要求。
3. 难度适中:无机化学610考研真题的难度适中,既有基础知识的考查,又有对知识点的综合运用和拓展。
二、备考方法备考无机化学610考研真题需要掌握一定的备考方法,以下是一些建议:1. 熟悉考纲:无机化学610考研真题的考纲是备考的重要依据,要认真研读考纲,了解考试的重点和难点。
2. 系统学习:无机化学是一个系统性的学科,备考时要注重系统学习,掌握各个知识点之间的联系和应用。
3. 多做真题:做真题是备考的重要环节,可以通过做真题来熟悉考试的题型和难度,同时也可以检验自己的学习成果。
4. 总结归纳:在做真题的过程中,要注意总结归纳,将做错的题目进行分析和总结,找出自己的不足之处,并加以改进。
三、重点知识点梳理无机化学610考研真题中的重点知识点主要包括以下几个方面:1. 元素周期表:要熟悉元素周期表的组成和结构,掌握各个元素的周期性规律和性质。
2. 配位化学:要了解配位化学的基本概念和原理,掌握配位化合物的构成和性质。
3. 晶体结构:要熟悉晶体结构的基本概念和分类方法,了解晶体的各种结构类型和性质。
4. 化学键:要掌握化学键的形成和性质,了解离子键、共价键和金属键等不同类型的化学键。
考研无机化学真题

考研无机化学真题2019年考研无机化学真题如下:1. 选择题(1) 无机化合物N2O3属于()。
A. 氮的+3氧化态的氮酸B. 氮的+2氧化态的氮亚酸C. 氮的+2氧化态的氮酸D. 氮的+3氧化态的氮亚酸(2) AgNO3和HCl反应生成了沉淀,沉淀是()。
A. AgClB. Ag2ClC. AgCl2D. AgCl3(3) 三氧化二铝是以氧为配体的配合物,其配位数为()。
A. 2B. 3C. 4D. 6(4) Na2CO3可以与化合物BaCl2反应生成沉淀,沉淀是()。
A. BaCO3B. NaClC. Na2CO3·BaCl2D. NaCl·BaCO32. 判断题(1) [Fe(CN)6]4-是一种低自旋配合物。
()(2) 双层结构钢产生腐蚀主要是由于内外两层金属化学成分不一样所引起的。
()(3) 锌是稀有金属。
()(4) 在分子能级理论中,电子的位置和动量可以同时确定。
()(5) 硝酸盐是碱性氧化物。
()3. 简答题(1) 分析并解释程序升温炉在实验室中的应用。
答:程序升温炉是一种常见的实验设备,主要用于在实验室中进行物质的热处理和热分析。
它的主要特点是能够精确控制温度和温度升降速率,使得实验结果更加准确可靠。
程序升温炉广泛应用于材料研究、催化剂制备、无机合成等领域。
(2) 解释化学键的概念,并以氯化钠为例说明离子键和共价键的特点。
答:化学键是由原子之间相互作用而形成的一种连接方式。
离子键是指电子从一个原子转移到另一个原子,形成正负离子相互吸引而形成的化学键。
氯化钠是由钠离子和氯离子通过离子键连接而成的。
离子键的特点是电子的转移和电荷的不平衡。
共价键是两个原子通过电子共享而形成的化学键。
氯化钠中氯原子与钠原子通过共价键连接。
共价键的特点是电子共享和电荷平衡。
通过以上的例子,可以看出离子键和共价键的特点是不同的,离子键中电子转移导致电荷的不平衡,而共价键中电子共享导致电荷的平衡。
四川大学884化工原理历年考研真题汇编

目 录2013年四川大学884化工原理考研真题
2012年四川大学884化工原理考研真题
2011年四川大学884化工原理考研真题
2010年四川大学884化工原理考研真题
2009年四川大学884化工原理考研真题
2008年四川大学884化工原理考研真题
2007年四川大学884化工原理考研真题
2006年四川大学884化工原理考研真题
2005年四川大学884化工原理考研真题
2004年四川大学884化工原理考研真题
2003年四川大学874化工原理考研真题
2002年四川大学587化工原理考研真题
2013年四川大学884化工原理考研真题
2012年四川大学884化工原理考研真题
2011年四川大学884化工原理考研真题
2010年四川大学884化工原理考研真题
2009年四川大学884化工原理考研真题
2008年四川大学884化工原理考研真题
2007年四川大学884化工原理考研真题
2006年四川大学884化工原理考研真题
2005年四川大学884化工原理考研真题
2004年四川大学884化工原理考研真题
2003年四川大学874化工原理考研真题
2002年四川大学587化工原理考研真题。
无机化学考研真题及答案

无机化学考研真题及答案(a) nano2和h2o(b) nano2,o2和h2o (c) nano3,n2o5和h2o (d) nano3,nano2和h2o 15. 2 分(1460)下列硫化物,能溶于na2s溶液生成硫代酸盐的是…………………………()(a) sns(b) sns2 (c) pbs(d) bi2s3二、填空题( 共12题30分) 16. 5 分(7452)n2o3很容易分解为和。
将棕黄色的no2冷却到0℃左右,它几乎全部转变为色的。
经x射线衍射研究,证明固体n2o5含有两种离子。
17. 5 分(1410)ncl3的水解产物是________________________和____________________;pcl3的水解产物是________________________和_____________________;sbcl3的水解产物是________________________和_____________________;bicl3的水解产物是________________________和_____________________;ascl3的水解产物是________________________和_____________________。
18. 2 分(4402)i2和cl2在碱性介质中的反应方程式是_________________________________。
i2和h2o2的反应方程式是________________________________________。
19. 2 分(7357)bn是一种重要的无机材料,六方bn与晶体结构相似,但它是无色的绝缘体,在高温、高压下,六方bn可以转变为立方bn,此时它与晶体结构相似。
20. 2 分(1477)h3bo3是极弱的一元酸,在定量分析中不能直接用强碱滴定,如果加一定量的_____________________,生成_________________________后,因酸性大为增强,则就可滴定了。
考研《无机化学》考研真题考点归纳一

考研《无机化学》考研真题考点归纳一无机化学考点归纳与典型题(含考研真题)详解(上册)第1章物质的状态1.1考点归纳一、气体1.气体的两个基本特性气体具有扩散性和可压缩性。
主要表现在:(1)气体没有固定的体积和形状;(2)不同的气体能以任意比例相互均匀地混合;(3)气体是最容易被压缩的一种聚集状态。
2.理想气体理想气体是一种人为的理想模型,理想气体具有以下特点:(1)分子本身不占有体积,是一个具有质量的几何点;(2)气体分子间不存在相互作用力,与器壁之间的碰撞为完全弹性碰撞;(3)在高温、低压下,实际气体的行为接近于理想气体。
3.理想气体状态方程(1)三个定律①波义耳定律:当n和T一定时,气体的V与p成反比,表示为。
②查理-盖·吕萨克定律:当n和p一定时,气体的V与T成正比,表示为。
③阿佛加德罗定律:当T和p一定时,气体的V与n成正比,表示为。
(2)理想气体状态方程将上述三个经验定律合并得出理想气体状态方程为:式中,R=8.314 J·mol-1·K-1,称为摩尔气体常数;p、V、T和n分别为压力、体积、温度和物质的量,单位分别为Pa、m3、K和mol。
该方程适用于理想气体,近似地适用于温度不太低、压力不太高的真实气体。
(3)理想气体状态方程的应用①计算p,V,T,n中的任意物理量②确定气体的摩尔质量根据,得出:其中,M单位为g·mol-1。
③确定气体的密度根据,得出:4.气体分压定律理想气体状态方程式不仅适用于单一组分的气体,也适用于多组分的混合气体或其中某一种组分气体。
在理想气体混合物中,若各组分之间不发生化学反应,也没有任何其他相互作用,则它们之间互不干扰,如同各自单独存在一样。
分压定律:混合气体的总压等于混合气体中各组分气体分压之和,这一定律被称为Dalton分压定律。
混合气体中某组分气体B对器壁产生的压力称为该组分气体的分压力pB。
组分气体即理想气体混合物中的每一种气体。
