第二章 水
第2章 水

续表2-1
食 乳制品 奶油 山羊奶 奶酪(含水量与品种有关) 奶粉 冰淇淋 人造奶油 焙烤食品 面包 饼干 馅饼 糖及其制品 蜂蜜 果冻、果酱 蔗糖、硬糖、纯巧克力 品 含水量(%) 15 87 40~75 4 65 15 35~45 5~8 43~59 20 <35 <1
2. 水在食品方面的功能
单个水分子的结构特征
• 水分子的四面体结构
有对称性
• H-O共价键具离子性
与电负性
• 氧的另外两对孤对电
子具有静电力
2. 水分子的缔合作用
①H-O键间电荷的非对 称分布(氧电负性大,使 氢原子带有部分正电荷且 电子屏蔽小,表现裸质子 特征)使H-O键具有极性, 这种极性使分子之间产生 引力。 ②由于每个水分子具有 数目相等的氢键供体和受 体,因此可以在三维空间 形成多重氢键网络结构。 ③静电效应。 为什么水分子间存 在强大吸引力能进 行高强度缔合? 氢键供体
不同的缔合形式,可导致水分子之间的缔合数大于4。
水的结构特征
水是呈四面体的网状结构。 水分子之间的氢键网络是动态的。 水分子氢键键合程度取决于温度。
温度(℃)
0 1.5
配位数
4 4.4
分子间距nm
0.276 0.290
8.3
4.9
0.305
为什么水的密度在3.98℃/4 ℃最大?
水分子之间的氢键网络是动态的; 水的氢键键合程度取决于温度; 0 ℃时,冰中水分子配位数是4,随着温 度上升,配位数增多,密度增大,在0-3.98 ℃时,配位数的影响占主导。但温度升高 密度降低;
第二章
水
Water
本章简介
本章作业
第2章 水
掌握内容 讲授
第二章 水

பைடு நூலகம்
水
四川旅游学院 食品科学系
主要内容
第一节 水的基本概述 一、 食物中水的存在 二、 水的化学组成和结构 第二节 水在食品中的性质和存在状态
一、食品中水的性质及在烹饪中的应用 二、生物和食品中水的存在状态 第三节 水分活度 一、水分活度的概念 二、水分活度的影响因素 三、水分活度的意义和应用 第四节 水在烹饪加工中的变化 一、食品水分的转移 二、烹饪和食品加工水分的变化
95 95 92 90 87 87
牛奶 马铃薯 香蕉 鸡 肉 面包
87 78 75 70 65 35
果酱 蜂蜜 奶油 稻米面粉 奶粉 酥油
28 20 16 12 4 0
表2.1 某些代表性食品的含水量
一、生物和食物中水的作用
1、水是食品的重要组成成分,是形成食品加工
工艺考虑的重要因素;
2、水分含量、分布和状态对于食品的结构、外 观、质地、风味、新鲜程度会产生极大的影响; 3、是引起烹饪化学变化及微生物作用的重要原 因,直接关系到食品的贮藏特性。
2.水的分散功能对食品的影响和在烹饪中的应用
从食品与水形成的各种分散体系的性质来看, 食品可分为富含水食品和低含水食品。 低含水食品宏观上是干燥的固体或富含油脂的 半固体食品。例如,干淀粉、食盐等 富含水食品为含水湿润状态,分为液态食品和 湿固态食品两大类。
•当水溶液结冰时,六方形是在大多数冷冻食品中重要 的结晶形式。
•水的冰点为0℃,可纯水并不在0℃就冻结,常常首先被冷
却到过冷状态,这时开始出现稳定晶核,冰晶围绕有限的晶核长 大。开始出现稳定晶核时的温度叫过冷温度。 •食品中含有一定水溶性成分,这将使食品的冻结点降低,大多
第二章 水
4 +
Cl
-
Br -I
-
NO
3
-
BrO
3
-
IO
3
-
ClO
4
-
等
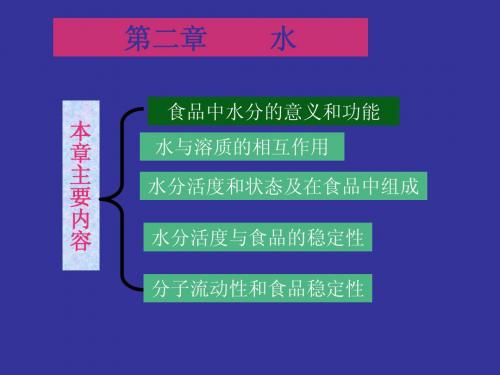
净结构形成效应(Net structure- forming
effect)
另外一些离子具有净结构形成效应(Net structure- forming effect),此时溶液具有比纯水较 差的流动性,这些离子大多是小离子和多价离子,电 场强度大,离子半径小,是净结构形成体。如:Li + Na + Ca 2+ Ba 2+ Mg 2+ Al 3+ F - OH - 等 如何判断离子对水结构的影响?
水与离子、离子基团的相互作用
一、水与离子基团的相互作用
水与简单无机离子产生偶极—离子的相互作用,作用强度 相对于氢键较强
溶质对水结构的影响
净结构破坏效应
(Net structure-breaking effect )
在稀水溶液中一些离子具有净结构破坏效应 (Netstructure-breaking effect),此时溶液具有 比纯水较好的流动性, 这些离子大多为单价离子 和大的正离子,产生较弱的电场,它们是净结构 破坏体,破坏了水的正常结构。如:K + Rb + Cs +
蛋白质 的水合 过程与 蛋白质 的性质
B、随着水分活度的增加,蛋白质的结 构也有不同,这对蛋白质的食品功能 性将产生较大影响。 C、随着水分活度的增加,溶菌酶 活性也不同,当有体相水存在时, 才表现出较明显的酶活性。这对理 解食品保藏及加工有重要意义。
七、水分活度(Aw)与相对蒸汽压
食品的水分含量和它的腐败性之间存在着一定的关系 在评价食品中水分时,除了注意水分的含量外,更注意水
第二章水文基础知识

W Q•T
y Q •T •103 Q •T (mm)
F •106
1000F
径流模数(M):流域出口断面上的流量与流域面积的比值。
M=1000Q/F
径流系数(α):某时段降雨量x所形成径流深y的比例数
α =y/x
因为降雨总是会有损失,所以一般α只能小于1。
3/3
(三)流域平均降雨量的计算
流域内各站降雨量是不同的,分析流域 降雨与径流关系时,需要由降雨量计算流域 平均面雨量,根据流域内雨量资料,常用以 下方法:
1. 算术平均法
式中
——某一指定时段的流域平均雨量,mm; ——流域内的雨量站数; ——流域内第站指定时段的雨量,mm。
2. 泰森多边形法
f4 f3
2. 降水的分类 按空气抬升形成动力冷却的原因可以把降水分
为4种类型:
强度大,范围小,历时短
降水
对流雨 地形雨 气旋雨
迎风面雨多,背风面雨少
温带气旋雨
气旋前方:暖锋云系及连续性降雨 气旋后方:狭窄的冷锋云系和降雨 气旋中部:暖气团,层云或毛毛雨
热带气旋雨 水汽充足,运动强烈,易带来狂风暴雨
锋面雨
冷锋雨 暖锋雨
水面蒸发常用蒸发器进行观测。换算关 系为:
式中
——天然水面蒸发量,mm; ——蒸发器实测蒸发量,mm; ——蒸发器折算系数。
(二) 土壤蒸发 土壤蒸发比水面蒸发要复杂得多。湿润
的土壤,其蒸发过程一般可以分为三个阶段。
(三)植物散发 土壤中的水分经植物根系吸收后,输送
至叶面,再从叶面散发到大气中,称为植物 散发。
(四) 流域总蒸发
流域总蒸发是流域内所有的水面、土壤以及植 被蒸发与散发的总和。目前采用的方法是从全流 域综合角度出发,用水量平衡原理来推算流域总 蒸发量。
第2章 水分

球状蛋白质的疏水相互作用
疏水基团缔合或发生 “疏水相互作用”, 引起了蛋白质的折叠。 疏水相互作用是蛋白 质折叠的主要驱动力。 同时也是维持蛋白质 三级结构的重要因素
2 水的存在形式
滞化水
自由水 毛细管水
水 结合水
自由流动水 化合水
邻近水
多层水
结合水
指通过化学键结合的水。根据被结合的牢固程度, 有几种不同的形式:
Ice-twelve (ice XII)
(5)冰形成的动力学过程
研究了过冷水(230K)体系中冰的形成 (Masakazu Matsumoto, NATURE /VOL 416 /28 ,03,2002 ) 四个阶段: -静态化学势能相对稳定期 (t=256–290 ns); -短暂的化学势能快速衰减期 (t=290-320ns) -短暂的化学势能快速增加期 (t=320-360ns) -终止期,化学势能虽有降低但 相对恒定,冰结构完全形成 (t>360ns)
演示1 演示2
在稀水溶液中一些离子具有净结构破坏效 应(Net structure-breaking effect), 这些离 子大多大的正离子。 另外一些离子具有净结构形成效应(Net structure-forming effect),这些离子大多是电 场强度大,离子半径小的离子。
(2) 水与有氢键键合能力中性基团的相互作用 Interaction of water with neutral groups possessing hydrogen-bonding apabilities
水分活度的测定方法 Measurement methods of Aw
1. 冰点测定法:先测样品的冰点降低和含水量 据下两式计算AW: aw=n1/(n1+n2) n2=G△Tf/(1000.Kf) G—溶剂克数 △Tf—冰点降低(℃) Kf—水的摩尔冰点降低常数(1.86)
食品化学 第二章 水 知识点总结

食品化学第二章水知识点总结第二章水食品中的水分含量及功能水分含量一般生物体及食品中水分含量为3~97% 水在生物体内的含量约70~80% 水在动物体内的含量特点随动物年龄的增加而减少,成人含水量为58~67%。
不同部位水分含量不同:皮肤 60~70%;肌肉及器脏 70~80%;骨骼 12~15%。
水在植物体内的含量特点营养器官组织含量最高 70~90%。
繁殖器官组织含量最低 12~15%。
某些食品的水分含量表2—1食品水分含量 ( % )白菜,菠菜90—95 猪肉 53—60 新鲜蛋74 奶88 冰淇淋65 大米12 面包35 饼干3—8 奶油 15--20 水的功能水在生物体内的功能1.稳定生物大分子的构象,使其表现特异的生物活性2.体内化学介质,使生物化学反应顺利进行3.营养物质,代谢载体4.热容量大,调节体温5.润滑作用此外,水还具有镇静、强壮效果;保护眼睛,降脂减肥和美容作用。
水的食品功能 1.食品的组成成分2.显示色、香、味、形、质构特征3.分散蛋白质、淀粉、形成溶胶4.影响鲜度、硬度5.影响加工,起浸透、膨胀作用6.影响储藏性水的物理性质水的三态1、以水—汽2、水—冰3、汽—冰特点: 具有水、汽、冰三相共存 * * 水的重要物理性质水的许多物理性质:如熔点、沸点、比热容、熔化热、蒸发热、表面张力和界电常数都明显偏高. * *原因:水分子间存在着三维氢键缔合的缘故1水的密度在4℃最大,为1;0℃时冰密度为,水结冰时,体积膨胀约9%(/L). 实际应用:这种性质易对冷冻食品的结构造成机械损伤,是冷冻食品行业中应关注的问题2. 水的沸点与气压呈正相关关系.当气压升高时,则其沸电升高;当气压下降,则沸点降低。
实际应用:(1)热敏性的食品如牛奶、肉汁、果汁等的浓缩通常采用减压或真空方式来保护食品的营养物质(2)不易煮烂的食物,如动物的筋、骨、牛肉等可采用高压蒸煮,低酸性的罐头的杀菌 (3)高原上做饭应采用高压 3.水的比热较大水的比热大是因为当温度升高时,除了分子动能需要吸收热量外,同时缔合的分子转化为单分子时也需要吸收热量所致。
第二章地球上的水循环

地球上的水分循环 和水量平衡
一、水分循环
(一)水分循环及其成因
地表水、地下水和生物有机体内的水,不断蒸发和蒸 腾,化为水汽,上升至空中,冷却凝结成水滴或冰晶, 在一定的条件下,以降水的形式落到地球表面。降落于 地表的水又重新产生蒸发、凝结、降水和径流等变化。 水的这种不断地蒸发、输送、凝结、降落的往复运动过 程称为水分循环。
水循环
陆地上地表水总量约360000km3,生物水量约2000km3。 陆地上的大气降水与冰雪融水消耗于蒸发、生物吸收和 渗透到地下,另有约36000km3通过径流返回海洋。陆地 上水体的自然更新一次的时间长短不一,河流约需10-20 天,土壤水约需280天,淡水湖约需1-100年,盐湖和内 海约需10-1000年。
1.大循环
从海洋表面蒸发的水汽,被气流带到大陆上空,在适 当的条件下,以降水的形式降落到地面后,其中一部分蒸 发到空中,另一部分经过地表和地下径流又流到海洋,这 种海陆之间的水分交换过程,称为大循环,也称海陆间循 环。它是由许多小循环组成的复杂的水分循环过程。
2.小循环
小循环是指水仅在局部地区(海洋或陆地)内完成 的循环过程。小循环可分为海洋小循环和陆地小循环。 海洋小循环就是从海洋表面蒸发的水汽,在空中 凝结,以降水形式降落海洋上的循环过程。
水循环
全球水分循环中各主要贮水库的总水量以及各主要贮水库之间水 分交换通量,在地质历史时期曾发生过重大变化。如白垩纪中晚期 地球表面没有冰盖,没有冰雪的贮水。再如第四纪冰期鼎盛时期,
以距今18000年末次冰期鼎盛时期为例,当时的全球平均气温要比
现代低6-7℃,全球陆上冰体总量要比现代多约50.72×106km3, 世界海洋水位要比现代低约130m,海面蒸发量要比现代少约
高中生物第二章 水和无机盐优秀课件

抗热等抗逆性增强 。
〔如:越冬植物、干种子等〕
5.种子萌发
种子晒干过程中失去的是自由水,可以萌发。 种子在烘烤过程中失去的是结合水。不能萌发。 种子萌发的根本条件:充足的水分、充足的氧气、适宜的温度。
将烘干的骨、小麦种子和植物秸秆 等点燃烧尽, 最终都会得到一些灰白色 的灰烬 , 请问这些灰烬是什么呢 ?
B:植物缺B〔
)
花而不实
细胞外液渗透压:Na+ 〔3〕维持细胞的渗透压和酸碱平衡 细胞内液渗透压: K+
血浆PH:HCO3-、HPO42-
思考&讨论
资料1 植物在缺乏N、P、K等营养物质时会出现各种病症,因此生产 过程中常要给植物施肥。玉米在生长过程中缺乏P,植株就
植物体缺p常表现为生长发育不正常,这说明什么? P是植物生命活动不可缺少的。
资料2 以下图是一种叶绿素分 子和血红素分子局部结构简图 。
讨论
1.植物体缺Mg会影响光合作用,为什么? 缺镁时叶绿素的形成受到阻碍,从而影响光合作用。
2.有一种贫血症叫缺铁性贫血症,为什么缺Fe会导致贫血? 当铁缺乏时,血红蛋白就不能合成,从而发生缺铁性贫血。
无机盐
3.无机盐生理功能的验证 (1)对照组 植物+完全培养液→正常生长 (2)实验组
无机盐
无子形式存在,少数以化合物 形式存在。
2.功能
〔1〕组成细胞中的化合物:
Mg2+叶绿素, Fe2+血红蛋白, I-甲状腺激素 PO43-磷脂 核酸 Ca2+骨骼、牙齿
CaCO3是动物和人体的骨骼、牙齿中的重要成分。
无机盐
〔2〕维持细胞和生物体的生命活动 Ca2+:血钙〔过高:肌无力 ;过低:抽搐 〕
第二章 水

4 水对食品品质的影响
4.2 水对食品的色泽和风味的影响
食品加工中常利用高温烘烤、油炸、辐射加热等方法使 食品成熟、脱水上色。
如油炸过程中食品中水分的主要变化如下: (1)自然水挥发阶段
表面水分蒸发,内部水向外渗透,完成表面淀粉糊化、蛋白质变性。
(2)脱水分解阶段
结合水开始失去,分解产生很多风味物质和中间产物
3 食品中水存在的状态
Vicinal water
它是处在非水组分亲水性最强的基团周围的第一层 位置的水(又称单分子层水)。 其中,与离子或离子基团相缔合的水是结合最紧密 的邻近水。
在-40℃下不结冰 无溶解溶质的能力 与纯水比较分子平均运动大大减少 不能被微生物利用
此种水很稳定,不易引起Food的腐败变质。
(3)脱水缩合、聚合
羰氨反应和焦糖化反应
5 食品中水含量的表示方法
食 品 中 水 分 的 表 示 方 法
食品含水量(或水分含量): 指温度、湿度一定时,与外界环境处于平 衡状态时食品的总含水量(结合水与体相水的 总和),它与食品腐败性之间存在着一定的关 系。但是,不同类型的食品中水分含量相同, 而它们的腐败性显著不同。因此,水分含量不 是食品腐败性的可靠指标。
课堂讨论:
冻结与解冻过程,何者快些?
冻结过程
外表层为冰
常温肌肉块
外表层为水
冷冻肌肉块
解冻过程
1 引言
1.2 水和冰的结构
(1) 单个水分子的结构特征
如左图所示,水分子中氧 原子的6个价电子参与杂化形 成4个杂化轨道,有近似四面 体的结构。其中2个杂化轨O-Hσ共价键。 氧原子的另2个杂化轨道上分 别排布着孤对电子。
② 由于每个水分子具有数目相
水化学:第二章 天然水的主要理化性质

(四)水具有很强的溶解与反应能力
水是一种溶解能力极强的溶剂 水的介电常数很大,使溶质在水中具有很大的电离度
(五)水具有很大的表面张力
特点:水(除汞)具有最大的表面张力,达72.75 dyn•cm-1 其他液体通常只有20-50 dyn•cm-1。
作用:显著的毛细、润湿和吸附作用 对于陆地和水域中生物的生命活动具有重要的意义
透过可见光和长波段紫外线,使在水
7
体深处可发生光合作用
第二节 天然水的化学组成
按不同组分含量与性质的差异,以及与水生生物的关系 天然水的化学成分分为六类:
常量元素 溶解气体 营养元素 有机物质 微量元素 有毒物质
8
一、常量元素
淡水中的八大离子:K+、Na+、Ca2+、Mg2+、HCO3-、CO32-、 SO42-、Cl-
10
三、营养元素
主要元素: N、P、Si(与水生生物生长有关的一些元素) 存在形式:多以复杂的离子形式或有机物的形式存在于水体
中,在水中含量通常较低,受生物影响较大,有时 又称为“非保守成分”或“生物制约元素”
11
四、有机物
分类: 颗粒态有机物 溶解态有机物
含量:较低,通常是无机成分的万分之一,一般1L水中仅几mg 成分:复杂,种类繁多,如糖类、脂肪、蛋白质及降解有机物
端为正极)
3
水分子的结构
4
三、水的异常特性
(一)水在通常条件下呈液态
水通常呈三种物理状态,即液态、气态和固态
(二)水的温度-体积效应异常
纯水结冰时体积不是收缩而是膨胀 在0-3.98℃,随着温度的升高,水的体积反而缩小( 3.98℃时水的体积最小,密度最大)
(三)水的比热容非常大
工程水文:第二章第一节 自然界的水文循环

57.7 *104 45 次
12900
一年365天,所以平均
365 45
8
天完成一次循环。
由于太阳能在地球上分布不均匀,且时间上也有变化, 因此由太阳能驱动的水文循环导致地球上降水量和蒸发量 的时空分布不均匀,使地球上有湿润地区和干旱地区;有 多水季节和少水季节、多水年和少水年的区别。
0
0
0
多年平均情况下
SC 0, S0 0
P RE
C
C
P R E
0
0
合并两式得多年平均全球水量平衡方程
P P E E,或 P E
C
0
C
0
即全球多年平均降水量与多年平均蒸发量相等。
水循环的主要环节:蒸发、水汽输送、降水(凝结、 降落)、径流
二、产生水循环的内外因及分类 1、水循环产生的内外因 产生循环的外因:太阳辐射和地心引力。
产生循环的内因:水常温下的三态转化,并不发 生化学变化。
2、水循环分类 按水循环的规模与过程可分为:
大循环:海洋-陆地间水分的交换
纵向交换:降水 蒸发
横向交换:通过河 流由陆地到海洋。
小循环:海洋-海洋;陆面-陆面间的水分交换。
陆面降水主要依赖于洋面上源源不断送来的水汽。即 大循环起主导作用。其次是内陆小循环起作用。
水在自然界中的循环,为人类带来了源源不绝的水资 源。也是地球上的生命得以延续的重要原因。
例;大气中的水量S为12900km3 ,地球上一年中的降水 量为57.7万km3 。。
水是良好的溶剂,水流具有携带物质的能力。自然界许 多物质(如泥沙、有机质、无机质等以水为载体,参与 各种物质循环。
水文循环有全球水文循环、流域或区域水文循环和水土-植物系统水文循环等三种不同尺度。
第二章 第二节水的天然循环

谢
谢
3、下列生活中的做法,不利于节约用水的是( ) A.用淘米水浇花 B.用洗过衣冲马桶 C.隔夜的白开水直接倒掉 D.洗手打肥皂时暂时关闭 水龙头 4、有关水的天然循环的说法不正确的是( ) A.是物理变化 B.是化学变化 C.这个过程水分子的 能量在不断变化 D.太阳为水提供能量 5、水是宝贵的自然资源.下列说法正确的是( ) A.水在自然界中不断循环,取之不尽、用之不竭 B.工业废水经过净化后再排放 C.为了节约用水,可以用工业废水直接浇灌农田 D.自来水中只含水分子,不含其它粒子
9、学习化学知识后,观察物质世界就要从化学视角看。水是一种 重要的物质,在日常生活和实验室中有着不可替代的作用。请按 要求回答下列问题: (1)从组成角度看:水是由 组成的,世界上形形色色的
(2)从微粒角度看:水是由 构成的,构成物质的基本微粒有 分子、原子、离子。 (3)从变化角度看:化学变化不但生成新物质而且还伴随能量变 化。水通电分解生成未来最理想的能源——氢气,是将 能转 化为化学能,但该方法不节能,需要寻找更为有效的节能方法, 以促进水的分解。 (4)从资源角度看:水是生命之源。看到右侧漫画,你的感想 是: (解读漫画或写一则节水广告或一条节水措施)。 10、白酒瓶敞口放置,酒的香味变淡。试用分子的观点解释。 11、你能用分子的观点解释水受热蒸发变成水蒸气这一现象吗?
简述水在自然界中的循环过程。 在水循环的每个环节上水分子是怎样运动的? 水分子的能量如何变化?是什么原因导致了水分子 的能量变化? 自然界中水的三态变化有什么重要意义?
体会感悟水的天然循环
观察课本中水的天然循环路线图,同 学们小组交流讨论: • 1、认识以下几个概念 冷凝 蒸发 蒸腾 蒸馏 升华 径流 沉积 • 2、充分体会“自然界的物质都在不断东岳中学 李兴宝
第二章 水

-6-
的结构,然后再介绍水的结构。 1. 纯冰 冰是由水分子有序排列形成的结晶。水分子之间靠氢键连接在一起形成非常
稀疏(低密度)的刚性结构,这一点已通过 X-射线、中子衍射、电子衍射、红外和 拉曼光谱分析研究得到阐明(图 2-5)。最邻近的水分子的 O—O 核间距为 2.76Å, O—O—O 键角约为 109º,十分接近理想四面体的键角 109º28'。从图 2-5 可以看 出,每个水分子能够缔合另外 4 个水分子即 1,2,3 和 W',形成四面体结构, 所以配位数等于 4。
以上对水的一些描述显得过于简单化,主要是为了便于理解。在纯净的水中 除含普通的水分子外,还存在许多其他微量成分,如由16O和1H的同位素17O、18O、 2H和3H所构成的水分子,共有 18 种水分子的同位素变体;此外,水中还有离子 微粒如氢离子(以H3O+存在)和氢氧根离子,以及它们的同位素变体,因此,实际 上水中总共有 33 种以上HOH的化学变体。同位素变体仅少量存在于水中,因此, 在大多数情况下可以忽略不计。
图 2-5 0℃时普通冰的晶胞(圆圈表示水分子中的氧原子)
当我们从顶部沿着 C 轴观察几个晶胞结合在一起的晶胞群时,便可看出冰 的正六方形对称结构,如图 2-6a 所示。图中 W 和最邻近的另外 4 个水分子显示 出冰的四面体亚结构,其中 W、1、2、3 四个水分子可以清楚地看见,第四个水 分子正好位于 W 分子所在纸平面的下面。当在三维空间观察图 2-6(a)时即可得 到如图 2-6(b)所示的图形。显然,它包含水分子的两个平面,这两个平面平行而 且很紧密地结合在一起,这类成对平面是由冰的基础平面组成。在压力作用下, 冰“滑动”或“流动”时,如同一个整体“滑动”,或者像冰河中的冰在压力的 作用下所产生的“流动”。
第2章_水分

第2章_⽔分第2章⽔分第⼀节引⾔⽔是唯⼀的以三种物理状态⼴泛存在的物质。
⽔是⾷品中⾮常重要的⼀种成分,也是构成⼤多数⾷品的主要组分,每种⾷品都有其特定的含⽔量。
⽔的重要功能:⽔在⾷品加⼯⽅⾯的功能:㈠⾷品理化性质:起着溶解、分散蛋⽩质、淀粉等⽔溶性成分的作⽤。
㈡⾷品质地⽅⾯:对⾷品的新鲜度、硬度、风味、流动性、⾊泽、耐贮性和加⼯适应性有影响。
㈢⾷品安全性:⽔是微⽣物繁殖的必需条件。
㈣⾷品⼯艺⾓度:⽔起着膨润、浸透、均匀化等功能;⼤多数⾷品加⼯的单元操作都与⽔有关,如⼲燥、浓缩、冷冻、⽔的固定等。
第⼆节⽔和冰的结构与性质⼀、⽔分⼦1、⽔分⼦:⽔分⼦中氧的6个价电⼦参与杂化,形成4个SP3杂化轨道,有近似四⾯体的结构,其中2个杂化轨道与2个氢原⼦结合成两个共价键,另2个杂化轨道呈未键合电⼦对。
单个⽔分⼦(⽓态)的键⾓由于受到了氧的未成键电⼦对的排斥作⽤,压缩为104.5o,接近正四⾯体的⾓度109o28ˊ,O-H核间距0.96A,氢和氧的范德华半径分别为1.2A和1.4A。
单个⽔分⼦的结构特征:①H2O分⼦的四⾯体结构有对称型;②H-O共价键有离⼦性;③氧的另外两对孤对电⼦有静电斥⼒;④⽔分⼦是偶极分⼦。
2、⽔分⼦的缔合:①H-O键间电荷的⾮对称分布使H-O键具有极性,这种极性使分⼦之间产⽣引⼒。
②由于每个⽔分⼦具有数⽬相等的氢键供体和受体,因此可以在三维空间形成多重氢键。
⼆、冰和⽔的结构1、冰的结构:每个⽔分⼦能够缔合另外4个⽔分⼦(配位数为4),形成四⾯体结构。
2、⽔的结构:纯⽔是具有⼀定结构的液体。
液体⽔发热结构与冰的结构的区别在于它们的配位数和⼆⽔分⼦之间的距离。
冰向⽔转变伴随着最接近的⽔分⼦间的距离的增加最接近的⽔分⼦的平均数⽬的增加。
⽔的密度在3.98℃达到最⼤。
密度增加:在0℃和3.98℃之间,配位数增加的效应占优势。
密度下降:超过3.98℃后,最接近的⽔分⼦间的距离增加的效应(热膨胀)占优势。
第二章 水环境基本理论

第二章水环境基本理论第一节天然水的化学组成一、纯水的结构与异常特性1、水的异常特性水是自然界中最常见的物质,具有许多特异的理化性质,也正是由于这些特性,才使水在自然界和人类生活中普遍发生巨大作用,成为支配自然和人类环境中各种现象的主要因素。
要研究水及其中杂质共同表现的水质特性,需先深入了解水本身的特性。
与同系化合物相比,水具有如表2-1所示的一系列异常特性。
表2-1 纯水的异常特性及其意义性质特点意义状态一般为液态提供生命介质、使水具有流动性热容在所有固体和液体中最高(NH3除外)使水成为良好的传热介质,调节环境和有机体的温度熔解热最大(NH3除外)使水处于稳定的液态,调节水温蒸发热在所有物质中最高对水蒸气的大气物理性质有重要意义,调节水温密度 3.98℃时极大对于水生生物在严冬冻结的淡水水体深层水中的生命活动具有重要意义表面张力在所有液体总最大(汞除外)生理学控制因素,控制液滴等表面现象介电常数所有液体中最高高度溶解离子性物质并使其电离水合非常广泛对污染物是良好溶剂和载带体,可改变溶质生物化学性质离解很小提供中性介质透明度相对较大透过可见光和长波段紫外线,使在水体深处可发生光合作用(1)水在通常条件下呈液态在地球表面的环境条件下,水可能呈三种物理状态,即液态、气态和固态。
由于沸点和冰点间温度范围相当宽,且相变热很大,所以地球表面大量的水还是呈液态,于是构成了各种类型的天然水体。
因此通常条件下呈液态这一点也正是水的最重要特点之一。
(2)水的温度-体积效应异常纯水与一般物质的热胀冷缩不同,当冻结时体积不是收缩而是膨胀。
在0—3.98℃,随着温度的升高,水的体积反而缩小,至3.98℃时体积最小,水的密度最大。
此外,当压力加大时,一般物质的凝固点均有所升高,而水的冰点却略为下降。
通常物质的热膨胀系数均随压力的升高而减小,而纯水在0—45℃范围内,热膨胀系数却随压力的升高而增大。
这些都是水在温度或压力变化时体积效应异常的表现。
烹饪化学《第二章 水》简答题

一、引起食品解吸与回吸出现滞后现象的原因是什么?
1、解吸过程中一些水分与非水分溶液成分作用而无法放出水分
2、不规则形状产生毛细管现象的部位,欲填满或抽出水分需不同蒸气压
3、解吸作用时,因组织改变,当再吸水时无法紧密结合水分,由此可导致回吸相同水
分含量时处于较高的水分活度。
4、温度、解吸速度和程度及食品类型都会影响滞后现象。
二、现代食品冷藏为什么要提倡速冻
现代冻藏工艺提倡速冻,因为该工艺下形成的冰晶体呈针状,比较细小,冻结时间缩短且微生物受到更大限制,因而食品品质好。
三、麦当劳的薯片的水分活度在0.4左右时最适合保存,为什么?
油炸薯片的脂类氧化酸败速度在活度0.4时最慢,高于或低于这个活度都会使反应加快。
四、烹饪食品中水的存在形式主要有哪两种状态,两种状态包含哪些种类?
答:体相水(自由水):不移动水(滞化水)、毛细管水、自由流动水
结合水(束缚水或固定水):构成水(化合水)、邻近水、多层水
五、引起食品解吸与回吸出现滞后现象的原因是什么?
①解吸过程中一些水分与非水分溶液成分作用而无法放出水分。
②不规则形状产生毛细管现象的部位,欲填满或抽出水分需不同蒸气压。
③解吸作用时,因组织改变,当再吸水时无法紧密结合水分,由此可导致同吸相同水
分含量时处于较高的水分活度。
④溫度、解吸速度和程度及食品类型都会影响滞后现象。
第二章:水
2.冰转变为水时的变化
2.1微观结构上的变化 2.2密度上的变化 两个因素: ①配位数 ②最邻近的水分子之间的距离
第七节 水与溶质的相互作用
1.几个一般概念 几个一般概念
溶质分子基团与水分子的两种作用 (1)溶质分子基团 亲水基团:即具有极性的基团。 疏水基团:即具有非极性的基团。 (2)两种作用 亲水相互作用:亲水基团和水分子之间发生的相吸作 用。 疏水相互作用:疏水基团和水分子之间发生的相互排 斥作用。
4.1中性基团(亲水性溶质)亲水的原因→ 分子 结构中含有亲水性基团。 举例说明中性基团的亲水性基团??? 羟基、氨基、羰基、酰胺基、亚氨基
4.2水与亲水性基团的作用力
种类和强度 对水结构的影响: 没有显著的影响。 “水桥”的形成: 维持大分子的特 定构象。
5.水与非极性物质的相互作用
5.1何谓非极性物质?举例说明。
凝胶扫描电镜观察
面条凝胶截面观察
2.2分子水平
2.2.1水分子和溶质分子作用力强弱的比较
2.2.2食品体系中水分子的存在状态
---从水分子和溶质分子作用力强弱上区别 (1)构成水 概念:指与非水物质结合最强的并作为 非水组分整体部分的结合水。 特点:
这部分水在高水含量食品(90%以上)中占很少部分。 在-40℃下不结冰,无溶剂能力。
3.1离子和离子基团:能在水中电离的物质(无
机离子),以及有机分子的离子基团。 举例。
3.2水分子与离子和离子基团的作用力
3.2.1种类 偶极↔离子 3.2.2强度:比H2O ↔ H2O氢键强,比共价 健弱。
3.3水分子与离子和离子基团的作用力对水 结构和性质的影响
①与离子最相邻的第一层 水分子将强烈地被打乱。 → 结构水、邻近水 ②第二层或更远的水分子 也将被改变。 → 多层水、体相水 ③ 在浓盐溶液和稀盐溶液 中,离子对水结构的影响 是不同的。
第二章 水分

RVP=p/p0=ERH/100 平衡相对湿度
通过测定食品的平衡相对湿度就可获得食品的水 分活度。 但实际测定时很难找到一种溶液,它的p/p0刚好为 食品的p/p0,故一般要采用系列饱和溶液。
重量变化 线性 (重量变化)
0.3 0.2 0.1 0 0.3 -0.1 -0.2 -0.3 -0.4 -0.5 0.4 0.5 0.6 0.7 0.8 0.9 1 1.1
1.水是细胞原生质的重要组成成分 细胞原生质的含水量:70%~80%以上。
2.水是细胞内物质的溶剂和新成代谢反应的介质。
盐类,氨基酸(AA),蛋白质,糖,维生素类
脂类:通过脂蛋白,胆汁酸类形成乳化剂溶于水。
生化反应:呼吸(糖代谢),脂,蛋白质,核酸代
谢都是在水的介质中进行的(人失水10%则会死亡)。
第二章 水分
问题?
固形物16% 固形物4%
含水量20%不长菌 含水量16%奶粉长菌
主要讨论内容:
水的生理功能和在食品中的作用
食品中水的存在状态:自由水、结合水 水分活度及其应用
第一节 水在生命活动和食品中的作 用
一、水在生物体内分布
二、水在生物体内的功能 处于代谢活跃状态的生物都具有极高的含水 量,一般都达70%~80%,果蔬类更高(P12表 2-1)。
样品重量变化
水分活度
康威氏(Conway)微量扩散皿
水分活度的测定原理
测定时注意:一定要达到水分平衡,且要用小样(小于或等于 1g)据研究,大样品在50C以下几乎是不可能达到平衡的。
定义:水分活度指在同一温度下,食品中水 分所显示出的蒸汽压P与同一温度下纯水的蒸
汽压P0之比。它是衡量食品中水分被微生物
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Why!!!
Compd. H2O H2S NH3 Methanol
M.P 0º C -83º C -78º C -98º C
B.P 100º C -60º C -33º C 65º C
2.水的结构 Structure of water
• Tetrahedral arrangement • Two free electrons of O act as H-bond acceptors while H acts as donor • Highly electronegative O pulls electrons from H, making H behave like a bare proton • Forms a dipole because of the electronegative O
移。
冰不是一个均匀体系,不仅含有普通 水分子,而且还有H+(H3O+)和OH-离 子以及HOH的同位素变体;
冰的结晶并不是完整的晶体,通常是 有方向性或离子型缺陷的。
冰结构中氢原子( ● )的位置 (A)瞬时 结构;(B)平均结构(也称半氢,鲍林或统 计结构);O为氧原子
• 冰晶并非总是完美的, 一般存在定向型或离 子型缺陷。 • 冰的HOH分子在温 度接近-180℃或更低 时 ,氢键才是完整 的。
①H-O键间电荷的非对称分布使H-O键具有极性,
这种极性使分子之间产生引力.
②由于每个水分子具有数目相等的氢键供体和
受体,因此可以在三维空间形成多重氢键.
③静电效应.
目前提出的3类水的结构模型: 混合模型:混合模型强调了分子间氢键的概念, 认为分子间氢键短暂地浓集于成簇的水分子之 间,成簇的水分子与其它更密集的水分子处于 动态平衡. 连续模型:分子间氢键均匀地分布于整个水样, 水分子的连续网络结构成动态平衡. 填隙式模型:水保留在似冰状或笼状结构中, 个别的水分子填充在笼状结构的缝隙中.
• 溶质的种类和数量可以影响冰晶的数量、大 小、结构、位臵和取向。此外,冷冻速度对 冰晶的形成也有影响。
①按冷冻速度和对称要素分,冰可分为四大类
六方型冰晶 不规则树枝状结晶 粗糙的球状结晶 易消失的球状结晶及各种中间体
②六方冰晶形成的条件:
在最适度的低温冷却剂中缓慢冷冻
溶质的性质及浓度均不严重干扰水分子的迁
(1)单个水分子的结构特征
H2O分子的四面体结构有对称型. H-O共价键有离子性. 氧的另外两对孤对电子有静电力. H-O键具有电负性.
(2)水分子的缔合
水分子在三维空间形成多重 氢键键合 —每个水分子具有相等数目的 氢键给体和受体,能够在三 维空间形成氢键网络结构
(3)水分子缔合的原因:
水和非极性基团具有相对抗作用 水调整自身结构以便尽可能少地与非极性基团接触
非极性物质的疏水相互作用
水在疏水表面的取向
第一种测略
疏水水合(Hydrophobic hydration) : 向水中添加疏水物质时,由于它们与 水分子产生斥力,从而使疏水基团附 近的水分子之间的氢键键合增强,使 得熵减小,此过程成为疏水水合。
Multilayer water: water that occupies remaining first-layer sites and forms several additional layers around hydrophilic groups of nonaqueous constituents; water-water and water-solute hydrogen bonds predominate. 大多数多层水在-40℃下不结冰,其余可结冰,但冰 点大大降低。 有一定溶解溶质的能力 与纯水比较分子平均运动大大降低 不能被微生物利用
下图所示为位于中心的水分子将 RNA酶中三个分离的残基联系起 来。在微生物RNA酶家族中,这 些水分子和他们的结合位点都保 留了下来。
4.水与疏水基团的相互作用 Interaction of water with nonpolar substances
水中加入疏水性物质 疏水基团与水分子产 生斥力,从而使疏水基团 附近的水分子之间的氢键 键合增强,结构更为有序 疏水基团之间相互聚 集,从而使它们与水的接 触面积减小,结果导致自 由水分子增多 非极性物质具有两种特殊的性 质: 蛋白质分子产生的疏水相互作 用(hydrophobic interaction) 非极性物质能和水形成笼形水 合物(clathrate hydrates)
疏水相互作用( Hydrophobic interaction) : 当水与非极性基团接触时,为减少水与非极性 实体的界面面积,疏水基团之间进行缔合,这 种作用成为疏水相互作用。
球状蛋白质的疏水相互作用
疏水基团缔合或发生 “疏水相互作用”, 引起了蛋白质的折叠 。
疏水相互作用是蛋 白质折叠的主要驱动 力。 同时也是维持蛋 白质三级结构的重要 因素
Bulk-phase water: water that occupies positions furthest removed from nonaqueous constituents; water-water hydrogen bonds predominate. 能结冰,但冰点有所下降 溶解溶质的能力强,干燥时易被除去 与纯水分子平均运动接近 很适于微生物生长和大多数化学反应,易引起 Food的腐败变质,但与食品的风味及功能性紧密相 关。
水分子的结构特征
水是呈四面体的网状结构
水分子之间的氢键网络是动态的
水分子氢键键合程度取决于温度
温度(℃) 0 1.5 83
配位数 4 4.4 4.9
分子间距nm 0.276 0.290 0.305
冰的结晶
• 冰有11种结晶类型,普通冰的结晶属于六方 晶系的双六方双锥体。在常压和温度0℃时, 这11种结构中只有六方型冰结晶才是稳定的 形式 。
笼形水合物(Clathrate hydrates):是象冰一 样的包含化合物,水为“宿主”,它们靠氢 键键合形成象笼一样的结构,通过物理方式 将非极性物质截留在笼内,被截留的物质称 为“客体”。一般“宿主”由20-74个水分子 组成,较典型的客体有低分子量烃,稀有气 体,卤代烃等。
• 在水中,CO2分子周围可以形 成由19个水分子构成的十二面 体壳层结构, CO2分子中的每 个氧原子直接同三个水分子结 合,然后以此为核心构成 CO2(H2O)278的二十面体结构。
2.水与离子基团的相互作用 Interaction of water with Ionic groups
- 大量证据表明一些离子 在稀溶液具有净结构破 坏效应(溶液比纯水具 有较高的流动性);而 另外一些离子具有净结 构形成效应(溶液比纯 水具有较低的流动性)
一种指定的离子改变净 结构的能力关系到它的 极化力或者它的电场强 度
3.水与有氢键键合能力中性基团的相互作用 Interaction of water with neutral groups possessing hydrogen-bonding capabilities
水与溶质之间的氢键 键合比水与离子之间的 相互作用弱。氢键作用 的强度与水分子之间的 氢键相近。 与溶质以氢键键合的水主要 是化合水和邻近水,水的移 动性比纯水明显减弱,结冰 也十分困难。
冰中质子缺陷示意图 (A) 定 向作用形成的方向性缺陷 (B) 离子型缺陷
2.3 食品中水的存在形式 Categories of water in foods
自由水 体相水 水 结合水
截留水 化合水 邻近水 多层水
Constitutional water: Water a nonaqueous constitutents. 在-40℃下不结冰 无溶解溶质的能力 与纯水比较分子平均运动为0 不能被微生物利用
mvapor chemical potential: energy/mole m food mfood RT ln aw = m vapor p = RT ln p o
2.4 水与溶质的相互作用 Water –solute interactions
1.水与溶质相互作用的分类
相互作用强弱 (与H2O-H2O氢键比较) 偶极-离子 H2O-游离离子 较强 H2O-有机分子带电基团 偶极-偶极 H2O-PR-NH, H2O-PR-CO 近乎相等 H2O-侧链OH 疏水水合 H2O+R→R(水合) △G>0 疏水相互作用 R(水合)+R(水合) →R2(水合)+ H2O △G<0 种类 实例
Vicinal water: Water that strongly interacts with specific hydrophilic sites of nonaqueous constituents by water-ion and water-dipole associations
在-40℃下不结冰 无溶解溶质的能力 与纯水比较分子平均运动大大减少 不能被微生物利用 此种水很稳定,不易引起Food的腐败变质。
○是疏水基团,圆球周围的“L -形”物质根据疏水表面定向的 水分子,●代表与极性基团缔合 的水分子
第二种策 略
• 非极性物质能和水形 成笼形水合物 (clathrate hydrates) • 笼状水合物代表水对 一种非极性物质最大 的结构形成响应 • “宿主”水分子与 “客体”分子的相互 作用一般是弱的范德 华力,与静电相互作 用
Chapter 2 Water
水
本章提要
重点:
水和冰的结构及其在食品体系中的行为 对食品的质地、风味和稳定性的影响。水分 活度与水分吸着等温线及水分活度对食品稳 定性的影响。食品中水分含量和水分活度的 测定方法。
难点: 分子淌度与食品稳定性的关系,笼形水 合物。
