《新食品原料安全性审查管理办法》解读
新资源食品管理办法

新资源食品管理办法【法规类别】食品卫生【发文字号】中华人民共和国卫生部令第56号【失效依据】新食品原料安全性审查管理办法【发布部门】卫生部(已撤销)【发布日期】2007.07.02【实施日期】2007.12.01【时效性】失效【效力级别】部门规章中华人民共和国卫生部令(第56号)《新资源食品管理办法》已于2006年12月26日经卫生部部务会议讨论通过,现予以发布,自2007年12月1日起施行。
部长陈竺二○○七年七月二日新资源食品管理办法第一章总则第一条为加强对新资源食品的监督管理,保障消费者身体健康,根据《中华人民共和国食品卫生法》(以下简称《食品卫生法》),制定本办法。
第二条本办法规定的新资源食品包括:(一)在我国无食用习惯的动物、植物和微生物;(二)从动物、植物、微生物中分离的在我国无食用习惯的食品原料;(三)在食品加工过程中使用的微生物新品种;(四)因采用新工艺生产导致原有成分或者结构发生改变的食品原料。
第三条新资源食品应当符合《食品卫生法》及有关法规、规章、标准的规定,对人体不得产生任何急性、亚急性、慢性或其他潜在性健康危害。
第四条国家鼓励对新资源食品的科学研究和开发。
第五条卫生部主管全国新资源食品卫生监督管理工作。
县级以上地方人民政府卫生行政部门负责本行政区域内新资源食品卫生监督管理工作。
第二章新资源食品的申请第六条生产经营或者使用新资源食品的单位或者个人,在产品首次上市前应当报卫生部审核批准。
第七条申请新资源食品的,应当向卫生部提交下列材料:(一)新资源食品卫生行政许可申请表;(二)研制报告和安全性研究报告;(三)生产工艺简述和流程图;(四)产品质量标准;(五)国内外的研究利用情况和相关的安全性资料;(六)产品标签及说明书;。
食品标签警示用语要点

食品标签警示用语要点添加新食品原料的食品标签警示语标示《新食品原料安全性审查管理办法》中明确规定:“食品中含有新食品原料的,其产品标签标识应当符合国家法律、法规、食品安全标准和国家卫生计生委公告要求”O如《卫生部等6部局关于含库拉索芦荟凝胶食品标识规定的公告》中规定:“若无法确保消费者芦荟日摄入量在安全范围内,应在包装上标注每日食用量警示语”。
因此,食品中使用新食品原料时,需要关注该新食品原料的不适宜人群以及相应的推荐每日食用量,以确保产品的安全性。
同时,应根据公告要求在标签中标示相关的警示用语。
例如:添加了透明质酸钠的糖果,婴幼儿、孕妇及哺乳期妇女不宜食用,标签及说明书应当标注不适宜人群,并标注推荐食用量≤200毫克/天;加了新食品原料“关山樱花”的食品,婴幼儿、孕妇和哺乳期妇女不宜食用,标签及说明书应当标注不适宜人群。
普通食品警示语的标示2.1炼乳《食品安全国家标准浓缩乳制品》(GB13102)规定,炼乳产品应标示“本产品不能作为婴幼儿的母乳代用品”或类似警语。
2.2果冻《食品安全国家标准果冻》(GB19299)规定,凝胶果冻应在外包装和最小食用包装的醒目位置处,用白底(或黄底)红字标示警示语和食用方法,且文字高度不应小于3mm。
警示语和食用方法应标示为“勿一口吞食;三岁以下儿童不宜食用,老人儿童须监护下食用”。
2.3食用盐《食品安全国家标准食用盐》(GB2721)规定,低钠盐的产品标签中应标示钾的含量,并应清晰标示:“高温作业者、重体力劳动强度工作者、肾功能障碍者及服用降压药物的高血压患者等不适宜高钾摄入的人群应慎用”。
2.4固体饮料《市场监管总局关于加强固体饮料质量安全监管的公告》要求,直接提供给消费者的蛋白固体饮料、植物固体饮料、特殊用途固体饮料、风味固体饮料以及添加可食用菌种的固体饮料最小销售单元,应在食品名称同一展示版面标示“本产品不能代替特殊医学用途配方食品、婴幼儿配方食品、保健食品等特殊食品”作为警示信息,所占面积不应小于其所在面的20%。
食品原料安全性审查管理办法(标准版)

( 安全管理 )单位:_________________________姓名:_________________________日期:_________________________精品文档 / Word文档 / 文字可改食品原料安全性审查管理办法(标准版)Safety management is an important part of production management. Safety and production are inthe implementation process食品原料安全性审查管理办法(标准版)第一条为规范新食品原料安全性评估材料审查工作,根据《中华人民共和国食品安全法》及其实施条例的有关规定,制定本办法。
第二条新食品原料是指在我国无传统食用习惯的以下物品:(一)动物、植物和微生物;(二)从动物、植物和微生物中分离的成分;(三)原有结构发生改变的食品成分;(四)其他新研制的食品原料。
第三条新食品原料应当具有食品原料的特性,符合应当有的营养要求,且无毒、无害,对人体健康不造成任何急性、亚急性、慢性或者其他潜在性危害。
第四条新食品原料应当经过国家卫生计生委安全性审查后,方可用于食品生产经营。
第五条国家卫生计生委负责新食品原料安全性评估材料的审查和许可工作。
国家卫生计生委所属卫生监督中心承担新食品原料安全性评估材料的申报受理、组织开展安全性评估材料的审查等具体工作。
第六条拟从事新食品原料生产、使用或者进口的单位或者个人(以下简称申请人),应当提出申请并提交以下材料:(一)申请表;(二)新食品原料研制报告;(三)安全性评估报告;(四)生产工艺;(五)执行的相关标准(包括安全要求、质量规格、检验方法等);(六)标签及说明书;(七)国内外研究利用情况和相关安全性评估资料;(八)有助于评审的其他资料。
另附未启封的产品样品1件或者原料30克。
第七条申请进口新食品原料的,除提交第六条规定的材料外,还应当提交以下材料:(一)出口国(地区)相关部门或者机构出具的允许该产品在本国(地区)生产或者销售的证明材料;(二)生产企业所在国(地区)有关机构或者组织出具的对生产企业审查或者认证的证明材料。
卫生部印发新食品原料申报与受理规定和新食品原料安全性审查

卫生部印发《新食品原料申报与受理规定》和《新食品原料安全性审查规程》国卫食品发〔2013〕23号各省、自治区、直辖市卫生厅局(卫生计生委),新疆生产建设兵团卫生局,委直属有关单位:为规范新食品原料安全性审查和许可工作,根据《中华人民共和国食品安全法》和《新食品原料安全性审查管理办法》的规定,我委组织制定了《新食品原料申报与受理规定》和《新食品原料安全性审查规程》(可从国家卫生计生委网站政务信息栏目下载)。
现印发给你们,请遵照执行,并将执行中的有关问题及时反馈我委。
国家卫生计生委2013年10月15日新食品原料申报与受理规定第一章 总则第一条 为规范新食品原料申报与受理工作,根据《新食品原料安全性审查管理办法》,制定本规定。
第二条 申请新食品原料行政许可的单位或者个人(以下简称申请人),向国家卫生和计划生育委员会(以下简称国家卫生计生委)所属卫生监督中心申报新食品原料安全性评估材料,应当符合本规定。
第三条 新食品原料应当具有食品原料的特性,符合应当有的营养要求,且无毒、无害,对人体健康不造成任何急性、亚急性、慢性或者其他潜在性危害。
符合上述要求且在我国无传统食用习惯的以下物品属于新食品原料的申报和受理范围:(一)动物、植物和微生物;(二)从动物、植物和微生物中分离的成分;(三)原有结构发生改变的食品成分;(四)其他新研制的食品原料。
第四条 以下情形不属于新食品原料的申报范围:(一)不具有食品原料特性;(二)已列入食品安全国家标准《食品添加剂使用标准》(GB2760)、《食品营养强化剂使用标准》(GB14880)的;(三)国家卫生计生委已作出不予行政许可决定的;(四)其他不符合有关法律、法规规定和新食品原料管理要求的。
第五条 申请人应当如实提交有关材料,对申请材料内容的真实性负责,并承担法律责任。
第二章 申请材料的一般要求第六条 申请人应当提交申请材料原件1份,复印件4份。
申请材料应当完整、清晰,前后内容表述一致。
国家卫生健康委员会关于《关于桃胶等15种“三新食品”的公告》的解读

国家卫生健康委员会关于《关于桃胶等15种“三新食品”的公告》的解读文章属性•【公布机关】•【公布日期】2023.10.07•【分类】法规、规章解读正文解读《关于桃胶等15种“三新食品”的公告》(2023年第8号)一、新食品原料解读材料(一)桃胶桃胶是以蔷薇科李属植物桃树(Prunuspersica(L.)Batsch)分泌的胶状物为原料,经采摘、分选、晾晒、清洗、干燥等工艺制成。
主要营养成分为膳食纤维、多糖、水分、蛋白质和维生素等。
桃胶在我国湖北、江苏及浙江等地区有一定的食用历史,食用方式主要有做汤、粥、羹、甜品等。
本产品推荐食用量为≤30克/天。
根据《中华人民共和国食品安全法》和《新食品原料安全性审查管理办法》规定,国家卫生健康委员会委托审评机构依照法定程序,组织专家对桃胶的安全性评估材料审查并通过。
新食品原料生产和使用应当符合公告内容以及食品安全相关法规要求。
鉴于桃胶在婴幼儿、孕妇和哺乳期妇女人群中的食用安全性资料不足,从风险预防原则考虑,上述人群不宜食用,标签及说明书中应当标注不适宜人群和食用限量。
该原料的食品安全指标按照公告规定执行。
(二)油莎豆本产品的基源植物为莎草科莎草属植物油莎草(CyperusesculentusL.var.sativusBoeck.),原产于中非洲,在地中海地区被广泛种植,于上世纪五十年代引入我国,目前在我国河北、甘肃和山东等地区种植。
申报产品油莎豆为其地下块茎,主要营养成分为碳水化合物、脂肪、膳食纤维、水分和维生素等。
欧洲将油莎豆作为普通食品管理;加拿大认为油莎豆奶具有作为食品安全食用的历史。
根据《中华人民共和国食品安全法》和《新食品原料安全性审查管理办法》规定,国家卫生健康委员会委托审评机构依照法定程序,组织专家对油莎豆的安全性评估材料审查并通过。
新食品原料生产和使用应当符合公告内容以及食品安全相关法规要求。
该原料的食品安全指标按照我国现行食品安全国家标准中坚果与籽类食品的规定执行。
新食品原料安全性审查管理办法

新食品原料安全性审查管理办法(国家卫生和计划生育委员会令第1号)中华人民共和国国家卫生和计划生育委员会2013-07-12《新食品原料安全性审查管理办法》已于2013年2月5日经原卫生部部务会审议通过,现予公布,自2013年10月1日起施行。
主任李斌2013年5月31日新食品原料安全性审查管理办法第一条为规范新食品原料安全性评估材料审查工作,根据《中华人民共和国食品安全法》及其实施条例的有关规定,制定本办法。
第二条新食品原料是指在我国无传统食用习惯的以下物品:(一)动物、植物和微生物;(二)从动物、植物和微生物中分离的成分;(三)原有结构发生改变的食品成分;(四)其他新研制的食品原料。
第三条新食品原料应当具有食品原料的特性,符合应当有的营养要求,且无毒、无害,对人体健康不造成任何急性、亚急性、慢性或者其他潜在性危害。
第四条新食品原料应当经过国家卫生计生委安全性审查后,方可用于食品生产经营。
第五条国家卫生计生委负责新食品原料安全性评估材料的审查和许可工作。
国家卫生计生委所属卫生监督中心承担新食品原料安全性评估材料的申报受理、组织开展安全性评估材料的审查等具体工作。
第六条拟从事新食品原料生产、使用或者进口的单位或者个人(以下简称申请人),应当提出申请并提交以下材料:(一)申请表;(二)新食品原料研制报告;(三)安全性评估报告;(四)生产工艺;(五)执行的相关标准(包括安全要求、质量规格、检验方法等);(六)标签及说明书;(七)国内外研究利用情况和相关安全性评估资料;(八)有助于评审的其他资料。
另附未启封的产品样品1件或者原料30克。
第七条申请进口新食品原料的,除提交第六条规定的材料外,还应当提交以下材料:(一)出口国(地区)相关部门或者机构出具的允许该产品在本国(地区)生产或者销售的证明材料;(二)生产企业所在国(地区)有关机构或者组织出具的对生产企业审查或者认证的证明材料。
第八条申请人应当如实提交有关材料,反映真实情况,对申请材料内容的真实性负责,并承担法律责任。
终止审查≠终止使用┃新食品原料终止审查目录大盘点

终止审查≠终止使用┃新食品原料终止审查目录大盘点
前几日,新食品原料终止审查目录又增加了磷脂酰丝氨酸、连翘叶两种原料。
截止目前,新食品原料终止审查目录共有37种原料。
为什么会终止审查?简单说来,就是因为你不具有“新”的特色,所以不能带上“新食品”的帽子。
终止的只是头衔,并不终止使用,这些原料均可做为食品原料使用。
各种终止审查的原料可依据新食品原料、地方特色食品、普通食品等进行分类管理,根据终止审查的目录我们对这37种原料进行分类分析:一、终止审查,按新食品原料管理与已公告的新食品原料实质等同。
根据《新食品原料安全性审查管理办法》,实质等同是指如某个新申报的食品原料与食品或者已公布的新食品原料在种属、来源、生物学特征、主要成分、食用部位、使用量、使用范围和应用人群等方面相同,所采用工艺和质量要求基本一致,可以视为它们是同等安全的,具有实质等同性。
按新食品原料管理的“终止审查”目录(13种)管理分类按新食品原料管理认定原则实质等同执行标准除可能使用到的原料工艺不同外,其他应按照已公告的有关内容执行,卫生安全指标按照我国相关标准执行。
原料名称1L-阿拉伯糖2γ-氨基丁酸3壳寡糖4裂壶藻来源的DHA藻油5磷虾油6磷脂酰丝氨酸7鱼油(3种)8中长链脂肪酸结构油(又更名为中长链脂肪酸食用油)9中长碳链
甘油三酯10人参组织培养物(后更名为人参组培不定根)11山参组培不定根(后更名为人参组培不定根)。
新食品原料申报与受理规定

新食品原料申报与受理规定第一章总则第一条为规范新食品原料申报与受理工作,根据《新食品原料安全性审查管理办法》,制定本规定。
第二条申请新食品原料行政许可的单位或者个人(以下简称申请人),向国家卫生和计划生育委员会(以下简称国家卫生计生委)所属卫生监督中心申报新食品原料安全性评估材料,应当符合本规定。
第三条新食品原料应当具有食品原料的特性,符合应当有的营养要求,且无毒、无害,对人体健康不造成任何急性、亚急性、慢性或者其他潜在性危害。
符合上述要求且在我国无传统食用习惯的以下物品属于新食品原料的申报和受理范围:(一)动物、植物和微生物;(二)从动物、植物和微生物中分离的成分;(三)原有结构发生改变的食品成分;(四)其他新研制的食品原料。
第四条以下情形不属于新食品原料的申报范围:(一)不具有食品原料特性;(二)已列入食品安全国家标准《食品添加剂使用标准》(GB2760)、《食品营养强化剂使用标准》(GB14880)的;(三)国家卫生计生委已作出不予行政许可决定的;(四)其他不符合有关法律、法规规定和新食品原料管理要求的。
第五条申请人应当如实提交有关材料,对申请材料内容的真实性负责,并承担法律责任。
[1]第二章申请材料的一般要求第六条申请人应当提交申请材料原件1份,复印件4份。
申请材料应当完整、清晰,前后内容表述一致。
外文应当译为规范的中文,文献资料可提供中文摘要,并将译文附在相应的外文资料前。
第七条新食品原料申请材料应当包括以下内容,并按照下列顺序排列成册,逐页标明页码,各项间应当有区分标志:(一)申请表;(二)新食品原料研制报告;(三)安全性评估报告;(四)生产工艺;(五)执行的相关标准(包括安全要求、质量规格、检验方法等);(六)标签及说明书;(七)国内外研究利用情况和相关安全性评估资料;(八)申报委托书(委托代理申报时提供);(九)有助于评审的其他资料。
另附未启封最小包装的样品1件或者原料30克。
第八条申请进口新食品原料的,除了提交第七条规定的材料外,还应当提交以下材料:(一)进口新食品原料出口国(地区)相关部门或者机构出具的允许该产品在本国(地区)生产或者销售的证明材料;(二)进口新食品原料生产企业所在国(地区)有关机构或者组织出具的对生产企业审查或者认证的证明材料。
大型食品生产企业监管模式创新探讨

大型食品生产企业监管模式创新探讨作者:王丽英来源:《中国民商》2022年第08期摘要:近年來,随着《食品安全法》、《食品安全法实施条例》等一系列法律法规的不断完善,对大型食品生产企业的食品安全监管提出了更高的要求。
基于此,本文围绕食品监管模式的发展变迁展开研究,简要阐述食品安全监管的重要性,深入分析大型食品生产企业开展监管工作的困境,积极探讨大数据时代大型食品生产企业监管模式创新的具体路径,希望能为现代大型食品生产企业提供一些有用的借鉴与参考。
关键词:食品生产企业;监管模式;创新路径面对日益严峻的食品安全问题,国家出台并颁布了一系列的法律法规,要求各大食品生产企业高度重视食品监管工作,充分发挥内部监管模式的效用,不断提升食品生产的安全系数与安全监管效率,切实保障广大消费者的人身健康,实现企业经济效益和社会效益的双向发展。
由此可见,如何创新、优化食品监管模式、加强对食品生产环节的监督、管理,是新时期大型食品生产企业必须深入思考与研究的首要课题。
一、食品监管模式的发展变迁与食品安全监管的重要性(一)食品监管模式的发展变迁在我国,食品监管模式的发展变迁最早可以追溯到1949,为保证食品安全成立了专门的卫生部门,并在1965年颁布了《食品卫生管理试行条例》,这是我国第一部有关食品卫生的管理法规。
随后,我国先后颁布了78部与食品安全相关的行政法规及管理办法,其中主要法律有11部、主要法规有16部。
与此同时,为进一步加强食品安全监管力度,国务院按照分段监管为主、品种监管为辅的监管原则,由不同部门对种植、养殖、生产加工、流通、消费等各个环节进行监管。
在此基础上,国务院决定设立食品药品监督管理局,统一管理食品生产的各个环节,并对本区域内的视频进行统一的抽样检查,在经过食品检验中心实验、检验之后,结合检验报告要求相关企业做出相应的整改、处罚。
由此,我国食品监管体系大致经历了三个阶段,分别为分段监管阶段、统一监管阶段、分级分类监管阶段。
新食品原料申报与受理规定

新食品原料申报与受理规定第一章总则第一条为规范新食品原料申报与受理工作,根据《新食品原料安全性审查管理办法》,制定本规定。
第二条申请新食品原料行政许可的单位或者个人(以下简称申请人),向国家卫生和计划生育委员会(以下简称国家卫生计生委)所属卫生监督中心申报新食品原料安全性评估材料,应当符合本规定。
第三条新食品原料应当具有食品原料的特性,符合应当有的营养要求,且无毒、无害,对人体健康不造成任何急性、亚急性、慢性或者其他潜在性危害。
符合上述要求且在我国无传统食用习惯的以下物品属于新食品原料的申报和受理范围:(一)动物、植物和微生物;(二)从动物、植物和微生物中分离的成分;(三)原有结构发生改变的食品成分;(四)其他新研制的食品原料。
第四条以下情形不属于新食品原料的申报范围:(一)不具有食品原料特性的;(二)已列入食品安全国家标准《食品添加剂使用标准》(GB2760)、《食品营养强化剂使用标准》(GB14880)的;(三)国家卫生计生委已作出不予行政许可决定的;(四)其他不符合有关法律、法规规定和新食品原料管理要求的。
第五条申请人应当如实提交有关材料,对申请材料内容的真实性负责,并承担法律责任。
第二章申请材料的一般要求第六条申请人应当提交申请材料原件1份,复印件4份。
申请材料应当完整、清晰,前后内容表述一致。
外文应当译为规范的中文,文献资料可提供中文摘要,并将译文附在相应的外文资料前。
第七条新食品原料申请材料应当包括以下内容,并按照下列顺序排列成册,逐页标明页码,各项间应当有区分标志:(一)申请表;(二)新食品原料研制报告;(三)安全性评估报告;(四)生产工艺;(五)执行的相关标准(包括安全要求、质量规格、检验方法等);(六)标签及说明书;(七)国内外研究利用情况和相关安全性评估资料;(八)申报委托书(委托代理申报时提供);(九)有助于评审的其他资料。
另附未启封最小包装的样品1件或者原料30克。
第八条申请进口新食品原料的,除了提交第七条规定的材料外,还应当提交以下材料:(一)进口新食品原料出口国(地区)相关部门或者机构出具的允许该产品在本国(地区)生产或者销售的证明材料;(二)进口新食品原料生产企业所在国(地区)有关机构或者组织出具的对生产企业审查或者认证的证明材料。
公共场所卫生管理条例实施细则(2017.12.26修)

公共场所卫生管理条例实施细则(修订版)2017年12月26日中华人民共和国国家卫生和计划生育委员会令第 18 号《国家卫生计生委关于修改〈新食品原料安全性审查管理办法〉等7件部门规章的决定》已于2017年12月5日经国家卫生计生委委主任会议讨论通过,现予公布,自公布之日起施行。
主任李斌2017年12月26日国家卫生计生委关于修改《新食品原料安全性审查管理办法》等7件部门规章的决定为深入推进政府职能转变和行政审批制度改革,依法推动简政放权、放管结合、优化服务,根据国务院取消、下放和调整行政审批项目等事项的决定,我委决定对以下部门规章的部分条款予以修改。
一、《新食品原料安全性审查管理办法》(一)将第五条第二款修改为:“国家卫生计生委新食品原料技术审评机构(以下简称审评机构)负责新食品原料安全性技术审查,提出综合审查结论及建议。
”(二)在第十四条后增加一条:“审评机构提出的综合审查结论,应当包括安全性审查结果和社会稳定风险评估结果。
”(三)将第二十一条第二款修改为:“以欺骗、贿赂等不正当手段通过新食品原料安全性审查并取得许可的,国家卫生计生委应当撤销许可,且申请人在三年内不得再次申请新食品原料许可。
”二、《食品添加剂新品种管理办法》(一)将该办法中的“卫生部”统一修改为:“国家卫生计生委”。
(二)第五条增加一款作为第二款:“国家卫生计生委食品添加剂新品种技术审评机构(以下简称审评机构)负责食品添加剂新品种技术审查,提出综合审查结论及建议。
”(三)删除第十条第三款。
(四)在第十一条后增加一条:“审评机构提出的综合审查结论,应当包括安全性、技术必要性审查结果和社会稳定风险评估结果。
”(五)在第十四条后增加一条:“申请人隐瞒有关情况或者提供虚假材料申请食品添加剂新品种许可的,国家卫生计生委不予受理或者不予行政许可,并给予警告,且申请人在一年内不得再次申请食品添加剂新品种许可。
“以欺骗、贿赂等不正当手段通过食品添加剂新品种审查并取得许可的,国家卫生计生委应当撤销许可,且申请人在三年内不得再次申请食品添加剂新品种许可。
贾旭东-新食品原料安全性评估.

(三)风险评估报告申请材料要求
内部讨论稿 仅供参考
一般要求
(一)符合《管理办法》相关规定; (二)外文译为规范中文:重要文献资料(如国 外权威机构出具的安全性评估报告等)需全文翻 译;其他可提供中文摘要; (三)申请人应如实全面提交有关资料,对提交 资料内容的真实性负责; (四)申请材料应满足安全性评估的需要。
(二)安全性评估报告
1.近期3批有代表性样品的污染物和微生物的检测结果及方法 2. 报告出具单位:A 我国;B资质(CMAF)
安全性评估报告
(一)成分分析报告; (二)卫生学检验报告; (三)毒理学评价报告; (四)微生物耐药性试验报告和产毒能力试验报告; (五)风险评估报告。
(二)安全性评估报告
1. 为什么 修改? 第四十四条 申请利用新的食品原料从事食 品生产或者从事食品添加剂新品种、食品相关产 品新品种生产活动的单位或者个人。。。。
2. 目前的定义?
第二条 新食品原料是指在我国无传统食用习惯的以下物品 (一)动物、植物和微生物; (二)从动物、植物和微生物中分离的成分; (三)原有结构发生改变的食品成分; (四)其他新研制的食品原料
《食品安全法》——与现行法规一致 与国际接轨——safety assessment
第四十四条 申请利用新的食品原料从事食品生产。。。,应当向国务 院卫生行政部门提交相关产品的安全性评估材料。。。。
(二)安全性评估报告
新《管理办法》
第六条 拟从事新食品原料生产、使用或者进口的 单位或者个人(以下简称申请人),应 当 提出申请并提交以下材料: (一)申请表; (二)新食品原料研制报告; (三)安全性评估报告; (四)生产工艺; (五)执行的相关标准; (六)标签及说明书; (七)国内外研究利用情况和评估资料; (八)有助于评审的其他资料。
《瑞士乳杆菌R0052等4种新食品原料、三赞胶等21种食品添加剂新品种、辛酸锌等28种食品相关产品新品种》解读

解读《关于瑞士乳杆菌R0052等53种“三新食品”的公告》(2020年第4号)一、新食品原料(一)瑞士乳杆菌R0052、婴儿双歧杆菌R0033和两歧双歧杆菌R00712010年瑞士乳杆菌、婴儿双歧杆菌和两歧双歧杆菌已列入我国《可用于食品的菌种名单》。
瑞士乳杆菌R0052(helveticus Lactobacillus R0052)从乳制品中分离得到,婴儿双歧杆菌R0033(infantis Bifidobacterium R0033)从婴儿肠道分离得到,两歧双歧杆菌R0071(bifidum Bifidobacterium R0071)从成人肠道分离得到。
3种菌株粉的性状均为米色颗粒状粉末。
瑞士乳杆菌R0052、婴儿双歧杆菌R0033和两歧双歧杆菌R0071已通过美国食品药品管理局认证为一般认为安全(GRAS)物质。
含有这3种菌株的产品已在加拿大、波兰、澳大利亚被批准用于婴幼儿。
国内外开展的多项婴幼儿临床研究证明,该3种菌株具有较好的食用安全性,且耐受性良好。
根据《食品安全法》和《新食品原料安全性审查管理办法》规定,审评机构依照法定程序,组织专家对瑞士乳杆菌R0052、婴儿双歧杆菌R0033和两歧双歧杆菌R0071的安全性评估材料进行审查并通过。
新食品原料生产和使用应当符合公告内容以及食品安全相关法规要求。
3种菌株原料的食品安全指标应当符合我国相关标准。
(二)赶黄草赶黄草(chinense Penthorum Pursh.)为虎耳草科、扯根菜属,在我国四川、广东、山西、浙江、黑龙江、吉林、辽宁、河北、陕西、甘肃、江苏、安徽、江西、河南、湖北、湖南、广西、贵州、云南等大部分地区均有分布。
民间有食用历史,食用方式以泡饮为主。
本次申报的产品为赶黄草的茎和叶,食用方式为泡饮。
根据《食品安全法》和《新食品原料安全性审查管理办法》,审评机构组织专家对赶黄草的安全性评估材料审查并通过。
新食品原料生产单位应当按照公告内容生产和使用,符合食品安全要求。
2021年新食品原料安全性审查管理办法全文

新食品原料安全性审查管理办法全文《新食品原料安全性审查管理办法》已于xx年2月5日经原卫生部部务会审议通过,以下是该办法全文。
第一条为规范新食品原料安全性评估材料审查工作,根据《中华人民 ___食品安全法》及其实施条例的有关规定,制定本办法。
第二条新食品原料是指在我国无传统食用习惯的以下物品:(一)动物、植物和微生物;(二)从动物、植物和微生物中分离的成分;(三)原有结构发生改变的食品成分;(四)其他新研制的食品原料。
第三条新食品原料应当具有食品原料的特性,符合应当有的营养要求,且无毒、无害,对人体健康不造成任何急性、亚急性、慢性或者其他潜在性危害。
第四条新食品原料应当经过国家卫生计生委安全性审查后,方可用于食品生产经营。
第五条国家卫生计生委负责新食品原料安全性评估材料的审查和许可工作。
国家卫生计生委所属卫生监督中心承担新食品原料安全性评估材料的申报受理、组织开展安全性评估材料的审查等具体工作。
第六条拟从事新食品原料生产、使用或者进口的单位或者个人(以下简称申请人),应当提出申请并提交以下材料:(一)申请表;(二)新食品原料研制报告;(三)安全性评估报告;(四)生产工艺;(五)执行的相关标准(包括安全要求、质量规格、检验方法等);(六)标签及说明书;(七)国内外研究利用情况和相关安全性评估资料;(八)有助于评审的其他资料。
另附未启封的产品样品1件或者原料30克。
第七条申请进口新食品原料的,除提交第六条规定的材料外,还应当提交以下材料:(一)出口国(地区)相关部门或者机构出具的允许该产品在本国(地区)生产或者销售的证明材料;(二)生产企业所在国(地区)有关机构或者组织出具的对生产企业审查或者认证的证明材料。
第八条申请人应当如实提交有关材料,反映真实情况,对申请材料内容的真实性负责,并承担法律责任。
第九条申请人在提交本办法第六条第一款第二项至第六项材料时,应当注明其中不涉及商业秘密,可以向社会公开的内容。
新《食品安全法》详解 —— 食品企业的必修课

新《食品安全法》详解——食品企业的必修课一、食品安全法出台背景与中国很多的法律法规的出台相似,2009年2月出台的《食品安全法》从一开始即承载着特定的背景和期望。
2008年三聚氰胺事件给中国食品监管体系敲响了警钟,作为众多措施之一,《食品安全法》在事件发生后半年内迅速出台。
实施了近四年后,随着公众对健康和安全需求的不断提升,政府能不能在食品安全上给老百姓一个满意的交代这也是对党和政府执政能力的一个重大考验;从食品产业(企业)本身来讲近年来的的增速出现收窄,结构调整和转型升级势在必行,但安全性是基础;再有《食品安全法》实施后,监管体制,产业发展、科技进步等方面的的变化,需要在法治建设上应对这些变化。
因此《食品安全法》于2014年进入全面修订。
历经三次审议,全国人大常委于今年4月24日颁布了新修订的《食品安全法》。
如此短时间内对一部上位法律进行重大修订,反映了中国复杂食品安全状况,也凸显了中央政府强化食品监管的强烈意志。
作为食品安全领域的上位法,《食品安全法》全局性统领食品监管法律体系。
对于该领域的各个主体,包括监管机构、中介机构、市场主体(包括食品生产者、销售方、运输方、和其他食品相关方),新法都将带来重大的影响。
因此这次《食品安全法》出台也被称为最为周到具体、最高的处罚力度、最广泛的追责,史上最严的的一步法律。
下面从食品行业市场主体的角度,为企业理解和应对新《食品安全法》提供思路和策略上的建议,同时,根据新《食品安全法》对于企业影响程度,为企业梳理新法带来的实质性变化。
二、企业应如何看待新《食品安全法》?新《食品安全法》对原法90%以上的条文进行了修改,条款数量增加了50%。
如此多的变化,企业应如何去繁取要,采取有效应对措施,建议可从以下几个方面着手。
1.分清变化和继承。
新法条文的改动甚多,但实际上,新法一方面有突破,另一方面是大量继承和吸纳已有的制度和规定(比如对新食品原料申请、剧毒农药不得使用、转基因食品标签说明等等),并在继承中进行调整。
国家卫生健康委员会解读《关于莱茵衣藻等36种“三新食品”的公告》(2022年第2号)

国家卫生健康委员会解读《关于莱茵衣藻等36种“三新食品”的公告》(2022年第2号)文章属性•【公布机关】国家卫生健康委员会,国家卫生健康委员会,国家卫生健康委员会•【公布日期】2022.05.11•【分类】法规、规章解读正文解读《关于莱茵衣藻等36种“三新食品”的公告》(2022年第2号)一、新食品原料(一)莱茵衣藻莱茵衣藻(Chlamydomonasreinhardtii)属于衣藻科、衣藻属。
经藻种培养、发酵罐异养扩大培养、干燥等工艺制成。
主要营养成分包括蛋白质、碳水化合物、脂肪、氨基酸、维生素和矿物质等,其中蛋白质≥30.0%、粗多糖≥10.0%。
莱茵衣藻在美国被列为“一般认为安全”物质,可作为膳食蛋白质来源;在新加坡被批准作为食品原料使用;在我国香港允许其进入市场销售。
根据《中华人民共和国食品安全法》和《新食品原料安全性审查管理办法》规定,国家卫生健康委员会委托审评机构依照法定程序,组织专家对莱茵衣藻的安全性评估材料审查并通过。
新食品原料生产和使用应当符合公告内容以及食品安全相关法规要求。
鉴于莱茵衣藻在婴幼儿食品中的使用安全性资料不足,从风险预防原则考虑,使用范围不包括婴幼儿食品。
该原料的食品安全指标按照我国现行食品安全国家标准中藻类及其制品的规定执行。
(二)长双歧杆菌长亚种BB536长双歧杆菌长亚种(原名称为“长双歧杆菌”)已被列入我国《可用于食品的菌种名单》,也已列入欧洲食品安全局资格认定(QPS)名单的推荐生物制剂列表以及国际乳品联合会公报(BulletinoftheIDF455/2012)的“在发酵食品中有技术必要性的微生物品种目录”。
长双歧杆菌长亚种BB536(Bifidobacteriumlongumsubsp.longumBB536)从健康婴儿肠道中分离得到,该菌株已在美国、日本被批准用于婴幼儿食品。
国内外开展的多项婴幼儿临床研究证明,该菌株具有较好的食用安全性。
根据《中华人民共和国食品安全法》和《新食品原料安全性审查管理办法》规定,国家卫生健康委员会委托审评机构依照法定程序,组织专家对长双歧杆菌长亚种BB536的安全性评估材料进行审查并通过。
食叶草等3种新食品原料公告和解读材料
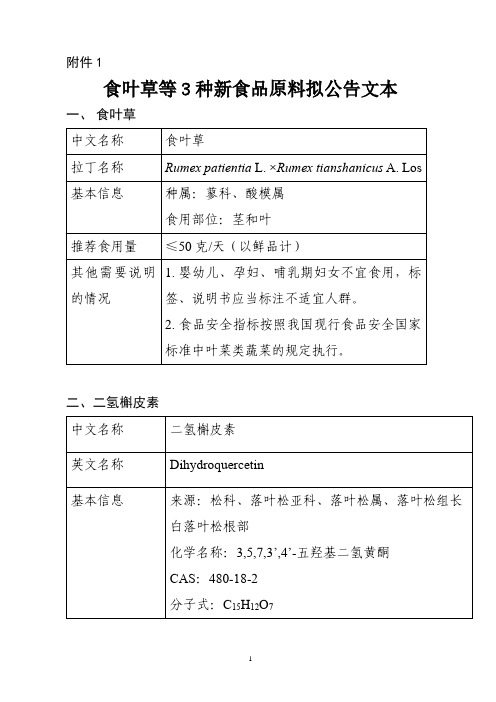
附件1食叶草等3种新食品原料拟公告文本一、食叶草二、二氢槲皮素以人工种植的长白落叶松的根部为原料,经去皮、撕裂处理,进行提取、浓缩、醇沉、上清液浓缩、萃取、再浓缩、结晶、离心分离、冷冻真空干燥、粉碎过筛等工艺制成。
天三、鼠李糖乳杆菌MP108附件2食叶草等3种新食品原料解读材料一、食叶草食叶草是我国引进的鲁梅克斯K-1酸模与我国野生巴天酸模回交选育生成的多年生蓼科酸模属草本植物。
食叶草在我国新疆、河北、河南、山东、山西、陕西、甘肃、北京、天津、浙江、江西、江苏、广东、广西、吉林、黑龙江、辽宁和内蒙等地区均有种植。
食叶草及其制品在我国约有20年食用历史,食用部位为茎和叶,食用方式有凉拌、榨汁、炒菜、泡茶、制作豆腐和面食等,未见人群食用不良反应报道。
本产品的推荐食用量为≤50克/天(以鲜品计)。
根据《食品安全法》和《新食品原料安全性审查管理办法》,审评机构依照法定程序,组织专家对食叶草的安全性评估材料审查并通过。
新食品原料生产和使用应当符合公告内容以及食品安全相关法规要求。
鉴于食叶草在婴幼儿、孕妇、哺乳期妇女人群中的安全性资料不足,从风险预防原则考虑,上述人群不宜食用,标签及说明书中应当标注不适宜人群。
该原料的食品安全指标按照我国现行食品安全国家标准中叶菜类蔬菜的相关规定执行。
二、二氢槲皮素二氢槲皮素(Dihydroquercetin)是多种植物中存在的一种二氢黄酮醇类化合物。
本产品是以人工种植的长白落叶松的根部为原料,经去皮、撕裂处理,进行提取、浓缩、醇沉、上清液浓缩、萃取、再浓缩、结晶、离心分离、冷冻真空干燥、粉碎过筛等工艺制成。
欧盟已批准落叶松来源的二氢槲皮素为新食品原料,俄罗斯已批准二氢槲皮素作为食品原料和食品添加剂使用。
本产品推荐食用量为≤100毫克/天,使用范围和最大使用量:饮料(20 mg/L),发酵乳和风味发酵乳(20 mg/kg),可可制品、巧克力和巧克力制品(70 mg/kg)。
读《新食品原料申报与受理规定》

生产工艺简述:以万寿菊花为原料,经过脱水粉碎、溶剂提取、低分子量醇纯化和真空浓缩等步骤生产而成。
使用范围:焙烤食品、乳制品、饮料、即食谷物、冷冻饮品、调味品和糖果。
使用量:≤12毫克/天
性状:深红棕色细小颗粒。
玉米黄质酯含量:< 4.2 %
在《新食品原料申报与受理规定》的第一章第三条写道:“新食品原料应当具有食品原料的特性,符合应当有的营养要求,且无毒、无害,对人体健康不造成任何急性、亚急性、慢性或者其他潜在性危害。
符合上述要求且在我国无传统食用习惯的以下物品属于新食品原料的申报和受理范围:
(一)动物、植物和微生物;
(二)从动物、植物和微生物中分离的成分;
结构式:
分子式:(C14H20NNaO11)n,n为200-10000
分子量:8.02×104—4.01×106
作用:广泛应用于高档化妆品行业,用于眼干燥综合症。
生产工艺简述
以葡萄糖、酵母粉、蛋白胨等为培养基,由马链球菌兽疫亚种经发酵生产而成。
使用范围:保健食品原料
食用量:≤200毫克/天
质量规格
性状
读《新食品原料申报与受理规定》
2013年10月15日,国家卫生计生委以国卫食品发〔2013〕23号印发《新食品原料申报与受理规定》。该《规定》分总则、申请材料的一般要求、材料的编制要求、审核与受理4章24条,自发布之日起实施。以往有关文件与本规定不一致的,以本规定为准。原卫生部《新资源食品安全性评价规程》和《新资源食品卫生行政许可申报与受理规定》予以废止。
2.新资源食品和保健食品的适用人群不同,前者适用于任何人群,而后者适宜于特定人群食用。
